稠杂环化合物的命名规则
第十八章--杂环化合物

混酸
浓 浓
2、SN 反应
喹啉能发生 SN 反应,主要发生 在吡啶环的 2-位上。
二甲苯
喹啉及其衍生物旳合成:常用斯克劳普 (Skraup)法,原料为苯胺和甘油,将原料 与脱水剂浓硫酸、氧化剂硝基苯共热制得
二、吲哚
从结构可以看出吲哚也具有一定 的上。
这些化合物通过分析可以知道,其结 构都符合休克儿规则,具有芳香性。
二、物理性质与光谱性质
物理性质 光谱性质
电流,此环电流可产生一种和外界磁 场相反旳感应磁场,环外旳质子处于感 应磁场回来旳磁力线上和外界磁场一致, 即在去屏蔽区域,故环上氢旳吸收峰向低 场移动,化学位移值一般在7左右因为外 磁场旳作用而诱导出一种围绕旳环。
例如
嘌呤
尿酸
腺嘌呤
鸟嘌呤
化学与毒品
毒品化合物构造
毒品旳分类
麻醉镇宁(鸦片、大麻、杜冷丁等) 催眠镇宁(巴比妥、利眠宁、安定等) 致幻剂(苯丙胺类兴奋剂、N-去甲肾上
腺素、麦角酰二乙胺等) 中枢神经兴奋剂(可卡因、咖啡因、冰
毒、安非他命、摇头丸等)
具有一定旳芳香性,环为平面构造,环上旳原子都是sp2杂化,每 个碳原子垂直于环平面旳p轨道有一种电子(与苯相同),杂原子 垂直于环平面旳p轨道有二个电子,形成闭合旳共轭体系,π电子 数为6个,符合休克尔规则。因为6个π电子分布于5个原子上,整 个环旳π电子几率密度比苯大,是富电子芳环,因而比苯环活泼, 亲电反应比苯快得多。 芳香性顺序为:噻吩 > 吡咯 > 呋喃,这与杂原子电负性顺序相反。
呋喃甲醛具备无α-H 醛的基本化 学性质.
主要反应
浓 浓
糠醇 -呋喃甲酸
卟啉化合物都具有卟吩环,在环旳中间空穴中,以 共价键、配位键和金属结合。如血红素具有铁,叶 绿素具有镁,维生素B12具有钴等。
有机化学第十五章 杂环化合物

+
N
N
NO 2
N
N S O 3H
Br
B r2/H 2 S O 4
H+
+
N
N
B r 2 /CCl 4
OH -
Br Br
N
K MnO 4 /H +
CO 2 H
N
CO 2 H
H 2/P t N H
易发生亲电取代和氧化
5
8
N
易发生亲核取代和还原3
N +C3 H I
N
+ N C3 H I N
N
Br
+Br2 NH 2 N
5
7 N
6
7
N1 2 6 7 H
O1 2 6 7
N1 2 2
N 3
4
N9
8
H
H
吲哚
苯并呋喃
苯并咪唑
嘌 呤 (9-H)
4
4
5
35
3
4( γ )
5
3
一个杂原子6
26
2( α 6)
2
N
O
O
1
1
1
吡啶
α -吡 喃
γ -吡 喃
(2-H)
(4-H)
4
4
4 N
六 两 个 杂 原 子 3N
55
35
3
元 杂 环
2
66
3、由于电荷分布不均匀,分子中应有偶极矩;
4、由于O、S、N上的电子均参与了共轭,因此其偶极矩应小 于吡啶,故其水溶性小于吡啶,水溶性:吡啶>吡咯>呋喃>噻吩;
5、吡咯分子中由于N原子的电子参与了共轭,降低了本身的电 子云密度,故吡咯分子应具有一定的酸性。
杂环化合物的命名-DICP

3 2N
1N H
N4
5 O6
4 5N
6N H
N3
2 O1
b) 共用杂原子都要编号,共用碳原子一般不编号,如需要编号时, 用前面相邻的位号加a、b…表示。
4
5
3b 3a 3
6 7
8
2
N 8a N1
杂环化合物的命名
杂环化合物的命名
一、杂环母核的命名
杂环化合物的命名比较复杂。我国采用“音译法”,按照英文名 称的读音,选用同音汉字加“口”旁组成音译名,其中“口”代表环
的结构。
1. 含一个杂原子的杂环:
含一个杂原子的杂环从杂原子开始编号。
2. 含两个或多个杂原子的杂环:
含两个或多个杂原子的杂环编号时应使杂原子位次尽可能小,并 按O、S、NH、N的优先顺序决定优先的杂原子,
5
4 3d
c N
e
b
6 N 2 Na
1
吡啶并[3,2-e]嘧啶
次序相反
4 3d e
2 1
4 5 N 3d e
c
6
N N 2bN a
1
吡嗪并[2,3-c]哒嗪
4 3d c
1 2b
次序相同
杂环化合物的命名
3. 周边编号:
为了标示稠杂环上的取代基、官能团或氢原子的位置,需要对整个 稠杂环的环系进行编号,称为周边编号或大环编号。
杂环化合物的命名
举例:
1
7
3 4
5
2a
1N
b
c N2
d
6 543
3-methylpyrrolo[1,2-a]pyrazine
【基础有机化学】第20章 杂环化合物

2、亲电取代反应
亲电取代反应比吡啶容易,比萘难,主要发生在 苯环上的5和8位。例如:
NO2
HNO3,H2SO4 0℃
N SO3H
+ N
NO2
浓H2SO4
22℃ N
N
Br
Br2 浓H2SO4
+
Ag2SO4
N
N
Br
3、亲核取代反应
亲核取代反应也吡啶容易,主要发生在吡啶环上 的2位。例如:
NaNH2 二甲苯 100℃
将苯胺与无水甘油、硝基苯、硫酸等共热,即可 得喹啉:
NH2 CH2OH
NO2 H2SO4
NH2
+ CHOH +
+
CH2OH
FeSO4
N
反应历程:
CH2 CH CH2 H2SO4 OH OH OH
CH2=CH-CHO + H2O
NH2 CH2=CH-CHO
H
H
N
H2SO4
N
H
-H2O
OH
1,2-二氢喹啉
• 在有机物中通常将除碳和氢之外的其
他元素称为杂原子。
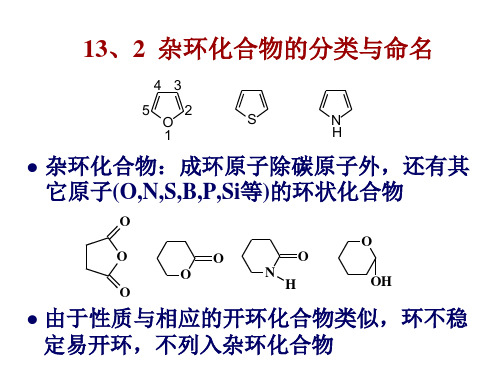
• 杂环化合物是指那些具有与苯环相
似的闭合共轭体系的杂环化合物, 它们具有不同程度的芳香性,所以, 也叫芳杂环。
一、分类和命名
(一)分类
单杂环 杂环
五元杂环 六元杂环
五元一杂 五元二杂 六元一杂 六元二杂
苯环与杂环稠合 稠杂环
杂环与杂环稠合
(二)命名
O 2H-吡喃(无芳香性)
2H-pyran
六元二杂:
N
N 嘧啶 pyrimidine
稠杂环:
N 喹啉 quinoline
杂环化合物的分类与命名
I(CH2)4I
浓 H2SO4 佯盐
噻吩的氢化还原
H2
S MoS2
S
C2H5OH,Na S 化学还原法
+
S
S
二氢噻吩
噻吩的S使催化剂中毒,需用不会被硫毒化的 催化剂,如MoS2
13、4 六员环的结构与性质 一、六员环的结构
..
.
.p
. . N .. sp2
N
未成键的sp2杂化轨道有一对电子,没有参与共轭,N 对C只有吸电子诱导效应,没有共轭效应,使碳上的电 子云密度降低,属缺π电子芳香杂环体系
N 25℃,0.3MPa
N
H
吡啶比呋喃、噻吩、吡咯难 还原,由于偶极矩的存在,比 苯易还原
吡啶与吡咯碱性比较
N
+ KOH
H
N -
K+
吡咯钾
+ HCl N
.HCl N
利用二者酸碱性不同分离
吡啶盐酸盐
一般化合物的碱性顺序
季铵碱>脂肪胺> 氨 > 吡啶 >苯胺> 尿素>酰胺>吡咯
pKb
3-4 4.75 8.6 9.4
呋喃
S
thiophene
噻吩
N
pyrrole
吡咯
N N
imidazole
咪唑
NN
pyrazole
吡唑
N S
thiazole
噻唑
3、稠杂环的命名
N H
indole
吲哚
N
N
NN H
purine
嘌呤
N
quinoline
喹啉
O
benzopyran
杂环化合物命名

杂环化合物命名杂环化合物杂环化合物分为脂杂环和芳杂环,脂杂环是一些内酯或其他结构。
而主要的是芳杂环,它又分为单杂环和稠杂环两种。
稠杂环有两个或以上单杂环稠和在一起的和苯环与单杂环稠和在一起的两种。
最常见的杂环化合物是五元和六元杂环及苯并杂环化合物等。
[2]五元杂环化合物有:呋喃、噻吩、吡咯、噻唑、咪唑等。
六元杂环化合物有:吡啶、吡嗪、嘧啶、哒嗪等。
稠环杂环化合物有:吲哚、喹啉、蝶啶、吖啶等。
杂环化合物中,最小的杂环为三元环,最常见的是五、六元环,其次是七元环。
杂环的成环规律和碳环一样,最稳定、最常见的杂环也是五元或六元的。
杂环化合物的中文名称是以口字旁标明其为杂环,另半部分表明杂原子的种类。
例如,以喃、噻分别表示为含氧、硫的杂环;以咯、唑、嗪、啶、啉表示为含氮的杂环,这些字是根据英文字的尾音创造的,其中咯、唑表示为五元含氮杂环,其余的指六元含氮杂环(含两个以上杂原子的五元单杂环:至少含一个N原子的通称为“某唑”;含两个以上杂原子的六元单杂环:至少含一个N原子的通称为“嗪”)。
杂原子超过一个者分别以二、三等字表示相同杂原子的数目,例如:二唑,表示该杂环化合物为含有一个氧和两个氮杂原子的五元杂环。
在环中不同的原子可有不同的排列方式,命名时各原子的位置编号遵循下列原则:①只含一个杂原子或一个以上相同杂原子的杂环,杂原子编最小号;②含两个不同杂原子时,不同杂原子的编号顺序为氧、硫、氮,例如1,2,3-?二唑,氧在第一位,两个氮原子分别在第二和第三位,其余为碳原子的五元杂环化合物。
稠杂环化合物编号:对于这类化合物,可以将其母核分解为两个特定名称的环系,并将其中一个定位基本换,另一个定位附加环。
命名是把附加环放在前面,两环名称间缀以方括号,方括号内分别用阿拉伯数字和小写英文字母表示两个环稠和情况。
例:噻吩并【2,3-b】呋喃基本环选择原则:芳碳环和杂环稠和的选择杂环为基本环;杂环与杂环组合的化合物,按O、S、NH、NR、N顺序选择基本环;大小不同的选择大的杂环做基本环;大小相同时杂原子数及种类最多为基本环;若杂原子数及种类相同,则编号最小为基本环。
大学化学--杂环化合物的命名规则

基本环各边用英文 字母表示。1,2原 子之间为a,2,3原 子之间为b …
3e d
aN
N
2
cb
N
1
吡啶并[2,3-d] 嘧啶
35
附加环 附加环
4
3
c b
d
5
2ae
SO
1
噻吩并[2,3-b]呋喃
3 a NH
b
O2 c
1 呋喃并 [3,2-b]吡咯
36
基本环
基本环
数字走向与基 本环一致
1N H
4 3cN
(pyridazine)
4
5
N3
6
2
N
1
嘧啶
(pyrimidine)
4 5N 3
6
2
N
1
吡嗪
(pyrazine)
(三)、常见的杂环母核
稠杂环化合物 1. 吲哚
吲哚是白色结晶,熔点52.5℃。极稀溶液有香味, 可用作香料,浓的吲哚溶液有粪臭味。素馨花、柑桔 花中含有吲哚。吲哚环的衍生物广泛存在于动植物体 内,与人类的生命、生活有密切的关系。
d 5e
b
N2aN1N
HH
4c
d 5e
b NaN
H
咪唑并[4,5-d]吡唑
5 4
1
5
N 2b Na
c S
d e4
1
N 2b
c
d
N aSeLeabharlann 33咪唑并[2,1-b]噻唑
37
3.环周边编号方法 为了标示稠杂环上的取代基、官能团或氢原子的
位置,需要对整个稠杂环的环系进行编号,称为周边 编号或大环编号。 (1)尽可能使所含的杂原子编号最低,在保证编号 最低的前提下,再考虑按O、S、NH、N的顺序编号。
杂环化合物命名

杂环化合物命名(一)特定杂环的俗名合半俗名IUPAC原则规定,具有特定俗名和半俗名的杂环共45个S O NHN NHNSNONNNNNNNNONNNN NNNNNNNNHN以上杂环氢的位置不同者,把H(大写、斜体)及其标号放在词首,在并环上者,注明边号(用a 、b 、c 表示)。
ONN当杂原子在环上的位置不同时,可视为异构体。
NHS NONN几点说明(1) 杂环的写法可以不同,但是位号不变。
(2) 单杂环的编号从杂原子开始,并使其他杂原子或指示氢位号尽可能小;杂原子不同时,要使优先的杂原子号小,常见的位O ,S ,-NH-,-N=顺序;只含一个杂原子的单杂环,也可对杂原子旁的碳用αβγ进行编号。
(3) 稠杂环有其固定的编号顺序,通常从一端开始,依次编号一周(公用碳不编号,如需编号时,用前一位加a,b,c 表示),并尽可能使杂原子,特别使优先的杂原子号小;也有的杂环按相应的环烃编号,此时杂原子编号最大(见咔唑,丫啶),嘌呤使个特例,不仅公用碳编号,且编号顺序也很特别。
(4) 含两个以上杂原子的五元单杂环,其中至少含一个氮原子的通称“某唑”;含两个以上杂原子(至少一个位氮)的六元单杂环多称为“某嗪”;含氧的称“恶”;含硫的称“噻”。
例如:ON NSNNNNNi a z o l ei a z o l ea zi n e(5) 杂环已经含有最大数目的非聚集双键之外,还含有的饱和氢原子(两个二价元素中间的饱和氢不算)称做“指示氢”或“额外氢”或“标氢”。
指示氢不同的异构体,以其位号加“H ”(斜体大写)作词首来表示。
(6) 若杂环尚未含有最大数目的非聚集双键,这样的饱和氢原子为外加氢。
命名时要指明加氢的位置和数目,全部饱和可以省略位置。
(7) 含活泼氢的杂环及其衍生物,可能存在互变异构体,结构不同,名称也异;命名时尚需标明两种可能的位号 。
(8) 杂环母环的名称确定之后。
就可参照芳香化合物的命名方法,将环上取代基位置,数目及名称,以词首或词尾的形式加在环名的前后,有时杂环也可以作为取代基命名。
稠杂环化合物的命名规则教学文案

稠杂环化合物的命名:对这类杂环化合物,可将其母核分解成两个有特定名称的环系,并将其中一个定为基本环,另一个定为附加环。
命名时将附加环名称放在前,基本环名称放在后,两环名称间缀以方括号,方括号内分别用阿拉伯数字和小写英文字母表示两环的稠合情况。
现就其具体方法说明如下:一、关于基本环的选择,主要按以下几条规则依次考虑。
①由杂环和芳环构成的稠杂环,优先选择杂环作基本环。
如还有选择时,应优先选择环数较多,且有特定名称的杂环作基本环。
例如:Ⅰ中噻唑为基本环,苯为附加环,称为苯并噻唑;Ⅱ称为苯并异喹啉(不称萘并吡啶)。
②由杂环和杂环构成的稠杂环,环大小不同时,优先选择大环作基本环;环大小相同时,按N、O、S的顺序优先选择基本环。
例如:Ⅲ的基本环是吡喃,称呋喃并吡喃;Ⅳ的基本环是呋喃,称噻吩并呋喃。
③杂环中杂原子数目不同时,含杂原子数目多的环优先;数目相同时,则含杂原子种类多的环优先。
例如:Ⅴ应称吡啶并哒嗪(杂原子数目多的优先);Ⅵ应称咪唑并噻唑(杂原子种类多的优先);但Ⅶ应称噻吩并吡咯(含氮杂环优先)。
④环的大小、杂原子的数目、种类都相同时,优先选择稠合前杂原子编号较小的杂环为基本环。
例如:Ⅷ应称吡嗪并哒嗪。
⑤含有共用杂原子的稠杂环,应视为两环都含有该共用杂原子来进行选择。
例如:Ⅸ应称为咪唑并噻唑(含杂原子种类多的优先)。
除以上规定外,尚有一些其他习惯使用的规定,此处不再赘述。
二、稠合方式的表达:为了将基本环与附加环的稠合方式表达清楚,应先将两部分各自按编号原则编号,再将基本环的每条边按编号方向依次用a、b、c、d……代表,然后将附加环稠合边原子序号写在前,基本环稠合边字母写在后,二者之间用“-”隔开,一起放到两环系名称之间的方括号内。
附加环稠合边原子序号在书写时应与基本环字母次序的方向一致,两者顺序相同时小数字在前,大数字在后;反之则大数字在前,小数字在后。
例如:该化合物两环稠合边编号方向相反,命名时应使其一致,所以应称为咪唑并[2,1-b]噻唑,而不称咪唑并[1,2-b]噻唑。
稠杂环化合物的命名规则
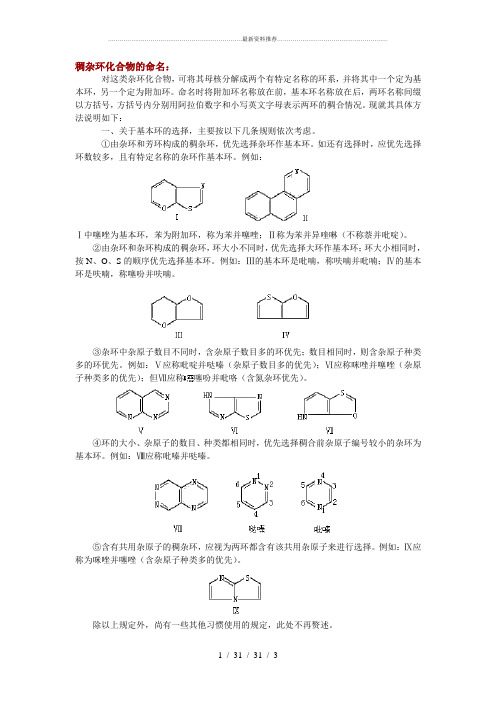
稠杂环化合物的命名:对这类杂环化合物,可将其母核分解成两个有特定名称的环系,并将其中一个定为基本环,另一个定为附加环。
命名时将附加环名称放在前,基本环名称放在后,两环名称间缀以方括号,方括号内分别用阿拉伯数字和小写英文字母表示两环的稠合情况。
现就其具体方法说明如下:一、关于基本环的选择,主要按以下几条规则依次考虑。
①由杂环和芳环构成的稠杂环,优先选择杂环作基本环。
如还有选择时,应优先选择环数较多,且有特定名称的杂环作基本环。
例如:Ⅰ中噻唑为基本环,苯为附加环,称为苯并噻唑;Ⅱ称为苯并异喹啉(不称萘并吡啶)。
②由杂环和杂环构成的稠杂环,环大小不同时,优先选择大环作基本环;环大小相同时,按N、O、S的顺序优先选择基本环。
例如:Ⅲ的基本环是吡喃,称呋喃并吡喃;Ⅳ的基本环是呋喃,称噻吩并呋喃。
③杂环中杂原子数目不同时,含杂原子数目多的环优先;数目相同时,则含杂原子种类多的环优先。
例如:Ⅴ应称吡啶并哒嗪(杂原子数目多的优先);Ⅵ应称咪唑并噻唑(杂原子种类多的优先);但Ⅶ应称噻吩并吡咯(含氮杂环优先)。
④环的大小、杂原子的数目、种类都相同时,优先选择稠合前杂原子编号较小的杂环为基本环。
例如:Ⅷ应称吡嗪并哒嗪。
⑤含有共用杂原子的稠杂环,应视为两环都含有该共用杂原子来进行选择。
例如:Ⅸ应称为咪唑并噻唑(含杂原子种类多的优先)。
除以上规定外,尚有一些其他习惯使用的规定,此处不再赘述。
二、稠合方式的表达:为了将基本环与附加环的稠合方式表达清楚,应先将两部分各自按编号原则编号,再将基本环的每条边按编号方向依次用a、b、c、d……代表,然后将附加环稠合边原子序号写在前,基本环稠合边字母写在后,二者之间用“-”隔开,一起放到两环系名称之间的方括号内。
附加环稠合边原子序号在书写时应与基本环字母次序的方向一致,两者顺序相同时小数字在前,大数字在后;反之则大数字在前,小数字在后。
例如:该化合物两环稠合边编号方向相反,命名时应使其一致,所以应称为咪唑并[2,1-b]噻唑,而不称咪唑并[1,2-b]噻唑。
杂环化合物

PhLi
N
+ LiH
N
CH3 N
N
NaNH2 130-160oC
NH2
CH3
N +
N
CH3 N
N NH2
3. 氧化还原反应
CH3
KMnO4
COOH N
N
N
KMnO4 / H+ N
COOH
CH3COOOH or H2O2
N
HNO3
+
N
H2SO4
O-
PCl3
+
N
N
吡啶-N-氧化物
O-
NO2
H NO2
H NO2
Ac2O
-10 oC
S NO2
磺化:
+ N
H
. SO3 100 oC N
+
. SO3 100 oC
O
N
N SO3H H
O SO3H
+
. SO3 100 oC
S
N
S SO3H
98% H2SO4
S
室温
S SO3H
Note: α-噻吩磺酸可溶于浓硫酸,可用于除去苯中含有的少量噻吩
傅-克酰基化:
+ (CH3CO)2O 200oC
N
H
N COCH3 H
+ (CH3CO)2O BF3 O
O COCH3
+ (CH3CO)2O H3PO4 S
S COCH3
N 浓 HNO3
N
N 发烟 H2SO4 O2N N
H
H
N
N
发烟 H2SO4
S HgSO4 , 250oC HO3S S
杂环化合物命名

杂环化合物的命名(一)有特定名称的稠杂环杂环化合物的命名比较复杂。
现广泛应用的是按IUPAC(1979)命名原则规定,保留特定的45个杂环化合物的俗名和半俗名,并以此为命名的基础。
我国采用“音译法”,按照英文名称的读音,选用同音汉字加“口”旁组成音译名,其中“口”代表环的结构。
见表14-1。
(二)杂环母环的编号规则当杂环上连有取代基时,为了标明取代基的位置,必须将杂环母体编号。
杂环母体的编号原则是:1.含一个杂原子的杂环含一个杂原子的杂环从杂原子开始编号。
见表14-1中吡咯、吡啶等编号。
2.含两个或多个杂原子的杂环含两个或多个杂原子的杂环编号时应使杂原子位次尽可能小,并按O、S、NH、N的优先顺序决定优先的杂原子,见表14-1中咪唑、噻唑的编号。
3.有特定名称的稠杂环的编号有其特定的顺序有特定名称的稠杂环的编号有几种情况。
有的按其相应的稠环芳烃的母环编号,见表14-1中喹啉、异喹啉、吖啶等的编号。
有的从一端开始编号,共用碳原子一般不编号,编号时注意杂原子的号数字尽可能小,并遵守杂原子的优先顺序;见表14-1中吩噻嗪的编号。
还有些具有特殊规定的编号,如表14-1中嘌呤的编号。
4.标氢上述的45个杂环的名称中包括了这样的含义:即杂环中拥有最多数目的非聚集双键(已经含有最多的双键)。
当杂环满足了这个条件后,环中仍然有饱和的碳原子或氮原子,则这个饱和的原子上所连接的氢原子称为“标氢”或“指示氢”。
用其编号加H(大写斜体)表示。
例如:N NH O O1H-吡咯2H-吡咯2H-吡喃4H-吡喃若杂环上尚未含有最多数目的非聚集双键(并非含有最多的双键),则多出的氢原子称为外加氢。
命名时要指出氢的位置及数目,全饱和时可不标明位置。
例如:N N OH H1,2,3,4-四氢喹啉2,5-二氢吡咯四氢呋喃含活泼氢的杂环化合物及其衍生物,可能存在着互变异构体,命名时需按上述标氢的方式标明之。
例如:NN NNNNNN HH9H-嘌呤7H-嘌呤(三)取代杂环化合物的命名当杂环上连有取代基时,先确定杂环母体的名称和编号,然后将取代基的名称连同位置编号以词头或词尾形式写在母体名称前或后,构成取代杂环化合物的名称。
第八章杂环化合物

H2N-
N
-SO2-NH-
N
第四节 苯稠杂环及稠杂环
一、苯稠杂环: 1.吲哚:
N H
CH2CHCOOH
N
NH2
H
CH2-CH2-NH2
N H
二、稠杂环: 嘌呤
N
N
NH N
NH23
O
N
N
HN
O
O
N HN
N HN
N
CH
CH
NN
H2N N N
H
H
N
O
N
NNΒιβλιοθήκη HH腺嘌呤(A) (6-氨基嘌呤)
鸟嘌呤(G)
O
呋喃
N H
吡咯
N
吡啶
N H
吲哚
N
N
S
噻唑
N H
咪唑
N
N
嘧啶
N
N
NN H
嘌呤
二、杂环化合物的命名
习惯采用译音法命名,即按外文谐音, 并以“口”字旁表示是环状化合物,如呋 喃(Furan)、吡啶(Pyridine)等。
• 杂环化合物编号原则如下:
1.当环上只有一个杂原子时,杂原子的编 号为1。如:
CH3
H3C O CH3
2,5-二甲基呋喃
N
4-甲基吡啶
2.当环上有两个相同杂原子时,连接有氢 原子或取代基的杂原子编号为1,并使另 一个杂原子的编号尽可能小。如:
CH3
N
N H
4-甲基咪唑
3.当环上有不相同的杂原子时,按氧、硫、 氮的顺序编号。如:
N
C2H5
S
5-乙基噻唑
第二节
1.吡咯:
N H
CH2-OH CH2OH
杂环化合物的分类和命名

杂环化合物的分类和命名n杂环苯环与单杂环的稠合杂环(苯并杂环)n稠杂环n两个或两个以上单杂环的稠合杂环nnnh17.1.2命名1.音译法以口字倚为杂环标志。
osnnh噻吩呋喃吡啶吡咯pyridinepyrrolefuramthiophene2.系统命名法nosh茂氧田硫田(环戊二烯)氮田nnn苯氮苯1,3-二氮苯3.取代杂环的命名①杂环的编号从杂原子起至依次1,2,3……(或:α,β,γ……)。
②如环上远不止一个卤原子时,则从o、s、n的顺序依次编号。
③存有两个相同卤原子的,需从甘胺h原子或替代基的已经开始编号。
④编号时特别注意卤原子或替代基的位次之和最轻。
h3c54n32nh214534nn13n2n1h52s2-氨基-4-甲基噻唑吡唑1ch31-甲基咪唑17.2五元杂环化合物――吡咯、呋喃、噻吩17.2.1结构1.经典结构nosh2.分子结构呋喃ooo:1s22s22p4噻吩sss:1s22s22p63s23p4吡咯nhnhn:1s22s22p3据现代物理方法证明:①呋喃、吡咯、噻吩是一个平面结构。
②环上的c原子和杂原子都就是以sp2杂化轨道成键的。
③五个没杂化的p轨道旋转轴环路平面,构成滑动共轭体系。
④属富电子芳环。
⑤环形π电子分布于杂环平面的上、下两方。
⑥共轭能共轭能kj/mol3.芳香性①合乎休克尔规则,π电子数为6。
2苯152噻吩125.5吡咯90.4呋喃71.1②芳香性比较(极易替代、容易差率、容易水解):苯>噻吩>吡咯>呋喃③表述环的稳定性:苯>噻吩>吡咯>呋喃17.2.2呋喃、噻吩、吡咯的制备o催化剂退羰基choni280℃o+nh3oal2o3430℃zno-cr2o3-mno2h2o400-415℃nhch3ch2ch2ch3+sch3ch=chch3ch3ch2ch=ch2650℃s+so2s帕尔-诺尔制备法:用1,4-二酮制备。
p2o5rosrrroorp2s5△r`nh2r17.2.3化学性质h+rnhr0.1431nm0.1371nm0.1423nm0.1370nm0.1429nm0.1371nmo0.1383nms0.1714nmn0.1383nm o1.73ds1.90dn1.58d非芳香性的杂环化合物只有诱导效应。
杂环化合物命名讲解

杂环化合物命名(一)特定杂环的俗名合半俗名IUPAC 原则规定,具有特定俗名和半俗名的杂环共45个SOHH SONNHH N以上杂环氢的位置不同者,把H (大写、斜体)及其标号放在词首,在并环上者,注明边号(用a 、b 、c 表示)。
O当杂原子在环上的位置不同时,可视为异构体。
S O几点说明(1)杂环的写法可以不同,但是位号不变。
(2)单杂环的编号从杂原子开始,并使其他杂原子或指示氢位号尽可能小;杂原子不同时,要使优先的杂原子号小,常见的位O ,S ,-NH-,-N=顺序;只含一个杂原子的单杂环,也可对杂原子旁的碳用αβγ进行编号。
(3)稠杂环有其固定的编号顺序,通常从一端开始,依次编号一周(公用碳不编号,如需编号时,用前一位加a,b,c 表示),并尽可能使杂原子,特别使优先的杂原子号小;也有的杂环按相应的环烃编号,此时杂原子编号最大(见咔唑,丫啶),嘌呤使个特例,不仅公用碳编号,且编号顺序也很特别。
(4)含两个以上杂原子的五元单杂环,其中至少含一个氮原子的通称“某唑”;含两个以上杂原子(至少一个位氮)的六元单杂环多称为“某嗪”;含氧的称“恶”;含硫的称“噻”。
例如:N Ni a z o l ei a z o l eSaz i n e (5)杂环已经含有最大数目的非聚集双键之外,还含有的饱和氢原子(两个二价元素中间的饱和氢不算)称做“指示氢”或“额外氢”或“标氢”。
指示氢不同的异构体,以其位号加“H ”(斜体大写)作词首来表示。
(6)若杂环尚未含有最大数目的非聚集双键,这样的饱和氢原子为外加氢。
命名时要指明加氢的位置和数目,全部饱和可以省略位置。
(7)含活泼氢的杂环及其衍生物,可能存在互变异构体,结构不同,名称也异;命名时尚需标明两种可能的位号。
(8)杂环母环的名称确定之后。
就可参照芳香化合物的命名方法,将环上取代基位置,数目及名称,以词首或词尾的形式加在环名的前后,有时杂环也可以作为取代基命名。
杂环化合物

N
or Na + C2H5OH
N H
(4).吡啶的亲核取代反应
+ NaNH2
N
100oC C6H5N(CH3)2
N
NH-Na+
H2O
N
NH2
亲核取代优先在α位上发生,如果α位上有取代基,则 反应在γ位上发生。
(2)喹啉
N
与吡啶类似, 喹啉有弱碱性(pKb=9.15)。
喹啉的亲电取代反应(如硝化、磺化、溴化 等)比吡啶容易,亲电试剂主要进攻苯环部分。 亲核取代反应则发生在吡啶环上,主要在2位取代。
N
H2/Ni
N
(2) 喹啉及其衍生物的制法 ——Skraup合成法 *****
+ NH2
OH OH OH H2C C CH2 H
浓H2SO4 NO2 , N
历程
H CH 2 CH 2
H CH CH 2
CH 2OH CHOH CH 2OH
CHO H2SO4 CH C6H5NH2 CH 2
H2S O4
五元杂环化合物
一. 五元杂环的结构与芳香性
N:2s2 2p
3
p 轨道 sp 2杂化
N
p轨道
H
s轨道
H
p 轨道
sp 2轨道
H O H
H H S H 噻吩
H
H
呋喃
N
1. 杂原子有一对电子参与环的共轭, (π56)是六电子五中心的 芳环,具有一定的稳定性;
2. 芳香性顺序:
环上电子云分布不均,芳香性不如苯。 电负性 O 、N、S 3.5 3.0 2.5
Br
RX(或RCOX) AlCl3
不反应
结论
第十五章-杂环化合物(D)

N
六元环
2. 按环的数目和连接方式分为: ①单杂环:
O
S
呋喃
噻吩
②稠杂环 :单杂环与苯环稠合而成 喹啉
N
(二)命名(其他国家多用习惯法 我国:音译法。同音汉字加“口”字)
1. 杂环母体的命名
O furan 呋喃
N H
S
pyrrole 吡咯
thiophene 噻吩
N pyridine
吡啶
N H
于β –位,反应条件苛刻。)
Br2 300℃
Br N
HNO3,H2SO4
NO2 N SO3H N
N
300℃ H2SO4 350℃
注意:不发生 付氏反应
3)亲核取代(与强亲核试剂反应,主要在α –位)
NaNH2
N
N
NH2
4)氧化与还原 (比苯稳定,环的氧化比苯难,同系物可被氧化)
CH3 N KMnO 4 _ OH COOH N
R4N OH > H2N
+
NH2
+
-
>
N
> 9.3
N .
4.7
_
8.8
N H
> (CH3)2NH > CH3NH2 > NH3 > CH3 > NH2 > O 2N
NH2
a. 与无机强酸成盐
+ HCl N
+
Cl
N H
b. 与卤烷成季铵盐
+ CH 3 I N
+
I
N CH 3
2)亲电取代(不如苯活泼,活性类似于硝基苯发生
0℃
S
+ CH3COONO 2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
稠杂环化合物的命名:
对这类杂环化合物,可将其母核分解成两个有特定名称的环系,并将其中一个定为基本环,另一个定为附加环。
命名时将附加环名称放在前,基本环名称放在后,两环名称间缀以方括号,方括号内分别用阿拉伯数字和小写英文字母表示两环的稠合情况。
现就其具体方法说明如下:
一、关于基本环的选择,主要按以下几条规则依次考虑。
①由杂环和芳环构成的稠杂环,优先选择杂环作基本环。
如还有选择时,应优先选择环数较多,且有特定名称的杂环作基本环。
例如:
Ⅰ中噻唑为基本环,苯为附加环,称为苯并噻唑;Ⅱ称为苯并异喹啉(不称萘并吡啶)。
②由杂环和杂环构成的稠杂环,环大小不同时,优先选择大环作基本环;环大小相同时,按N、O、S的顺序优先选择基本环。
例如:Ⅲ的基本环是吡喃,称呋喃并吡喃;Ⅳ的基本环是呋喃,称噻吩并呋喃。
③杂环中杂原子数目不同时,含杂原子数目多的环优先;数目相同时,则含杂原子种类多的环优先。
例如:Ⅴ应称吡啶并哒嗪(杂原子数目多的优先);Ⅵ应称咪唑并噻唑(杂原子种类多的优先);但Ⅶ应称噻吩并吡咯(含氮杂环优先)。
④环的大小、杂原子的数目、种类都相同时,优先选择稠合前杂原子编号较小的杂环为基本环。
例如:Ⅷ应称吡嗪并哒嗪。
⑤含有共用杂原子的稠杂环,应视为两环都含有该共用杂原子来进行选择。
例如:Ⅸ应称为咪唑并噻唑(含杂原子种类多的优先)。
除以上规定外,尚有一些其他习惯使用的规定,此处不再赘述。
二、稠合方式的表达:
为了将基本环与附加环的稠合方式表达清楚,应先将两部分各自按编号原则编号,再将基本环的每条边按编号方向依次用a、b、c、d……代表,然后将附加环稠合边原子序号写在前,基本环稠合边字母写在后,二者之间用“-”隔开,一起放到两环系名称之间的方括号内。
附加环稠合边原子序号在书写时应与基本环字母次序的方向一致,两者顺序相同时小数字在前,大数字在后;反之则大数字在前,小数字在后。
例如:
该化合物两环稠合边编号方向相反,命名时应使其一致,所以应称为咪唑并[2,1-b]噻唑,而不称咪唑并[1,2-b]噻唑。
又例如前面所见到的Ⅰ应称为苯并[d]唑(苯环的稠合边原子序号在此无需标出),Ⅳ称为噻吩并[2,3-b]呋喃,Ⅵ称为咪唑并[5,4-d]噻唑,Ⅷ称为吡嗪并[2,3-d]哒嗪。
三、整个稠杂环的编号:
当此类化合物分子中存在有其他取代基或官能团时,需要对整个化合物进行统一编号(此编号方式与表示稠合方式的编号无关),其编号方式应注意以下几点:
①应尽可能使所有杂原子都有最低位次,其次按O、S、NH、N的顺序选择优先编号的杂原子,例如:
②共用碳原子一般不编号(个别例外),但在满足上一条规则的前提下,应尽可能使其具有较低的序号(其编号方式是依整个分子的编号方向在其前一个原子的编号下加注“a”、“b”、“c”等)。
例如:下面化合物可有三种不同的编号方式,得到杂原子的编号均为1、4、5、8,但第一种共用碳原子的编号为4a,后两种则为8a,故正确的编号方式应为第一种。
③氢原子和指示氢的编号应尽可能低。
例如:
命名实例:。
