杆状病毒表达系统
昆虫表达系统介绍

杆状病毒是已知昆虫病毒中最大的类群发现最早、研究最多且实用意义也是最大的昆虫病毒。
杆状病毒表达载体系统Baculovirus expression vector systemBEVS自1983年问世以来Smith Summer1983Maeda et al 1984由于其具有高效的表达能力、安全易操作等特点已成为研究和生产各种原核、真核蛋白的用力而普及的工具已成功表达了大量的外源基因几乎覆盖了所有物种可开发利用的大部分基因。
1 分类杆状病毒——有囊膜的双股DNA大型病毒仅限于无脊椎动物有尾噬菌体目Caudovirales 杆状病毒科Baculoviridae 核型多角体病毒属NucleopolyhedrovirusNPV ———苜蓿蠖核型多角体病毒Autographa Californica NPV ———家蚕核型多角体病毒Bombyx mori MPV 颗粒体病毒属GranulovirusGV ———苹果蠹蛾颗粒体病毒Cydia pomonella GV 多角体与颗粒体的区别NPV和GV均有包涵体形式NPV的称多角体后者称为颗粒体多角体内含有许多病毒子都在宿主细胞核内存在颗粒体内含一个病毒子偶尔是两个绝大部分在核内形成但某些GV在胞浆中形成颗粒体2 发育循环杆状病毒包含两个独特的时相又称双相生活循环biphase life cycle 第一相出现在PI0-24hr 核衣壳于胞核内病毒发生基质上进行装配通过细胞质出芽获得囊膜这种病毒称为细胞释放型病毒子Cell-released virusCRV又称胞外型病毒Extracellular virusECV或出芽型病毒Budded virusBV 第二相出现在PI20-72hr 当20hr后核内出现病毒包涵体时第二相显著出现一直持续到感染细胞溶解为止72hr 随着第二相开始CRV急剧减少从第二相开始留在核内的核衣壳被封入核内新装配的囊膜中以后许多核内获得囊膜的病毒子被包埋入多角体蛋白的结晶基质中逐渐形成多角体。
杆状病毒——昆虫细胞表达系统

实验材料:1. 重组杆状病毒质粒:Bacmid/nsp-6及阳性对照Bacmid/CAT,已构建成功。
2. 昆虫细胞Sf9、High Five及其相关培养基、转染试剂均购自Invitrogen公司。
抗His单克隆抗体购自Oncogene公司,CAT-ELISA试剂盒购自Roche。
实验步骤:一、昆虫细胞转染:1. Sf9细胞计数,取6孔板中的两孔,每孔加入9×10 5个细胞(其中一孔设为正常对照),并以全培培养至少1小时,使细胞贴壁。
2.准备重组质粒和细胞转染试剂的混合物:a. 溶解1μg纯化重组杆状病毒重组质粒于100μl 无添加成分的Grace’s Medium。
b. 转染试剂充分摇匀后取6μl加入100μl 无添加成分的Grace’s Medium,混匀。
c. 将上述稀释好的质粒及稀释好的转染剂混匀,室温孵育20min。
3.重组质粒与转染剂混合液孵育的同时,以2ml无添加成分的Grace’s Medium洗涤待转染的一孔细胞并弃去洗液。
4.取0.8ml无添加成分的Grace’s Medium加入质粒与转染剂的混合液中,轻轻混匀后,总体积约为1ml。
加入上步洗涤后的细胞孔中,27℃继续培养5h。
5.移除质粒、转染剂混合物,加入2ml全培。
27℃湿盒孵育,直到病变现象产生。
二、病毒贮液的制备:1. 病毒感染晚期(正常24-72h)可见细胞停止生长、黏附,呈颗粒状外观。
即收集含病毒的培养上清,500g离心5min,去除细胞和碎片。
2. 上清即为P1病毒贮液,移入新的离心管中4℃避光保存。
长期保存分装冻存于-80℃。
3. 病毒贮液的扩增,按以下公式进行所需病毒P1贮液的量:感染所需病毒贮液量(ml)=[MOI(pfu/cell) ×细胞数÷病毒贮液效价(pfu/ml)]注:若不进行病毒空斑测定,P1贮液效价按照1×10 6到1×10 7计。
4. 扩增P1液制备P2病毒贮液方法如下:a. 转染当天,取2×106个细胞/孔加入六孔板中,贴壁生长至少1h。
昆虫杆状病毒表达系统(BEVS)

姓名:宋志瑞 专业:生物工程 学号: 2015304120207
NO.1
BEVS 简介
BEVS简介
昆虫杆状病毒表达载体系统(BEVS)是基于昆虫杆状病 毒及其宿主细胞建立起来的表达体系;是继大肠杆菌, 酵母,哺乳动物细胞表达系统建立起来的,始于上世纪 80年代。
NO.2
BEVS 优点
2
Bac-to-Bac
3
BaculoDirect源自BacPAKBac-to-Bac
BaculoDirect
三大体系的区别
NO.5
BEVS常用宿主
常用宿主
Thanks
√
√ √ Sometimes Sometimes
Glycosylation
Acylation
√
√
表达高
加工 修饰
安全
B E VS
高效
容量大
NO.3
BEVS 原件
BEVS原件
1. 转移载体 2. 杆状病毒(AcNPV) 3. 宿主(培养细胞或虫体)
NO.4
BEVS三大系统
BEVS三大系统
1
BacPAK
BEVS优点
Features Simple to use Protein size Multiple gene expression Signal peptide cleavage BEVS √ unlimited √ √ Bacterial √ <100kD
Intron splicing
Functional protein Phosphorylation
杆状病毒昆虫细胞表达系统:原理探微与常见问题解决指南

杆状病毒昆虫细胞表达系统:原理探微与常见问题解决指南在生物技术的广阔天地中,杆状病毒昆虫细胞表达系统以其独特的魅力和广泛的应用前景,正逐渐受到研究者们的青睐。
这一系统巧妙地利用经过改造的杆状病毒基因组,在大肠杆菌中高效复制,并通过精密的转座过程将目的基因精准地插入到bacmid的特定位点。
这一过程不仅展示了生物技术的精巧与奇妙,更为科研工作者提供了强大的工具,用以探索和研究蛋白质的功能与结构。
然而,任何技术在实际应用中总会遇到一些问题和挑战。
为了帮助大家更好地掌握和运用这一系统,本文将深入探讨其原理,并分享在实际操作中可能遇到的常见问题及其解决方案,以期为大家的科研工作提供有益的参考和指导。
杆状病毒昆虫细胞表达系统原理:经过精心改造的病毒基因组(即杆状病毒穿梭载体Bacmid)在此系统中展现了非凡的复制能力。
它们能在大肠杆菌如DH10Bac菌株中自如地繁衍。
这一复制过程得益于供体质粒中目的基因两侧所锚定的Tn7转座原件。
这些原件与DH10Bac菌株中的helper质粒所编码的转座酶活性相互作用,将目的基因精准地转座到bacmid的特定位点上。
当目的基因成功插入后,会导致bacmid上的LacZ基因发生移码,进而通过蓝白斑筛选法轻松鉴定出阳性重组bacmid。
经过提取后,这些bacmid便能转染昆虫细胞,开启其在昆虫细胞中的高效表达之旅。
昆虫-杆状病毒表达平台的常见问题解答1、义翘神州是否接受已构建的表达载体进行蛋白表达?对于众多常规蛋白表达项目,义翘神州确实欢迎并接受客户直接提供的表达载体,如pFastBac等,进行专业的蛋白表达。
我们深知每个蛋白的特性独一无二,因此,我们始终致力于与客户保持紧密的沟通,共同探讨并确定最佳的纯化方案,确保最终交付的产品符合客户的期望和需求。
我们承诺,通过我们的专业知识和丰富经验,将客户的表达载体转化为高质量的蛋白产品。
2、义翘神州是否接受包被好的杆状病毒直接进行蛋白表达?对于一些常规蛋白表达项目我们同样也可以直接使用客户制备好的杆状病毒进行蛋白表达,我们也会根据蛋白的实际特性与客户沟通交流纯化方案和最终交付形式。
杆状病毒表达系统简介-9页精选文档

体外基因表达系统包括原核细胞系统和真核细胞系统。
原核细胞系统主要是大肠杆菌细胞,它操作简便、周期短收益大及表达产物稳定,但是表达基因的相对分子质量有限,不宜过大,且不能对表达产物进行一些翻译后加工、修饰。
真核细胞系统包括 CHO等哺乳动物细胞、酵母细胞和昆虫细胞等。
昆虫细胞表达系统(即杆状病毒表达系统)具有独特的生物学特性,日益受到人们的重视。
1、杆状病毒的生物学特性杆状病毒只来源于无脊椎动物,虽然已发现600多种杆状病毒,但进行分子生物学研究的不到20种。
杆状病毒的基因组为单一闭合环状双链DNA分子,大小为80~160 kb,其基因组可在昆虫细胞核复制和转录。
DNA复制后组装在杆状病毒的核衣内,后者具有较大的柔韧性,可容纳较大片段的外源DNA插入,因此是表达大片段DNA的理想载体。
其中,用作外源基因表达载体的杆状病毒,目前仅限于核型多角体病毒(nuclear polyhedrosis virus,NPV)。
该病毒颗粒在细胞内可由多角体蛋白包裹形成长度约1~5 m 的包含体病毒,呈多角体形状。
核型多角体病毒有两种形式:一种为包含体病毒(occluded virus,OV),另一种则为细胞外芽生病毒(budded virus,BV)。
它们在病毒感染中扮演的角色不同,包含体病毒是昆虫间水平感染的病毒形式,昆虫往往是食入污染OV的食物后引起感染。
包含体病毒外层裹了一层蛋白晶体,即为29 000的多角体蛋白,它对病毒的水平感染起以下作用:①保护病毒颗粒在外界传播过程中免遭环境因素的破坏而失活。
②保证病毒颗粒在适当的位置释放,引起感染。
昆虫中肠上皮局部的强碱性环境(pH=10.5),可使病毒颗粒释放蛋白酶溶解多角体。
BV病毒是个体内细胞间的感染形式,由细胞芽生出BV,进入血淋巴系统中感染其它部位的细胞或直接在临近细胞内感染。
近几十年,有关杆状病毒基因结构、功能和表达调节的研究进展迅速,其中研究最深入的是苜蓿银蚊夜蛾(autogra— phacalifornica)多核型多角体病毒(multiple nuclear polyhedro-sis virus,MNPV),简称AcMNPV或AcNPV。
bac-to-bac expression system

Thank you!
Bac-to-Bac expression system
专业:生物化学与分子生物学 姓名:蒋琢璞 学号:200730200
简介
杆状病毒表达系统(Baculovirous Expression Vector System,BEVS)与细菌, 酵母,哺乳动物细胞一起被公认为当今世界 的基因工程的四大表达系统。它作为一种新 型的表达系统,因为其许多特有的优势特点, 逐渐引起了人们越来越多的关注
基本原理
AcNPV为环状双链的DNA病毒,分子量在 90~130kd,是目前应用最广泛的杆状病毒 表达载体。其中的多角体蛋白(Polyhedrin) 对于感染过程不是必需的,因此可以用一 个外源基因来代替多角体蛋白基因,用这 样一个重组的杆状病毒来感染昆虫细胞, 从而实现目的蛋白的高效表达。
为了在昆虫细胞中表达外源基因,重组病毒 质粒的构建和纯化筛选,常常需要依赖基 本的转染和斑点分析方法,这个过程通常 会花费4~6周。然而,如果利用一个既能 在大肠杆菌(Escherichia coli)中进行复制 的,又能感染敏感的鳞翅目昆虫细胞的病 毒穿梭载体(bacmid),那么就可以将周期 降低到几天。
特点
能对高效表达的蛋白质进行较完善的翻译后加工,如糖基 化,磷酸化,酰基化,信号肽的切除等; 与其他真和细胞表达系统相比能获得重组蛋白的高水平表 达,最高甚至可达到细胞总蛋白的50%; 对脊椎动物无感染性,并且也已经证明它们的启动子在大 多数的哺乳动物细胞中也是没有活性的,因此这对于表达 一些致癌基因和潜在的毒蛋白比其他的表达系统更有优势; 能容纳大分子片段的插入和表达; 能同时在一个细胞和载体上表达多个外源基因; 能保证高表达的外源蛋白在细胞内进行正确的折叠,二硫 键的搭配等。
Bac-to-bac中文说明书
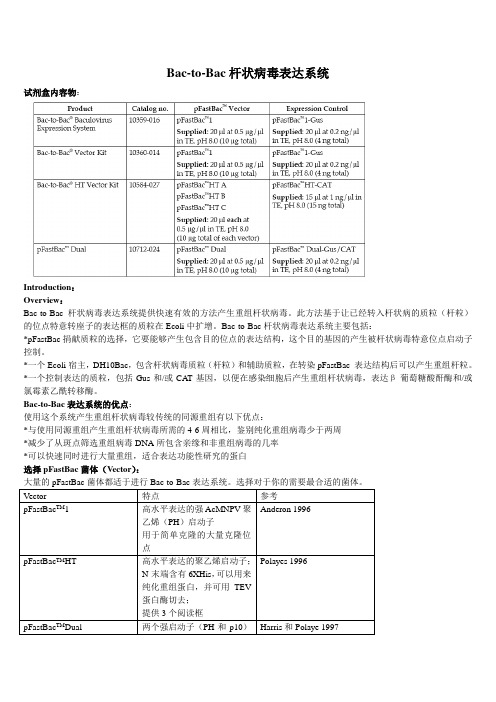
Bac-to-Bac杆状病毒表达系统试剂盒内容物:Introduction:Overview:Bac-to-Bac杆状病毒表达系统提供快速有效的方法产生重组杆状病毒。
此方法基于让已经转入杆状病的质粒(杆粒)的位点特意转座子的表达框的质粒在Ecoli中扩增。
Bac-to-Bac杆状病毒表达系统主要包括:*pFastBac捐献质粒的选择,它要能够产生包含目的位点的表达结构,这个目的基因的产生被杆状病毒特意位点启动子控制。
*一个Ecoli宿主,DH10Bac,包含杆状病毒质粒(杆粒)和辅助质粒,在转染pFastBac 表达结构后可以产生重组杆粒。
*一个控制表达的质粒,包括Gus和/或CAT基因,以便在感染细胞后产生重组杆状病毒,表达β-葡萄糖酸酐酶和/或氯霉素乙酰转移酶。
Bac-to-Bac表达系统的优点:使用这个系统产生重组杆状病毒较传统的同源重组有以下优点:*与使用同源重组产生重组杆状病毒所需的4-6周相比,鉴别纯化重组病毒少于两周*减少了从斑点筛选重组病毒DNA所包含亲缘和非重组病毒的几率*可以快速同时进行大量重组,适合表达功能性研究的蛋白选择pFastBac菌体(Vector):大量的pFastBac菌体都适于进行Bac-to-Bac表达系统。
选择对于你的需要最合适的菌体。
指南用途:指南提供了一个对于Bac-to-Bac表达系统的概述,并对以下提供指导:1、克隆目的基因到pFastBac TM供体质粒的选择2、转化pFastBac TM 结构到最高效的DH10Bac TM产生重组质粒3、转染重组质粒DNA到昆虫细胞产生重组杆状病毒4、扩增滴定(Amplify and titer)杆状病毒株,使用病毒株感染昆虫细胞表达目的重组蛋白重要的:Bac-to-Bac杆状病毒表达系统是用来帮助你产生重组杆状病毒,在昆虫细胞中进行高水平表达目的基因的系统。
虽然他可以帮助你很容易的产生杆状病毒表达你的重组蛋白,但是使用这系统更倾向于有杆状病毒生物学和昆虫表达背景的使用者。
杆状病毒表达系统00000001

昆虫杆状病毒系统高效表达重组蛋白●杆状病毒表达系统介绍●杆状病毒蛋白表达系统的优势●杆状病毒表达载体系统(BEVS)●杆状病毒表达宿主细胞●表达优化条件●翻译后修饰对蛋白表达的影响●高通量表达●总结杆状病毒介绍1.杆状病毒是一类具有囊膜包裹的双链环状DNA病毒。
2.杆状病毒在其生命周期中有两种不同的形态:一种为出芽型病毒(budded virus, BV),另一种为包含体病毒(Occlusion‐derived virus, OV)。
3. BV由糖蛋白GP64包裹的单一囊膜蛋白和膜蛋白构成。
4. OV由蛋白结晶基体包裹的多囊膜病毒粒子。
5. 研究最多的杆状病毒株为苜蓿银蚊夜蛾(autogra—phacalifornica)多核型多角体病毒(multiple nuclearpolyhedro‐sis virus,MNPV),简称AcMNPV或AcNPV。
6. AcMNPV只侵染鳞翅类幼虫。
杆状病毒生命周期●早期(0‐6h PI)•核衣壳迁移到细胞核•病毒DNA释放•开始早期基因表达●晚期(6‐24h PI)•更多DNA复制•新产生的核衣壳离开细胞核,随后在离开细胞质•的过程中得到囊膜蛋白•产生新的出芽病毒●极晚期Courtesy: Dr. Linda Lua, The University of Queensland, Australia •出芽病毒减少•核衣壳在细胞核内得到囊膜蛋白形成MNPVs•MNPVs以多晶体形式出芽,主要是多角体蛋白,形成包含体病毒。
多角体启动子是杆状病毒表达载体系统的主要元件。
优点缺点大肠杆菌成本低、表达量高。
缺乏蛋白质翻译后加工机制;目的蛋白不可溶,蛋白生物活性低。
酵母表达量高,可以翻译后加工,易实现高密度发酵。
蛋白质量不理想。
哺乳动物细胞重组蛋白生物活性高。
成本高;表达水平低,技术和环境要求高。
昆虫细胞重组蛋白生物学活性高;表达水平高;能同时表达多个基因。
重组蛋白糖基化程度低。
Bac to Bac

Bac-to-Bac杆状病毒表达系统是一种快速、高效产生重组苜蓿银纹夜蛾核型多角体病毒(AcNPV)的技术(Luckow et al., 1993),利用细菌转座子原理,在大肠杆菌内就能完成重组病毒的构建,取名为Bac-to-Bac表达系统,意即从细菌(bacterium)到杆状病毒(baculovirus),革命性地改变了重组昆虫杆状病毒的构建方法。
其基本原理为:将一个改造后的AcNPV基因组转化入大肠杆菌,使它像普通质粒一样能在细菌中复制(由于太大,只限单拷贝),将其称之为杆状病毒穿梭载体(baculovirus shuttle vector,又称病毒质粒baculovirus plasmid,将其首尾合写而成为Bacmid),通过位点特异性转座,在大肠杆菌内完成病毒基因组的重组。
杆状病毒穿梭载体Bacmid含有细菌单拷贝数mini-F复制子、卡那霉素抗性选择标记基因及编码β-半乳糖苷酶α肽的部分DNA片段。
在lacZα基因的N氨基末端插入一小段含有细菌转座子Tn7整合所需的靶位点(mini-att Tn7),但它的插入不影响lacZα基因的表达阅读框。
将杆状病毒穿梭载体(130kb)转化入大肠杆菌DH10β,获得转化子将其命名为DH10Bac。
因此,杆状病毒穿梭载体像一个大质粒一样,可以在大肠杆菌中增殖并使细菌细胞获得卡那霉素抗性,且与存在与受体菌染色体上的lacZα缺失产生互补,在IPTG诱导和X-gal或Blue-gal生色底物存在下转化体产生蓝斑(lacZ+)。
重组Bacmid通过pFASTBAC供体质粒(donor plasmid)上的mini-Tn7转座子,在另一个辅助质粒(helper plasmid,13.2kb)的功能作用下将外源目的基因插入到Bacmid中来完成。
Helper plasmid表达转座酶并含有四环素(tetracycline)抗性基因。
pFASTBAC系列供体质粒具有共同的特征:每个质粒都含有杆状病毒启动子(polh或p10启动子),在mini-Tn7左右臂间由一个完整的表达框,包括庆大霉素(gentamincin)抗性基因、杆状病毒启动子、多克隆位点及SV40 poly(A)。
杆状病毒表达系统简介

体外基因表达系统包括原核细胞系统和真核细胞系统。
原核细胞系统主要是大肠杆菌细胞,它操作简便、周期短收益大及表达产物稳定,但是表达基因的相对分子质量有限,不宜过大,且不能对表达产物进行一些翻译后加工、修饰。
真核细胞系统包括 CHO等哺乳动物细胞、酵母细胞和昆虫细胞等。
昆虫细胞表达系统(即杆状病毒表达系统)具有独特的生物学特性,日益受到人们的重视。
1、杆状病毒的生物学特性杆状病毒只来源于无脊椎动物,虽然已发现600多种杆状病毒,但进行分子生物学研究的不到20种。
杆状病毒的基因组为单一闭合环状双链DNA分子,大小为80~160 kb,其基因组可在昆虫细胞核复制和转录。
DNA复制后组装在杆状病毒的核衣内,后者具有较大的柔韧性,可容纳较大片段的外源DNA插入,因此是表达大片段DNA的理想载体。
其中,用作外源基因表达载体的杆状病毒,目前仅限于核型多角体病毒(nuclear polyhedrosis virus,NPV)。
该病毒颗粒在细胞内可由多角体蛋白包裹形成长度约1~5 m的包含体病毒,呈多角体形状。
核型多角体病毒有两种形式:一种为包含体病毒(occluded virus,OV),另一种则为细胞外芽生病毒(budded virus,BV)。
它们在病毒感染中扮演的角色不同,包含体病毒是昆虫间水平感染的病毒形式,昆虫往往是食入污染OV的食物后引起感染。
包含体病毒外层裹了一层蛋白晶体,即为29 000的多角体蛋白,它对病毒的水平感染起以下作用:①保护病毒颗粒在外界传播过程中免遭环境因素的破坏而失活。
②保证病毒颗粒在适当的位置释放,引起感染。
昆虫中肠上皮局部的强碱性环境(pH=10.5),可使病毒颗粒释放蛋白酶溶解多角体。
BV病毒是个体内细胞间的感染形式,由细胞芽生出BV,进入血淋巴系统中感染其它部位的细胞或直接在临近细胞内感染。
近几十年,有关杆状病毒基因结构、功能和表达调节的研究进展迅速,其中研究最深入的是苜蓿银蚊夜蛾(autogra— phacalifornica)多核型多角体病毒(multiple nuclear polyhedro-sis virus,MNPV),简称AcMNPV或AcNPV。
杆状病毒表达系统(昆虫细胞的培养及杆状病毒滴度测定) PPT

杆状病毒滴度测定
两种病毒滴度测定方法的比较:
空斑实验法测定滴度依赖于病毒在感染细胞中的复制以及感染 周边细胞形成局灶型病变;而免疫染色法只需要病毒感染靶细 胞并表达病毒所编码的蛋白。因此,免疫染色法(infectious units per ml, or IFU/ml)测定病毒滴度需要的时间比空斑法 (PFU/ml)更短。
获得重组杆状病毒——转染Sf9 cells
1. 小提好的Bacmid DNA,置4 ℃不超过1周
2. 转染试剂:Cellfectin® ⅡReagent
3. 转染后细胞的形态变化
细胞 变大
增殖明显变慢 或不增殖
脱落 或
融合(VSV/G)
裂解
4. 收毒,短期内4 ℃避光保存,长期保存分装后置-80 ℃
杆状病毒表达系统(昆虫细胞的培养及杆状 病毒滴度测定)
杆
昆虫细胞的培养
状
病 重组pFastBac质粒的构建
毒
表
重组Bacmid的产生与鉴定
达
获得重组杆状病毒
系
统
蛋白表达&病毒扩大
Overview
Bac-to-Bac Baculovirus Expression System能快速并有 效的获得重组杆状病毒,其重组是基于供体质粒表达盒 与杆状病毒穿梭载体Bacmid间发生位点特异性转座。
pipetting across the monolayer scraping cell scrapers hitting the flask against the palm of your hand
Preservation:
90% serum, 10% DMSO 严格程序降温,-80 ℃过夜后转移液氮保存。
Bac-to-bac中文说明书

Bac-to-Bac杆状病毒表达系统Introduction:Overview:Bac-to-Bac杆状病毒表达系统提供快速有效的方法产生重组杆状病毒。
此方法基于让已经转入杆状病的质粒(杆粒)的位点特意转座子的表达框的质粒在Ecoli中扩增。
Bac-to-Bac杆状病毒表达系统主要包括:*pFastBac捐献质粒的选择,它要能够产生包含目的位点的表达结构,这个目的基因的产生被杆状病毒特意位点启动子控制。
*一个Ecoli宿主,DH10Bac,包含杆状病毒质粒(杆粒)和辅助质粒,在转染pFastBac 表达结构后可以产生重组杆粒。
*一个控制表达的质粒,包括Gus和/或CAT基因,以便在感染细胞后产生重组杆状病毒,表达β-葡萄糖酸酐酶和/或氯霉素乙酰转移酶。
Bac-to-Bac表达系统的优点:使用这个系统产生重组杆状病毒较传统的同源重组有以下优点:*与使用同源重组产生重组杆状病毒所需的4-6周相比,鉴别纯化重组病毒少于两周*减少了从斑点筛选重组病毒DNA所包含亲缘和非重组病毒的几率*可以快速同时进行大量重组,适合表达功能性研究的蛋白选择pFastBac菌体(Vector):大量的pFastBac菌体都适于进行Bac-to-Bac表达系统。
选择对于你的需要最合适的菌体。
指南用途:指南提供了一个对于Bac-to-Bac表达系统的概述,并对以下提供指导:1、克隆目的基因到pFastBac TM供体质粒的选择2、转化pFastBac TM 结构到最高效的DH10Bac TM产生重组质粒3、转染重组质粒DNA到昆虫细胞产生重组杆状病毒4、扩增滴定(Amplify and titer)杆状病毒株,使用病毒株感染昆虫细胞表达目的重组蛋白重要的:Bac-to-Bac杆状病毒表达系统是用来帮助你产生重组杆状病毒,在昆虫细胞中进行高水平表达目的基因的系统。
虽然他可以帮助你很容易的产生杆状病毒表达你的重组蛋白,但是使用这系统更倾向于有杆状病毒生物学和昆虫表达背景的使用者。
杆状病毒表达系统——有效的VLP构建工具

杆状病毒表达系统——有效的VLP构建工具刘拂晓1,2 柳增善2 王志亮1【摘要】杆状病毒表达系统是以杆状病毒为外源基因载体,昆虫细胞或活体昆虫为受体的真核表达系统。
相对于其他表达系统,杆状病毒表达系统具有特殊的优势:杆状病毒基因组作为表达载体可以容纳更多外源基因;杆状病毒极晚期启动子能有效调控外源蛋白的表达;昆虫细胞作为受体能够对外源蛋白进行加工修饰;杆状病毒通常只感染节肢动物,不会对人畜构成危害。
因此,该系统越来越受到人们的重视,并已应用于亚单位疫苗的研发与生产,特别其对于构建病毒样颗粒,即由一种或多种病毒结构蛋白自行装配而成且不含病毒基因组的蛋白颗粒,具有不可比拟的优势。
对此做详细评述并展望病毒样颗粒疫苗的发展趋势。
【期刊名称】生物技术通报【年(卷),期】2012(000)006【总页数】7【关键词】杆状病毒昆虫细胞病毒样颗粒杆状病毒表达系统疫苗1983年,Smith等[2]成功实践了美国学者Miller的提出的杆状病毒作为载体在昆虫细胞中表达外源基因的可行性理论:他们将干扰素基因插入至苜蓿银纹夜蛾核型多角体病毒(Autographa californi-ca nuclear polyhedrosis virus,AcNPV)表达载体,然后将其转染草地贪夜蛾(Spodoptera frugiperda,Sf)细胞,成功表达了具有生物活性的人β干扰素。
此后,杆状病毒蛋白表达技术逐步建立并完善起来。
相对于传统大肠杆菌、酵母及哺乳动物细胞蛋白表达技术,杆状病毒技术在病毒样颗粒(virus-like particle,VLP)的构建及应用方面具有不可比拟的优势。
VLP是含有一个或多个病毒结构蛋白的空心颗粒,高度模仿真实病毒的衣壳空间构象而不含其基因组。
大多数VLP 是良好的免疫原,既可诱导体液免疫又可诱导细胞免疫[3-5]。
随着杆状病毒蛋白表达技术的成熟,利用其构建VLP的报道也屡见不鲜。
1 杆状病毒分子生物学根据国际病毒分类委员会最新病毒分类报告,杆状病毒科(Baculoviridae)分为4个属,即α杆状病毒属(Alphabaculovirus)、β杆状病毒属(Betabaculovirus)、δ杆状病毒属(Deltabaculovirus)、γ杆状病毒属(Gammabaculovirus)。
杆状病毒表达载体是什么?

杆状病毒表达载体是什么?
结构组成及表达元件
杆状病毒表达系统的基本元件:(1)启动子:多个启动子同时表达多个外源基因。
(2)poly A加尾信号: (3)同源重组序列。
(4)穿梭载体必需元件。
除带有病毒自身的复制起始位点外,还带有pUC质粒的复制子及以ampr,可以在细菌内进行扩增。
(5)筛选标记。
特点或优点
①重组蛋白具有完整的生物学功能:接近天然蛋白。
②能进行翻译后的加工修饰:研究糖基化对蛋白质结构与功能影响方面的理想模型。
③表达水平高:最高可使目的蛋白的量达到细胞总蛋白的50%。
④能容纳大分子的插入片段:上限未知。
⑤能同时表达多个基因:在同一细胞内同时表达多个基因。
⑥能表达基因组DNA:昆虫杆状病毒表达系统具有剪切的功能。
⑦对重组蛋白进行定位的功能:如将核蛋白转送到细胞核上,膜蛋白则定位在膜上,分泌蛋白则可分泌到细胞外等。
备注
杆状病毒科病毒,杆状病毒颗粒,双链闭合环状DNA病毒,专一性感染无脊椎动物将外源基因先克隆到转移载体上,再与病毒基因组共同转染细胞,通过细胞内的同源重组获得带有外源基因的重组病毒的策略。
杆状病毒表达载体系统生产重组蛋白

杆状病毒表达系统的优缺点
优点 ❖ 对外源基因容量大 ❖ 适合表达细胞毒性蛋白 ❖ 安全性且表达产量高 ❖ 后加工过程完全 ❖ 可以同时表达多个外源基因 ❖ 体内表达
❖ 杆状病毒表达载体系统的建立和发展,被誉为20 世纪80 年代真核表达研究领域的一个重大进展,现已成为基因 工程四大表达系统(即杆状病毒、大肠杆菌、酵母、哺乳 动物细胞表达系统)之一 。
❖ 杆状病毒表达载体系统主要包括苜蓿银纹夜蛾核型多角 体病毒 (Autographa californica multiple nuclear polyhedrosis virus, AcMNPV )表达系统和家蚕核型多 角体病毒(Bombyx mori nuclear polyhedrosisi virus, BmNPV )表达系统。
弃滤液。重复洗涤一次。 ❖ 9 室温或风干DNA,加入50-80ulEluent溶液,冰上溶解
10min ,4℃保存。
Sf9细胞转染
❖ 1.37℃预热Sf900TM- III SFM培养基; ❖ 2.准备重组质粒和细胞转染试剂的混合物:
a.溶解5μl纯化的杆状病毒重组质粒于100μl Sf900TMIII SFM培养基;
缺点 ❖ 瞬时表达 ❖ 糖基化简单
2:基本原理
❖ 1:目的基因插入转移载体。 ❖ 2:目的基因转移到病毒基因组靶位点,空斑纯
化获得重组病毒。
❖ 3:重组病毒感染宿主培养细胞或幼虫。
❖ 4:纯化目的蛋白
杆状病毒表达载体的构建
❖ 转移载体 通常由三部分组成: ❖ E. coli质粒的复制原点和抗生素抗性基因(如Ampr),保
[医学]杆状病毒表达系统(昆虫细胞的培养及杆状病毒滴度测定)
![[医学]杆状病毒表达系统(昆虫细胞的培养及杆状病毒滴度测定)](https://img.taocdn.com/s3/m/39cdc444964bcf84b9d57bd9.png)
DH10Bac:杆状病毒穿梭载体Bacmid + 辅助质 粒
Bac-to-Bac 表达系统的组成和工作原理
Bac-to-Bac 表达系统的组成和工作原理
Expermiantal outline
昆虫细胞的培养
Insect Cell Lines:
用途
疾病诊断 病毒分离株的鉴定 不同病毒株的抗原关系研究 疫苗免疫原性的评 免疫血清的质量评价 测定实验动物血清中是否存在抗体
材料
1. 病毒
(1)冻存的病毒不能重复使用 (2)进行中和实验前,需先进行病毒滴定(TCID50)的滴定
进行病毒定量
2. 血清样品
(1)血清样品分装冻存于-20℃ ,一般不要反复冻融3次以上。 (2)血清样品不溶血,不长期冻存,以减少对细胞的毒性。 (3)需要有阳性和阴性对照血清,实验前需56℃灭活30分钟。
杆状病毒滴度测定
两种病毒滴度测定方法的比较:
空斑实验法测定滴度依赖于病毒在感染细胞中的复制以及感染 周边细胞形成局灶型病变;而免疫染色法只需要病毒感染靶细 胞并表达病毒所编码的蛋白。因此,免疫染色法(infectious units per ml, or IFU/ml)测定病毒滴度需要的时间比空斑法 (PFU/ml)更短。
将96孔细胞培养板放入37 ℃ 5% CO2培养箱中作用 45 min—60 min。
感作完成后每孔加入100 µl细胞悬液,继续置37℃ 5% CO2培养箱培养,逐日观察并记录结果,一般要 观察4-5天。
结果计算,按Reed-Muench两氏法或Karber法进 行。
中和效价(PD50)的计算:
(2)置37 ℃,5 % CO2温箱中培养72 h后,收取细胞上清。 (3)详细阅读说明书的实验步骤(不同牌子试剂盒稍有不
昆虫杆状病毒细胞表达系统 课件

5) Capacity to express unspliced genes
Insect cells have the capability to perform intron/exon splicing. However, certain virus-, tissue- or species-specific splicing patterns will not be obtained if they require the presence of particular splicing factors which are not available in the infected insect cell environment. In general, for high protein expression levels, a cDNA insert rather than a genomic DNA fragment is recommended.
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
同源重组:先将外源基因克隆到转移载体上,然后与线性 化Bacmid上共转染转染昆虫细胞,获得重组杆状病毒:
“转座”和“同源重组”目前都在使用中。 “转座”方式的代表是ThermoFisher的Bac-to-Bac系统。 采用“同源重组”方式的有Clontech的BacPAK系统、OET 的FlashBac系统,以及Bacmid Ltd.的qBac系统。 这两种方式与外源基因的表达量无关。
J Virol. 1993 Aug;67(8):4566-79. Luckow VA, Lee SC, Barry GF, Olins PO.
Bacmid polyhedrin位点附近序列细节: 目前使用的Bacmid大都源于这个Bacmid。
获得重组病毒的方式
转座:先将外源基因克隆到转移载体上,然后在大肠杆菌 中通过转座,将外源基因转移到Bacmid上。提取重组 Bacmid,转染昆虫细胞,获得重组杆状病毒:
无论如何,相对于其他表达系统,杆状病毒表达载体系统 (BEVS)是个比较均衡的表达系统:
经过长期优化,杆状病毒表达载体系统的产量已经有了极 大的提高:
目前外源蛋白的生产成本大幅度下降,使杆状病毒表达载 体系统能进. Kaba et al. / Journal of Virological Methods 122 (2004) 113–118
敲除p26,p10,p74极大地提高了外源基因的产量:
Cell Biol Toxicol (2010) 26:57–68
糖基化改造 把昆虫细胞中缺少的糖基化酶克隆到Bacmid上,使蛋白的 糖基化更像哺乳动物细胞:
用重组的质粒和野生型的AcMNPV共同感染Sf细胞。
得到的病毒通过空斑筛选(0.5%),得到重组病毒。
用重组病毒感染Sf细胞,得到β-干扰素。
解决重组效率太低的问题
1990年P. A. Kitts把一个Bsu36I位点引入到多角体基因附近。 用Bsu36I线性化的AcMNPV后,重组效率提高15-150倍, 30%的空斑是阳性克隆。
杆状病毒表达载体系统
1981年L. K. Miller根据AcMNPV分子生物学性质及现代分 子生物学技术,从理论上阐述了杆状病毒作为载体表达外 源基因的可行性。 1983年G. E. Smith等成功地利用AcMNPV作为载体在Sf细 胞中表达了人β-干扰素基因,完成了从理论到实践的飞跃。
G. E. Smith将AcMNPV的EcoRI-I片段(包含多角体蛋白基 因)克隆到pUC8质粒上,然后把人β-干扰素基因克隆到 BamHI位点。
杆状病毒表达系统
西北农林科技大学生命科学学院 2018年
杆状病毒简介
杆状病毒是一类专一性感染节肢动物的DNA病毒,病毒粒 子呈杆状,基因组为双链环状DNA分子,DNA以超螺旋 形式压缩包装在杆状衣壳内,大小在90~180 Kb之间。模 式种是苜蓿银纹夜蛾核型多角体病毒(AcMNPV). 核型多角体病毒有两种形式:一种为芽生病毒(budded virus, BV) ,另一种则为包涵体病毒(occluded virus, OV)。
budded virus
occluded virus
杆状病毒生活周期
芽出病毒: 可以通过细胞细胞间感染进 行传播。 包涵体病毒: 释放到环境中 后,通过昆虫 摄食进行传播。 如果仅用于感 染昆虫细胞系, 包涵体形成相 关的基因都不 是必需的。
杆状病毒基因表达的不同表达时相
立即早期 延迟早期 晚期 极晚期:该时相表达 的蛋白(polyhedrin and p10)与包涵体 形成相关,并且表达 量极高。生物工程中 可以利用这两个蛋白 的启动子表达外源蛋 白。
1993年P. A. Kitts把两个Bsu36I位点一起引入,结果使重组 效率达到90%,但还是需要空斑筛选(多角体,蓝白斑)。
直接通过病毒基因组DNA与转移载体(Transfer vector)重组示意图
构建Bacmid
1993年V. A. Luckow用miniF-Kan替换了多角体polyhedrin基 因,构建了能在昆虫细胞和大肠杆菌之间穿梭的杆状病毒 重组DNA,命名为Bacmid。该名称取自Baculovirus和 plasmid。
Trichoplusia ni 细胞系 商业化的High Five细胞系 不适用于转染后获得重组病毒 适用于蛋白表达,产量高于Sf细胞
总结
杆状病毒表达载体系统具有如下优点: 1. 快速高产 2. 具备翻译后修饰系统 3. 生物安全性好 4. 表达的蛋白能正确折叠 5. 允许用于人类医学
杆状病毒表达载体系统的缺点: 1. 它是个瞬时表达系统 2. 产量远低于原核系统 3. 糖基化修饰还不理想
几种获得重组病毒过程的对比
杆状病毒表达系统的优化
启动子、Kozak序列和UTR的优化改造。 虽然p10或polyhedrin启动子已经是强启动子,但通过改变 上下游相关序列依旧能极大地提高外源基因的产量:
PLoS ONE 2014 9(5): e96562
敲除影响外源基因表达/非必需的病毒基因。 比如敲除几丁质酶和组织蛋白酶(ChiA/Cath)有助于分 泌蛋白的表达:
抗凋亡Bacmid 将靶向昆虫凋亡效应蛋白 Caspase的小RNA序列克 隆到Bacmid上,使病毒 感染的昆虫细胞抗凋亡, 从而提高外源基因的产量:
Zhang et al. BMC Biotechnology (2018) 18:24
宿主细胞
Spodoptera frugiperda 细胞系 常用的有Sf9、Sf21细胞系 适用于转染后获得重组病毒 适用于蛋白表达
