材料科学基础第四章作业参考答案
材料科学基础-作业参考答案与解析
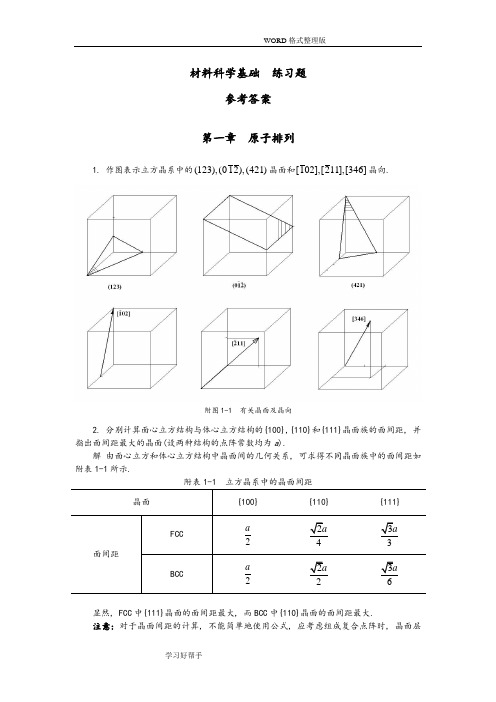
材料科学基础练习题参考答案第一章原子排列1. 作图表示立方晶系中的(123),(012),(421)晶面和[102],[211],[346]晶向.附图1-1 有关晶面及晶向2. 分别计算面心立方结构与体心立方结构的{100},{110}和{111}晶面族的面间距, 并指出面间距最大的晶面(设两种结构的点阵常数均为a).解由面心立方和体心立方结构中晶面间的几何关系, 可求得不同晶面族中的面间距如附表1-1所示.附表1-1 立方晶系中的晶面间距晶面{100} {110} {111}面间距FCC2a24a33aBCC2a22a36a显然, FCC中{111}晶面的面间距最大, 而BCC中{110}晶面的面间距最大.注意:对于晶面间距的计算, 不能简单地使用公式, 应考虑组成复合点阵时, 晶面层数会增加.3. 分别计算fcc和bcc中的{100},{110}和{111}晶面族的原子面密度和<100>,<110>和<111>晶向族的原子线密度, 并指出两种结构的差别. (设两种结构的点阵常数均为a) 解原子的面密度是指单位晶面内的原子数; 原子的线密度是指晶面上单位长度所包含的原子数. 据此可求得原子的面密度和线密度如附表1-2所示.附表1-2 立方晶系中原子的面密度和线密度晶面/晶向{100} {110} {111} <100> <110> <111>面/线密度BCC21a22a233a1a22a233aFCC22a22a2433a1a2a33a可见, 在BCC中, 原子密度最大的晶面为{110}, 原子密度最大的晶向为<111>; 在FCC 中, 原子密度最大的晶面为{111}, 原子密度最大的晶向为<110>.4. 在(0110)晶面上绘出[2113]晶向.解详见附图1-2.附图1-2 六方晶系中的晶向5. 在一个简单立方二维晶体中, 画出一个正刃型位错和一个负刃型位错. 试求:(1) 用柏氏回路求出正、负刃型位错的柏氏矢量.(2) 若将正、负刃型位错反向时, 说明其柏氏矢量是否也随之反向.(3) 具体写出该柏氏矢量的方向和大小.(4) 求出此两位错的柏氏矢量和.解正负刃型位错示意图见附图1-3(a)和附图1-4(a).(1) 正负刃型位错的柏氏矢量见附图1-3(b)和附图1-4(b).(2) 显然, 若正、负刃型位错线反向, 则其柏氏矢量也随之反向.(3) 假设二维平面位于YOZ坐标面, 水平方向为Y轴, 则图示正、负刃型位错方向分别为[010]和[010], 大小均为一个原子间距(即点阵常数a).(4) 上述两位错的柏氏矢量大小相等, 方向相反, 故其矢量和等于0.6. 设图1-72所示立方晶体的滑移面ABCD平行于晶体的上下底面, 该滑移面上有一正方形位错环. 如果位错环的各段分别与滑移面各边平行, 其柏氏矢量b // AB, 试解答:(1) 有人认为“此位错环运动离开晶体后, 滑移面上产生的滑移台阶应为4个b”, 这种说法是否正确? 为什么?(2) 指出位错环上各段位错线的类型, 并画出位错移出晶体后, 晶体的外形、滑移方向和滑移量. (设位错环线的方向为顺时针方向)图1-72 滑移面上的正方形位错环 附图1-5 位错环移出晶体引起的滑移解 (1) 这种看法不正确. 在位错环运动移出晶体后, 滑移面上下两部分晶体相对移动的距离是由其柏氏矢量决定的. 位错环的柏氏矢量为b , 故其相对滑移了一个b 的距离.(2) A ′B ′为右螺型位错, C ′D ′为左螺型位错, B ′C ′为正刃型位错, D ′A ′为负刃型位错. 位错运动移出晶体后滑移方向及滑移量见附图1-5.7. 设面心立方晶体中的(111)晶面为滑移面, 位错滑移后的滑移矢量为[110]2a .(1) 在晶胞中画出此柏氏矢量b 的方向并计算出其大小.(2) 在晶胞中画出引起该滑移的刃型位错和螺型位错的位错线方向, 并写出此二位错线的晶向指数.解 (1) 柏氏矢量等于滑移矢量, 因此柏氏矢量的方向为[110], 大小为2/2a .(2) 刃型位错与柏氏矢量垂直, 螺型位错与柏氏矢量平行, 晶向指数分别为[112]和[110], 详见附图1-6.附图1-6 位错线与其柏氏矢量、滑移矢量8. 若面心立方晶体中有[101]2a b =的单位位错及[121]6a b =的不全位错, 此二位错相遇后产生位错反应.(1) 此反应能否进行? 为什么?(2) 写出合成位错的柏氏矢量, 并说明合成位错的性质.解 (1) 能够进行.因为既满足几何条件:[111]3a b b ==∑∑后前,又满足能量条件: . 22222133b a b a =>=∑∑后前. (2) [111]3a b =合, 该位错为弗兰克不全位错. 9. 已知柏氏矢量的大小为b = 0.25nm, 如果对称倾侧晶界的取向差θ = 1° 和10°, 求晶界上位错之间的距离. 从计算结果可得到什么结论?解 根据bD θ≈, 得到θ = 1°,10° 时, D ≈14.3nm, 1.43nm. 由此可知, θ = 10°时位错之间仅隔5~6个原子间距, 位错密度太大, 表明位错模型已经不适用了.第二章 固体中的相结构1. 已知Cd, In, Sn, Sb 等元素在Ag 中的固熔度极限(摩尔分数)分别为0.435, 0.210, 0.130, 0.078; 它们的原子直径分别为0.3042 nm, 0.314 nm, 0.316 nm, 0.3228 nm; Ag 的原子直径为0.2883 nm. 试分析其固熔度极限差异的原因, 并计算它们在固熔度极限时的电子浓度.答: 在原子尺寸因素相近的情况下, 熔质元素在一价贵金属中的固熔度(摩尔分数)受原子价因素的影响较大, 即电子浓度e /a 是决定固熔度(摩尔分数)的一个重要因素, 而且电子浓度存在一个极限值(约为1.4). 电子浓度可用公式A B B B (1)c Z x Z x =-+计算. 式中, Z A , Z B 分别为A, B 组元的价电子数; x B 为B 组元的摩尔分数. 因此, 随着熔质元素价电子数的增加, 极限固熔度会越来越小.Cd, In, Sn, Sb 等元素与Ag 的原子直径相差不超过15%(最小的Cd 为5.5%, 最大的Sb 为11.96%), 满足尺寸相近原则, 这些元素的原子价分别为2, 3, 4, 5价, Ag 为1价, 据此推断它们的固熔度极限越来越小, 实际情况正好反映了这一规律; 根据上面的公式可以计算出它们在固熔度(摩尔分数)极限时的电子浓度分别为1.435, 1.420, 1.390, 1.312.2. 碳可以熔入铁中而形成间隙固熔体, 试分析是α-Fe 还是γ-Fe 能熔入较多的碳. 答: α-Fe 为体心立方结构, 致密度为0.68; γ-Fe 为面心立方结构, 致密度为0.74. 显然, α-Fe 中的间隙总体积高于γ-Fe, 但由于α-Fe 的间隙数量多, 单个间隙半径却较小, 熔入碳原子将会产生较大的畸变, 因此, 碳在γ-Fe 中的固熔度较α-Fe 的大.3. 为什么只有置换固熔体的两个组元之间才能无限互熔, 而间隙固熔体则不能?答: 这是因为形成固熔体时, 熔质原子的熔入会使熔剂结构产生点阵畸变, 从而使体系能量升高. 熔质原子与熔剂原子尺寸相差越大, 点阵畸变的程度也越大, 则畸变能越高, 结构的稳定性越低, 熔解度越小. 一般来说, 间隙固熔体中熔质原子引起的点阵畸变较大,故不能无限互熔, 只能有限熔解.第三章 凝固1. 分析纯金属生长形态与温度梯度的关系.答: 纯金属生长形态是指晶体宏观长大时固-液界面的形貌. 界面形貌取决于界面前沿液相中的温度梯度.(1) 平面状长大: 当液相具有正温度梯度时, 晶体以平直界面方式推移长大. 此时, 界面上任何偶然的、小的凸起深入液相时, 都会使其过冷度减小, 长大速率降低或停止长大, 而被周围部分赶上, 因而能保持平直界面的推移. 长大过程中晶体沿平行温度梯度的方向生长, 或沿散热的反方向生长, 而其它方向的生长则受到限制.(2) 树枝状长大: 当液相具有负温度梯度时, 晶体将以树枝状方式生长. 此时, 界面上偶然的凸起深入液相时, 由于过冷度的增大, 长大速率越来越大; 而它本身生长时又要释放结晶潜热, 不利于近旁的晶体生长, 只能在较远处形成另一凸起. 这就形成了枝晶的一次轴, 在一次轴成长变粗的同时, 由于释放潜热使晶枝侧旁液体中也呈现负温度梯度, 于是在一次轴上又会长出小枝来, 称为二次轴, 在二次轴上又长出三次轴……由此而形成树枝状骨架, 故称为树枝晶(简称枝晶).2. 简述纯金属晶体长大机制及其与固-液界面微观结构的关系.答: 晶体长大机制是指晶体微观长大方式, 即液相原子添加到固相的方式, 它与固-液界面的微观结构有关.(1) 垂直长大方式: 具有粗糙界面的物质, 因界面上约有50% 的原子位置空着, 这些空位都可以接受原子, 故液相原子可以进入空位, 与晶体连接, 界面沿其法线方向垂直推移, 呈连续式长大.(2) 横向(台阶)长大方式: 包括二维晶核台阶长大机制和晶体缺陷台阶长大机制, 具有光滑界面的晶体长大往往采取该方式. 二维晶核模式, 认为其生长主要是利用系统的能量起伏, 使液相原子在界面上通过均匀形核形成一个原子厚度的二维薄层状稳定的原子集团, 然后依靠其周围台阶填充原子, 使二维晶核横向长大, 在该层填满后, 则在新的界面上形成新的二维晶核, 继续填满, 如此反复进行.晶体缺陷方式, 认为晶体生长是利用晶体缺陷存在的永不消失的台阶(如螺型位错的台阶或挛晶的沟槽)长大的.第四章 相图1. 在Al-Mg 合金中, x Mg 为0.15, 计算该合金中镁的w Mg 为多少.解 设Al 的相对原子量为M Al , 镁的相对原子量为M Mg , 按1mol Al-Mg 合金计算, 则镁的质量分数可表示为Mg MgMg Al Al Mg Mg 100%x M w x M x M =⨯+.将x Mg = 0.15, x Al = 0.85, M Mg = 24, M Al = 27代入上式中, 得到w Mg = 13.56%.2. 根据图4-117所示二元共晶相图, 试完成:(1) 分析合金I, II的结晶过程, 并画出冷却曲线.(2) 说明室温下合金I, II的相和组织是什么, 并计算出相和组织组成物的相对量.(3) 如果希望得到共晶组织加上相对量为5%的β初的合金, 求该合金的成分.图4-117 二元共晶相图附图4-1 合金I的冷却曲线附图4-2 合金II的冷却曲线解 (1) 合金I的冷却曲线参见附图4-1, 其结晶过程如下:1以上, 合金处于液相;1~2时, 发生匀晶转变L→α, 即从液相L中析出固熔体α, L和α的成分沿液相线和固相线变化, 达到2时, 凝固过程结束;2时, 为α相;2~3时, 发生脱熔转变, α→βII.合金II的冷却曲线参见附图4-2, 其结晶过程如下:1以上, 处于均匀液相;1~2时, 进行匀晶转变L →β;2时, 两相平衡共存, 0.50.9L β;2~2′ 时, 剩余液相发生共晶转变0.50.20.9L βα+;2~3时, 发生脱熔转变α→βII .(2) 室温下, 合金I 的相组成物为α + β, 组织组成物为α + βII .相组成物相对量计算如下:αβ0.900.20100%82%0.900.050.200.05100%18%0.900.05w w -=⨯=--=⨯=- 组织组成物的相对量与相的一致.室温下, 合金II 的相组成物为α + β, 组织组成物为β初 + (α+β).相组成物相对量计算如下:αβ0.900.80100%12%0.900.050.800.05100%88%0.900.05w w -=⨯=--=⨯=- 组织组成物相对量计算如下:β(α+β)0.800.50100%75%0.900.500.900.80100%25%0.900.50w w -=⨯=--=⨯=-初 (3) 设合金的成分为w B = x , 由题意知该合金为过共晶成分, 于是有β0.50100%5%0.900.50x w -=⨯=-初 所以, x = 0.52, 即该合金的成分为w B = 0.52.3. 计算w C 为0.04的铁碳合金按亚稳态冷却到室温后组织中的珠光体、二次渗碳体和莱氏体的相对量, 并计算组成物珠光体中渗碳体和铁素体及莱氏体中二次渗碳体、共晶渗碳体与共析渗碳体的相对量.解 根据Fe-Fe 3C 相图, w C = 4%的铁碳合金为亚共晶铸铁, 室温下平衡组织为 P + Fe 3C II + L d ′, 其中P 和Fe 3C II 系由初生奥氏体转变而来, 莱氏体则由共晶成分的液相转变而成, 因此莱氏体可由杠杆定律直接计算, 而珠光体和二次渗碳体则可通过两次使用杠杆定律间接计算出来.L d ′ 相对量: d L 4 2.11100%86.3%4.3 2.11w '-=⨯=-. Fe 3C II 相对量: 3II Fe C 4.34 2.110.77100% 3.1%4.3 2.11 6.690.77w --=⨯⨯=--.P 相对量: P 4.34 6.69 2.11100%10.6%4.3 2.11 6.690.77w --=⨯⨯=--. 珠光体中渗碳体和铁素体的相对量的计算则以共析成分点作为支点, 以w C = 0.001%和w C = 6.69%为端点使用杠杆定律计算并与上面计算得到的珠光体相对量级联得到.P 中F 相对量: F P 6.690.77100%9.38%6.690.001w w -=⨯⨯=-. P 中Fe 3C 相对量: 3Fe C 10.6%9.38% 1.22%w =-=.至于莱氏体中共晶渗碳体、二次渗碳体及共析渗碳体的相对量的计算, 也需采取杠杆定律的级联方式, 但必须注意一点, 共晶渗碳体在共晶转变线处计算, 而二次渗碳体及共析渗碳体则在共析转变线处计算.L d ′ 中共晶渗碳体相对量: d Cm L 4.3 2.11100%41.27%6.69 2.11w w '-=⨯⨯=-共晶L d ′ 中二次渗碳体相对量: d Cm L 6.69 4.3 2.110.77100%10.2%6.69 2.11 6.690.77w w '--=⨯⨯⨯=--II L d ′ 中共析渗碳体相对量:d Cm L 6.69 4.3 6.69 2.110.770.0218100% 3.9%6.69 2.11 6.690.77 6.690.0218w w '---=⨯⨯⨯⨯=---共析 4. 根据下列数据绘制Au-V 二元相图. 已知金和钒的熔点分别为1064℃和1920℃. 金与钒可形成中间相β(AuV 3); 钒在金中的固熔体为α, 其室温下的熔解度为w V = 0.19; 金在钒中的固熔体为γ, 其室温下的熔解度为w Au = 0.25. 合金系中有两个包晶转变, 即1400V V V 1522V V V (1) β(0.4)L(0.25)α(0.27)(2) γ(0.52)L(0.345)β(0.45)w w w w w w =+===+==℃℃解 根据已知数据绘制的Au-V 二元相图参见附图4-3.附图4-3 Au-V 二元相图第五章 材料中的扩散1. 设有一条直径为3cm 的厚壁管道, 被厚度为0.001cm 的铁膜隔开, 通过输入氮气以保持在膜片一边氮气浓度为1000 mol/m 3; 膜片另一边氮气浓度为100 mol/m 3. 若氮在铁中700℃时的扩散系数为4×10-7 cm 2 /s, 试计算通过铁膜片的氮原子总数.解 设铁膜片左右两边的氮气浓度分别为c 1, c 2, 则铁膜片处浓度梯度为7421510010009.010 mol /m 110c c c c x x x --∂∆-≈===-⨯∂∆∆⨯ 根据扩散第一定律计算出氮气扩散通量为 722732410(10)(9.010) 3.610 mol/(m s)c J D x---∂=-=-⨯⨯⨯-⨯=⨯∂ 于是, 单位时间通过铁膜片的氮气量为 3-22-63.610(310) 2.5410 mol/s 4J A π-=⨯⨯⨯⨯=⨯最终得到单位时间通过铁膜片的氮原子总数为-62318-1A () 2.5410 6.02102 3.0610 s N J A N =⨯=⨯⨯⨯⨯=⨯第六章 塑性变形1. 铜单晶体拉伸时, 若力轴为 [001] 方向, 临界分切应力为0.64 MPa, 问需要多大的拉伸应力才能使晶体开始塑性变形?解 铜为面心立方金属, 其滑移系为 {111}<110>, 4个 {111} 面构成一个八面体, 详见教材P219中的图6-12.当拉力轴为 [001] 方向时, 所有滑移面与力轴间的夹角相同, 且每个滑移面上的三个滑移方向中有两个与力轴的夹角相同, 另一个为硬取向(λ = 90°). 于是, 取滑移系(111)[101]进行计算.222222222222k s cos 3001111cos 2001(1)01cos cos 60.646 1.57 MPa.m mϕλϕλτσ==++⨯++==++⨯-++=====即至少需要1.57 MPa 的拉伸应力才能使晶体产生塑性变形.2. 什么是滑移、滑移线、滑移带和滑移系? 作图表示α-Fe, Al, Mg 中的最重要滑移系. 那种晶体的塑性最好, 为什么?答: 滑移是晶体在切应力作用下一部分相对于另一部分沿一定的晶面和晶向所作的平行移动; 晶体的滑移是不均匀的, 滑移部分与未滑移部分晶体结构相同. 滑移后在晶体表面留下台阶, 这就是滑移线的本质. 相互平行的一系列滑移线构成所谓滑移带. 晶体发生滑移时, 某一滑移面及其上的一个滑移方向就构成了一个滑移系.附图6-1 三种晶体点阵的主要滑移系α-Fe具有体心立方结构, 主要滑移系可表示为 {110}<111>, 共有6×2 = 12个; Al 具有面心立方结构, 其滑移系可表示为 {111}<110>, 共有4×3 = 12个; Mg具有密排六方结构, 主要滑移系可表示为{0001}1120<>, 共有1×3 = 3个. 晶体的塑性与其滑移系的数量有直接关系, 滑移系越多, 塑性越好; 滑移系数量相同时, 又受滑移方向影响, 滑移方向多者塑性较好, 因此, 对于α-Fe, Al, Mg三种金属, Al的塑性最好, Mg的最差, α-Fe 居中. 三种典型结构晶体的重要滑移系如附图6-1所示.3. 什么是临界分切应力? 影响临界分切应力的主要因素是什么? 单晶体的屈服强度与外力轴方向有关吗? 为什么?答:滑移系开动所需的作用于滑移面上、沿滑移方向的最小分切应力称为临界分切应力.临界分切应力τk的大小主要取决于金属的本性, 与外力无关. 当条件一定时, 各种晶体的临界分切应力各有其定值. 但它是一个组织敏感参数, 金属的纯度、变形速度和温度、金属的加工和热处理状态都对它有很大影响.如前所述, 在一定条件下, 单晶体的临界分切应力保持为定值, 则根据分切应力与外加轴向应力的关系: σs= τk/ m, m为取向因子, 反映了外力轴与滑移系之间的位向关系, 因此, 单晶体的屈服强度与外力轴方向关系密切. m越大, 则屈服强度越小, 越有利于滑移.4. 孪生与滑移主要异同点是什么? 为什么在一般条件下进行塑性变形时锌中容易出现挛晶, 而纯铁中容易出现滑移带?答: 孪生与滑移的异同点如附表6-1所示.附表6-1 晶体滑移与孪生的比较锌为密排六方结构金属, 主要滑移系仅3个, 因此塑性较差, 滑移困难, 往往发生孪生变形, 容易出现挛晶; 纯铁为体心立方结构金属, 滑移系较多, 共有48个, 其中主要滑移系有12个, 因此塑性较好, 往往发生滑移变形, 容易出现滑移带.第七章 回复与再结晶1. 已知锌单晶体的回复激活能为8.37×104J/mol, 将冷变形的锌单晶体在-50 ℃进行回复处理, 如去除加工硬化效应的25% 需要17 d, 问若在5 min 内达到同样效果, 需将温度提高多少摄氏度?解 根据回复动力学, 采用两个不同温度将同一冷变形金属的加工硬化效应回复到同样程度, 回复时间、温度满足下述关系:122111exp t Q t R T T ⎛⎫⎛⎫=-- ⎪ ⎪ ⎪⎝⎭⎝⎭整理后得到221111ln T t R T Q t =+.将41211223 K,/5/(172460),8.3710 J/mol, 8.314 J/(mol K)4896T t t Q R ==⨯⨯==⨯=⋅代入上式得到2274.7 K T =.因此, 需将温度提高21274.722351.7 T T T ∆=-=-=℃.2. 纯铝在553 ℃ 和627 ℃ 等温退火至完成再结晶分别需要40 h 和1 h, 试求此材料的再结晶激活能.解 再结晶速率v 再与温度T 的关系符合阿累尼乌斯(Arrhenius)公式, 即exp()Q v A RT=-再 其中, Q 为再结晶激活能, R 为气体常数.如果在两个不同温度T 1, T 2进行等温退火, 欲产生同样程度的再结晶所需时间分别为t 1, t 2, 则122112122111exp[()]ln(/)t Q t R T T RTT t t Q T T =--⇒=-依题意, 有T 1 = 553 + 273 = 826 K, T 2 = 627 + 273 = 900 K, t 1 = 40 h, t 2 = 1 h, 则58.314826900ln(40/1)3.0810J/mol 900826Q ⨯⨯⨯=⨯-3. 说明金属在冷变形、回复、再结晶及晶粒长大各阶段的显微组织、机械性能特点与主要区别.答: 金属在冷变形、回复、再结晶及晶粒长大各阶段的显微组织、机械性能特点与主要区别详见附表7-1.附表7-1 金属在冷变形、回复、再结晶及晶粒长大各阶段的显微组织、机械性能第八章固态相变。
材料科学基础习题参考答案.docx

材料科学基础习题参考答案 第一章材料结构的基本知识8.计算下列晶体的离于键与共价键的相对比例。
(1) NaF (2) CaO (3) ZnS解:(1)查表得:X Na =0.93,X F =3.98--(0.93-3.98)2根据鲍林公式可得NaF 中离子键比例为:[1-e 4 ]x 100% = 90.2%共价键比例为:1-90.2%=9.8%--(1.00-3.44 )2(2) 同理,CaO 中离子键比例为:[1-e 4 ]x 100% = 77.4%共价键比例为:1-77.4%=22.6%(3) ZnS 中离子键比例为:Z“S 中离子键含量=[1 -£-1/4'2-58-165)2]x 100% = 19.44% 共价键比例为:1-19.44%=80.56%10说明结构转变的热力学条件与动力学条件的意义.说明稳态结构与亚稳态结构之间的关 系。
答:结构转变的热力学条件决定转变是否可行,是结构转变的推动力,是转变的必要条件; 动力学条件决定转变速度的大小,反映转变过程中阻力的大小。
稳态结构与亚稳态结构之间的关系:两种状态都是物质存在的状态,材料得到的结构是 稳态或亚稳态,取决于转变过程的推动力和阻力(即热力学条件和动力学条件),阻力小时得 到稳态结构,阻力很大时则得到亚稳态结构。
稳态结构能量最低,热力学上最稳定;亚稳态 结构能量高,热力学上不稳定,但向稳定结构转变速度慢,能保持相对稳定甚至长期存在。
但在一定条件下,亚稳态结构向稳态结构转变。
1.第二章九材料中的騒須勾)与[2廊1)与[112], (110)与[111], (132)与[123], (322)与[236]指数。
题: 系的 (21 在立方晶系的一个晶胞虫画出(111丄和丄112、日面.才晶系的画出同M1)、■'朋两晶面交钱亠 1]晶向。
112) d2. 有一正交点阵的a=b, c=a/2o 某晶面在三个晶轴上的截距分别为6个、2个和4个原子 间距,求该晶面的密勒指数。
材料科学基础习题第四章答案与翻译

4.2 根据本章给出的结构,画出下列链节结构:(1)聚氟乙烯:—CH2—CHF—;(2)聚三氟氯乙烯:—CF2—CFCl—(3)聚乙烯醇:—CH2—CHOH—4.3 计算下列聚合物的链节分子量(1)聚氯乙烯:—CH2—CHCl— : m = 2⨯12.011+2⨯1.008+35.453=61.491g/mol (2)聚对苯二甲酸乙二醇酯:—OCH2-CH2OCOC6H4CO—m = 10⨯12.011+8⨯1.008+4⨯15.999=192.17g/mol(3)聚碳酸酯:m = 16⨯12.011+14⨯1.008+3⨯15.999=254.285g/mol (4)聚二甲硅氧烷:C2H6OSim = 28.086+2⨯12.011+6⨯1.008+3⨯15.999 = 106.153g/mol 4.4 聚丙烯的数均分子量为1,000,000 g/mol,计算其数均聚合度。
答:链节为—CH3CH—CH2—,其分子量:m = 3⨯12.011+6⨯1.008=42.081 g/mol4.5 (a) 计算聚苯乙烯链节的分子量答:链节为-CHC6H5-CH2-,分子量:m = 8⨯12.011+8⨯1.008=104.152(b) 计算重均聚合度为25000的聚苯乙烯的重均分子量答:= 25000⨯104.152 g/mol = 2603800 g/mol4.6 下表列出了聚丙烯的分子量,计算(a) 数均分子量(b) 重均分子量(c) 数均聚合度(d) 重均聚合度分子量分布x i w i(g/mol)8,000-16,000 0.05 0.0216,000-24,000 0.16 0.1024,000-32,000 0.24 0.2032,000-40,000 0.28 0.3040,000-48,000 0.20 0.2748,000-56,000 0.07 0.21答:(a)= 0.05⨯12000+0.16⨯20000+0.24⨯28000+0.28⨯36000+0.20⨯44000+0.07⨯52000 = 600+3200+6720+10080+8800+3640 = 33040 (g/mol)(b)= 0.02⨯12000+0.1⨯20000+0.20⨯28000+0.30⨯36000+0.27⨯44000+0.21⨯52000 = 240+2000+5600+10800+11880+10920 = 41440 (g/mol)(c)聚丙烯链节的分子量:m = 42.081 g/mol(d)4.7 下表列出了某聚合物的分子量分布。
第四章晶体中的点缺陷与线缺陷作业题答案

Al O
'
Al2 O3 2MgO 2Mg 'Al VO 2OO CaF2 '' 2YF3 2YCa VCa 6FF
(2) (4)
CaF2 YF3 YCa Fi' 2FF
CaF
'
2 B、 2YF3 2YCa VCa 6FF
CaF
"
A 可能性较大。因萤石晶体中存较多的八面体空隙,F-离子半径较小,形成填隙型固溶体比较稳定。 6、CeO2 为萤石结构,其中加入 15mol%CaO 形成固溶体,测得固溶体密度 D=7.01g/cm3,晶胞参数 a0= 0.5417nm,试通过计算判断生成的是哪一种类型固溶体。(已知原子量 Ce 140.12,Ca 40.08,O 16.00) 解:对于 CaO-CeO2 固溶体来说,从满足电中性来看,可以形成氧离子空位的固溶体也可形成 Ca2+嵌入阴 离子间隙中的固溶体,其固溶方程为:
当 CaCl2 中 Ca2+置换 KCl 中 K+而出现点缺陷,其缺陷反应式如下:
KCl ' CaCl2 Ca K 2ClCl +VK
CaCl2 中 Ca2+进入到 KCl 间隙中而形成点缺陷的反应式为:
KCl ' CaCl2 Ca i 2ClCl +2VK
5. 试写出以下缺陷方程(每组写出二种),并判断是否可以成立,同时简单说明理由。
CeO 2 CaO Ca " Ce VO O O CeO 2 2CaO Ca " Ce Ca i 2O O
材料科学基础第四版答案

材料科学基础第四版答案【篇一:材料科学基础课后习题答案】txt>第一章材料结构的基本知识4. 简述一次键和二次键区别答:根据结合力的强弱可把结合键分成一次键和二次键两大类。
其中一次键的结合力较强,包括离子键、共价键和金属键。
一次键的三种结合方式都是依靠外壳层电子转移或共享以形成稳定的电子壳层,从而使原子间相互结合起来。
二次键的结合力较弱,包括范德瓦耳斯键和氢键。
二次键是一种在原子和分子之间,由诱导或永久电偶相互作用而产生的一种副键。
6. 为什么金属键结合的固体材料的密度比离子键或共价键固体为高?答:材料的密度与结合键类型有关。
一般金属键结合的固体材料的高密度有两个原因:(1)金属元素有较高的相对原子质量;(2)金属键的结合方式没有方向性,因此金属原子总是趋于密集排列。
相反,对于离子键或共价键结合的材料,原子排列不可能很致密。
共价键结合时,相邻原子的个数要受到共价键数目的限制;离子键结合时,则要满足正、负离子间电荷平衡的要求,它们的相邻原子数都不如金属多,因此离子键或共价键结合的材料密度较低。
9. 什么是单相组织?什么是两相组织?以它们为例说明显微组织的含义以及显微组织对性能的影响。
答:单相组织,顾名思义是具有单一相的组织。
即所有晶粒的化学组成相同,晶体结构也相同。
两相组织是指具有两相的组织。
单相组织特征的主要有晶粒尺寸及形状。
晶粒尺寸对材料性能有重要的影响,细化晶粒可以明显地提高材料的强度,改善材料的塑性和韧性。
单相组织中,根据各方向生长条件的不同,会生成等轴晶和柱状晶。
等轴晶的材料各方向上性能接近,而柱状晶则在各个方向上表现出性能的差异。
对于两相组织,如果两个相的晶粒尺度相当,两者均匀地交替分布,此时合金的力学性能取决于两个相或者两种相或两种组织组成物的相对量及各自的性能。
如果两个相的晶粒尺度相差甚远,其中尺寸较细的相以球状、点状、片状或针状等形态弥散地分布于另一相晶粒的基体内。
如果弥散相的硬度明显高于基体相,则将显著提高材料的强度,同时降低材料的塑韧性。
工程材料第四章固态扩散作业答案

2. 一含 w(C)=0.1%的碳钢在 930℃渗碳,渗到 0.05cm 的地方碳的浓度达到 0.45%。在 t >0 的全部时间,渗碳气氛保持表面成分为 1%,假设
Dc 2.0 105 exp(140000 / RT )(m 2 / s )
(a) 计算渗碳时间; (b) 若将渗层加深一倍,则需多长时间? (c) 若规定 0.3%C 作为渗碳层厚度的量度, 则在 930℃渗碳 10 小时的渗层厚度为 870 ℃ 渗碳 10 小时的多少倍?
在温度从 25℃升高到 600℃时,扩散系数 D 分别提高 4.9 10 和 9.5 10 倍,表明温度是
9 28
影响扩散系数的最重要的因素之一。当扩散激活能增大,温度对扩散系数(或速度)的影响 越大。 6. 已知 Al 在 Al2O3 中扩散常数 D0=2.8×10-3(m2/s), 激活能 477 (KJ/mol) , 而O (氧) 在 Al2O3 中的 D0=0.19(m2/s),Q=636(KJ/mol)。 (a) 分别计算两者在 2000K 温度下的扩散系数 D; (b) 说明它们扩散系数不同的原因。 解:(a) 根据阿累尼乌斯方程 D D0 exp
(b) 在同一温度下,两个不同距离 x1 和 x2 所对应的时间 t1 和 t2 有如下关系
x1 Dt1
温度相同时,D1=D2,所以 t 2
x2 Dt 2
2 x2 0.12 t 1.0 104 4.0 104 s 2 1 2 x1 0.05
(c) 根据题意可知
x930 C x870 C
解:(a) 930℃时碳在γ铁中的扩散系数
140000 2 D 2.0 10-5 exp m / s 1.67 10-11 m 2 / s 1.67 10-7 m 2 / s 8.314 1203
第四章作业答案_第三次

根据时移性可得
1 2
gωc
− j2π ω
(ω ) e ωc
=
1 2
gωc
− j2πω
(ω ) e ωc
↔
ωc 4π
Sa
⎡ ⎢ωc ⎢ ⎢
⎛ ⎜ ⎝
t
− 2
2π ωc
⎞ ⎟ ⎠
⎤ ⎥ ⎥ ⎥
=
ωc 4π
Sa
⎡ωct ⎢⎣
− 2
2π
⎤ ⎥⎦
⎢
⎥
⎢⎣
⎥⎦
故 h(t)
=
ωc 4π
⎡ ⎢⎣
Sa
⎛ ⎜⎝
ωct 2
10ω0 12ω0
ω
y (t ) = x2 (t ) ∗ h2 (t ) ↔ X2 ( jω ) ⋅ H2 ( jω ) ,得响应 y (t ) 的频谱函数Y ( jω ) 为
Y ( jω)
−2ω0
2ω 0
ω
4-24 已知 f (t ) = Sa (ωct ) , s (t ) = cos (ω0t ) ,且ω0 ωc ,试求题图 4-24 所示系统的输
jω 2
gωc
(ω) +
jω 2
gωc
( )ω e−
j2
π
ω ωc
⎤ ⎥
⋅
⎡ ⎢
⎥⎦ ⎣
1 jω
+
πδ (ω )⎤⎥
⎦
=
⎡ ⎢
1
⎢⎣ 2
gωc
(ω) +
1 2
gωc
− j2π ω
(ω ) e ωc
⎤ ⎥ ⎥⎦
+
⎡ π⎢
⎢⎣
jω 2
gωc
材料化学-第四章高分子材料化学习题及答案

第四章高分子材料化学习题:1、高聚物相对分子质量有哪些测试方法?分别适用于何种聚合物分子,获得的相对分子质量有何不同?(10分)答:测定高聚物相对分子质量的方法:渗透压、光散射、粘度法、超离心法、沉淀法和凝胶色谱法等。
这些方法中,有些方法偏向于较大的聚合物分子,有的方法偏向于较小的聚合物分子。
聚合物相对分子质量实际是指它的平均相对分子质量。
(1)数均相对分子质量( Mn ) 采用冰点降低、沸点升高、渗透压和蒸气压降低等方法测定的数均相对分子质量,即总质量除以样品中所含的分子数。
(2)质均相对分子质量( Mω) 采用光散射等方法测定质均相对分子质量。
(3)粘均相对分子质量( Mη) 采用粘度法测定粘均相对分子质量。
2、详述高分子聚合物的分类及各自的特征并举例。
(20分)答:高分子化合物常以形状、合成方法、热行为、分子结构及使用性能进行分类。
1、按高聚物的热行为分类(1) 热固性高聚物高聚物受热变成永久固定形状的高聚物(有些不需加热)。
不可再熔融或再成型。
结构:加热时,线型高聚物链之间形成永久的交联,产生不可再流动的坚硬体型结构,继续加热、加压只能造成链的断裂,引起性质的严重破坏。
利用这一特性,热固性高聚物可作耐热的结构材料。
典型的热固性高聚物有环氧树脂、酚醛树脂、不饱和聚酯树脂、有机硅树脂、聚氨酯等。
(2) 热塑性高聚物熔融状态下使它成型(塑化),冷却后定型,但是可以再加热又形成一个新的形状,可以多次重复加工。
结构:没有大分子链的严重断裂,其性质也不发生显著变化,称为热塑性高聚物。
根据这一特性,可以用热塑性高聚物碎屑进行再生和再加工。
聚乙烯、聚氯乙烯、ABS树脂、聚酰胺等都属于热塑性高聚物。
2、按高聚物的分子结构分类(1) 碳链高聚物大分子主链完全由碳原于组成,绝大部分烯类聚合物属于这一类。
如聚乙烯、聚苯乙烯、聚丁二烯等。
(2) 杂链高聚物大分子主链中除碳原子外,还有氧、氮、硫等杂原子。
如聚醚、聚酯、聚硫橡胶等。
工程材料第四章习题答案

工程材料作业(4)答案1.解释下列现象:(1) 在相同含碳量下,除了含Ni和Mn的合金钢外,大多数合金钢的热处理加热温度都比碳钢高。
奥氏体形成分为形核、长大、残余渗碳体溶解,奥氏体均匀化4阶段。
多数合金元素减缓A形成,Cr、Mo、W、V等强碳化物形成元素与碳亲和力大,形成的合金元素的碳化物稳定、难溶解,会显著减慢碳及合金元素的扩散速度。
但为了充分发挥合金元素的作用,又必须使其更多的溶入奥氏体中,合金钢往往需要比含碳量相同的碳钢加热到更高的温度,保温更长时间。
Co、Ni等部分非碳化物形成元素,因增大碳的扩散速度,使奥氏体的形成速度加快。
而Al、Si、Mn等合金元素对奥氏体形成速度的影响不大。
阻碍晶粒长大,合金钢需要更高的加热温度,更长的保温时间,才能保证奥氏体均匀化。
(加热温度升高了,但一般不会引起晶粒粗大:大多数合金元素都有阻碍奥氏体晶粒长大的作用。
碳化物形成元素的作用最明显,因其形成的碳化物高温下稳定性高,很难完全溶入奥氏体,未溶的细小碳化物颗粒,分布在奥氏体晶界上,有效的阻止晶粒长大,起到细化晶粒的作用。
所以,合金钢虽然热处理加热温度高,但一般不用担心晶粒粗大。
强烈阻碍晶粒长大的元素:V、Ti、Nb、Zr;中等阻碍的:W、Mo、Cr;影响不大的:Si、Ni、Cu;促进晶粒长大的:Mn、P、B)(2) 在相同含碳量下,含碳化物形成元素的合金钢比碳钢具有较高的回火稳定性。
回火过程一般分为:马氏体分解、残余奥氏体转变、碳化物类型转变和碳化物长大。
合金元素在回火过程中,推迟马氏体的分解和残余奥氏体的转变(即在较高温度才出现分解和转变),提高铁素体的再结晶温度,使碳化物难以聚集长大而保持较大的弥散度。
因此,提高了钢对回火软化的抗力,即提高了钢的回火稳定性。
使得合金钢在相同温度下回火时,比同样质量分数的碳钢具有更高的硬度和强度(对工具钢,耐热钢更重要),或在保证相同强度的条件下,可在更高的温度下回火,而韧性更好(对结构钢更重要。
材料科学基础习题第四章答案与翻译
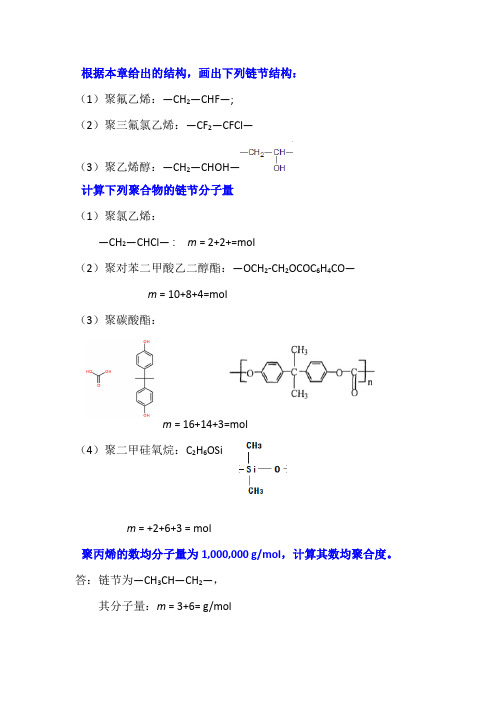
根据本章给出的结构,画出下列链节结构:(1)聚氟乙烯:—CH2—CHF—;(2)聚三氟氯乙烯:—CF2—CFCl—(3)聚乙烯醇:—CH2—CHOH—计算下列聚合物的链节分子量(1)聚氯乙烯:—CH2—CHCl— : m = 2+2+=mol(2)聚对苯二甲酸乙二醇酯:—OCH2-CH2OCOC6H4CO—m = 10+8+4=mol(3)聚碳酸酯:m = 16+14+3=mol(4)聚二甲硅氧烷:C2H6OSim = +2+6+3 = mol聚丙烯的数均分子量为1,000,000 g/mol,计算其数均聚合度。
答:链节为—CH3CH—CH2—,其分子量:m = 3+6= g/mol(a) 计算聚苯乙烯链节的分子量答:链节为CHC6H5CH2,分子量:m = 8+8=(b) 计算重均聚合度为25000的聚苯乙烯的重均分子量答:= 25000 g/mol = 2603800 g/mol下表列出了聚丙烯的分子量,计算(a) 数均分子量(b) 重均分子量(c) 数均聚合度(d) 重均聚合度x i w i 分子量分布(g/mol)8,00016,00016,00024,00024,00032,00032,00040,00040,00048,00048,00056,000答:(a)= 12000+20000+28000+36000+44000+52000 = 600+3200+6720+10080+8800+3640 = 33040 (g/mol)(b)= 12000+20000+28000+36000+44000+52000 = 240+2000+5600+10800+11880+10920 = 41440 (g/mol)(c)聚丙烯链节的分子量:m = g/mol(d)下表列出了某聚合物的分子量分布。
计算(a) 数均分子量(b) 重均分子量(c) 如果已知这一聚合物的重均聚合度为780,指出此聚合物为表所列聚合物中的哪一个为什么(d) 这一材料的数均聚合度为多少分子量分布(g/mol)x i w i15,00030,00030,00045,00045,00060,00060,00075,00075,00090,00090,000105,000105,000120,000120,000135,000答:(a)= 22500+37500+52500+67500+82500+97500+112500+127500 = 900+2625+8400+17550+19800+11700+9000+3825 = 73800 (g/mol)(b)= 22500+37500+52500+67500+82500+97500+112500+127500 = 225+1500+5775+16200+22275+15600+13500+ 6375 = 81450 (g/mol)(c)此聚合物为聚苯乙烯根据下面的分子量分布和重均聚合度为585的条件,判断是否为聚甲基丙烯酸甲酯均聚物分子量分布(g/mol)x i w i8,00020,00020,00032,00032,00044,00044,00056,00056,00068,00068,00080,00080,00092,000答:聚甲基丙烯酸甲酯链节分子式为:C5H8O2(—CH2CH3COOCH3C—);其分子量m = 5+8+2=mol重均分子量为:=14000+26000+38000+50000+62000+74000+86000=140+1300+4560+12500+16740+15540+7740=58520与条件相符,能形成均聚物高密度聚乙烯通过诱导氯原子随机取代氢而被氯化。
《材料科学基础》第四章习题

《材料科学基础》第四章 固体中原子即分子的运动1.名词:扩散 自扩散 互扩散 扩散系数 互扩散系数 扩散激活能 扩散通量 上坡扩散 间隙扩散 空位扩散 原子迁移 界面扩散 表面扩散 柯肯达尔效应 反应扩散 稳态扩散2. 设有一条内径为30mm 的厚壁管道,被厚度为0.1mm 的铁膜隔开,通过管子的一端向管内输入氮气,以保持膜片一侧氮气浓度为1200mol/m 3,而另一侧的氮气浓度为100 mol/m 3,如在700℃下测得通过管道的氮气流量为2.8×10-8mol/s ,求此时氮气在铁中的扩散系数。
解:通过管道中铁膜的氮气通量为 )/(104.4)03.0(4108.22424s m mol J ⋅⨯=⨯⨯=--π膜片两侧氮浓度梯度为:m mol x c /101.10001.010012007-⨯=-=∆∆- 据Fick ’s First Law : s m xc J D x c D J /104/211-⨯=∆∆-=⇒∂∂-=3. 有一硅单晶片,厚0.5mm ,其一端面上每107个硅原子包含两个镓原子,另一个端面经处理后含镓的浓度增高。
试求在该面上每107个硅原子须包含几个镓原子,才能使浓度梯度成为2×1026 atoms/m 3,硅的点阵常数为0.5407nm 。
4. 950℃下对纯铁进行渗碳,并希望在0.1mm 的深度得到w 1(C)=0.9%的碳含量。
假设表面碳含量保持在w 2(C)=1.20%,扩散系数 为D ɤ−Fe=10-10m 2/s ,计算为达到此要求至少要渗碳多少时间。
5. 在一个富碳的环境中对钢进行渗碳,可以硬化钢的表面。
已知在1000℃下进行这种渗碳热处理,距离钢的表面1-2mm 处,碳含量从x = 5%减到x =4%。
估计在近表面区域进入钢的碳原子的流人量J (atoms/m 2s )。
(γ-Fe 在1000℃的密度为7.63g/cm 3,碳在γ-Fe 中的扩散系数D o =2.0×10-5 m 2/s ,激活能Q =142kJ/mol)。
材料科学基础 张晓燕1-5章作业及题解.

第一章 作业题解1. 原子中一个电子的空间位置和能量可用哪四个量子数来决定?2. 在多电子的原子中,核外电子的排布应遵循哪些个原则?3. 在元素周期表中,同一周期或同一主族元素原子结构有什么共同特点?从左到右或从上到下元素结构有什么区别?性质如何递变?解、同一周期元素具有相同原子核外电子层数,但从左到右,核电荷依次增多,原子半径逐渐减小,电离能增加,失去电子的能力降低,得到电子能力增加,金属性减弱,非金属性增强,同一主族元素最外层电子数相同,但从上→下,电子层数最多,原子半径增大,电离能降低,失去电子能力增加,得到电子能力降低,金属性增加,非金属性降低。
4. 铬的原子序数为24,共有四种同位数:4.31%的Cr 原子含有26个中子,83.76%含有28个中子,9.55%含有29个中子,且2.38%含有30个中子。
试求铬的原子量。
解、=Ar 0.0431X (24+26)+0.8376X (24+28)+0.0955X (24+29)+0.0238X(24+30)=52.0575. 原子间的结合键共有几种?各自特点如何? 解、6. 按分子材料受热的表现分类可分为热塑性和热固性两大类,试从高分子链结构角度加以解释之。
解、热塑性;具有线性和枝化高分子链结构,加热后变软,可反复加工再成形;热固性;具有体型(立体网状)高分子链结构,不溶于任何溶剂,也不能熔融,一旦定型后不能再改变形状,无法再生。
第二章 作业题解1、归纳总结三种典型的晶体结构的晶体学特征。
解、2、试证明理想密排六方结构的轴比c/a=1.633。
解、见图所示,等边三角形的高 a h ⋅=43 氢键;分子间作用力,氢桥,具有饱和性结合键化学键;主价键 物理键;次价键,也称范德华健 金属键;电子共有化,无饱和性,无方向性。
离子键;以离子而不是以原子为结合单元,无饱和性,无方向性。
共价键;共用电子对,有饱和性方向性。
hd2c343222222a c h c d +=⎪⎭⎫⎝⎛+⎪⎭⎫ ⎝⎛= 理想密排六方晶体结构中a d = 故633.138==a c 3、Ni 的晶体结构为面心立方结构,其原子半径为r=0.1243nm ,试求Ni 的晶格常数和密度。
[工学]无机材料科学基础--标准化作业本
![[工学]无机材料科学基础--标准化作业本](https://img.taocdn.com/s3/m/1a37f381d1f34693dbef3e01.png)
第一章结晶学基础一、名词解释1.晶体:2.空间点阵与晶胞:3.配位数与配位多面体:4.离子极化:5.同质多晶与类质同晶:二、填空与选择1.晶体的基本性质有五种:,,,和。
2.空间点阵是由在空间作有规律的重复排列。
(A 原子B离子C几何点D 分子)3.在等大球体的最紧密堆积中有和二种排列方式,前者的堆积方式是,后者的堆积方式是。
4.如晶体按立方紧密堆积,单位晶胞中原子的个数为,八面体空隙数为,四面体空隙数为;如按六方紧密堆积,单位晶胞中原子的个数为,八面体空隙数为,四面体空隙数为;如按体心立方近似密堆积,单位晶胞中原子的个数为,八面体空隙数为,四面体空隙数为。
5.等径球体最紧密堆积的空隙有两种:四面体空隙和八面体空隙。
一个球的周围有个四面体空隙、个八面体空隙;n个等径球体做最紧密堆积时可形成个四面体空隙、个八面体空隙。
不等径球体进行堆积时,大球,小球。
6.在离子晶体中,配置于正离子周围的负离子数(即负离子配位数),决定于正、负离子半径比(r+/r-)。
若某离子化合物的r+/r-值为0.564,其负离子配位数应是。
(A3 B4 C 6 D 8)三、(1)a≠b≠c,α=β=γ=90°的晶体属什么晶系?(2) a≠b≠c,α≠β≠γ≠90°的晶体属什么晶系?(3)你能否据此确定这两种晶体的布拉菲点阵?四、(1)一晶面在x、y、z轴上的截距分别为2a、3b和6c,求出该晶面的密氏指数;(2)一晶面在x、y、z轴上的截距分别为a/3、b/2和c,求出该晶面指数。
五、以NaCl晶胞为例,说明面心立方紧密堆积中的八面体和四面体空隙的位置和数量。
六、计算体心立方、面心立方、密排六方晶胞中的原子数、配位数、致密度。
七、计算立方体配位、八面体配位、四面体配位、三角形配位的临界半径比。
八、画出面心立方结构的(111)、(110)、(100)晶面的原子排布图,并计算其面间距及原子密度(原子个数/单位面积)九、有一个面心立方密堆结构的晶体,它的密度是8.94/cm3。
第四章作业答案

8. 进行阴离子聚合反应或配位聚合反应时预先要对原料及 聚合容器进行怎样的处理?为什么?试写出相关的反应式。 因为离子聚合和配位聚合的引发剂及活性链均很活泼, 许多杂质及空气中的水、O2、CO2均可破坏引发剂使活性中 心失活,因此,需预先将原料和聚合容器净化、干燥、除 去空气并在密封及N2保护条件下进行。
7. 化学计量聚合:
阴离子的活性聚合由于其聚合度可由单体和引发剂的浓 度定量计算确定,因此也称为化学计量聚合。 8 立构规整度: 立构规整聚合物的质量占总聚合物质量的分率。 9 遥爪聚合物: 是一种分子两端带有反应性官能团的低分子量聚合物。 10. 热塑弹性体: 常温下具有橡胶的弹性,高温下具有可塑化成型的一类 弹性体。既具备传统交联硫化橡胶的高弹性、耐老化、耐 油性各项优异性能,同时又具备普通塑料加工方更、加工 方式广的特点。
很少短支链 强度高,熔 低压配位聚 点较高 合(Z-N) 8/1000C (130-135)
短支链 (可控) 介于上面两 低压配位聚 种之间 合(Z-N)
7. 配位聚合反应实施方法有哪几种?与自由基反应有何不 同?为什么? 配位聚合常用的实施方法有: 1.淤浆聚合(溶液聚合);2.气相聚合;3.本体聚合 由于配位聚合必须在无水、无氧条件下进行,所以不能采 用自由基聚合通常采用的悬浮聚合及乳液聚合这两种以水 为介质的实施方法。
3. 苯乙烯在萘钠的四氢呋喃溶液中聚合为典型的(9) 阴离 子 聚合,其产物的特点是(10) 分子量分布窄 ,当用0.002 摩尔的萘钠引发208克苯乙烯单体聚合,转化率达到100%时, 所得聚苯乙烯的分子量为(11) 2.08x105。 4. 合成顺丁橡胶的聚合反应式(12) ,工业上最常采用 的引发体系为(Ziegler-Natta引发剂,烯丙基过渡金属型引 发剂,烷基锂引发剂),顺丁橡胶因为其高顺式含量也属于 (13) (全同聚合物,立构规整聚合物,结晶聚合物)。
材料科学基础习题与参考答案

第一章材料的结构一、解释以下基本概念空间点阵、晶格、晶胞、配位数、致密度、共价键、离子键、金属键、组元、合金、相、固溶体、中间相、间隙固溶体、置换固溶体、固溶强化、第二相强化。
二、填空题1、材料的键合方式有四类,分别是(),(),(),()。
2、金属原子的特点是最外层电子数(),且与原子核引力(),因此这些电子极容易脱离原子核的束缚而变成()。
3、我们把原子在物质内部呈()排列的固体物质称为晶体,晶体物质具有以下三个特点,分别是(),(),()。
4、三种常见的金属晶格分别为(),()和()。
5、体心立方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),晶胞中八面体间隙个数为(),四面体间隙个数为(),具有体心立方晶格的常见金属有()。
6、面心立方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),晶胞中八面体间隙个数为(),四面体间隙个数为(),具有面心立方晶格的常见金属有()。
7、密排六方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),具有密排六方晶格的常见金属有()。
8、合金的相结构分为两大类,分别是()和()。
9、固溶体按照溶质原子在晶格中所占的位置分为()和(),按照固溶度分为()和(),按照溶质原子与溶剂原子相对分布分为()和()。
10、影响固溶体结构形式和溶解度的因素主要有()、()、()、()。
11、金属化合物(中间相)分为以下四类,分别是(),(),(),()。
12、金属化合物(中间相)的性能特点是:熔点()、硬度()、脆性(),因此在合金中不作为()相,而是少量存在起到第二相()作用。
13、CuZn、Cu5Zn8、Cu3Sn的电子浓度分别为(),(),()。
14、如果用M表示金属,用X表示非金属,间隙相的分子式可以写成如下四种形式,分别是(),(),(),()。
材料科学基础习题及答案

第一章材料的结构一、解释以下基本概念空间点阵、晶格、晶胞、配位数、致密度、共价键、离子键、金属键、组元、合金、相、固溶体、中间相、间隙固溶体、置换固溶体、固溶强化、第二相强化。
二、填空题1、材料的键合方式有四类,分别是(),(),(),()。
2、金属原子的特点是最外层电子数(),且与原子核引力(),因此这些电子极容易脱离原子核的束缚而变成()。
3、我们把原子在物质内部呈()排列的固体物质称为晶体,晶体物质具有以下三个特点,分别是(),(),()。
4、三种常见的金属晶格分别为(),()和()。
5、体心立方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),晶胞中八面体间隙个数为(),四面体间隙个数为(),具有体心立方晶格的常见金属有()。
6、面心立方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),晶胞中八面体间隙个数为(),四面体间隙个数为(),具有面心立方晶格的常见金属有()。
7、密排六方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),具有密排六方晶格的常见金属有()。
8、合金的相结构分为两大类,分别是()和()。
9、固溶体按照溶质原子在晶格中所占的位置分为()和(),按照固溶度分为()和(),按照溶质原子与溶剂原子相对分布分为()和()。
10、影响固溶体结构形式和溶解度的因素主要有()、()、()、()。
11、金属化合物(中间相)分为以下四类,分别是(),(),(),()。
12、金属化合物(中间相)的性能特点是:熔点()、硬度()、脆性(),因此在合金中不作为()相,而是少量存在起到第二相()作用。
13、CuZn、Cu5Zn8、Cu3Sn的电子浓度分别为(),(),()。
14、如果用M表示金属,用X表示非金属,间隙相的分子式可以写成如下四种形式,分别是(),(),(),()。
材料科学基础作业答案

• 2. 根据材料的性能特点和用途,材料分为
结构材料 和 功能材料 两大类。 • 根据原子之间的键合特点,材料分为 金属 、
陶瓷(无机非金属) 、 高分子 和复合材料四大类。
• 12、硅酸盐晶体结构中的基本结构单元是 硅 氧四面体[SiO4]。
• 13、几种硅酸盐晶体的络阴离子分别为[Si2O7]6-、 [Si2O6]4-、[Si4O10]4-、[AlSi3O8]1-,它们的晶体 结构类型分别为 组群状 , 链状 , 层状 ,和 架状 。
• 14、表征晶体中晶向和晶面的方法有 解析法 和 图示 法。(晶体投影图 )
• MgO的分子量为(24.305 +15.999 )40.30, •阿佛加得罗常数是6.0238×1023, •每个MgO 分子的质量A为: 40.30/(6.0238×1023)。
MgO结构:z=4 • MgO的密度ρ
Z M a /3 N A 4 4 (0 0 ..3 4 0 2 4 /( 6 .1 0 0 2 7 )1 3 0 2 3 ) 3 .5 1 (g /c m 3 )
第三章 晶体结构缺陷 P116
• 一、填空题 • 1、按几何组态,晶体中的缺陷分为 点缺陷 、 线
缺陷 、面缺陷 和体缺陷。 • 2、点缺陷主要包括 空位、 间隙原子、置换原子 ;
线缺陷有 位错 ;面缺陷包括 晶界、相界、表面 等。 • 3、描述位错性质及特征的是 柏氏矢量b 。 • 4、位错的类型有 刃位错 、 螺位错 和 混合位 错。
• 5、位错线与柏氏矢量垂直的位错为 刃位错 ,位错 线与柏氏矢量平行的位错称为 螺位错 。
材料科学基础课后习题及答案

第二章答案2-1略。
2-2(1)一晶面在x、y、z轴上的截距分别为2a、3b、6c,求该晶面的晶面指数;(2)一晶面在x、y、z轴上的截距分别为a/3、b/2、c,求出该晶面的晶面指数。
答:(1)h:k:l==3:2:1,∴该晶面的晶面指数为(321);(2)h:k:l=3:2:1,∴该晶面的晶面指数为(321)。
2-3在立方晶系晶胞中画出下列晶面指数和晶向指数:(001)与[],(111)与[],()与[111],()与[236],(257)与[],(123)与[],(102),(),(),[110],[],[]答:2-4定性描述晶体结构的参量有哪些定量描述晶体结构的参量又有哪些答:定性:对称轴、对称中心、晶系、点阵。
定量:晶胞参数。
2-5依据结合力的本质不同,晶体中的键合作用分为哪几类其特点是什么答:晶体中的键合作用可分为离子键、共价键、金属键、范德华键和氢键。
离子键的特点是没有方向性和饱和性,结合力很大。
共价键的特点是具有方向性和饱和性,结合力也很大。
金属键是没有方向性和饱和性的的共价键,结合力是离子间的静电库仑力。
范德华键是通过分子力而产生的键合,分子力很弱。
氢键是两个电负性较大的原子相结合形成的键,具有饱和性。
2-6等径球最紧密堆积的空隙有哪两种一个球的周围有多少个四面体空隙、多少个八面体空隙答:等径球最紧密堆积有六方和面心立方紧密堆积两种,一个球的周围有8个四面体空隙、6个八面体空隙。
2-7n个等径球作最紧密堆积时可形成多少个四面体空隙、多少个八面体空隙不等径球是如何进行堆积的答:n个等径球作最紧密堆积时可形成n个八面体空隙、2n个四面体空隙。
不等径球体进行紧密堆积时,可以看成由大球按等径球体紧密堆积后,小球按其大小分别填充到其空隙中,稍大的小球填充八面体空隙,稍小的小球填充四面体空隙,形成不等径球体紧密堆积。
2-8写出面心立方格子的单位平行六面体上所有结点的坐标。
答:面心立方格子的单位平行六面体上所有结点为:(000)、(001)(100)(101)(110)(010)(011)(111)(0)(0)(0)(1)(1)(1)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
矿产资源开发利用方案编写内容要求及审查大纲
矿产资源开发利用方案编写内容要求及《矿产资源开发利用方案》审查大纲一、概述
㈠矿区位置、隶属关系和企业性质。
如为改扩建矿山, 应说明矿山现状、
特点及存在的主要问题。
㈡编制依据
(1简述项目前期工作进展情况及与有关方面对项目的意向性协议情况。
(2 列出开发利用方案编制所依据的主要基础性资料的名称。
如经储量管理部门认定的矿区地质勘探报告、选矿试验报告、加工利用试验报告、工程地质初评资料、矿区水文资料和供水资料等。
对改、扩建矿山应有生产实际资料, 如矿山总平面现状图、矿床开拓系统图、采场现状图和主要采选设备清单等。
二、矿产品需求现状和预测
㈠该矿产在国内需求情况和市场供应情况
1、矿产品现状及加工利用趋向。
2、国内近、远期的需求量及主要销向预测。
㈡产品价格分析
1、国内矿产品价格现状。
2、矿产品价格稳定性及变化趋势。
三、矿产资源概况
㈠矿区总体概况
1、矿区总体规划情况。
2、矿区矿产资源概况。
3、该设计与矿区总体开发的关系。
㈡该设计项目的资源概况
1、矿床地质及构造特征。
2、矿床开采技术条件及水文地质条件。
