α-苯乙胺的制备与拆分
苯乙胺的合成与拆分

实验三1.刘卡特反应(R.leuchart reaction)—外消旋苯乙胺、萘乙胺系列合成2.外消旋苯乙胺和萘乙胺的拆分研究以下是“外消旋α-苯乙胺的合成与拆分”实验参考讲义。
在此基础上,设计并完成以 α-萘乙酮或β-萘乙酮为原料的合成及外消旋产物的拆分。
一、实验目的和要求1.实验目的(1)通过苯乙酮与甲酸铵反应生成α-苯乙胺,学习醛、酮与伯胺的反应——Leuchart 反应。
(2)通过制备α-苯乙胺学习活蒸气水蒸气蒸馏和减压蒸馏操作。
(3)学习用化学方法将外消旋的化合物拆分为其对映异构体。
(4)学习用旋光仪测定化合物的旋光性。
(5)学习使用数字显微熔点仪。
(6) 学习试剂、溶剂的回收再利用,培养绿色化学理念。
2.具体要求(1)认真预习、完成预习报告(包括实验流程图)。
(2)按讲义要求完成实验,认真做好实验纪录。
(3)产品上交时要有完整的物理数据,如比旋光度、熔点、沸点等。
(4)认真完成实验报告包括思考题。
(5)按要求如期保质保量完成所有规定的实验项目。
二、反应原理1.刘卡特反应(R.leuchart reaction)醛、酮与甲酸和氨(或伯、仲胺),或与甲酰胺作用发生还原胺化反应,称为刘卡特反应。
反应通常不需要溶剂,将反应物混合在一起加热(100~180ºC )即能发生。
选用适当的胺(或氨)可以合成伯、仲、叔胺。
反应中氨首先与羰基发生亲核加成,接着脱水生成亚胺,亚胺随后被还原生成胺。
与还原胺化不同,这里不是用催化氢化,而是用甲酸作为还原剂。
反应过程如下:O HC ONH4HCO 2H +NH 3C O +NH3C NHNH 2+-2CO 2+C NH 2H +苯乙酮在高温下与甲酸铵反应得到(±)-α-苯乙胺:O C 6H 5CCH 3O C 4H 185o CNH 2C 6H 5CHCH 3OC 6H 5CCH 3NH 2C 6H 5CHCH 3+2HCO 2NH 4C 6H 5CH NHCHO CH 3C 6H 5CH NHCHO CH 3+++NH CO 2H 2OHCl +H 2OCH 3C 6H 5CHNH 3Cl +-+HCO 2HCH 3C 6H 5CHNH 3Cl +-+NaOH+NaCl +H 2O(±)-α-苯乙胺2.(±)-α-苯乙胺的拆分原理用化学方法拆分外消旋体,其原理是用旋光性试剂把外消旋的对映异构体变成可分离的非对映异构体混合物,再利用非对映异构体的物理性质不同,将其分离。
D-酒石酸拆分外消旋α-苯乙胺工艺研究

D-酒石酸拆分外消旋α-苯乙胺工艺研究古凤强;吕远洋;吕世柱;唐建荣;李镇锋;刘天穗;陈亿新;陈国术【摘要】以D-酒石酸为拆分试剂,采用程序降温结晶法,对外消旋α-苯乙胺的拆分工艺进行了探究.通过对结晶的工艺、溶剂、温度等条件的优化试验,确定了外消旋α-苯乙胺的最佳拆分工艺,其中(R)-(+)-α-苯乙铵·D-酒石酸盐晶体收率高达95.0%,水解、精馏得(R)-(+)-α-苯乙胺,收率86.5%,ee值为93.0%,[α]D +38.3°.同时,开发了一种在四氢呋喃溶液中硫酸酸化D-酒石酸钠回收D-酒石酸的新方法,D-酒石酸的回收率93.0%.其拆分工艺简单,生产成本低,具有良好的工业应用价值.【期刊名称】《广州化工》【年(卷),期】2013(041)005【总页数】3页(P5-7)【关键词】D-酒石酸;(±)-α-苯乙胺;拆分;酒石酸回收【作者】古凤强;吕远洋;吕世柱;唐建荣;李镇锋;刘天穗;陈亿新;陈国术【作者单位】广州大学化学化工学院,广东广州 510006【正文语种】中文【中图分类】TQ246.3光学纯的α-苯乙胺是一种应用广泛的有机酸类手性拆分剂,又是优良的手性助剂和合成原料[1],使用便利、价格适中。
光学纯的α-苯乙胺通常是采用选择性结晶的方法制备,已见报道的手性拆分剂主要有光学纯的酒石酸、苹果酸等[2-5]。
酒石酸拆分法是外消旋α-苯乙胺的传统拆分方法,具有原料价格便宜,拆分工艺简单,产品光学纯度较高等优点。
然而,酒石酸拆分外消旋α-苯乙胺工艺仍存在以下问题:(1)溶剂用量大。
工业上一次拆分1吨外消旋α-苯乙胺,大约需用13 t的甲醇溶剂;(2)收率低。
光学纯苯乙胺的收率一般只在60.0%~65.0%;(3)结晶时间长。
结晶时间需要24~48 h;(4)酒石酸回收工艺复杂,成本高。
针对上述问题,作者开发的程序控温结晶法和硫酸酸化酒石酸钠回收酒石酸的四氢呋喃溶剂法,实现了D-酒石酸高产率、高光学纯度的连续拆分外消旋α-苯乙胺工艺。
合成化学实验四 α
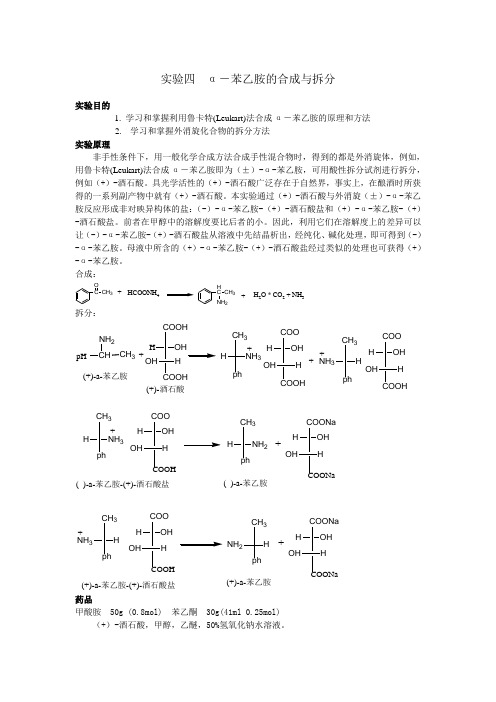
实验四 α-苯乙胺的合成与拆分实验目的1. 学习和掌握利用鲁卡特(Leukart)法合成α-苯乙胺的原理和方法2. 学习和掌握外消旋化合物的拆分方法实验原理非手性条件下,用一般化学合成方法合成手性混合物时,得到的都是外消旋体,例如,用鲁卡特(Leukart)法合成α-苯乙胺即为(±)-α-苯乙胺,可用酸性拆分试剂进行拆分,例如(+)-酒石酸。
具光学活性的(+)-酒石酸广泛存在于自然界,事实上,在酿酒时所获得的一系列副产物中就有(+)-酒石酸。
本实验通过(+)-酒石酸与外消旋(±)-α-苯乙胺反应形成非对映异构体的盐:(-)-α-苯乙胺-(+)-酒石酸盐和(+)-α-苯乙胺-(+)-酒石酸盐。
前者在甲醇中的溶解度要比后者的小。
因此,利用它们在溶解度上的差异可以让(-)-α-苯乙胺-(+)-酒石酸盐从溶液中先结晶析出,经纯化、碱化处理,即可得到(-)-α-苯乙胺。
母液中所含的(+)-α-苯乙胺-(+)-酒石酸盐经过类似的处理也可获得(+)-α-苯乙胺。
合成:C OCH 3HCOONH 4HC CH 3NH 2++H 2O * CO 2 + NH 3拆分:pHCHNH 2CH 3+3_++NH +_(+)-a-苯乙胺(+)-酒石酸_3+( )-a-苯乙胺-(+)-酒石酸盐_2+_( )-a-苯乙胺_NH (+)-a-苯乙胺-(+)-酒石酸盐+_NH +(+)-a-苯乙胺药品甲酸胺 50g (0.8mol) 苯乙酮 30g(41ml 0.25mol)(+)-酒石酸,甲醇,乙醚,50%氢氧化钠水溶液。
实验步骤(±)-α-苯乙胺的合成装置:以250ml三口瓶作反应器,搭建一蒸馏装置,侧口装温度计,温度计插到液面下,尾气吸收。
用电炉加热。
在250ml三口瓶中加入22.2g甲酸胺,12mL苯乙酮及几粒沸石,缓慢加热至150-155℃,混合物开始溶解同时有馏分馏出,并不断放出气泡(氨和二氧化碳),反应 1.5h,温度可达185-190℃,停止加热,将馏分倒入分液漏斗中。
α-苯乙胺 的制备 及 拆分

实验1外消旋a 苯乙胺的制备一、实验目的1. 学习Leuchart 反应合成外消旋体a-苯乙胺的原理和方法。
2. 通过外消旋a -苯乙胺的制备,进一步综合运用回流、蒸馏、萃取的测定等基本操作。
3. 通过本实验提高实验化学的研究能力和素质。
二、实验原理醛、酮与甲酸和氨(或伯、仲胺),或与甲酰胺作用发生还原胺化反应,称为鲁卡特 (Leuchart )反应。
反应通常不需要溶剂,将反应物混合在一起加热(100〜180°C )即能发生。
选用适当的胺(或氨)可以合成伯、仲、叔胺。
反应中氨首先与羰基发生亲核加成,接着脱水生成亚胺,亚胺随后被还原生成胺。
与还原胺化不同,这里不是用催化氢化,而是用甲酸作为还原剂。
它是由羰基化合物合成胺的一种重要方法。
本实验是苯乙酮与甲酸铵作用得到外消旋体(土)-a -苯乙胺。
反应过程为:HCOONH 4HCOOH+NH 3依照前面的机理生成的a -苯乙胺再与过量的甲酸形成甲酰胺,经酸水解形成铵盐,再用碱将其游离,得到a -苯乙胺。
a -苯乙胺的旋光异构体可作为碱性拆分剂用于拆分酸性外消旋体。
a -苯乙胺是制备精细化学品的一种重要中间体,它的衍生物广泛用于医药化工领域,主要用于合成医药、染料、香料乳化剂等。
三、实验用品仪器与材料:圆底烧瓶、三口烧瓶、球型冷凝管、直型冷凝管、空气冷凝管、烧杯、锥形瓶、分液漏斗、蒸馏头、锥形瓶、玻璃小漏斗、温度计、电炉或酒精灯等。
药品:苯乙酮、甲酸铵、氯仿、甲苯、浓HCl ,50%NaOH 溶液、固体NaOH 。
)C=O+NH 3片―OHNH 2—O 厂-O-C-H+)C=j+H 2-HO,)C=NH NH+-;C =N H 2IH-q-NH +C°2©心皿+2HCOONH 4——C H 3Q-CH-NHCHO+HCI +H 2OC H3 O (H-NHCHO+NH 3T +CO 2T +H 2OC H3*Cj-CH-NH 3C 「 +HCOOHCH 3◎-C H -NH 3CCH3—,Q-CH -NH 2+NaCl+H 2O四、实验步骤1.合成在250(100)mL圆底烧瓶中,加入22.5mL(0.2mol)(12.0g)苯乙酮,40g(约0.64mol)(22.2g)甲酸铵和几粒沸石,装上蒸馏头并装配成简单蒸馏装置。
α-苯乙胺的合成及拆分

α-苯乙胺的合成及拆分
周霞
【期刊名称】《广东化工》
【年(卷),期】2008(35)7
【摘要】文章综述了外消旋α-苯乙胺由苯乙酮,苯甲腈,苯甲胺的合成,进一步介绍了光学活性α-苯乙胺由肟醚苯甲醛苯乙酮苯甲腈的不对称合成,以及由拆分方法制备光学活性α-苯乙胺,如用手性酰化试剂选择性与苯乙胺形成酰胺的动力学拆分,通过选择性生成结晶盐拆分.笔者用组合方法拆分α-苯乙胺并加入不同添加剂得出不同的结果.最后得出结论,寻找合适的添加剂是有效拆分的一条有希望的途径.
【总页数】5页(P78-82)
【作者】周霞
【作者单位】中山火炬职业技术学院生物医药系,广东,中山,528439
【正文语种】中文
【中图分类】TQ2
【相关文献】
1.新拆分试剂R(-)四氢噻唑-2-硫酮-4-羧酸对R,S-α-苯乙胺拆分的研究 [J], 李叶芝;郭纯孝;刁家寅;黄化民
2.(R)-α-苯乙胺拆分全顺式-3-N-叔丁氧羰基氨基-5-甲氧羰基环己基甲酸 [J], 张军;林志忠;邓金根
3.外消旋α-苯乙胺的合成及拆分 [J], 刘道明;
4.一种新型α-苯乙胺拆分剂 [J], 胡勇男;杨会芬
5.消旋棉酚拆分的研究——Ⅱ.手性α-甲基苯乙胺及α-甲基苄胺为拆分剂 [J], 郑多楷;司伊康;孟佳克;黄量
因版权原因,仅展示原文概要,查看原文内容请购买。
合成化学实验报告

合成化学实验报告班级姓名合作者XXXXX大学化学化工系实验者基本信息合成化学实验报告书写要求一、实验题目二、实验内容简介(摘要):简单介绍本次实验的目的、意义、产物应用领域、通过实验,了解相关领域的基本知识,实验方法与实验结果的简单叙述。
三、实验药品与仪器写出实验中所涉及到的主要的化学试剂的物理常数、规格、用量、生产厂家;实验仪器型号、生产厂家。
四、实验原理与方法:用化学反应式表述反应过程、必要时可配有必要的文字说明。
五、实验步骤与实验现象、实验数据记录:以简练的语言描述实验过程、实验现象、实验数据。
实验现象、实验数据必须当时完成,不得事后补填。
六、实验结果与数据处理:必须指出实验结论、对产物用文字(如外观、状态、颜色、气味等)和数据(如产率、体积、质量、产率、熔点、沸程、折光率等)进行描述七、分析与讨论实验结束后,应仔细分析实验现象、实验数据、从理论上、实验技术上对实验作出有价值论断,指出实验要点、技巧;自己实验的不足、改进的方法;对实验方法的合理化建议等。
实验分析要理论结合实际,要对实验有深刻的理解。
八、回答问题对课后思考题作出符合题意的解答。
说明:课前预习写在实验报告上(包括实验题目、摘要、仪器与药品、实验步骤),数据在实验过程中填写,分析讨论、回答问题课后写,实验三天后交报告。
合成化学实验报告实验目的:实验原理:实验仪器和化学试剂第页 /共页第页/共页实验结果与数据处理实验成绩和评语第页/共页实验一Jone’s试剂氧化法制备薄荷酮薄荷酮存在于天然植物中,用于香精和香料的制造。
薄荷醇有8种异构体。
从天然薄荷油中分离所得到的是左旋薄荷醇,它是薄荷植物的主要成分,有杀菌、防腐的作用,广泛用于医药、饮料、香料和化妆品工业。
(-)-薄荷醇和(-)-薄荷酮都具有稳定的全平状构象。
实验目的:1.了解Jone’s试剂及其氧化反应特点2.学习半微量合成技术/减压蒸馏技术3.学习薄层展开技术实验原理:Jone's试剂试剂与用量:薄荷醇1.0g(4.0m mol); 丙酮20mL; 三氧化铬,硫酸。
实验二十三外消旋α-苯乙胺的合成和拆分

实验二十三外消旋α-苯乙胺的合成和拆分实验二十三外消旋α-苯乙胺的合成和拆分一、实验目的1、学习外消旋α-苯乙胺的合成方法。
2、掌握外消旋体的拆分的基本原理和方法、学习旋光度的测定方法 3二、基本原理在非手性条件下,由一般合成反应所得的手性化合物为等量的对映体组成的外消旋体,故无旋光性。
利用拆分的方法,把外消旋体的一对对映体分成纯净的左旋体和右旋体,即所谓的消旋体的拆分。
拆分外消旋体最常用的方法是利用化学反应把对映体变为非对映体。
如果手性化合物分子中含有一个易于反应的极性基团,如羧基,氨基等,就可以使它与一个纯的旋光化合物(拆解剂)反应,从而把一对对映体变成两种非对映体。
由于非对映体具有不同的物理性质,如溶解性,结晶性等,利用结晶等方法将他们分离、精制,然后再去掉拆解剂,就可以得到纯的旋光化合物,达到拆分目的。
常用的拆解剂有马钱子碱、奎宁和麻黄素等旋光纯的生物碱(拆分外消旋的有机酸)以及酒石酸、樟脑磺酸等旋光纯的有机酸(拆分外消旋的有机碱)。
外消旋的醇通常先与丁二酸酐或邻苯二甲酸酐形成单酯,用旋光醇的碱把酸拆分,再经碱性水解得到单个的旋光性的醇。
对映体的完全分离当然是最理想的,但是实际工作中很难做到这一点,常用光学纯度表示被拆分后对映体的纯净程度,它等于样品的比旋光除以纯对映体的比旋光。
光学纯度(op)=样品的[a]/纯物质的[a]*100%。
本实验用(+)-酒石酸为拆解剂,它与外消旋α-苯乙胺形成非对映异构体的盐。
旋光纯的酒石酸在自然界颇为丰富,它是酿酒过程中的副产物。
由于(-)-胺(+)-酸非对映体的盐比另一种非对映体的盐在甲醇中的溶解度小,故易从溶液中呈结晶析出,经稀碱处理,使(-)-α-苯乙胺游离出来。
母液中含有(+)-胺(+)-酸盐,原则上经提纯后可以得到另一个非对映体的盐,经稀碱处理后得到(+)-胺。
本实验只分离对映异构体之一,即左旋异构体,因右旋异构体的分离对学生来说显得困难。
本实验用(+)-酒石酸为拆解剂,它与外消旋α-苯乙胺形成非对映异构体的盐。
实验 二α-苯乙胺的拆分与旋光度测定

实验操作
1. s-(-)-α-苯乙胺的分离
(-)-胺(+)-酒石酸盐制备
250 mL锥型瓶
6.3g(+)-酒石酸、90mL甲醇 5g α-苯乙胺
加热近60 ℃使互溶 搅拌下缓慢滴加
冷至室温,塞住瓶口,放置24h以上,应析出白色棱状晶体 抽滤,冷甲醇洗涤晶体,干燥, 得(-)-胺(+)-酒石酸盐约4g
实验 二
α-苯乙胺的拆分与旋光度测定
实验目的
1、掌握外消旋体的拆分的基本原理和方法
2、学习旋光度的测定方法
拆分原理
COOH CHNH2 CH3 (+)- - 苯乙胺 H + HO OH H COOH (+)- 酒石酸
CH3 H NH3 H HO COO OH H COOH (+)- 胺 (+)- 酸盐 + NH3 CH3 H H HO COO OH H COOH ( )- 胺 (+)- 酸盐
(1)必须得到棱状晶体,这是实验成功的关键。如溶 液中析出针状晶体,可采取如下步骤: A、可加热反应混合物至恰好针状晶体已完全溶解 而棱状晶体未开始溶解为止,重新放置过夜。 B、分出少量棱状晶体,加热反应混合物至其余晶 体全部溶解,稍冷却后用取出的棱状晶体作种晶。 (2)蒸馏α-苯乙胺时,容易起泡,可加入1-2滴消泡剂 (聚二甲基硅烷0.001%的已烷溶液)。
α-苯乙胺的1H NMR
A B C D
1.355 4.050 1.87 7.18 to 7.38
思考题
你认为本实验中关键步骤是什么?如何控制
反应条件才能分离出纯的旋光异构体?
拆分外消旋体最常用的方法是利用化学反应把一对对映 体变成两种非对映体。由于非对映体具有不同的物理性质, 利用结晶等方法将其分离、精制,然后再去掉拆解剂,就可 以得到纯的旋光化合物,达到拆分目的。
微波合成苯乙胺及苯乙胺的拆分

+
NH2 NH3 C OH α— 氨基 醇 — _H O 2
NH H2/Ni C
NH2 C
C 亚胺 胺
如果用甲酸做还原剂来替代H2/Ni,那么这个还 原胺化过程就被称为鲁卡特反应。
2、微波加速化学反应的机理
有两种观点:A、微波是一种内加热方式; 有加热速度快,加热均匀,无滞后效应 等特点;B、微波作用机理复杂,一方面 反应物分子吸收微波能量,提高分子运 动速度,导致熵的增加;另一方面微波 对极性分子的作用,迫使其按电磁场作 用运动(2.45X109次/S),导致熵的减少。
将上述所获(-)-α-苯乙胺-(+)-酒石酸盐溶入 10ml水中,加入1.5ml50%氢氧化钠溶液,充 分振摇后溶液呈强碱性。用乙醚对溶液萃取三 次(3×10ml )合并乙醚萃取液,用无水硫酸 钠干燥,过滤,热水浴蒸除乙醚,即得(-)-α-苯 乙胺粗品。 称重、测旋光度并计算产率和比旋光度,通过 与其纯样品的比旋光度比较,求出实验样品的 光学纯度。 纯(-)-α-苯乙胺mp184~1860C
3、反应方程式
O CCH3 + 2 HCOONH4 NHCHO CHCH3 + 2 H2O + CO2 + NH3
NHCHO CHCH3 + H 2O + HCl NH2 + NaOH CHCH3 α
NH3Cl CHCH3 + HCOOH
NH3Cl CHCH3
+
NaCl +
H 2O
苯乙胺
(二)仪器和试剂
(三)实验方法
1、 微波反应器使用方法 、 (1) 按电源键。 (2) 设温度:按住“模式”键至出现红色 “C 02”字符(约2S),可用增加“∨”或减 少“∧”键来设定T。其中数字的倍率可通过 “位移”键来改变,再按模式至“STOP”出现。 (3) 微波反应器顶部的孔中不得放入金属导 线(包括水银温度计),以免微波泄露。 (4) 运行:关上门;按“启动”键;此时风 扇开始工作。
α-苯乙胺的制备与拆分

•α-苯乙胺的制备与拆分Ⅰ. 预习报告一、实验目的•学习并掌握诺伊卡特反应(Leuchart reaction),并用以合成(±)-a-苯乙胺;•学习并掌握外消旋体化合物的拆分方法,并用酒石酸拆分(±)-a-苯乙胺•学习旋光仪测定物质旋光度的方法;•通过学习熟悉外消旋a-苯乙胺的制备,巩固萃取、水蒸气蒸馏等基本操作,学习掌握水蒸气蒸馏的原理、作用及操作技术;•熟练掌握各种操作,提高实验技能,达到训练的目的。
二、实验原理(1)醛或酮在高温下与甲酸铵作用得到伯胺的反应称为R.Leuchart反应,方程式如下:在反应中氨首先与羰基发生亲和加成,接着脱水生成亚胺,亚胺随后被还原生成胺。
与还原胺化不同,这里不是用催化氢化,而是用甲酸作为还原剂,反应过程如下:外消旋á-苯乙胺的合成:制备:实验是苯乙酮与甲酸铵作用得到外消旋–α–苯乙胺,反应过程如下:拆分:实验采用L–(+)–酒石酸与(±)–α–苯乙胺反应,产生两个非对映异构体的盐的混合物,这两个盐在甲醇中的溶解度有显著差异,可以用分步结晶法将它们分离开来,然后再分别用碱对这两个已分离的盐进行处理,就能使(+)、(–)–α–苯乙胺分别游离出来,从而得到纯的(+)–α–苯乙胺和(–)–α–苯乙胺。
(3)仪器与试剂仪器:圆底烧瓶、三口烧瓶、蒸馏装置、分液漏斗、水蒸汽蒸馏装置、锥形瓶、分液漏斗等。
拆分所需仪器包括量筒必须干燥。
试剂:苯乙酮,甲酸铵,浓盐酸,氢氧化钠,甲苯,L-(+)-酒石酸,a-苯乙胺,甲醇,乙醚,50%的氢氧化钠溶液,粒状NaOH。
(4)物理性质熔点 -65℃沸点 194.5-195℃相对密度 0.9640溶解情况溶于水,易溶于醇和醚性状、味道苯乙胺为无色具的鱼腥味的强碱性液体特性苯乙胺能吸收空气中的二氧化碳,成相应的碳酸盐。
用冷冻盐水冷却也不固化(熔点-65℃)。
苯乙胺盐酸盐为片状结晶。
熔点217℃(从醇中析出),易溶于水、溶于醇,但不溶于醚。
外消旋α-苯乙胺的合成及拆分

Journal of Organic Chemistry Research 有机化学研究, 2019, 7(2), 63-69Published Online Jnue 2019 in Hans. /journal/jocrhttps:///10.12677/jocr.2019.72009The Preparation and Splitting of Racemateα-PhenylethylamineDaoming LiuAnhui Jinbang Pharmaceutical Chemical Co., Ltd., Chuzhou AnhuiReceived: June 4th, 2019; accepted: June 19th, 2019; published: June 26th, 2019AbstractS-(-)-α-phenylethylamine is an intermediate for the preparation of fosfomycin, which is one of the first choices for splitting the acidic racemic compounds as well. In this article, racemate-pheny- lethylamine was synthesized by the Leuckart reaction of acetophenone and ammonium formate.Then α-phenylethylamine was split by the L-tartaric acid in methanol. Finally, the infrared and ul-traviolet spectra of the products were analyzed. Through conditional experiments, the best ratio of reactants in the synthesis of racemic-phenylethylamine is 1:5 mole ratio of acetophenone to ammonium formate. The best temperature for splitting racemate-phenylethylamine is 70˚C. The best splitting time is 20 mins; the best stirring speed is 240 r/min. Under these optimal conditions, the best yield of α-phenylethylamine is 43.72%, and the best optical purity after splitting is80.22%.KeywordsRacemate-Phenylethylamine, Synthesize, Split, Optical Purity外消旋α-苯乙胺的合成及拆分刘道明安徽金邦医药化工有限公司,安徽滁州收稿日期:2019年6月4日;录用日期:2019年6月19日;发布日期:2019年6月26日摘要S-(-)-α-苯乙胺是制备磷霉素的中间体,并且是首选的酸性外消旋化合物拆分剂之一。
a-苯乙胺的拆分-上课用

OH
① 通过甲醇分步结晶分离
结晶
+ (-)-C6H5CH-NH3²(+)OOCCH-CHCOOH
母液
+ (+)-C6H5CH-NH3²(+)OOCCH-CHCOOH
CH3
HO
NaOH
OH
CH3
HO
NaOH
OH
(-)-C6H5CH-NH2 + (+)NaOOCCH-CHCOONa CH3 HO
四、实验步骤
1、成盐与分步结晶 在250 mL锥形瓶中放入6.3gD-(+)-酒石酸和90 mL甲醇, 装上回流冷凝管后在水浴上加热至接近沸腾(约60℃)。待 D-(+)-酒石酸全部溶解后,停止加热,稍冷后移去回流冷凝 管,在振摇下用滴管将5克 (±)-α-苯乙胺慢慢加入热溶液中 。加完稍加振摇,冷至室温后,塞紧瓶塞,放置24 h以上。 瓶内应生成颗粒状棱柱形晶体,若生成针状晶体与棱柱形结 晶混合物,应置于热水浴中重新加热溶解,再让溶液慢慢冷 却。待析出棱状结晶完全后,减压过滤,晶体用少量冷甲醇 洗涤,晾干,得到的主要是(-)-α-苯乙胺· (+)-酒石酸盐。称量 (产量约4 g)并计算产率。母液保留用于制备另一种对映 体。
外消旋α-苯乙胺的 的拆分
一、实验目的
1.学习将外消旋体转变为非对映异构体拆分 外消旋体的原理和方法。 2.学习旋光度的测定方法。了解对光学活性 物质纯度的初步评价。
二、实验原理
在实际工作中,要得到单个旋光纯的对映体,并 不是件容易的事情,往往需要冗长的拆分操作和反复 的重结晶才能完成。而要完全分离也是很困难的。常 用光学纯度表示被拆分后对映体的纯净程度,它等于 样品的比旋光度除以纯对映体的比旋光度。
α-苯乙胺的制备及拆分

姓名: 学号: 专业:实验五( )-α-苯乙胺的合成一、实验目的1. 学习Leuchart 反应合成外消旋体α-苯乙胺的原理和方法。
2. 通过外消旋α-苯乙胺的制备,进一步综合运用回流、蒸馏、萃取的测定等基本操作。
3. 通过本实验提高实验化学的研究能力和素质。
二、实验原理醛、酮与甲酸和氨(或伯、仲胺),或与甲酰胺作用发生还原胺化反应,称为鲁卡特(Leuchart )反应。
反应通常不需要溶剂,将反应物混合在一起加热(100~180℃)即能发生。
选用适当的胺(或氨)可以合成伯、仲、叔胺。
反应中氨首先与羰基发生亲核加成,接着脱水生成亚胺,亚胺随后被还原生成胺。
与还原胺化不同,这里不是用催化氢化,而是用甲酸作为还原剂。
它是由羰基化合物合成胺的一种重要方法。
本实验是苯乙酮与甲酸铵作用得到外消旋体(±)-α-苯乙胺。
反应过程为:依照前面的机理生成的α-苯乙胺再与过量的甲酸形成甲酰胺,经酸水解形成铵盐,再用碱将其游离,得到α-苯乙胺。
α-苯乙胺的旋光异构体可作为碱性拆分剂用于拆分酸性外消旋体。
α-苯乙胺是制备精细化学品的一种重要中间体,它的衍生物广泛用于医药化工领域,主要用于合成医药、染料、香料乳化剂等。
C=O + NH 3 -H 2O C —OH NH 2 C=NH NH 4++ C=NH 2 HCOONH 4 HCOOH + NH 3 + C=NH 2 -O=H-C-NH 2 + CO 2 + 2HCOONH 4-C-CH 3 O=CH 3 -CH-NHCHO + NH 3↑+ CO 2↑ + H 2O CH 3 -CH-NHCHO + HCl + H 2O + CH 3-CH-NH 3Cl -+ HCOOH+ CH 3 -CH-NH 3Cl - + NaOH CH 3 -CH-NH 2+ NaCl + H 2O三、实验用品仪器与材料:圆底烧瓶、三口烧瓶、球型冷凝管、直型冷凝管、空气冷凝管、烧杯、锥形瓶、分液漏斗、蒸馏头、锥形瓶、玻璃小漏斗、温度计、电炉或酒精灯等。
α-苯乙胺思考题

D 由羰基合成酰胺类化合物。 3、为什么用苯对水解溶液进行萃取? A 萃取反应产物。 B 提纯反应产物。 C 萃取未反应的苯乙酮。 (正确) D 提取甲酸胺。 4、水汽蒸馏时,馏出液是什么? A 馏出液是水。 B 馏出液是苯乙酮 C 馏出液是氢氧化钠
Байду номын сангаас
D 馏出液是苯乙胺加水。 (正确) 5、水汽蒸馏时蒸汽倒入管应插入到什么位置? A 液面上。 B 三口瓶瓶口处。 C 液面与瓶底1/2位置处。 D 尽量接近瓶底。 (正确) 6、 (+)-α-苯乙胺的拆分应该用什么拆分剂? A (+)-酒石酸。 B (+)-麻黄碱。 C (+)-苯乙醇酸。
(+)-α-苯乙胺的合成及拆分思考题
1、 α-苯乙胺的用途是什么? A 制备医药、香料等的中间体。 (正确) B 食品添加剂 C 杀虫剂、防腐剂等中间体 D 橡胶、塑料等促进剂 2、鲁卡特反应是由什么原料来制备什么产物的反映? A 由醇类制取醚类化合物。 B 由醛、酮制酸基化合物 C 由羰基合成胺类化合物。 (正确)
D (+)-酒石酸。 (正确) 7、拆分时,溶剂量(甲醇)太少,有什么后 果? A (+)- α-苯乙胺- (+)-酒石酸析不出。 B (-) - α-苯乙胺- (+)-酒石酸析不出。 C (+)- α-苯乙胺- (+)-酒石酸先析出。 D (-) - α-苯乙胺- (+)-酒石酸和(+)- α苯乙胺- (+)-酒石酸一同析出,无法分离。 (正确)
实验八 苯乙胺

实验八外消旋α-苯乙胺的制备及拆分一、实验目的1.学习由鲁卡特反应制取胺的原理及实验方法,掌握蒸馏的操作技术。
2.学习碱性外消旋体的拆分原理和实验方法。
二、实验内容手型拆分:手性拆分(Chiral resolution),亦称光学拆分(Optical resolution)或外消旋体拆分,为立体化学上,用以分离外消旋化合物成为两个不同的镜像异构物的方法。
为生产具有光学活性药物的重要工具。
手性拆分方法主要有以下四种:结晶拆分法,化学法,酶解法和柱色谱法。
本实验中用到化学法:一对对映异构体的物理、与非手性试剂反应的化学性质相同,因此一般的分离方法无法将其拆分出来。
化学拆分法是用一个纯的光活性异构体D -碱去处理这一D-酸和L-酸的混合物,与其分别反应衍生化,形成一对非对映体:D-酸-D-碱和 L-酸-D-碱。
非对映体很容易通过普通的物理方法如分级结晶法分离出来。
在分离出非对映体之后,只要用强酸处理便可以分别得到纯的D-酸和L-酸。
化学拆分法适用于含有易反应基团,而且反应后也容易再生出原来的对映体化合物的分子。
最常见的易反应基团为酸碱基团,这是由于酸碱反应非常简便,生成的盐类比较容易结晶,拆分剂酸、碱(通常为天然存在的酸或生物碱)廉价易得或可方便回收,也比较容易制得旋光纯。
常用的酸性拆分剂有:(+)-酒石酸、(+)-樟脑酸、(+)-樟脑-10-磺酸、L-(+)-甘氨酸等;常用的碱性拆分剂有:(−)-马钱子碱、(−)-番木鳖碱、D-(−)-麻黄碱、(+)或(−)-α-苯乙胺等。
整个实验需10-12学时。
三、实验原理在非手性条件下,由一般合成方法所得的手性化合物为等量的对映体组成的外消旋体。
如:外消旋α-苯乙胺的常规合成方法:外消旋α-苯乙胺含一个手性碳原子,具有旋光性。
但此化合物得到50%的R-构型和50% S-构型两个对映体的混合物:(±)-α-苯乙胺,这种等量的对映体的混合物称为外消旋体,旋光度(α)=0。
实验 二α-苯乙胺的拆分与旋光度测定

实验二α-苯乙胺的拆分与旋光度测定引言手性是化学中一个重要的概念。
手性分子与非手性分子具有不同的化学和生物学性质。
在有机合成中,总是会产生手性分子和非手性分子的混合物,在分离和分析这些分子中,需要采用分离技术和手性分析技术。
手性化合物在生物学上也很重要,如药物作用的优选等。
因此,研究手性分子的拆分和手性测定方法极其重要。
实验目的了解手性分子的拆分方法,掌握α-苯乙胺的拆分方法;学习旋光法并掌握旋光度测定方法;探究实验过程中可能出现的问题及对策。
实验原理1.手性分子手性分子具有不对称的结构,它们的立体化学特性直接影响着其性质和功能。
一个分子的手性性质取决于其对映异构体的存在情况和其对映异构体的相对构型。
手性分子的拆分成为两个相对构型不同的对映异构体,称为手性拆分。
在化学合成的过程中,总是会生成不对称化合物的混合物,通常还会夹杂着化学反应的副产物、不纯物等。
分离这些化合物成为分离化学物质的重要手段,包括挤压色谱、微柱色谱、反相高效液相色谱等方法。
2.α-苯乙胺的拆分α-苯乙胺是一种含有手性中心的分子,可以通过拆分反应得到对映异构体。
其拆分反应机理如下:苯乙酮和一分子的对映体触媒,然后在碱催化下发生反应,生成对映异构体的化合物。
3.旋光法旋光法是一种测定手性分子光学活性的方法。
它的基本原理是:在手性分子的存在下,假设部分平面偏振光(可以是左旋偏振光或右旋偏振光)通过一个等长的样品(可以是水、无机盐等)后,形成的平面偏振光被旋转一定的角度,就是旋光角度。
无色无味的立体异构体之间就可以通过旋光角度来区别。
旋光度测定时一般使用的仪器是旋光仪。
旋光仪分为手摇旋光仪和电动旋光仪。
它们之间的差别是:前者的旋光度测定精度较低,后者的精度较高。
4.光学活性体与光学异构体在反射和折射现象中,较简单的是线偏振光和部分偏振光。
它们的限制性较强,适用性局限性也较大,改变光的传播方向只能在一条直线上进行。
光学异构体是具有相同物理化学性质但旋光性相反的两种对映异构体,称为对映异构体。
实验八 苯乙胺

实验八外消旋α-苯乙胺的制备及拆分一、实验目的1.学习由鲁卡特反应制取胺的原理及实验方法, 掌握蒸馏的操作技术。
2.学习碱性外消旋体的拆分原理和实验方法。
二、实验内容手型拆分: 手性拆分(Chiral resolution), 亦称光学拆分(Optical resolution)或外消旋体拆分, 为立体化学上, 用以分离外消旋化合物成为两个不同的镜像异构物的方法。
为生产具有光学活性药物的重要工具。
手性拆分方法主要有以下四种: 结晶拆分法, 化学法, 酶解法和柱色谱法。
本实验中用到化学法: 一对对映异构体的物理、与非手性试剂反应的化学性质相同, 因此一般的分离方法无法将其拆分出来。
化学拆分法是用一个纯的光活性异构体D -碱去处理这一D-酸和L-酸的混合物, 与其分别反应衍生化, 形成一对非对映体: D-酸-D-碱和 L-酸-D-碱。
非对映体很容易通过普通的物理方法如分级结晶法分离出来。
在分离出非对映体之后, 只要用强酸处理便可以分别得到纯的D-酸和L-酸。
化学拆分法适用于含有易反应基团, 而且反应后也容易再生出原来的对映体化合物的分子。
最常见的易反应基团为酸碱基团, 这是由于酸碱反应非常简便, 生成的盐类比较容易结晶, 拆分剂酸、碱(通常为天然存在的酸或生物碱)廉价易得或可方便回收, 也比较容易制得旋光纯。
常用的酸性拆分剂有:(+)-酒石酸、(+)-樟脑酸、(+)-樟脑-10-磺酸、L-(+)-甘氨酸等;常用的碱性拆分剂有:(−)-马钱子碱、(−)-番木鳖碱、D-(−)-麻黄碱、(+)或(−)-α-苯乙胺等。
整个实验需10-12学时。
三、实验原理在非手性条件下, 由一般合成方法所得的手性化合物为等量的对映体组成的外消旋体。
如: 外消旋α-苯乙胺的常规合成方法:外消旋α-苯乙胺含一个手性碳原子, 具有旋光性。
但此化合物得到50%的R-构型和50%S-构型两个对映体的混合物:(±)-α-苯乙胺, 这种等量的对映体的混合物称为外消旋体, 旋光度(α)=0。
微波合成苯乙胺及苯乙胺的拆分
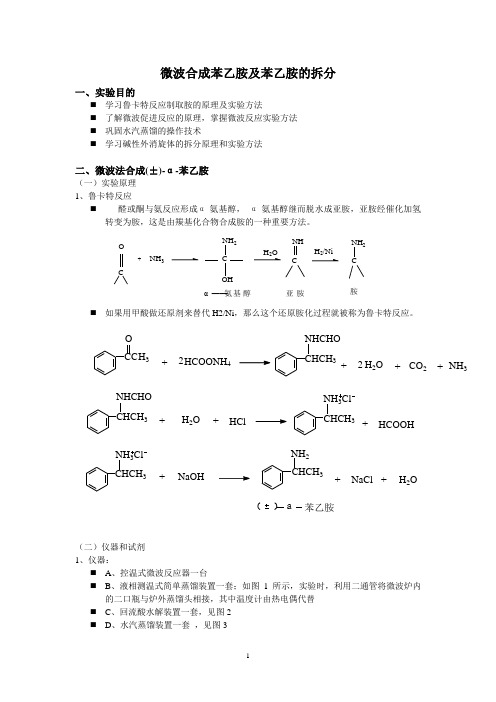
微波合成苯乙胺及苯乙胺的拆分一、实验目的⏹ 学习鲁卡特反应制取胺的原理及实验方法⏹ 了解微波促进反应的原理,掌握微波反应实验方法 ⏹ 巩固水汽蒸馏的操作技术⏹ 学习碱性外消旋体的拆分原理和实验方法二、微波法合成(±)-α-苯乙胺(一)实验原理 1、鲁卡特反应⏹ 醛或酮与氨反应形成α-氨基醇, α-氨基醇继而脱水成亚胺,亚胺经催化加氢转变为胺,这是由羰基化合物合成胺的一种重要方法。
⏹ 如果用甲酸做还原剂来替代H2/Ni ,那么这个还原胺化过程就被称为鲁卡特反应。
(二)仪器和试剂 1、仪器:⏹ A 、控温式微波反应器一台⏹ B 、液相测温式简单蒸馏装置一套;如图1所示,实验时,利用二通管将微波炉内的二口瓶与炉外蒸馏头相接,其中温度计由热电偶代替 ⏹ C 、回流酸水解装置一套,见图2 ⏹ D 、水汽蒸馏装置一套 ,见图3C C H 3O H C O O N H 4N H C H O H 2OC O 2N H 3H C lH C O O HN aO HN aC l+2C H C H 3++2+N H C H O H 2O++N H 3C l+N H 3C l N H 2+++H 2O苯乙胺aC H C H 3C H C H 3C H C H 3C H C H 3微波蒸馏装置 (图1) 回流装置(图2)水蒸汽蒸馏装置(图3)2、试剂及用量⏹ 甲酸铵17克(0.27mol) ,⏹ 苯乙酮12ml (12 . 8克, 0. 107mol ); ⏹ 苯95ml ; 浓盐酸12ml ; ⏹ 25%NaOH 水溶液40ml(三)实验方法1、 微波反应器使用方法⏹ (1) 按电源键。
⏹ (2) 设温度:按住“模式”键至出现红色“C 02”字符(约2S ),可用增加“∨”或减少“∧”键来设定T 。
其中数字的倍率可通过“位移”键来改变,再按模式至“STOP”出现。
⏹ (3) 微波反应器顶部的孔中不得放入金属导线(包括水银温度计),以免微波泄露。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学综合实验Bα-苯乙胺的制备与拆分(α-phenyl ethylamine and resolution)一,实验目的1,掌握通过Leuckart反应,用苯乙酮和甲酸铵反应可制得外消旋α-苯乙胺的原理和方法。
2,学习碱性外消旋体的拆分原理和试实验方法。
3,巩固萃取、分馏、水蒸汽蒸馏、干燥等基本操作。
4,复习不同实验装置和仪器的安装及使用方法。
二,参考文献[1]复旦大学,兰州大学化学系有机化学教研室编,有机化学实验(第二版)[M],北京:高等教育出版社,1994。
[2]杨善中等,基础化学实验[M],北京:化学工业出版社,2009-02。
[3]张华,手性物α-苯乙胺的制备和分析研究[J],四川大学,应用化学,2004。
[4]吴海霞等,α-苯乙胺的微波合成研究[J],应用化工,2006(35)5 。
[5]吴华昌等, 脂肪酶拆分外消旋α-苯乙胺的研究进展[J],中国酿造,2010(5)。
[6]周霞, α-苯乙胺的合成及拆分[J], 广东化工, 2008 35(7)。
三,实验部分1,实验原理(1)苯乙胺中文名称:2-苯乙胺,2-苯基乙胺;分子式:C8H11N:C6H5CH2CH2NH2分子量:121.18;基本特性:熔点:-65℃沸点:194.5-195℃相对密度:0.9640。
溶解情况:溶于水,易溶于醇和醚。
性状、味道:苯乙胺为无色具的鱼腥味的强碱性液体特性:苯乙胺能吸收空气中的二氧化碳,成相应的碳酸盐。
用冷冻盐水冷却也不固化(熔点-65℃)。
苯乙胺盐酸盐为片状结晶。
熔点217℃(从醇中析出),易溶于水、溶于醇,但不溶于醚。
用途 苯乙胺为重要的医药和染料中间体,在医药上主要用于合成一下药物兴奋药、迷幻剂、神入感激发剂。
生理作用:人体会自动合成,释放苯乙胺,被科学家形象称为"爱情的化学分子",如果能在日常生活中适当从食物中摄取苯乙胺,爱情的保质期会变的更长久。
(2)α-苯乙胺的制备 醛或酮在高温下与甲酸胺反应得到伯胺的反应称为R.Leuchart 反应。
例如:C 6H 5CCH 3O HC O ONH 4185℃C 6H 5CHCH 3NH 2反应中氨首先与羰基发生亲和加成,接着脱水生成亚胺,亚胺随后被还原生成胺。
与还原胺化不同,这里不是用催化氢化,而是用甲酸作为还原剂。
反应过程如下:HC O ONH2H + NH 3C=O + NH 3C=NHNH 4+C=NH 2+C OC=NH 2+CO 2 + H C NH 2反应式:C 6H 5CCH 3O 2HCO 2NH 4C 6H 5CH NH CHOCH3NH CO 22H 2OC 6H 5CH CH 3NH CH OHClH 2OCH 3C 6H 5CHNH 3ClHCO 2HC 6H 5CHNH 3ClCH 3NaOHCH 3C 6H 5CHNH 2NaClH 2O(3)α-苯乙胺的拆分 实验采用(+)-酒石酸为拆解剂,它与外消旋α-苯乙胺形成非对称异构体的盐。
其反应如下:CH NH 2CH 3H OH H H OCO 2HCO 2HHNH 3CH 3CO 2HCO 2OH H H OH H 3NCH 3HH OH H H OCO 2CO 2H旋光的酒石酸在自然界颇为丰富,它是酿酒过程中的副产物。
由于(-)-胺·(+)-酸非对影体的盐比另一种非对映体的盐在甲醇中的溶解度小,容易从溶液中呈现晶体析出,经稀碱处理,使(-)-α-苯乙胺游离出来。
母液中含有(+)-胺·(+)-酸盐,原则上经提纯后可以得到另一个非对映体的盐,经稀碱处理后得到(+)-胺。
本实验只分离对映体之一,即左旋异构体。
2,实验装置图简单蒸馏微沸回流水层 有机层转入分液漏斗,加水15ml水层 上层水汽蒸馏空气蒸馏水浴蒸馏分液3,实验流程图(1) α-苯乙胺的合成蒸馏150-185℃馏出液 反应瓶内分层 继续加热,180-185℃,1.5h上层下层6ml氯仿萃取2次12ml盐酸,蒸出氯仿水层有机层回流0.5h,检验pH值冷却,6ml氯仿萃取3次上层有机层水层下层50%NaOH水蒸气蒸馏,测pH剩余物馏出物甲苯萃取3次上层有机层水层下层水层有机层干燥(NaOH)蒸馏剩余物产物(2)α-苯乙胺的拆分+甲醇+50%NaOH溶解(1)15ml乙醚萃取两次,无水硫酸钠干燥乙醚萃取(2)蒸馏时间实验步骤实验现象备注第一天8:30在100mL蒸馏瓶中加入11.8mL 苯乙酮,20g甲酸铵和几粒沸石8:35 安装反应器在蒸馏头上口装上插入瓶底的温度计,侧口连接冷凝管装配成蒸馏装置8:40 在石棉网上用小火缓缓加热至反应混合物温度升至150℃-155℃甲酸铵开始熔化并分为两项,8:45 继续加热变为均相8:50 反应剧烈,有白色的烟,放出气泡气泡中含有NH3,需要对气体进行吸收9:30 继续缓慢加热至温度达到185℃,停止加热(约需1.5h)冷凝管中出现白色颗粒为碳酸铵,为防止1,S-(-)-α-苯乙胺的分离四,结果与讨论1,产品与产率(1)产品α-苯乙胺为无色澄清液体。
产率=错误!未找到引用源。
(2)比旋光度的的测定产物(-)-α-苯乙胺为无色澄清液体。
m=错误!未找到引用源。
=0.9395x2.5=2.3487g错误!未找到引用源。
[错误!未找到引用源。
]=错误!未找到引用源。
e.e% 错误!未找到引用源。
92.02,实验过程的问题解释(1)采用鲁卡特反应合成(+)-α-苯乙胺为什么只能获得其外消旋体?欲获得(+)或(-)-α-苯乙胺,如何进行拆分?在鲁卡特反应中,甲酰胺先与羰基形成亚胺,然后起还原作用的甲酸根离子上的氢转移至亚胺,由于氢负离子可以从亚胺分子的任一侧导入,故还原的产物是外消旋体。
欲获得(+)或(-)-α-苯乙胺,可以用手性的酸,如酒石酸,与其成盐,从而使(±)-α-苯乙胺外消旋体由对映体转变为非对映体,根据两个非对映体溶解度的不同,将两者通过结晶的方式分开,然后通过酸碱中和反应将其转变成相应的(+)或(-)-α-苯乙胺,从而达到拆分的目的。
(2)本实验为什么要严格地控制反应温度?在反应过程中,若温度过高,可能导致部分碳酸铵凝结在冷凝管中,因此,温度不宜超过185℃。
(3)苯乙酮与甲酸铵反应后,用水洗涤的目的是什么?苯乙酮与甲酸铵反应后,用水洗涤的目的是去除反应体系中过量的甲酰胺。
(4)为什么要用溶剂对水解溶液进行萃取?因为水解溶液中含有部分α-苯乙胺,因此要将其从水相中萃取出来。
(5)本实验尚未对母液中所包含的(+)-α-苯乙胺-(+)-酒石酸盐进行处理,拟实验方案,从母液中提取出(+)-α-苯乙胺。
将母液浓缩,除去部分甲醇溶剂,冷至室温,静置过夜,有针状的(+)-α-苯乙胺-(+)-酒石酸盐晶体析出,过滤,将所得晶体溶于水中,用NaOH水溶液中和至强碱性,用乙醚萃取三次,合并萃取液,并用无水硫酸钠干燥,过滤,水浴蒸除乙醚,即得(+)-α-苯乙胺.(6)简述外消旋体的化学拆分原理及相应的拆分试剂。
外消旋体的化学拆分原理是首先将对映体转变成非对映体,然后利用非对映体之间其他物理性质的差异,使用一般方法将其分离,再将所得非对映体转变为原来的旋光化合物,从而达到拆分的目的。
拆分酸性外消旋体,常用旋光性生物碱,如(-)-麻黄碱,(-)-马钱子碱等:拆分碱性外消旋体,常用旋光性酸,如酒石酸,樟脑-β-磺酸等:如果被拆分对象不带酸或碱性基团,例如外消旋醇,则可先引入酸性基团,然后按拆分酸性外消旋体的方法拆分。
3,Luckart反应优缺点及评价醛或酮与氨反应形成错误!未找到引用源。
-氨基醇,错误!未找到引用源。
-氨基醇继而脱水成亚胺,亚胺经催化加氢转变为胺,这是有羧基化合物合成胺的一种重要方法:如果用甲酸作还原剂来代替H2/Ni,那么这个还原氨化过程就被称作鲁卡特反应。
在鲁卡特反应条件下,甲酸或甲酸根离子(HCOO-)起还原作用,氢原子以强还原性氢负离子(H-)的形式转移至亚胺;如果参加反应的羧基分子具有前手性面,在鲁卡反应中,由于氢负离子可以从亚胺分子的任一侧导入,故得到的还原产物是外旋体。
如果要想获得有旋光性的对映异构体,还需进行拆分。
应该指出,上述反应中并没有直接形成游离的胺,而是先生成其N-甲酰化物,后者须经酸解及碱中和后才能获得胺。
在鲁卡特反应,以醛酮作原料分别与氨、伯胺或仲胺反应可以得到相应的伯、仲、叔胺。
鲁卡特反应通用性较强,可以处理多数脂肪酮、脂环酮、脂肪-芳香酮、杂环酮等,尤其是芳香酮及高沸点芳香酮更为适用。
但是,有时Luckart反应时间较长,建议考虑使用适当的添加剂以减少反应时间。
五,展望由于光学对映体在生物活性、毒性及代谢机理上都有所不同,因此单一对映体的制备极为重要。
而手性物α-苯乙胺就是制备单一对映体的重要中间体之一,它既可作外消旋体的手性拆分试剂,又可作不对称合成的手性原料,所以它的制备和分析具有重要意义错误!未找到引用源。
采用微波辐射法合成α-苯乙胺,较常规加热合成相比,使反应物摩尔比更接近理论比(甲酸铵与苯乙酮摩尔比从3.8:1降至2.6:1),降低了反应物用量,缩短了反应时间(从3 h降至2 h),降低了反应温度(从185℃降至165℃),产率可达44.50%~46.93%错误!未找到引用源。
而利用脂肪酶拆分外消旋α-苯乙胺是目前生产光学纯α-苯乙胺的重要方法之一,可以从脂肪酶拆分机理、脂肪酶的选择、酰化剂的选择及反应体系溶剂的确定等方面来提高产率错误!未找到引用源。
当外消旋α-苯乙胺由苯乙酮,苯甲腈,苯甲胺合成,光学活性α-苯乙胺由肟醚苯甲醛苯乙酮苯甲腈的不对称合成,以及由拆分方法制备光学活性α-苯乙胺,如用手性酰化试剂选择性与苯乙胺形成酰胺的动力学拆分,通过选择性生成结晶盐拆分。
用组合方法拆分α-苯乙胺并加入不同添加剂得出不同的结果。
所以寻找合适的添加剂是有效拆分的一条有希望的途径.错误!未找到引用源。
