固体比热容的测量
固体物理-固体比热容

离子比热容
离子比热容是由于固体中离子的振动和移动而引起的热容。它是离子质量 和离子间相互作用力的函数,与温度密切相关。
离子比热容的大小取决于离子的振动频率和扩散系数,不同的离子化合物 具有不同的离子比热容。
在低温下,离子比热容通常表现为线性温度依赖性,而在高温下则表现出 更复杂的非线性行为。
磁性比热容
环境污染物治理
在环境污染物治理中,某些具有特定 比热容的吸附剂可以用于吸附和去除 环境中的有害物质,如重金属离子和 有机污染物等。
05
固体比热容的研究前景
新材料的比热容研究
新材料比热容研究
随着科技的发展,新型材料不断涌现,研究 这些材料的比热容对于理解其热学性质和潜 在应用具有重要意义。例如,新型高温超导 材料、纳米材料和二维材料的比热容研究, 有助于发现新的物理现象和潜在应用。
要点二
高温高压下的比热容测量技术
高温高压下的比热容测量需要高精度的实验技术和设备。 例如,激光加热技术、闪光量热计和高压装置的结合使用 ,可以在极端条件下对材料的比热容进行测量。
比热容与微观结构的关系研究
比热容与微观结构的关系
固体材料的比热容与其微观结构密切相关。通过对比热 容的研究,可以深入了解材料的微观结构和动力学性质 。
02
固体比热容的分类
晶格振动比热容
晶格振动比热容是由于固体晶格结构的振动而引起的热容。它是固体中原子或分子的振动幅度和频率 的函数,与温度密切相关。
晶格振动比热容的大小取决于晶体的对称性和周期性,不同的晶体结构具有不同的晶格振动比热容。
高温下则表现为更复杂的非线性行为。
比热容随物质种类的变化
总结词
不同物质具有不同的比热容
VS
实验五 固体比热容的测量(电热法)

实验五 固体比热容的测量(电热法)金属是重要的固态物质,本文对固体物质比热容的测量重点介绍了金属比热容的测量,金属比热容是金属物质的重要特性,本文重点介绍电热法测量固体比热容。
【实验目的】1、掌握基本的量热方法——用量热器测热量法。
2、学习用电热法测固体的比热容。
【实验仪器】热学综合实验平台、量热器、待测钢球、测温探头【实验原理】固体比热容指单位质量的热容量,也是特定粒子电子、原子、分子等结构及其运动特性的宏观表现。
测量固体物质比热容对于了解固体物质性质,物质内部结构等都具有重要的意义,常用于测量固体物质比热容的方法有动态法、混合法、冷却法等。
金属是重要的固态物质,本书对固体物质比热容的测量重点介绍了金属比热容的测量,金属比热容是金属物质的重要特性,本实验重点介绍电热法测量固体比热容。
在量热器中加入质量为m 的待测物,并加入质量为0m 的水,如果加在加热器两端的电压为U ,通过电阻的电流为I ,通电时间为t ,则电流作功为:UIt A = (5-1)如果这些功全部转化为热能,使量热器系统的温度从1T ℃升高至2T ℃,则下式成立()()1201100T T c c m c m mc UIt -+++=ω (5-2)c 为待测物的比热容,0c 为水的比热热容,1m 为量热器内筒的质量,1c 为量热器内筒的比热容, 2m 为铜电极和铜搅拌器总质量,2c 为铜比热容。
由(5-2)式得()[]m c c m c m T T UIt c //0110012ω----= (5-3)为了尽可能使系统与外界交换的热量达到最小,在实验的操作过程中就应注意以下几点:1、不应当直接用手去把握量热筒的任何部分,不应当在阳光直接照射下进行实验。
实验四 固体比热容的测量

实验四固体比热容的测量【实验目的】1.用混合法测定金属的比热容。
2.掌握基本的量热方法——混合法。
【实验仪器】量热器、温度计(0 ~ 50 ºC两支、0 ~ 100 °C一支)、物理天平、待测金属块、加热器或电炉、冰、停表等。
量热器:又称卡计,是测量热量的仪器。
简单的量热器如图所示,m1为内筒,筒内贮有一定量的纯水m0 ,T为温度计,m2 为搅拌器,为了将由内筒及其盛的物质构成的热学系统看成为孤立系统,故将内筒置于外筒C并由绝热架I2 支撑,上面盖上绝热盖I1 ,同时,将内外筒的表面电镀或打磨得十分光亮以减少由于辐射而产生得热传递。
【实验原理】温度不同得物体混合后,热量将由高温物体传递给低温物体。
如果在混合过程中和外界没有热交换,最后将达到均匀稳定的平衡温度,在这过程中,高温物体放出的热量等于低温物体所吸收的热量,此称为热平衡原理。
本实验即根据热平衡原理用混合法测定固体的比热。
将质量为m、温度为T1 的金属块投入量热器的水中。
设金属块、水、量热器内筒、搅拌器和浸入水中的温度计的比热分别为c、c0、c1、c2 和c3 ,质量分别为m、m0、m1、m2和m3 ,待测物投入水中之前的水温为T2 。
在待测物投入水中以后,其混合温度为θ,则在不计量热器与外界的热交换的情况下,将存在下列关系:mc (T1 −θ ) = ( m0c0 + m1c1 + m2c2 + m3c3 ) ( θ−T2 )即:)-()-)(+++(=112 332211θTmTθcmcmcmcmc式中,温度计插入水中的部分的热容量为m3c3 = 1.9{V}cm³,V为温度计插入水中部分的体积,{V}cm³表示V 以cm3为单位的数值,具体算法参照书后附。
上述讨论是在假定量热器与外界没有热交换时的结论。
实际上,只要有温度差异就必然会有热交换存在,因此,必须防止或进行修正热散失的影响。
热散失的途径主要有三:第一是加热后的物体在投入量热器水中之前散失的热量,这部分热量不易修正,应尽量缩短投放时间。
固体比热容的测定及误差分析

固体比热容的测定及误差分析郭超200802050234 08物理(2)班摘要:比热容是物质的一个重要物理特性,比热容的测量是热学中的一个基本测量,在新能源的开发和新材料的研制中,物质的比热容的测量往往是不可缺少的,但由于散热因素多而且不容易控制和测量,使量热实验的准确度往往较低,因此,设法改进实验方法,提高使用精确度便成为人们关注的问题,本实验用混合法测出来金属块的比热容,并进行了散热修正是误差减小到了最低。
关键词:固体、比热容、误差分析Abstract: The specific heat capacity is an important material and physical properties, specific heat capacity of thermal measurement is a basic measurement, development of new energy and new material, the material specific heat capacity measurements are indispensable, but the heat factor more and not easy to control and measurement, so that calorimetry experiments are often less accurate, therefore, seek to improve the experimental methods, increase the accuracy of people have become issues of concern, the experiment measured by the piece of metal mixed with the specific heat capacity, and amendment to the heat reduced to a minimum error.Key words: solid, specific heat capacity, error analysis一、实验原理:1.1实验原理的引入:测量固体的比热容的方法与有很多种,例如混合法、比较法、冷却法等,但是这些方法在实际操作中都会引入较大的误差。
固体比热容

c0
4.取出量热器的内筒,称其总质量并减去 m+ m ,即为 1 水的质量 m ; 0 5.小量筒测出温度计浸入水中的体积V;另换温水,重 复上述实验一次。 6.实验时应注意 (1)本实验的误差主要来自温度的测量,因此在测量温 度时要特别注意,读数迅速且要准确(准确到0.1℃); (2)倒入量热器中的温水不要太少,必须使投入的金属 块悬挂浸没在其中。 水的比热容 c0 为 4.187×103 J ⋅ kg−1⋅oC−1
实验结果分析和处理
1.将实验中测出的各个数值填入下表:
前8分钟 t(℃) 次 1 2 3 4 t 次 (℃) 5 6 7 8 次 1 2 3 4 中间2分钟 t(℃) 次 5 6 7 8 t(℃) 次 1 2 3 4 后8分钟 t(℃) 次 5 6 7 8 t(℃)
t2(℃) m 0(kg) m (kg) m1(kg) C(J·k—1·℃—1)
在上述混合过程中,实际上系统总要与外界交换热量, 这就破坏了(1)式的成立条件。为消除影响,需要采用散 热修正。本实验中热量散失的途径主要有三个方面。第一, 若用先加热金属块投入量热器的混合法,则投入前有热量损 失,且这部分热量不易修正,只能用尽量缩短投放时间来解 决;第二,将室温的金属块投入盛有热水的量热器中,混合 过程中量热器向外界散失热量,由此造成混合前水的温度与 混合后水的温度不易测准。为此,绘制水的温~时曲线,
实验仪器
电子温度计;量热器;天平
实验步骤
测环境温度 测内桶和搅拌器质量 加水,测总质量 备冰 投冰,搅拌,测温 测至系统温度有上升为止 测内桶及水总质量 测环境温度 绘制温度时间曲线,求冰的溶解热
注意事项
投冰前应将其拭干,且不得直接用手触摸;其质量 不能直接放在天平盘上称衡,而应由投冰前、后量 热器连同水的质量差求得。 为使温度计示值确实代表系统的真实温度,整个实 验过程中(包括读取前)要不断轻轻地进行搅拌 (搅拌的方式应因搅拌器的形状而异)。
比热容是如何测量的?

比热容是如何测量的?比热容是热学中一个重要的物理量,它用来描述物体在吸热或放热过程中的热量变化情况。
本文将介绍比热容的定义以及几种常用的测量方法。
一、比热容的定义比热容是指单位质量物质在单位温度变化下吸收或释放的热量。
它的计量单位是焦耳每千克每开尔文(J/kg·K)。
比热容可以用来表征物质的热惯性,即物体吸收或放出热量所需的温度变化。
二、恒压热容法恒压热容法是一种常用的测量比热容的方法。
在恒定的压力条件下,通过测量物质在不同温度下的热量变化,可以计算出比热容。
具体的实验步骤如下:1. 将待测物质置于一个恒温容器中,比如热水浴或恒温槽。
2. 在容器中加入一定量的热量,使物质温度升高。
3. 同时记录物质温度与所输入的热量变化值。
4. 通过计算物质的比热容,可以得出比热容的数值。
恒压热容法适用于固体、液体和气体等不同状态的物质,具有广泛的应用。
三、差热法差热法也是一种常用的测量比热容的方法。
它通过测量物质与热源之间的温度差异,计算比热容。
实验步骤如下:1. 将物质与热源接触,在一段时间内加热或冷却物质。
2. 同时记录物质温度的变化以及与热源接触的时间。
3. 利用热流量和温度差的关系,计算出物质的比热容。
差热法对于固体和液体热容的测量更为常见,它的优点是不需要特殊的设备,适用于简单实验。
四、绝热量热容法绝热量热容法是一种精确测量比热容的方法。
它通过控制物体与外界的热量交换,在绝热条件下测量比热容。
实验步骤如下:1. 将待测物质置于一个绝热容器中,确保与外界几乎没有热量交换。
2. 在一定时间范围内记录物质温度的变化。
3. 通过计算物质热量变化和温度变化的关系,得到比热容的数值。
绝热量热容法的优点是可以减少外界的热量干扰,提高测量的精确性。
但它需要精密的仪器和较长的实验时间。
综上所述,比热容可以通过恒压热容法、差热法和绝热量热容法进行测量。
每种方法都有其适用的范围和优缺点。
科学家们通过不断改进和创新,使比热容的测量方法更加准确和方便,为热学研究提供了重要的工具。
固体比热测定

固体比热容的测定指导老师:王亚辉小组成员:李彦辉张燚杨朋波胡宏明电热法测固体比热容实验的改进1引言在传统的混合法测固体比热容实验中, 量热器等的吸热和散热一直是制约实验结果准确度的一个关键因素. 为了消除此类热量传递对测量结果的影响, 在一定的实验条件下, 可以近似地用作图法消除热交换的影响, 其次还要考虑量热器、搅拌器等的等效比热容和质量, 处理过程相当麻烦. 本实验采用电热法, 通过控制放试件和不放试件两种情况下的初末温度和液面高度, 将上述种种热散失抵消掉, 使测量较准确, 操作较简单. 另外, 本实验采用传感器加模拟电路来测量温度, 使温度的测量更准确; 用不锈钢杜瓦瓶代替传统的量热器筒和保温套筒,减少了向外界的热量散失, 且使用方便2实验改进方法实验装置如图1所示. 待测样品及水放在杜瓦瓶中, 并设置了AD590温度传感器和电加热器、搅拌器. 水面高度为杜瓦瓶的3/ 5左右;样品不宜太大或太小; AD590和样品大致位于水深的中部; 电加热器置于偏下部.设加热电压为U, 电流为I, 则电加热器在时间T内放出的热量为UIS. 此热量使量热器的整体温度由t1 升至t2. 根据能量守恒定律, 可得如下方程UIT= (mc+ m0c0+ C1 + C2 + C3) (t2 - t1) + ΔQ ( 1)式中, m, c为待测物的质量和比热容; m0, c0 为水的质量和比热容; C1, C2, C3 分别为在此实验状况下量热器( 包括搅拌器) 、电加热器、温度传感器的等效热容量; ΔQ为其它因素散失的热量.本实验测量的困难在于C1, C2, C3 及ΔQ均为未知的参量. 为解决这一问题, 采用同等实验条件下的系统误差差值消去法.实验分两步进行: 第一步不加待测试件, 加热T1时间后, 系统从t1 升温至t2; 第二步放入t1温度的水和试件, 且要求水位和第一步等高, 加热T2 时间后, 同样使温度升高到t2. 据( 1) 式有UIT1 = (m01c0+ C1+ C2 + C3)(t2 - t1) + Δ Q1 ( 2)UIT2= (m02c0 + C1+ C2+ C3+ mc)(t2- t1) + ΔQ2( 3)( 2) 式减去( 3) 式得UI ( T1 - T2) =- mc( t2- t1) + ( m01 - m02) c0( t2 - t1) +ΔQ1 -ΔQ2故\( m01- m02) c0( t 2- t 1) - UI( T1- T2) +Q1 -Q2∆∆( 4) c=m( t2- t1)考虑到在前后两步测量中, 初末温度相同,水的高度相同, 环境条件也相同, 因此量热器热量交换情况基本相同, 其差别仅在于电加热的时间T1 与T2 略有差别, 造成ΔQ1 与ΔQ2 略有不同. 由于用了高真空杜瓦瓶作为量热器, ΔQ1与ΔQ2 均很小, 而其差值将更小. 测试结果也表明平衡后系统的温度随时间的变化极缓慢, 如图2所示. 因此, 可以忽略该项差别, 认为ΔQ1- ΔQ2= 0, 则( 4) 式化得为( m01- m02) c0( t 2- t 1) - UI( T1- T2)c=m( t2- t1)本实验应该注意的几个问题:1) 本实验的关键之一在于两步实验初末温度的控制, 最好相同, 稍有差别也是可以的, 但一定要保证t2-t1 相同.2) 加热过程中要充分地、不断地搅拌, 否则传感器即数字毫伏表反映的温度与实际平衡温度会有差别.3) 计时器的开关要迅速及时, 必要时可两人配合. 关闭加热器和计时器后应继续搅拌片刻, t2 应取最大读数值.4) 要选择恰当的电加热功率. 功率太大, 会使计时器的控制难度加大, 且增加量热器内温度的不均匀性; 太小会使实验时间延长, 增大散热引起的误差.数据记录:烧杯:m1=66.3 筒:m2=66.6 筒+水:m3=212.1g筒+水+珠:m4=298.7g 烧杯+铜珠:m5=166.4g只加水: U=11.99v I=1.026A稍加热停止时末温T0 T1 T221.2℃21.8℃22.2℃继续加热停止时末温时间T3 T4 T132℃32.4℃599.1s水+珠:稍加热停止时 末温 '0T '1T '2T21.0℃ 21.7℃ 22.2℃继续加热停止时 末温 时间'3T '4T '5T31.8℃ 32.4℃ 590.1s数据处理:m=m5-m1=100.1g m10=m3-m2=145.5gm20=m4-m-m2=132gC 测珠=m m m 2010-*Co 水-)24()21(T T m t t VI -- =1.1001325.145-×4.2×103J/g ℃-)2.224.32(**1.100)1.5901.599(_*026.1*99.11103---J/(g ℃) =566.4 J/g ℃-108.4 J/g ℃=458 J/g ℃误差分析:因为数字毫伏表容许误差为0.1℃,电压表,电流表准确度分别为0.1V,0.01A,启停数字计数器的误差之和为0.4s,天枰的感量为0.02g.u( t1) = u( t2) = 0. 1/ 3 = 0. 06℃u( U) = 0. 1/ 3 = 0. 06Vu( I) = 0. 01/ 3 = 0. 006Au( Ʈ1) = u(Ʈ 2) = 0. 4/ 3 = 0. 23su( m01) = u( m02) = u( m) =0. 02/ 3= 0. 016g则故u( c) = u2( c1) + u2( c2) = 5J/ ( g *℃)取公认值480J/(g*℃)测量值与真实值之差与标准值取百分比 η=480458480 *100%=4.6% 在允许百分误差(5%)以内,故该实验测量比热容是可行的。
4 固体比热容的测量
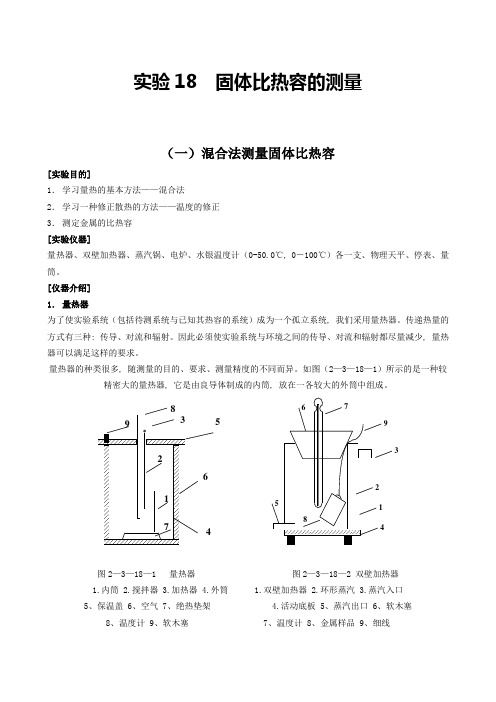
实验18 固体比热容的测量(一)混合法测量固体比热容[实验目的]1.学习量热的基本方法——混合法2.学习一种修正散热的方法——温度的修正3.测定金属的比热容[实验仪器]量热器、双壁加热器、蒸汽锅、电炉、水银温度计(0-50.0℃, 0-100℃)各一支、物理天平、停表、量筒。
[仪器介绍]1.量热器为了使实验系统(包括待测系统与已知其热容的系统)成为一个孤立系统, 我们采用量热器。
传递热量的方式有三种: 传导、对流和辐射。
因此必须使实验系统与环境之间的传导、对流和辐射都尽量减少, 量热2.外筒是双层结构, 空气封闭其中, 因为空气是热的不良导体, 故可避免空气传导而引起热量的损失;外筒上端的木盖可严密地盖着, 避免空气对对流所引起的热量损失;外筒的内壁和内筒的外壁均电镀得十分光亮, 可减少热辐射, 外筒的底部放上一个隔外筒的外表再包一层绒布, 这样就能使整个系统尽可能根据上述测量的T-t数据, 以T为纵坐标, 以t为横坐标, 即得如图(2—3—18—4)的T-t曲线。
A点对应的时刻就是测水温开始的时间 , B点对应的时刻就是, 而不是5分钟末的时间。
然后作图即得混合前后冷水的初温和末温T。
把各个物理量的测量值代入式(2-3-18-1)即可算出金属样品的比热容。
图(2—3—18—4)中的G点所对应的温度应为室温所在的位置, 这样才不影响温度的修正。
[实验内容和要求]1. 混合法测定铜块的比热容2.混合过程中散热的温度修正法3.混合前量热器(含水)系统温度低于室温(加冰块), 测量系统随时间吸热变化的温度。
4. 混合过程快速测量变化的温度5. 数据处理:Cx与标准值求百分误差[注意事项]1. 作温度值修正法曲线图, FE垂直于t轴, 满足S1=S2, 图中G点对应的温度接近室温为佳。
2. 从曲线图中定出初温T2和末温T。
[实验思考]请分析本实验主要的误差来源。
(二)冷却法测量金属的比热容[实验目的]学习冷却法测量金属比热容的方法[实验仪器]FB312型冷却法金属比热容测量仪[实验原理]根据牛顿冷却定律, 用冷却法测定金属的比热容是量热学常用方法之一。
固体比热容的测量

实验简介19世纪,随着工业文明的建立与发展,特别是蒸汽机的诞生,量热学有了巨大的进展。
经过多年的实验研究,人们精确地测定了热功当量,逐步认识到不同性质的能量(如热能、机械能、电能、化学能等)之间的转化和守恒这一自然界物质运动的最根本的定律,成为19世纪人类最伟大的科学进展之一。
从今天的观点看,量热学是建立在“热量”或“热质”的基础上的,不符合分子动理论的观点,缺乏科学内含。
但这无损量热学的历史贡献。
至今,量热学在物理学、化学、航空航天、机械制造以及各种热能工程、制冷工程中都有广泛的应用。
比热容是单位质量的物质升高(或降低)单位温度所吸收(或放出)的热量。
比热容的测定对研究物质的宏观物理现象和微观结构之间的关系有重要意义。
本实验采用混合法测固体(锌粒)的比热容。
在热学实验中,系统与外界的热交换是难免的。
因此要努力创造一个热力学孤立体系,同时对实验过程中的其他吸热、散热做出校正,尽量使二者相抵消,以提高实验精度。
实验原理混合法测比热容设一个热力学孤立体系中有种物质,其质量分别为,比热容为()。
开始时体系处于平衡态,温度为,与外界发生热量交换后又达到新的平衡态,温度为,若无化学反应或相变发生,则该体系获得(或放出)的热量为假设量热器和搅拌器的质量为,比热容为,开始时量热器与其内质量为的水具有共同温度,把质量为的待测物加热到后放入量热器内,最后这一系统达到热平衡,终温为。
如果忽略实验过程中对外界的散热或吸热,则有式中为水的比热容。
代表温度计的热容量,其中是温度计浸入到水中的体积。
⏹系统误差的修正在量热学实验中,由于无法避免系统与外界的热交换,实验结果总是存在系统误差,有时甚至很大,以至无法得到正确结果。
所以,校正系统误差是量热学实验中很突出的问题。
为此可采取如下措施:●要尽量减少与外界的热量交换,使系统近似孤立体系。
此外,量热器不要放在电炉旁和太阳光下,实验也不要在空气流通太快的地方进行。
●采取补偿措施,就是在被测物体放入量热器之前,先使量热器与水的初始温度低于室温,但避免在两热器外生成凝结水滴。
电热法测固体比热容

将以上数据代人 ( — ) 中得 := 6 . /k . 。注意本 实验必 15式 c 398 ( g J ℃) 须保持同等条件 的系统误差消去法。本实验 中温度精确到 O 1 时 . ℃, O 间T 精确到 1 , s质量 m可精确到 O 1 , . g 精确度高。黄铜 的固体 比热容 0 为 302/k. . 7 . ( gC)用电热法所测量 的实验误差为 00 4 J o .5 % 传统 的固液混合法日 用修正法找初末温度精确度大于 01 . . C 时间  ̄ 精确 到 l , s质量可精 确到 0 l, . g 测得 的 C 3 0 (g . 固液混 O =6. J k. 用 8 / ℃) 合法的实验误差 为 27 . %
图 2 电热法实验数据图
表 1 电热 法 实 验 数 据 表
t 度 , l 度
5 . 00
T/ 秒
72 7
T √秒
72 9
ng d
1 55 3.
m 以
1o 6o
U, R
5l
图 1 电热法测 固体 比热容实验装 置图
3 .0 00
设稳压电源电压为 u 电加热器的电阻为 R, , 水温从温度 t 。 升至 t
混合法测比热容实验报告

混合法测比热容实验报告混合法测比热容实验报告实验目的:掌握用混合法测定固体比热容的方法。
实验原理:物质的比热容是指在温度保持不变时,单位质量物质的吸收或放出的热量与质量之比值,这种性质叫做比热容。
所以,可利用此原理来测量某些固态物质的比热容。
本次实验主要是探索如何用混合法测量硅酸盐晶体(如食盐)和非金属矿物(如石膏、石英等)的比热容,为学习使用化学分离和提纯技术打下基础。
一、原理用混合法测量物质的比热容,就是把已知的固态或液态物质置于适当的容器中,充满其他未知物质,然后根据各组成部分加热前后质量差计算该固体的比热容。
若选择不当,会导致测得的结果偏高或偏低。
如欲求木炭的比热容,则应先称量木炭的质量m1,再将其完全烧成灰,并将质量 m2 转化为碳元素的质量,而不能简单地看成化学反应前后物质总质量减少了 M1,从而由公式:二、仪器水槽:底面直径10厘米,长25厘米,内盛经过充分预热后的空气和酒精灯。
另备有小刀、镊子、橡皮塞、玻璃棒、直尺和滴管。
三、操作步骤1.将大小相同的石蜡块放入水中浸泡数秒钟,目的是让石蜡吸足水分。
2.将固体石蜡块取出,在上面铺一张白纸,再向白纸上撒些食盐粉末,注意撒盐均匀。
3.用手扶住小刀,沿着刻线划切割开石蜡。
4.用玻璃棒轻敲并加热石蜡。
5.冷却后将溶液倒人事先准备好的水槽里,并用玻璃棒搅拌均匀,如有凝结可用玻璃棒稍微搅拌一下。
6.取下白纸和玻璃棒,往水中逐渐加入乙醇,观察比重变化情况,再逐渐增大体积,以达到石蜡完全溶解为止。
7.将上述试样转移至容量瓶中,用水洗涤容器,用干燥滤纸进行过滤。
8.待冷却后,用干燥滤纸将容量瓶中残留的乙醇过滤掉。
9.用分析天平测量它们的质量,记录下来。
10.待试样完全溶解后,用小刀沿着刻痕切割,并仔细除去碎屑,再按照石蜡切割方法切割。
11.将各种规格的硅酸盐晶体分别装入容量瓶中,用水洗涤容量瓶两次,用分析天平测量其质量,记录下来。
12.根据比热容表查出自己所需要晶体的比热容值,算出它的摩尔质量 M1,并换算成克每立方厘米的质量。
固体比热容

冷却过程。通过 O 点作与时间轴垂直的一条直线交 AB、CD 的延长线于������和������,使面积 BEO 与面积 CFO 相等。这样,������和������点对应的温度就是热交换进行无限快的温度,分别为水的初 温������1和系统的终温������。
式中的比热容。
热学理论认为,温度不同的两个或几个物体相互热体传递给低温物体。如果热交换过程中系统没有向外界环境散失热量也没有自外界环
境吸收热量,那么系统最终达到均匀稳定的平衡温度时,高温物体放出的热量等于低温物体
吸收的热量,这就是热平衡原理:
Q放 Q 吸
(2)
1.选取水的初温
实验中,量热器总是会与外界存在热交换,为了减小实验误差,需合理选择水的初温������1。 操作中要使初温������1在投放待测固体之前低于环境温度������0(即室温),温度差为(������0 − ������1);而混
合后的热平衡温度������高于环境温度������0,温度差为 t t0 ,并且尽量使(������0 − ������1) = (������ − ������0)。这
§4.6 用混合法测定固体的比热容
比热容是热学中一个重要的物理量,物质比热容的测量是物理学的基本测量之一,对于 了解物质的结构、确定物质的相变、鉴定物质的纯度以及新能源的开发和新材料的研制等方 面,都起着重要作用。
根据热平衡原理用混合法测定固体或液体的比热容,是量热学中一种常用方法,所使用 的基本仪器为量热器。本实验测定铝块的比热容,在实验过程中,采用冷热补偿法和图线外 推法补偿量热系统与外界的热交换,是量热学中减小系统误差的常用方法。
比热容测定实验

比热容测定实验比热容测定实验是一种重要的物理实验,它可以帮助我们了解物质的热性质。
在本文中,我们将详细讨论比热容的定义和定律,并解释比热容测定实验的具体步骤和实验室准备工作。
此外,我们还会探讨该实验的应用和其他专业性角度。
首先,让我们来了解一下比热容是什么。
比热容是指物质在单位质量下吸收或释放的热量与其温度变化之间的关系。
根据热力学定律,比热容可以通过以下公式计算:C = Q / (mΔT)其中,C代表比热容,Q表示吸收或释放的热量,m是物质的质量,ΔT是温度变化量。
测量比热容的实验通常涉及加热和冷却物体,并测量其温度变化。
下面是步骤的详细解释:1. 实验准备:- 确定实验所需的材料和仪器。
通常情况下,我们会选择一个绝热杯,温度计,加热器和计时器等工具。
- 挑选适当的材料作为实验样品。
根据实验目的和需求,可以选择固体、液体或气体样品。
2. 温度测量:- 在实验开始之前,确保温度计已经校准并且准备好使用。
- 将温度计插入样品中,并记录开始时的温度。
3. 加热过程:- 将样品放入绝热杯中,并使用加热器逐渐加热样品。
- 使用计时器定时,同时记录样品的温度随时间的变化。
- 当样品达到所需的温度时停止加热。
4. 冷却过程:- 停止加热后,立即开始记录样品的温度随时间的变化。
- 使用计时器定时,直到样品的温度达到室温。
完成实验后,我们可以利用实验数据计算比热容。
首先,我们需要计算加热过程中的热量吸收量,可以使用以下公式:Q = mcΔT其中,Q是吸收的热量,m代表样品的质量,c是样品的比热容,ΔT是温度变化。
对于冷却过程,我们可以使用相同的公式计算释放的热量。
通过将热量吸收和释放的数据代入比热容的定义公式,我们可以得到比热容的数值。
比热容测定实验在许多实际应用中都具有重要意义。
比热容的值可以提供有关物质内部结构和相互作用的信息。
它在工程领域中用于设计和优化热交换装置,以便有效利用热量和能源。
此外,比热容也被广泛用于食品科学、材料科学和环境科学等领域的研究。
热容与比热容的测量实验

热容与比热容的测量实验热容(C)和比热容(c)是描述物体对热量变化的性质的物理量,它们在热力学和热传导等领域有着重要的应用。
本文将探讨热容和比热容的测量实验,包括实验准备、实验过程以及实验的应用和其他专业性角度。
一、实验准备在进行热容和比热容的测量实验之前,我们需要准备一些实验装置和材料。
常用的实验装置包括加热器、热源、测温仪器、容器和热绝缘材料等。
实验材料通常是固体样品,例如金属块或液体,其重要性在于其质量和特性对于热容和比热容的测量结果具有重要影响。
实验准备的第一步是确定实验中使用的试样材料。
要进行比热容的测量,样品应该是纯净的且质量稳定。
其次,我们需要测量样品的初始温度T1和最终温度T2,这些数据可以用于计算热容和比热容。
同时,需要准备一台高精度的温度计来测量温度变化。
二、实验过程在进行热容和比热容的测量实验时,首先需要将试样放置在加热器内。
加热器可以通过通电来提供热源。
然后,我们需要将温度计定位在试样附近,以测量试样的温度变化。
在实验过程中,我们需要记录试样的初始温度T1和最终温度T2,并通过测量时间t来计算实验时的温度变化率(dT/dt)。
利用这些数据,我们可以计算出试样的热容C以及比热容c。
三、实验应用及其他专业性角度热容和比热容的测量实验在许多领域都有着重要的应用。
以下是一些实验应用和其他专业性角度的讨论:1. 材料科学:热容和比热容的测量实验可以用于评估不同材料的热性质。
这对于材料选择和设计具有重要意义,例如在制冷剂和隔热材料的研发中。
2. 热学研究:热容和比热容的测量实验可帮助研究人员深入了解热力学特性和状态方程。
通过这些实验,可以研究物质在不同温度和压力下的热行为,从而为研究热力学过程提供重要的数据和参数。
3. 能源技术:热容和比热容的测量实验对于能源技术的研发也具有重要意义。
例如,在燃料电池和太阳能电池等能源转换系统中,热容和比热容的测量实验可用于评估系统的性能和效率。
4. 环境科学:热容和比热容的测量实验在环境科学中也有广泛应用。
比热容测试国标

比热容测试国标中国国家标准GB/T 3398.1-2009《材料比热容、比热容增量、熔融热和汽化热的测定第1部分:热盘法》规定了采用热盘法测定材料比热容、比热容增量、熔融热和汽化热的方法。
该标准适用于固体材料、液体材料和气体材料的比热容、比热容增量、熔融热和汽化热的测定。
该标准规定了热盘法的原理、仪器设备、样品制备、实验条件、数据处理和误差分析等内容,并提供了相应的实验步骤和操作规范。
在该标准中,热盘法被认为是一种快速、准确、可靠的方法,适用于各种材料的比热容测试。
此外,中国还有其他一些关于材料比热容测试的国家标准,如GB/T 15062-2009《材料比热容、比热容增量、熔融热和汽化热的测定第2部分:热箱法》、GB/T 21834-2009《材料比热容、比热容增量、熔融热和汽化热的测定第3部分:热电偶法》等。
这些标准也都提供了相应的实验方法和规范,以便进行准确的材料比热容测试。
1. GB/T 3398.1-2009《材料比热容、比热容增量、熔融热和汽化热的测定第1部分:热盘法》该标准规定了采用热盘法测定材料比热容、比热容增量、熔融热和汽化热的方法。
热盘法是一种常用的测定材料比热容的方法,适用于固体材料、液体材料和气体材料的比热容测试。
该标准适用于各种材料的比热容测试,包括金属、陶瓷、聚合物、复合材料等。
该标准规定了实验的基本原理、仪器设备、样品制备、实验条件、数据处理和误差分析等内容,并提供了相应的实验步骤和操作规范。
其中,实验条件包括温度稳定性、热盘和样品之间的热传递、测量精度等方面的要求。
数据处理和误差分析方面,该标准提出了多种数据处理方法和误差修正方案,以便得到更加准确的比热容测试结果。
2. GB/T 15062-2009《材料比热容、比热容增量、熔融热和汽化热的测定第2部分:热箱法》该标准规定了采用热箱法测定材料比热容、比热容增量、熔融热和汽化热的方法。
热箱法是一种常用的测定材料比热容的方法,适用于固体材料和液体材料的比热容测试。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
固体比热容的测量
一、 实验目的
1、 掌握基本的量热方法——混合法;
2、 测定金属的比热容;
3、 学习一种修正散热的方法。
二、 实验仪器
量热器、温度计(0、00-50、00 0C 与0、0-100、0 0C 各一支)、物理天平、待测金属粒、冰、停表、加热器、量筒等。
三、 实验原理
1、 混合法测比热容
依据热平衡原理,温度不同的物体混合后,热量将由高温物体传给低温物体,如果在混合过程中与外界无热量交换,最后达到均匀稳定的平衡温度。
根据能量守恒定律,高温物体放出的热量就应等于低温物体吸收的热量,即:
本实验即根据热平衡原理用混合法测定固体的比热。
设量热器(包括搅拌器与温度计插入水中部分)的热容为C,实验时,量热器内先盛以质量为0m ,温度为1t 的冷水,之后,把加热到温度为2t 质量为m 的待测金属块投入量热器中,经过热交换后,水量热器与金属块达到共同的末温θ,依热平衡方程有:
))(()(1002t C c m t mc -+=-θθ (1)
即 )
())((2100θθ--+=t m t C c m c (2) 量热器的热容C 可以根据其质量与比热容算出。
设量热器筒与搅拌器由相同的物质制成,其质量为1m ,比热容为1c ,则
C c m C '+=11 (3)
式中C '为温度计插入水中部分的热容。
C '的值可由下式求出:
{}{
}3109.1cm C J V C ='-⋅ 式中V 为温度计插入水中部分的体积。
{}10-⋅'C J C 表示C '以J ·0
C -1为单位时的数值,而{}3cm V 表示V 以cm 3为单位时的数值。
2、 系统误差的修正
上述讨论就是在假定量热器与外界没有热交换时的结论。
实际上只要有温度差异就必然会有热交换存在,因此实验结果总就是存在系统误差,有时甚至很大,以至无法得到正确结果。
所以,校正系统误差就是量热学实验中很突出的问题。
为此可采取如下措施:
1)要尽量减少与外界的热量交换,使系统近似孤立体系。
此外,量热器不要放在电炉旁与太阳光下,实验也不要在空气流通太快的地方进行。
2)采取补偿措施,就就是在被测物体放入量热器之前,先使量热器与水的初始温度低于室温,但避免在两热器外生成凝结水滴。
先估算,使初始温度与室温的温差与混合后末温高出室温的温度大体相等。
这样混合前量热器从外界吸热与混合后向外界放热大体相等,极大地降低了系统误差。
3)缩短操作时间,将被测物体从沸水中取出,然后倒入量热器筒中并盖好的整个过程,动作要快而不乱,减少热量的损失。
4)严防有水附着在量热筒外面,以免水蒸发时带走过多的热量。
5)沸点的校正。
在实验中,我们就是取水的沸点为被测物体加热后的温度,但压强不同,水的沸点也有所不同。
为此需用大气压强计测出当时的气压,再由气压与沸点的关系通过查表查出沸点的温度。
采取以上措施后,散热的影响仍难以完全避免。
被测物体放入量热器后,水温达到最高温度前,整个系统还会向外散热。
所以理论上的末温就是无法得到的。
这就需要通过实验的方法进行修正:在被测物体放入量热器前4-5min 就开始测度量热器中水的温度,每隔1min 读一次。
当被测物体放入后,温度迅速上升,此时应每隔0、5min 测读一次。
直到升温停止后,温度由最高温度均匀下降时,恢复每分钟记一次温度,直到第15min 截止。
由实验数据作出温度与时间的关系t T -曲线,如图1所示。
图1 温度与时间的关系曲线 为了推出公式(2)中水的初温度1t 与末温θ,在图1中,对应于室温在曲线上之O 点作一垂直与横轴的直线。
然后将曲线上升部分AE 及下降部分FD 延长,与此垂线分别相交于B 点与C 点,这两个交点的温度坐标可瞧成就是理想情况下的T 1与T 2,即相当于热交换无限快时水的初温1t 与末温θ。
四、 实验内容与步骤
1、称出质量为m 的金属粒,放入加热器中隔水加热。
在沸水中至少15min,才可认为金属粒与水同温。
水沸腾后测出大气压强P 。
2、在金属粒加热的同时,称出量热器内筒及搅拌器质量1m ,然后倒入适量的水,并加入冰屑使水温降低到室温下6~4(注意:不能使筒外表有水凝结),称出总质量10m m +,求出水的质量0m 。
3、在倒入金属粒前,一面用棒轻轻搅动,一面每隔一分钟测一次水温,计时5分钟后将加热好的金属粒迅速而准确地倒入量热器内(注意:不能使量热器中水溅出,又切勿碰到温度计),立即将盖盖好并继续搅拌,同时,每隔半分钟测一次水温。
至水温均匀下降,每隔一分钟测一次水温,连续10min 左右为止。
4、用排水法将温度计浸没于水下的体积在小量筒中测得。
先将水注入小量筒中,记下其体积1V ,然后将温度计插入水中,使温度计插入水中的体积与在量热筒中没入水中的体积相同(以从量热筒中取出温度计上水印为准),读出液面升高后的体积2V ,则温度计插入量热筒水中的体积为:12V V V -=(注意:实验中温度计中的水银泡一定要没入水中,但又不能碰到锌粒)。
5、查表得到实验气压条件下水的沸点T ',即作为金属粒加热后的温度2t 。
6、作温度-时间曲线,求出1T 与2T ,即公式(2)中水的初温度1t 与末温θ。
五、数据记录及处理
自拟表格记录测量的有关数据。
根据公式(2)求出金属粒的比热c ,并与其标准比热比较,求出相对误差。
六、思考题:
1.混合量热法的原理就是什么?它的基本实验条件就是什么?如何保证?
2.实验中质量称衡采用了精度较低的物理天平,为什么测量温度却采用了分度值为0.10
C 的精密水银温度计?
3.为了提高量热精度,实验中采取了哪些措施?
4.试分析您在实验中对各参量(如温度、水的质量等)的选取就是否得当?
[附记]
温度计插入水中部分的热容可如下求出:已知水银的密度为13.6g ·cm -3,比热容为0、139J ·g -1·0C -1,其1cm 3的热容为1、89 J ·cm -3·0C -1。
而制造温度计的耶那玻璃的密度为2.58 g ·cm -3,比热容为0、83 J ·g -1·0C -1,其1cm 3的热容为2、14J ·cm -3·0C -1,它与水银的很相近,因为温度计插入水中部分的体积不大,其热容在测量中占次要地位,因此可认为它们1cm 3的热容就是相同的。
设温度计插入水中部分的体积为V(以cm 3为单位),则该部分的热容C '的数值可取为{}{}3109.1cm C J V C ='-⋅,V 可用盛水的小量筒去测量。
