精细有机化学8
精细有机合成习题答案

精细有机合成习题答案【篇一:08应化精细有机合成复习题答案】txt>一.单项选择题(8)在下列每小题的四个备选答案中选出一个正确的答案,并将其字母标号填入题干的括号内。
1.如果分子本身包含一个反应活性低的官能团在适当的阶段,通过某种专一性的反应,可转化为反应活性较高的官能团。
这种官能团称为:(b)a.亲电官能团;b.潜官能团;c.亲核官能团;d.极性官能团;2.想象选择一个合适的位置将分子的一个键切断,使分子转变为两个不同的部分。
用双线箭头符号和画一条曲线穿过被切断的键来表示。
这种方法称为:(c)a.极性反转;b.反向分析;c.分子切断;d. 反应选择性;在一系列的转变的某一阶段,引入一个原子或原子团,使后续的反应过程能按设计的要求,有控制地进行,从而保证系列反应能够高效率地完成。
这种引入的原子或原子团称为:(a)a.控制因素;b.潜官能团;;c.极性官能团;d.极性反转;4.在合成设计中使某个原子或原子团的反应特性发生了暂时性的转换称为:(b)a. 关键反应;b.极性转换;c.反应选择性;d.控制因素;5.在复杂化合物的合成中,有些反应转化率很低或正副产物很难分离纯化,反应时间长,这些反应称为:(c)a.反应选择性;b.反应的专一性;c.关键反应;d. .控制因素;6.目标分子—中间体—化工原料的分析过程称为:(b)a.正向合成分析法;b .逆向合成分析法; c.不对称合成分析法;d.关键反应分析法;7.一个反应在底物的不同部位和方向进行,从而形成几种产物时的选择程度称为:(d)a.反应的专一性;b.反应的控制性;c.反应的对称性;d,反应选择性;8.将分子的一个键切断,使分子转变为两个不同的部分,这不同的部分叫:(a)a.合成子;b.合成等价物;c.目标分子;d. 有机中间体;9.绿色化学是指在制造和应用化学品时( a )a.应有效利用(最好可再生)原料,消除废物和避免使用有毒的或危险的试剂和溶剂。
精细有机合成技术:化学氧化剂及其类型

2. 三氧化铬-吡啶复合物氧化
三氧化铬-吡啶复合物主要用于制备羧酸和醌类。但是在温和 的条件下也可以制取醛和酮,以及在芳环上引入羟基。
三氧化铬-吡啶复合物和CH2Cl2组成的溶液称作Collins试剂, 当有机物分子中含有对酸敏感的官能团时,常使用Collins试剂。 尤其是在无水条件下使用Collins试剂非常有效,可以将伯醇和仲 醇氧化成醛和酮而不影响对酸敏感的官能团。例如:
• 二氧化锰是较温和的氧化剂,其用量与所用硫酸的浓度 有关。在稀硫酸中氧化时,要用过量较多的二氧化锰; 在浓硫酸中氧化时,二氧化锰稍过量即可。
• 二氧化锰可以使芳环侧链上的甲基氧化为醛,可用于芳 醛、醌类的制备及在芳环上引入羟基等。例如:
三、铬化合物氧化 1. 重铬酸钠氧化
重铬酸钠容易潮解,但是其价格比重铬酸钾便宜得多,在水中的 溶解度大,所以在工业生产中一般都使用重铬酸钠。重铬酸钠可以在 各种浓度的硫酸中使用。其氧化反应式如下:
副产的Cr2(SO4)3和Na2SO4的复盐称为“铬矾”,可以用于制革 工业和印染工业,也可以将Cr2(SO4)3转变为Cr2O3,用于颜料工业。
重铬酸钠主要用于将芳环侧链的甲基氧化成羧基。例如:
重铬酸钠在中性或碱性水介质中是温和的氧化剂,可用于 将 — CH3、—CH2OH、—CH2Cl、—CH=CHCH3 等 基 团 氧 化 成醛基。
2. 有机过氧化物氧化
有机过氧化物主要用于游离基型聚合反应的引发剂。 有些也可以作为氧化剂、漂白剂或交联剂。一般有机过氧 化物均具有强的氧化性,对催化剂、干燥剂、铁、铜、冲 击和摩擦都比较敏感,有爆炸危险性。一般都是以湿态在 低温下贮存和运输。
精细有机合成化学及工艺学

羰基可与亲核试剂发生缩合反应,生成醇、醚或酯类化合物;也可与亲电试剂发生加成反 应,生成烯烃或卤代烃类化合物。
羰基的α-卤代与α-氨基化
在羰基α位引入卤素或氨基,可生成α-卤代酮或α-氨基酮类化合物。常用的卤化剂有卤素、 N-卤代酰胺等,氨基化试剂有氨、胺类化合物等。
氨基官能团转化与合成策略
其他领域
此外,精细有机合成还在染料、香料、 涂料、食品添加剂等领域有着广泛的 应用。
02
基本原理与方法
有机合成反应类型及机理
亲电取代反应
亲电试剂进攻有机分子中的电 子云密度较大的部位,发生取 代反应。
消除反应
有机化合物在特定条件下失去 小分子,形成不饱和键。
亲核取代反应
涉及亲核试剂对有机化合物中 的离去基团进行攻击,形成新 的化学键。
大环化合物合成技术
01
线性合成策略
通过逐步增长碳链的方法合成大环化合物,如酰胺化、酯化等缩合反应
构建大环。
02
模板合成法
利用模板效应控制分子内成环反应,实现大环化合物的合成,如分子内
Diels-Alder反应、分子内Michael加成等。
03
片段连接法
将预先制备好的片段通过高效连接反应组合成大环化合物,如Suzuki偶
初始阶段
早期的有机合成主要依赖于天然产物的提取和分离,合成方法相对 简单。
发展阶段
随着有机化学理论的不断发展和合成方法的不断创新,精细有机合 成逐渐成为一个独立的学科领域。
成熟阶段
现代精细有机合成已经发展成为一个高度成熟的领域,合成方法和技 术不断更新和完善,能够合成出各种复杂结构和功能的有机化合物。
未来研究方向和挑战
复杂天然产物的全合成
精细有机合成单元反应基础PPT课件

➢有机合成反应理论 ➢磺化、硫酸化反应 ➢硝 化 反 应 ➢烷 基 化 反 应 ➢羟 基 化 反 应
➢还 原 反 应ห้องสมุดไป่ตู้➢卤 化 反 应 ➢酰 化 反 应 ➢氧 化 反 应 ➢酯 化 反 应
1
绪论
一、精细化学品的释义 欧美 产量小、纯度高的化工产品。
日本
具有高附加价值、技术密集型、设备投资少、 多品种、小批量生产的化学品。
三大合成材料:塑料、合成橡胶、合成纤维 。
注意:原料与产品的划分不是绝对的。有的化学品从 上游看是产品从下游看则是原料。划分的界限也有所 不同。
10
第1章 绪论/1、精细化工及相关行业的概念
产品生产过程的顺序:
精细化工产品
起始原料
基础有机原料
基本有机化学品
三大合成材料
起始原料:石油、天然气、煤、农林产品(副产品)。
中国 原则上采用日本对精细化学品的释义。
2
美国克林教授的释义
无差别化学品: 差别化学品:
具有固定熔点或沸点,能以分子式或结构 式表示其结构的
不具备上述条件的
通 用 化 学 品 大量生产的无差别化学品(无机酸、碱、甲醇等)
准通用化学品 较大量生产的差别化学品(塑料、合成纤维等)
精细化学品 专用化学品
第一门类又可分为许多小类。中国的分类暂行规定中,不
包括国家医药管理局管理的药品。
5
三、精细化工的特点
1)除化学合成反应、前后处理外,还常涉及剂型制备和 商品化(标准化)才得到最终商品 2)生产规模小,生产流程大多为间歇操作的液相反应,常 采用多品种综合生产流程或单元反应流程 3)固定投资少、资金产出率高 4)产品质量要求高,知识密集度高;产品更新换代快、寿命 短;研究、开发难度大,费用高
精细有机化学合成
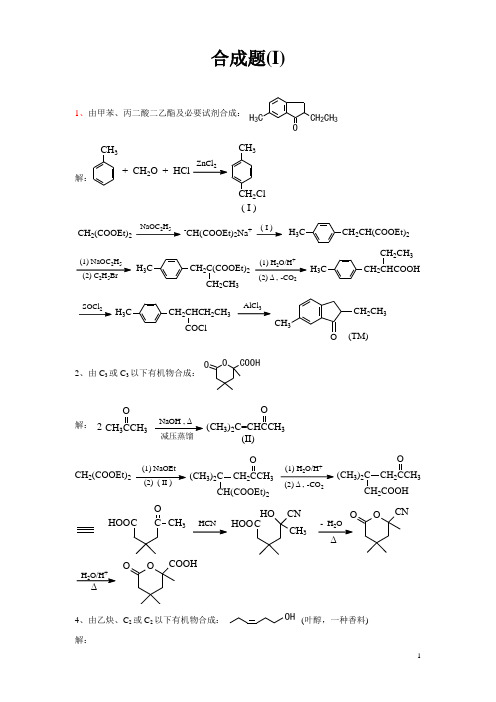
合成题(I)1、由甲苯、丙二酸二乙酯及必要试剂合成:OH 3CCH 2CH 3解:CH 3CH 3CH 2Cl + CH 2O + HCl2( I )2+2CH 2(COOEt)225-CH(COOEt)2Na +( I )H 3C CH 2CH(COOEt)22525H 3C CH 2C(COOEt)22CH 3H 3CCH 2CH 2CH 32H 3CCH 2CHCH 2CH 33CH 3OCH 2CH 3(TM)2、由C 3或C 3以下有机物合成:O COOHO解: CH 33ONaOH , ∆2(CH 3)23O(II)CH 2(COOEt)2(2) ( II )(1) NaOEt (CH 3)2C CH 23OCH(COOEt)22+2(CH 3)2CCH 23OCH 2COOHOO CN2CC CH 3OHOO CHO CN CH 3HOOH 2O/H ∆OO COOH4、由乙炔、C 2或C 2以下有机物合成:OH (叶醇,一种香料)解:CH 3CH 2CCMgBrO 干醚H 2O CH 3CH 2C CCH 2CH 2OHH 2C=CHHCH 2CH 2OH CH 3CH 2CH CHCH CNaCH CCH 2CH 33C H Br25(TM)5、由Br 为有机原料合成:COOCH 3 解:BrNaCNCNH 2O COOHCOClCHO2H /Pd-BaSOBr COOHCOOCH 3Br3+4NaOH/醇COOCH 3ZnBrCHO干醚H 2O COOCH 3- H 2O COOCH3(TM)6、由O 合成3解:OCH 3OHCH 3CH MgI H 2O 24(1) B H 22CH 3HH (TM)7、由丙二酸二乙酯合成COO -N +H 3解:Br Br CH(COOEt)2CH 2(COOEt)2NH O KOHNK O NCH(COOEt)2O(1) C H ONa 322NC(COOEt)2OOCH 2CH(CH 3)22+2(CH 3)2CHCH 2CHCOOH2NH 3COO -+即:8、由苯合成ICl Cl Cl解:NO 2NH 2NHCOCH 3HNO 3H 2SO 432Fe + HClNHCOCH 3NH 2NHCOCH 32Cl ClFe + HCl2NaNO 2+过量HCl。
精细有机合成化学与工艺学唐培堃冯亚青答案

课后习题答案2-1李摆正离子CT卓于大分子所构成的软酸.它客易与大分于或大原干所构成的软緘相结合.以下ffl隔子被Q*从水相梅取到有机相时T从易到难的次洋是:C6H3o->r>Br->cr, CH3Q->F-2-2从理论匕讲,应该用菲质子传運、强扱性有机寤札最合适的瀋剂是二甲基亚碉。
优点足:常压沸点189V;反应可在常压进行;具商较好的电子对给电性,屋良好的离子化涪剂「对金耀正离子有良好的榕刑化作用•对氟化钾有较好的潜解性.使F”成为活泼的裸负离子帚低秦卒缺点是:爆蚱下限2.6% (悻积人张炸上隈28$嵋(^):在常压蕉堀时会部分发生甘解.有时会发生康炸。
N,N•二甲墓甲St胺对金8»正离予也有良好的洛剂牝作用,但是它常压沸点只有153X:,如需在190~200匸反应,琥需翼在高压釜中带压操作,不方便*环丁讽的抉点尼:虽然也足强扱性非质子传遏治虬但不是好的离子化溶剂,对羸化钾的谙解度小”优点是;常压沸序高达胡7・3弋,闪点166C,热穆定性好,可使反应在常压235-245t r®tTf反应克毕后*可先过滤除去尢韶分无机盐’然后驗压At 懈,先蒸出反应产物对昭基氛葦(常压沸点Z04^205t >和未反应的对硝着氯苯(常压稱点242C),再回收环丁狠“N-甲基毗略規IH(常压務点204-2O6T2)的觥点是,虽然也是軽极性非质子传逼溶礼但無电于对给体性不显著,也不是好的离子化涪笊.对氛化钾落解度小.不宜单歿用作上述反应的幡剂。
忧点是;鷄稳定性好,闪点95V.燃点M6V,可用于混督藩剂°在二甲基亚血申据合适■的N-甲墓吐喀烷團・配成谨合帶刑,可缓解二甲基亜碘在高沮回源时的爆坤危险性。
关于相转移催化剂.李锈盐中的节基三乙基孰化鞍价廉易得,如果在190-200V 时季铁盐不穂定*可改用链状棄乙二壽或其单烷基■(开对于本反应也可■不用相转移催牝剂'3-6因为生成的产物2.6•二氯-4-硝基苯胺在水外质中很难再引入第三个氯基妨3-10分别写出如下。
精细有机合成化学复习重点

第1章绪论1.1精细化学品的释义关于精细化学品的释义,国际上有三种说法:传统释义:产量小、纯度高的化工产品。
日本的释义:具有高附加值、技术密集型、设备投资少、多品种、小批量生产的化学品。
我国原则上采用日本对精细化学品的释义。
1.5 精细有机合成的原料资源精细有机合成的原料资源是煤、石油、天然气和动植物。
第2章精细有机合成基础2.1.2. 环上已有取代基的定位规律两类定位基:邻、对位定位基(第一类定位基):-O-, -N(CH3)2, - NH2, -OH, -OCH3, -NHCOCH3, -OCOCH3,-F, -Cl, -Br, -I, -CH3, -CH2Cl, -CH2COOH, -CH2F等。
间位定位基(第二类定位基):-N+(CH3)3, -CF3, -NO2, -CN, -SO3H, -COOH, -CHO,-COOCH3, -COCH3, -CONH2, -N+H3, -CCl3等。
2.1.3 苯环上取代定位规律2.1.3.1 已有取代基的电子效应诱导效应(I):由电负性大小决定。
共轭效应(T):包括π-π共轭和p-π共轭。
有+I,无T:2.1.4 苯环上已有两个取代基时的定位规律2.1.4.1 两个已有取代基的定位作用一致两个已有取代基为同一类型定位基,且处于间位。
两个已有取代基为不同类型定位基,且处于邻、对位。
2.1.4.2 两个已有取代基的定位作用不一致两个已有取代基为不同类型定位基,且处于间位。
——取决于第一类定位基两个已有取代基为同一类型定位基,且处于邻、对位。
——取决于定位能力的强弱2.4 精细有机合成中的溶剂效应(3)溶剂极性的本质——溶剂化作用每一个被溶解的分子或离子被一层或几层溶剂分子或松或紧地包围的现象,叫做溶剂化作用,它包括溶剂与溶质之间所有专一性和非专一性相互作用的总和。
按Lewis酸碱理论分类按起氢键给体的作用分类按专一性溶质、溶剂相互作用分类无机溶剂与有机溶剂;极性溶剂(电子对受体(EPA)溶剂与电子对给体(EPD)溶剂)与非极性溶剂。
精细有机合成化学与工艺学答案

精细有机合成化学与工艺学答案【篇一:精细有机合成化学及工艺学期末复习资料】ss=txt>1. 写出制备2,6-二氯苯胺的其他合成路线的反应式。
2. 制clt酸时,将920kg甲苯用2880kg100%硫酸进行一磺化,然后通入710kg氯气进行氯化,试计算以下数据并进行讨论。
(1)h2so4/c7h7摩尔比;(2)磺化后∏值;(3)磺化后总酸度;(4)cl2/c7h7摩尔比;(5)氯化后总酸度。
13.写出由十二烷基苯用不同方法制十二烷基苯磺酸钠时的主要磺化方法和分离方法,并进行对比。
4.写出由环氧乙烷制备2-氨基乙基磺酸钠的几个合成路线和各步反应的名称。
25.常见杂环化合物结构式及其名称。
345【篇二:精细有机合成化学及工艺学复习参考题】ass=txt>精细化学品:“凡能增进或赋予一种(类)产品以特定功能,或本身具有特定功能的小批量或高纯度化学品”。
精细化学品的特点:①产品功能性强(专用性)②批量小③品种多④利润率高⑤更新换代快精细化工:“生产精细化学品的工业”。
“它属于一类化工产品的生产行业” 。
精细化工的特点:①多品种、小批量②综合生产流程和多功能生产装置③高技术密集度④大量应用复配技术⑤新产品开发周期长,费用高⑥商品性强、市场竞争激烈2、新领域精细化学品的类别。
食品添加剂、饲料添加剂、电子化学品、造纸化学品、塑料助剂、皮革化学品、表面活性剂、水处理剂等。
3、精细化率的定义、我国目前的精细化率。
精细化工率(精细化率)?精细化工产品的总值?100%化工产品的总值精细化率是一个国家或地区化学工业发达程度和化工科技水平高低的重要标志。
我国目前的精细化率为45%。
4、世界精细化工的发展趋势。
发达国家新领域精细化工发展迅速、重视化境友好绿色精细化学品和超高功能及超高附加值产品,发展绿色化生产与生物工程技术。
传统精细化工向发展中国家转移。
5、我国精细化工的现状与存在的主要问题。
●我国精细化工产品的自我供应能力已有了大幅度的提升,传统精细化工产品不仅自给有余,而且大量出口;新领域精细化工产品的整体市场自给率达到70%左右。
2023年精细化工专业考研书目

2023年精细化工专业考研书目1.《有机化学》(第八版)
作者:赵德昌,程积民,苑虹
出版社:高等教育出版社
2.《物理化学》(第七版)上下册
作者:陈儒文,顾诚
出版社:高等教育出版社
3.《分析化学》(第八版)
作者:陈一新,周文金,李佳芝
出版社:高等教育出版社
4.《工程化学》(第三版)
作者:郑欣鹏,钱莉英
出版社:清华大学出版社
5.《材料化学》(第二版)
作者:陈凯歌,朱振中,王玉峰
出版社:高等教育出版社
6.《精细有机合成》(第二版)
作者:吴公俊,高劲松
出版社:高等教育出版社
7.《化学反应工程》(第二版)
作者:朱集成,王恩康,赵艳萍
出版社:化学工业出版社
8.《催化与催化反应工程》(第二版)
作者:张琼,李新民
出版社:清华大学出版社
9.《化学工程原理》(第四版)
作者:曾良锋,董志华,王道华
出版社:高等教育出版社
10.《化学生物学》(第二版)
作者:杨明,向涛
出版社:高等教育出版社
以上书目为精细化工专业考研推荐的必读书目,涵盖了有机化学、物理化学、分析化学、工程化学、材料化学、化学工程原理等多个领域。
这些书籍具有理论严谨、内容详尽、权威性高等特点,对于精细化工专业考研学生来说,有着极高的学习价值。
精细有机合成原理与工艺思考题-化工02

精细有机合成原理与⼯艺思考题-化⼯02精细有机合成原理与⼯艺思考题第⼀章绪论1、衡量⼀个国家或地区化学⼯业发达程度和化⼯科技⽔平⾼低的重要标志是什么?2、什么叫精细化⼯产品(或精细化学品)?基本特点有哪些?3、精细化⼯的定义;精细化⼯的基本特点有哪些?4、化⼯产品⽣产过程的顺序是怎样的?5、化⼯⾏业类别有哪些?6、精细化⼯的产⽣和发展与什么有关?7、⽬前国外精细化⼯的发展趋势是什么?8、化学⼯业精细化率(精细化⼯率)是怎样定义的?它的标志性意义是什么?9、我国近期出台的《“⼗⼀五”化学⼯业科技发展纲要》将哪些精细化⼯领域列为“⼗⼀五”精细化⼯技术开发和产业化的重点?10、⾃2007年起我国将全⾯禁⽌哪5种⾼毒农药在农业上使⽤?11、我国建设的化⼯园区有哪些?12、中国精细化⼯发展⽐较先进的领域有哪些?举例说明。
13、中国精细化⼯⽣产中存在的问题主要有哪些?14、有机化⼯⽣产的起始原料和主要基础有机原料有哪些?15、精细化⼯专业技术⼈才应具备的素质有哪些?16、有机化⼯原料发展的三个阶段和两次转换各是什么?以农林副产品为原料⽣产的化⼯产品延续⾄今的主要有哪些?为什么能延续⾄今?17、煤化⼯的兴起与发展阶段主要包括哪⼏个⽅⾯?被称为“有机合成⼯业之母”的产品是什么?18、⽯油化⼯的兴起与发展经历了哪⼏个阶段?⽯油化⼯诞⽣的标志是什么?19、⼀个国家有机化⼯发展⽔平的标志是什么?20、⽯油烃裂解(⼄烯装置)可以得到哪些化⼯产品?21、单元反应的概念?最重要的单元反应有哪些?22、合成⽓的⽣产⽅法有哪些?何谓C1化学,C1化学的发展有何意义?合成⽓的定义是什么?23、⽣产糠醛的原料有哪些?糠醛的⽤途有哪些?24、⽯油芳烃⽣产的⽣产⼯艺主要有哪些?芳烃抽提中常⽤的溶剂有哪些?25、写出以下基本化⼯原料主要来⾃哪种资源?⑴甲烷;⑵⼀氧化碳;⑶⼄炔;⑷⼄烯;⑸ C18-C30直链烷烃;⑹苯;⑺萘;⑻ C12-C18直链脂肪酸。
精细有机化学

精细有机化学
辅助剂
在磺化过程中为了抑制氧化、砜的生成 或多磺化等副反应,或是为了改变定位 作用,常常加入适量的辅助剂。
精细有机化学
辅助剂的影响
可以影响磺酸基进入的位置。
O
O
SO3H 磺化
精细有机化学
(1)芳磺酸的异构化芳磺酸在浓硫酸中的异构 化,一般认为是通过水解再磺化而完成的。
在发烟硫酸中的异构化(例如萘二磺酸的异构 化)一般认为是通过分子内重排而完成的。
精细有机化学
异构化
(a)多数情况是磺酸基 水解再磺化的过程。
SO 3H
160℃异构化 SO 3H
(b)无水生成或参与反 应时,可以认为是分子内 重排。
硫酸的浓度对磺化反应的速度有很大 影响。(反应后期保温或提高温度)
精细有机化学
4.1.3反应热力学—磺酸的异构化和水解
以浓硫酸或发烟硫酸为磺化剂的磺化反应是可逆的, 即在一定条件下,可以发生磺酸的异构化反应或磺 基水解的脱磺基反应。 一般认为磺酸的异构化和水解都是可逆的平衡反应。
SO 3H
160℃异构化 SO 3H
2H2SO4
SO3 + H3O+ + HSO4-
2H2SO4
H3SO4+ + HSO4-
3H2SO4
H2S2O7 + H3O+ + 2HSO4-
3H2SO4
HSO3+ + H3O+ + 2HSO4-
精细有机化学
SO3•H2SO4中电离平衡:
SO3 + H2SO4 H2S2O7 + H2SO4
H2S2O7 H3SO4+ +HS2O7-
精细有机合成化学及工艺学复习参考题

1、精细化学品与精细化工的概念与特点。
精细化学品:“凡能增进或赋予一种(类)产品以特定功能,或本身具有特定功能的小批量或高纯度化学品”。
精细化学品的特点:① 产品功能性强(专用性)② 批量小③ 品种多④ 利润率高⑤ 更新换代快精细化工 :“生产精细化学品的工业”。
“它属于一类化工产品的生产行业” 。
精细化工的特点:① 多品种、小批量 ② 综合生产流程和多功能生产装置③ 高技术密集度 ④ 大量应用复配技术 ⑤ 新产品开发周期长,费用高 ⑥ 商品性强、市场竞争激烈2、新领域精细化学品的类别。
食品添加剂、饲料添加剂、电子化学品、造纸化学品、塑料助剂、皮革化学品、表面活性剂、水处理剂等。
3、精细化率的定义、我国目前的精细化率。
精细化率是一个国家或地区化学工业发达程度和化工科技水平高低的重要标志。
我国目前的精细化率为45%。
4、世界精细化工的发展趋势。
发达国家新领域精细化工发展迅速、重视化境友好绿色精细化学品和超高功能及超高附加值产品,发展绿色化生产与生物工程技术。
传统精细化工向发展中国家转移。
5、我国精细化工的现状与存在的主要问题。
●我国精细化工产品的自我供应能力已有了大幅度的提升,传统精细化工产品不仅自给有余,而且大量出口;新领域精细化工产品的整体市场自给率达到70%左右。
一些产品在国际市场上具有较大的影响力。
●目前国内精细化工产品尚难以满足细分市场需求。
以中低档产品为主,难以满足高端市场要求,以电子化学品为代表的高端精细化学品严重依靠进口。
● 在快速变化的市场面前,我国的研发力量还很不足的,特别是薄弱的%100⨯=化工产品的总值精细化工产品的总值)精细化工率(精细化率精细化工的基础性研究已成为我国开发新技术和新产品的重要制约因素。
●部分国家以保护环境和提高产品安全性为由,陆续实施了一批新的条例和标准;我国也在不断加大与人民生活息息相关的工业品的安全管理力度和提高安全标准,这些因素对精细化工的发展提出更高的要求和挑战。
(最新整理)重氮盐的制备及其相关性质

NH2
NH2
NO2 Cl
NO2
NO2
NO2
H3CO
S NH2
N
即先将芳伯胺溶解于4-5倍质量的浓硫酸中,然后在一定温 度下加入微过量的亚硝酰硫酸溶液。为了节省硫酸用量,简 化工艺,也可以向芳伯胺的浓硫酸溶液中直接加入干燥的粉 状亚硝酸钠。
2021/7/26
15
精细有机合成化学与工艺学
8-2 重氮化反应
• 重氮化反应的终点控制要准确。由于重氮化反应是定量进行的, 亚硝酸钠用量不足或过量均严重影响产品质量。因此事先必须 进行纯度分析,并精确计算用量,以确保终点的准确。
•重氮化反应的设备要有良好的传热措施。由于重氮化是放热 反应,无论是间歇法还是连续法,强烈的搅拌都是必需的, 以利于传质和传热,同时反应设备应有足够的传热面积和良 好的移热措施,以确保重氮化反应安全进行。
3
精细有机合成化学与工艺学
8-1 概述
• 用途
重氮盐的制备及其相关性质.
Ar-N2+X- + Ar’-NH2 偶合 Ar-N=N-Ar’-NH2 Ar-N2+X- + Ar’-OH 偶合 Ar-N=N-Ar’-OH
Ar-N2+X- NaSO还3, 原NaHSOA3 r-NHNH2
重氮基转化
ArN2X-
NH2 CH3
NH2 CH3
铵盐不溶于水:快速顺法CH3
H2N
NH2
NH2
即在室温将芳伯胺溶解于过量较少的稀盐酸或稀硫酸中,加
冰冷却至一定温度,然后先快后慢地加入亚硝酸钠水溶液,
直20到21/亚7/26硝酸钠过量为至。
13
精细有机合成化学与工艺学
8-2 重氮化反应
精细有机合成技术:在电解质溶液中的铁屑还原

(4)溶剂 用铁屑还原硝基物时,可用甲醇、乙醇、冰醋酸和水作
为溶剂。用冰醋酸作为溶剂时,反应速度快,产物容易分离, 但产物中含有大量氨基酰化物。
用乙醇作溶剂时,酰化物的含量可明显减少,但是还 原速度减慢。
• 最常用的溶剂是水,而水同时又是还原反应中氢的来源。为 了保证有效的搅拌,加强反应中的传热和传质,水通常是过 量的。但水量过多时,设备的生产能力和电解质的浓度将降 低,一般采用硝基化合物与水的物质的量之比为1:(50~ 100)。对于活性较低的化合物,则可用乙醇、甲醇等能与水 相混溶的溶剂,以利于还原反应的进行。
在电解质溶液中用铁屑还原硝基化合物是一种古老的方法。由于铁 屑价格低廉、工艺简单、适用范围广、副反应少、对反应设备要求低, 所以到目前为止铁屑还原法仍有很大的用途。但是铁屑还原法排出大量 的含胺的铁泥和废水,如果不及时处理将会对环境产生很大的污染。同 时随着机械加工行业的技术进步,铁屑的来源也受到限制,因此产量大 的一些胺类已采用加氢还原法。但对一些生产吨位小的芳胺,尤其是含 水溶性基团的芳胺仍Βιβλιοθήκη 用铁屑还原法。棉织物 染色
溶靛素蓝O4B的制 备 用类似方法,可以 将一系列还原染料 进行还原-硫酸酯化 制成可溶性还原染 料。
反应历程
反应历程
电解质溶液中的铁屑还原
感谢观看
1.反应历程 铁屑在金属盐如FeCl2、NH4Cl等存在下,在水介质中使
硝基物还原,由下列两个基本反应来完成:
所生成的二价铁和三价铁按下式转变成黑色的磁性氧化 铁(Fe3O4)
• 整理上述反应式得到总反应式:
Fe3O4俗称铁泥,它是FeO和Fe2O3的混合物。
2.影响因素
(1)被还原物的结构 对于不同结构的硝基化合物,采用铁屑还原时,反应条
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
HCl NOCl
稀H2SO4 N2O3 小
无机酸浓度 [HX]增加:重氮化质点浓度增加 ]增加: 降低; [ArNH2]降低; [HX]降低:[ArNH2]增加 ]降低: 重氮化质点浓度降低。 重氮化质点浓度降低。
8.2.5 重氮化方法
碱性较强的芳胺 碱性较强的芳胺 较强 特点:带供电基,铵盐稳定, 特点:带供电基,铵盐稳定,不易水解为游离胺 方法: 方法: 铵盐溶于水:慢速正(顺)重氮化法 铵盐溶于水:慢速正(
H (1) HO3S
NH2OH OH(2) SO3H
HO3S N N HO3S
NH2OH N N SO3H NO2
OH HO3S
OH NH2
H N O N NH2 HO3S
NH2 NO2 Cl NO2 NH2 NO2 NO2 H3CO S N NH2
氨基磺酸或氨基羧酸 特点:( :(1 易形成内盐,在酸性介质下不溶; 特点:(1)易形成内盐,在酸性介质下不溶; 可以溶于碱。 (2)可以溶于碱。 方法:碱溶酸析;正重氮化法;反重氮化法 方法:碱溶酸析;正重氮化法;
NH2 H2 N SO3H SO3H
用途
Ar-N2+X- + Ar’-NH2 Ar-N2+X- + Ar’-OH Ar-N2 ArN2 X+X-
偶合 偶合
Ar-N=N-Ar’-NH2 Ar-N=N-Ar’-OH
NaSO3, NaHSO3
还原
Ar-NHNH2
重氮基转化
ArY Y=F, Cl, Br, I, CN, OH, H等 等
8.2.2 重氮化历程
NH2 NO2
CH3 NO2 NH2
NH2 Cl Cl
弱碱性芳胺 特点:( :(1 有两个或两个以上强吸电基; 特点:(1) 有两个或两个以上强吸电基; 不溶于稀酸。 (2)不溶于稀酸。 方法:以浓H 为介质; 方法:以浓 2SO4或CH3COOH为介质; 为介质 亚硝基硫酸法( 亚硝基硫酸法(NO+HSO4-)。
第8章 重氮化和重氮盐的反应
重氮化反应 (Diazotization) 重氮基的转化反应
8.1 概述
1、脂链伯胺重氮盐不稳定 2、芳伯胺(芳杂伯胺)在低温下稳定,具 有很高的反应活性。(*) (重氮盐勿干燥,易爆炸)
RNH2
+
NaNO2
+
2HCl
R N N+ Cl
+ NaCl + H2 O
8.2 重氮化反应
重氮盐被羟基置换8.3.3 重氮盐被羟基置换-水解
SN1历程
慢
+
ArN2+X-
Ar
+
X
+
N2
Ar
+
+
快
H2 O
ArOH
+H
+
H3PO3(或C2H5OH)还原剂 或 还 ArH 脱 氨 基 反应
(1)H2O ArOH (2)H2O,CuSO4催化
ArN2+
ROH, 干 燥 的 重 氮 盐 与醇 共 热
KI(直接加) (
ArI
BF4 ArN2+ BF4 Schiemann反应 反
ArF
CH3 磺化 H2SO4
CH3 硝化 混酸 SO3H
CH3 Cl NH2
CH3 NO2 氯化 Cl2,Fe SO3H
CH3 NaNO2,HCl 重氮化 Cl N2+Cl
CH3 Cl NO2 H+,水解 Cl
CH3 NO2
低温反应: 10℃ (3)低温反应:0~10℃
HNO2 H2O+NO
Ar N N OH
Ar
N2
OH
(4)重氮盐不稳定
8.2.4 重氮化反应影响因素
芳胺碱性
ArNH2 + HCl ArNH3+Cl-
无机酸性质
表 不同无机酸中重氮化亲电质点
无机酸 亲电质点 活性
浓H2SO4 NO+ 大
HBr NOBr
NO2
Na2S2 部分还原 NO2
NH2
H 2SO 4,NaNO 2 重氮化 NO 2
N 2+ HSO 4
H +,H 2O, 水解 NO 2
OH
8.3.4 重氮基被卤原子置换
HCl,Cu2Cl2 Sandmeyer反应 反 HBr,Cu2Br2 Sandmeyer反应 反 ArCl
ArBr
ArN2+
O O R CH2 C CH3 O N N CH3
CH3 C CH2 C NH
CONH2
HO N O
乙酰乙酰芳胺
吡唑酮衍生物
吡啶酮衍生物
偶合反应历程: 偶合反应历程:
ArN2+ O [ Ar N N H O ] H+ Ar Hale Waihona Puke N OArN2+
NH2
[ Ar N N H
+ NH2] H
Ar N N
重氮化反应质点 1、稀盐酸中
NaNO2 ON-OH
+ +
H Cl H Cl
ON-OH ON-Cl
+ +
NaCl H2 O
重氮化反应质点
2、稀硫酸中
2 ON-OH
3、浓硫酸中
ON-OH
ON-NO2+ H O 2
+ 2 H2SO4
ON+ + 2 HSO4-
+
H3 O+
重氮化反应质点活泼性
NO+>ON-Br>ON-Cl>ON-NO2>ON-OH
8.2.2 重氮化反应历程
ArNH2 N O Cl 慢 H [ Ar N N O ] H Cl
H [ Ar N N O ] H
快
ArN2
H 2O
ArNH2
N O N O O
慢
H [ Ar N N O ] H ArN2 H 2O
NO2
H [ Ar N N O ] H
快
8.2.3反应特点(一般反应条件) 反应特点(一般反应条件) 反应特点
OH
-
pH>12 > 反式重氮酸盐
Ar N NO
亚硝胺
(2)NaNO2微过量
Ar-N=N-NHAr
2HNO2
2KI 2H2O
O
0.5~2秒 0.5~
I2
2KCl
2H2O 2NO
使淀粉碘化 钾试纸变蓝
H2N C NH2
H 2 NSO 3 H
HNO2
HNO 2
CO2
H 2 SO 4
N2
N2
3H2O
H 2O
特点 (1)酸要过量
ArNH2 2HX NaNO2 ArN2+X- NaX 2H2O
理论量: 理论量:n(HX):n(ArNH2)=2:1 2:1 实际比: 2.5~ 实际比: n(HX):n(ArNH2)=2.5~4 : 1 2.5
酸的作用: 酸的作用:
①溶解芳胺: 溶解芳胺:
ArNH2 + HCl ArNH3+ClHNO2 + NaCl
+
Na2SO3:NaHSO3(1:1)
NaHSO3
ArNHNH2
Ar N NH SO3Na SO3Na 芳肼-N,N’芳肼-N,N -磺酸钠
ArN N SO3Na
重氮重氮-N-磺酸钠
+H2O -NaHSO4
+HCl+H2O ArNHNH SO3Na -NaHSO4 芳肼磺酸钠
ArNHNH2 HCl
芳肼盐酸盐
N
N X
1 2
Nu
R
①保留氮的重氮基转化反应 ②放出氮的重氮基转化反应
N N Nu
Nu
8.3.1 重氮盐还原为芳肼
在亚硫酸盐和亚硫酸氢盐1:1的混合物 亚硫酸盐和亚硫酸氢盐1:1的混合物 1:1 的作用下,重氮盐可以还原芳肼。 的作用下,重氮盐可以还原芳肼。
ArN2 X
ArN2+X Na2SO3 -NaX
氨基酚类的重氮化(易氧化,弱酸性介质) 氨基酚类的重氮化(易氧化,弱酸性介质) 带吸电子基正重氮化法 正重氮化法) (带吸电子基正重氮化法) 二胺类的重氮化 邻苯二胺(稀盐酸中) 邻苯二胺(稀盐酸中)
+
NH2 NH2 N NaNO2,HCl NH2
NCl
HCl
N N N H
8.3 重氮盐的反应
δ+
SO3H
CH3 Cu2Cl2,HCl Cl 转化 Cl
还原 H2,Ni
COOH NH 2
H 2SO 4,NaNO 2 10 C以 下
o
COOH N 2+ HSO 4
KI
COOH I
A rN 2 + X
BF4
A rN 2 + B F 4
A rF + N 2
+ BF3
8.3.5 偶合反应
定义 重氮盐与芳环、 重氮盐与芳环、杂环或具有活泼亚甲基 的化合物反应,生成偶氮化合物 偶氮化合物的反应叫做 的化合物反应,生成偶氮化合物的反应叫做 偶合反应。 偶合反应。
NH2(OH) Ar N N NH2(OH)
ArN2X
偶合组分 酚类: (1)酚类:
OH OH OH CONH R
2-羟基-3-萘甲酰胺 羟基-
(2)胺类
NH2 NH2
(3)氨基萘酚磺酸
NH2OH HO3S SO3H OH HO3S OH NH2 HO3S NH2
H酸
J酸
