静脉针检验规程
全国临床检验操作规程 静脉采血法

全国临床检验操作规程静脉采血法全国临床检验操作规程中的静脉采血法是一种自静脉抽取血标本的方法,临床上最常用的是真空采血法。
以下是静脉采血法的操作流程:
1. 贴标签和条形码,核对医嘱、检查申请单,然后将标签贴于标本容器外壁上。
2. 携带采血用物至病人床旁,依据检验申请单,核对病人的床号、姓名、住院号、腕带、申请单标本容器以及标签是否一致,向病人及家属说明标本采集的目的及配合方法。
3. 选择合适的静脉,将一次性垫巾置于穿刺部位下。
4. 消毒皮肤,直径不少于5厘米,由内向外、由上向下进行。
5. 用针头在已经消毒的静脉穿刺处刺入血管,一次成功地抽到回血后,然后将针头固定在塑料管的下端,并将适量血液引入标体容器内,必要时用肝素抗凝。
6. 采血后及时拔针,用棉球压迫止血3~5分钟。
7. 采集的标本及时送检。
按照这个操作规程进行静脉采血可以保证血液标本的质量和安全性,为临床检验提供可靠的依据。
静脉血标本采集操作流程

1、将用物携至患者床旁,核对,解释,告知患者∕家属目的及采血前后注意事项,取得患者的配合。
5
2、根据检查目的不同,并粘贴好采血条码。
5
3、选择合适静脉,在穿刺点上方约6cm处扎止血带,常规消毒皮肤。
5
4、戴手套,左手拇指绷紧静脉下端皮肤,右手持采血针与皮肤呈20°进针,刺入静脉,插入真空采血管,按顺序采集血标本。
10、脱手套,洗手。协助患者取舒适卧位。
3
11、用物分类处理,标本连同化验单同时送检。
7
质量
评定
1、与患者沟通贯穿于整个操作过程,患者能知晓护士告知的事项,对服务满意。
3
2、护士操作过程规范,准确。
5
3、采集血标本的方法正确,标本不发生溶血,抗凝标本无凝血,符合检验要求。
5
4、用物齐备,处理规范。
2
15
5、采血完毕,松开止血带,以干棉签置穿刺点处迅速拔出针头。
5
6、按压穿刺点5~10min,勿揉。凝血机制差的患者适当延长按压时间。
5
7、取全血标本时,轻轻转动采血管,防止血液凝固。
15
8、取血清标本时,避免震荡,以防红细胞破裂以造成溶血。
9、采血培养标本时,消毒培养瓶,待血液注入瓶内后轻轻摇匀,在采多样标本时先采血培养。
静脉血标本采集操作流程
操作流程及质量标准
标准分
准
备
人员:衣帽整洁、洗手、戴口罩
5
用物:一次性采血针、一次性手套、安尔碘、棉签、止血带、弯盘、检验单、采血条码、按需备真空采血管。
5
患者及环境:评估患者的病情、穿刺部位的皮肤、静脉充盈程度、心理反应。询问患者是否按照要求进行采血前准备,例如:是否空腹。
静脉穿刺操作流程及其评分标准

静脉穿刺操作流程及其评分标准静脉穿刺是一种常见的医疗操作,用于静脉采血、输液、注射药物等情况下。
它是通过针头穿刺皮肤,插入静脉内,将所需物质引入或抽出体内。
在进行静脉穿刺时,需要遵循一定的操作流程,并且根据操作的准确性和安全性对操作进行评分。
本文将详细介绍静脉穿刺的操作流程,以及相关的评分标准。
一、静脉穿刺操作流程1. 准备工作:在进行静脉穿刺操作之前,操作者需要做好以下准备工作:- 检查所需器械和材料的完整性和清洁程度,包括穿刺针、消毒棉球、一次性注射器、透明胶带等。
- 检查患者的个人信息,确认患者身份和操作需求。
- 与患者进行沟通,解释操作过程和可能的不适感,获得患者的合作。
2. 患者准备:- 让患者舒适地坐下或平躺,将需要穿刺的部位暴露。
- 使用消毒剂清洁穿刺部位,进行局部麻醉(根据需要)。
3. 穿刺操作:- 利用无菌操作,戴上手套,拿起穿刺针。
- 在消毒后的部位上,用一只手将皮肤固定住,用另一只手拿起穿刺针,以约30度角插入皮肤。
- 当感觉到针尖进入皮下组织后,将穿刺针与静脉保持在一条直线上,缓慢推进。
- 当触感到静脉内的阻力消失时,表示穿刺成功。
- 将针头与注射器连接,检查是否能抽出血液。
- 抽出所需的血液或进行输液、注射等操作。
- 完成后,轻轻按压穿刺口,取出穿刺针,用透明胶带固定穿刺口。
4. 操作结束:- 将使用过的器械和材料进行正确的处理,避免交叉感染。
- 将患者的相关信息记录在医疗记录中,包括穿刺部位、操作者、操作时间等。
二、静脉穿刺操作评分标准静脉穿刺的操作评分标准可以根据各个医疗机构或学术组织的要求而有所不同,下面是一个常见的评分标准示例:1. 操纵技术(10分):- 操作时采取正确的无菌技术。
- 操作过程中手的稳定性,保持穿刺针与静脉的正确角度。
- 针头插入和退出的顺畅程度。
- 操作者对针头位置的准确掌握。
2. 患者准备与合作(10分):- 对患者进行有效的沟通和解释,获得其合作。
(019)初始污染菌检验规程

1、目的通过检验产品的初始污染菌,了解产品在生产过程中受微生物的情况,以便更好地提高产品质量。
2、范围本方法适用于本公司生产的一次性使用静脉输液针(简称:输液针)、一次性使用无菌配药注射器带针(简称:配药注射器)、一次性使用无菌注射器带针(简称:注射器)、一次性使用输液器带针(简称:输液器)、一次性使用袋式输液器带针(简称:袋式输液器)及其配件、无菌产品初始包装等的初始污染菌的检验。
3、依据GB 15979-2002 一次性使用卫生用品卫生标准中华人民共和国药典2010版第二部GB 8368 一次性使用输液器GB/T 19973.1-2005 (ISO 11737-1:1995)医疗器械的灭菌微生物学方法第1部分:产品上微生物总数的估计GB 15980 一次性使用医疗用品卫生标准4、要求灭菌产品管道类内腔污染菌数:应≤10cfu/件次,外部应≤100cfu/件次;非管道类应≤100cfu/件次;敷料类应≤100cfu/g;消毒产品应≤1000cfu/件次或重量(g),具体见表1。
5 检验方法5.1卵磷脂、吐温80-营养琼脂培养基的配制:成份:蛋白胨 20 g牛肉膏药 3 g氯化钠 5 g琼脂 15 g卵磷脂肪 1 g吐温80 7 g蒸馏水 1000 g制法:先将卵磷脂加到少量蒸馏水中,加热溶解,加入吐温80,将其他成分(除琼脂外)加到其余的蒸馏水中,溶解。
加入已溶解的卵磷脂、吐温80,混匀,调pH值为7.1~7.4加入琼脂,121℃高压灭菌20min,储存于冷暗处备用。
5.2 样品采样数量:各类产品每批随机抽取10件样品。
5.3 供试液制备5.3.1.供试品是敷料、可以破坏性类可用无菌手续称取10g,放入100ml灭菌生理盐水中充分振荡后取样。
作为1:10的供试液。
5.3.2.供试品是液体取10ml加至100ml灭菌生理盐水中充分振荡后取样。
作为1:10的供试液。
5.3.3.对供试品不能采用破坏性取样可用浸有无菌生理盐水拭子涂抹采样,被采表面积为100cm2,加入灭菌生理盐水100ml。
静脉采血操作流程及标准

静脉采血操作流程及标准1. 操作准备- 准备所需要的设备:采血针、采血管、适量的一次性消毒用品、输血检验申请单等。
- 确保工作区域整洁,采血椅或床的高度合适,保证采集者和患者的舒适度。
- 查看患者的基本信息、医嘱和过敏史。
- 与患者进行交流,解释采血过程并取得患者的同意。
2. 患者准备- 患者在采血前应保持局部清洁,特别是手臂内侧肘窝附近的皮肤应干净。
- 让患者松开衣袖,露出上臂。
3. 操作步骤3.1 洗手- 采集者需正确洗手,采用正确的洗手步骤,保持手部清洁。
3.2 准备采血部位- 用一次性消毒用品清洁采血部位,如内侧肘窝。
- 轻轻按压局部静脉,使静脉充分明显。
3.3 穿刺- 采集者拿起采血针,以30度至45度的角度刺入静脉。
- 连通管穿透静脉后,保持稳定并等待血液进入管内。
- 采血完成后,须立即停止穿刺,还要及时将针头收回,防止血液外溢。
3.4 顺利导管- 一旦血液充满管道,就可以顺利导管。
- 同时,注意不要使导管脱落或移位。
3.5 拆除装置- 在血液充满采血管之后,可以将采血管从导管上拆除。
- 拆除时要保持导管的稳定,避免血液外溢。
4. 采血后处理- 将血液样品妥善保存。
- 对采血点进行适当的处理和清洁,可以使用一次性消毒用品。
- 将采血管等一次性用品进行正确的处理和处置。
标准- 操作过程应规范,医护人员需经过专业培训和资质认证。
- 采血设备和用品应为一次性,以确保操作的卫生和安全。
- 术前术后对患者进行交流,尊重患者权益,取得患者的同意。
- 操作时应使用正确的穿刺角度和运用适度的力度。
- 操作者应遵循洗手流程,确保操作区域和操作者的清洁。
- 采血完成后,应及时处理废弃物并妥善保存采血样品。
- 针头和一次性用品等应进行正确的处理和处置,防止传播感染。
以上是静脉采血操作流程及标准的简要介绍。
在进行静脉采血时,请确保遵循相关的操作流程和标准,以确保采血的卫生和安全。
检验科凝血四项检验操作规程

检验科凝血四项检验操作规程
全血凝固时间检验(CT)
【标本】
静脉取血3ml。
【方法与操作】
试管法、硅管法操作参见《全国临床检验操作规程》(第二版)。
【附注】
1.静脉取血要一针见血,尽量减少组织液和空气混入。
2.水浴箱温度要恒定,过高或过低,可影响结果。
活化部分凝血活酶时间测定(APTT)
【标本】
自静脉取血,用109mmol/L枸椽酸钠作1:9抗凝。
【试剂】
市售成套试剂。
【方法与操作】
按试剂及有关仪器说明书要求进行。
【附注】
1.标本应及时检测,最迟不超过2h。
2.分离血浆应在3000r/min,离心10min。
3.本试验较试管法全血凝血时间敏感,能检出因子Ⅷ:C<25%轻型血友病。
血浆凝血酶原时间测定(PT,一期法)
【标本】
静脉血1.8ml,用109mmol/L枸椽酸钠0.2ml抗凝。
【试剂】
1.组织凝血活酶浸出液;
2.0.025mol/LCaCl2液;
【方法与操作】
见《全国临床检验操作规程》(第二版)。
【附注】
1.采血后宜在1h内完成,置冰箱4℃保存,不应超过4h,-20℃下可放置2周,-70℃可放置6个月。
2.水温箱控制在37℃±1℃,过高过低均影响结果。
简易凝血活酶生成试验(STGT)
【标本】
取全血0.04ml加5ml蒸馏水,混匀,即成溶血液,备用。
【方法与操作】
见《全国临床检验操作规程》(第二版)。
注射剂检验标准操作规程

一、目的:建立注射剂检验标准操作规程,防止错检、漏检的发生。
二、范围:适用于注射剂的检验操作方法。
三、责任:质量部、化验室相关操作人员。
四、内容:注射剂注射剂(《中国药典》2010年版二部附录IB)系指药物与适宜的溶剂或分散介质制成的供注入体内的溶液、乳状液或混悬液,以及供临用前配制或稀释成溶液或混悬液的粉末或浓溶液的无菌制剂。
注射剂可分注射液(其中供静脉滴注用的大体积注射液也称静脉输液)、注射用无菌粉末与注射用浓溶液。
注射剂除应按药典品种项下规定的检验项目外,还应检查“装量”或“装量差异”、“可见异物”和“无菌”。
静脉用注射剂应加查“热原”或“细菌内毒素”;溶液型静脉用注射液、溶液型静脉注射用粉末及注射用浓溶液应加查“不溶性微粒”;静脉输液及插管注射用注射液应加查“渗透压摩尔浓度”。
混悬型注射液,除另有规定外,药物粒度应控制在l5um以下,含15~20um(间有个别20~50um)者,不应超过10%,若有可见沉淀,振摇时应容易分散均匀;乳状液型注射液不得有相分离现象;静脉用乳状液型注射液分散相球粒的粒度90%应在lum以下,并不得有大于5um的乳滴。
“装量”检查法1 简述1.1本法适用于50ml及50ml以下的单剂量注射液的装量检查,其目的在于保证单剂量注射液的注射用量不少于标示量,以达到临床用药剂量要求。
1.2标示装量为50ml以上的注射液和注射用浓溶液,按最低装量检查法标准操作规范检查,应符合规定。
1.3 凡规定检查含量均匀度的注射液(如塞替派注射液).可不进行“装量”检查。
2 仪器与用具2.1注射器及注射针头。
2.2量筒(量入型)规格l、2、5、1O、20及50ml的量筒,均应预经标化。
3 操作方法3.1 按下表规定取用量抽取供试品。
标示装量供试品取用量(支)2ml或2ml以下52ml以上至50ml33.2取供试品,擦净瓶外壁,轻弹瓶颈部使液体全部下落,小心开启,将每支内容物分别用相应体积的干燥注射器(包括注射器针头)抽尽,注入预经标化的量筒内,在室温下检视,读出每支装量。
血液检验操作规程

血液检验操作规程血液检验是一种常见的医学检验方法,通过对血液样本的分析可以了解患者的身体健康状况。
为了确保检验结果的准确性和安全性,进行血液检验时需要遵循一定的操作规程。
以下是血液检验的操作规程,供参考:一、术前准备1.检查器材准备:准备好使用的血液采样管、一次性采血针、无菌棉球、酒精棉球、标本袋、标签等。
2.个人准备:佩戴好手套,保持双手清洁。
3.工作环境准备:保持工作环境的整洁与干净,确保充足的通风。
4.患者准备:告知患者检验的目的和操作过程,取得患者的配合和同意。
二、采集血液样本1.选择采样部位:一般采用手心或者肘部内侧的静脉进行采样。
2.消毒操作:使用75%酒精棉球对采样部位进行消毒,注意消毒时间至少要十五秒。
3.穿刺操作:将一次性采血针插入采样部位的静脉中,注意角度和深浅的控制。
4.填充采血管:将采血管连接到采血针上,成功进入静脉后,血液自动流入采血管中。
5.采集足够血量:根据检验项目的要求,采集足够的血液样本,一般为静脉血5-10ml。
三、标本处理1.标本编号:在标本管上使用无菌笔或标签贴上标本编号,确保标本的唯一性与追溯性。
2.标本保存:轻轻翻转标本管,使血液与抗凝剂充分混合,避免凝结。
有特殊要求的项目(如血细胞分类计数、凝血功能等)需按照相关规定进行标本处理。
3.标本保存温度:按照检验项目的要求,将标本保存在相应的温度下,如室温保存、冷藏或冷冻保存。
四、记录与传送1.记录标本信息:在病人申请单上填写清楚标本信息,包括患者的基本信息、采样时间等。
2.记录操作过程:记录血液检验的操作过程、采血量、抗凝剂类型等信息。
3.传送标本:按照规定的方式将标本送往检验科室,遇到需要特殊处理或迅速检测的标本,及时与检验科协调处理。
五、操作注意事项1.严格遵守无菌操作规范,避免污染标本。
2.穿刺时注意穿刺角度和深度,避免伤及神经、动脉等重要结构。
3.采血过程中尽量减少患者的疼痛和不适感。
4.在操作过程中确保采样集中,避免因各种原因导致标本的浓度变化。
(升级版)静脉抽血技术规范

(升级版)静脉抽血技术规范1. 引言为了进一步规范静脉抽血操作流程,提高临床检测结果的准确性,确保患者安全,特制定本规范。
本规范适用于所有医疗机构的静脉抽血操作。
2. 准备工作2.1 环境准备- 保持操作区域干净、整洁、明亮。
- 温度控制在18-22℃。
- 操作前30分钟关闭门窗,避免空气对流。
2.2 设备与物品准备- 一次性无菌手套。
- 一次性无菌注射器。
- 一次性无菌真空采血管。
- 消毒棉球、棉签。
- 75%酒精、碘伏。
- 创可贴。
- 医疗废物垃圾桶。
2.3 人员准备- 操作者应具备专业技术资格,熟悉静脉抽血操作流程及应急预案。
- 操作者穿着整洁的工作服、戴口罩、帽子,洗手并戴口罩。
3. 操作流程3.1 评估与解释- 向患者解释操作过程、目的及可能出现的不适,取得患者配合。
- 评估患者血管情况,选择合适的穿刺部位(首选手背静脉,其次选头皮静脉、足背静脉)。
3.2 准备与消毒- 戴一次性无菌手套。
- 选择合适的采血管,检查是否漏气、破裂。
- 选择合适的穿刺部位,用75%酒精或碘伏消毒,消毒范围大于5cm。
3.3 穿刺与采血- 操作者示指固定静脉,针头与皮肤成15-30°角,快速穿刺。
- 见回血后,缓慢进针至静脉深处。
- 固定针头,抽取所需血液量。
- 采血过程中,注意观察患者反应,如出现不适,立即处理。
3.4 拔针与按压- 采血完成后,迅速拔针,顺静脉方向按压穿刺点5-10分钟。
- 必要时用创可贴固定。
3.5 处理与核对- 核对患者信息,确保采血无误。
- 将采血管按照规定顺序放入专用送检,及时送检。
- 清理操作区域,废弃物放入医疗废物垃圾桶。
4. 注意事项- 严格执行无菌操作,防止交叉感染。
- 注意保护患者隐私,尊重患者意愿。
- 观察患者面色、神志变化,发现异常立即处理。
- 采血过程中,避免剧烈震荡,防止红细胞破裂。
- 采血后,指导患者正确按压穿刺点,防止出血和血肿。
5. 培训与质控- 定期对操作人员进行静脉抽血技术培训,提高操作技能。
输液针检验规程

一次性使用静脉输液针成品检验规范1.范围本规程规定了本公司一次性使用静脉输液针的检验方法。
本规程适用于本公司生产的一次性使用静脉输液针成品检验,供质管部在成品检验时参照执行。
2.引用标准GB18671-2002 一次性使用静脉输液针GB1962.1-2001 注射器、注射针和其他医疗器械6%(鲁尔)圆锥接头第1部分:通用要求GB1962.2-2001 注射器、注射针和其他医疗器械6%(鲁尔)圆锥接头第2部分:锁定要求GB2828-2003 逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB2829-2003 周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)GB/T14233.1-1998 医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T14233.2-1993 医用输液、输血、注射器具检验方法第2部分:生物试验方法GB18457-2001 制造医疗器械用不锈钢针管GB6682—1992 分析实验室用水规格和试验方法YY/T0296-1997 一次性使用注射针识别色标YY/T0242—1996 医用输液、输血、注射器用聚丙烯专用料YY/T0313-1998 医用高分子制品包装、标志、运输和贮存3.抽样及抽样量3.1抽样方法:在请验批产品中作随机抽样。
3.2抽样量:出厂检验按GB2828-87规定样本量进行取样检验;3.3抽样方案3.3.1周期检查(型式检验)型式检验为全性能检验。
按GB18671-2002中第6章、第9.1条和第10章规定的各项要求各随机抽检5套。
3.3.2逐批检查(物理要求出厂检查)4.检验项目及方法4.1色标输液针应以针柄和的颜色作为针管的公称外径的色标。
其颜色应符合YY/T0296的要求。
4.2微粒污染按以下方法测定,200mL洗脱液中,15~25um的微粒数不得超过1 个/mL;大于25um的微粒数不得超过0.5 个/mL。
使用仪器:微粒计数仪过滤装置通过瓶塞穿刺器与装有氯化钠注射液的输液瓶连接,过滤装置下端接三通转换开关,下接软管至微粒计数器取样杯。
输液针检验规程

一次性使用静脉输液针成品检验规范1.范围本规程规定了本公司一次性使用静脉输液针的检验方法。
本规程适用于本公司生产的一次性使用静脉输液针成品检验,供质管部在成品检验时参照执行。
2.引用标准GB18671-2002 一次性使用静脉输液针GB1962.1-2001 注射器、注射针和其他医疗器械6%(鲁尔)圆锥接头第1部分:通用要求GB1962.2-2001 注射器、注射针和其他医疗器械6%(鲁尔)圆锥接头第2部分:锁定要求GB2828-2003 逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB2829-2003 周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)GB/T14233.1-1998 医用输液、输血、注射器具检验方法第1部分:化学分析方法GB/T14233.2-1993 医用输液、输血、注射器具检验方法第2部分:生物试验方法GB18457-2001 制造医疗器械用不锈钢针管GB6682—1992 分析实验室用水规格和试验方法YY/T0296-1997 一次性使用注射针识别色标YY/T0242—1996 医用输液、输血、注射器用聚丙烯专用料YY/T0313-1998 医用高分子制品包装、标志、运输和贮存3.抽样及抽样量3.1抽样方法:在请验批产品中作随机抽样。
3.2抽样量:出厂检验按GB2828-87规定样本量进行取样检验;3.3抽样方案3.3.1周期检查(型式检验)型式检验为全性能检验。
按GB18671-2002中第6章、第9.1条和第10章规定的各项要求各随机抽检5套。
3.3.2逐批检查(物理要求出厂检查)4.检验项目及方法4.1色标输液针应以针柄和的颜色作为针管的公称外径的色标。
其颜色应符合YY/T0296的要求。
4.2微粒污染按以下方法测定,200mL洗脱液中,15~25um的微粒数不得超过1 个/mL;大于25um的微粒数不得超过0.5 个/mL。
使用仪器:微粒计数仪过滤装置通过瓶塞穿刺器与装有氯化钠注射液的输液瓶连接,过滤装置下端接三通转换开关,下接软管至微粒计数器取样杯。
静脉血液采集标准操作规程

静脉血液采集标准操作规程1、目的:检验科抽取静脉血标本以做各项检验。
2、适用范围:适用于本科做生化、免疫、血常规等项目所需血液标本的采集.3、物品准备:止血带、一次性垫巾、无菌棉签、复合碘消毒液、一次性采血针、负压真空管(数量和种类根据要求选取后检查生产日期、有效期及有无漏气及破损)、试管架、记号笔、一次性口罩、帽子及手套。
4、检验申请单填写要求:4。
1检验申请单门诊医师用电脑机打,使用正楷字,打印字迹清楚,申请单填写完整。
4。
2填写内容包括:受检者姓名、性别、年龄、临床诊断、检验项目、申请年月日时、申请医生等.5、操作步骤:5.1查对检验申请单的受检者姓名、性别、核对检验项目(患者身份识别),核对无误后在电脑上打印条形码及患者取单凭证,告知患者取单的地点及方法等事项。
然后根据不同的检验项目选取不同抗凝剂的采血管,在采血管上贴好与检验项目相对应的条形码。
5.2选择患者血管:常用肘窝静脉、肘正中静脉、前臂内侧静脉,小儿可采用颈外静脉、大隐静脉。
5.3在穿刺部位肢体下放一次性垫巾、扎止血带.5.4用复合碘棉签以穿刺点为中心直径大约5cm左右范围进行消毒两次.5.5嘱受检者握紧拳头,使静脉充盈明显.5.6穿刺:使用真空采血技术。
摘掉静脉穿刺针上的保护套,进行静脉穿刺,穿刺成功后,用贴好条形码的负压真空采血管采集静脉血。
5。
7采血顺序为:凝血项目管(蓝帽)→血沉管(黑色)→血清管(红色或黄色)→肝素血浆管(绿色)→EDTA管(紫色).松开止血带,让患者松拳,用输液贴压住进针处,拔出针头,嘱患者轻轻按压3——5分钟,直到不出血为止。
凝血功能障碍的患者可以嘱其多按压一段时间。
5。
8嘱患者整理衣袖,不要压迫采血胳膊太紧,以防从针眼处渗血。
5。
9采血完毕后,产生的医疗垃圾按规定分类处理。
6、注意事项6。
1采血前应核对好姓名和检验项目,明确标本要求。
6。
2抗凝管收集血标本后,立即将试管轻轻颠倒8次以上,使血液与抗凝剂充分混匀。
医疗器械产品无菌检验操作规程

医疗设备器械产品无菌检验操作规程1、目的通过无菌检验,确保灭菌后产品能够达到无菌的要求。
2、适用范围适用于灭菌后医疗器械产品(列举)的无菌检验。
3、检验依据本厂产品注册标准(编号)EN1174-1996医疗器械灭菌产品中微生物数量的评估《中国药典》(2005年版)GB14233.2-2005医用输液、输血、注射器具检验方法第二部分:生物试验方法GB15980-1995一次性使用医疗用品卫生标准4、仪器、设备百级层流超净工作台、电热干燥箱、电热恒温培养箱、霉菌培养箱、压力蒸汽灭菌器、集菌仪(器)、电子天平、PH计、冰箱、恒温水浴锅、酒精灯、三角烧瓶,接种环、无菌棉签、镊子,试管架,大试管若干等。
5、无菌检验室的环境要求5.1无菌检验应在环境洁净度10000级下的局部百级的单向流空气区域内进行。
5.2缓冲区与外界环境、无菌检验室与缓冲区之间空气应保持正压,阳性对照室与缓冲区之间空气应保持负压。
无菌检验室与室外大气之间静压差应大于10Pa。
无菌检验室的室温应保持18~26℃,相对湿度:45~65%。
5.3无菌检验室的单向流空气区、工作台面及环境应定期按《医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法》的现行国家标准进行悬浮粒子、浮游菌和沉降菌的监测。
每年至少检测一次。
5.4无菌检验过程中应同时检查超净工作台单向流空气中的菌落数:每次操作时在层流空气所及台面的左中右置3个营养琼脂平板,暴露30min,于30~35℃培养48小时,菌落数平均应不超过1CFU/平板。
6、无菌检验前的准备6.1器具灭菌、消毒6.1.1灭菌:试验过程中与供试品接触的所有器具必须采用可靠方法灭菌。
可经电热干燥箱160℃以上干烤2小时,或置压力蒸汽灭菌器内121℃蒸汽灭菌30分钟后使用(根据灭菌效果验证决定灭菌参数)。
所有的灭菌物品不应超过2周即用毕,否则应重新灭菌。
6.1.2消毒:凡检验中使用的器材无法灭菌处理的,使用前必须经消毒处理。
静液常规流程

1、检查核对。
在开始输液之前,需要检查核对患者的姓名等个人信息以及输注的相关药物信息是否一致,并且要再次询问患者是否对输注的相关药物有过敏史,确认完毕后,进行皮试。
2、排气。
检查输液器的有效期以及包装是否完好无损,将输液管插入瓶塞中,将输液的药物瓶挂到输液架上,然后对输液管进行排气。
3、消毒。
穿刺扎针输液,一般选取四肢的浅表易见的静脉进行透皮穿刺,在此之前,要先消毒,穿刺部位要用碘伏或者75%的酒精反复消毒2-3次,并待消毒液体基本挥发后,进行穿刺。
4、穿刺。
在穿刺见回血后,可先暂时开放输液器,快速地固定穿刺针,松开止血带,调节器,等待输液药物滴入通畅时再进行针头的进一步固定。
5、调滴速。
调整至合适的滴速,因为药物的性质不同,滴速也不尽相同,例如快速滴注甘露醇才能够达到脱水的功效,缓慢滴注氯化钾溶液才能够防止快速滴注引起针孔疼痛感以及心脏的不适感。
患者的年龄和性别的不同,滴速也有差别。
6、拔针。
密切关注药液的量,确保在输注完毕之后能及时拔出针头,并且按压针孔2-3分钟,等到针孔凝血后松手即可。
一次性使用输液器检验规程

一次性使用输液器检验规程一、抽样方案将同日生产、同一规格型号、同一灭菌时间的产品组成批,抽样方案采用正常随机一次抽样方案,其不合格分类、判别水平、RQL(不合格质量水平)均按该产品国家标准进行。
二、检验1、包装检测:目测(1)单包装检查应仔细核查商品的“有效期”、“生产批号”标识,另检验包装的密封是否完整,有无漏气,保护套是否脱落、有无异物,静脉针的颜色是否同包装标识一致。
(2)中包装检查应仔细核查商品的标识信息是否符合标准要求,并附有合格证。
(3)外包装的信息应符合YY/T0313的要求。
2、外观尺寸检测:卷尺、游标卡尺、千分尺、目测随机抽取样品,打开单包装,取出输液器,仔细检查调节器、穿刺器等有无毛边、毛刺、塑流、缺陷等,软管应透明无杂质,静脉针应锋利不弯曲。
用游标卡尺仔细测量穿刺器的外径(φ5.2 ±0.1 0.2mm),尖端长度(28±1mm);软度外径不小于6.5mm。
卷尺测量软管末端到滴斗的软管的长度应不小于250mm。
用千分尺测量软管的壁厚不小于0.4mm。
3、性能检测(1)物理要求:专用设备微粒污染:用200ml的洗脱液冲洗内腔通道表面,并通过专用检测设备收集微粒,15um~25um的微粒数不得超过1个/ml;大于25um微粒数不得超过0.5个/ml。
密封性:把输液器安装在专用设备上,浸入20~30℃水中,通入高于20kPa 的大气压保持10秒钟,应不漏气。
连接强度:各组件的连接,应能承受不小于15N的静拉力,并保持15秒钟不脱落。
(2)化学要求:专用设备易氧化物:检验液和空白液消耗KMnO4的体积之差应超过2.0ml。
金属离子:检验液中钡、钙、铜、铅、锡的总含量不超过1ug/ml,镉含量不超过0.1ug/ml。
酸碱度:检验液与空白液PH值差不超过1.5。
(3)生物要求:专用设备无菌、无热源试验:参照GB/T14233.2的要求进行。
静脉采血操作标准
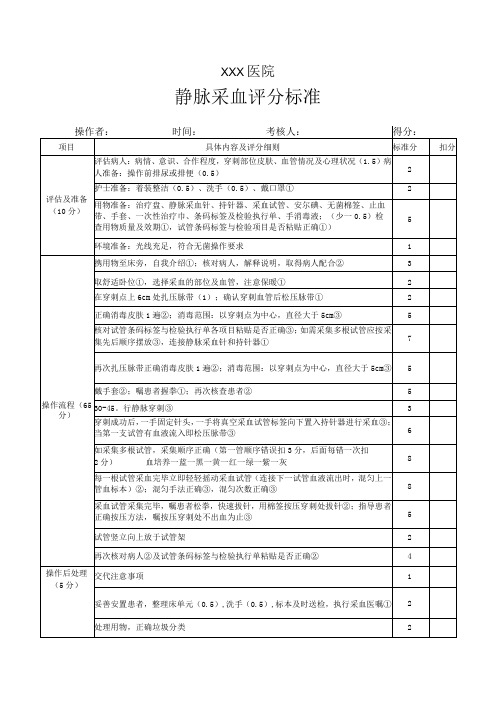
操作后处理(5分)
交代注意事项
1
妥善安置患者,整理床单元(0.5),洗手(0.5),标本及时送检,执行采血医嘱①
2
处理用物,正确垃圾分类
2
人文关怀(5分)
沟通适宜、有效②,关爱患者、保障安全③
5
质量评定
(5分)
现场操作切题,与场景相符③;护理操作程序正确,动作熟练②
5
无菌观念(5分)
跨越无菌区2次及以上全扣
2分)血培养一蓝一黑一黄一红一绿一紫一灰
8
每一根试管采血完毕立即轻轻摇动采血试管(连接下一试管血液流出时,混匀上一管血标本)②;混匀手法正确③,混匀次数正确③
8
采血试管采集完毕,嘱患者松拳,快速拔针,用棉签按压穿刺处拔针②;指导患者正确按压方法,嘱按压穿刺处不出血为止③
5
试管竖立向上放于试管架
2
再次核对病人②及试管条码标签与检验执行单粘贴是否正确②
5
理论提问(5分)
5
考分
总分
IOO
7
再次扎压脉带正确消毒皮肤1遍②;消毒范围:以穿刺点为中心,直径大于5cm③
5
戴手套②;嘱患者握拳①;再次核查患者②
5
30-45。行静脉穿刺③
3
穿刺成功后,一手固定针头,一手将真空采血试管标签向下置入持针器进行采血③;当第一支试管有血液流入即松压脉带③
6
如采集多根试管,采集顺序正确(第一管顺序错误扣3分,后面每错一次扣
5
环境准备:光线充足,符合无菌操作要求
1
操作流程(65分)
携用物至床旁,自我介绍①;核对病人,解释说明,取得病人配合②
3
取舒适卧位①,选择采血的部位及血管,注意保暖①
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一次性使用静脉输液针成品检验规程1.范围本规程规定了本公司一次性使用静脉输液针的成品检验试验方法。
本规程适用于本公司生产的一次性使用静脉输液针成品检验,供质管部在成品检验时参照执行。
2.抽样及抽样量2.1抽样方法:在请验批产品中作随机抽样。
2.3.1周期检查(型式检验)2.3.2型式检验为全性能检验,按GB18671-2009中第6章、9.1和第10 章各项要求各随机抽检5套。
3.物理检验项目及方法3.1色标输液针应以针柄和/或保护套的颜色作为针管公称外径颜色。
3.2微粒污染在层流条件下,取5支输液针,在1m静压头下,使冲洗液分别流过5支各500ml,供收集500ml洗脱液。
然后在微粒分析仪上检测各粒径的微粒数,并按下表所给尺寸各供试静脉输液针(至少5支)只进行一次试验,以每支静脉输液针三个尺寸分类的平均微粒计数作为分析结果。
微粒计数试验报告中记录测得的空白对照液的各值(用同样的试验器具,但不通过供试样品,按上表给出的3个尺寸分类测得的500ml水样的平均微粒数),用以计算污染指数。
空白中的微粒数(Nb)应不超过9,否则应拆开试验装置重新清洗,并重新进行背景试验。
试验报告中应注明空白测定值。
按以下计算污染指数:对各尺寸分类的5个静脉输液针中平均微粒数分别乘以评价系数,各结果相加即得出静脉输液针的微粒数,Na。
再对各尺寸分类的空白对照样品中的微粒数分别乘以评价系数,各结果相加即得空白样品的微粒数,Nb。
Na减Nb即得污染指数。
静脉输液针(试件)中的微粒数:--Na=Na1*0.1+Na2*0.2+Na3*5空白样品中的微粒数:Nb=Nb1*0.1+Nb2*0.2+Nb3*5污染指数:N=Na-Nb≤903.3泄露试验当按以下试验时,应无气体泄漏现象。
使用仪器:气压表将输液针的针管堵住,浸入20~30℃的水中,从连接座锥孔通入高于大气压强50kpa的气压10s,检查输液针漏气的迹象。
3.4连接牢固度试验3.3.1输液针针柄与针管连接处施加20N的轴向拉力10s,应不断开或松动。
3.3.2输液针软管与针柄及软管与连接座之间的连接应能承受15N或伸长为50﹪的静态轴向拉力持续10s,各连接处无松动或分离。
3.4 流量试验将输液针连接到试验仪器上,使出口端与液面保持同一水平,用冲气球向系统内加3.5针管长度针管公称长度小于或15mm时,针管长度应为公称值±1.0mm,公称长度大于15mm时,针管长度应为公称+1.5mm-2.0mm3.6 针尖输液针针尖应锋利,在放大2.5倍条件下,用正常或矫正视力检查时,针尖应无毛边、毛刺和弯钩等缺陷。
3.7润滑剂如果针管涂有润滑剂,用正常或矫正视力观察,针管的外表面不应有可见的润滑剂积聚。
3.8连接座连接座的圆锥接头应符合GB/T1962.1或GB/T1962.2的要求.3.9针柄输液针针柄应完整,标识清晰,针柄应与针尖第一斜面在同一方向其斜度应不大于30°3.9.1软管输液针的软管应柔软、透明、光洁,并无明显机器杂质、异物、扭结,其透明度应保证能观察气泡和回血。
3.9.2保护套、保护帽输液针保护套、保护帽不应自然脱落并于拆除。
4 化学性能4.1供试液的制备取25支输液针,去除保护套并将软管部分剪成1cm长小段,连针管部分一同放入玻璃容器中,加入250mL符合GB/T6682的二级水并在37±1℃下恒温2h,收集全部液体冷却至室温作为检验液。
取同体积水置于玻璃容器中,不装样品同法制备对照液。
4.2还原物质(易氧化物)按下述方法试验时,检验液和空白液消耗0.002mol/L的高锰酸钾溶液的体积之差应不超过2.0mL。
4.2.1试剂配制:a.稀硫酸(20%):取H2SO4128ml,缓缓注入500mL,冷却后稀释至1000mL。
b.淀粉指示剂:取可溶性淀粉0.5g,溶于100ml水中,加热煮沸后放冷却备用(应临用时新制)c.高锰酸钾溶液:取3.3gKMnO4加水1050ml,煮沸15min,加水至1050ml,密封后静置两天以上,用微孔玻璃漏斗过滤,摇匀,标定其浓度。
标定:取1050C下干燥至恒重的基准草酸钠0.25g,精确称重,加入100ml硫酸溶液(8+92)搅拌使之溶解。
自滴定管中迅速将25ml待标定的KMnO4标准溶液加入到本液中,待褪色后,加热到650C,继续滴定至溶液呈液红色并保持30s不褪。
当滴定终点时,溶液温度应不低于550C,同时做空白试验。
每6.7mg草酸钠相当于0.02mol/LKMnO4标准溶液1ml,根据本液的消耗量与草酸钠的取用量算出本液的实际浓度,即得。
d.c(KMnO4)=0.002 mol/L:临用前取0.02 mol/L KMnO4加水稀释10倍e.硫代硫酸钠(0.1 mol/L):称取26gNa2S2O3.5H2O或16g无水Na2S2O3,加0.2无水碳酸钠,溶于1000ml水中,缓缓煮沸10min,冷却,加水至1000ml.置两周后过滤,标定其浓度。
标定:称取0.18g于1200C烘干至恒重的基准重铬酸钾。
精确称量。
置于碘量瓶中,溶于25ml水,加2g碘化钾及20ml稀硫酸(20%),摇匀,于暗处放置10min,加水150ml,用配制好的Na2S2O3溶液[c(Na2S2O3)=0.1 mol/L]滴定,近终点时加2ml淀粉指示液(10g/L)继续滴定至溶液由蓝色变为亮绿色,同时作空白试验。
每1ml的Na2S2O3(0.1 mol/L)相当于4.9031mg的重铬酸钾,根据本液的消耗量与重铬酸钾的取用量算出本液的浓度即得。
f.c(Na2S2O3)=0.01 mol/L:备用前取0.1 mol/L Na2S2O3用新煮沸并冷却的水稀释10倍。
4.2.2试验:取供试液10ml,加入250ml碘量瓶中,精密加入H2SO41ml和0.002mol/L的KMnO4溶液10ml,加热至沸3min,迅速冷却,再加碘化钾0.1g,密塞,摇匀。
立即用相同浓度的Na2S2O3标准溶液滴定至淡黄色,再加淀粉指示剂5滴,继续用Na2S2O3标准溶液滴定至无色,即为终点,同时作空白试验,二者之差应不得超过2.0ml。
4.3金属离子试验4.3.1试剂的配制:a.乙酸盐缓冲液(PH3.5):取乙酸铵25g,加水25ml溶解后,加盐酸液(7mol/L)38ml,用盐酸液(2mol/L)或氨溶液(5 mol/L)准确调节PH值3.5(电位法),用水稀释到100ml。
b.硫代乙酸酰胺试液:取硫代乙酰胺4g,加水使溶解成100ml,置冰箱中保存。
临用前取混合液[由氢氧化钠(1mol/L)15ml,水5.0ml及甘油20ml组成]5.0ml,加上述硫代乙酰溶液1.0ml,置水浴上加热20s,冷却,立即使用。
C.铅标准贮备液:称取1100C干燥恒重的硝酸铅0.160g。
用10ml硝酸溶液(1+9)溶解,移入1000ml容量瓶中,用水稀释至刻度线。
铅标准溶液:临用前精密量取贮备液稀释至所需浓度4.3.2试验:取检验液25ml于25ml纳氏比色管中,另取一支25ml纳氏比色管,加入铅标液25ml,于上述两比色管中加入乙酸盐缓冲液(PH3.5)各2ml,再分别加入硫代乙酰胺试液各2ml摇匀,放置2min,置白色背景下从上方观察,比较颜色深浅。
4.4酸碱度:按下列方法试验时,检验液与空白液的PH值之差应不超过1ml。
将0.1mlTashiro指示剂加入20ml检验液的烧杯中,如果溶液颜色呈紫色,则用氢氧化钠标准溶液(0.01mol/L)滴定;如果呈绿色,则用盐酸标准溶液(0.01mol/L)滴定,直至显现浅灰色。
4.5蒸发残渣按下列方法试验时,蒸发残渣的总量应不超过2mg。
将蒸发皿在105℃恒温箱内烘2小时,再放在干燥器中冷却至恒重,精确称重。
取50ml 水浸液于蒸发皿中,在水浴上蒸干并在105℃恒温箱中烘干至恒重,置于干燥器中冷却至恒重,精确称重,计算出不挥发物含量。
蒸发残渣重W=(W12-W11)-(W02-W01)W12:加入检验液的蒸发皿重量g;W11:未加入检验液的蒸发皿重量g;W02:加入空白液的蒸发皿重量g;W01:未加入空白液的蒸发皿重量g;4.6紫外吸光度按下列方法试验时,检验液的吸光度应不大于0.1。
使用仪器:757分光光度计将已制备好的检验液用0.45um的微孔滤膜过滤,在5h内用1cm检验池以空白对照液为参比在250nm-320nm的波长范围内测定吸光度。
5.生物性能5.1无菌试验静脉输液针应无菌。
5.1.1供试液的制备:取至少3付静脉输液针样品,在无菌室内静脉输液针按管内表面积每10cm2流过管内腔1ml浸提介质,流量为10ml/min。
按下列要求试验应符合规定。
5.1.2与供试液接触的所有器具应灭菌。
置压力蒸汽灭菌器内1210C30min或电热干燥箱内1800C2h灭菌。
5.1.3在使用前,细菌培养基经30~350C培养48h,霉菌培养基经20~250C培养72h。
证明无菌后方可使用。
(管内厌气区小于液面高度的三分之一不得使用)5.1.4无菌室环境应符合要求(3只培养皿上生长的菌落数平均应不超过1个)。
5.1.5对照菌液:取金黄色葡萄球菌的琼脂斜面新鲜培养物,接种一白金耳至需(厌)气菌培养基内,在30~350C培养24h后,用无菌的0.9%NaCl稀释成1:10即得。
5.1.6无菌检查每批供试液分别接种于需气菌,厌气菌培养基5管,其中一管接种金葡菌1ml作为阳性对照,另接种于霉菌培养基2管。
分装量按下表:5.1.7结果判定5.1.7.1阳性对照管在24h内无菌时,根据观察判定结果。
5.1.7.2如需(厌)气菌及霉菌培养管均为澄清或虽混浊但经证明并非有菌生长,判供试液为合格。
5.1.7.3如需(厌)气菌及霉菌管中任何一管显混浊并确证为有菌生长时,应重新取样依法复试两次,不得有菌生长,否则判供试品为不合格。
5.1.7.4如在加入供试液后培养基出现混浊或沉淀,经培养不能从外观上判断时,可转种另一支相同的培养基中或斜面培养基上,培养48~72h后观察有无菌生长。
5.1.8 或检测对灭菌过程进行常规控制所用的指示剂。
5.2热原(细菌内毒素检查法)静脉输液针应无致热原。
5.2.1供试液的制备取至少3支静脉输液针,在无菌条件下,每套静脉输液针内腔注入5ml细菌内毒素检查用水,内腔充满后将剩余的一起置37±10C恒温箱中,保持1h,取出后将全部试液汇聚在无热原的玻璃器皿中,供试液贮存不得超过2h,按下列要求进行试验应符合规定。
5.2.2与供试液接触的所有器具应除热原。
5.2.3试验步骤:将鲎试剂(0.25EU/ml)和细菌内毒素工作标准品分别按标示量加入细菌内毒素检查用水溶解,细菌内毒素工作标准品逐次稀释至2.0λ浓度,供作阳性对照。
