pH标准缓冲溶液(pH=1.68)
标准缓冲液pH值与温度对照表

常用蛋白质分子量标准参照物
高分子量标准参照 蛋白质 肌球蛋白 β-半乳糖苷酶 磷酸化酶B 牛血清清蛋白 过氧化氢酶 醛缩酶 中分子量标准参物 低分子量标准参照 Mr Mr 蛋白质 97 400 212 000 磷酸化酶B 66 200 116 000 牛血清清蛋白 55 000 97 400 谷氨酸脱氢酶 42 700 66 200 卵清蛋白 40 000 57 000 醛缩酶 31 000 40 000 碳酸酐酶 21 500 大豆胰蛋白酶抑制剂 14 400 溶菌酶 蛋白质 碳酸酐酶 大豆胰蛋白酶制剂 马心肌球蛋白 溶菌酶 肌球蛋白(F1) 肌球蛋白(F2) 肌球蛋白(F3) Mr 31 000 21 500 16 900 14 400 8 100 6 200 2 500
(四)凝胶过滤层析介质的技术数据
凝胶过滤介质 名称 分离范围 Superdex 30 Superdex 75 Superdex200 Superose 6 Superose 12 Sephacryl S-100 HR Sephacryl S-200 HR Sephacryl S-300 HR Sephacryl S-400 HR Sepharose 6 Fast Flow Sepharose 4 Fast Flow Sepharose 2B Sepharose 4B Sepharose 6B Sepharose CL-2B Sepharose CL-4B Sepharose CL-6B 45~165 60000~20×105 10000~4×106 45~165 颗粒 大小 (μm) 24~44 <10000 24~44 3000~70000 24~44 3 000 10000~600000 20~40 20~40 5000~5×106 25~75 1000~300000 1000~ 100000 25~75 5000~250000 10000~1.5×106 20000~8×106 10000~4×106 60000~20×106 70000~40×106 60000~20×106 10000~4×106 70000~40×106 45~165 45~165 60~200 25~75 25~75 平均90 平均90 60~200 特性/应用 肽类、寡糖、小蛋白等 重组蛋白、细胞色素 单抗、大蛋白 蛋白、肽类、多糖、核酸 蛋白、肽类、寡糖、多糖 肽类、小蛋白 蛋白,如清蛋白 蛋白、抗体 多糖、具延伸结构的大分 子如蛋白多糖、脂质体 巨大分子 巨大分子如重组乙型肝 炎表面抗原 pH稳定性工作 耐压(Mpa) 最 快 流速 (cm/h) 0.3 100 3~12 0.3 100 3~12 0.3 100 3~12 0.4 30 3~12 0.7 30 3~12 0.2 20~39 3~11 3~11 3~11 3~11 2~12 2~12 4~9 0.2 0.2 0.2 0.1 0.1 0.004 0.008 0.02 0.005 20~39 20~39 20~39 300 250 10 11.5 14 15
ph标准缓冲溶液

ph标准缓冲溶液PH标准缓冲溶液。
PH标准缓冲溶液是一种用于维持溶液PH值稳定的溶液,通常用于实验室中的生物化学、生物工程和生物医学研究中。
它能够在一定范围内抵抗外界酸碱的影响,保持其PH值不变,从而确保实验结果的准确性和可重复性。
PH标准缓冲溶液通常由酸和碱的盐酸或醋酸盐溶液组成,其PH值可以根据实验需要进行调整。
在实验室中,常用的PH标准缓冲溶液有PH 4.01、PH 6.86和PH 9.18等。
这些溶液可以在不同的实验条件下提供稳定的PH值,确保实验结果的准确性。
PH标准缓冲溶液在实验中起着至关重要的作用。
首先,它可以用于校准PH计,确保PH计的准确性和可靠性。
其次,它可以用于调节实验溶液的PH值,使实验条件得到标准化和统一化。
此外,PH标准缓冲溶液还可以用于稀释样品、冲洗实验仪器和保存实验样品等多种用途。
在选择PH标准缓冲溶液时,需要根据实验需要和样品的PH值范围来进行选择。
一般来说,PH标准缓冲溶液的选择应该覆盖实验样品的PH值范围,并且要考虑实验条件下的温度和压力等因素。
在使用PH标准缓冲溶液时,需要注意避免溶液的污染和变质,以免影响实验结果。
总之,PH标准缓冲溶液在生物化学、生物工程和生物医学研究中起着重要的作用。
它能够稳定溶液的PH值,保证实验结果的准确性和可重复性。
因此,在实验室中正确选择和使用PH标准缓冲溶液是非常重要的,这不仅关系到实验结果的准确性,也关系到实验数据的可信度和科研成果的真实性。
综上所述,PH标准缓冲溶液是实验室中不可或缺的重要试剂,它的正确选择和使用对于保证实验结果的准确性和可靠性至关重要。
希望本文能够帮助读者更好地理解PH标准缓冲溶液的作用和意义,正确选择和使用PH标准缓冲溶液,从而提高实验结果的准确性和可重复性。
ph标准缓冲液

ph标准缓冲液PH标准缓冲液。
PH标准缓冲液是在化学实验和生物实验中常用的一种试剂,它可以维持溶液的酸碱度不变,使实验结果更加准确可靠。
PH标准缓冲液通常用于校准PH计、酶活性实验、细胞培养等领域,具有非常重要的作用。
本文将介绍PH标准缓冲液的基本原理、常见类型以及使用注意事项,希望能够对大家有所帮助。
PH标准缓冲液的基本原理是利用一种酸和它的共轭碱(或碱和它的共轭酸)的混合物,在一定温度下,当外加少量强酸或强碱时,溶液的PH值变化不大。
这是因为缓冲液含有相对较多的共轭酸和碱,它们可以迅速中和外加的酸或碱,使溶液的PH值保持相对稳定。
因此,PH标准缓冲液可以在一定范围内维持溶液的酸碱度,使实验结果更加准确可靠。
常见的PH标准缓冲液包括磷酸盐缓冲液、乙酸盐缓冲液、三羟甲基氨基甲烷缓冲液等。
它们分别适用于不同的PH范围,可以根据实验需要选择合适的缓冲液。
例如,磷酸盐缓冲液适用于PH值在2.1-7.4范围内的实验,而乙酸盐缓冲液适用于PH值在3.6-5.6范围内的实验。
选择合适的PH标准缓冲液对于实验结果的准确性至关重要。
在使用PH标准缓冲液时,有一些注意事项需要牢记。
首先,需要严格按照说明书上的配制方法来配制缓冲液,以确保溶液的PH值准确。
其次,配制好的缓冲液需要密封保存,避免受到外界杂质的影响。
最后,在使用缓冲液时,需要用PH计进行准确测量,避免PH值的误差对实验结果造成影响。
总之,PH标准缓冲液在化学实验和生物实验中起着至关重要的作用。
它能够维持溶液的酸碱度不变,使实验结果更加准确可靠。
在选择和使用PH标准缓冲液时,需要根据实验需要选择合适的类型,并严格遵循配制和使用方法,以确保实验结果的准确性。
希望本文对大家有所帮助,谢谢阅读!。
ph标准缓冲溶液

ph标准缓冲溶液PH标准缓冲溶液。
PH标准缓冲溶液是一种用于调节溶液PH值的重要试剂,广泛应用于生物化学、生物工程、药物研发等领域。
在实验室中,我们经常需要对溶液的PH值进行精确控制,以保证实验结果的准确性和可重复性。
而PH标准缓冲溶液则是帮助我们实现这一目标的重要工具。
PH标准缓冲溶液的制备。
PH标准缓冲溶液的制备需要精确的配制和标定。
首先,我们需要选择适当的缓冲体系,常用的缓冲体系包括磷酸盐缓冲体系、乙酸盐缓冲体系、三羟甲基氨基甲烷缓冲体系等。
在选择缓冲体系时,需要考虑实验条件、所需PH范围以及缓冲液对实验物质的影响等因素。
选定缓冲体系后,我们需要准确称取相应的缓冲盐和酸碱溶液,按照一定的配比将它们溶解在去离子水中,制备出一系列不同PH值的缓冲溶液。
接下来,我们需要对制备的PH标准缓冲溶液进行标定。
标定的过程包括使用PH计测定溶液的PH值,并与理论值进行比较,以验证溶液的准确性。
在标定过程中,我们需要注意保持实验环境的稳定,避免外界因素对PH值的影响,确保标定结果的准确性。
PH标准缓冲溶液的应用。
PH标准缓冲溶液在实验室中有着广泛的应用。
首先,它常用于生物化学实验中对酶活性的研究。
许多酶对PH值非常敏感,因此在研究酶的活性和稳定性时,我们需要使用不同PH值的缓冲溶液来模拟不同的生理环境,以确定酶的最适工作PH范围。
其次,PH标准缓冲溶液也常用于细胞培养和细胞实验中。
细胞对PH值的变化也非常敏感,不同PH值的培养基对细胞的生长、分化和代谢都会产生影响。
因此,我们需要使用PH标准缓冲溶液来调节培养基的PH值,以提供适宜的生长环境。
此外,PH标准缓冲溶液还常用于药物研发领域。
许多药物的稳定性和溶解性都与PH值密切相关,因此在药物的研发和质量控制过程中,我们需要使用PH标准缓冲溶液来进行相关的实验和分析。
结语。
PH标准缓冲溶液作为一种重要的实验试剂,在生物化学、生物工程、药物研发等领域发挥着重要的作用。
实验用PH计说明书--奥豪斯

一个标准 pH 缓冲溶液并显示,待仪器 判断 pH 电极响应已达终点后,仪器显 示如左图,并已完成三点校准,然后 仪器自动进入 pH 测量模式。并同时显 示经过 pH 溶液校准后的 pH 电极性能 状态图标。 在经过三点校准后,仪器具有最佳的测量精度。特别适合需大宽度 测量范围下的 pH 精密测量,并可修正由于 pH 电极线性不佳而带来的测 量误差。 在进行 pH 校准时,当 LCD 上的“MTC”图标闪烁,提醒您目前的 pH 温度补偿方式是人工输入温度值(MTC),并请确认目前显示的溶液温度 值,此时可按<∧>、﹤∨>键对溶液温度值进行修改设置,然后按<校 准>键确认输入的温度值并进行 pH 电极校准。
图标⑥:pH 电极性能图标 Offset 图标:pH 电极零电位图标。
Slope 图标:pH 电极斜率图标。 5. 操作键
仪器共有六个操作键,分别是: : 仪器开关键。当仪器关机后,电源适配器没有从 AC220V 插座上拔 下,仪器处于微功耗的待机状态。 pH/mV: 功能键。短按(按键时间小于 1.5 秒)用于切换仪器的测量功能 (pH 测量功能/mV 测量功能)。长按(按键时间大于 1.5 秒)用于仪器 功能参数设置。 校准: 校准键。用于 pH 电极校准。 ∧ :人工温度设定键(增大)、功能参数设定键。
:电极性能优良;
:电极性能一般,可以继续使用;
:电极性能差,建议尽快更换电极。
图标②:测量稳定状态图标 、 : :此图标显示时,表明仪器测量值已达平衡稳定状态,但仪器 继续在进行测量。 :此图标显示时,表明仪器测量值已达平衡稳定状态,并保持 此测量值(自动终点功能),但仪器不继续进行测量。
ph标准缓冲溶液

ph标准缓冲溶液PH标准缓冲溶液。
PH标准缓冲溶液是一种具有稳定PH值的溶液,通常用于实验室中的生物化学、生物工程和生物医学等领域。
它可以在一定范围内保持稳定的PH值,对于许多实验和研究工作都具有重要的作用。
下面将介绍PH标准缓冲溶液的相关知识和使用方法。
PH标准缓冲溶液的组成和原理。
PH标准缓冲溶液通常由酸和碱的盐酸盐或醋酸盐构成,通过调节其浓度比例可以得到不同PH值的标准缓冲溶液。
其原理是利用酸碱中和反应来抵消外界因素对溶液PH值的影响,从而使溶液的PH值保持稳定。
在实验室中,科研人员可以根据需要选择不同PH值的标准缓冲溶液,以满足实验的要求。
PH标准缓冲溶液的种类和用途。
根据PH值的不同,PH标准缓冲溶液可以分为酸性、中性和碱性三种类型。
酸性缓冲溶液通常用于酶促反应和DNA电泳实验中,中性缓冲溶液适用于大多数生物化学实验,碱性缓冲溶液则常用于细胞培养和蛋白质电泳等实验。
在生物医学领域,PH标准缓冲溶液也被广泛应用于药物研发和临床诊断等方面。
PH标准缓冲溶液的制备和保存。
制备PH标准缓冲溶液时,需要严格按照配制方法和配方比例进行操作,以确保溶液的PH值准确稳定。
在制备过程中,还需要使用PH计等仪器进行准确测量,以保证溶液的质量。
制备好的PH标准缓冲溶液应该密封保存在阴凉干燥的环境中,避免阳光直射和高温,以免影响溶液的稳定性。
PH标准缓冲溶液的使用注意事项。
在使用PH标准缓冲溶液时,需要注意以下几点,首先,应该根据实验需要选择合适PH值的缓冲溶液;其次,使用前应该充分搅拌均匀,以确保溶液的PH值准确稳定;最后,使用后应该及时密封保存,避免溶液受到外界因素的影响。
结语。
PH标准缓冲溶液作为实验室常用试剂,在生物化学、生物工程和生物医学领域具有广泛的应用前景。
通过本文的介绍,相信大家对PH标准缓冲溶液有了更深入的了解,希望能够在实验和研究工作中更加准确、稳定地使用PH标准缓冲溶液,为科学研究做出更大的贡献。
ph标准缓冲溶液

ph标准缓冲溶液
PH标准缓冲溶液。
PH标准缓冲溶液是一种具有稳定PH值的溶液,通常用于实验室中对PH值进行校准和调节。
它能够有效地维持溶液的PH值,使实验结果更加准确可靠。
在化学、生物学和医学等领域,PH标准缓冲溶液都扮演着重要的角色。
本文将介绍PH标准缓冲溶液的基本原理、制备方法和应用场景。
PH标准缓冲溶液的基本原理是利用酸碱中和反应来维持溶液的PH值稳定。
它由一种弱酸和其共轭碱或一种弱碱和其共轭酸组成,通过调节弱酸和其共轭碱的浓度比例,可以使溶液的PH值保持在特定的范围内。
当溶液的PH值发生变化时,PH标准缓冲溶液能够迅速吸收或释放氢离子,使PH值恢复到设定的数值。
制备PH标准缓冲溶液的方法主要包括选择合适的弱酸或弱碱、确定所需的PH值、计算所需的物质的量、溶解物质并调节PH值等步骤。
在实验室中,常用的PH标准缓冲溶液有磷酸盐缓冲溶液、乙酸盐缓冲溶液、硼酸盐缓冲溶液等。
在制备过程中,需要严格控制物质的浓度和溶液的体积,以确保PH值的准确性和稳定性。
PH标准缓冲溶液在实验室中有着广泛的应用场景。
首先,它常用于校准PH计和PH电极,确保这些仪器的准确性和稳定性。
其次,它可以用于调节实验溶液的PH值,保证实验结果的准确性。
此外,PH标准缓冲溶液还常用于生物学实验中,维持生物体内外环境的稳定性,促进生物反应的进行。
总之,PH标准缓冲溶液作为一种重要的实验试剂,在化学、生物学和医学领域发挥着重要作用。
通过了解其基本原理、制备方法和应用场景,我们可以更好地利用和管理PH标准缓冲溶液,提高实验的准确性和可靠性,推动科学研究的进步和发展。
ph标准缓冲液

ph标准缓冲液PH标准缓冲液。
PH标准缓冲液是实验室常用的一种重要试剂,它在生物化学、生物工程、药学等领域都有着广泛的应用。
PH标准缓冲液的主要作用是维持溶液的PH值稳定,使实验结果更加准确可靠。
本文将介绍PH标准缓冲液的基本概念、制备方法和常见应用,希望能够对大家有所帮助。
首先,我们来了解一下PH标准缓冲液的基本概念。
PH值是指溶液的酸碱度,通常用来表示溶液的酸性或碱性程度。
PH值的范围是0-14,其中7表示中性,小于7表示酸性,大于7表示碱性。
而PH标准缓冲液则是一种能够稳定维持特定PH值的溶液,通常用来校准PH计和维持实验溶液的PH稳定。
PH标准缓冲液通常是由一种弱酸和其共轭碱或一种弱碱和其共轭酸组成的。
其次,我们来看一下PH标准缓冲液的制备方法。
制备PH标准缓冲液的关键是选择合适的弱酸和其共轭碱或弱碱和其共轭酸,并按照一定的摩尔比混合配制。
常用的PH标准缓冲液有磷酸盐缓冲液、乙酸盐缓冲液、琼脂缓冲液等。
以磷酸盐缓冲液为例,其制备方法如下,首先,按照所需PH值选择适当比例的Na2HPO4和NaH2PO4溶液,然后将它们混合并用水稀释至所需体积,最后用PH计调节PH 值至目标值。
制备PH标准缓冲液需要严格控制PH值和溶液浓度,确保其稳定性和准确性。
最后,我们来了解一下PH标准缓冲液的常见应用。
PH标准缓冲液广泛应用于生物化学、生物工程、药学等领域的实验中。
在酶活性测定、蛋白质电泳、细胞培养等实验中,常常需要使用PH标准缓冲液来维持溶液的PH稳定,确保实验结果的准确性。
同时,PH标准缓冲液也常用于校准PH计和酸碱度计,保证其准确性和可靠性。
在实验中,选择合适的PH标准缓冲液对于实验结果的准确性和可重复性至关重要。
总之,PH标准缓冲液作为一种重要的实验试剂,在实验室中有着广泛的应用。
正确理解PH标准缓冲液的基本概念,掌握其制备方法和应用技巧,将有助于提高实验结果的准确性和可靠性,为科研工作提供有力的支持。
QC缓冲液配制标准操作规程
一、目的:建立缓冲液配制规程,规定了缓冲液的配制内容、方法与要求。
二、范围:适用于缓冲液的配制操作。
三、职责:化验室对实施本规程负责。
四、内容:1.缓冲液配制操作:1.1 乙醇-醋酸铵缓冲液(pH3.7):取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml,即得。
1.2 三乙胺缓冲液(pH3.2):取磷酸8ml,三乙胺4ml,加水稀释到1000ml,用三乙胺调节pH值至3.2,加水500ml,混匀,即得。
1.3 三羟甲基氨基甲烷缓冲液(pH8.0):取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0,即得。
1.4 三羟甲基氨基甲烷缓冲液(pH8.1):取氯化钙0.294g,加0.2mol/L三羟甲基氨基甲烷溶液40ml使溶解,用lmol/L盐酸溶液调节pH值至8.1,加水稀释至100ml,即得。
1.5 三羟甲基氨基甲烷缓冲液(pH9.0):取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g、氯化钠5.8g、乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至9.0,即得。
1.6 乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml,即得。
1.7 巴比妥缓冲液(pH7.4):取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至7.4,滤过,即得。
1.8 巴比妥缓冲液(pH8.6):取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml,即得。
1.9 巴比妥-氯化钠缓冲液(pH7.8):取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH 值至7.8,再用水稀释至500ml,即得。
ph标准缓冲液

ph标准缓冲液PH标准缓冲液。
PH标准缓冲液是一种用于调节溶液酸碱度的重要试剂,广泛应用于生物化学、生物工程、医药等领域。
它能够稳定溶液的PH值,使实验结果更加准确可靠。
本文将介绍PH标准缓冲液的基本原理、常见类型及其应用。
一、基本原理。
PH标准缓冲液是一种能够在一定范围内稳定溶液PH值的溶液。
其基本原理是利用缓冲液中的酸碱成分对氢离子浓度进行调节,从而抵消外界对溶液PH值的影响。
当外界有酸或碱加入时,缓冲液能够吸收或释放氢离子,使溶液的PH值保持相对稳定。
这种稳定性对于许多生化实验至关重要,因为许多生物体内的酶活性、代谢等都对PH值非常敏感。
二、常见类型。
PH标准缓冲液根据PH值的不同分为多种类型,常见的有PH 4.01、PH 6.86、PH 7.00、PH 9.18等。
这些缓冲液分别适用于不同范围的PH值调节,可以满足实验室在不同领域的需求。
此外,还有一些特殊用途的缓冲液,比如在生物学实验中常用的PBS缓冲液,其PH值在7.2-7.6之间,适用于生物细胞的培养和实验。
三、应用。
PH标准缓冲液在生物化学、生物工程、医药等领域有着广泛的应用。
在生物化学实验中,常常需要调节溶液的PH值以适应不同的实验条件,比如酶活性的测定、蛋白质的结晶等。
在生物工程领域,培养基的PH值对于细胞培养和发酵过程至关重要,PH标准缓冲液能够帮助维持培养基的稳定性。
在医药领域,一些药物的稳定性和溶解性也与PH值密切相关,因此PH标准缓冲液也被广泛应用于药物研发和生产过程中。
综上所述,PH标准缓冲液作为一种重要的试剂,在生物化学、生物工程、医药等领域发挥着重要作用。
它的稳定性和准确性对于实验结果的可靠性至关重要,因此在实验中的选择和使用需要特别注意。
希望本文能够帮助您更好地了解PH标准缓冲液的基本原理、常见类型及其应用,为您的实验工作提供一些帮助。
默克pH1.68缓冲液说明书

DIN EN ISO/IEC 17025:2005
Guide to the Expression of Uncertainty in
Measurement
50.0
1.712
Date of release: 2012-04-25
Minimum shelf life: 2015-04-30
MeasurementUncertainty:
Theexpanded uncertaintyUin the certified value is calculated in accordance to GUM and EA-4/02 asU=k·ucwherek = 2 is the coverage factor for a 95%coverage probability. The combined uncertaintyucis obtained from the contributions of the primary reference material, the temperature and the measuring system.
Certificate of Analysis
Certipur®Reference Material
Certified Secondary Standard Reference Buffer Solution
pH(S)=1.681(25℃),Potassium Tetroxalate Dihydrate
PTB1):Physikalisch-TechnischeBundesanstalt, Braunschweig, Germany
标准缓冲液pH值与温度对照表
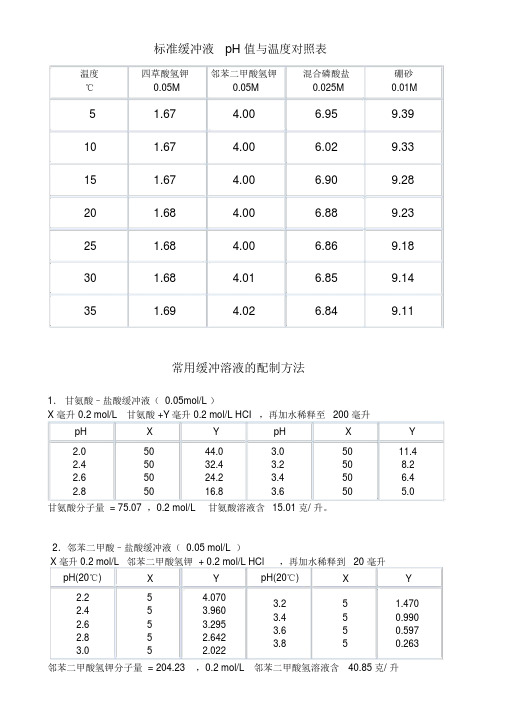
标准缓冲液pH 值与温度对照表温度四草酸氢钾邻苯二甲酸氢钾混合磷酸盐硼砂℃0.05M0.05M0.025M0.01M5 1.67 4.00 6.959.3910 1.67 4.00 6.029.3315 1.67 4.00 6.909.2820 1.68 4.00 6.889.2325 1.68 4.00 6.869.1830 1.68 4.01 6.859.1435 1.69 4.02 6.849.11常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液( 0.05mol/L )X 毫升 0.2 mol/L甘氨酸 +Y毫升 0.2 mol/L HCI,再加水稀释至200 毫升pH X Y pH X Y2.05044.03.05011.42.45032.43.2508.22.65024.23.450 6.42.85016.83.650 5.0甘氨酸分子量 = 75.07 ,0.2 mol/L甘氨酸溶液含15.01 克/ 升。
2.邻苯二甲酸–盐酸缓冲液( 0.05 mol/L )X 毫升 0.2 mol/L邻苯二甲酸氢钾 + 0.2 mol/L HCl,再加水稀释到20 毫升pH(20℃)X Y pH(20℃)X Y2.25 4.0703.25 1.4702.453.9603.450.9902.653.2953.650.5972.85 2.6423.850.2633.05 2.022邻苯二甲酸氢钾分子量 = 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85 克/ 升3.磷酸氢二钠–柠檬酸缓冲液0.2mol/L0.1mol/L0.2mol/L0.1mol/LpH Na2HPO4柠檬酸pH Na2HPO4柠檬酸(ml)(ml)(ml)(ml)2.20.4010.60 5.210.729.282.4 1.2418.76 5.411.158.852.6 2.1817.82 5.611.608.402.83.1716.83 5.812.097.913.04.1115.896.012.637.373.24.9415.066.213.22 6.783.4 5.7014.30 6.413.85 6.153.6 6.4413.56 6.614.555.453.87.1012.90 6.815.454.554.07.7112.297.016.47 3.534.28.2811.727.217.39 2.614.48.8211.187.418.17 1.834.69.3510.657.618.73 1.274.89.8610.147.819.150.855.010.309.708.019.450.55 Na2HPO4分子量 = 142.98,0.2 mol/L溶液为 28.40克/ 升。
ph缓冲液标准

ph缓冲液标准Ph缓冲液是一种具有强度、稳定性和水溶性的特性的一种溶液,是现代实验室中不可缺少的重要部分。
它通常用来控制和维护实验室环境中的酸碱平衡,以及调节生物体内的酸碱平衡。
由于改变Ph值的好处,它的使用日益增加,因此,有必要对Ph缓冲液的标准进行研究和制定。
Ph缓冲液标准的基本要求是提供实验室环境中最佳酸碱平衡,以便满足各种实验需求。
最常用的Ph缓冲液是以氢氧化钠为基础的,根据研究,氢氧化钠溶液的Ph值为7.00,允许有所浮动,但浮动幅度不得超过0.2度。
此外,它可以在溶液中添加盐,以改变Ph值,如氯化钠、氯化钾等,以满足实验室的实验要求。
另一方面,Ph缓冲液的标准还包括它的稳定性。
一般来说,Ph 缓冲液的稳定性是指它在不断改变环境下仍能保持Ph值的一致性。
一般来说,Ph缓冲液在保持Ph值稳定的情况下可以使用一段时间,但是这一段时间取决于缓冲液的组分。
在研究中发现,除非Ph缓冲液在高温下存在,否则它的稳定性可达几个月或数年。
最后,Ph缓冲液的硬度也是一个重要的标准。
硬度是指溶液中离子浓度的大小,由不同的物质决定,如氢氧化钠、氯化钠等。
为了确保缓冲液的质量,需要保持一定的硬度。
例如,氢氧化钠溶液的Ph值为7.00,则最小硬度必须达到1 mol/L,最大硬度也不能超过2 mol/L。
对Ph缓冲液标准的研究和制定,对于实验室环境中的酸碱平衡有着重要的意义。
Ph缓冲液标准的应用可以明显提高实验室环境的平衡性,减少由于温度和盐的影响而引起的稳定性变化,以保证实验室环境达到最佳状态。
因此,严格按照Ph缓冲液标准进行控制,可以有效地提高实验室中实验和分析的准确性和准确度,为实验室环境的稳定性提供有力保障。
标准缓冲液pH值与温度对照表
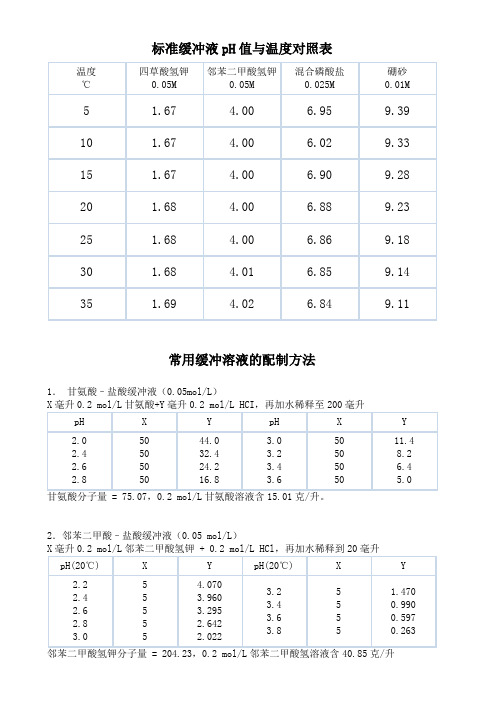
标准缓冲液pH值与温度对照表常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)3.磷酸氢二钠–柠檬酸缓冲液Na 2HPO 4分子量 = 142.98,0.2 mol/L 溶液为28.40克/升。
Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液含35.61克/升。
C 4H 2O 7·H 2O 分子量 = 210.14,0.1 mol/L 溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液 ① 使用时可以每升中加入1克克酚,若最后pH 值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
②柠檬酸C 6H 8O 7·H 2O :分子量210.14,0.1 mol/L 溶液为21.01克/升。
6872柠檬酸钠Na 3 C 6H 5O 7·2H 2O :分子量294.12,0.1 mol/L 溶液为29.41克/毫升。
227.磷酸盐缓冲液242NaH 2PO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
242KH 2PO 4分子量 = 136.09,1/15M 溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M )10.Tris –盐酸缓冲液(0.05M ,25℃)50毫升0.1M 三羟甲基氨基甲烷(Tris )溶液与X 毫升0.1N 盐酸混匀后,加水稀释至100毫升。
232升。
Tris 溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严。
2472硼酸H 2BO 3,分子量=61.84,0.2M 溶液为12.37克/升。
硼砂易失去结晶水,必须在带塞的瓶中保存。
2472硼酸H 2BO 3,分子量=61.84, 0.2M 溶液为12.37克/升。
硼砂易失去结晶水,必须在带塞的瓶中保存。
12.甘氨酸–氢氧化钠缓冲液(0.05M )13.硼砂-氢氧化钠缓冲液(0.05M 硼酸根)14.碳酸钠-碳酸氢钠缓冲液(0.1M )232NaHCO 3分子量=84.0;0.1M 溶液为8.40克/升。
pH标准缓冲溶液.

-
氢氧化钙标准缓冲溶液
在25℃,用无二氧化碳的蒸馏水制备氢氧化钙的饱和溶液。氢氧化钙溶液的浓度c[1/2Ca(OH)2]应在(0.0400~0.0412)mol/L。氢氧化钙溶液的浓度可以酚红为指示剂,用盐酸标准溶液[c(HCl)=0.1mol/L]滴定测出。存放时要防止空气中的二氧化碳的进入。出现混浊应弃去重新配制
ph标准缓冲溶液ph标准缓冲溶液ph标准缓冲溶液standarphbufersolutionsph标准缓冲溶液standarphbufersolutions名称namecompoundingway不同温度时的phures101520253035standardphbuffersolutionsph标准缓冲溶液ph标准缓冲溶液standarphbufersolutionsph标准缓冲溶液standarphbufersolutions名称namecompoundingway不同温度时的phures101520253035ph标准缓冲溶液ph标准缓冲溶液ph标准缓冲溶液standarphbufersolutonsph标准缓冲溶液standarphbufersolutons名称namecompoundingway不同温度时的phferentures101520253035standardphbuffersolutionsph标准缓冲溶液ph标准缓冲溶液standarphbufersolutionsph标准缓冲溶液standarphbufersolutions名称namecompoundingway不同温度时的pherentures101520253035名称namecompoundingway不同温度时的ph值phdifferenttemperatures10152025303540草酸盐标准缓冲溶液ckh3c2o422h2o为005moll
PH标准缓冲溶液制备

pH标准缓冲溶液Standard pH Buffer SolutionspH标准缓冲溶液Standard pH Buffer Solutions名称(Name)配 制(Compounding way)不同温度时的pH值(pH in different temperatures0℃5℃10℃15℃20℃25℃30℃草酸盐标准缓冲溶液c[KH3(C2O4)2·2H2O]为0.05mol/L。
称取12.71g四草酸钾[KH3(C2O4)2·2H2O]溶于无二氧化碳的水中,稀释至1000ml1.67 1.67 1.67 1.67 1.68 1.68 1.69不同温度时的pH值(pH in different temperatures45℃50℃55℃60℃70℃80℃90℃1.70 1.71 1.72 1.72 1.74 1.77 1.79酒石酸盐标准缓冲溶液在25℃时,用无二氧化碳的水溶解外消旋的酒石酸氢钾(KHC4H4O6),并剧烈振摇至成饱和溶液不同温度时的pH值(pH in different temperatures0℃5℃10℃15℃20℃25℃30℃----- 3.56 3.55不同温度时的pH值(pH in different temperatures45℃50℃55℃60℃70℃80℃90℃3.55 3.55 3.55 3.56 3.58 3.61 3.65苯二甲酸氢盐标准缓冲溶液c(C6H4CO2HCO2K)为0.05mol/L,称取于(115.0±5.0)℃干燥2~3h的邻苯二甲酸氢钾(KHC8H4O4)10.21g,溶于无CO2的蒸馏水,并稀释至1000ml(注:可用于酸度计校准)不同温度时的pH值(pH in different temperatures0℃5℃10℃15℃20℃25℃30℃4.00 4.00 4.00 4.00 4.00 4.01 4.01不同温度时的pH值(pH in different temperatures45℃50℃55℃60℃70℃80℃90℃4.05 4.06 4.08 4.09 4.13 4.16 4.21磷酸盐标准缓分别称取在(115.0±5.0)℃干燥不同温度时的pH值(pH in different temperatures冲溶液2~3h的磷酸氢二钠(Na2HPO4)(3.53±0.01)g和磷酸二氢钾(KH2PO4)(3.39±0.01)g,溶于预先煮沸过15~30min并迅速冷却的蒸馏水中,并稀释至1000ml(注:可用于酸度计校准)0℃5℃10℃15℃20℃25℃30℃6.98 6.95 6.92 6.90 6.88 6.86 6.85不同温度时的pH值(pH in different temperatures 45℃50℃55℃60℃70℃80℃90℃6.83 6.83 6.83 6.84 6.85 6.86 6.88硼酸盐标准缓冲溶液c(Na2B4O7·10H2O)称取硼砂(Na2B4O7·10H2O)(3.80± 0.01)g(注意:不能烘!),溶于预先煮沸过 15~30min并迅速冷却的蒸馏水中,并稀释至1000ml。
ph1.68缓冲液溶液成分

pH 1.68缓冲液通常含有酸性物质和碱性物质,以维持其酸碱平衡。
这些缓冲液通常用于医疗诊断、药物生产和生物实验等领域。
在医疗诊断中,pH 1.68缓冲液通常用于检测尿液、血液和其他体液中的pH值。
这些缓冲液通常含有弱酸和弱碱,如柠檬酸和碳酸氢钠,以维持其pH值的稳定。
在药物生产中,pH 1.68缓冲液通常用于控制药物的酸碱平衡,以确保药物的稳定性和有效性。
这些缓冲液通常含有弱酸和弱碱,如乳酸和氢氧化钠,以维持其pH值的稳定。
在生物实验中,pH 1.68缓冲液通常用于维持细胞生长和分裂的酸碱平衡。
这些缓冲液通常含有弱酸和弱碱,如磷酸和氢氧化钠,以维持其pH值的稳定。
需要注意的是,不同的pH 1.68缓冲液可能含有不同的弱酸和弱碱组合物,具体成分可能会因用途而异。
如果您需要了解特定缓冲液的成分信息,建议查阅相关文献或咨询专业人士。
污水检测中各种参数检测方法

污水水质测量一.物理指标:(一)色度:(粕钻比色法)原理:用氯伯酸钾与氯化钻配成与自然 水黄色色调相同的标准比色列,用于水样目视比色测定。
规定1ml∕L 钳所具有的颜色称为1度,作为色度单位。
仪器:100ml 比色管一套(10~12支),5ml 及10ml 移液管各一支。
试剂:铝钻标准溶液:氯铝酸钾K2PtCI6 1.2456g (内含0.5g 伯),氯化钻CθCI2∙6H2O 1.000g,浓盐 酸100ml,配成溶液1L,其色度为500度。
钻钳标准代用液:重将酸钾K2Cr2O7 0.0874g,硫酸钻CoS04∙7H20 2.00g,浓硫酸1ml,配成溶液 1L,其色度相当于500度。
用次标准溶液稀释为不同色度的标准比色列:标准原液(ml )稀释水液(ml )00色度(度)00(二)嗅(气味):②热法:提取100ml 水样,置于250ml 锥形瓶中, (三)浑浊度:(比浊法)用具:100ml 具塞比色管;250ml 、100ml 容量瓶:250ml 具塞无色玻璃瓶。
试剂:二氧化硅浊度标准溶液:称取3克纯白陶土,置于研钵中,加入少量水,充分研磨成糊状, 移入1升的量筒中,加水至标线。
充分搅拌后静置24小时,用虹吸法弃去表面的5厘米液层,收集500 毫升中间层的溶液。
取50毫升次悬浊液,置于恒重的蒸发皿中,在水浴上蒸干,在105C 烘干箱中烘 2 小时,再在干燥箱内冷却30分钟,称重。
重复烘干并称重,直至恒重。
求出每毫升悬浊液中所含白陶土的 重量(亳克)。
在边震边摇状态中,吸取含250毫克白陶土的悬浊液,置1000毫升容量瓶中,加水至标线。
次溶液 的浊度为100度的标准溶液。
步骤:测定浊度在1〜10毫克/升的水样时,先吸取浊度为100度的标准液0、1.00、2.00、4.00、6.00、 8.00、10.00毫升,置于100毫升比色管中,加水至标线,其浊度以此为0、1.0、2.0. 4.0、6.0、8.0. 10∙0度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
北京雷根生物技术有限公司
pH 标准缓冲溶液(pH=1.68)
简介:
pH 标准溶液的pH 值是已知的,并达到规定的准确度,其pH 值有良好的复现性和稳定性,具有较大的缓冲容量,较小的稀释值和较小的温度系数。
该pH 标准缓冲溶液常用于酸度计的定位和斜率校准,其准确度范围在±0.01pH 。
pH 标准缓冲溶液(pH=1.68)是特指在25℃下,pH=1.68。
组成:
操作步骤(仅供参考):
1、 按实验具体要求操作。
2、 将pH 电极在纯水中清洗干净并甩干。
用温度计测量pH 标准缓冲溶液的温度,并将pH 计的温度值调整准确。
自动温度pH 计无需该步骤。
注意事项:
1、 如果每次的使用量很小,可以适当分装后再使用。
2、 显示pH 校准数值时,pH 值会随温度不同而不同,例如在定位校正中,25℃时显示6.86,15℃时就显示6.90。
3、 根据pH 等温测量原理,被测溶液的温度与校准溶液的温度越接近,其测量的准确度就越高。
4、 为了您的安全和健康,请穿实验服并戴一次性手套操作。
有效期:12个月有效。
相关:
编号
名称
OR0040 OR0040 OR0040 Storage pH 标准缓冲溶液(pH=1.68)
50ml 100ml 500ml 4℃ 使用说明书 1份
编号 名称 DC0032 Masson 三色染色液 DF0135 多聚甲醛溶液(4% PFA) NR0001
DEPC 处理水(0.1%) PT0013 考马斯亮蓝快速染色液。
