chapter3立体化学
合集下载
化学第三章立体化学

C=Y
CY (Y) (C)
Y为C、O、N等常见原子,是几重键就相当于连几 个相同的原子。
H (C) CH CH2 相当于 C C H
(C) H
H(C) H(C)
相当于 (C)
H
( C)
(C)
H
H (C)
(C) (C) C CH 相当于 C C H
(C) (C)
(N) (C) C N 相当于 C N
H
H
CC C6H5
CH3 CC
H
H
(顺,顺)
H CC
C6H5
H H
CC
H
CH3
(顺,反)
H
C C6H5
H
CH3
CC
C
H
H
(反,反)
H
H
H
CC
CC
C6H5
H
CH3
(反,顺)
H
CH2CH3 CH3CH2
CH(CH3)2
CC
CC
CH3
CH2CH2CH3 CH3
CH2CH2CH3
(三) Z , E - 命名法
H5 4 H
CC
CH3
3 2H CC 1
H
COOH
(2E,4Z) – 2,4- 己二烯酸
(四)顺反异构体的性质(一般规律的比较)
顺、反-丁烯二酸的物理性质
异构体
熔点/℃ 密度
溶解度( 25℃) /(g/100g·H2
O)
顺-丁烯二酸 130
1.590
78.8
反-丁烯二酸 287
1.625
0.7
1.构造式(结构式)相同(分子的结构相同,构型不同)
2. 比较各种取代原子或原子团的排列顺序时,先比 较直接相连的第一个原子的原子序数。如果是相同 原子,那就再比较第二个、第三个……原子的原子 序数。 C(CH3)3 > CH(CH3)2 > CH2CH3 > CH3
本科有机化学 第三章 立体化学
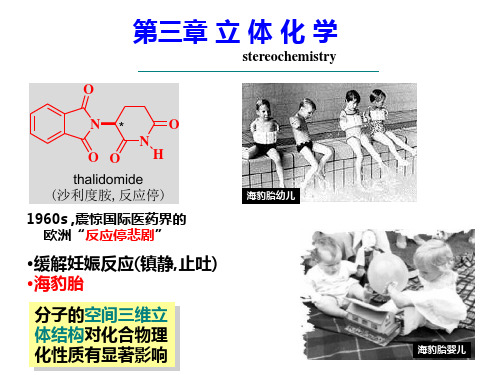
constitutional
isomers
stereoisomers
构造异构
顺反异构: 分子中原子 或取代基在 双键或环状 结构中的相 对位置不同 而产生的异 构现象的排 列方式不同
立体异构
configurational 构型异构 conformational
构象异构
cis/trans
顺反异构
CH3 H CH3 H CH3 H H CH3
7
•对称中心(symmetric center):假想中心,分子中任意一个原子经 过该点再延长到等距离处时都能遇到一个相同的原子.
Cl H H H CH3 H Cl
对称中心
H . H
CH3 H H
有对称中心,非手性分子
Cl H H H . H H Cl H CH3 H
CH3 H
CH3 H
CH3 H
constitutional
isomers
构造异构
官能团异构 位置异构
Br C C C C C C C C Br
立体异构
stereoisomers
碳链异构
C C C C C C C C
R CN R NC
•构造异构:分子中原子连接顺序不同 •立体异构:构造相同,分子中原子在三维空间的排列方式不同
2
同分异构
手性面
两分子不能重合!
• 手性轴(chiral axis):分子的手性是由某些原子或基团对分子 中某一轴呈不对称分布引起的,该轴称为手性轴 两分子不能重合!
手性轴
1,1’-联二萘酚
11
注意
• 手性分子必定具有手性因素 • 但具有手性因素的分子却不一定都是手性分子.
12
手性和旋光性
isomers
stereoisomers
构造异构
顺反异构: 分子中原子 或取代基在 双键或环状 结构中的相 对位置不同 而产生的异 构现象的排 列方式不同
立体异构
configurational 构型异构 conformational
构象异构
cis/trans
顺反异构
CH3 H CH3 H CH3 H H CH3
7
•对称中心(symmetric center):假想中心,分子中任意一个原子经 过该点再延长到等距离处时都能遇到一个相同的原子.
Cl H H H CH3 H Cl
对称中心
H . H
CH3 H H
有对称中心,非手性分子
Cl H H H . H H Cl H CH3 H
CH3 H
CH3 H
CH3 H
constitutional
isomers
构造异构
官能团异构 位置异构
Br C C C C C C C C Br
立体异构
stereoisomers
碳链异构
C C C C C C C C
R CN R NC
•构造异构:分子中原子连接顺序不同 •立体异构:构造相同,分子中原子在三维空间的排列方式不同
2
同分异构
手性面
两分子不能重合!
• 手性轴(chiral axis):分子的手性是由某些原子或基团对分子 中某一轴呈不对称分布引起的,该轴称为手性轴 两分子不能重合!
手性轴
1,1’-联二萘酚
11
注意
• 手性分子必定具有手性因素 • 但具有手性因素的分子却不一定都是手性分子.
12
手性和旋光性
第三章 立体化学

第三章
立体化学
Stereochemistry
主要内容
• 一、手性和手性分子
• 二、含不对称碳原子的分子的立体化学
• 三、不含不对称碳原子的分子的立体化学
• 四、 构象与构象分析
• 五、 立体化学的应用
构造 (Constitution)
官能团异构 碳骨架异构 官能团位置异构
互变异构
分子式相同,原子 的成键顺序不同。
二、含不对称碳原子的分子的立体化学
1、具有一个手性中心的对应异构体
对映异构体的构型和描述
注意:分子的旋光度符号和构型(D,L)之间没 有简单的关系。不是都象甘油醛那样D-是右旋, L-是左旋;例如,L-丙氨酸这个氨基酸是右旋的。
2、具有两个手性中心的对应异构体
例如:
旋光异构体的数目
三、不含不对称碳原子的光活异构体
1.丙二烯型的旋光异构体 (A)两个双键相连
实例:a=苯基,b=萘基,1935年拆分。
(B)一个双键与一个环相连(1909年拆分)
H H3C
COOH H
H CH3
H C CH3
(C)螺环形
H H3C
NH2 H
H COOH
NH2 H
2. 联苯型的旋光异构体
X1 X2
3. 对动态反应选择性的影响
立体专一反应和立体选择反应 • 立体专一反应是指:在相同的反应条件下, 由立体异构的起始物得出立体异构的不同产 物。 • 立体选择性反应是指:在特定反应中,单一 一种反应物能够形成两种或更多种立体异构 产物,但观察到的是其中一种异构体的形成 占优势。
某些立体专一反应
对烯的立体专一加成反应:
5 6 3 4 2 1
0.18nm 4 5 6 1
立体化学
Stereochemistry
主要内容
• 一、手性和手性分子
• 二、含不对称碳原子的分子的立体化学
• 三、不含不对称碳原子的分子的立体化学
• 四、 构象与构象分析
• 五、 立体化学的应用
构造 (Constitution)
官能团异构 碳骨架异构 官能团位置异构
互变异构
分子式相同,原子 的成键顺序不同。
二、含不对称碳原子的分子的立体化学
1、具有一个手性中心的对应异构体
对映异构体的构型和描述
注意:分子的旋光度符号和构型(D,L)之间没 有简单的关系。不是都象甘油醛那样D-是右旋, L-是左旋;例如,L-丙氨酸这个氨基酸是右旋的。
2、具有两个手性中心的对应异构体
例如:
旋光异构体的数目
三、不含不对称碳原子的光活异构体
1.丙二烯型的旋光异构体 (A)两个双键相连
实例:a=苯基,b=萘基,1935年拆分。
(B)一个双键与一个环相连(1909年拆分)
H H3C
COOH H
H CH3
H C CH3
(C)螺环形
H H3C
NH2 H
H COOH
NH2 H
2. 联苯型的旋光异构体
X1 X2
3. 对动态反应选择性的影响
立体专一反应和立体选择反应 • 立体专一反应是指:在相同的反应条件下, 由立体异构的起始物得出立体异构的不同产 物。 • 立体选择性反应是指:在特定反应中,单一 一种反应物能够形成两种或更多种立体异构 产物,但观察到的是其中一种异构体的形成 占优势。
某些立体专一反应
对烯的立体专一加成反应:
5 6 3 4 2 1
0.18nm 4 5 6 1
高等有机化学课件3-第三章 立体化学

联苯类化合物
NO2 CO2H
NO2 CO2H
有对称面(能同镜影分子重选),非手性。
NO2 CO2H
CO2H NO2
CO2H NO2
NO2 CO2H
手性分子
6
Br Br 6'
Br
Br
2' 2 Cl Cl
Cl
Cl
(R)-2,2’-二氯-6,6’-二溴联苯
(R)-2,2’-dibromo-6,6’-dichlorobiphenyl
构型异构: 顺反异构: H
Cl CH3 Cl H
COOH H OH CH3 HO
CH3 H
COOH H CH3
H
对映异构:
D-(-)-乳酸 mp: 52.8° 非对映异构: H
H COOH OH OH CH3
L-(+)-乳酸
COOH H HO OH H CH3
构象异构:
H H
CH3 H H CH3
V U X
R R
V W Z W Z
S S
V
V W X W X
S R
U X
U Z
R S
U Z
Y (A)
Y ( B)
Y (C)
Y ( D)
A和B(C和D)为对映异构体,A和C或者D(B和 C或者D)为非对映异构体。
• 对映异构体之间有相同的性质(除了对偏 振光和手性环境),然而非对映异构体具 有不同的熔点、沸点、溶解度、反应性等 物理、化学及光谱性质。 • 多手性中心的分子最多具有2n个异构体(n =分子中手性中心数),但有时分子内存 在着对称面,这时异构体数减少。
今有两试管分别置入(-)乳酸和(+)乳酸,我 们如何知道它们的构型?
NO2 CO2H
NO2 CO2H
有对称面(能同镜影分子重选),非手性。
NO2 CO2H
CO2H NO2
CO2H NO2
NO2 CO2H
手性分子
6
Br Br 6'
Br
Br
2' 2 Cl Cl
Cl
Cl
(R)-2,2’-二氯-6,6’-二溴联苯
(R)-2,2’-dibromo-6,6’-dichlorobiphenyl
构型异构: 顺反异构: H
Cl CH3 Cl H
COOH H OH CH3 HO
CH3 H
COOH H CH3
H
对映异构:
D-(-)-乳酸 mp: 52.8° 非对映异构: H
H COOH OH OH CH3
L-(+)-乳酸
COOH H HO OH H CH3
构象异构:
H H
CH3 H H CH3
V U X
R R
V W Z W Z
S S
V
V W X W X
S R
U X
U Z
R S
U Z
Y (A)
Y ( B)
Y (C)
Y ( D)
A和B(C和D)为对映异构体,A和C或者D(B和 C或者D)为非对映异构体。
• 对映异构体之间有相同的性质(除了对偏 振光和手性环境),然而非对映异构体具 有不同的熔点、沸点、溶解度、反应性等 物理、化学及光谱性质。 • 多手性中心的分子最多具有2n个异构体(n =分子中手性中心数),但有时分子内存 在着对称面,这时异构体数减少。
今有两试管分别置入(-)乳酸和(+)乳酸,我 们如何知道它们的构型?
第三章立体化学

第三章立体化学
CH3
CH3
H
C
C OH HO
H
Ph
Ph
非对称分子 不对称分子
手性分子
对映体 旋光活性
第三章立体化学
不对称分子一定是手性分子 而手性分子不一定是不对称分子
COOH HO H
H OH COOH
左旋酒石酸
COOH H OH HO H
COOH
右旋酒石酸
COOH H OH H OH
COOH
第三章立体化学
两种同分异构体A和B
A和B的连接顺序是否相同
否
是
构造异构
立体异构体
A和B是否具有不能叠合的实物和镜像的关系
否
是
非对映异构体
对映异构体
第三章立体化学
构造异构体
碳链异构 位置异构
C H 3C H 2C H 2C H 3
C H 3C H C H 3 C H 3
C H 2 = C H C H 2 C H 3 C H 3 C H = C H C H 3
官能团异构 互变异构
C H 3 C H 2 O H C H 3 O C H 3
OO
O HO
C H 3 C C H 2 C O C H 2 C H 3 C H 3 C = C H C O C H 2 C H 3
第三章立体化学
立体异构体
顺反异构 对映异构 构象异构
H 3 H CCCH C H 3
HH H 3 CCCC H 3
第三章 有机立体化学
Organostereochemistry
2010年3月18日
第三章立体化学
1
对映异构体
2
动态立体化学
3
CH3
CH3
H
C
C OH HO
H
Ph
Ph
非对称分子 不对称分子
手性分子
对映体 旋光活性
第三章立体化学
不对称分子一定是手性分子 而手性分子不一定是不对称分子
COOH HO H
H OH COOH
左旋酒石酸
COOH H OH HO H
COOH
右旋酒石酸
COOH H OH H OH
COOH
第三章立体化学
两种同分异构体A和B
A和B的连接顺序是否相同
否
是
构造异构
立体异构体
A和B是否具有不能叠合的实物和镜像的关系
否
是
非对映异构体
对映异构体
第三章立体化学
构造异构体
碳链异构 位置异构
C H 3C H 2C H 2C H 3
C H 3C H C H 3 C H 3
C H 2 = C H C H 2 C H 3 C H 3 C H = C H C H 3
官能团异构 互变异构
C H 3 C H 2 O H C H 3 O C H 3
OO
O HO
C H 3 C C H 2 C O C H 2 C H 3 C H 3 C = C H C O C H 2 C H 3
第三章立体化学
立体异构体
顺反异构 对映异构 构象异构
H 3 H CCCH C H 3
HH H 3 CCCC H 3
第三章 有机立体化学
Organostereochemistry
2010年3月18日
第三章立体化学
1
对映异构体
2
动态立体化学
3
有机化学第三章-立体化学

第三章 立体化学
同分异构
同分异构
碳链(碳架)异构
构造异构
官能团位置异构 官能团异构
互变异构
立体异构
构型异构 构象异构
顺反异构 对 映异构
立体异构
分子的构造式相同,但分子中的原子在 空间的排列方式不同。
顺反异构、对映异构、构象异构。
第二节 分子的平面模型表示法
费歇尔投影式 锯架投影式 纽曼投影式
HC
H
HO
CH3
OH
CH3
CH
H
H3C
OH
CH3
OH
-
对映异构体:分子的构造相同,但构型不
同,形成实物与镜象的两种分子,互称为
对映异构体。
二. 含有一个手性C化合物的对映异构
手性碳原子C*
COOH
C
H
OH
CH3
CH3 C*H乳C酸OOH
OH
手性分子
镜子
COOH
C
HO
H
CH3
对映异构体
COOH
COOH
2
H C NHCH3 CH3
(-)-伪麻黄碱
(1R,2R)
1
H C OH H3CHN C2 H
CH3 (+)-伪麻黄碱
(1S,2S)
说明:
1、n个不同C* , 产生 2n 个对映异构体
2、部分手性碳构型相同,部分不同的旋光 异构体互称“非对映体”(差向异构体)
3、非对映体的旋光性不同,其他物理和化 学性质也有差异。
Cl
Ⅲ
Ⅲ和Ⅰ构型相同,Ⅱ和Ⅰ(Ⅲ)构型不同。
操作法则
允许在纸平面上旋转180度 允许固定一个基团,其余三个依次轮换位置 允许中心碳上任意两基团对调偶数次
同分异构
同分异构
碳链(碳架)异构
构造异构
官能团位置异构 官能团异构
互变异构
立体异构
构型异构 构象异构
顺反异构 对 映异构
立体异构
分子的构造式相同,但分子中的原子在 空间的排列方式不同。
顺反异构、对映异构、构象异构。
第二节 分子的平面模型表示法
费歇尔投影式 锯架投影式 纽曼投影式
HC
H
HO
CH3
OH
CH3
CH
H
H3C
OH
CH3
OH
-
对映异构体:分子的构造相同,但构型不
同,形成实物与镜象的两种分子,互称为
对映异构体。
二. 含有一个手性C化合物的对映异构
手性碳原子C*
COOH
C
H
OH
CH3
CH3 C*H乳C酸OOH
OH
手性分子
镜子
COOH
C
HO
H
CH3
对映异构体
COOH
COOH
2
H C NHCH3 CH3
(-)-伪麻黄碱
(1R,2R)
1
H C OH H3CHN C2 H
CH3 (+)-伪麻黄碱
(1S,2S)
说明:
1、n个不同C* , 产生 2n 个对映异构体
2、部分手性碳构型相同,部分不同的旋光 异构体互称“非对映体”(差向异构体)
3、非对映体的旋光性不同,其他物理和化 学性质也有差异。
Cl
Ⅲ
Ⅲ和Ⅰ构型相同,Ⅱ和Ⅰ(Ⅲ)构型不同。
操作法则
允许在纸平面上旋转180度 允许固定一个基团,其余三个依次轮换位置 允许中心碳上任意两基团对调偶数次
第三章 立体化学讲解

优势构象
叔丁基是一个很大的基团,一般占据e键。
某些取代环己烷,张力特别大时,环 己烷的椅式构象会发生变形,甚至会 转变为船式构象
CH3
H
H3C
CH3
C
H
C(CH3)3 C(CH3)3
C(CH3)3 H
椅式
船式 优势构象
一般对优势构象的讨论,只是从取代 基的体积影响进行分析,对于烷基这类基 团来说是正确的。但有时非键合原子间的 其它作用力 如偶极-偶极间的电效应也会 影响分子的构象稳定性。
109o28'
60o
105o
3.3.1Baeyer张力学说
当碳原子的键角偏离109°28′时,便会产生一种 恢复正常键角的力量。这种力就称为张力。键角偏离 正常键角越多,张力就越大。
偏转角度=
109°28′内角
2
N=3 4 5 6 7
偏转角度
24o44’ 9o44’ 44’ -5o16’ -9o33’
…… n个C*
…………
AB+ B-
C+ C- C+ C-
D+D- D+D-D+D-D+D-
…………
2 4
8 16 …… 2n
例如: 一个C* 二个C* 三个C*
R\S RR\SS RS\SR RRR\SSS RRS\SRR RSR\SRS RSS\RRS
(2)非对映体
不呈镜影关系的旋光异构体为非对映异构体。非对映体具有不 同的旋光性,不同的物理性质和不同的化学性质。
立体异构体的定义:分子中的原子或原子团互相连接的 次序相同,但在空 间的排列方向不同而引起的异构体。
3.1 轨道的杂化和碳原子价键的方向性
第三章 立体化学

构象异构
HH
H
conformational HH H H H
异构现象:由化学键的刚性和方向性引起的
2
3.1 构象与构象分析
• 构象:
由单键旋转所形成的分子中基团在空间不同排列的立体 形象。
是立体异构中的一个重要结构层次,是在构造、构型确 定的基础上因为单键的旋转而产生的分子中的原子或原子团 在空间的排列。
CH3
H
H
CH3
H
CH3
H3CCH3
HCH3
H
H
CH3
对位交叉式
H
H
H
邻位交叉式
H H
HH
H3C H
H
全重叠式 部分重叠式
构象稳定性: 对位交叉式 > 邻位交叉式 > 部分重叠式 > 全重叠式 最稳定的对位交叉构象是优势构象,能量最低。。
7
正 丁 烷 构 象 分 析 势 能 图
8
注意:并不是任何化合物都是对位交叉构象所占比例 大于邻位交叉构象。
碳链(碳架)异构
构造异构
官能团位置异构
constitutional
OH OH OH
isomers
同
官能团异构 CH3CH2OH CH3 O CH3
分 异 构
enantiomers
configurational 对映异构
构型异构
顺反异构
非对映异构
立体异构
stereoisomers
diastereomers 光学异构( 非物象关系)
第三章 立体化学
Stereochemistry
• 立体化学(Stereochemistry)就是空间化学(1874) • 立体化学的任务:研究分子的立体形象及与立体形象相 联系的特殊物理性质和化学性质的科学。 • 有机立体化学
有机化学第三章立体化学基础(2024)

实例三
手性药物的合成。手性药物是指具有手性中心的药物分子。在合成手性药物时,需要利用 立体化学原理来控制产物的立体构型。例如,通过引入手性辅剂或利用不对称催化等方法 ,可以实现手性药物的高效合成。
22
06
2024/1/25
立体化学在药物设计中的重要性
23
药物活性与手性关系
手性对药物活性的影响
手性药物的两个对映异构体可能具有 不同的生物活性,其中一个可能具有 治疗效果,而另一个可能无效或有毒 。
手性中心判断方法
7
2024/1/25
03
观察碳原子连接的四个基团或 原子是否相同,若不相同则为 手性中心。
04
使用Cahn-Ingold-Prelog规则 (CIP规则)进行判断。
9
手性分子表示方法
2024/1/25
Fischer投影式
01
将碳链竖直表示,横前竖后,横向基团朝右,纵向基团朝上。
透视式
一个物体不能通过旋转和平移操作与其镜 像完全重合的性质。
对称性的定义
一个物体可以通过旋转和平移操作与其镜 像完全重合的性质。
手性与对称性的关系
手性是对称性的一个特例,即没有对称中 心或对称面的物体具有手性。
手性在化学中的应用
手性化合物在生命体系中具有重要的作用 ,如氨基酸、糖类等。
5
构型与构象
构型的定义
02
将碳链放平,基团朝向观察者方向。
Newman投影式
03
沿碳-碳键的键轴方向观察,将碳原子和与之相连的基团放在纸
平面上,其他基团则竖立在纸平面上。
10
2024/1/25
03
对称性与对称操作
11
对称元素及类型
手性药物的合成。手性药物是指具有手性中心的药物分子。在合成手性药物时,需要利用 立体化学原理来控制产物的立体构型。例如,通过引入手性辅剂或利用不对称催化等方法 ,可以实现手性药物的高效合成。
22
06
2024/1/25
立体化学在药物设计中的重要性
23
药物活性与手性关系
手性对药物活性的影响
手性药物的两个对映异构体可能具有 不同的生物活性,其中一个可能具有 治疗效果,而另一个可能无效或有毒 。
手性中心判断方法
7
2024/1/25
03
观察碳原子连接的四个基团或 原子是否相同,若不相同则为 手性中心。
04
使用Cahn-Ingold-Prelog规则 (CIP规则)进行判断。
9
手性分子表示方法
2024/1/25
Fischer投影式
01
将碳链竖直表示,横前竖后,横向基团朝右,纵向基团朝上。
透视式
一个物体不能通过旋转和平移操作与其镜 像完全重合的性质。
对称性的定义
一个物体可以通过旋转和平移操作与其镜 像完全重合的性质。
手性与对称性的关系
手性是对称性的一个特例,即没有对称中 心或对称面的物体具有手性。
手性在化学中的应用
手性化合物在生命体系中具有重要的作用 ,如氨基酸、糖类等。
5
构型与构象
构型的定义
02
将碳链放平,基团朝向观察者方向。
Newman投影式
03
沿碳-碳键的键轴方向观察,将碳原子和与之相连的基团放在纸
平面上,其他基团则竖立在纸平面上。
10
2024/1/25
03
对称性与对称操作
11
对称元素及类型
最新第三章立体化学(Stereochemistry)PPT

一、不对称碳、手性碳、 手性分子、对映体
1. 不对称碳:饱和碳原子上连有互不相同的 四个原子或原子团(用*表示)。
2. 手性:物质的分子和它的镜像不能重叠。
3. 手性分子:具有手性的分子。
4. 对映体:互为镜像关系,但不能完全重合 的一对异构体,互为对映体。他们都具有 旋光性。
LIYING
2021/1/20
OH L a c tic a c id 乳酸
第三章立体化学(Stereochemistry)
Locating a Stereocenter
Br
* C3HC2HC2HC2HC2HC C2HC2HC2HC3H
H
LIYING
2021/1/20
第三章立体化学(Stereochemistry)
Locating a Stereocenter
1848年
酒 石 酸 钠 铵 晶
巴斯德
体
LIYING
2021/1/20
Crystals of Sodium Ammonium Tartrate
第三章立体化学(Stereochemistry)
对映体 (Enantisomers)
❖Isomers that are non-superimposable
LIYING
2021/1/20
(+)
表示
[t
cl
右旋, (-) 表示 左旋
:旋光度;[]:比旋光度;t:温 度;:光波长;c:样品浓度,单 位g/ml;l:样品管长度,单位dm
第三章立体化学(Stereochemistry)
第二节 对映异构现象与 分子结构的关系
LIYING
2021/1/20
第三章立体化学(Stereochemistry)
第三章-立体化学
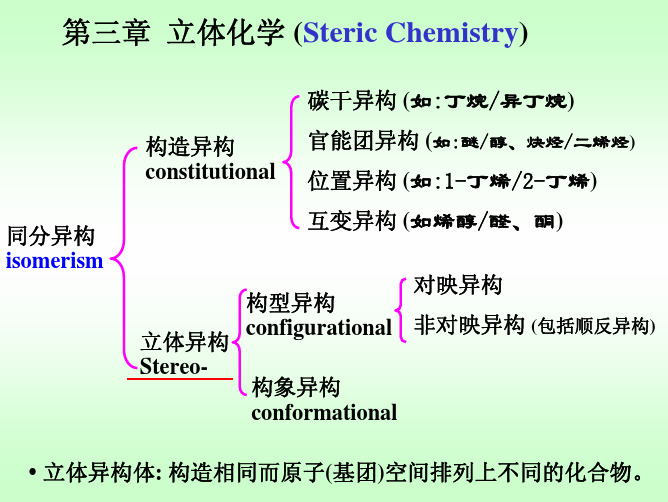
非对称分子和不对称分子为手性分子,具有旋光性, 能产生对映异构
手性分子的一般判断:
•有对称面或对称中心 •既无对称面也无对称中心
分子无手性 分子有手性
一、含一个手性中心的化合物
• 含手性碳的分子
例 乳酸:
COOH H OH
CH3
COOH HO H
CH3
HOOC
COOH
H C OH HO C H
注意: 1. 分子旋光度符号(+/-)和构型(R/S, D/L)之间没有简单关系 2. 含手性中心 ≠ 手性化合物: 如该化合物含对称中心, 对称面等 对称因素则为非手性
分子的对称元素:对称轴、对称面、对称中心和更迭对称轴
¾ 对称轴 (Cn):
Cl
H
C H
C
Cl
180° Cl
H
CC
H
Cl
分子旋转的角度为
H3C H
H
H
绕轴旋转180oC
H
CH3
H
H
CH3
H
H3C
H
Cl
Cl
i
ii
i = iii
Cl
H3C
H
H
H
H
CH3
Cl iii
分子的对称性:
) 具有对称面、对称中心或更迭对称轴的分子称为对称分子 ) 无对称面、对称中心,仅存在简单的对称轴的分子称为
非对称分子 ) 不含有任何对称元素的分子称为不对称分子。
• 立体异构体: 构造相同而原子(基团)空间排列上不同的化合物。
H2N
COOH
O
NH2
(S)−天冬酰胺
苦味
H2N
COOH
O
有机化学第三章立体化学基础

H
HO
CHO
C H2O H
R
H
HO
CHO
C H2O H
结论:当最小基团处于竖键位置时,其余三个基 团从大到小的顺序若为顺时针,其构型为R;反 之,构型为S。
判断基团大小的依据是我们已经熟悉的顺 序规则
OH
COOH
COOH
COOH
CH HOOC CH3
(S)-
CH
CH3
OH
(S)-
C H
HO CH3 (R)-
Cl
Cl
H
H
-
H
(二) 判别手性分子的依据
A.有对称面、对称中心、交替对称轴的分子均可 与其镜象重叠,是非手性分子;反之,为手性分子。
至于对称轴并不能作为分子是否具有手性的判据。
B.大多数非手性分子都有对称轴或对称中心, 只有交替对称轴而无对称面或对称中心的化合物是 少数。
∴既无对称面也没有对称中心的,一般 判定为是手性分子。
如果在两个棱镜之间放一个盛液管,里面装 入两种不同的物质。
亮
丙酸
α
暗
亮
乳酸
结论: 物质有两类:
(1)旋光性物质——能使偏振光振动面旋转的性质, 叫做旋光性;具有旋光性的物质,叫做旋光性物质。
(2)非旋光性物质——不具有旋光性的物质,叫做 非旋光性物质。
旋光性物质使偏振光旋转的角度,称为旋光度,
以“α”表示。
COOH
H CH3CH2 COOH
CH3
COOH H CH2CH3
CH3
CH3 H COOH
CH2CH3
S
S
S
S
试判断下列Fischer投影式中与(s)-2-甲基丁酸成对 映关系的有哪几个?
高等有机第三章立体化学ppt课件

结构解析与精修 利用直接法、帕特森函数等方法解析晶体结构,并通过最 小二乘法进行结构精修。
核磁共振波谱在确定结构中应用
核磁共振原理
利用核自旋磁矩在外磁 场中发生能级分裂,通 过射频脉冲激发核自旋 跃迁,产生核磁共振信 号。
数据收集与处理
通过调整射频脉冲频率 和磁场强度收集不同核 的核磁共振信号,并利 用计算机程序进行数据 处理和谱图分析。
糖类的立体化学与生物活 性
糖类的立体构型对其生物活性具有重要影响, 如多糖的免疫调节作用、糖蛋白的识别作用等。
生物活性小分子中立体化学问题
手性小分子的生物活性
许多生物活性小分子具有手性中心,其不同的立体构型可能会导致不同的生物活性。
小分子与生物大分子的相互作用
生物活性小分子如激素、神经递质等,与生物大分子如受体、酶等的相互作用具有立体 选择性。
醇在酸性条件下失去质子形成碳正离子,然后发生1,2-重排生成更稳定的碳正离子,最后捕 获质子生成重排产物。
Pinacol重排
二醇在酸性条件下失去一分子水形成碳正离子,然后发生1,2-重排生成醛或酮。
立体化学结果
重排反应的立体化学结果取决于底物的构型和重排过程中涉及的中间体的稳定性。
影响立体化学反应因素
拉曼光谱原理
利用光与分子相互作用产生的拉 曼散射光谱进行分析。
结构解析与验证
根据特征峰位、峰强等参数推断 分子结构中的官能团和化学键信 息,并通过与其他实验数据相互
验证。
其他实验方法及技术
圆二色光谱
01
用于研究生物大分子(如蛋白质)的二级结构和构象变
化。
质谱技术
02
用于确定化合物的分子量和元素组成,以及研究分子间
底物结构
核磁共振波谱在确定结构中应用
核磁共振原理
利用核自旋磁矩在外磁 场中发生能级分裂,通 过射频脉冲激发核自旋 跃迁,产生核磁共振信 号。
数据收集与处理
通过调整射频脉冲频率 和磁场强度收集不同核 的核磁共振信号,并利 用计算机程序进行数据 处理和谱图分析。
糖类的立体化学与生物活 性
糖类的立体构型对其生物活性具有重要影响, 如多糖的免疫调节作用、糖蛋白的识别作用等。
生物活性小分子中立体化学问题
手性小分子的生物活性
许多生物活性小分子具有手性中心,其不同的立体构型可能会导致不同的生物活性。
小分子与生物大分子的相互作用
生物活性小分子如激素、神经递质等,与生物大分子如受体、酶等的相互作用具有立体 选择性。
醇在酸性条件下失去质子形成碳正离子,然后发生1,2-重排生成更稳定的碳正离子,最后捕 获质子生成重排产物。
Pinacol重排
二醇在酸性条件下失去一分子水形成碳正离子,然后发生1,2-重排生成醛或酮。
立体化学结果
重排反应的立体化学结果取决于底物的构型和重排过程中涉及的中间体的稳定性。
影响立体化学反应因素
拉曼光谱原理
利用光与分子相互作用产生的拉 曼散射光谱进行分析。
结构解析与验证
根据特征峰位、峰强等参数推断 分子结构中的官能团和化学键信 息,并通过与其他实验数据相互
验证。
其他实验方法及技术
圆二色光谱
01
用于研究生物大分子(如蛋白质)的二级结构和构象变
化。
质谱技术
02
用于确定化合物的分子量和元素组成,以及研究分子间
底物结构
有机化学第三章 立体化学

两种标记方法绝大多数情况下一致,即顺式 就是Z 式,反式就是E式。但有时却刚好相反。
H C H3 CO O H C H3 H C H3 C H3 CO O H
C=C
C=C
_ _ _ _ 顺 2 甲基 2 丁烯酸 _ _ _ _ 2 甲基 2 丁烯酸 (E)
_ _ _ _ 反 2 甲基 2 丁烯酸 _ _ _ _ (Z) 2 甲基 2 丁烯酸
1、测得一个葡萄糖溶液的旋光角为+3.4°,而 葡萄糖的比旋光度为+ 52.7(°)· ml· g-1· dm-1,若 盛液管长度为1dm,计算出葡萄糖的浓度为
3.4 1 B 0.0646 ( g.m l ) m· l 52.7 1
同样也可通过已知旋光度物质的浓度而求得该 物质的比旋光度。
(-)-麻黄碱 (1R,2S)
2
1
H C OH H C NHCH3 CH3
(+)-麻黄碱 (1S,2R)
2
1
HO C H H C NHCH3 CH3
2
1
H C OH H3CHN C H CH3
(+)-伪麻黄碱
(1S,2S)
2
1
(-)-伪麻黄碱 (1R,2R)
说明:
1、n个不同C* , 产生 2n 个对映异构体
L-(-)-甘油醛
CHO HO H CH2OH
Br2/H2O
COOH HO H CH2OH
L-(-) -甘油醛
L-(+) -甘油酸
说明:D,L-构型与旋光方向无简单对应关系, 旋光方向是由旋光仪实际测得的。
(二) R、S 标记法
(序旋标记法)
1.排序:将四个基团按顺序规则排序,a>b>c>d。 2.定向:从最小基团d的对面进行观察,C-d键。
H C H3 CO O H C H3 H C H3 C H3 CO O H
C=C
C=C
_ _ _ _ 顺 2 甲基 2 丁烯酸 _ _ _ _ 2 甲基 2 丁烯酸 (E)
_ _ _ _ 反 2 甲基 2 丁烯酸 _ _ _ _ (Z) 2 甲基 2 丁烯酸
1、测得一个葡萄糖溶液的旋光角为+3.4°,而 葡萄糖的比旋光度为+ 52.7(°)· ml· g-1· dm-1,若 盛液管长度为1dm,计算出葡萄糖的浓度为
3.4 1 B 0.0646 ( g.m l ) m· l 52.7 1
同样也可通过已知旋光度物质的浓度而求得该 物质的比旋光度。
(-)-麻黄碱 (1R,2S)
2
1
H C OH H C NHCH3 CH3
(+)-麻黄碱 (1S,2R)
2
1
HO C H H C NHCH3 CH3
2
1
H C OH H3CHN C H CH3
(+)-伪麻黄碱
(1S,2S)
2
1
(-)-伪麻黄碱 (1R,2R)
说明:
1、n个不同C* , 产生 2n 个对映异构体
L-(-)-甘油醛
CHO HO H CH2OH
Br2/H2O
COOH HO H CH2OH
L-(-) -甘油醛
L-(+) -甘油酸
说明:D,L-构型与旋光方向无简单对应关系, 旋光方向是由旋光仪实际测得的。
(二) R、S 标记法
(序旋标记法)
1.排序:将四个基团按顺序规则排序,a>b>c>d。 2.定向:从最小基团d的对面进行观察,C-d键。
有机化学 第三章 立体化学

[t
cl
式中:——测量时所采用的光波波长; t ——测量时的温 度;α——由仪器测得的溶液的旋光度;l ——盛液管的长度,单 位为dm(1dm=10cm); C ——溶液的浓度,单位为g.mL-1。
2020/3/27
15
物质的比旋光度与测量时的温度、光源的波长以 及所使用的溶剂有关。表示比旋光度时,需要标明。
conformational
2020/3/27
2
例如:
HO
COOH HOOC
OH
H NH2
HO
(+)-多巴
(造成粒状白细胞减少)
H2N H OH
(-)-多巴 (抗帕金森病)
2020/3/27
3
举例:反应停事件 于1956年在原西德上市,主要治疗妊娠 呕吐反应,临床疗效明显,因此迅速流行于欧洲、亚洲(以日本 为主)、北美、拉丁美洲的17个国家。到1960年左右,上述国家 突然发现许多新生儿的上肢、下肢特别短小,其形状酷似“海 豹”。部分新生儿还伴有心脏和消化道畸形、多发性神经炎等。 大量的流行病学调查和大量的动物实验证明这种“海豹肢畸形” 是由于患儿的母亲在妊娠期间服用反应停所引起。“海豹肢畸形” 患儿在日本大约有1000名,在西德大约有8000名!全世界超过1 万人!这就是著名的“反应停事件”。
CH3
H3C 无对称面
1,2二甲基环丙烷
对称面的对称操作是反映(即照镜子)。
2020/3/27
19
(乙)对称中心
设想分子中有一个点,从分子中任何一个原子出 发,向这个点作一直线,再从这个点将直线延长出去, 则在该点前一线段等距离处,可以遇到一个同样的原 子,这个点就是对称中心.
Cl
H
有机化学-第3章-立体化学

复习烷烃构象的表示方法
透视式 锯架式
H C
H H
H C
H H
H
HH H HH
H C
H H
H CH H
H H
H H
HH
Newman投影式
HH
H H
H H
H
H
H
H
H
H
乙烷重叠式和交叉式构象的透视式、锯架式和Newman投影式
➢手性分子的表示法
C2H5
CH3
CH Br
CH3
H C C2H5 Br
•一对对映体的透视式表示法 •直观,但书写麻烦
COOH
COOH
H3CH C OH 实物
镜子
HO C HCH3 镜象
乳酸分子的一对对映体
四面体碳
连接四个不同原子(团)
C
§3.2 偏振光和分子的旋光性(P61)
旋光度:a
平面偏振光:通过Nicol棱镜后,只在一个方向上振动的光 旋光性(光学活性, optical activity):物质使平面偏振光发生旋
OH
观察
OH CHO CH2OH
H C CHO 为顺时针方向
CH2OH
R-型
四、 从Fischer投影式判断构型
CH3 H OH
CH=CH2
•S
§3.7 相对构型和绝对构型 -- D/L构型标记法(P70)
复习:R/S标记法是根据什么来标记的?
答:根据手性碳原子上所连的四个原子或 原子团在空间的实际排列方式来标记的。
如何依据结构判断分子是否有旋光性?
与分子的对称性有关——需要考虑的对 称元素主要有以下三种:
(甲) 对称轴(Cn)
以设想直线为轴旋转360。/ n,得到与原分子相同的分子,该直 线称为n重对称轴axis symmetry (又称Cn阶对称轴)
Chapter3 立体化学(二)

α
L x C
比旋光度
溶液的浓度(g/ml)
波长 (钠光D)
盛液管长度(分米dm)
当物质溶液的浓度为1g/ml,盛液管的长度为1分
米时,所测物质的旋光度即为比旋光度。若所测物质
为纯液体,计算比旋光度时,只要把公式中的C换成
液体的密度d 即可。
最常用的光源是钠光(D),λ=589.3nm, 所
测得的旋光度记为 [α ] D 所用溶剂不同也会影响物质的旋光度。因此在 不用水为溶剂时,需注明溶剂的名称。
• 对映体的一般物理性质(熔点,沸点,相对密度...,以
及光谱)都相同,只有对偏振光的作用不同.
偏正光的形成
偏正光的旋转
旋光性的表示方法: • 旋光性--能旋转偏正光的振动方向的性质叫旋光性 • 旋光性物质(或叫光活性物质)--具有旋光性的物质. • 右旋物质--能使偏正光的振动方向向右旋的物质. 通常用 “d” 或 “+” 表示右旋. • 左旋物质--能使偏正光的振动方向向左旋的物质. 通常用 “ ” 或 “-” 表示左旋. l • 旋光度-- 偏正光振动方向的旋转角度.用“”表 示. •在有机化学中,凡是手性分子都具有旋光性(有些手 性分子旋光度很小);而非手性分子则没有旋光性.
有机化学 Organic Chemistry 第三章 立体化学
教 授
制作:李德江
三峡大学化生学院
立体化学
• 立体化学是有机化学的重要组成部分.它的主要内 容是研究有机化合物分子的三度空间结构(立体结 构),及其对化合物的物理性质和化学反应的影响.
立体异构体——分子的构造(即分子中原子相互联结
的方式和次序)相同,只是立体结构(即分子中原子在 空间的排列方式)不同的化合物是立体异构体.
L x C
比旋光度
溶液的浓度(g/ml)
波长 (钠光D)
盛液管长度(分米dm)
当物质溶液的浓度为1g/ml,盛液管的长度为1分
米时,所测物质的旋光度即为比旋光度。若所测物质
为纯液体,计算比旋光度时,只要把公式中的C换成
液体的密度d 即可。
最常用的光源是钠光(D),λ=589.3nm, 所
测得的旋光度记为 [α ] D 所用溶剂不同也会影响物质的旋光度。因此在 不用水为溶剂时,需注明溶剂的名称。
• 对映体的一般物理性质(熔点,沸点,相对密度...,以
及光谱)都相同,只有对偏振光的作用不同.
偏正光的形成
偏正光的旋转
旋光性的表示方法: • 旋光性--能旋转偏正光的振动方向的性质叫旋光性 • 旋光性物质(或叫光活性物质)--具有旋光性的物质. • 右旋物质--能使偏正光的振动方向向右旋的物质. 通常用 “d” 或 “+” 表示右旋. • 左旋物质--能使偏正光的振动方向向左旋的物质. 通常用 “ ” 或 “-” 表示左旋. l • 旋光度-- 偏正光振动方向的旋转角度.用“”表 示. •在有机化学中,凡是手性分子都具有旋光性(有些手 性分子旋光度很小);而非手性分子则没有旋光性.
有机化学 Organic Chemistry 第三章 立体化学
教 授
制作:李德江
三峡大学化生学院
立体化学
• 立体化学是有机化学的重要组成部分.它的主要内 容是研究有机化合物分子的三度空间结构(立体结 构),及其对化合物的物理性质和化学反应的影响.
立体异构体——分子的构造(即分子中原子相互联结
的方式和次序)相同,只是立体结构(即分子中原子在 空间的排列方式)不同的化合物是立体异构体.
