第十二章-糖类
2020春九年级化学第十二章导学案及单元测试+答案

人类重要的营养物质学习目标:1、能说出人体所需要的六大营养素。
2、知道蛋白质、糖类、油脂、维生素与人体健康的关系。
学习过程:预习导学:知识点1、六大营养素【阅读】课本90页的相关内容,填写下列空白:1、营养素包括、、、、、等六大类。
知识点2、蛋白质【阅读】课本90-92页与蛋白质有关的内容,填写下列空白:2、是构成细胞的基本物质。
蛋白质的主要功能是构造机体、修复组织。
富含蛋白质的食物有、、、等。
3、血红蛋白是人体中的输送者,与一氧化碳的结合能力很强,若空气中含有一氧化碳时容易发生中毒。
4、蛋白质遇到、、等会发生变质。
5、某洗衣粉不仅能去除汗渍,而且有较强的除血渍、奶渍等蛋白质污渍,这是因为在洗衣粉中加了()A 碳酸钠B 烧碱C 蛋白酶D 淀粉酶知识点3、糖类【阅读】课本93页与糖类有关的内容,填写下列空白:6、糖类是维持人体正常活动所需的营养素之一。
糖是提供人体的主要物质。
能提供糖类的食物有、、等。
7、蔗糖的化学式为,葡萄糖的化学式为。
葡萄糖在酶的作用下产生和,同时放出。
知识点4、油脂【阅读】课本94页与油脂有关的内容,我发现:8、油脂包含和,它放出的热量比同质量的糖类要(填高或低),是重要的能源备用物质。
9、含油脂的食物有、、、。
知识点5、维生素【阅读】课本94页与维生素有关的内容,我知道:10、维生素的作用是,和。
11、富含维生素的食物有。
12、缺乏维生素将使人体患病。
缺乏维生素A会引起,缺乏维生素C会引起。
【反思与小结】:学完本节课我知道了有效训练:1、下列物质不属于糖类的是()A、纤维素B、淀粉C、酒精D、葡萄糖2、医学上所称的“低血糖”,是指人体中缺少()A、矿物质B、纤维素C、蔗糖D、葡萄糖3、检验食物中是否含有淀粉可以用()A、pH试纸B、酚酞C、石蕊D、碘的水溶液4、下列说法正确的是()A、碳水化合物就是碳和水形成的混合物B、凡是糖类物质都是甜的C、油脂是指油和脂,“油”一般是植物脂肪,“脂”指的是动物脂肪D、油脂也是C、H、O三种元素组成的,它属于碳水化合物5、下列说法正确的是()A、有甜味的物质都是糖类B、吸烟使人精神振奋,有益健康C、胃酸过多可以服用稀氢氧化钠溶液D、纤维素属于糖类6、下列物质中不含蛋白质的是()A、虾B、豆腐C、血液D、矿泉水7、下列对蛋白质的认识不正确的是()A、蛋白质是构成人体细胞的基础物质B、人的头发主要成份是蛋白质C、蛋白质能被人的小肠直接吸收D、如果人体摄入蛋白质量不足,会引起发育迟缓、体重减轻、贫血等8、发芽霉变的花生不能食用,是因为其中含有()A、黄曲霉素B、乙醇C、甲醛D、维生素9、下列说法正确的是()A、维生素是由生命体产生的,分子结构复杂,人工不可能合成B、喜欢吃的食品多吃点,不喜欢吃的食品不吃,不会影响身体健康C、食用凉拌蔬菜,有利于获得较多的V CD、维生素不是营养品,故缺少维生素不会引起营养不良10、青菜中一般不含有()A、水B、纤维素C、维生素D、蛋白质11、我国科学家于1965年9月在世界上第一个用化学方法合成了具有生命活力的蛋白质——结晶牛胰岛素,它的原料应该是()A、葡萄糖B、氨基酸C、维生素D、油脂12、连线题蔬菜、水果蛋白质备用能源花生、牛油糖类主要的供能物质米面、土豆油脂构成细胞的基本物质鸡蛋、牛奶维生素维持身体健康自我测评:1.鸡蛋、鱼和牛奶提供的主要营养素是()A.糖类 B.油脂 C.蛋白质 D.无机盐2.下列物质中,不能向人体提供能源的是()A.糖类 B.油脂 C.蛋白质 D.无机盐3.下列物质中,不属于糖类的是()A.麦芽糖 B.淀粉 C.蔗糖D.蛋白质4.从对人体有害的角度考虑,你认为炒锅用下列哪种材料最好()A.铝 B.铁 C.铜 D.铝合金5.“食品安全无小事”,下列做法不会导致食品对人体健康有害的是()A.用干冰保存容易变质的食物 B.用硫磺熏制白木耳粉丝等食品C.用甲醛浸泡易腐烂的食品D.用工业食盐腌制泡菜6.脂肪成分的获得主要来自()A.豆类、肉类、奶类制品 B.猪、牛、羊的油、花生油、豆油C.粮食作物、豆类、植物的根茎 D.蔬菜、水果及植物种子7.下列物质不会引起人体中毒的是( )A.一氧化碳 B.亚硝酸钠(NaNO2) C.甲醛水溶液 D.葡萄糖8.5月31日是“世界无烟日”。
糖类习题

第十二章糖类习题
一、选择题
1、有一组化合物可以用银氨溶液鉴别的是()
A. 葡萄糖和果糖
B. 葡萄糖和麦芽糖
C. 麦芽糖和蔗糖
D. 麦芽糖和纤维二糖
2、下列哪组糖产生相同的糖脎()
A.乳糖、葡萄糖、果糖B.葡萄糖、麦芽糖、果糖C.甘露糖、葡萄糖、果糖D.蔗糖、果糖、葡萄糖E.半乳糖、甘露糖、葡萄糖
3、区别葡萄糖和果糖最好的方法是()
A. Tollen试剂
B. Fehling试剂
C. 班氏试剂
D. 溴水
E. 成脎
4、下列化合物不能使溴水褪色的是()
A. 果糖
B. 葡萄糖
C. 丙烯
D. 苯酚
E. 丙炔
5、下列化合物哪些具有还原性()
A. 半乳糖
B. 果糖
C. 甘露糖
D. 蔗糖
E. 麦芽糖
6、下列试剂可用来区分甲醛和苯甲醛的是()
A. 溴水
B. 银氨溶液
C. 苯肼
D. 斐林试剂
E. 饱和NaHSO3溶液
7、下列试剂可用来区分葡萄糖和果糖的是()
A. 溴水
B. 银氨溶液
C. 苯肼
D. 斐林试剂
E. 饱和NaHSO3溶液。
12糖类

第二节 双 糖
二、非还原性双糖
(三) 化学性质
结构特征 化性特征
因为蔗糖分子中都没有苷羟基,所 以不具有还原性和变旋现象 。
化学反应
第十二章 糖 类
第二节 双 糖
二、非还原性双糖
(三) 化学性质
结构特征 化性特征
1.不能与托伦试剂、斐林试剂和班氏试剂反应。 2.不能形成糖脎和糖苷。 3.在稀酸或酶的作用下,水解生成两分子单糖。
多糖分子中虽然有苷羟基,但因分子量很大,因此它们 没有还原性和变旋光现象。多糖可以水解,但要经历多步过 程,水解的最终产物是葡萄糖。
第十二章 糖 类
第三节 多 糖
一、淀粉
(一)淀粉的结构 淀粉是由许多α -D-葡萄糖分子脱水缩合而成的多糖。
根据结构不同, 淀粉可分为
直接淀粉
支链淀粉
第十二章 糖 类
CHO HO H
H OH HO H
H OH CH2OH
D-(-)-艾杜糖
CHO H OH H OH HO H H OH
CH2OH
D-(-)-古罗糖
CHO HO H HO H
H OH H OH
CH2OH
D-(+)-甘露糖
CHO H OH H OH H OH H OH
CH2OH
D-(+)-阿洛糖
CHO OH HO H HO H H OH
第十二章 糖 类
第一节 单 糖
单糖的鉴别方法:
1.常用莫立许试剂来鉴别糖的存在。 2.用托伦试剂、斐林试剂和班氏试剂来鉴别还原糖和 非还原糖。 3.利用生成糖脎的晶形和熔点不同来鉴别不同的糖。 4.用塞利凡诺夫试剂来鉴别醛糖和酮糖。
第十二章 糖 类
第一节 单 糖
12糖类的生物合成

多分支,提高水 溶性,利于储存;
多处磷酸化酶作 用点,提高效率, 迅速提供能量
2、变位 G-1-P 磷酸葡萄糖变位酶
G-6-P
3、G的生成(只存在于肝、肾中,肌组织中没有此步骤)
G-6-
G
P
葡萄糖-6-磷酸酶
糖原的合成与分解代谢
UDP
Gn+1
Pi
Gn
糖原合酶 分支酶
UDPG
糖原磷酸化酶
Gn
• 酵解途径与糖异生途径多数反应是共有 的,除了酵解途径中3个不可逆反应。 糖异生方向
1.丙酮酸 磷酸烯醇式丙酮酸 2.1,6-双磷酸果糖 6-磷酸果糖 3.6-磷酸葡萄糖 葡萄糖
丙 酮
丙酮酸羧化酶
草 酰 磷酸烯醇式丙酮酸羧化激酶
酸
乙
CO2 ATP ADP+Pi酸 GTP GDP CO2
磷酸 烯醇 式丙 酮酸
3.调节酸碱平衡
长期饥饿时,肾糖异生增加,排氢保钠。 有利于维持酸碱平衡。
谷氨酰胺
谷氨酸
H2O
NH3
+
原尿H+
NH4+
-酮戊二酸 NH3
糖异生
糖异生的调节
1.激素的调节作用
6-磷酸果糖和1,6-双磷酸果糖之间,糖酵解和糖异 生之间
肝脏:胰高血糖素 腺苷酸环化酶
(无活性) 腺苷酸环化酶(活性)
ATP
2 胰高血糖素,主要的升血糖激素。
3 糖皮质激素,可引起血糖升高,肝糖原增加。
4 肾上腺素,强有力的升血糖激素。
• 胰岛素:降低血糖的唯一激素 1、促进G转运入细胞,加强利用 2、增强磷酸二酯酶的活性,降低cAMP水平,
激活糖原合酶,抑制磷酸化酶
第十二章 糖 类

一、单糖的结构 (一)葡萄糖的结构 1.开链式
2.氧环式
H H HO H H
OH C C C C C CH2OH OH H OH O
H C H HO H H C C C C
O OH H OH OH
HO H HO H H
H C C C C C CH2OH OH H OH O
CH2OH
(四)半乳糖 半乳糖为结晶。半乳糖与葡萄糖结合成乳 糖存在于哺乳动物的乳汁中。也是脑苷和 神经节苷的组分,这两种苷存在于大脑和 神经组织中。 (五)氨基糖 单糖分子中醇羟基被氨基或烃氨基取代而 成的化合物称为氨基糖。氨基糖常以结合 态存在于体内的粘多糖中。链霉素、软骨 素和甲壳素中都含有氨基糖。
2.绞股蓝皂苷 绞股蓝为葫芦科多年生草质藤本植物。它 含有多种生物活性物质,皂苷为其主要活 性成分。绞股蓝皂苷有抗癌作用,临床用 于20多种癌症的治疗,其抗癌机理既直接 作用与癌细胞,又调节了机体的免疫功能。 研究还表明,长期饮用绞股蓝提取物可促 进肝脏核酸和蛋白质的合成,对大脑中枢 有良好的兴奋和镇静双向调节作用,并且 有抗疲劳、抗衰老和降血脂等功能。
第十二章 糖 类
许昌卫生学校
郑学锋
学习目标 葡萄糖、果糖、核糖、脱氧核糖的哈沃斯 结构,双糖和多糖的结构。 单糖重要化学性质的化学现象,还原糖和 非还原糖的含义。
第一节 概述
糖类,又做碳水化合物。是自然界中存在最 多的一类有机物。植物干重的50%~80%为 糖类化合物。糖是重要的食物之一,生物体 维持生命活动所不可缺少的物质之一。 糖类是绿色植物吸收空气中的CO2,经过复杂 的光合作用而产生的。
(二)果糖 纯净的果糖是无色棱形晶体,易溶于水, 可溶于乙醚及乙醇中。 (三)核糖和脱氧核糖 核糖为片状结晶。核糖是核糖核酸(RNA) 的重要组成部分。脱氧核糖是脱氧核糖核 酸(DNA)的重要组成部分。RNA参与蛋白 质和酶的生物合成过程,DNA是传送遗传 密码的要素。它们是人类生命活动中非常 重要的物质。
第十二章糖类

(பைடு நூலகம்)
CH2OH O OH H H H OH H OH H OH
α-D-(+)-吡喃葡萄糖 D-(+)-葡萄糖
β-D-(+)-吡喃葡萄糖
在哈沃斯式中,成环的原子在同一 平面上,粗线表示环平面向前的边缘, 细线表示向后的边缘。成环的碳元素 符号不写出,连在手性碳原子上的 H 也可略去。原来在投影式左边的羟基, 处于环平面上方;原来在投影式右边 的羟基,处于环平面下方(即“左上 右下”);而 C6 上羟甲基在环平面上 方者为 D- 型。在 D- 型糖中,半缩醛羟 基在环下者为 α- 型,在环上者为 β- 型。
COOH CHO COOH H OH H OH H OH Br -H O HO H HO H 稀 HNO 2 2 3 HO H H OH H OH H OH H OH H OH H OH CH OH CH OH COOH 2 2
葡萄糖酸
葡萄糖
葡萄糖二酸
葡萄糖在肝内,在酶的作用下能氧 化成葡萄糖醛酸,即葡萄糖末端上的 羟甲基被氧化成羧基。葡萄糖醛酸的 结构式如下:
但是,哈沃斯式把环当作平面,把 原子和原子团垂直的排布在环的上、 下方,仍然不能真实的反映出糖的立 体结构。环己烷是以船式和椅式两种 构象存在,葡萄糖的吡喃环型结构, 就相当于环己烷的一个亚甲基被氧原 子取代,其构象式应该是类似的。葡 萄糖的船式构象极不稳定,只有椅式 构象能稳定存在。
CH OH 2 O H O H H e H H O OH a OH H
CHO COOH H OH O OH H HO H H OH H H OH H OH H OH OH COOH 葡萄糖醛酸 H
葡萄糖醛酸的药名叫“肝泰乐”。
(三)成酯反应 单糖环状结构中的羟基都可酯化。 在生物体内重要的是糖的磷酸酯, 葡萄糖在代谢过程中经磷酸酯化转 变为葡萄糖-1-磷酸酯(俗称1-磷酸 葡萄糖)和葡萄糖-6-磷酸酯(6-磷 酸葡萄糖)。在酶的作用下,可相 互转变。
初中化学第十二章知识点(精华版)

第十二单元化学与生活课题一、人类重要的营养物质1、六大营养素:蛋白质、糖类、油脂(脂肪)、维生素、无机盐和水(无机盐和水可被人体直接吸收)其中能放出能量的是糖类、脂肪、蛋白质2、蛋白质:①功能:是构成细胞的基本物质,是机体生长的主要原料②蛋白质的变性:破坏蛋白质的结构,使其变质③引起变质的因素:物理:高温、紫外线化学:强酸、强碱、甲醛、重金属盐(Ba2+、Hg2+、Cu2+、Ag+等)[注]甲醛可使蛋白质变质,但利用这个性质,可用甲醛水溶液(福尔马林)制作动物标本,使标本长期保存3、糖类:是生命活动的主要供能物质(60%—70%)①组成:由C、H、O三种元素组成。
糖类又叫做碳水化合物②常见的糖:a.淀粉,存在于植物种子或块茎中,如稻、麦、马铃薯等b.葡萄糖C6H12O6(人体可直接吸收的糖)c.蔗糖:生活中白糖、冰糖、红糖的主要成分是蔗糖4、植物油脂称油,动物油脂称脂肪。
脂肪的功能:提供大量能量(39.3KJ/g),是维持生命活动的备用能源。
5、维生素是人和动物为了维持正常的生理功能而必须从食物中获得的一类微量有机物质,在人体生长、代谢、发育过程中发挥着重要的作用。
存在于水果、蔬菜等食物中。
缺维生素A:夜盲症;缺维生素C:坏血症6、无机盐是存在于体内和食物中的矿物质营养素,人体已发现有20余种必需的无机盐,其中含量较多的为钙、磷、钾、钠、氯、镁、硫七种7、CO中毒机理:血红蛋白与CO结合能力比与O2结合能力强200倍,因血红蛋白无法输送氧气而导致缺氧而死8、吸烟危害:CO、尼古丁、焦油等课题2化学元素与人体健康1、组成人体的元素①常量元素(11种):在人体中含量>0.01%,O>C>H>N>Ca>P>K>S>Na>Cl>Mg②微量元素:在人体中含量<0.01%,如Fe、Zn、Se、I、F等几种微量元素对人体的作用:元素对人体的作用对人体的影响Fe血红蛋白的成分,能帮助氧气的运输缺铁会引起贫血Zn影响人体发育缺锌会引起食欲不振,生长迟缓,发育不良Se(硒)有防癌、抗癌作用缺硒可能引起表皮角质化和癌症。
第十二章 糖类

正常人空腹血糖的浓度为3.9~6.1mmol/L。
第十二章 糖类
第一节 单糖
第二节 二糖
一、二糖的概念和分类
二、常见的二糖
杨艳杰 漯河医学高等专科学校
第十二章 糖类
第二节 二糖
一、二糖的概念和分类
二糖可看成是2分子单糖间脱水缩合以苷键相连的产物。 根据结构中是否有苷羟基可分为 还原性二糖 非还原性二糖
第十二章 糖类
第一节 单糖
第一节 单糖
四、常见的单糖
(一)D-葡萄糖 (二)D-果糖 间产物。 (三)D-核糖和D-2-脱氧核糖 核糖和脱氧核糖与某些含 氮杂环化合物形成核糖核苷和脱氧核糖核苷,再经磷酸酯化 形成核苷酸,核苷酸是组成核酸的基本单位。 存在于人体血液中的葡萄糖称为血糖。 果糖磷酸酯是体内糖代谢过程中重要的中
二、常见的二糖
(一)麦芽糖
6 5 4 6
CH2OH O
1 2 4
CH2OH O
1
苷羟基
还原糖
OH
3
OH
3 2
~HOH
OH
O
α -1,4-苷键
OH
OH
α-D-吡喃葡萄糖 第十二章 糖类 第二节 二糖
D-吡喃葡萄糖
第二节 二糖
(二)乳糖
6
OH
4
5
C H 2O H O OH
3 1 2
β -1,4-苷键
O
OH
1
OH
OH
OH
H
H
OH
H
OH
α-D-(+)-吡喃葡萄糖
β-D-(+)-吡喃葡萄糖
HO
e
HO HO
CH2OH O H OH
生物化学及分子生物学(人卫第八版)-第12章-物质代谢的联系与调节1

脂酸合成
氨基酸代谢 嘌呤合成 嘧啶合成 核酸合成
乙酰辅酶A羧化酶
谷氨酸脱氢酶 谷氨酰胺PRPP酰胺 转移酶 天冬氨酸转甲酰酶 脱氧胸苷激酶
柠檬酸,异柠檬酸
ADP,亮氨酸,蛋氨酸
长链脂酰CoA
GTP,ATP,NADH AMP,GMP CTP,UTP
dCTP,dATP
dTTP
目录
2.代谢途径的起始物或产物通过变构调节影响 代谢途径 催化亚基 变构酶 调节亚基
调节某些细胞的代谢及功能,并通过各种激素的互相协
调而对机体代谢进行综合调节。
目录
一、细胞水平的代谢调节主要调节 关键酶活性
• 细胞水平的代谢调节主要是酶水平的调节。 • 细胞内酶呈隔离分布。 • 代谢途径的速度、方向由其中的关键酶(key enzyme)的活性决定。
• 代谢调节主要是通过对关键酶活性的调节而
各种物质代谢之间互有联系,相互依存。
目录
二、机体物质代谢不断受到精细调节
内外环境 不断变化 影响机体代谢
适应环境 的变化
机体有精细的调节 机制,调节代谢的 强度、方向和速度
目录
三、各组织、器官物质代谢各具特色
结构不同 不同的组 织、器官 酶系的种类、 含量不同 代谢途径不同、 功能各异
目录
四、各种代谢物均具有各自共同的 代谢池
进行调节,这种调节称为原始
调节或细胞水平代谢调节。
目录
高等生物 —— 三级水平代谢调节
• 细胞水平代谢调节
• 激素水平代谢调节
高等生物在进化过程中,出现了专司调节功能的内
分泌细胞及内分泌器官,其分泌的激素可对其他细胞发
挥代谢调节作用。
• 整体水平代谢调节
在中枢神经系统的控制下,或通过神经纤维及神经 递质对靶细胞直接发生影响,或通过某些激素的分泌来
第十二章 添加剂(二)--甜味剂及其测定

(3)非洲竹芋甜素 (Thaumation)
又名沙马丁,是从西非植物非洲竹芋的 果实中提取出来的甜味剂。 它具有增加风味、掩蔽异味、甜度高低 营养等优点,可广泛用于食品、医药、 化妆yle公司已生产出这 种甜味剂,商品名为Tatalin。
(四)化学合成甜味剂
蜜饯中添加糖精钠的目的
掩蔽果胚中原有的酸味 收敛作用,是表面干燥 一般添加量450-1000mg/kg
5 糖精钠的测定方法
按我国目前卫生标准规定有酚磺酞比色 法及紫外分光光度法。 (1)酚磺酞比色法 样品经除去蛋白质、果胶、CO2、 酒精等,在酸性条件下,用乙醚提取、 分离糖精钠,然后与酚和硫酸在175℃作 用生成酚磺酞,再与氢氧化钠反应,生 成红色化合物,用分光光度比色,定量。
2 复合甜味剂的优点
(1)协同增效,降低成本 由于甜味剂之间的协同增效作用,甜度超 过两种甜味剂的总和而成倍的增加。 例如: 以自身甜度大、具有很好的甜味协同作用的果 糖为例,10℅的果糖和蔗糖的混合液 (F\S=60/40)比10℅的蔗糖水溶液的甜度高 30℅; 而ACK和其它甜味剂混合使用也有明显的增效作 用,
其甜度一般为蔗糖的350-400倍. 由于糖精没有营养价值,仅在棒冰等中 使用. 但对糖尿病患者,当用量不超过总重量 的0.15‰时使用糖精是比较适宜的。
(三)甜味剂—糖精钠的测定
1 人工合成甜味剂在食品卫生标准中
已规定了使用标准, 2 应用较为广泛的有糖精与糖精钠, 其学名为邻-磺酰苯甲酰亚胺,分式 为C7H5O3NS。
合并洗液, 无水硫酸钠过滤脱水 脂肪抽提器去乙醚 挥发 乙醚 加入2ml乙醇溶解
9 点样
10 展开
展开至 10cm 取出,挥发干燥,紫外灯下观察 定性:根据样品点与标准点比较值定性, 根据斑点的大小进行半定量测定
第12章 第4讲 生命中的基础有机化学物质

进入导航
第十二章
第 4讲
系列丛书
(3) 盐 析 : 向 蛋 白 质 溶 液 中 加 入 某 些 ________[ 如 (NH4)2SO4、Na2SO4等,重金属盐除外]溶液达到一定浓度 时,可以使蛋白质的溶解度降低而从溶液中析出,这一作 用称为盐析。盐析属于物理过程,是________的。采用多
进入导航
木材、ቤተ መጻሕፍቲ ባይዱ花
制硝酸纤维、纤维素乙酸 酯、造纸、粘胶纤维
第十二章 第 4讲
高三总复习 · RJ · 化学
系列丛书
三、氨基酸 氨基酸是组成蛋白质的基本结构单位,是蛋白质水
解的最终产物。
1.氨基酸的结构 氨基酸中含有两种官能团 (填名称):________。组成 蛋白质的氨基酸几乎都是 α -氨基酸,即氨基在羧基的 ______ 位 上 , α - 氨 基 酸 的 结 构 简 式 可 表 示 为 ________________________。
高三总复习 · RJ · 化学
进入导航
第十二章
第 4讲
系列丛书
五、酶 1.酶是一类由细胞产生的对生物体内的化学反应具
有催化作用的蛋白质,是一种生物________,一种特殊的
蛋白质。 2.酶的催化作用具有以下特点 (1) 条件 ________ 、 ________ 。在接近体温和接近中 性的条件下,酶就可以起催化作用。 30~50 ℃时酶的活 性最强,超过适宜的温度时,酶将失去活性。
进入导航
第十二章
第 4讲
系列丛书
六、核酸 1.概述:核酸是一类含 ________的生物高分子化合
物,一般由几千到几十万个原子组成,相对分子质量可达
十几万 至几百万。因最早由 ________ 中分离得到,且具有 ________而得名。 2 . 分 类 : 核 酸 可 分 为 ________________ 和 ________。
第十二章 糖类

宁德职业技术学院
(二)支链淀粉
支链淀粉约由600~6000个α -葡萄糖分子相互脱水, 以α -1,4-苷键连接成直链外,还有以α -1,6-苷键相连而 引出支链.大约每隔20~25个葡萄糖单位有一个分支,纵横 关联,构成树枝状结构.
宁德职业技术学院
支链淀粉不溶于水,热水中则溶胀而成糊状,无还原性.支 链淀粉遇碘呈现紫红色. 酸或酶的催化下可以逐步水解,生成 与碘呈现不同颜色的糊精、麦芽糖,最后水解为葡萄糖.
宁德职业技术学院
醛糖如葡萄糖, 用溴水氧化时, 得到葡萄糖酸. 而果糖 与溴水无作用. 所以, 可用溴水区别醛糖和酮糖. 葡萄糖用 硝酸氧化得到葡萄糖二酸, 酮糖与强氧化剂作用, 碳链断裂, 生成小分子的羧酸混合物.
宁德职业技术学院
凡是能够还原多伦试剂或斐林试剂的糖都称还原糖. 从结构上看,还原糖都含有α-羟基醛或α-羟基酮的结构. 因此, 所有的单糖都是还原糖.
宁德职业技术学院
四.果胶质
果胶质广泛存在于植物的细胞壁中,能使细胞粘合在一起. 在植物的果实、种子、浆果、块茎及叶子里都含有果胶质,但 以水果和蔬菜中含量较多. 果胶质是一类成分比较复杂的多糖, 其化学组成常因来源不同而有差别. 根据其结合状况和理化性 质,可把果胶质分为原果胶、可溶性果胶和果胶酸. 1.原果胶 原果胶主要存在于未成熟的水果中,是可溶性果胶与纤维 素合成的高分子化合物. 原果胶在稀酸或果胶酶的作用下即转 变为可溶性果胶. 2.果胶酸 果胶酸是由许多半乳糖醛酸通过α -1,4-糖苷键结合而成 的高分子化合物.
蔗糖分子中不存在半缩醛羟基,因而无还原性.蔗糖在 酸或酶的作用下水解,生成葡萄糖和果糖的混合物,这种混 合物称为转化糖.
宁德职业技术学院
第三节
糖类化合物

α
D
112。 19。
华东理工大学
22
无论哪一种,其水溶液的旋光度均发生改变,最后达到一 个定值+52.7° ,这种变化可用右图表示:
α
D
时间
象这种单糖溶液的[α]D随时间的变化而改变,最后 达到一个定值的现象,叫做变旋光现象 变旋光现象。 变旋光现象
华东理工大学 23
(b)D-(+)-葡萄糖不能与NaHSO3发生加成(与 醛的性质不符)。 (c)在HCl存在下,葡萄糖与甲醇作用仅生成一分子加成产物 (醛可以与两分子醇作用),形成的 甲基-D-葡萄糖苷有两 种结构,它们都没有变旋光现象。 mp 165℃ [α]=+158° 甲基-α-D-葡萄糖苷 mp 107℃ [α]=-33° 甲基-β-D-葡萄糖苷
CHO H OH H OH CH2OH 赤藓糖
HNO3
COOH H OH H OH COOH
无旋光性 内消旋体
故: OH 在右边
华东理工大学
17
在这方面的研究,德国化学家 最为突出, 在这方面的研究,德国化学家Fischer最为突出,为 最为突出 此曾获1902年Nobel化学奖。经研究确定,葡萄糖具有 化学奖。 此曾获 年 化学奖 经研究确定, 下面的构型: 下面的构型:
CHO H OH HO H H OH H OH 6 CH2OH Fischer 投影式 2R , 3S ,4R , 5R - 2,3,4,5 -五羟基己醛
1
简写成
那么,若用 标记法又如何进行标记呢? 那么,若用D / L 标记法又如何进行标记呢?
华东理工大学 18
CHO H OH HO H H OH H OH CH2OH
华东理工大学
2
有机化学——第12章糖类化合物

葡萄糖单元是通过α-1,4-苷键相连。与直链不同的是,每隔20-25
个葡萄糖单元,就有一个以α-1,6-苷键相连的支链。
α-1,6-苷键
α-1,4-苷键
32
性质:
(1) 水溶性: 热水
直链淀粉:溶解 支链淀粉:糊化
(2) 水解性:大分子 淀粉 蓝糊精
小分子 无色糊精 麦芽糖 D-葡萄糖
红糊精
(3) 显色反应:
-苷键
甲基 - -D-吡喃葡萄糖苷 20
6、酯化反应
应用制备酯的通用方法可以在糖中的每一个有羟基的位点发生成 酯反应。
快 Ac2O NaAc 0oC 无水 ZnCl2 Ac2O 0oC 慢 100oC 相对较快 -D-吡喃葡萄糖 -D-吡喃葡萄糖 快 Ac2O NaAc 0oC Ac2O, NaOAc 100oC相对较慢
鼠李糖 (C6H12O5)
戊糖 根据碳原子数不同: 己糖 单糖 (monosaccharides) 分类: 根据羰基的不同: 醛糖 酮糖
低聚糖 (Oligosaccharides) 2-10个单糖
多聚糖 (Polysaccharides) > 10 个单糖
2
第一节 单糖
单糖是多羟基醛或多羟基酮。
除丙酮糖外,所有单糖都有旋光性。多数单糖有变旋现象。
14
五、单糖的化学性质: 1、碱催化的异构化反应
15
2、氧化反应
还原糖和非还原糖的概念:
凡是对斐林试剂、托伦试剂、本尼迪试剂呈正反应的糖称为还 原糖,呈负反应的糖称为非还原糖。 醛糖具有醛基(或半缩醛羟基),可以被弱氧化剂氧化;酮糖在碱 性条件下发生互变异构形成醛糖,也可被氧化。
黄原酸纤维素:
35
纤维素酯
糖类化合物1解释下列名词变旋光现象差向异构体
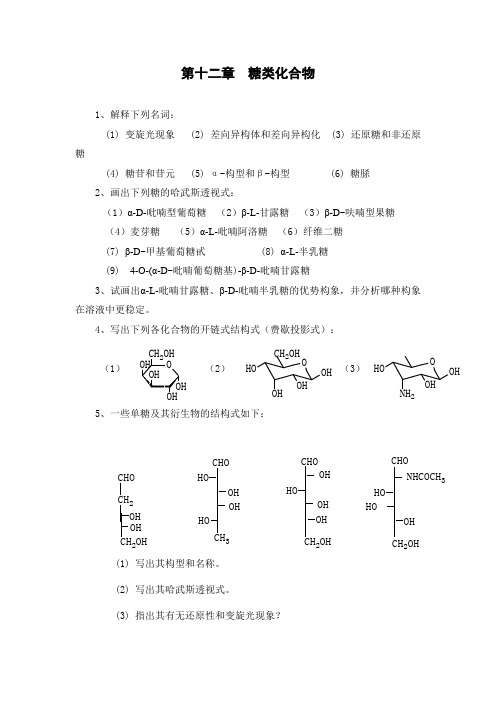
HO OH O OH CH 2OH HO OHO OH2第十二章 糖类化合物1、解释下列名词:(1) 变旋光现象 (2) 差向异构体和差向异构化 (3) 还原糖和非还原糖(4) 糖苷和苷元 (5) α-构型和β-构型 (6) 糖脎 2、画出下列糖的哈武斯透视式:(1)α-D-吡喃型葡萄糖 (2)β-L-甘露糖 (3)β-D -呋喃型果糖 (4)麦芽糖 (5)α-L-吡喃阿洛糖 (6)纤维二糖 (7) β-D -甲基葡萄糖甙 (8) α-L-半乳糖 (9) 4-O-(α-D -吡喃葡萄糖基)-β-D-吡喃甘露糖3、试画出α-L-吡喃甘露糖、β-D-吡喃半乳糖的优势构象,并分析哪种构象在溶液中更稳定。
4、写出下列各化合物的开链式结构式(费歇投影式):(1)(2) (3)5、一些单糖及其衍生物的结构式如下:(1) 写出其构型和名称。
(2) 写出其哈武斯透视式。
(3) 指出其有无还原性和变旋光现象?HO OH OH CH 2OHOHHOCHO3NHCOCH 3HOCHO CHOHOOH OH 2OHOH CHO CH 2HO OHOH 2OH(4) 指出哪些可发生水解反应?6、指出下列化合物中哪些具有还原性?哪些没有还原性?(1)β-D -甘露糖 (2)D -果糖 (3)L -半乳糖 (4)纤维素 (5)麦芽糖(6)乳糖 (7)纤维二糖 (8)淀粉 (9)甲基-β-D -葡萄糖 (10)蔗糖7、完成下列反应式:(1)(2) (A ) 内消旋酒石酸(3)(B ) 旋光性丁四醇 (4) 果糖(5)8、写出D-(+)-葡萄糖与下列试剂反应的主要产物。
(1) 稀HNO 3 (2) Br 2/H 2O (3) 过量苯肼 (4) NH 2OH (5) (CH 3CO)2O(6) CH 3OH /无水HCl (7) (CH 3)SO 4/NaOH (8) H 2/Ni (9)NaBH 4 9、用怎样的方法可以证明D -甘露糖、D -果糖和D -葡萄糖这三种糖的C 3,C 4,C 5具有相同的构型?10、用简单的化学方法鉴别下列各组化合物:(1) 葡萄糖、蔗糖和淀粉 (2) 淀粉和纤维素(3) 葡萄糖和半乳糖 (4)葡萄糖、果糖和纤维素 (5) α-D -葡萄糖甙和β-D -葡萄糖苷11、两个互为对映体的丁醛糖,还原后生成的四元醇是内消旋体,没有旋光性。
生物化学习题答案

第一章糖一.填空1.糖类是具有多羟基醛或多羟基醇结构的一大类化合物。
根据其分子大小可分为单糖、寡糖和多糖三大类。
2.判断一个糖的D-型和L-型是以离羰基碳最远的手性碳原子上羟基的位臵作依据。
3.蔗糖是由一分子D-葡萄糖和一分子D-果糖组成,他们之间通过α,β-1,2糖苷键相连。
4.麦芽糖是由两分子D-葡萄糖组成,他们之间通过α-1,4糖苷键相连。
5.乳糖是由一分子D-半乳糖和一分子D-葡萄糖组成,他们之间通过β-1,4糖苷键相连。
6.肽聚糖的基本结构是以N-乙酰D-葡糖胺与N-乙酰胞壁酸组成的多糖链为骨干,并与四肽连接而成的杂多糖。
7.糖肽的主要连接键有N-糖肽键和O-糖肽键。
8.由于糖和苯肼生成糖脎,其晶体形状不同,熔点也不同,可以定性鉴定唐。
二.简答1.纤维素和糖原的什么结构特性使得他们的物理特性有那么大的差别?纤维素和糖原的结构特性确定了他们什么生物学作用?答:天然纤维素是由通过β(1→4)糖苷键连接的葡萄糖单位组成的,这种糖苷键迫使聚合物链成伸展的结构。
这种一系列的平行的聚合物链形成分子间的氢键,他们聚集成长的、坚韧的不溶于水的纤维。
糖原主要是由通过α(1→4)糖苷键连接的葡萄糖单位组成的,这种糖苷键能引起链弯曲,防止形成长的纤维。
另外体验版是个具有高分支的聚合物。
他的许多羟基暴露于水,可被高度水合,因此可分散在水中。
纤维素由于他的坚韧特性,所以他是植物中的结构材料。
糖原是动物中的贮存燃料。
2.葡萄糖溶液为什么有变旋现象?答:主要原因是由于葡萄糖具有不同的环状结构,当葡萄糖由开链结构变为环状结构时,C1原子同时变成不对称碳原子,同时产生了两个新的旋光异构体。
一个叫α-D-吡喃葡萄糖,另外一个叫β-D-吡喃葡萄糖,这两种物质互为异头物,在溶液中可以开链式结构发生相互转化,达到最后平衡,其比旋光度为+52°。
三.补充概念1.凝集素:一类非抗体的糖蛋白或蛋白质,它能与糖专一的非共价结合,并具有凝结细胞和沉淀聚糖和复合糖的作用。
第13章 糖类2016

O
H O C H 2 OH H 3 OH 4 H OH 5 CH2OH
1
5
HO CH2
4
O H
2
H
1
H OH
H 3
OH OH
β-D-呋喃核糖
D-核糖(开链结构)
α-D-呋喃核糖
31
单糖环状结构的哈沃斯式和构象式
由开链式写哈沃斯式: ①画出杂环骨架(朝前的3个C-C键用粗线 表示)。 ②氧原子写在右上角,按顺时针将碳环编 号。C5上的羟甲基在环平面上方为D型。 ③将开链式中左边的写在环平面的上方, 右边的写在环平面的下方。即“左上右下”
9
第一节 单糖
一、单糖的分类
1. 据官能团分:醛糖、酮糖
最小的醛糖
最小的酮糖
2.据碳原子数分:丙、丁、戊、已 糖
10
二、单糖的结构
1.单糖的开链结构和构型 一般单糖碳链无支链
醛糖:C1为醛基 酮糖:C2为酮基
其它碳上都各连有一个羟基
CHO (CHOH)n CH2OH
醛糖
CH2OH C O (CHOH) n CH2OH
D—阿洛酮糖
CH2OH C O HO H H OH H OH CH2OH
D—果糖
CH2OH C O H OH HO H H OH CH2OH
D—山梨糖
CH2OH C O HO H HO H H OH CH2OH
D—塔洛糖
18
2.葡萄糖的环状结构和变旋光现象
(1)变旋光现象
葡萄糖具有羰基和羟基的典型反应 但是还有一些性质却不能用开链结构说明
洋地黄毒苷
5
氨基糖苷类抗生素是一大类含糖的抗生素,其
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
根据分子中碳的数目可分为 丙糖、戊糖、丁糖、己糖等 最常见的单糖:戊糖、己糖
确定单糖D,L构型的方法
用化学反应将单糖与甘油醛联系起来,以 甘油醛为标准确定D,L构型
羰基在上方,考虑与羰基相距最远的手性 碳原子的构型,羟基在右侧的为D型
二、单糖的链式结构与Fischer投影式
CHO CH2OH
五、单糖的化学性质
醛酮、醇以及氧环式半缩醛酮的特殊性质
1、氧化反应
弱氧化剂氧化 单糖的还原性
单糖的还原性:都可被Tollen试剂、 Fehling试剂、 Benedict试剂(硫酸铜、碳 酸钠和柠檬酸钠的混合液,兰色)氧化而显 还原性 糖与Benedict试剂反应常用于测定血液和尿 中葡萄糖的含量
由一分子α-D-葡萄糖的半缩醛羟基与一分 子β-D-果糖的半缩醛羟基脱水成糖苷 无半缩醛羟基,无还原性,无变旋现象、 不与苯肼试剂反应 (+)-海藻糖
12.3 多糖
多糖:由数百个以至数千个单糖分子以糖 苷键相连形成的天然高分子化合物 多糖无游离的半缩醛羟基,不具有单糖的 一般性质,水溶性降低,没有甜味,在酸 的作用下可彻底水解为单糖 重要多糖:纤维素、淀粉、糖原等
图12-2 支链淀粉示意图
2、纤维素
纤维素类似于直链淀粉,葡萄糖单元以β1,4-糖苷键相连 淀粉酶不能水解纤维素,食草动物消化道内 的微生物分泌可水解β-1,4-糖苷键的酶
相关题型分析
单糖的D,L构型表示法 单糖的Haworth透视式 单糖的化学性质 醛糖与酮糖的鉴别 二糖的形成、连接方式 还原性双糖、非还原性双糖 淀粉的鉴别
3、环状结构的表示与命名
(1)费歇尔投影式--吡喃葡萄糖
能看出C2与C5发生缩合反应,形成半缩醛 不能反映原子和基团在空间的关系
(2)透视式(哈武斯式Haworth)
哈武斯式的几点说明
C1半缩醛羟基与决定构型的C5未反应前 的羟基位于环的同侧,命名为α-,异侧 命名为β能清楚表示C1的醛基与C5的羟基发生缩 合反应,环上各基团的顺反关系,准确 定义α、β异构体 不能真实反映单糖环状结构的三维空间 构造
由一分子β-D-半乳糖的半缩醛羟基和一分子D-葡 萄糖第四位的醇羟失水 葡萄糖部分仍保留着一个半缩醛羟基
3、非还原性二糖及性质
6 4
-1,2-糖苷键
CH2OH
5 3 2
HO HO
O OH
1
OH O
2
3
4
O
5
OH CH2OH
6
-1,2-糖苷键 蔗糖
CH2OH
1
-D-呋喃果糖基--D-吡喃葡萄糖苷
14、3 双糖 1、双糖的形成
二糖:两分子单糖脱水形成的缩合物 还原性二糖:一分子单糖的半缩醛羟基与另一分子 单糖的醇羟基脱水 非还原性二糖:两分子单糖的半缩醛羟基之间脱水
2、还原性双糖及性质
保留半缩醛羟基,有变旋现象、还原性, 能与苯肼反应等 β-(+)-麦芽糖、乳糖等
乳糖 的结构
第十二章 糖类
12.1 单糖 12.2 双糖 12.3 多糖
糖类的分类
根据能否水解分为:
单糖:不能再水解的多羟基醛或酮
低聚糖(寡糖):水解为2-10个单糖单元的糖
多糖:水解为十个以上,甚至成百上千个
单糖单元的碳水化合物,又称多聚糖
12.1 单糖
一、单糖的分类
根据所含羰基的结构分为:
醛糖:分子中含有醛基的糖 酮糖:分子中含有酮基的糖
呋喃葡萄糖的哈武斯透视式
6 6
CH2OH HO
5 4
H
O
CH2OH OH
1
HO
5 4
H
O
H
1
OH OH
3
H
2
H
OH OH
3
H
2
OH
H
OH
H
OH
-D-呋喃葡萄糖
-D-呋喃葡萄糖
吡喃果糖的哈武斯透视式
• (2008农学联考)
•
(3)构象式
α-D-吡喃果糖的构象
四、单糖的物理性质
无色结晶,易溶于水 糖浆:糖的过饱和溶液 变旋现象:新配置的单糖水溶液在放置 过程中,由于产生链式结构与环式异构 体的互变,产生几种旋光度不同的异构 体,使该水溶液旋光度逐渐改变,直到 平衡后,旋光度稳定在某一数值不再改 变的现象
作业
P 279:1, 2,4,5, P 280: 7, 8,10
2、Fischer等人发现葡萄糖氧环状结构
在葡萄糖水溶液中存在此平衡
几个重要概念
α-异构体:新形成的手性碳的羟基与C5的 羟基在碳链的同侧 β-异构体:新形成的手性碳的羟基与C5 的羟基在碳链的反侧 差向异构体(异头物):含多手性碳的旋 光异构体中,只一个手性碳构型相反,其 它手性碳构型相同的非对映异构体
1、淀粉
直链淀粉
α-1,4-糖苷键相 连,含量约为10-30%
葡萄糖单体以
图12-1 直链淀粉与碘形成配位化合 物示意图
直链淀粉链非直线,借助分子内氢键卷曲成 螺旋状 直链淀粉遇碘,碘分子可钻入螺旋空隙中, 形成蓝色配位化合物
支链淀粉
葡萄糖单体以α-1,4-糖苷键,α-1,6-糖苷键 相连,比例为20:1
红外光谱中没有羰基峰存在 加入NaHSO3析不出晶体 只能与一分子CH3OH/H+反应 在冷乙醇中结晶出的葡萄糖[α]D20 =+112°, 20 在热吡啶中结晶出的葡萄糖 [α]D =+18.7°, 若将二者的水溶液放置,旋光度逐渐变化, 达到+52.7°时不再变化 变旋现象:旋光度自行发生改变的现象。
6、甲基化(成醚作用)
缩醛与醚的区别
缩醛可在酸性下水解为糖与醇,而醚不能 具有半缩醛羟基,可显示还原性
甲基化反应的应用
未被甲基化的羟基氧化成酮,羰基两侧断裂 C5不带甲氧基,葡萄糖的环形结构为六员环 成醚反应可确定单糖的环状结构
7、酯化反应
单糖的磷酸酯是糖代谢的重要中间产物 单糖中醇羟基与半缩醛羟基均能与酸反应
D-(+)-甘油醛
CHO
CHO H OH OH
CH2OH
D-(-)-核糖
CH2OH
D-2-脱氧核糖
CH2OH C O
CHO
CHO
CHO
CH2OH
D-果糖
CH2OH
D-(+)-葡萄糖
CH2OH
D-(+)-甘露糖
CH2OH
D-(-)-半乳糖
三、单糖的氧环状结构
1、葡萄糖开链结构不能解释的实验事实
(2008农学联考)
5、糖苷的形成(形成缩醛)
糖苷:糖的半缩醛羟基与其它羟基化合物 (醇 或酚)反应,形成的缩醛,也称糖甙或配糖物
糖苷性质稳定,不能再转化为开链结构,无 变旋现象,无还原性,在碱中不发生差向异 构化,不与苯肼反应,稀酸水解为糖与醇
关于几个糖苷的几个概念
Hale Waihona Puke 糖基:糖部分 配基:非糖部分,如醇、酚等 α糖苷:由α型单糖形成的 β糖苷:由β型单糖形成的 糖苷键:糖基与配基之间的缩醛型醚键
3、差向异构化
差向异构体
C2-差向异构体:2号碳原子构型相反
D-葡萄糖的差向异构化
差向异构化: 在多个手性碳的分子中,只使一 个手性中心的构型转化的作用
4、成脎反应(与苯肼反应)
醛糖和酮糖发生在C1, C2上,α-羟醛或酮 糖脎为黄色结晶,根据晶形、熔点和生成时间鉴别糖 D-葡萄糖、D-甘露糖和D-果糖的糖脎相同
环状结构对一些实验现象的解释
开链结构浓度极低,在红外光谱中显示不出 羰基的特征峰 开链结构浓度极低,与NaHSO3反应不能析 出晶体 环状结构为半缩醛,只与一分子甲醇反应生 成缩醛 在冷乙醇中析出α-异构体,在热吡啶中析出 β -异构体,在水溶液中α、 β异构体通过开 链结构互变达到平衡组成(37% α-,63% β-)
还原糖
(reducing sugar): 能与Tollen试剂、 Fehling试剂、 Benedict试剂发生反应的糖
非还原糖
(nonreducing sugar): 不能与上述 试剂发生反应的糖
溴水氧化
鉴别醛糖、酮糖
强氧化剂氧化
酶催化氧化
高碘酸氧化
2、还原反应
还可用LiAlH4,NaBH4和异丙醇铝等
