分子晶体
【知识解析】分子晶体

分子晶体温故1.晶体中的粒子可以是分子、原子或离子;粒子间的相互作用可以是共价键、离子键、金属键或分子间作用力。
2.根据晶体中粒子间的相互作用及排列方式,可把晶体分为分子晶体、共价晶体、离子晶体和金属晶体。
1 分子晶体的定义只含分子的晶体,或者分子间以分子间作用力结合形成的晶体叫分子晶体。
如I2、H2O、NH3、H3PO4、萘等在固态时都是分子晶体。
名师提醒(1)定义中的“分子”指真实存在的小分子、分子的聚集体、缔合分子、大分子(高分子),因此,H2SO4、H2O2、C4H10等既是化学式也是分子式。
(2)离子化合物、金属单质、原子间相互结合形成空间网状结构(如金刚石、SiO2)的物质中没有分子,因此,Na2O2、Fe、SiO2等是化学式而不是分子式。
(3)稀有气体的分子是单原子分子,因此,由稀有气体单质形成的晶体也是分子晶体。
2 分子晶体中的粒子及粒子间的相互作用3 常见的典型分子晶体(1)所有非金属氢化物:H2O、H2S、NH3、CH4、HX(卤化氢)等。
(2)部分非金属单质:X2(卤素单质)、O2、H2、S8、N2、P4、C60、稀有气体等。
(3)部分非金属氧化物:CO2、SO2、NO2、P4O6、P4O10等。
(4)几乎所有的酸:H2SO4、HNO3、H3PO4、H2SiO3等。
(5)绝大多数有机物:苯、四氯化碳、乙醇、冰醋酸、蔗糖等。
4 分子晶体的物理性质(1)分子晶体具有较低的熔、沸点和较小的硬度。
分子晶体熔化时要破坏分子间作用力,由于分子间作用力很弱,所以分子晶体的熔、沸点一般较低,部分分子晶体易升华(如干冰、碘、红磷、萘等),且硬度较小。
(2)分子晶体不导电。
分子晶体在固态和熔融状态下均不存在自由移动的离子或电子,因而分子晶体在固态和熔融状态下都不能导电。
有些分子晶体的水溶液能导电,如HI、乙酸等。
(3)分子晶体的溶解性一般符合“相似相溶”规律,即极性分子易溶于极性溶剂,非极性分子易溶于非极性溶剂。
分子晶体

BC
A组 Cl键键 Ⅰ.H—I键键能大于H—Cl键键 I键键能大于H Cl 能 C1键键 Ⅱ.H—I键键能小于H—C1键键 I键键能小于H C1 能 HI分子间作用力大于 分子间作用力大于HCl Ⅲ.HI分子间作用力大于HCl 分子间作用力 HI分子间作用力小于 分子间作用力小于HCl Ⅳ.HI分子间作用力小于HCl 分子间作用力
5,关于下列常见晶体说法正确的是
2 60
冰中每个水分子周围有12 12个紧邻的水分子 B.冰中每个水分子周围有12个紧邻的水分子 C.水在固态时密度一定比液态小 干冰中, 个分子周围有12的紧邻分子, 12的紧邻分子 D.干冰中,1个分子周围有12的紧邻分子, 密度比冰小. 密度比冰小.
有下列两组命题,B组中命题正确,且能用A ,B组中命题正确 6,有下列两组命题,B组中命题正确,且能用A组 命题加以正确解释的是 A. Ⅰ ① B. Ⅱ ② C. Ⅲ ③ D. Ⅳ ④
B组 ①HI比HCI稳定 HI比HCI稳定 ②HCl比HI稳定 HCl比HI稳定 ③HI沸点比HCl高 HI沸点比HCl 沸点比HCl高 ④HI沸点比HCl低 HI沸点比HCl 沸点比HCl低
�
5,典型的分子晶体
(1)所有非金属氢化物: (1)所有非金属氢化物: H2O,H2S,NH3,CH4,HX 所有非金属氢化物 (2)部分非金属单质:X (2)部分非金属单质:X2,O2,H2, S8,P4, C60,稀有气体 部分非金属单质 60, (除硼,金刚石,晶体硅) 除硼,金刚石,晶体硅) (3)部分非金属氧化物: CO2, SO2, NO2, P4O6, P4O10 (3)部分非金属氧化物: 部分非金属氧化物 (除二氧化硅) 除二氧化硅) (4)几乎所有的酸: (4)几乎所有的酸:H2SO4,HNO3,H3PO4 几乎所有的酸 (5)大多数有机物的晶体:冰醋酸, (5)大多数有机物的晶体:冰醋酸,蔗糖 大多数有机物的晶体
分子晶体_课件

典型分子晶体
典型的分子晶体有哪些 ?(1)所有_非__金___属__氢__化__物___,如H2O、NH3、CH4等 ;(2)部分__非__金__属__单___质__,如卤素、O2、S8、C60、稀有气体等 ;(3)部分_非___金__属__氧__化___物__,如CO2、SO2、P4O6、P4O10等 ;(4)几乎所有的_酸___,如HNO3、H2SO4、H3PO4等 ;(5)绝大多数__有__机__物___的晶体,如蔗糖、乙醇等 。
干冰就是CO2的晶体,外观像冰,硬度也和冰相似,而熔 点比冰低得多,易升华(想想为什么),在工业上广泛用 作制冷剂。
分子晶体的结构特征
(2)分子非密堆 积此时分子间有氢键——氢键具有方向性和饱和性,使晶体中
的空间利用率不高,留有相当大的空隙。这种晶体不具有分 子密堆积特征,如:HF、NH3、冰等。
444.6 ℃
C.熔点1400 ℃ ,可做半导体材料,难溶于水
分子晶体
练习2:下列属于分子晶体的一组物质是 B
(
)A.CaO、NO、乙醇l4、H2O2、
HeC.CO2、HNO3、NaClD.CH4、O2、Na2O
分子晶体
1、下列分子晶体,关于熔、沸点高低叙述中,正确的是(B )A.Cl2>I2 B.SiCl4>CCl4 C.NH3<PH3 D.C(CH3)4>CH3(CH2)3CH3
( A )A.CO2
B.O2
C.NH4Br
D.Ar
分子晶体
3.SiCl4的分子结构与CCl4相似,下列推测不正确的是(B )A.SiCl4晶体是分子晶体B.常温、常压下SiCl4是气体C. SiCl4的分子是由极性键形成的非极性分子D.SiCl4的熔点 高于CCl4
分子晶体
《分子晶体》课件

在生物学中的应用
分子晶体在生物学中也有着广泛的应用,如用于研究生物大分子的结构和功能。生物大分子如蛋白质 、核酸和多糖等具有复杂的结构和功能,通过研究和了解它们的结构和功能,可以更好地理解生命过 程和疾病机制。
对称面
某些分子晶体中存在对称 面,使得晶体具有对称性 。
对称中心
某些分子晶体中存在对称 中心,使得晶体具有对称 性。
03
分子晶体的分类
有机分子晶体
总结词
有机分子晶体是指由有机分子构成的晶体,其结构单元是碳原子和氢原子等有 机元素。
详细描述
有机分子晶体在自然界中广泛存在,如蛋白质、核酸等生物大分子都是有机分 子晶体。此外,许多塑料、合成纤维等高分子材料也是有机分子晶体。这些晶 体的结构和性质与构成它们的有机分子密切相关。
《分子晶体》ppt课 件
目 录
• 分子晶体简介 • 分子晶体的结构 • 分子晶体的分类 • 分子晶体的应用 • 分子晶体的未来发展
01
分子晶体简介
分子晶体的定义
01
分子晶体是由分子通过分子间作 用力(范德华力)相互结合形成 的晶体。
02
分子晶体中不存在离子或共价键 的结合,而是分子与分子之间的 相互作用。
详细描述
科研人员正在探索新型的分子晶体材 料,这些材料具有更高的稳定性、更 优秀的物理和化学性能,能够满足各 种高科技领域的需求。
分子晶体在新能源领域的应用
总结词
分子晶体在新能源领域的应用前景广 阔,如太阳能电池、燃料电池等。
详细描述
分子晶体

3、典型物质
ቤተ መጻሕፍቲ ባይዱ
(1)碘晶体
长方体
每个晶胞中有 4 个碘分子
什么体? 几个分子?
3、典型物质
(2)干冰 面心立方 每个晶胞中有 4 个二氧化碳分子
什么体? 几个分子?
3、典型物质
(3)冰 氢键具有方向 性
冰中1个水分子周围有4个水分子
冰的结构
4、物理性质 (1)分子晶体有低熔点(破坏的是分子间作用力) (2)不导电(三态下均不存在带电荷的离子,共价 键没有被破坏)(水溶液 中有些导电有些不导电) (3)相似相溶 (4)易挥发、硬度小(分子间作用力弱)
3.下列化学式既能表示物质的组成,又能表示物质 分子式的是 ( C )。 A.NH4NO3 B.SiO2 C.C2H5OH D.Fe 4.氮化铝(AlN)常做砂轮及高温炉衬材料,熔化状态 下不导电,可知它属于 ( C )。 A.离子晶体 B.分子晶体 C.原子晶体 D.金属晶体
1 .当下列物质以晶体形式存在时,其所属晶体类 型和所含化学键类型分别相同的是 ( C )。 A.氯化钠和氯化氢 B.二氧化碳和二氧化硅 C.四氯化碳和四氯化硅 D.单质铁和单质碘 2.下列有关物质的熔点高低顺序不正确的是( C ) A.HF>HCl,HCl<HBr B.CF4<CCl4<CBr4 C.I2>SiO2 D.H2O>H2S,SO2<SeO2
1、定义:分子间通过分子间作用力构成的晶体称 为分子晶体。
注意点: I 构成分子晶体的粒子是分子。 II 在分子晶体中,分子内的原子间以共价键结合, 而相邻分子靠分子间作用力相互吸引。
例 CO2 H2O 存在分子
2、结构特点:由于分子间作用力不具有 方向性 ,所以分子晶体在堆积排列时尽可能的 ________ 利用空间采取紧密堆积的方式。
常见分子晶体

常见分子晶体分子晶体是由大量的有机分子(或者有机分子和无机分子的混合)组成的三维晶体。
它们是化学物质的纯净结晶形态,具有高度定向的分子团簇结构,因此具有各种独特的化学和物理特性。
常见的分子晶体有芳烃晶体、烷烃晶体、烯烃晶体、萘烷晶体和苯烷晶体等。
芳烃晶体是指碳原子四面有同种或不同种芳基的晶体结构。
芳烃的晶体常由四面环结构所组成,这些环可以是环状的(例如苯和芘),也可以是网状的(例如吡啶)。
芳烃晶体的晶体结构的分子间的互相接触是由共价键形成的,因此它们具有非常高的熔点,比其它晶体都要高。
烷烃晶体是指由碳原子四面均附有烷基(由一个羟基和一个不饱和羟基连接而成)的晶体结构。
它们具有非常高的熔点,晶体结构的分子间由共价键构成的范式,如甲烷的「空气状(cellular)」晶体结构。
烯烃晶体也是四面均有烷基附有的晶体,但是具有一个不饱和三环(即烯烃),而不是共价键构成的范式。
烯烃晶体有大量的晶体结构类型,其中包括有萘烷(naphthalene)、芘(phenanthrene)和芪(acenaphthene)等。
萘烷晶体是指一种晶体结构,由两个连在一起的萘环(含有八个碳原子)所组成。
由于其具有古老的烯烃结构,萘烷晶体通常具有较高的熔点和灭火点,而且还具有很强的光学特性,如上转换性、荧光光谱和悬浮特性等。
苯烷晶体是指碳原子四面都附有苯基的晶体结构。
它们的分子间的相互作用是由共价键构成的,而不是烯烃晶体的烯环,因此它们的晶体结构就像甲烷一样,并且具有较高的熔点。
苯烷晶体有一种变体,称为叶绿素晶体,它由二环芳烃和两个饱和羟基所组成,具有丰富的荧光特性和传输性。
总之,常见的分子晶体有芳烃晶体、烷烃晶体、烯烃晶体、萘烷晶体和苯烷晶体等,它们均具有高度定向的分子团簇结构,因此具有各种独特的化学和物理特性。
其中,芳烃晶体是由碳原子四面有同种或不同种芳基的晶体结构组成,而烷烃晶体和烯烃晶体则是由碳原子四面均附有烷基的晶体结构,萘烷晶体是由两个连在一起的萘环构成,而苯烷晶体则是由碳原子四面都附有苯基的晶体结构。
分子晶体

分子晶体分子晶体,指分子间以范德华力相互结合形成的晶体。
大多数非金属单质及其形成的化合物如干冰(CO2)、I2、大多数有机物,其固态均为分子晶体。
分子晶体是由分子组成,可以是极性分子,也可以是非极性分子。
分子间的作用力很弱,分子晶体具有较低的熔、沸点,硬度小、易挥发,许多物质在常温下呈气态或液态,例如O2、CO2是气体,乙醇、冰醋酸是液体。
同类型分子的晶体,其熔、沸点随分子量的增加而升高,例如卤素单质的熔、沸点按F2、Cl2、Br2、I2顺序递增;非金属元素的氢化物,按周期系同主族由上而下熔沸点升高;有机物的同系物随碳原子数的增加,熔沸点升高。
但HF、H2O、NH3、CH3CH2OH等分子间,除存在范德华力外,还有氢键的作用力,它们的熔沸点较高。
分子组成的物质,其溶解性遵守“相似相溶”原理,极性分子易溶于极性溶剂,非极性分子易溶于非极性的有机溶剂,例如NH3、HCl极易溶于水,难溶于CCl4和苯;而Br2、I2难溶于水,易溶于CCl4、苯等有机溶剂。
根据此性质,可用CCl4、苯等溶剂将Br2和I2从它们的水溶液中萃取、分离出来。
物质类别及举例所有非金属氢化物:如水、硫化氢部分非金属单质:如卤素单质部分非金属氧化物:如CO2、SO2绝大多数有机物(有机盐除外)几乎所有的酸(除外:一水合高氯酸的是离子晶体)离子晶体物理学概念,指离子间通过离子键结合形成的晶体。
离子间通过离子键结合形成的晶体。
在离子晶体中,阴、阳离子按照一定的格式交替排列,具有一定的几何外形,例如NaCl是正立方体晶体,Na+离子与Cl-离子相间排列,每个Na+离子同时吸引6个Cl离子,每个Cl-离子同时吸引6个Na+。
不同的离子晶体,离子的排列方式可能不同,形成的晶体类型也不一定相同。
离子晶体中不存在分子,通常根据阴、阳离子的数目比,用化学式表示该物质的组成,如NaCl表示氯化钠晶体中Na+离子与Cl-离子个数比为1∶1,CaCl2表示氯化钙晶体中Ca2+离子与Cl-离子个数比为1∶2。
10-典型晶体简介(分子晶体)
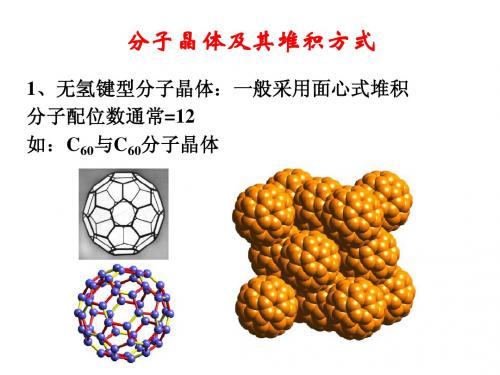
1、无氢键型分子晶体:一般采用面心式堆积 、无氢键型分子晶体: 分子配位数通常=12 分子配位数通常 如:C60与C60分子晶体
分子晶体及其堆积方式
1、无氢键型分子晶体:一般采用面心式堆积 、无氢键型分子晶体: 分子配位数通常=12 分子配位数通常 分子晶体(干冰) 如:CO2与CO2分子晶体(干冰)
分子晶体熔点的相对高低规律之四
讨论: 讨论: 实验测得气态氯化铝的相对分子质量等于267,则其分 实验测得气态氯化铝的相对分子质量等于 , 子式为 ,其结构式可能为 。
分子晶体小结
• 分子晶体的一般情况: 分子晶体的一般情况:
所有非金属氢化物、部分共价化合物 所有非金属氢化物、部分共价化合物 非金属氢化物 物质种类 少数盐类 盐类, 少数盐类,如AlCl3 单核或多核的) 晶体中的微粒 (单核或多核的)分子 微粒间的作用力 范德华力或氢键 微粒内部的 微粒内部的 无化学键 有非极性共价键或 作用力 或有非极性共价键或有极性共价键 干冰、 典型代表 氦、氢、干冰、冰 He 、 H2 、 CO2 、 H2O 化学式 较软易碎、部分可溶于水、 较软易碎、部分可溶于水、 物理共性 熔点沸点较低、晶体导电导热性差 熔点沸点较低、晶体导电导热性差
分子晶体熔点的相对高低规律之四
升华问题: 升华问题: 某些分子晶体受热时 不经过熔化直接变成气态 这种现象叫升华 这种现象叫升华 升华的条件 条件是 升华的条件是: 在一定的压强条件下物质的熔点 熔点>沸点 在一定的压强条件下物质的熔点 沸点 能升华的常见物质有: 能升华的常见物质有: 干冰、 苯甲酸、 干冰、碘、萘、苯甲酸、氯化铝等
分子晶体熔点的相对高低规律之一
参考f=k·m1·m2/r2 (1)组成与结构相似时:—二
分子晶体和原子晶体

分子晶体和原子晶体
图2-15 金刚石原子晶体示意图
分子晶体和原子晶体
二氧化碳和方石英都是第Ⅳ A元素化合物, 由于前者是分子晶体,后者是原子晶体,导致 物理性质差别较大。CO2在-78.5 ℃时即升华, 而SiO2的熔点却高达1610 ℃,说明晶体结构 不同,微粒间的作用不同,物质的物理性质也 不同。
分子晶体和原子晶体
在原子晶体中,不存在独立的小分子,而只能把整个晶体看成是 一个大分子,没有确定的相对分子质量。由于共价键具有饱和性和方 向性,所以原子晶体的配位数一般不高。以典型的金刚石原子晶体为 例,每一个碳原子在成键时以sp3等性杂化形成4个sp3共价键,构成 正四面体,所以碳原子的配位数为4。无数的碳原子相互连接构成, 如图2-15所示晶体结构。原子晶体中,原子间以共价键相连,所以 表现出有较高的硬度和较高的熔点(金刚石硬度最大,熔点为3849 K)。 通常这类晶体不导电、不导热,熔化时也不导电,但硅、碳化硅等具 有半导体性质,可以有条件地导电。
分子晶体和原子晶体
图2-14 CO2分子晶体示意图
分子晶体和原子晶体
二、 原子晶体
在晶格结点上排列的微粒为原子,原子之间以 共价键结合构成的晶体称为原子晶体,如碳(金刚 石)、硅(单晶硅)、锗(半导体单晶)及第Ⅳ A族元素 的单质都属于原子晶体,化合物中的碳化硅(SiC)、 砷化镓(GaAs)、方石英(SiO2)等也属于原子晶体。
无机化学
分子晶体和原子晶体
一、 分子晶体
在晶格结点上排列着分子,通过分子间力而形成的晶体, 称为分子晶体,如非金属单质和非金属元素之间的固体化合物 CO2是分子晶体,其晶体结构如图2-14所示。分子晶体中存在 着独立的分子,分子晶体内是共价键,分子晶体间的作用力是 分子间力,由于分子间力很弱,因此分子晶体的熔点低,具有 较大的挥发性,硬度较小,易溶于非极性溶剂,通常是电的不 良导体。若干极性分子晶体在水中解离生成离子,则其水溶液 导电,如HCl溶液。
第二节分子晶体与共价晶体

第三章晶体结构与性质第二节分子晶体与共价晶体【学习目标】1.能辨识常见的分子晶体,并能从微观角度分析分子晶体中各构成微粒之间的作用和对分子晶体物理性质的影响。
2.能利用分子晶体的通性推断常见的分子晶体,理解分子晶体中微粒的堆积模型,并能用均摊法对晶胞进行分析。
3.能辨识常见的共价晶体,并能从微观角度分析共价晶体中各构成微粒之间的作用对共价晶体物理性质的影响。
4.能利用共价晶体的通性推断常见的共价晶体,并能利用均摊法对晶胞进行分析。
【基础知识】一、分子晶体(一)分子晶体的概念与性质1、分子晶体的概念只含分子的晶体,或者分子间以分子间作用力结合形成的晶体叫分子晶体。
2、分子晶体中的粒子及粒子间的相互作用3、常见的典型分子晶体(1)所有非金属氢化物:如H2O、H2S、NH3、CH4、HX(卤化氢)等。
(2)部分非金属单质:如X2(卤素单质)、O2、H2、S8、P4、C60、稀有气体等。
(3)部分非金属氧化物:如CO2、SO2、NO2、P4O6、P4O10等。
(4)几乎所有的酸:如H2SO4、HNO3、H3PO4、H2SiO3等。
(5)绝大多数有机物:如苯、四氯化碳、乙醇、冰醋酸、蔗糖等。
4、分子晶体的物理性质(1)分子晶体熔、沸点较低,硬度很小。
(2)分子晶体不导电。
(3)分子晶体的溶解性一般符合“相似相溶”规律。
5、分子晶体的判断方法(1)依据物质的类别判断部分非金属单质、所有 非金属氢化物 、部分非金属氧化物、几乎所有的酸、绝大多数有机物都是分子晶体。
(2)依据组成晶体的粒子及粒子间作用判断组成分子晶体的微粒是分子,粒子间的作用力是分子间作用力。
(3)依据物质的性质判断分子晶体的 硬度 小, 熔、沸点 低,在熔融状态或固体时均不导电。
6、分子晶体熔、沸点高低的判断(1)组成和结构相似,不含氢键的分子晶体,相对分子质量越 大 ,范德华力越 强 ,熔、沸点越 高 ,如I 2>Br 2>Cl 2>F 2,HI >HBr >HCl 。
分子晶体和原子晶体

HXC60P106, P1010都形成分子晶体,只有很少的一部分和______SiO2,碳化硅,第二节分子晶体和原子晶体一、分子晶体(一)、概念:分子间以______________________ (_____________ , ________________ )相结合的晶体叫分子晶体。
注意:(1)构成分子晶体的粒子是 ______________________ 。
(2 )在分子晶体中,分子内的原子间以结合,而相邻分子靠或相互吸引。
(3 )范德华力化学键的作用:(4 )分子晶体熔化破坏的是O(二)•分子晶体的物理特性:(1)___ 的熔点和沸点,(2) ______________ 的硬度,________ 挥发, _________ 升华(3)—般都是________ 体,固体和熔融状态都__________________ 导电。
(4)分子晶体的溶解性与溶质和溶剂的分子的___________________ 相关一一____________________思考:1、为什么分子晶体熔沸点低、易挥发、易升华、硬度小?原因:分子晶体发生这些变化时_只破坏 __________________________ , ________________ 很弱,克服它时需要的能量小。
所以分子晶体熔沸点低、易挥发、易升华、硬度小。
2、为什么分子晶体在晶体和熔融状态均不导电?它们在晶体和熔融状态均不存在_______________________ 。
部分分子晶体溶于水在水分子作用下发生_____________ 导电,如HCI, H2S04 ;有些溶于水与水反应生成_______________________________ 而导电,晶体硼等。
)(四)分子晶体结构特征1. ______________________________ __ 分子密堆积每个分子周围有______________ 个紧邻的分子,如:C60、干冰、12、02——不具有分子密堆积特征P1,CH4,2,冰中1个水分lmol冰周I韦]有mol氢键。
3.2分子晶体和原子晶体

氢键具有方向性
冰中1个水分子周围有几个水分子?为什么?
冰中1个水分子周围有4个水分子
【思考与交流】
1.分子晶体有哪些物理特性,为什么? 2.怎样判断分子间作用力的大小?分子间作用力 对分子的熔沸点有什么影响?
5.分子晶体的物理性质
(1)性质:
分子晶体熔沸点低、硬度小、易升华,固体 和熔融状态不导电,有些在水溶液中能导电。
12g金刚石C-C键数为多少NA?
①金刚石中每个C原子以sp3杂化,分别与4个 相邻的C 原子形成4个σ 键,故键角为 109°28′,每个C原子的配位数为4; ②每个C原子均可与相邻的4个C构成实心的正 四面体,向空间无限延伸得到立体网状的金刚 石晶体,在一个小正四面体中平均含有 1+4×1/4 =2个碳原子; ③在金刚石中最小的环是六元环,1个环中平 均含有6×1/12=1/2个C原子,含C-C键数为 6×1/6=1; ④金刚石的晶胞中含有C原子为8个,内含4个 小正四面体,含有C-C键数为16。
4.分子晶体的结构特征
(1)只有范德华力,无分子间氢键 —分子密堆积
每个分子周围有12个紧邻的分子
如: C60、干冰 、O2 等
(2)有分子间氢键 —分子非密堆积 如:HF 、冰、NH3 水分子之间的主要作用力是 氢键
氢键具有 方向性 有 紧邻的 4 个 水分子
,由于
,故在冰的每个水分子周围只
分子的非密堆积
(2)本质原因:
分子间作用力很弱。 ---分子间作用力强弱 (3)熔沸点的比较: A.组成和结构相似的物质,相对分子质量越大, 熔沸点越高。 B.组成和结构不相似的物质,分子极性越大, 熔沸点越高。 C.分子间有氢键的物质熔沸点反常。
【问题探究】
分子晶体

5、比较下列几组晶体熔沸点高低的顺序(由高到低) 1、金刚石、氯化钠、晶体硅、干冰
金刚石、晶体硅、氯化钠、干冰
2、石英、铝硅合金、晶体硅、冰
石英、晶体硅、铝硅合金、冰
3、氧化钙、氯化钾、氯化钙、碘化钾 氧化钙、氯化钙、氯化钾、碘化钾 4、氧化镁、氧气、水、氮气
氧化镁、水、氧气、氮气
6、有A、B、C三种晶体,分别由C、H、Na、Cl 四种元素 中的一种或几种形成,对这三种晶体进行实验,结果如下:
4、下列八种晶体:A水晶 B冰醋酸 C氧化镁 D白磷 E氩晶 体 F硫酸铵 G铝 H金刚石 ⑴属于原子晶体的化合物是 A E 分子晶体是 。 ⑵含有共价键的离子晶体是 是 DE 。 F ,直接由原子构成的 属于分子晶体的单质 G
⑶在一定条件下,能导电而不发生化学变化的
受热 熔化后不发生化学键断裂的是 化需克服共价键的是 AH 。 BD
分子晶体
制作:田俊良
四.分子晶体
1.概念
分子间以分子间作用力(范德华力, 氢键)相结合的晶体叫分子晶体。 **构成分子晶体的粒子是分子, 粒子间的相互作用是分子间作用力 .
分子晶体有哪些物理特性,为什么?
2.分子晶体的物理特性
由于分子间作用力很弱,所以分子晶体一般具 有: ①较低的熔点和沸点 ②较小的硬度。 ③一般都是绝缘体,熔融状态也不导电。
7、HgCl2的稀溶液可用做手术刀的消毒剂,已知HgCl2的 熔点是277℃,熔融状态的HgCl2不能导电,且稀溶液有弱 的导电能力,则下列叙述中正确的是 AD
A、 HgCl2 属于共价化合物 C、 HgCl2 属于非电解质 B、 HgCl2属于离子化合物 D、 HgCl2属于弱电解质
8、有关晶体的叙述中正确的是
3.1四种晶体

2、常见离子晶体
强碱、金属氧化物、部分盐类 ①NaCl 晶体
阴离子配位数 6
阳离子配位数 6
NaCl 晶体
每个晶胞中 Cl—有 4 个 Na +有 4 个 每个Cl— 周围最近且等距离的Cl—有 12 个 每个Na+周围最近且等距离的Na+有 12 个
__2_:_3___.
小结1:分子晶体与原子晶体的比较
相邻原子间以共价键相结 分子间以分子间 合而形成空间网状结构 作用力结合
原子 共价键 很大 很大 不溶于任何溶剂
不导电,个别为半导体
分子 分子间作用力
较小
较小 部分溶于水 固体和熔化状态 都不导电,部分 溶于水导电
第三章 晶体的结构与性质
第三节 金属晶体
简单立方堆积的空间占有率 =52%
球半径为r 正方体边长为a =2r
②体心立方堆积(钾型)K、Na、Fe
体心立方堆积的配位数 =8
体心立方堆积的空间占有率 =68%
体对角线长为c 面对角线长为b 棱线长为a 球半径为r
c2=b2+a2 b2=a2+a2 c=4r (4r)2=3a2
③六方最密堆积(镁型)Mg、Zn、Ti
12
6
3
A
54
B
A
B A
六方最密堆积的配位数 =12
六方最密堆积的晶胞
六方最密 堆积的晶胞
六方最密堆积的空间占有率 =74% 上下面为菱形 边长为半径的2倍 2r
高为2倍 正四面体的高
2 6 2r 3
温馨提示:为更好地满足您的学习和使用需求,课件在下载后可以自由编辑,请您根据实际情况进行调整!Thank you for
高中化学-分子晶体和共价晶体

第二节分子晶体和共价晶体一、分子晶体1.概念:只含分子的晶体。
2.粒子间的作用分子晶体中相邻的分子间以分子间作用力相互吸引。
3.常见分子晶体及物质类别【注】稀有气体为的分子为单原子分子,因此,有稀有气体单质形成的晶体也是分子晶体。
4.物理特性(1)分子晶体的熔、沸点较低,密度较小,硬度较小,较易熔化和挥发,部分分子晶体易升华,(如干冰、碘、红磷等)。
(2)一般是绝缘体。
分子晶体在固态和熔融状态下均不存在自由移动的离子或自由电子,因而分子晶体在固态和熔融状态下都不能导电。
有些分子晶体的水溶液能导电,如HI、乙酸等。
(3)溶解性符合“相似相溶规律”。
【注】分子晶体熔、沸点高低的比较规律①分子晶体中分子间作用力越大,物质熔、沸点越高,反之越低。
②具有氢键的分子晶体,熔、沸点反常高。
5.分子晶体的常见堆积方式6.常见分子晶体的结构分析(1)冰①水分子之间的主要作用力是氢键,当然也存在范德华力。
②氢键有方向性,它的存在迫使在四面体中心的每个水分子与四面体顶角方向的4个相邻水分子互相吸引。
(2)干冰①干冰中的CO 2分子间只存在范德华力,不存在氢键。
②每个晶胞中有4个CO 2分子,12个原子。
每个CO 2分子周围等距离紧邻的CO 2分子数为12个。
【注】冰晶体中,每个水分子与其他4个水分子形成氢键,每个水分子平均形成2个氢键(每个氢键由2个水分子均摊,故4×21=2)二、共价晶体1.定义:所有原子都以共价键相互结合形成共价键三维骨架结构的晶体叫共价晶体。
2.构成微粒及微粒间的作用力共价晶体⎩⎨⎧ 构成粒子:原子粒子间作用力:共价键【注】①共价晶体中不存在单个分子,因此,共价晶体的化学式不代表其实际组成,只表示其组成的原子个数比。
①共价晶体融化时被破坏的作用力是共价键。
①共价晶体中只有共价键,但含有共价键的晶体不一定是共价晶体。
如CO2、H2O等分子晶体中也含有共价键。
3.常见的共价晶体4.共价晶体的物理性质(1)熔点很高。
分子晶体

高级教师:夏磊
分子晶体与原子晶体
复习总结:
微粒间作用
微粒为分子: 分子间作用力(或范德华力)或氢键; 微粒为原子:极性共价键或非极性共价键; 微粒为离子:离子键。
一、分子晶体
1、 只含分子的晶体称为分子晶体。如碘晶体只含 I2分子,属于分子晶体。在分子晶体中,分子内的原 子间以共价键结合,而相邻分子靠分子间作用力或氢 键相互吸引。 碘 晶 体 结 构 **构成分子晶体的粒子是分 子,粒子间的相互作用是分 子间作用力或氢键
分子晶体有哪些物理特性,为什么?
2、分子晶体的一般宏观性质 ①较低的熔沸点 ②较小的硬度 ③固态或熔融状态下都不导电 ④分子晶体的溶解性与溶质与溶剂的 分子的极性相关 —— 相似相溶 构成分子晶体的粒子是分子,粒子间的相互作 用是分子间作用力或氢键
3、属于分子晶体的化合物类别举例 (1)所有非金属氢化物:H2O,H2S,NH3,CH4, HX (2)部分非金属单质:X2,O2,H2, S8,P4, C60 (3)部分非金属氧化物:CO2, SO2, NO2, P4O6,P4O10 (4)几乎所有的酸:H2SO4,HNO3,H3PO4 (5)绝大多数有机物晶体:乙醇,冰醋酸,蔗糖
(1)只有范德华力,无分子间氢键-分子密堆积 (每个分子周围有12个紧邻的分子,如:C60、干冰 、 I2、O2 (2)有分子间氢键-不具有分子密堆积特征 (如:HF 、冰、NH3 )
思 考与交流
CO2和SiO2的一些物理性质如下表所示,通过比较试 判断SiO2晶体是否属于ห้องสมุดไป่ตู้子晶 体。
4.晶体分子结构特征 (1)只有范德华力,无分子间氢键-分子密堆积 (每个分子周围有12个紧邻的分子,如:C60、干 冰 、I2、O2) (2)有分子间氢键-不具有分子密堆积特征(如: HF 、冰、NH3 )
分子晶体的特征

分子晶体的特征
分子晶体是由一系列单个分子或分子簇构成的晶格,是实际应用最为广泛的一种晶体。
分子晶体的特征主要可以分为物理性质、化学性质和结构性质三部分。
1.物理性质
分子晶体的物理性质包括晶体的晶格常数、晶体的热学性质以及导电性等。
晶格常数是指构成晶体单元格的四周的距离,通常由晶体结构所决定,物质类型和温度也有影响。
晶体的热学性质是指晶体的热导率、热容量等,热容量是指晶体贮存的热量。
晶体的导电性是指晶体的电导率,电导率取决于晶体结构以及温度。
2.化学性质
分子晶体的化学性质包括缔合性质、溶解度、酸碱度及抗腐蚀性等。
缔合性质是指分子晶体中分子簇之间的结合性,而溶解度则可以用来衡量晶体在溶剂中的分解速度。
酸碱度可以用来衡量晶体的酸化和碱化反应是否可以发生,而抗腐蚀性可以用来衡量晶体在多种腐蚀性介质中的耐受度。
3.结构性质
分子晶体的结构性质最常见的表现形式是其单元格结构,晶体结构的形式可分为单斜晶体、二斜晶体、三斜晶体和体心立方晶体等。
另外,晶体的显微结构还会受到分子簇之间的结合性以及晶体热力学稳定性的影响。
- 1 -。
第三章 第二节 第1课时 分子晶体(教师版)

第二节分子晶体与原子晶体第1课时分子晶体一、分子晶体及其结构特点1.概念分子间通过分子间作用力相结合形成的晶体。
2.微粒间作用分子晶体中相邻的分子间以分子间作用力相互吸引。
3.常见分子晶体及物质类别物质类别实例所有非金属氢化物H2O、NH3、CH4等部分非金属单质卤素(X2)、O2、N2、白磷(P4)、硫(S8)等部分非金属氧化物CO2、P4O10、SO2、SO3等几乎所有的酸HNO3、H2SO4、H3PO4、H2SiO3等绝大多数有机物的晶体苯、乙醇、乙酸、乙酸乙酯等4.两种典型分子晶体的组成与结构(1)干冰①每个晶胞中有4个CO2分子,12个原子。
②每个CO2分子周围等距离紧邻的CO2分子数为12个。
(2)冰①水分子之间的作用力有范德华力和氢键,但主要是氢键。
②由于氢键的方向性,使在四面体中心的每个水分子与四面体顶角方向的4个相邻水分子相互吸引。
判断正误(1)分子晶体中,一定存在共价键和分子间作用力() (2)分子晶体中只存在分子间作用力() (3)共价化合物一定属于分子晶体() (4)干冰晶胞中含有4个CO2分子()(5)分子晶体中一定含有分子间作用力,不一定含有化学键()答案(1)×(2)×(3)×(4)√(5)√1.下列物质中,属于分子晶体的是________。
①二氧化硅 ②碘 ③食盐 ④蔗糖 ⑤磷酸答案 ②④⑤解析 由常见分子晶体对应的物质类别可知:碘、蔗糖、磷酸都属于分子晶体。
2.甲烷晶体的晶胞结构如图所示(1)晶胞中的球只代表1个__________。
(2)晶体中1个CH 4分子有______个紧邻的CH 4分子。
(3)甲烷晶体熔化时需克服______。
(4)1个CH 4晶胞中含有______个CH 4分子。
答案 (1)甲烷分子 (2)12 (3)范德华力 (4)4解析 (1)题图所示的甲烷晶胞中的球代表的是1个甲烷分子。
(2)由甲烷晶胞分析,位于晶胞顶点的某一个甲烷分子与其距离最近的甲烷分子有3个,而这3个甲烷分子在晶胞的面上,因此每个都被2个晶胞共用,故与1个甲烷分子紧邻的甲烷分子数目为3×8×12=12。
分子晶体

◆从性质上判断: 从性质上判断:
离子晶体; ●熔沸点和硬度;(高:原子晶体;中:离子晶体; 熔沸点和硬度; 高 原子晶体; 分子晶体) 低:分子晶体 熔融状态的导电性。 导电 离子晶体) 导电: ●熔融状态的导电性。(导电:离子晶体
● A.食盐和蔗糖熔化 B.钠和硫熔化 食盐和蔗糖熔化 钠和硫熔化 C.二氧化硅和氧化钠熔化 D.碘和干冰升华 二氧化硅和氧化钠熔化 碘和干冰升华
二氧化碳晶体结构模型
一个晶胞中CO2 一个晶胞中 分子的个数: 分子的个数: 8×1/8+6×1/2=4 × ×
干冰的晶体结构图
可见:每个二氧化碳分子周围与之距离最近且相 每个二氧化碳分子周围与之距离最近且相 等的二氧化碳分子有 12 个
晶体类型的判断
◆从组成上判断(仅限于中学范围): 从组成上判断(仅限于中学范围): 从组成上判断
晶体熔沸点高低的判断
⑴不同晶体类型的熔沸点比较 一般:原子晶体>离子晶体>分子晶体(有例外) 一般:原子晶体>离子晶体>分子晶体(有例外) ⑵同种晶体类型物质的熔沸点比较 离子晶体: ①离子晶体: 组成相似的离子晶体 离子半径越小、离子电荷数越多 离子半径越小、 熔沸点越高 原小→键长越短→键能越大 熔沸点越高 ③分子晶体: 组成和结构相似的分子晶体 分子晶体: 相对分子质量越大 熔沸点越高
分子晶体
1、分子晶体: 、分子晶体: (1)定义:分子间通过分子间作用力结合而 )定义: 成晶体。 成晶体。 构成微粒: 构成微粒: 微粒间的作用力: 微粒间的作用力: 分子 分子间作用力
分子晶体的物质类别

分子晶体的物质类别
分子晶体是一种晶体结构,由分子组成。
根据分子间的相互
作用和排列方式,可以将分子晶体分为以下几种物质类别:
1.共价分子晶体:共价分子晶体由共价键连接的分子组成。
在这种晶体中,每个分子都保持其完整的结构和完整的共价键。
例如,石墨是由碳原子构成的共价分子晶体,在石墨中,碳原
子形成了层状结构,并以弱的范德华力相互吸引。
2.极性分子晶体:极性分子晶体由带有正负电荷的极性分子
组成。
这些极性分子通过静电相互作用形成结晶。
例如,氯化
钠是典型的极性分子晶体,由带有正电荷的钠离子和带有负电
荷的氯离子组成。
3.范德华分子晶体:范德华分子晶体由非极性分子组成,分
子间相互作用主要是范德华力。
这种晶体的分子间力较弱,因
此通常具有较低的熔点和挥发性。
例如,固体二氧化碳(干冰)就是一个范德华分子晶体。
4.氢键分子晶体:氢键分子晶体是通过氢键相互连接的分子
构成的晶体。
氢键是一种静电吸引力,通常是在一个氢原子与
一个电负性较强的原子之间形成的。
许多生物分子和有机化合
物可以形成氢键分子晶体,例如冰和尿素晶体。
5.配位分子晶体:配位分子晶体由金属离子和有机配体分子
组成。
在这种晶体中,金属离子作为中心原子与多个配体分子
形成化学键。
这种晶体具有较高的熔点和硬度,通常具有特殊的化学和物理性质。
这些是分子晶体的一些基本物质类别,每种类别都有其特定的结构和性质。
分子晶体在化学、材料科学和生物学等领域具有重要的应用价值。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、分子晶体
6、分子晶体物理特性:※※※※※ ①较低的熔点和沸点(易升华或易挥发) ②较小的硬度
③只存在分子,不存在离子,一般都是绝缘体,固态 及熔融状态也不导电。溶于水时部分导电 ④多数能溶于适当的溶剂(相似相溶)。
【问题探究】
1、分子晶体是否导电?什么条件下可以导电? 由于构成分子晶体的粒子是分子,不管是晶体或 晶体熔化成的液体,都没有带电荷的离子存在,因此, 分子晶体以及它熔化成的液体都不导电。 分子晶体溶于水时,水溶液有的能导电,如 HCl溶于水,有的不导电,如C2H5OH溶于水。
4、选择以下物体填写下列空白
A干冰
AD(填写序号,下同) ⑵晶体中既有离子键又有共价键的是 BC ⑶熔化时不需要破坏共价键的是 ACD ⑷常况下能升华的是 AD
⑴晶体中存在分子的是 5、下列分子晶体:①HCl ②HBr ③HI ④CO ⑤N2 ⑥H2熔沸点由高到低的顺序是③②①④⑤⑥
B氯化铵
C烧碱
【小结】
晶体类型 分子晶体
构成晶体的粒子类 型 结构
粒子间的相互作用 力 硬度 熔沸点 性质 导电性 溶解性 物质 类别
分子 分子间作用力(范德华力、金属氢化物、部分非金属单质、部分非 金属氧化物、几乎所有酸、绝大多数有机物
【科学视野】 天然气水合物 — 一种潜在的能源 笼状化合物
①密堆积:如果分子间作用力只有范德华力,无分子间 氢键-分子采用密堆积,如:C60、干冰 、I2、O2。 重要结论:与CO2分子距离最近的CO2分子共有12个 即配位数为12
一、分子晶体
4、分子晶体的两种堆积方式: ②非密堆积:如果分子间作用力还有氢键-采用非密 堆积(如:HF 、冰、NH3 )
冰的结构
重要结论:1个水分子周围距离最近有4个水分子
一、分子晶体
5、常见的分子晶体
①所有非金属氢化物: H2O、H2S、NH3、CH4、HX ②几乎所有的酸: H2SO4、HNO3、H3PO4(碱和盐则是离子晶体) ③部分非金属单质: X2、O2、H2、 S8、P4、C60 、稀有气体 ④部分非金属氧化物: CO2、SO2、NO2、 P4O6、 P4O10 ⑤绝大多数有机物的晶体: 乙醇、冰醋酸、蔗糖、 苯、萘、蒽、苯甲酸等
【资料卡片】
能“燃烧”的冰
1、下列属于分子晶体的一组物质是 A 、CaO、NO、CO B、 CCl4、H2O2、He C、 CO2、SO2、NaCl D 、CH4、O2、Na2O
B
2、下列性质符合分子晶体的是 B A、 熔点1070℃,易熔于水,水溶液能导电 B、 熔点是10.31℃,液体不导电,水溶液能导电 C、 熔点97.81℃,质软,能导电,密度是0.97g/cm3 D、 熔点870℃ ,熔化时能导电,水溶液也能导电 3、四氯化硅的分子结构与四氯化碳类似,对其作出如 下推测①四氯化硅晶体是分子晶体。②常温常压下四氯 化硅是液体。③四氯化硅分子是由极性键形成的分子。 ④四氯化硅熔点高于四氯化碳。其中正确的是 A只有① B只有①② C只有②③ D①②③④ D
金刚石
干冰
干冰 干冰
金刚石
1、 CO2和SiO2的原子个数比相同,为什么 二者的熔点、沸点、硬度却差距很大? 2、金刚石为什么被称为硬度大王?
一、分子晶体
【思考交流1】 观察下列两种晶体的晶胞找出两种晶体的共同点?
碘晶胞
二氧化碳晶胞
结论:构成微粒都是分子。 都是面心立方晶胞。
一、分子晶体
4、分子晶体的两种堆积方式:
4、五边形和六边形数目的求法: 设五边形为 x个,六边形为y个, 则有:5x/3+2y=n n+(x+y) - 3n/2=2(欧拉定理: 顶点数+面数-棱边数=2)
D固体碘
方法指导:
1、Cn中有五边形和六边形,每个五边形占有的碳原子 数为5/3个,而每个六边形占有的碳原子数为6/3个(因为 每个碳原子与另3个碳原子结合) 2、由于每个孤立的碳原子周围有3个键(1个双键,2个单 键),而每个键又是2个碳原子所共有,因此棱数=3n/2 3、单、双键数的求法:单键数+双键数=总棱边数 单键数=2*双键数
2、怎样判断分子晶体的溶解性? “相似相溶” :非极性溶质一般能溶于非极性溶剂; 极性溶质一般溶于极性溶剂。 当某些分子晶体溶于水时,若能与水分子之间形成 氢键,则溶质的溶解度会显著增大。如NH3极易溶于水, 甲醇、乙醇、甘油、乙酸等能与混溶,就是它们与水形 成了分子间氢键的缘故。
【问题探究】
3、是不是在分子晶体中分子间只存在范德华力? 4、为何分子晶体的硬度小,熔沸点低? ①构成晶体的微粒是分子 ②分子之间以分子间作用力(主要是范德华力)相结 合,范德华力远小于化学键的作用 5、分子晶体的密度取决于晶体的体积,取决于紧密堆 积程度,分子晶体的紧密堆积由以下两个因素决定: ①分子间作用力的强弱 ②分子间的排列顺序 6、为何干冰的熔沸点比冰低,密度却比冰大? 由于冰中除了范德华力外还有氢键作用,破坏分子 间作用力较难,所以熔沸点比干冰高。 由于分子间作用力特别是氢键的方向性,导致晶体 中有相当大的空隙,所以相同状况下体积较大。 由于CO2的相对分子质量>H2O,所以干冰的密度大。
