海水的物理性质
《第二节海水的性质》公开课优秀教案教学设计

《第二节海水的性质》公开课优秀教案教学设计第二节海水的性质一、教学目标1. 知识与技能目标:- 了解海水的组成成分及其含量;- 掌握海水的物理性质和化学性质;- 能够分析海水溶解物质的来源和影响因素。
2. 过程与方法目标:- 通过参与课堂讨论和实验操作,培养学生主动探究的意识和科学实践能力;- 引导学生分析物质组成、观察现象、实验操作、结果分析等环节的科学思维方法。
3. 情感、态度与价值观目标:- 培养学生的海洋环保意识,强调对海洋资源的珍惜、保护;- 培养学生的科学探究兴趣和对海洋科学的好奇心。
二、教学重难点1. 教学重点:- 海水的组成成分及其含量;- 海水的物理性质和化学性质。
2. 教学难点:- 海水中不同成分的相互作用及其影响因素;- 海水溶解物质的来源与变化。
三、教学过程与方法1. 创设情境教师介绍《第二节海水的性质》主题,并与学生进行互动,引发学生对海水特性的兴趣和思考。
例如:你们平时去海边玩的时候有没有观察到海水的不同之处?海水是什么颜色的?为什么海水咸呢?2. 学法指导教师引导学生通过观察、实验、分析等方式,主动参与探究海水性质。
例如:让学生观察一瓶盐水和一瓶淡水,分析两者的区别,并预测海水与淡水的差异。
3. 学习活动Step 1: 海水的组成成分及其含量- 学生观察海水的颜色、咸味等特点,思考海水中含有哪些物质;- 学生利用历史数据或实验数据,分析海水中盐类、矿物质、有机物质等成分的含量。
Step 2: 海水的物理性质- 学生进行实验,测量海水的密度、沸点、冰点等物理性质,并与淡水进行对比;- 学生探究海水的导电性、折射率等性质,并解释其现象。
Step 3: 海水的化学性质- 学生进行一些简单的化学反应实验,观察海水与不同试剂的反应,并解释反应原理;- 学生分析海水的酸碱性、氧化还原性等化学性质,指出其中的关键因素。
Step 4: 海水溶解物质的来源与变化- 学生通过资料和实验,了解海洋对大气、陆地、火山等来源的溶解物质;- 学生分析海水溶解物质受温度、光照、生物活动等因素的影响程度。
物理海洋--整理
....... 第四章 水团分析
第一节 水团的基本概念和术语 水团:是在一定的时期中形成于同一源地的、一定体积的水体,在同一水团内,主要海 洋学特征(温度、盐度等)在空间上具有相对的均一性,在时间上具有大体一致的变化 趋势,与其周围海水的物理、化学性质及其变化规律存在明显差异。 核心,边界,强度,形成和变性,运动和海流
可从纬向,经向,区域,垂向各个方面讨论。 大洋密度的时间变化 密度跃层(温度跃层):春季形成,夏季强盛,秋冬衰亡。
第六节 海洋温度、盐度、密度的细微结构 双扩散对流:当高温高盐水和低温低盐水重叠且呈稳定层结时,若上下密度差异小,由 于分子热传导效应比盐度扩散效应强得多,则上层海水因失热较快而冷却下沉,下层则 因受热较快而增温上升,于是形成双扩散对流。 盐指:由于双扩散对流,而在界面上出现的簇状小长柱结构。 多层阶梯状结构:界面上下的水层,因升降盐指的搅拌而趋于均匀,逐渐形成多层阶梯 状结构。
小。 渗透压:渗透作用达到平衡状态时,膜两侧的压力之差。 粘度:相邻水层之间存在相对运动,由于分子不规则运动,产生动量传递,从而形成切 应力。
第一节 海洋热平衡分量
第三章 海洋表面热平衡和水平衡
穿过海表面热交换的四个过程:
来自太阳的短波辐射 ——太阳辐射能
大气与海洋之间的长波(红外光部分)辐射热交换 ——有效回辐射
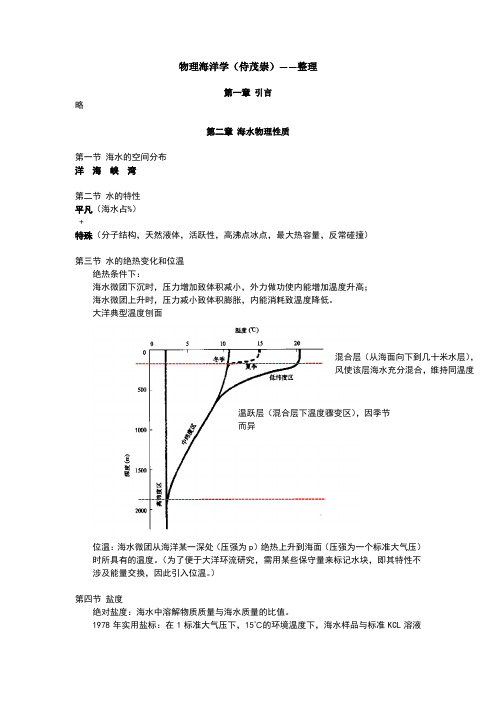
混合层(从海面向下到几十米水层), 风使该层海水充分混合,维持同温度
温跃层(混合层下温度骤变区),因季节 而异
位温:海水微团从海洋某一深处(压强为 p)绝热上升到海面(压强为一个标准大气压) 时所具有的温度。(为了便于大洋环流研究,需用某些保守量来标记水块,即其特性不 涉及能量交换,因此引入位温。) 第四节 盐度 绝对盐度:海水中溶解物质质量与海水质量的比值。 1978 年实用盐标:在 1 标准大气压下,15℃的环境温度下,海水样品与标准 KCL 溶液
海洋物理学的基本原理和应用

海洋物理学的基本原理和应用海洋物理学是研究海洋的物理性质、过程和现象的科学学科。
它探究海洋中的水文、气象、波浪、潮汐、海流等各种物理过程,以及它们在海洋环境中的相互作用和影响。
海洋物理学的研究为我们理解和预测海洋的运动和变化提供了重要的基础和方法。
同时,海洋物理学在海洋资源开发、环境保护、海洋工程等领域也有着广泛的应用。
一、海洋物理学的基本原理海洋物理学的研究基于以下几个基本原理:1. 海水的性质:海水的物理性质如密度、温度和盐度对海洋物理过程具有重要影响。
海水的密度决定了海洋中的水团运动和混合,而温盐变化则直接影响海洋的密度结构和环流。
2. 海洋的运动:海洋中的运动包括水平和垂直方向的运动。
水平运动主要是海流,它受到风、地转偏向力、潮汐等影响。
垂直运动主要包括垂直混合和水团下沉等过程,它们对海洋环境中养分供应和能量传递起着重要作用。
3. 波浪和潮汐:海洋中的波浪和潮汐现象受到地球引力和海底地形的影响。
波浪是海洋中的表面波动,它们对海岸侵蚀、海水交换和航海安全等具有重要影响。
潮汐是由太阳和月亮引力造成的周期性海平面变化,它对海岸线、海洋生物和能源利用等都具有一定影响。
二、海洋物理学的应用海洋物理学的研究成果在许多领域具有重要的应用价值。
1. 海洋资源开发:海洋物理学可以通过研究海水中的养分分布和海流运动,为海洋渔业、沿海水产养殖等资源开发提供科学依据。
2. 海洋环境保护:海洋物理学可以用于研究海洋污染物的传输和扩散规律,预测海洋环境的受污染程度,从而制定有效的环境保护措施。
3. 海洋工程建设:海洋物理学可以用于研究海浪、海流对海洋工程结构和船舶安全的影响,为设计和建设海洋工程提供技术支持。
4. 气象预报和海上安全:海洋物理学可以通过观测和分析海洋中的风、波浪和气象变化,提供海上气象预报和航海安全预警。
5. 气候变化研究:海洋物理学的研究对于理解全球气候变化有着重要作用,海洋作为地球的热力和碳汇,其运动和变化对全球气候具有重要影响。
海水的性质

海水的性质
2021-02-20
海水的性质主要包括海水温度、海水密度、海水的颜色和透明度、海水成分、海水的盐度、营养盐类等。
海水的密度比纯水大,约为1.022~1.028g/cm3它随温度、盐度和气压而变化。
海水的性质
1海水的性质
海水的物理性质主要包括温度、密度、透明度、海冰等。
海水温度是度量海水热量的一个重要指标,也是海洋热能的一种表现形式。
海洋热能不仅驱动大部分的大洋环流,而且还制约着海洋生物系统运转的速率。
海洋热量的收入,主要是来自太阳辐射的热量。
有研究表明,到达海面的太阳总辐射的年总量达12.6*1020~
13.6*1020kJ。
其中8%的热量被反射回大气,其他的全部被海水所吸收。
海洋表面年平均温度在-2℃~30℃,全球海洋年平均水温为17.4℃,相比全球年平均气温,要高出3.1℃。
海水的物理化学特性

如何把已经产生的过剩CO2除去就更令人感兴趣。
3、 海水中的营养元素
海水中由N、P、Si等元素组成的某些盐类,是海洋植物生长 必需的营养盐,通常称为“植物营养盐、“微量营养盐”或 “生源要素”。
②降水 为海洋水收入的最重要因子。每年达411~416×103km3。
③大陆径流 大陆径流及地下水入海是海洋水量收入的另一重要因子。 进入各大洋的径流量最大的为大西洋,其次为印度洋。对太 平洋来说,注入最大的河流是中国的长江。
④结冰与融冰 结冰与融冰为海洋水平衡中的可逆过程。 海冰被海水冲击到陆地上使海洋失去水量,相反,冻结在陆 地上冰的融化会使海洋水量增加。 如果被冻结在陆地上的冰全部融化流入海洋,将使海平面上 升66m。 就目前地质年代而言,结冰与融冰的量基本上是平衡的。
食盐:烹调必须的成份,化学工业的重要原料。海水质量 的3.5%是溶解固体物,其中氯化钠占71%。
镁:海水中仅次于氧、氢、氯、钠含量最多的元素。在各 种建筑结构中有广泛用途。
溴:海水中丰度列第九位的元素,是海水制盐或海水提镁 的副产物,它可用作汽油的抗爆化合物,也可用于制药。
铀:在海水中的浓度是溴的1/2000,即使如此,许多国家 仍在开展海水提取铀的研究,以期获得铀的稳定来源。但目前 陆源的铀成本低得多,故海水提铀尚难进入商业化。
(4)水的密度变化有反常 “热胀冷缩”是一般物质的性质。 纯水在大气压力下,温度4℃时密度最大,为1000kg·m3; 4℃以上时,密度随温度的降低而增大; 4℃以下时却随温度的降低而减小,即所谓“反常膨胀”。 水结冰时体积增大,密度减小,可达916.7 kg·m3,所以冰总
第三章 海水的物理性质

3
• 由于水分子的偶极子结构,使其 溶点和沸点大幅提高,否则只能 以气体形式存在,不能形成海洋 和生命! • 水是地球上唯一可同时存在固、 液、气三态的物质 • 水的溶解力很强 • 水分子有很强的极性,容易吸引 溶质表面的分子或离子,使其脱 离溶质的表面进入水中 • 水可轻易将盐分解为离子状态 • 海水的溶解性和腐蚀性更强
• 海洋的平均盐度为34.7;红海最高36-38;波罗地海最低7-8 • 影响盐度的因素:
外海大洋:蒸发和降雨 沿岸海域:径流
• 低、高纬度海区的盐度,哪一个高?
18
盐量的循环
• 海浪破碎会产生大量气泡,气泡上升到海面破碎 形成小水滴,大风时风会直接将波峰撕裂而生成 水滴,水滴在空中蒸发而成为盐粒子,成为海盐 气溶胶进入大气中,饱和水汽以它为凝结核,形 成雨滴落到陆地上,最后汇聚到河流又回到海洋
3 4 5 10.67869 R15 5.98624 R15 1.32311R15
为15ºC,一个标准大气压(101325 Pa)下,水样的电 导率C(S,15,0)与盐度精确为35‰的标准海水电导率C(35,15,0) 之比值,通过测定海水的电导率来推算盐度值 • 国际“海洋学常用表和标准联合专家小组”(JPOTS)于 1969年推荐使用此新定义 • 缺点:
“1kg海水中的碳酸盐全部转换成氧化物,溴和碘以氯当 量置换,有机物全部氧化后所剩固体物质的总克数”。单 位是g/kg,用符号‰表示
• 该方法测定盐度非常繁琐,不适用于海洋调查
12
海水的盐度
• Knudsen公式(化学方法) 基于海水组成恒定性规律,用测定海水氯 含量的方法来计算盐度 S ‰ = 0.03 + 1.805 CI ‰
盐度越大越容易结冰吗?
九年级化学海水中的化学知识点

九年级化学海水中的化学知识点海洋是地球上最广阔的水生环境,其中最重要的代表就是海水。
海水中包含了各种化学成分,对人类和地球生态系统都有着重要的影响。
在九年级化学中,我们学习了海水中的化学知识点,本文将围绕这些知识点展开讨论。
1. 海水的物理性质海水是一种混合物,其中包含了多种物理性质。
首先是海水的颜色,它通常为蓝绿色。
这是因为海水吸收了红色和橙色的光线,而反射了蓝色和绿色的光线。
此外,海水的深度对色彩的呈现也有影响。
水深越浅,颜色越明亮;水深越深,则颜色越暗淡。
其次是海水的密度。
海水的密度比淡水高,这是因为海水中含有各种盐类和矿物质。
随着深度的增加,海水的密度也逐渐增加。
这对生物在不同深度的海水中生存和繁衍都有很大的影响。
最后是海水的盐度。
海水中含有多种化学物质,其中以氯化钠的含量最大。
盐度的浓度会影响海水的密度和温度,从而对海洋环境和生物产生影响。
2. 海水中的离子和淡水相比,海水中含有更多的离子和化学物质。
其中最重要的是氯化物、钠离子、硫酸根离子和碳酸根离子。
这些离子在海洋环境中扮演了非常重要的角色。
氯化物是海水中含量最多的离子。
它们来自海洋中的多种化合物,如氯化钠和氯化镁等。
氯化物能保持海水的电解质平衡,同时对海洋生物的生存和繁殖也有贡献。
钠离子是海水中第二多的离子。
它们和氯化离子一样,来自多种化合物,特别是氯化钠。
钠离子在维持人体的酸碱平衡、肌肉和神经系统正常运作等方面具有重要作用。
硫酸根离子是来自硫酸的离子。
它们在海洋环境中起到了稳定盐度和pH值的重要作用。
同时,硫酸根离子还参与了海洋环境中的多种化学反应,如钙离子的沉淀等。
碳酸根离子则是海洋环境中最重要的电解质之一。
它们在碳酸盐循环中发挥了至关重要的作用。
碳酸循环是地球上最大的自然平衡之一,通过生物和非生物过程,使得地球上的海洋和大气中的二氧化碳得到平衡。
3. 海水的影响海洋中的化学物质和离子对人类和生态系统都有着很大的影响。
首先,海洋中的氯化物、钠离子和硫酸根离子都能影响海洋生物的生存和繁殖。
海水的理化性质#精选

海水的理化性质(一)海水的化学性质海洋是地球水圈的主体,是全球水循环的主要起点和归宿,也是各大陆外流区的岩石风化产物最终的聚集场所。
海水的历史可追溯到地壳形成的初期,在漫长的岁月里,由于地壳的变动和广泛的生物活动,改变着海水的某些化学成分。
1.海水的化学组成海水是一种成分复杂的混合溶液。
它所包含的物质可分为三类:①溶解物质,包括各种盐类、有机化合物和溶解气体;②气泡;③固体物质,包括有机固体、无机固体和胶体颗粒。
海洋总体积中,有96%~97%是水,3%~4%是溶解于水中的各种化学元素和其他物质。
目前海水中已发现80多种化学元素,但其含量差别很大。
主要化学元素是氯、钠、镁、硫、钙、钾、溴、碳、锶、硼、硅、氟等12种(表5.5),含量约占全部海水化学元素总量的99.8%~99.9%,因此,被称为海水的大量元素。
其他元素在海洋中含量极少,都在1mg/L以下,称为海水的微量元素。
海水化学元素最大特点之一,是上述12种主要离子浓度之间的比例几乎不变,因此称为海水组成的恒定性。
它对计算海水盐度具有重要意义。
溶解在海水中的元素绝大部分是以离子形式存在的。
海水中主要的盐类含量差别很大(表5.6)。
由表5.6可知,氯化物含量最高,占88.6%,其次是硫酸盐,占10.8%。
海水中盐分的来源,主要来自两个方面:一是河流从大陆带来。
河流不断地将其所溶解的盐类输送到海洋里,其成分虽与海水不同(表5.7)(海水中以氯化物为最多,河水则以碳酸盐类占优势),但是,因为碳酸盐的溶解度小,流到海洋里以后很容易沉淀。
另一方面,海洋生物大量地吸收碳酸盐构成骨胳、甲壳等,当这些生物死后,它们的外壳、骨胳等就沉积在海底,这么一来,使海水中的碳酸盐大为减少。
硫酸盐的收支近于平衡,而氯化物消耗最少。
由于长年累月生物作用的结果,就使海水中的盐分与河水大不相同。
二是海水中的氯和钠由岩浆活动中分离得来。
这从海洋古地理研究和从古代岩盐的沉积、以及最古老的海洋生物遗体都可证实古海水也是咸的。
教案第三章海水物理性质

第三章海水的物理特性和世界大洋的层化结构海水组成(ConstituentsofSeawater)一、海水组成(ConstituentsofSeawater):11种主要无机盐,占99.99%;海水:混合溶液=淡水+无机盐+有机物+悬浮质+……二、海水组成恒定性原理(Principleofconstantproportion):Marcet原理或Dittwar定律无论海水所溶解的盐类的浓度大小如何,其中常量离子间比值总是恒定的。
海水的物理性质一、淡水(Freshwater)分子结构(Molecularstructure):极性,分子缔合力溶解力强:水分子有很强的极性密度变化异常:不遵从“热胀冷缩”。
最大密度时温度是4摄氏度沸点(boilingpoint)和融点(meltingpoint)、比热(specificheat)、蒸发潜热(latentheatofvaporization)等热性质比氧的同族化合物高。
二、海水的热力学性质(Energeticpropertyofseawater)1)热容(seatcapacity)、比热容(specificheat)热容(heatCapacity):海水温度升高1K所吸收的热量。
(单位:J/K)比热容((specificheatcapacity)):单位质量海水的热容。
单位:J/(Kkg)定压比热Cp:在一定压力下测定的比热容。
定容比热Cv:在一定体积下测定的比热容。
二者皆是温(T)、盐(S)、压(P)的函数。
Cp在海洋学中较常用,比Cv值略大。
Cp值随盐度的增高而降低,随温度的变化比较复杂,低温、低盐时随温度升高而减小,高温、高盐时随温度升高而增大。
2)热膨胀热膨胀系数:温度升高1K单位体积海水的增量。
是T、S、P的函数。
海水的热膨胀系数比纯水的大,且随温度、盐度和压力的增大而增大;在大气压力下,低温、低盐海水的热膨胀系数为负值,说明当温度升高时海水收缩。
海水的物理性质

② 铅直分布:存在盐度跃层。 ③ 盐度变化:盐度变化规律比较复杂,具体海域要做 具体分析。盐度等值线与大洋环流类似
海冰的性质
一、海冰的盐度 二、海冰的密度 三、海冰的热性质
一、海冰的盐度
定 义:海冰的盐度是指 海冰融化后所得的海水盐 度。
海冰中的盐类,并不像海 水那样均匀地分布,而是
以“盐泡”的形式存在。
一、海冰的盐度
海水结冰时,是其中的水冻结,
而将其中的盐分排挤出来,部
分来不及流走的盐分以卤汁的 形式被包围在冰晶之间的空隙
四、1978年实用盐标(PSS1978)
盐度公式: 2≤ S ≤ 42
式中K15 是在“一个标准大气压力”下,温度15℃时, 海水样品的电导率与标准KCl 溶液的电导率之比。 特点:用电导方法,但不依赖海水的氯度,而是以可 以精确测定的KCl溶液(32.4356 ‰ ),作为电导标准。
五、海洋盐度的分布变化
热带气旋相关图片
热带气旋相关图片
热带气旋相关图片
热带气旋过去统称为台风,现在根据中心附近最大风 力的大小,分为四个等级。 热带低压:6-7级风力 热带风暴: 8-9级风力
强热带风暴: 10-11级风力
台风: 大于或等于12级风力
三、海洋温度的分布变化
① 水平分布:大洋表层的海水水温主要与太阳 辐射变化和大洋环流、海陆分布有关系。等 温线大致表现为平行于纬度线的带状分布。 ② 铅直分布:混合层,温跃层,冷水区。
海水物理性质

§2-1 海水的物理性质 五、海水的比容
比容随压力的变化,用 压缩率T表示。 图 4 表 示 海 水 在 0℃ , 各 种压力、盐度时的压缩 率。
• 其垂直分布规律:从表层向深层逐渐增加。 • 海水密度是决定洋流运动的重要因素之一。
§2-1 海水的物理性质 五、海水的比容
• 比容是密度的倒数。 • 纯水的比容随温度、压力的变化: 温度在0≤T≤45℃,压力在1≤p≤1000巴范围 内,可用下式表示:
V纯水= V0,1一C log{(B+p)/(B+1)} (2.13) 式中,B=2688.0+19.867T-0.311T2+1.77810-3T3
§2-1 海水的物理性质 一、海水的温度
海水表层温度分布具有如下水温并不位于赤 道上,而是出现在赤道以北,称为热赤道。
从热赤道向两极逐渐降低。
2)由于陆地集中于北半球,故北半球海水等温线分 布不规则,而南半球等温线近似平行于纬线。同 时,北半球水温略高于南半球同纬度的水温。
• 海水密度有现场密度和条件密度之分。
• 现场密度是指在现场温度、盐度和压力条件下所 测得的海水密度;
• 条件密度是指当大气压等于零时的密度。
§2-1 海水的物理性质 四、海水的密度
•海水的密度s,,p是盐度(S),温度()和压力(p)的函数, 但用数值表示时,采用下式表示的s,,p:
s,,p=(s,,p -1)1000
C=0.315 V0,1
§2-1 海水的物理性质 五、海水的比容
•海水的比容Vs随盐度、温度、压力的变化: 在温度(T)0≤T≤20℃,压力(p)在1≤p≤1000巴,盐度(S) 在30-40‰的范围内为:
Vs= V1-(1-10-3S)C log{(B+P)/(B+1)} 式中:B=(2670.8+6.89656S)+(19.39-0.0703178S)T-0.223T2
2 海水物理性质

水温测定
测定表层水温一用海水表面温度表、电测 表面温度计及其他的测温仪器,在卫星上 通常用红外线表面温度计测量海表水温, 在海洋浮标上一装有自记的仪器。 深层水温的测定,主要用常规仪器(如CTD) 及一些自容式温盐深自记仪器(如STD、 CTD)等。
粘滞性
由于海水分子的不规则运动,相邻水层内 的分子便要产生交换作用,如果相邻的水 层具有速度梯度,那么这种交换作用便将 引起动量的转移,从而就在海水水层中出 现摩擦应力,对于x方向,相邻水层之间单 位面积上的摩擦应力为
海水样品中所溶解的固体物质的总质量除以该 样品的质量。源自传统盐度定义的条件:
所有碳酸盐转变为氧化物、全部溴和碘被氯置换、所 有有机物被氧化。
这种测定方法的操作繁杂,为了应用方便,在海 水组成恒定原理基础上,自北海、波罗的海、红 海等海区采集了 9个表层水样,测定了它们的盐 度和氯度,从这些数据归纳出盐度和氯度(Cl)的关 系式 S‰=0.030+1.8050Cl‰ 后来,又将其改为: S‰=1.80655Cl‰
独特的分子结构
O= H+ H+
纯水的物理特性
极性分子 可形成缔合分子 溶解力强 沸点高 密度反常
海水温度
海水含有盐分, 导致海水的冰点 和最大密度温度 发生变化。 海水温度在-5~ 33℃之间。 在海洋深层,温 度一般都很低, 大体在-1~4℃间。
海表温度与表皮温度
估算声速,经验公式
C 1449.2 4.6t 0.055t 2 0.00029t 3 1.34 0.010t S 35 0.016z
深海声速垂直分布
海水粘度密度与温度对照表

海水粘度密度与温度对照表海水是地球上最丰富的水资源之一,它的性质和特点对于海洋科学、工程建设以及生物生态系统都具有重要影响。
海水的粘度和密度是其中两个重要的物理性质,它们与海水的温度密切相关。
本文将通过一个对照表的形式,详细介绍海水粘度密度与温度之间的关系。
一、海水粘度与温度的关系粘度是液体内部阻力的量度,衡量了液体的黏性和黏度。
海水的粘度与其温度呈正相关关系,即温度升高时,海水的粘度也随之增加。
以下是海水粘度与温度的对照表:温度(℃)粘度(mPa·s)0 1.795 1.3110 1.0415 0.8720 0.7425 0.6530 0.57从对照表中可以清晰地看出,海水的粘度随着温度的升高而减小,这与一般液体的变化规律相反。
这是因为海水的组分复杂,其中所含的盐类和溶解气体对其粘度产生了影响。
二、海水密度与温度的关系密度是描述物质质量与体积关系的物理量,它对于海洋的水文学和海洋学研究非常重要。
海水的密度与其温度呈负相关关系,即温度升高时,海水的密度逐渐减小。
以下是海水密度与温度的对照表:温度(℃)密度(g/cm³)-2 1.0350 1.0255 1.01910 1.01315 1.00720 1.00125 0.99530 0.989从对照表中可以看出,海水的密度随着温度的升高而减小。
这是因为在高温下,海水中的水分子具有更高的动能,分子之间的间距相对增大,导致单位体积海水中所含的质量减小,从而使得海水的密度降低。
三、海水的粘度密度与海洋科学的应用海水的粘度和密度是许多海洋科学研究的重要参数。
举例而言,粘度与流体动力学密切相关,对于海洋工程设计和海洋运输有重要意义。
密度则是地球物理学和海洋学中常用的物理变量,它用于研究海洋循环、海洋混合、水团形成以及海水密度梯度对生物分布等方面的影响。
总结:海水的粘度与温度呈正相关关系,而密度与温度呈负相关关系。
这种关系对于理解海洋环境和开展海洋科学研究至关重要。
物理海洋学 第二章 海水的物理性质

10
11
涡动
12
13
第三节 海水的力学性质
分子粘性对海-气界面物质交换过程非常重 要。
二、海水的渗透压 • 海水的渗透压(osmotic pressure)—
—被半渗透膜(水分子可通过,但盐分 子不能通过)分开的海水和淡水,由于 淡水一侧的水慢慢地渗向海水一侧,使 得海水一侧的压力增大,直到达到平衡 状态,此时膜两边的压力差。 海水渗透压随海水盐度的增高而增大。 海洋生物的细胞壁是一种半透膜。渗透压 对于海洋生物的生存十分重要。
小。
绝热温度梯度——海水绝热温度变化随压
海水压缩系数一般很小。海水被看做是不 力(深度)的变化率。海洋的绝热温度梯
可压缩流体。
度平均为0.11℃/km。
海水运动研究中重要的物理假设,使方程 在分析深海区的水温铅直结构时,不可忽
得到简化。
视绝热变化的影响。
在比较不同深处的海水温度时,不宜仅看 现场温度值来判断。
海冰限制了海洋向大气输送热量,使得海 洋的蒸发失热大为减少,从而形成海洋保 护层。
27
六、海冰的分布
南半球冰界以9月为最大,3月为最小,多为2-3米
海冰具有显著的季节和年际变化。
厚的“一冬冰”。
北半球冰界以3-4月为最大,8-9月为最小。流冰 群主要围绕洋盆边缘流动,多为3-4米厚的多年冰。
南极洲是世界上最大的天然冰库,占全球冰雪总 量的90%以上。
6
7
三、海水的压缩系数
四、海水的绝热变化
• 压缩系数(compression coefficient): 1、海水的绝热变化
单位体积的海水,当压力增加1MPa时, 其体积的负增量。
海水物理性质

• 体积巨大——海水体积极大,它所拥有的 多种成分的总量也十分巨大,外界的影响 (如大陆径流等)很难使其相对组成发生 明显的变化。
4
• 三、盐的循环
事实1:河流将岩石风化产生的盐带到大海每年1015克/年 事实2:海洋盐度在过去15亿年中保持不变
Anion 阴离子
水合作用: 溶质的分子或离子与溶剂的分子相结合的作用对于水溶液来 讲称为水合作用
8
密度变化异常:“热胀冷缩”?
密度随温度变化-----分段函数 最大密度温度
9
• 沸点和融点、比热、蒸发潜热等热性质比氧的同 族化合物高
二、海水的热力学性质
10
热容、比热容:
热容:海水温度升高1K所吸收的热量。单位: (J/K)
淡水结冰 :表层开始结冰。
海水结冰
当盐度大于24.695时,海冰冰点高于最大密度温度,只有当对流混合层的温度同 时达到冰点时,海水才会结冰
海水结冰的特点:主要是纯水的冻结,盐分大部排出冰外,增大了冰下海水的 盐度,加强了冰下海水的对流和进一步降低了冰点;同时冰层阻碍了其下海水热 量的散失,从而大大减缓了冰下海水继续冻结的速度;海冰表面比较粗糙。
稳定状态
盐的输入率等于输出率
5
第二节 海水的物理性质
一、淡水
分子结构:极性,分子缔合力
6
H2O: 唯一一种能在地球表面以固态、液态、气态同时存在的物质。 三种相下的分子状态见下图:
分子缔合
7
溶解力强(极性)
Sodium Chloride 氯化钠
NaCl
Na+
Cation 阳离子
海水的温度盐度密度的分布规律

海水的温度盐度密度的分布规律一、海水的基本性质海水是指地球表面被覆盖的水体,通常来自海洋、海湾、海峡等大面积的水域。
海水是由淡水和盐水混合而成的,其主要成分包括水分子、钠离子和氯离子,还有少量的镁离子、钾离子、硫酸根离子等。
海水的温度、盐度和密度是描述海水物理性质的三个重要参数,它们相互影响,共同决定了海水的状态和特性。
1. 温度海水的温度是指海水中各点的温度值。
海水的温度受到多种因素的影响,如季节变化、地理位置、海洋环流等。
通常情况下,海水的温度会受到太阳辐射的影响,表现为昼夜温度差异大,白天温度高,夜晚温度低的特点。
海水的温度会影响海水的密度,影响海水的流动状况,还会对海洋生物的生长和分布产生重要影响。
2. 盐度海水的盐度是指海水中各点的盐度值。
海水的盐度主要来源于地表径流和海底地形的影响,是海水中溶解的各种盐类和矿物质的总和。
海水的盐度会受到降水、蒸发和河流径流等因素的影响,通常情况下海水的盐度在全球各地都有一定的变化范围。
盐度高的海水通常密度较大,而盐度低的海水密度较小,影响海水的流动和热交换。
3. 密度海水的密度是指海水的质量与体积的比值,通常以千克/立方米(kg/m³)为单位。
海水的密度受到温度和盐度的影响,通常情况下海水的密度在不同地区有一定的差异。
密度较大的海水往往在深水区,而密度较小的海水则通常在浅水区。
海水的密度差异会影响海水的流动和环流过程,还会对海洋生物的生长和分布产生重要影响。
二、海水的温度、盐度和密度分布规律海水的温度、盐度和密度在不同地区和深度都有一定的分布规律,这些规律主要受到海洋环流、地形地貌、气候变化等因素的影响。
下面将分别介绍海水的温度、盐度和密度的分布规律及其影响因素。
1. 温度分布规律海水的温度在不同地区和深度有着不同的分布规律,主要受到以下因素的影响:(1)季节变化:海水的温度会受到季节变化的影响,通常情况下夏季海水温度较高,冬季海水温度较低,造成昼夜温度差异大,影响海水的热交换和环流过程。
海水的物理性质

Lehodey,P. et al., 2000. El Nino Southern Oscillation and tuna in the western Pacific. Science
Temperature distribution in California coastal area
长江水的扩展
热性质特殊
沸点(boiling point)和融点(melting point)、比热(specific heat)、蒸发潜热 (latent heat of vaporization)等热性质比氧的同族化合物高
2.2 温度、盐度和密度的概念及关系 Temperature, Salinity and Density
• Ocean and Sea
– Four Principle Ocean – Hydrological features of ocean, sea, fjord(bay), strait(channel)
§2 海水的物理性质 Physical Properties of Sea Water
2.1 Water
– ITS-90: the International Temperature Scale of 1990 – ITS-68: the International Temperature Scale of 1968
• At 0℃ they are the same, and above ℃ its-90 is slightly cooler. • t90-t68 = -0.002 at 10 ℃; -0.005 at 20 ℃, -0.007 at
The effect of Temperature
The effect of Salinity
第三章海水的物理性质和世界大洋的层化结构

第三章:海水的物理特性和世界大洋的层化结构一、海水的主要热学和力学性质(一)水的密度水结冰时,密度减小,体积增大,所以冰总是浮在水面上,这与一般物质的性质“热胀冷缩”不同,是一种反常膨胀。
水的密度随温度的这种不正常的变化,是由水分子的缔合造成的。
(二)水的热性质特殊水的熔点、沸点、比热、蒸发潜热和表面引力值都比氧的同族氢化物高。
其原因就在于熔化和汽化时,缔合分子的溶解需要消耗较多的能量。
(三)海水的盐度海水是含有多种无机盐类的溶液,盐度是其浓度的一种量度,它是描述海水特征的基本物理量之一。
海洋中发生的许多现象都与盐度的分布和变化密切相关。
长期以来,人们对盐度的定义、计算标准和测量技术进行了广泛的研究和讨论,先后有1902年盐度、氯度定义;1969年的电导盐度定义;1978年的实用盐标。
1、1902年盐度、氯度定义大量海水分析结果表明,不论海水中含盐量的大小如何,各主要成分之间的浓度比基本上是恒定的,这种规律称为“海水组成恒定性”又称为马赛特原则。
海水组成恒定性规律的发现,为测定海水的盐度提供了方便条件。
1902年,克努森(Knudsen)等人建立了盐度、氯度定义。
1)盐度:1千克海水中的碳酸盐全部转换成氯化物,溴和碘以氯当量置换,有机物全部氧化之后所剩固体物质的总克数,单位:克每千克,用符号S‰表示。
2)氯度:1千克海水中的溴和碘以氯当量置换,氯离子的总克数,单位是克每千克。
(氯度量稍大于海水中实际氯含量)用硝酸银滴定法测定海水的氯度时,需要知道硝酸银的浓度,为此,配置一种标准的知道其氯度值的标准海水,作为国际统一标准硝酸银溶液的浓度。
国际上统一使用氯度值精确为19.374‰的大洋水作为标准,称为标准海水,其盐度值对应为35.000‰。
2、1969年的电导盐度定义考克斯等1976年对由大洋和不同海区不深于100米的水层内采集的135个水样,准确的测定其氯度值计算盐度,同时测定水样的电导比R15,得除了盐度S‰与电导比之间的关系式:但此种盐度测定仍然未脱离对氯度测定的依赖,直至1978年实用盐标的建立,才使得盐度测定脱离了对氯度测定的依据。
海水的恒定性原理

海水的恒定性原理
海水的恒定性原理是指海水在一定条件下具有一定的稳定性。
海水的成分和性质在绝大部分情况下保持不变,即使受到外部环境的影响也能够保持相对的稳定。
这一原理在海洋学和地球科学领域具有重要意义。
海水成分的恒定性
海水是淡水和盐类溶解物质的混合物。
海水中主要含有氯化钠、镁、钙等盐类元素以及各种微量元素。
尽管海水在不同地区和深度略有差异,但总体成分保持相对恒定。
这种稳定性使得海水成为全球范围内的一个重要稳定化学环境。
海水性质的恒定性
除了成分外,海水的物理性质也具有恒定性。
比如海水的密度随着深度和温度的变化而变化,但相对较小的范围内密度基本保持稳定。
海水的热容量大使得海水对温度变化具有缓冲作用,保持了海水的相对稳定性。
海水环境的恒定性
海水环境中的其他因素,如盐度、 pH 值、氧含量等也具有一定的恒定性。
海水中的生物和化学过程受到这些环境因素的影响,而这些环境因素相对恒定有助于维持海洋生态系统的平衡。
恒定性的重要意义
海水的恒定性原理对于海洋科学研究和人类生活都具有重要意义。
在气候变化的背景下,海水的恒定性有助于我们更好地理解海洋环境的变化趋势和生态系统的演化。
同时,海水的恒定性也为海洋资源的利用提供了基础,例如海水淡化、海水养殖等技术均依赖于海水的相对恒定性。
综上所述,海水的恒定性原理是海洋环境稳定性的基础,它对于维持海洋生态平衡、促进人类社会的可持续发展具有重要作用。
进一步研究和理解海水的恒定性将有助于我们更好地保护海洋环境、利用海洋资源,并推动海洋科学领域的发展。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
tρ (max) = 3.95 − 2.0 ×10−1 S −1.1×10−3 S 2 + 0.2 ×10−4 S −3
26
海水的压缩性
• 单位体积的海水,当压力增大1Pa时,其体 积的负增量称为压缩系数
• 定盐等温压缩系数
βt
=
1
α
⎜⎜⎝⎛
∂α
∂p
⎟⎟⎠⎞ S,t
10
海水中的溶质
• 痕量元素:海洋中极小量的无机成分。
• 痕量元素主要包括Li、I、Mo、Zn、Fe、Al等
• 上述痕量元素的含量分别为170、60、10、10、 10、10ppb。(ppb=parts per billion)
• 痕量元素的含量虽然小,但对某些生物化学反应 至关重要
11
海水中的溶质
• L受盐度影响很小,可只考虑温度的影响
Dietrich(1980)给出如下计算公式 (0~300C)
L = (2502.9 − 2.720t) ×103 J/kg 0 ≤ t ≤ 30D C
31
海水的饱和水汽压
• 饱和水汽压 对纯水而言,饱和水汽压是指水分子有水面逃出 和同时回到水中的过程达到平衡时,水面上水汽 所具有的压力。
• 实用盐度不再使用符号‰
18
实用盐度计算公式
• Lewis(1980)给出任意温度的盐度公式
Kt 为任意温度下的电导率之比
S = 0.0080 − 0.1692Kt1/2 + 25.3851Kt
+14.0941Kt3/2 − 7.0261Kt2 + 2.7081Kt5/2 + ΔS
ΔS
=
1+
t −15 0.0162(t
• 实际利用CTD测量得 到的电导率是任意盐 度、温度和压力情况 下获得的,需要对压 力进行修正。
• 盐度是物理海洋学的 一个重要参数。
21
盐量的循环
• 由于海浪破碎或被风撕裂,形成海盐气溶 胶进入大气中,饱和水汽以它为凝结核, 形成雨滴落到陆地上,最后归聚河流又回 到海洋 大气
波浪
降雨
海洋
海洋
22
• 热带气旋、台风、飓风的 生成
33
海水的热传导
• 相邻海水温度不同时,由于海水分子或海水块体的交换, 会使热量由高温向低温处转移,称为热传导
• 单位时间内通过某一截面的热量,称为热流率。 • 单位面积的热流率称为热流率密度,单位Wm-2.
q = −λ ∂t
∂n
λ 为热传导系数
34
海水的传导性
• 由分子的随机运动引起的热传导,称为分子热传 导,海水分子热传导系数为10-1量级
28
海水的位温
• 位温 海洋中某一深度的海水微团,绝热上升到 海面时所具有的温度称为该深度海水的位 温,海水微团此时相应的密度称为位密。
• 海水的位温显然比其现场温度低。为什 么?
29
世界大洋深层水的位温和盐度柱状 图
盐度变化小,位温变化较大
30
海水的蒸发潜热
• 比蒸发潜热 使单位质量海水化为同温度的蒸汽所需的 热量,称为海水的比蒸发潜热 L。
• 气体:主要包括N2、O2、CO2、H2、Ar、Ne、 He。
• 前三者分别占总气体的47.5%、36.0%和15.1%, 其余占1.4%
• N2和惰性气体很少参与生物活动,而O2和CO2很 大程度上受控于生物的光合和呼吸作用,所以它 们不是保守量,取决于植物和动物的丰富性和活 动
12
海水中的溶质
• 对海水而言,由于盐度存在,则单位面积海面上 平均水分子数目要少,限制了海水蒸发,使饱和 水汽压降低
• 海面的蒸发量与海面上水汽压与饱和水汽压的差 成正比,饱和水汽压小不利于蒸发
32
海水蒸发与气候变化
• 由于海水蒸发,海洋平均 每年失去126cm厚的海水
• 为何不见海面降低?
• 伴随海水蒸发,海洋不仅 失去水分,同时失去大量 热量,由水汽携带而输向 大气。
S15 = 0.0080 − 0.1692K115/2 + 25.3851K15 +14.0941K135/ 2 − 7.0261K125 + 2.7081K155/ 2
K142 其中K15 为一个大气压下,温度150C,海水样品的电导率 与标准KCI溶液的电导率之比
24
海水的膨胀
• 体积热膨胀系数
η = 1 ⎜⎛ ∂V ⎟⎞
V ⎝ ∂t ⎠ p,S
η
=
1
α
⎜⎛ ⎝
∂α
∂t
⎟⎞ ⎠
p,S
α 为单位质量海水的体积,在海洋学上称 为比容
25
海水的膨胀
• 海水的热膨胀系数比纯水 大,且随温度、盐度和压 力的增大而增大
• 低温低盐时,海水的热膨 胀系数为负值,说明当温 度升高时海水收缩
张(洋中脊居中) • 中国四大海及其分界 • 海岸、海滩(潮间带)和岸下坡 • 大陆架、大陆坡和大陆隆
1
中央裂谷(重要更正)
• 大洋中脊的轴部有沿 其走向延伸的断裂谷 底,称为中央裂谷。
• 中央裂谷是海底扩张 中心和海洋岩石圈增 生的场所,火山活动 中心区。
2
第三章 海水的物理性质
• 海水的构成是什么?
• 主要成份即海水中的阳离子和阴离子,占所有溶 质的99.99%,是不随时间变化的保守量
8
海水组成恒定性原理
• 海水组成恒定性原理:尽管不同样品的主要成 分绝对量不同,但它们的比值不变。即任何两 种溶于海水中的主要成分比值不变,如CI1/SO42-,Na+/K+
9
海水中的溶质
• 营养盐:对植物生长至关重要,主要包括氮(N)、磷 (P)和硅(Si)的化合物
• 由电导率推算盐度可准确到±0.003
• 测盐度的仪器事先用标准海水来标定
• 盐度35的标准海水取自大西洋北部,封装在 275ml的玻璃瓶中,根据实用盐度标准标定其 电导率比和盐度。自1989年起,由设在英国 的Ocean Scientific International分发到世 界各地
20
海水盐度的测定
• 海水的压缩系数随温度、盐度和压力的增 大而减小,海水压缩系数一般很小
27
海水的绝热变化
• 什么叫绝热变化?
• 海水绝热下沉时,压力增大使体积缩小, 温度升高,绝热上升时,压力减小使体积 膨胀,导致温度降低。
• 海水绝热温度变化随压力(深度)的变化 率称为绝热温度梯度。海洋的绝热温度梯 度平均为 0.11ºC/km
6
纯水的热性质
• 与其它氧族氢化物相 比,其溶点和沸点要 高得多,其理论上分 别为-900C和-800C, 而实际上为00C和 1000C
• 水的比热、蒸发潜热 和表面张力都比氧的 同族化合物高
7
海水中的溶质
• 海水的溶解性非常强,可将大部分物质溶解为极 小颗粒
• 从化学上可将这些溶质分为5类:主要成份,营 养盐、气体、痕量元素和有机化合物。
• 该方法测定盐度非常繁琐
14
海水的盐度
• Knudsen公式(化学方法) 基于海水组成恒定性规律,用测定海水氯 含量的方法来计算盐度
S ‰ = 0.03 + 1.805 CI ‰
CI ‰为氯度,即1kg海水中的溴和碘以氯当量置换,氯离子的总克数
• 其用知氯道Ag度ANg值ON3精O滴3确的定为浓法1度测9.,定37国海4 际水‰的上的大统氯洋一度水使时作用,为一需标种要 准,对应的盐度值为35.000 ‰,称为标准海 水
[0.0005 −15)
−
0.0056Kt1/ 2
−
0.0066Kt
−
0.0375Kt3/ 2
−
0.0636Kt2
−
0.0144K
5/ t
2
]
Kt = C(S,t, 0) / C(KCI ,t, 0)
20 C < t < 350 C
• 上面公式又进一步推广到任意压力(Millero,
1996)
19
关于实用盐度
• 具有相同电导率比的所有海水具有相同的 盐度值
为使海水的盐度值与氯度脱钩,选择一种
精确浓度(32.4356‰)的氯化钾(KCI) 溶液作为可再制的电导标准,用海水相对 于KCI溶液的电导比来确定海水的盐度值
K15
=
C(35,15,0) C(32.4356,15,0)
=1
17
实用盐度计算公式
• 温度为150C海水盐度公式
• 海水沸点和冰点与盐 度有关
• 三者在海水中的含量分别为0.5ppm、0.07ppm和 3ppm。(ppm=parts per million)
• 由于生物吸收和释放,海水中的营养盐随地点和时间而 变,是非保守量
• 植物不能直接吸收N和P元素,而是吸收可溶解的PO43-和 NO3-。
• 虽然Si不直接参与细胞植物生长,但它对SiO2沉降至关重 要,SiO2是硅藻和散线虫类动物的骨骼成份。
5
纯水的特性
• “热胀冷缩”? • 水在温度4ºC时密度最大? • 温度低于40C时,有利于分子
的缔合
• 冻结为冰时,水分子全部缔 合成一个巨大的分子缔合 体,称为分子晶体。结构排 列松散,密度减小
• 水温从00C到40C时,主要过 程是较大缔合分子离解成较 小的缔合分子
• 温度进一步升高时,分子热 运动增强,导致体积膨胀, 密度减小
• 1966年修改为 S ‰ = 1.80655 CI ‰
15
海水的盐度(电导方法)
• 化学方法一直沿用到20世纪60年代 • 盐度的电导率定义(Cox et al., 1967)
s ‰= − 0.08996 + 28.29720R15 + 12.80832R125
