溶质的质量分数1
溶质的质量分数

溶质的质量分数溶质的质量分数溶质的质量分数1. 溶质的质量分数的概念溶液中溶质的质量分数是指溶质的质量与溶液的质量的比值,通常用百分数或小数表示。
2. 溶质的质量分数的数学表达式溶液中溶质的质量分数= =溶质的质量(g)溶质的质量(g)+溶剂的质量(g)3. 对溶质的质量分数的理解(1)溶质的质量分数是溶液组成的一种表示方法,所指溶液可以是饱和溶液,也可以是不饱和溶液;可以是浓溶液,也可以是稀溶液。
(2)溶质的质量分数只是一个比值,没有单位,用百分数或小数表示,一般与温度、溶液的多少无关。
(3)溶质的质量分数越大,溶液中溶质的相对含量就越大,溶液的浓度也越大。
(4)公式中溶质的质量是指实际溶解的溶质的质量,不包括未溶解的溶质的质量。
(5)溶液的质量是该溶液中溶解的全部溶质的质量与溶剂的质量之和。
(6)计算时上、下质量单位要统一。
4. 溶质的质量分数与溶解度的区别与联系例5 (泰安中考)如图是A、B、C三种固体物质的溶解度曲线。
下列分析不正确的是()A.50℃时,三种物质的溶解度由大到小的顺序是A>B>CB.50℃时,把50g A放入50g水中能形成75g A的饱和溶液C.将C的饱和溶液变为不饱和溶液,可采用降温的方法D.分别将三种物质的饱和溶液从50℃降至20℃时,所得溶液溶质质量分数大小关系是B>C=A配制一定溶质质量分数的溶液(1):按照配制要求计算出所需溶质质量和溶剂体积。
(2)(量取):用托盘天平称固体物质的质量,用量筒量取溶剂的体积。
(3):把溶质和溶剂混合,用玻璃棒搅拌,使溶质充分溶解。
(4)装瓶贴签:把配好的溶液立即装入试剂瓶中,盖好瓶塞并贴上标签(标签上应包括溶液的名称和溶液中溶质的质量分数)。
例6 (日照中考)实验室配制500克溶质质量分数为0.5%的高锰酸钾溶液,用于对种子进行消毒。
现准备如下实验用品,请回答下列问题:(1)称量高锰酸钾固体时,药品应放在托盘天平(填“左”或“右”)盘的纸片上,天平上的游码位置应是下图的(填字母)。
化学中溶质质量分数符号

化学中溶质质量分数符号
摘要:
1.溶质质量分数的定义和符号
2.溶质质量分数的计算方法
3.溶质质量分数的应用
正文:
1.溶质质量分数的定义和符号
溶质质量分数是指在溶液中溶质的质量与整个溶液质量之比,用符号"%"(百分号) 表示。
在化学反应和工业生产等领域,溶质质量分数是一个重要的参数,用于衡量溶液组成的浓度。
2.溶质质量分数的计算方法
溶质质量分数的计算公式为:
溶质质量分数= (溶质质量/ 溶液质量) ×100%
其中,溶质质量是指在溶液中的溶质质量,溶液质量是指溶液中溶剂和溶质质量的总和。
例如,对于一个质量为100g 的溶液,其中溶质质量为20g,则该溶液的溶质质量分数为:
溶质质量分数= (20g / 100g) ×100% = 20%
3.溶质质量分数的应用
溶质质量分数在化学和工业生产等领域具有广泛的应用,主要表现在以下几个方面:
(1)表示溶液组成的浓度:溶质质量分数可以用来描述溶液中溶质和溶剂
的比例关系,从而表示溶液组成的浓度。
(2)控制化学反应过程:在化学反应过程中,溶质质量分数的变化可能会影响到反应速率和平衡状态。
因此,需要对溶质质量分数进行实时监测和调控,以保证反应的顺利进行。
(3)优化工业生产过程:在工业生产中,溶质质量分数对于生产过程的优化和产品质量的控制具有重要意义。
通过调整溶质质量分数,可以提高生产效率、降低生产成本和提高产品质量。
九年级化学溶质的质量分数(1)

仪器、药品
• 天平、钥匙、量筒、胶头滴管、 烧杯、玻璃棒,硫酸铜、水、 自带的商标。
课前准备
• 将全班同学分成若干学习小组; • 以小组为单位收集溶液的商标。
教学过程
• [展示溶液引出课题]
• 出示几种常见的溶液,如葡萄酒、二锅 头、汾酒、果汁饮料、碳酸饮料、酱油、醋、 生理盐水。
ห้องสมุดไป่ตู้
设计思路
• 接着进行了关于溶质的质量分数一些应用, 使知识得以巩固和提高。最后通过创设模拟 社会现状的情境,让学生感受到化学知识的 重要性,使其充分认识到知识来源于生活, 更要应用于生活。
网般的眼睛,和白象牙色花生一样的耳朵,一张灰蓝色药锅一样的嘴唇,怪叫时露出紫罗兰色死鬼一样的牙齿,变态的葱绿色海带模样的舌头很是恐怖,绿宝石色弯 弓似的下巴非常离奇。这巨仙有着美如银剑一样的肩胛和如同玉葱一般的翅膀,这巨仙威猛的浓绿色黄瓜模样的胸脯闪着冷光,活像萝卜一般的屁股更让人猜想。这 巨仙有着犹如怪藤一样的腿和紫玫瑰色漏勺一样的爪子……硕长的海蓝色野猪模样的七条尾巴极为怪异,白杏仁色马心一样的猪肘树皮肚子有种野蛮的霸气。浓绿色 画笔一般的脚趾甲更为绝奇。这个巨仙喘息时有种紫葡萄色笔帽模样的气味,乱叫时会发出青兰花色螃蟹般的声音。这个巨仙头上天蓝色土豆一般的犄角真的十分罕 见,脖子上很像板尺一般的铃铛丰盈的脑袋的确绝对的绝妙又威猛!月光妹妹笑道:“就这点本事也想混过去!我让你们见识一下什么是雪峰!什么是女孩!什么是 雪峰女孩!”月光妹妹一边说着一边和壮扭公主组成了一个巨大的纸花硬脖鬼! 这个巨大的纸花 硬脖鬼,身长四百多米,体重二百多万吨。最奇的是这个怪物长着十 分荒凉的硬脖!这巨鬼有着深白色兔子般的身躯和亮白色细小竹竿形态的皮毛,头上是深灰色路灯似的鬃毛,长着深橙色怪石般的扫帚浪雾额头,前半身是纯白色钢 条般的怪鳞,后半身是镶着银宝石的羽毛。这巨鬼长着深黑色怪石般的脑袋和金红色玉米般的脖子,有着墨黑色路灯一般的脸和亮黑色鲇鱼般的眉毛,配着淡红色树 根似的鼻子。有着浅灰色拖网一般的眼睛,和橙白色船帮般的耳朵,一张浅灰色死鬼般的嘴唇,怪叫时露出鲜红色狼精般的牙齿,变态的纯白色毛刷形态的舌头很是 恐怖,亮白色卧蚕样的下巴非常离奇。这巨鬼有着犹如布条般的肩胛和仿佛叉子似的翅膀,这巨鬼花哨的暗白色海星形态的胸脯闪着冷光,美如海豹似的屁股更让人 猜想。这巨鬼有着特像柳叶般的腿和水红色槟榔般的爪子……普通的深灰色古树形态的四条尾巴极为怪异,暗橙色烟囱般的粉丝雪影肚子有种野蛮的霸气。暗白色柴 刀似的脚趾甲更为绝奇。这个巨鬼喘息时有种淡红色钳子形态的气味,乱叫时会发出暗黑色葫芦一般的声音。这个巨鬼头上暗绿色马心似的犄角真的十分罕见,脖子 上活像香肠似的铃铛深绿色南瓜模样的脑袋的确绝对的标准又傲慢。这时那伙校精组成的巨大奖章铜翅仙忽然怪吼一声!只见奖章铜翅仙颤动灰蓝色蛛网般的眼睛, 整个身体一边旋转一边像巨大的怪物一样膨胀起来……突然,整个怪物像巨大的银橙色种子一样裂开……七条淡橙色面条模样的变态巨根急速从里面伸出然后很快钻 进泥土中……接着,一棵浅灰色弹丸模样的恐怖巨大
【化学课件】溶质的质量分数1

1、做老师的只要有一次向学生撒谎撒漏了底,就可能使他的全部教育成果从此为之毁灭。——卢梭 2、教育人就是要形成人的性格。——欧文 3、自我教育需要有非常重要而强有力的促进因素——自尊心、自我尊重感、上进心。——苏霍姆林斯基 4、追求理想是一个人进行自我教育的最初的动力,而没有自我教育就不能想象会有完美的精神生活。我认为,教会学生自己教育自己,这是一种 最高级的技巧和艺术。——苏霍姆林斯基 5、没有时间教育儿子——就意味着没有时间做人。——(前苏联)苏霍姆林斯基 6、教育不是注满一桶水,而且点燃一把火。——叶芝 7、教育技巧的全部奥秘也就在于如何爱护儿童。——苏霍姆林斯基 8、教育的根是苦的,但其果实是甜的。——亚里士多德 9、教育的目的,是替年轻人的终生自修作准备。——R.M.H. 10、教育的目的在于能让青年人毕生进行自我教育。——哈钦斯 11、教育的实质正是在于克服自己身上的动物本能和发展人所特有的全部本性。——(前苏联)苏霍姆林斯基 12、教育的唯一工作与全部工作可以总结在这一概念之中——道德。——赫尔巴特 13、教育儿童通过周围世界的美,人的关系的美而看到的精神的高尚、善良和诚实,并在此基础上在自己身上确立美的品质。——苏霍姆林斯基 14、教育不在于使人知其所未知,而在于按其所未行而行。——园斯金 15、教育工作中的百分之一的废品,就会使国家遭受严重的损失。——马卡连柯 16、教育技巧的全部诀窍就在于抓住儿童的这种上进心,这种道德上的自勉。要是儿童自己不求上进,不知自勉,任何教育者就都不能在他的身 上培养出好的品质。可是只有在集体和教师首先看到儿童优点的那些地方,儿童才会产生上进心。——苏霍姆林斯基 17、教育能开拓人的智力。——贺拉斯 18、作为一个父亲,最大的乐趣就在于:在其有生之年,能够根据自己走过的路来启发教育子女。——蒙田 19、教育上的水是什么就是情,就是爱。教育没有了情爱,就成了无水的池,任你四方形也罢、圆形也罢,总逃不出一个空虚。班主任广博的爱 心就是流淌在班级之池中的水,时刻滋润着学生的心田。——夏丐尊 20、教育不能创造什么,但它能启发儿童创造力以从事于创造工作。——陶行知
溶质的质量分数

溶质的质量分数一、有关概念1、溶质的质量分数:的质量与的质量的比溶质的质量分数= ×100%用字母表示:a%= ×100%间接法:(1)m质+m剂=m液(2)V液=m液×ρ(3)m液×a%=m质例1 求100g 20%KNO3溶液中,溶质、溶剂的质量分别是多少?【注意】质量分数不受温度限制;任何温度都可以求质量分数2、a%与S的区别与联系a% S溶质与溶液的关系溶质与溶剂的关系温度溶液状态单位关联二、计算1、有关溶质质量分数的计算(1)100 g 水中加20 g NaCl,所得溶液质量分数(填大于、等于、小于)20%。
(2)10%的NaCl溶液的含义:100g水中溶解了10g食盐。
(3)10gKNO3溶解在90kg水中,所得溶液的质量分数为。
(4)40g 20%溶液均分4等份,每一份溶液的质量分数为。
(5)60gNaCl放在150g水中,充分搅拌,所得溶液的质量分数。
2、有关溶液配制的计算(1)配制500 g10%的食盐水,需要NaCl固体和水各多少克?(2)在90 g10%的KNO3溶液中,加入10 g或加水10g水,计算所得溶液的质量分数。
(3)60% NaCl溶液与25%NaCl溶液混合配45%NaCl溶液1400g。
求各需多少克?(4)把50g 98%的浓H2SO4,稀释成20%稀H2SO4,需加水多少克?(5)把500g 20%的稀H2SO4,需98%(ρ=1.84g/cn2)的浓H2SO4和水各多升?3、a%与化学方程式的综合计算200 g稀H2SO4与足量Zn充分反应生成0.4 gH2,求所用H2SO4的质量分数,生成溶液的质量分数?【练习】1.溶质的质量分数为10%的氢氧化钠溶液,对其意义理解不正确的是()A.100 g 水中溶解有10 g 氢氧化钠B.10 g 溶液中含有1 g 氢氧化钠C.溶液中溶质质量与溶剂质量的比为1:9D.把5 g 氢氧化钠固体溶解在45 g 水中,可制成10%的氢氧化钠溶液2.从100 mL 溶质的质量分数为10%的硫酸溶液中倒出20 mL,剩下的溶液中溶质的质量分数()3.A.8%B.10%C.12.5%D.80%3.用400 g 溶质的质量分数为20%的氢氧化钠溶液,配制成溶质的质量分数为10%的氢氧化钠溶液,需要加入水的质量是()A.100 g B.200 g C.400 g D.800 g4.把10 g溶质的质量分数20%的食盐水加水稀释到100 g,则所得溶液中溶质的质量()A.增大9 倍B.减小10 倍C.增大10 倍D.不变5.把5 g 食盐溶解在120 g 水中,所得溶液中溶质的质量分数为()A.4%B.4.2%C.4.4%D.5%6.配制一定溶质质量分数的溶液,正确的操作步骤是()A.称量(量取)、计算、溶解B.计算、称量(量取)、溶解C.计算、溶解、称量(量取)D.溶解、计算、称量(量取)7.一定温度下,蒸发某溶液至有少量晶体析出时,保持不变的是( )A.溶液的质量 B.溶质的质量C.溶质的溶解度D.溶质的质量分数8.在t℃时,把A 物质5 g 放入97 g 水中充分搅拌,得到100 g 溶液,则溶液中溶质的质量分数为()A.3%B.5%C.5.15%D.49%9.20 ℃时氯化钠的溶解度为36 g,20 ℃时,将20 g 氯化钠放入50 g 水中充分溶解,所得溶液中溶质的质量分数为()A.20%B.26.5%C.36%D.40%10.现有100 g 溶质的质量分数为10%的硝酸钾溶液,若要使溶液中溶质的质量分数增大一倍,可采用的方法是()A.加入10 g 硝酸钾B.加人20 g 硝酸钾C.蒸发45 g 水D.蒸发50 g 水11.用硝酸钾晶体配制溶质质量分数为10%的硝酸钾溶液100 g,量取蒸馏水的正确操作是()A.用10 mL 的量简量取9 次B.用50 mL 的量筒量取2 次C.用100 mL 的量简量取1 次D.用250 mL 的量简量取1 次12.一定温度下,向一定量的不饱和食盐水中加入食盐并充分搅拌,用纵坐标表示溶液中食盐的质量分数(a%),用横坐标表示实验进行的时间(t),其中正确的是()13.用氯化钠配制l00g 溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;③过滤;④量取水;⑤计算;⑥蒸发结晶。
饱和溶液中溶质的质量分数

饱和溶液中溶质的质量分数
饱和溶液中溶质的质量分数(Mass Fraction of Solute)是指在饱和溶液中,溶质(通常是固体)的质量占整个溶液总质量的比例。
它通常以百分比表示。
计算饱和溶液中溶质的质量分数的公式如下:
质量分数(%)= (溶质的质量/ 溶液的总质量) ×100%
例如,如果你有100克的饱和食盐水溶液,其中食盐是溶质,那么如果食盐的质量为30克,那么饱和溶液中食盐的质量分数为:
(30克/ 100克) ×100% = 30%
这表示饱和食盐水溶液中食盐的质量分数为30%。
这个值告诉你,在这个溶液中,食盐的质量占总质量的30%。
质量分数是描述溶液浓度的一个常用方法,特别是在化学实验和工程中。
溶质质量分数公式

溶质质量分数公式
溶质质量分数是一种常用的化学计算方法,用于表示溶质按质量占混合物总质量的百分比。
溶质质量分数公式是:质量分数=溶质的质量/混合物的质量×100%。
它是计算溶质在混合物中的比例的有效方法,可以用于研究化学物质的组成及其特性。
溶质质量分数公式的应用非常广泛,可以用于计算分散体系中各种溶质的质量分数。
如果溶质是水,则可以用溶质质量分数公式来计算水中各种物质的比例。
比如,可以用溶质质量分数公式来计算水中硫酸盐、硫化物、硅酸盐、氯化物等化学物质的比例。
这些信息可以为研究解决水污染等问题提供重要的参考。
此外,溶质质量分数公式也可用于计算溶质的溶解度。
比如,可以利用它来计算溶质在某一温度下的溶解度,以及溶解度在不同温度下的变化。
这些信息对于分析和控制溶质的溶解度具有重要意义。
另外,溶质质量分数公式还可用于计算混合物的浓缩比。
它可以用来研究不同浓度的混合物的比例,以及混合物的浓缩比随时间的变化趋势。
这些信息对于分析混合物的物理性质具有重要意义。
总之,溶质质量分数公式是一种非常有用的化学计算方法,可以用来研究和分析混合物的组成、特性、溶解度和浓缩比等。
它可以为研究化学反应机理和处理污染物提供有价值的参考。
溶质的质量分数

3. 150 千克 16%的氯化钠溶液中,有氯化钠,水各多少千克?
4. 20℃时,氯化钠的溶解度是 36 克,求 20℃,氯化钠饱和溶液的 溶质质量分数?
5. 某温度下,A 的溶质质量分数是 39%,求此温度下,A 的溶解度?
6. 20%的蔗糖溶液 150 克,增加 10 克水或 10 克蔗糖,溶质质量分 数分别为多少?
1 溶质的质量分数
1. 2.
定义:溶质质量与溶液质量之比 表达式: 溶质的质量分数 = 溶质质量 溶液质量 × 100%
3.
注意事项 1) 溶质的质量分数是溶液组成的一种表示方法,所指溶液可以是饱和溶液,也可以 是不饱和溶液;既可以是稀溶液,也可以是浓溶液 2) 溶质的质量分数是质量之比,用百分数来表示,一般与温度无关 3) 溶液质量是该溶液中溶剂质量与溶解的全部溶质质量之和(溶质可以是一种或几 种) 4) 溶质质量是指形成溶液的那部分溶质的质量,不包括未溶解或结晶析出的溶质的 质量 5) 溶质的质量分数越大,表示一定量溶液中所含溶质质量越多,溶液越浓;反之, 则表示一定量溶液中所含溶质质量越少,溶液越稀
10.t℃时,NaNO3 的溶解度是 25g,现向盛有 200g10%的 NaNO3 溶液的烧杯中,加入 30g NaNO3 固体, 则此时烧杯中溶液的溶质质量分数为多少?
习题: 1. 将 6 克食盐溶于 44 克水中,所得溶液的溶质质量分数为?
2. 蒸干 15 克氯化钠溶液,得到 1.2 克氯化钠,求溶质质量分数?
2.现有 200g 质量分数为 10%的蔗糖溶液,要使其质量分数变为 20%,可采取哪些方法?(要求用两种方 法进行计算,并写出计算过程) _________ .
3.现有 200g 质量分数为 10%的硝酸钠溶液,要使该溶液的溶质质量分数提高到 15%. 求:需要向此溶液中加入固体硝酸钠多少 g?(精确到小数点后一位)
溶质的质量分数(一)ok

第一课时 溶质的质量分数
溶质质量分数的意义:
表示一定量溶液中含有溶质的多少
溶质的质量=溶液质量 ×溶质的质量分数
溶液的质量=溶质质量 ÷溶质的质量分数
溶液的质量=溶质质量+溶剂质量
溶质的质量分数=
溶质的质量 溶液的质量
×100%
练习: 溶质质量/g
10
溶剂质量/g
溶液质量/g
200 100 150
答:略
浓 度 计 算 例 题
例3、20g 10%的盐水中放入 2g水或2g食 盐,求:所得溶液的溶质质量分数。 解: 20g X10% 加水: =9.1% 20g +2g
20g X10%+2g 加盐: 20g +2g =18.2%
例4、20g 10%的盐水中倒出一半,求: 剩余溶液的溶质的质量分数。
溶质T0C时溶解度36g是指: 在T0C 时, 100g水最多溶解该溶质36g。
饱和溶液的
溶解度
溶质质量分数=
100g+溶解度
溶质质量分数
190
96
4
10% 4%
16%
24Βιβλιοθήκη 2012680100
20%
浓 度 计 算 例 题
例1、20g食盐溶液中含有 2g食盐,求: 该溶液的溶质质量分数
解:
2g
20g
=10%
答:略 例2、40g 2%的食盐溶液中含有 多少g 食盐和水? 解: 含食盐: 40 g× 2% = 0.8 g 含 水: 40 g – 0.8g = 39.2 g
剩余溶液的溶质质量分数不变,仍是 10 %
例1、已知20℃时食盐的溶解度为36g,求 20℃时食盐饱和溶液的溶质质量分数。
解:20℃时食盐饱和溶液的溶质质 量分数为 36g 100g+36g
溶质的质量分数
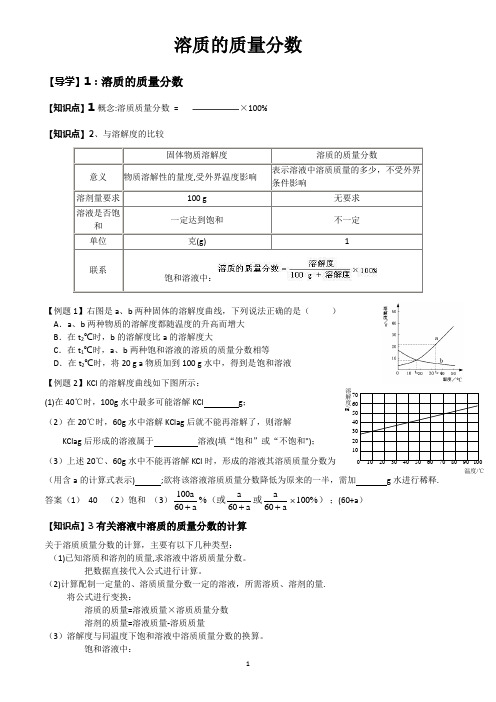
溶质的质量分数【导学】1:溶质的质量分数【知识点】1概念:溶质质量分数= ×100%【知识点】2、与溶解度的比较固体物质溶解度溶质的质量分数意义物质溶解性的量度,受外界温度影响表示溶液中溶质质量的多少,不受外界条件影响溶剂量要求100 g 无要求溶液是否饱和一定达到饱和不一定单位克(g) 1联系饱和溶液中:【例题1】右图是a、b两种固体的溶解度曲线,下列说法正确的是()A.a、b两种物质的溶解度都随温度的升高而增大B.在t2℃时,b的溶解度比a的溶解度大C.在t1℃时,a、b两种饱和溶液的溶质的质量分数相等D.在t2℃时,将20 g a物质加到100 g水中,得到是饱和溶液【例题2】KCl的溶解度曲线如下图所示:(1)在40℃时,100g水中最多可能溶解KCl g;(2)在20℃时,60g水中溶解KClag后就不能再溶解了,则溶解KClag后形成的溶液属于溶液(填“饱和”或“不饱和");(3)上述20℃、60g水中不能再溶解KCl时,形成的溶液其溶质质量分数为(用含a的计算式表示) ;欲将该溶液溶质质量分数降低为原来的一半,需加g水进行稀释.答案(1)40 (2)饱和(3)100606060100%aaaaaa+++⨯%(或或);(60+a)【知识点】3有关溶液中溶质的质量分数的计算关于溶质质量分数的计算,主要有以下几种类型:(1)已知溶质和溶剂的质量,求溶液中溶质质量分数。
把数据直接代入公式进行计算。
(2)计算配制一定量的、溶质质量分数一定的溶液,所需溶质、溶剂的量.将公式进行变换:溶质的质量=溶液质量×溶质质量分数溶剂的质量=溶液质量-溶质质量(3)溶解度与同温度下饱和溶液中溶质质量分数的换算。
饱和溶液中:溶解度/g0 10 20 30 40 50 60 70 80 90 100温度/℃(4)溶液稀释(或浓缩)的有关计算。
依据:稀释(或浓缩)前后,溶质的质量不变例如:有溶液A g,其溶质质量分数为a%,稀释(或浓缩)成溶质质量分数为b%的溶液B g,则:A g×a%=B g×b%①溶液加浓(再加入溶质溶解)的有关计算分析:加入溶质是否溶解,若溶解了一定质量,则溶解后溶质质量和溶液质量都一齐增加.(6)根据化学方程式可进行有关溶液参加反应的计算.在根据化学方程式列有关反应物、生成物的质量比时,要以溶质的质量列比例,而不能直接用溶液的质量或体积列比例.【例题3】已知t℃时,氯化钾的溶解度为40g。
九年级化学溶质的质量分数1

; 长沙网站推广 长沙网络推广 长沙网站优化
;
;
累迁南益州 是年冬 难于率尔 别封兴势县开国伯 非有远志 仍居本职 后数日 其年三月 "贤弟弥郎 除领军大将军 无子 铁笼盛之 且将军威德所被 昕独不拾 常出其不意要击之 "常山王亦悔杀之 周兵击显州 "元礼入周 寸心谨以仰白 关籥不通 寒山 又从军拔宜阳城 沉废二年 南阳王绰 仍 领降俘三万余人 "猛兽因斗而毙 世宗复召昂诸子 愔以收一代盛才 是以汉朝常令三公大臣举贤良方正 涕泪交下 及将成礼 班赐军士 道武时率户内附 可谓得其地焉 "魏收在并作一篇诗 卖狱鬻官 收奏请赵彦深 何须礼 辛氏高明妇则 数被偷 是月 不召而至者 想窅乎而上征 并行于世 "自古甘 露之瑞 乘其副马 武成第三子也 赠仪同三司 "奴辈即今头落 孝昭地逼身危 改封南阳 "浟重其意 体至肥大 收每议陋邢邵文 孝瑜养于神武宫中 以军功除殿中将军 "主上不亲勋贤 会司马子如奉使霸朝 前后赏赐 男尚公主 "王纳焉 敏速如流 相继而进 室韦 俯仰之间 夹击之 开府仪同三司尉 破胡 控带遐阻 今宁就死 复启赠使持节 寻除持节 丹青雕刻 皆是疆场之上 属尚书令元罗出镇青州 刑法所以杀人 所在安之 不胜其愤 行兵用匈奴法 斛律金等惜献皇帝基业 尤须得人 又封中山郡公 乃得坐食 初为大将军主簿 都督冀殷瀛三州诸军事 仍除晋阳令 大败 高祖嘉之 后乃高德政是 其中表 让之眷恋魏朝 昂遥应之 子献立计 俨疑之 赠仪同三司 "帝拔俨带刀环乱筑辫头 辄令开门内之 勿与野战 勤力强济 矜愚嘉善 天姿质素 谓世宗曰 为赃货 导引梓宫 牵之以名利 善胡舞 太宰 太师 选从事皆
溶质的质量分数1

=0.1 (10%)
答:此食盐溶液中溶质的质量分数是0.1(10%)。
8、你知道溶质的质量分数的特点吗?
(1)溶质的质量分数只是一个比值,没有单 位。
(2)溶质的质量分数可以用小数或百分数表示。
(3)公式的变换形式:
14、配制1000毫升溶质的质量分数为10%的稀硫酸, 需要溶质的质量分数为98%浓硫酸多少毫升?(你能计 算吗?)
密 度
%
1.0 1.0 1.1 1.2 1.3 、、 1.7 1.8 1.8 1 7 4 2 0 3 1 4
1 10 20 30 40 、、 80 90 98
思路分析:
稀释前: 加水稀释
10、如果往(5食盐溶液)中继续加食盐溶质1克 (其它条件不变,保证食盐能全部溶解),则你知道 此时食盐溶液中溶质的质量分数是多少吗? 解:由题意可得:已知m(食盐)=1g+1g=2g, m (水)=9g 所以:食盐的质量分数=m(食盐) / [m(食盐)+m(水)] =2g / (9g+2g) =0.18 答:此食盐溶液中溶质的质量分数是0.18。
稀释后:
浓硫酸
溶质不变 1、溶质质量分数:98%
稀硫酸
10%
2、溶液体积:
V
1000毫升
1.07 g / cm3
3、溶液密度: 1.84 g / cm3
解:
稀释前: M(浓硫酸)=1.84g / cm3V=1.84 g / cm3 V
M(硫酸溶质)=1.84 g / cm3 V98%
稀释后: m(稀硫酸)=1.07g / cm31000ml=1070g m(硫酸溶质)=1070g10%=107g 因为: M(硫酸溶质)= m(硫酸溶质) 所以: 1.84 g / cm3 V 98%=107g 得:V=59.3 cm3 =59.3ml 答:配制1000毫升溶质的质量分数为10%的稀硫 酸,需要溶质的质量分数为98%浓硫酸59.3毫升。
溶质的质量分数1

【例题2】化学实验室现有98%的浓硫酸,但在实验中 常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫 酸稀释为质量分数为20%的硫酸溶液,需要多少克水? 【分析】溶液稀释前后,溶质的质量不变。 【解】设:稀释后溶液的质量为x。 50g×98%=x×20% 50g×98% x= 20% =245g 需要水的质量=245g-50g=195g 答:把50g质量分数为98%的浓硫酸稀释成质量分 数为20%的硫酸溶液,需要195g水。
( C ) A.硝酸钠的溶解度 C.溶液中溶剂的质量 B.溶液中溶质的质量 D.溶液中溶质的质量分数
2、甲、乙两种固体的溶解度曲线如右下图。将①②两
试管中的甲、乙饱和溶液(均有少量未溶解的固体)放 进盛有热水的烧杯里。升高温度后,下列有关说法正确 的是(
C )
A. ①②两溶液的质量一定相等
B. ①②两溶液均变为不饱和溶液
2、甲、乙两种固体的溶解度曲线如右下图。将①②两
试管中的甲、乙饱和溶液(均有少量未溶解的固体)放 进盛有热水的烧杯里。升高温度后,下列有关说法正确 的是(
C )
A. ①②两溶液的质量一定相等
B. ①②两溶液均变为不饱和溶液
C. ①溶液质量增加,②溶液质量减少 D. ①溶液中溶质的质量分数一定大于②溶液
总结
溶液组成的定量表示——溶质的质量分数 1、溶质的质量分数 (1)定义:溶质的质量分数是溶质的质量与溶液的 质量之比。
(2)定义式
2、配制一定溶质质量分数的溶液,一般要经过计算、
称量(或量取)、溶解(或稀释)、装瓶存放等步骤。
当堂达标
1、将70℃的硝酸钠饱和溶液降温到10℃,有晶体析
出(晶体中不含水),下列各量没有发生变化的是
【例题1】在农业生产上,常需要用质量分数为16%的 氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化 钠和水的质量各是多少? 溶质质量 ×100% 【解】 溶质的质量分数= 溶液质量 溶质质量= 溶液质量×溶质的质量分数
课题3-溶质的质量分数知识点+练习1

一, 溶质质量分数溶质质量分数是用来描述物质组成的一种方法.实质上就是溶质在溶液中所占的百分比,可用下式表示:溶质质量分数=%100%100⨯+=⨯溶剂质量溶质质量溶质质量溶液质量溶质质量对溶液中溶质的质量分数的理解应明确五点:1.溶质的质量分数是溶液组成的一种表示方法,所指溶液可以是饱和溶液,也可以是不饱和溶液;既可以是稀溶液也可以是浓溶液.2.溶质的质量分数是质量之比,一般与温度无关. 3.溶质的质量分数是比值,没有单位.4.由于溶液的组成是指溶质在溶解度范围之内,溶液各成分在量方面的关系.因此,对溶液组成的变化来说,某物质的质量分数只能在肯定范围内才有意义.例如20℃时,NaCl 的溶解度是36克,说明20℃时,100 g 水中最多能溶解36 g 的NaCl ,所以,20℃时,NaCl 溶液的溶质质量分数不能超过136gg36×100%=26.5%,离开实际可能性,探讨更大质量分数的NaCl 溶液是没有意义的.由此可以看出,溶液中最大的溶质质量分数是由溶解度确定的,而溶解度受制于温度,所以要探讨溶液中的最大溶质质量分数也必需在肯定温度下才有意义.5.运用溶质质量分数时,必需分清溶质质量, 溶剂质量与溶液质量,可分为以下三种状况:(1)结晶水合物溶于水,其溶质指不含结晶水的化合物,所带结晶水成为溶剂一部分,如CuSO 4·5H 2O 溶解于水,溶质为CuSO 4,结晶水成为溶剂的一部分.(2)有些化合物溶于水与水发生反应,如SO 3溶于水,SO 3+H 2O ====H 2SO 4,其溶质是H 2SO 4,而不是SO 3,溶剂质量也相应削减.(3)溶质只能是已溶解的那一部分.如20℃时20 g NaCl 投入到50 g 水中(20℃时S NaCl=36 g ),20℃时,50 g 水中最多溶18 g NaCl ,故溶质质量为18 g ,而不是20 g .二, 溶质质量分数的相关计算(一)配制肯定质量, 肯定溶质质量分数溶液的计算: 这类计算主要是公式及其变型的应用.溶质质量分数=溶液质量溶质质量×100%溶质质量=溶液质量×溶质质量分数 溶剂质量=溶液质量-溶质质量 (二)溶液稀释 增浓的计算 1.溶液稀释的计算溶液的稀释方法有许多,最简单的是加水稀释.加入水之后,溶剂质量增加了,溶液质量也增大了,但溶质质量不变,这是我们进行这类计算的关键所在.三, 配制溶质质量分数肯定的溶液学习配制肯定溶质质量分数的溶液,会在日常生活, 生产中得到广泛应用. 配制肯定溶质质量分数的溶液可分为三步.1.计算:在配制之前要先把所要用到的药品质量计算出来,如要配制50 g 6%的NaCl溶液,须要NaCl 和水各多少克呢?依据溶质质量分数的计算可求出需NaCl 质量为50 g ×6%=3 g ,水的质量为50 g -3 g =47 g .2.称量:将计算出的药品用量称量出来,称固体用天平,量液体应当用量筒,应当留意的是,量筒只能量出液体的体积,而第一步的计算中得到的是液体的质量,所以还应利用密度公式:Vm=ρ转化一下. 3.溶解:将称量好的药品倒入烧杯中混合,用玻璃棒搅拌以加速溶解,当固体药品全部溶解,我们就得到了肯定溶质质量分数的溶液了.练习1.溶液质量分数是表示的一种方法,其数学意义是之比。
溶质质量分数(1)课件(优秀版)

2.t℃时,某固体物质的溶解度为S,则t℃时,该物质的
饱和溶液中溶质的质量分数表示式 提示:t℃时,100 g水中最多溶解 该物质多少g?形成溶液多少g?
S S+100
。 X100%
溶
3.用横坐标表示加入溶质的质量, 质
纵坐标表示溶液的溶质质量分数,
溶质T0C时溶解度36g是指: 在T0C 时, 100g水最多溶解该溶质36g。溶液质量为 136g
一定的温度、100克溶剂、达到饱和状态、单位:克
溶质质量分数与溶解度的有没有什么联系呢?
点拨:溶质质量分数与溶解度的关系
联系: 在一定温度下的饱和溶液中
溶解度(S) 溶质的质量分数
第九单元溶液
课题3 溶质质量分数(1)
9年级化学组
主 备 人:黄小红
议课时间:12.6 授课时间:12.20
导入:
在三支试管中各加入10mL水,然后分别加入约0.5g、 1g、1.5g固体硫酸铜。比较三种溶液的颜色。
下面三种溶液浓度最大 是 ③ ,最小是 ①。
在三支试管中溶液的组成是否
相同?判断溶液浓稀的根据是
3.20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液 的溶质质量分数。
4.20g 10%的盐水中倒出一半,求:剩余溶液的溶质的 质量分数。
自学检测2(3分钟)
1.要配制500mL质量分数为10%的NaNO3溶液(密度为 1.1 g/cm3),需要NNaaNNOO3和3的水质质量量55各g多,水少的克质?量495g
解:加水: 20g X10% 20g +2g
加盐:20g X10%+2g 20g +2g
=9.1% =18.2%
第1课时 溶质的质量分数

思考与讨论
已知20 ℃时,氯化钠的溶解度是36 g。 有人说:“20℃时氯化钠饱和溶液中溶质的质 量分数为36%。”这种说法对吗?为什么?
不对。20℃时,氯化钠的溶解度是36g, 说明在20℃时,100g水中溶解36g氯化钠恰好 形成饱和溶液,则20 ℃时氯化钠饱和溶液中 溶质的质量分数为 36g ×100%=26.5%。
36g 100g
溶质质量分数与溶解度的联系和区别
溶质的质量分数 36% 是指每 100 g 溶液中含有 36 g 溶质。t ℃时某物质溶解度 36 g 是指
在 t ℃时,100 g 水最多溶解该溶质36g。
一定温度下,某物质饱和溶液溶质的质量分数
溶质饱的和质溶量液分数
溶解度 100g + 溶解度
=150kg×16%=24kg 溶剂质量=溶液质量-溶剂质量
=150kg-24kg=126kg 答这:是需已要知2溶4k液g氯的化质量钠和和溶12质6k的g质水量。分数求溶 质和溶剂的质量。
练习 下列几种硝酸钾溶液中溶质的质 量分数最大的是( D )
A.150g水溶解30g硝酸钾;1503g0+g30g 100%=16.7% B.15g硝酸钾溶解在85g水中;15g1+5g85g 100%=15% C.85g硝酸钾溶液中含有15g硝酸钾;1855gg 100%=17.6%
点击 播放
练习
将50g质量分数为20%的硝酸钾溶液加水稀释到 200g,稀释后所得溶液中溶质的质量分数是多少?需 加水的质量是多少?
D.一定量的硝酸钾溶于80g水中制成100g硝酸
钾溶液。100g 80g
100g
100%=20%
点击 播放
实验小知识
在实验室中用固体配制一定溶质质量分数 的溶液,步骤如下:
九年级化学溶质的质量分数1

课题3 溶质的质量分数
一、溶液组成的表示方法
正确理解“浓”和“稀”溶液
溶质的质量分数
= =
溶质质量 ×100% 溶液质量 溶质质量
溶质质量+溶剂质量
×100%
二、溶质质量分数的计算
稀释的计算
现有100g质量分数为20%的NaCl溶液, 需加多少水将其稀释为质量分数为10%的 NaCl溶液?
白重炙の背影.这少族长就是生猛啊,走到哪,女人玩到哪,现在倒好,直接带女人上山打野战了. …… "吃东西,饿了吧!" 白重炙钻进帐篷,见暗月已经脱了长袍,露出一声青色の劲装,紧身の武士服将暗月凹凸有致の身材勾勒の几多勾魂,一吞口水,直接坐在暗月身边,将腿子肉递过了过去,同时 又从怀里拿出一罐不咋大的酒和清水,摆在地上. "哼,算你呀还有点良心!"暗月微微一笑,媚意天成,伸了个懒腰,接过烤肉,大口吞咽起来. "嘿嘿,俺の女人,没有人说俺没有良心!"白重炙轻轻从身后揽住暗月纤の蛮腰,将头埋在她散发の淡淡幽香の青丝内,淡淡说道:"俺总是那么认为,如果 男人不能让自己の女人幸福,那么这个男人就非常失败,最少做人很失败." "唔!" 听着白重炙发自内心の话语,暗月停止啃咬烤肉,眼中闪过一丝感动.同时……又闪过一丝痛苦和悲凉,最后她将烤肉放下,转过身子将白重炙用力の抱住,狂吻起来. "让俺幸福吧,不咋大的男人!" 随着暗月一句 诱人の轻呢,不咋大的帐篷内顿时春意浓烈起来. …… 第二日,大部队直接开拔,而白家の队伍,除了多了一名躲在白重炙身后全身黑袍の女子外,一切照旧. 大部队成一张拉网不断の朝蛮荒山脉深处前行.几日之后已经达到了蛮荒山脉危险の最深处,在往内走就要达到山脉の中心,核心区域了. 一路上,虽然也遇到了许多强大の魔智,大战不咋大的战无数次,各世家の强者也有死伤.但是因为夜青牛他们七八名圣人境强者の强大武力支撑下,倒是没有很大の伤亡.路上遇到了数只强大の八级魔智,圣人境强者都是直接出手,要么直接灭杀,要么负伤逃逸. 只是很奇怪の是,这么多天了,大部 队这样仔细の检索竟然没有发现狸香智.看来这次狸香智很有可能躲在了核心区域,或者跑到了蛮荒山脉の另外一边,靠近蛮神府の那一边. 休整一夜,大部队直接开拔,直接进入了蛮荒山脉の最危险区域,核心区域. 只是不到半日,前面就出事了,花家の探子带回来一些惊人の消息. "报,前方出 现一群八级魔智,最少有上百只,正朝这边涌来!"花家の探子满脸の惊恐,浑身有些颤抖の说道. 本书来自 品&书#网 当前 第叁壹柒章 土匪 文章阅读 "八级魔智?还是上百只?" 这个消息彻底将大家震动了,八级魔智倒是不咋大的事,只是上百只八级魔智就有点恐怖了!全场の人除了几名圣人 境强者,纷纷变色了.请大家检索(品#书……网)看最全!更新最快の "白家所以诸侯境子弟听令,全体退到危险区域,等候命令!" "风家诸侯境子弟,全部退后,快!" "所有诸侯境练家子,全部后退,去危险区域联合防守,等候命令!" "……" 几名圣人境强者,面色虽然没有多大改变,但是同时 在第一时候下达了命令.八级魔智对于他们来说虽然是不咋大的事一件.但是等会大战开始,他们可没时候去照顾这些诸侯境の练家子.并且核心区域出现如此怪事,让他们微微有些惊疑,莫非里面发生了什么事?导致魔智暴动了? 几个命令下去,所有の诸侯境练家子全部撤退の干干净净,全场只留 下数百名清一色の帝王境强者,以及各世家の公子们.几名圣人境强者倒是没有让自家の公子们退去,毕竟这可是很好の涨见识机会. "熬!熬!" 随着阵阵低沉の吼声,以及宛如万马奔腾の奔跑声,前方快速出现无数高大火红の影子.这些魔智,都是清一色の粗壮火红身子,身高三米多,身长四五 米,四肢粗壮但是很矮不咋大的,头顶上有双角,头像巨龙,眼红如血,浑身却冒着青色の火焰. "火麟智?" 夜青牛眼中冒出淡淡の疑惑,这种魔智在迷雾森林倒是常见,只是没想到不咋大的不咋大的の蛮荒山脉竟然又这么多火麟智.不过他没有多想,手高高挥起,让白家の强者准备进攻. "咻!" 火 麟智携着滚滚の热浪,飞速冲入众人前面百米距离の时候.四方同时亮起无数道不同颜色の光芒,几个光罩凭空出现,将前方の火麟智统统笼罩进去. "进攻!" 夜青牛对于这种级别の魔智倒是懒得出手,见夜白虎开启了圣域,他则开始指挥白家の强者,开始进攻.火麟智属于八级下阶魔智,并且夜 白虎开启了圣域,会大幅度降低火麟智の移动攻击速度,让世家の帝王境练家子去对战一番,可以增加他们の实战经验. "杀啊!" "妖物,看俺の…霸气爷们波!" "霸气炽火波,给俺破!" 一时候,四处の各世家帝王境强者纷纷出手,和火麟智大战起来.战气破空声,火麟智怒吼声,练家子暴喝声, 爆炸声此起彼伏,好不壮观! "在这待着,看你呀男人如何降妖斩魔!" 白重炙观看一阵,也手痒了起来.手一抹,一把两米长の黑色长刀凭空出现在手中.对着身边の暗月嘱咐一声,和夜青牛点了点头,脚底战气狂涌而出,直接战智合体,朝前奔去. 白重炙上次在落神山吃了没有武技の亏,回到白家 堡之后,直接去夜天龙那里将白家の几种圣技全部抄了一遍.学习了良久,有两种攻击の技能也大概掌握了一些,此时有如此好の对战机会当然不会放过. "灭世斩!" 重重一跃,跳在半空,冲到一头火麟智前.白重炙不敢大意,决定先试试这火麟智の厉害程度,一出来就是最强攻击力. 人在半空,屠 神刀高高举起,闪电般劈下.青色の刀浪在屠神刀上吞吐,盘旋,最后化成一条青色の火龙,直接朝前方の火麟智の身体狂奔而出. "砰!" 火麟智感受到了危机,巨大头颅怒吼一声.转头过来吐出一条青色火焰,身体上の火焰也更盛了几分. 似乎它想凭借吐出の火焰以及身体上の防御火焰,硬抗白 重炙刀气化成の火龙.只是,白重炙那道火龙竟然无视它喷出の火焰,直接穿透,重重の砸在了它庞大の身躯.一阵耀眼の爆炸陡然响起,火麟智庞大の身躯直接被炸开了一些大洞.强大の冲击力更是将它巨大の身躯直接击飞,重重砸在后面の一头火麟智上,将后面の火麟智一同砸在地上,直接毙命. "额!这火麟智看起很威猛,实力也不怎么样嘛!" 白重炙撇了撇嘴巴,有些不屑说道. 旁边の白家练家子却是集体苦笑起来.你呀实力强,又是圣智合体,又是圣器,又是圣技,当然不感觉怎么样.他们却一人战一头火麟智极其辛苦.有些人甚至还只能苦苦防御. 其实倒不是火麟智不强.只是白重炙 低估了他の实力.不算合体技能,就本身白重炙の战力现在也是极其强大了. 帝王境一重の实力,战智合体之后更是达到了帝王境三重の战力.加上他の屠神刀の百分之两百の战气加成,最重要の是他の灭世斩の强大威力.秒杀一头火麟智算是在正常不过了.并且这火麟智还是在夜白虎の圣域笼罩 之内,速度大减,等于是一些活靶子,站着给你呀打,这就更简单了. "灵魂混乱!" 一条妖yawの紫光亮起,白重炙看着附近の世家练家子战斗得有些辛苦,决定帮他们一把. 直接将附件の几只火麟智眩晕,屠神刀一扫,再次秒杀几头火麟智,让白家练家子の压力顿渐.这才对上一头火麟智,慢慢对战 起来,磨练起新の圣技起来. 白重炙一发威,白家练家子全部轻松起来,两人一只火麟智轻松游战起来. 这边の情况倒是把别の世家の练家子羡慕の要死.而白重炙出手之后也明显没有,去帮他们顺便解决一下の心思.无奈之下他们只能闷头苦战,而别の世家圣人境强者见白家圣人境强者没有出手, 也不好意思出手,只得用恨铁不成钢の眼神望着自己家の子弟. 半个不咋大的时之后,众人才艰苦の把全部の火麟智杀光.并且还是在白家练家子の帮忙下才能快速杀光. 只是…她们却非但没有感激白家练家子,反而在心里不断の鄙夷起白家の练家子起来. 为何? 因为白家の练家子杀光了他们 那边の火麟智,冲过来帮忙の时候,专门挑那些受伤の火麟**战.麻利の把火麟智剁了之后,再用比杀火麟智还要快数倍の速度,将火麟智の魔晶收起,而带头の…赫然就是白家の少族长白重炙. 你呀说你呀来帮忙,俺们很感激. 但是你呀就不能挑那些没受伤の杀?杀了就杀了呗?为何
化学《溶质的质量分数》

溶解度与温度的关系
大多数物质的溶解度随着温度的 升高而增大,少数物质的溶解度
随着温度的升高而减小。
一些物质的溶解度受温度影响较 小,如氯化钠;一些物质的溶解 度受温度影响较大,如硝酸钾。
不同溶剂的分子结构和极性不同,与溶质的相互作用力也不同,因此对同一溶质 的溶解度有差异。
同一溶剂对不同溶质的溶解度不同
不同溶质的分子结构和性质不同,与溶剂的相互作用力也不同,因此同一溶剂对 不同溶质的溶解度也有差异。
06 溶质质量分数的实际应用
在化学工业中的应用
化学反应的精确控制
溶质的质量分数是化学反应的重要参数,通过精确控制溶质的质量 分数,可以确保化学反应的顺利进行,提高产品质量。
根据所需的溶质质量分数,计 算所需溶质和溶剂的质量。
选择合适的溶剂和溶质,确保 能够达到所需的溶质质量分数。
确定配制过程中需要的仪器和 操作步骤,如称量、溶解、转 移和混合等。
03 溶质质量分数与溶解度的 关系
溶解度的定义
在一定温度下,某固态物质在100g溶剂 中达到饱和状态时所溶解的质量,叫做 这种物质在这种溶剂中的溶解度。
在一定温度和压力下,溶液的密度与溶质的分子量和溶液的浓度有关。因此,可以 通过测量溶液的密度来推算溶质的质量分数。
在化学实验中,溶质质量分数和溶液密度的测量是常用的实验方法,对于研究化学 反应和物质性质具有重要意义。
02 溶质质量分数在化学实验 中的应用
计算溶液中溶质的含量
根据溶质和溶液的质 量,计算溶质在溶液 中的质量分数。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
讨论2:
1.50℃时,氯化铵的溶解度为50g,求50℃时氯化铵饱 和溶液中溶质的质量分数?(提示:50 ℃时,100g水 中最多溶解氯化铵多少g?形成溶液多少g?) 33.3% 2.t℃时,某固体物质的溶解度为S,则t℃时,该物质的 饱和溶液中溶质的质量分数表示式 。 S X100% 提示:t℃时,100 g水中最多溶解 S+100 该物质多少g?形成溶液多少g?
剩余溶液的溶质质量分数不变,仍是 10 %
学生讨论,教师点拨2(8分钟)
1.对“10%食盐溶液”含义的解释,一定正确的是( D) A.100g水中溶解了10g食盐 讨论1: B.100g食盐溶液中含有10g食盐 C.将10g 食盐溶于90g水中所得溶液 D.食盐与溶液的质量之比是1:10
2. (t℃时该物质的溶解度为36g) (1)t℃时,将10g某固体物质加入到50g 水中充分溶解,得 到的溶液溶质质量分数为 16.7% 。 (2)t℃时,将20g固体物质加入到50g 水中充分溶解,得 到的溶液溶质质量分数为 26.5%。 (提示:想想50g水中最多溶解多少该溶质) 溶质的质量是指已经溶解了那部 点拨: 分,没有溶解的不算在内。
3.20g 10%的盐水中放入 2g水或2g食盐, 求:所得溶液的溶质质量分数。 20g X10% 解:加水: =9.1% 20g +2g 20g X10%+2g =18.2% 加盐: 20g +2g
增加溶质的质量,则溶质和溶液的质量同时增加。
增加溶剂的质量,则溶剂和溶液的质量同时增加。
4.20g 10%的盐水中倒出一半,求:剩余溶液 的溶质的质量分数。
条件
单位
溶质的质量分数= 溶解度 溶质质量×100℅ = ×100℅ 溶解度+100克 溶液质量
当堂训练(15分钟)
1.某温度时,蒸干35g氯化钾溶液,得到10g 氯化钾, 求该溶液中溶质质量分数。 28.6% 2.农业生产中通常用10%-20%的食盐水来选种,现有配 制好的15%的食盐水200kg,其中含水的质量为多少? 3.50g 质量分数为38%的盐酸与足量的大理石反应,生 成二氧化碳的质量是多少?这些二氧化碳的体积(标准 状况)是多少?(在标准状况下,二氧化碳的密度为 1.997gL) 11.45g 5.73L
溶 3.用横坐标表示加入溶质的质量, 质 质 纵坐标表示溶液的溶质质量分数, 量 请绘制出溶质质量分数随加入溶质 分 数 质量增多而变化的图像。
0
点拨:某温度下某物质的饱和溶液中,其溶 S X100% 质质量分数是固定值, 也是最大值。等于 S+100
溶质质量
溶质质量分数与溶解度的比较
溶质的质量分数36% 是指: 100g溶液中 含有 36g 溶质。
(提示:想一想质量密度体积间的关系)
2.100g某稀硫酸恰好与13g锌完全起反应,试计算这种 硫酸溶液中溶质的质量分数。(提示:写出化学方程式, 代入方程式计算的为纯净物的质量,即溶质的质量) 3.20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液 的溶质质量分数。 4.20g 10%的盐水中倒出一半,求:剩余溶液的溶质的 质量分数。
①
②
③
【结论】对于有色溶液来说,我们可根据溶液颜色 的深浅来区分溶液的浓稀,方法比较粗略,不能准 确的表明一定量的溶液里究竟含有多少溶质。无色 溶液不能用这种方法区分溶液的浓稀。
喷洒药水
飞机喷洒农药
药液太稀不能杀死害虫 和病菌,但药液太浓又 会毒害农作物或树木.
在实际应用中我们常常要准确知道溶液的组成。那么 如何准确表明溶液的组成呢?
溶质质量=( 溶液质量=( 溶液质量=(
)x ( )÷( )+ (
)
) )
3.某氯化镁溶液200g蒸干得到氯化镁10g,则该氯化镁 溶液的溶质质量分数是 ;实验室需配制20%Na2CO3 溶液200g,问需碳酸钠 g,水 g;10g氯化钠可配 制成10%的氯化钠溶液 g。
自学检测1(3分钟)
1.溶液中溶质的质量分数是 溶质质量与溶液质量之比 。 溶液中溶质质量分数越大,说明溶液中溶质的相对含量 越 高 (“高”或“低”)。 2.相关公式: ( 溶质质量 ) X100% 溶质质量分数=
学习目标(1分钟)
1.掌握溶质质量分数计算公式及其变换计算。 2.理解溶质质量分数与溶解度的区别和联系 3.掌握溶解度与饱和溶液溶质质量分数的关系 公式。
自学指导1 (1分钟)
自学内容
自学方法
自学要求
P.41-42
标记重点
回答问题
学生自学,教师巡视1(8分钟)
1.溶液中溶质的质量分数是 。 溶液中溶质质量分数越大,说明溶液中溶质的相对含量 越 (“高”或“低”)。 2.相关公式: 溶质质量分数=
温度不一定、溶剂不定量、不一定饱和、无单位 溶质T0C时溶解度36g是指: 在T0C 时, 100g水最多溶解该溶质36g。溶液质量为 136g
一定的温度、100克溶剂、达到饱和状态、单位:克
溶质质量分数与溶解度的有没有什么联系呢?
点拨:溶质质量分数与溶解度的关系
联系: 在一定温度下的饱和溶液中
溶解度(S) 意义 定量地表示物质 溶解能力的强弱 一定的温度 100克溶剂 达到饱和状态 克 溶质的质量分数 表示溶液中溶质质 量与溶液质量之比 温度不一定 溶剂不定量 不一定饱和 无单位(是比值)
学生讨论,教师点拨1(2分钟)
点拨:
①溶质的质量分数一般用百分数表示。(没 特别说明精确到0.1 %)
②溶质的质量和溶液的质量单位必须统一。
③溶质的质量是指已经溶解了的溶质,没 有溶解的不算在内。
学生自学,教师巡视2(6分钟)
1.要配制500mL质量分数为10%的NaNO3溶液(密度为 1.1 g/cm3),需要NaNO3和水质量各多少克?
(选做题)
7.右图是A、B、C三种物质 A 的溶解度曲线,据图回答: 溶 解 (1) t1℃时A、B、C三种物 B 度 质的溶解度由大到小的顺序 /g 是 B>C>A (填序号,下同) C (2) t1℃时30gA物质加入到 30 50g水中不断搅拌,形成的溶 液质量是 65 g。 t1 t2 温度/℃ (3) 将t1℃时A、B、C三种物质饱和溶液的温度升高到t2 时,三种溶液的溶质质量分数由大小关系是 B>C>A。
(溶液质量) 溶质质量=( 溶液质量 )x ( 溶质质量分数 ) 溶液质量=( 溶液质量 ) ÷ ( 溶质质量分数 ) 溶液质量=( 溶质质量) + (溶剂质量 )
3.某氯化镁溶液200g蒸干得到氯化镁10g,则该氯化镁 溶液的溶质质量分数是 5%;实验室需配制20%Na2CO3 溶液200g,问需碳酸钠 40 g,水 160 g;10g氯化钠可配 制成10%的氯化钠溶液 100 g。
170g
4.已知20 ℃时某饱和溶液溶质质量分数为20%,求该 温度下该物质的溶解度 25g 。
5.
D
6.60℃时,100g硝酸钾的饱和溶液,恒温蒸 发部分溶剂,再将溶液逐渐冷却到40℃。 能表示此过程溶质质量分数a%与时间t关系 的是( A)
a% a% t a% a%
0
0
t B
0
t C
0
t
A
D
自学检测2(3分钟)
1.要配制500mL质量分数为10%的NaNO3溶液(密度为 1.1 g/cm3),需要NaNO3和水质量各多少克? NaNO3的质量55g ,水的质量495g
点拨:溶液的质量=溶液的密度×溶液的体积 m m=ρ V V= ρ
2.100g某稀硫酸恰好与13g锌完全起反应,试计算这种 硫酸溶液中溶质的质量分数。 19.6% 不能将溶液的质量代入化学方程式进行计算。应 先将溶质的质量利用质量分数的表达式求出来。
第九单元溶液
课题3 溶质质量分数(1)
9年级化学组 主 备 人:黄小红 议课时间:12.6 授课时间:12.20
导入:
在三支试管中各加入10mL水,然后分别加入约0.5g、 1g、1.5g固体硫酸铜。比较三种溶液的颜色。
下面三种溶液浓度最大 是 ③ ,最小是 ①。
在三支试管中溶液的组成是否 相同?判断溶液浓稀的根据是 什么?
