泛昔洛韦分散片稳定性的研究
RP-HPLC法测定泛昔洛韦分散片的含量及有关物质

r t d fom am ccov r Con l so T he m e ho a i pl ae r f i l i. cu in t d w ss m e,a c a e a d s e ii c ur t n p c fc,a d c l e u e ort e n ou d b s d f h q lt on r lo a cc o i s e sbl a l t . ua iy c t o ff m il v rdip r i e t b e s
r . 9 9 ; 均 回收 率 为 10 1 , D为 0 3 % , =0 99 8 平 0 . RS . 0 一9 泛 昔 洛 韦 与 有 关 物 质 能 完 全 分 离 。 结 论 本 方 法 简 便 、 确 、 属 性 强 , ; 准 专
可 用 于 泛 昔 洛 韦 分 散 片 的 含 量 及 有 关 物质 的测 定 。
ijcin v lme Re ut A g o ie rt so t ie n t er n eo 9 4  ̄ 8 . 0 g ml( 一 0 9 9 8 . ne t o u . o s ls o dl a i wa b an d i h a g f2 . 0 8 2 u / n y , . 99 ) .
The a e a e r c e y off mcc o i s 00 1 v r g e ov r a il v rwa 1 . (2 9)wih RSD .3 .The r l t d s s a e r e a ,= t 0 0 ea e ub t nc swe e s p —
W e huiw a g a d G a — n ng S — n n o Zu qi
to , hou 5 01) ( uin P o ica n t uef rDr F j r vn ilI si t o ug Con r l Fuz 3 00 a t
【药品名】泛昔洛韦【英文名】Famciclovir【别名】泛维尔;法昔洛韦;海正...

【药品名】泛昔洛韦【英文名】Famciclovir【别名】泛维尔;法昔洛韦;海正韦克;丽珠风;Famvir【剂型】片剂:125mg,250mg,500mg。
【药理作用】本药是喷昔洛韦(penciclovir)的前体药,和阿昔洛韦一样,它也是鸟苷类似物,可通过干扰病毒DNA聚合酶的活性抑制疱疹病毒DNA合成。
由于激活本药的第一步是转化成单磷酸盐,而单磷酸盐易被胸苷激酶催化,故本药极易被病毒胸苷激酶催化,而不易被人体酶催化,因此几乎对人体DNA无影响。
体外试验证实,本药和喷昔洛韦对人疱疹病毒的作用谱与阿昔洛韦相似,二者对抗单纯疱疹及水痘带状疱疹病毒的活性均好。
大多数临床分离到的耐阿昔洛韦的单纯疱疹和水痘带状疱疹毒株同样也耐受喷昔洛韦。
体外实验证实,少数耐阿昔洛韦的毒株对喷昔洛韦敏感,且喷昔洛韦对乙肝病毒有活性。
PCV 的体外抗病毒活性与ACV相似,但PCV在细胞内浓度高、半衰期长,其磷酸化率、稳定性、磷酸盐衍生物的浓度及对病毒DNA多聚酶的亲和力均高于ACV。
【药动学】本药由胃肠道吸收迅速,口服后0.7~0.9h血药浓度即达峰值,该峰值若按本药剂量计分别为:服用单剂500mg,为4mg/ml(范围为3.3~4.7mg/ml);服用250mg、500mg和750mg,各为1.6~1.9mg/ml、3.3~3.4mg/ml和5.1~5.3mg/ml。
本药吸收后通过去乙酰化和氧化作用在小肠壁和肝脏内迅速转变为喷昔洛韦,生物利用度为75%~77%。
它在血浆中浓度很低,主要分布于组织中。
本药在体内的总蛋白结合率小于20%,分布容积在静脉给药后为1.08L/kg。
多数喷昔洛韦通过肾小管的分泌和肾小球的过滤以原形由尿排出,其中口服后最初6h排出60%,总排出73%,静脉给药可排出94%。
本药口服后肾脏清除率为每小时27.7L,老年受试者的肾脏清除率较正常值低22%。
此外,另有27%的喷昔洛韦可经粪便排出。
本药的血清半衰期约2.5h,类似于阿昔洛韦,但前者的细胞内半衰期要长10~20倍。
泛昔洛韦片工艺技术要点

泛昔洛韦片工艺技术要点泛昔洛韦片是一种常用的口服溶解片,也是一种常用的药物制剂,其工艺技术是制备泛昔洛韦片的关键。
下面将介绍泛昔洛韦片工艺技术的要点。
首先,泛昔洛韦片的原料选择是制备该片剂的基本要素之一。
泛昔洛韦是一种抗病毒药物,因此其原料的纯度和质量必须得到保证。
药品生产厂家在选择原料时,必须参照相关药典的标准,确保原料符合规定的质量标准。
其次,制备泛昔洛韦片需要考虑制剂的稳定性和吸收性。
制剂的稳定性主要涉及药物在制剂中的分解和氧化反应,因此制备过程中必须注意保护药物的化学结构,防止药物的降解。
另外,为了提高制剂的吸收性,可以选择合适的辅料和溶剂,并采取适当的工艺控制方法,提高药物的溶解度和生物利用度。
第三,片剂的加工工艺是制备泛昔洛韦片的另一个重要方面。
加工工艺主要包括干燥、混合、压片和包衣等步骤。
在干燥过程中,需要注意控制温度和湿度,以避免药物的热分解和水解。
混合过程中,应该均匀加入辅料,并采取适当的搅拌方法,确保药物和辅料的均匀分散。
在压片过程中,需要控制压力和速度,以得到均匀致密的片剂。
另外,对于需要包衣的片剂,应选择适当的包衣材料,并采取合适的包衣方法,提高片剂的质量。
最后,泛昔洛韦片的包装也是该工艺技术的一个重要环节。
包装过程需要注意药品的无菌和密封性,以避免药品的污染和氧化。
在包装过程中,可以选择适当的包装材料和包装方法,确保片剂的质量和稳定性。
总之,泛昔洛韦片的工艺技术要点包括原料的选择、制剂的稳定性和吸收性、加工工艺的控制以及包装的质量。
药品生产厂家需要遵循相关的法规和标准,采取合理的工艺控制方法,确保泛昔洛韦片的质量和安全性。
泛昔洛韦治疗带状疱疹的临床观察

泛昔洛韦治疗带状疱疹的临床观察目的:观察泛昔洛韦治疗带状疱疹的疗效。
方法:患者口服泛昔洛韦治疗带状疱疹,观察其疗效及治疗过程中出现的不良反应。
结果:泛昔洛韦治疗带状疱疹止疱、止痛、痊愈时间均较阿昔洛韦明显缩短。
结论:泛昔洛韦治疗带状疱疹比阿昔洛韦起效快,能有效缩短病程。
标签:带状疱疹;泛昔洛韦;阿昔洛韦我院2008年2月~2009年5月分别采用泛昔洛韦与阿昔洛韦治疗带状疱疹,观察治疗效果与不良反应,现报道如下:1 资料与方法1.1 一般资料选择我院就诊的具有典型症状和体征的带状疱疹患者,在发病的5 d内,年龄18~50岁,不限性别,患者及家属同意使用泛昔洛韦或阿昔洛韦治疗者并定期复诊者。
对于下列情况不予选择:妊娠和哺乳期妇女;应用皮质类固醇或免疫抑制者;老年体弱或患恶性肿瘤等免疫功能低下者;对核苷类药物及多种药物过敏者;使用氨基糖苷类、磺胺类、环孢霉素A、丙磺舒及头孢菌素等肾毒性药物;精神异常者、肝肾功能出现异常者;1个月内外用、口服或注射过核苷类药物者。
治疗过程中,由于发生不良反应未完成疗程的病例不统计疗效,统计为不良反应。
将病例按治疗组∶对照组为2∶1的比例随机分组。
1.2 治疗方法治疗组口服泛昔洛韦,每次250 mg,每日3次,7 d为1个疗程。
对照组口服阿昔洛韦,每次200 mg,每日5次,7 d为1个疗程。
两组均不再使用其他药物。
1.3 观察项目观察患者在治疗前和开始服药第3、7、12、18天的治疗情况,个别有疱疹后神经痛患者延续观察到30 d。
记录患者皮损止疱、结痂、止痛、痊愈时间等。
疱疹后神经痛设为观察项目,但有无疱疹后神经痛不作为痊愈的项目。
对患者自觉症状和皮疹进行评分,皮疹项目包括水疱数目,水疱内容物性质,水疱塌陷、干涸、破溃、结痂、坏死进展情况,皮损面积,疼痛、瘙痒、烧灼感,有无全身症状及区域性淋巴结肿大等。
在用药7 d内观察并记录不良反应的症状、发生及持续的时间、反应程度、措施与转归等。
膦甲酸钠氯化钠注射液联合泛昔洛韦分散片治疗带状疱疹的疗效评价

膦甲酸钠氯化钠注射液联合泛昔洛韦分散片治疗带状疱疹的疗效评价【摘要】目的:探讨并分析膦甲酸钠氯化钠注射液联合泛昔洛韦分散片治疗带状疱疹的临床治疗有效性。
方法:选取我中心门诊部2021年8月到2022年8月期间的60例带状疱疹患者为本次研究对象。
并采取计算机表法对其进行研究,分为研究组和对照组,每组30例患者,对照组带状疱疹患者采取泛昔洛韦分散片治疗,研究组患者在对照组的前提下采取膦甲酸钠氯化钠注射液联合治疗。
结果:研究组带状疱疹患者的止疱时间、水疱干涸时间、结痂时间以及疼痛消退时间等疱疹改善情况均显著优于对照组;药物治疗有效性(96.67%)高于对照组(76.67%),组间存在差异;药物不良反应的发生情况与对照组相比,组间不存在差异(P>0.05)。
结论:选用膦甲酸钠氯化钠注射液联合泛昔洛韦分散片用于带状疱疹患者的临床治疗中,治疗效果显著,能够有效改善患者临床症状,同时用药安全性较高,值得推广应用。
关键词:膦甲酸钠;泛昔洛韦;带状疱疹带状疱疹是一种感染性疾病,主要是由于水痘-带状疱疹病毒所引发的一种临床表现[1]。
目前临床中对于带状疱疹通常采用药物治疗,从而有效控制患者病情,改善患者的疼痛及皮疹情况。
泛昔洛韦是临床中常用的抗病毒药物,但对于部分治疗效果并不理想的患者,通常会采用其它药物联合治疗,从而增强临床疗效[2]。
膦甲酸钠能够有效抑制病毒活性,止疱、止痛作用更为明显,能够有效促进患者康复[3]。
因此,最后选取我中心门诊部60例带状疱疹患者为本次研究对象探究分析两组药物的临床有效性,具体报告内容如下。
1资料和方法1.1一般资料选取我中心门诊部2021年8月到2022年8月期间的60例带状疱疹患者为本次研究对象。
并采取计算机表法对其进行研究,分为研究组和对照组,每组30例患者,研究组患者的男女比例为20/10,平均年龄为(55.32±3.24)岁,平均发病时间为(3.48±0.49)d;对照组患者的男女比例为18/12,平均年龄为(55.64±3.65)岁,平均发病时间为(3.58±0.39)d,将研究组与对照组患者的上述基本资料进行对比分析,结果表明组间差异并无统计学意义(P>0.05),因此可以进行本次研究比较。
泛昔洛韦颗粒干燥失重方法学研究

泛昔洛韦颗粒干燥失重方法学研究摘要:目的:研究泛昔洛韦颗粒干燥失重方法学,探索出适合乳糖含量较高的泛昔洛韦颗粒的干燥失重的实验方案,研究不同干燥剂对泛昔洛韦颗粒干燥失重的影响,建立一种准确度高、重复性好的检验方法。
方法:分别使用硅胶、无水氯化钙、五氧化二磷为干燥剂,在减压干燥器中,于80 ℃下将泛昔洛韦颗粒干燥至恒重。
比较使用这3种干燥剂时泛昔洛韦颗粒干燥失重结果,并与费休氏法测定的样品水分含量进行比较。
结果:使用硅胶、无水氯化钙、五氧化二磷为干燥剂测得的泛昔洛韦颗粒干燥失重分别为0.17%、2.04%和2.61%。
利用费休氏法测定样品中水分含量为2.6%,与使用五氧化二磷为干燥剂测得的干燥失重结果一致。
五氧化二磷作为干燥剂测得的干燥失重结果主要为样品中结晶水和游离水的减失重量。
使用无水氯化钙为干燥剂的结果比五氧化二磷的较低,其干燥失重结果主要为样品中部分结晶水和游离水的减失重量;使用硅胶为干燥剂测定的干燥失重结果最低,只有0.17%,主要为样品中的游离水。
结论:使用五氧化二磷和无水氯化钙为干燥剂测得的干燥失重结果都主要是乳糖中结晶水的减失重量,而使用硅胶为干燥剂不但能够克服乳糖中结晶水的影响,还能克服因结晶水导致的不易达到恒重的问题。
使用硅胶作为干燥剂的检测方法耐用性较好,准确度高,重复性好,能够轻松达到质量控制的目的。
关键词:泛昔洛韦颗粒;干燥失重;乳糖;游离水;干燥剂Methodological study on loss on drying of Famciclovir GranulesWEI Piaopiao, YANG Zhanwei, LI Chengyuan, SHEN Huixin, SHENG Bei,CHEN Xiaojiao, NI Meng(Wuhan Humanwell Pharmaceutical Co., Ltd. Wuhan 430000, China)Abstract Objective: This work is aim to the study of loss on drying of Famciclovir Granules, toexplore an experimental program suitable for Famciclovir Granules with high content of glucose, and to study the effect of different desiccants on loss on drying of Famciclovir, finally establish amethod with high accuracy and good reproducibility.Methods:Famciclovir Granules were dried to constant weight in avacuu m desiccator at 80°C with silica gel, anhydrous calcium chloride, and phosphorus pentoxide as desiccants, respectively. The results of loss on drying with these three desiccants were compared, and theywere compared with moisture content measured by the Fi sher’s method. Results: The loss on drying of Famciclovir Granules with a desiccantof silica gel, anhydrous calcium chloride, and phosphorus pentoxide were 0.17%, 2.04% and 2.61%, respectively. The moisture content in the sample measured by Fisher's method is 2.6%, which is consistent withthe loss on drying measured with phosphorus pentoxide as the desiccant. The loss of drying measured with phosphorus pentoxide as a desiccantis mainly the weight loss of crystal water and free water in the sample. The result with anhydrous calcium chloride as the desiccant is lower than that of phosphorus pentoxide, and the loss on drying is mainly the weight loss of part of the crystal water and free water in the sample; the loss on drying measured using silica gel as the desiccant is the lowest, as low as 0.17%. Conclusions: The weight loss on drying measured using phosphorus pentoxide and anhydrous calcium chloride as desiccants are mainly the weight loss of crystal water in lactose, while using silica gel as a desiccant is able to eliminatethe influence of crystal water in lactose. Besides, it can also overcome the difficulty in reaching constant weight because of crystal water. In addition, the detection method using silica gel as the desiccant has advantages, such as good durability, high accuracy, and good repeatability. With this detection method, the purpose of quality control can be easily achieved.Keywords: Famciclovir Granules; loss on drying; lactose; free water; desiccant泛昔洛韦是抗病毒类药物中的一种,主要用于带状疱疹和原发性生殖器疱的治疗[1-3]。
正文主体部分之“讨论”
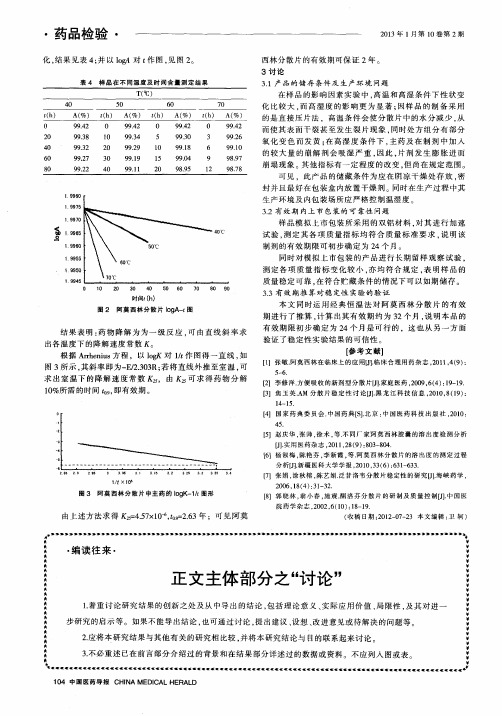
验证 了稳 定性 实 验结 果 的可信 性 。
【 参 考文 献】
【 l 1张 敏 . 阿 奠 西 林 在 临 床 上 的 应 用 咖. 临 床合 理 用药 杂 志 , 2 O l l , 4 ( 9 ) :
5 — 6 .
图3 所示 , 其斜 率 即为 一 E l 2 . 3 0 3 R; 若 将 直线 外 推至 室温 , 可 求 出室 温 下 的降 解 速 度 常 数 ,由 K 可求 得药 物 分 解 1 0 %所需 的时 间 t 即有效 期 。
1 / t× l 0
2 0 0 6 , 1 8 ( 4 ) : 3 1 — 3 2 .
图 3 阿莫西林分散片中主药的 I o g K - 1 / t 图形
[ 8 ] 郭 晓林 , 翁小 春 , 施震. 酮 洛 芬 分 散 片 的研 制及 质 量 控 制 f J ] . 中 国 医
院药学杂志 , 2 0 0 2, 6 ( 1 0 ) : 1 8 — 1 9 . ( 收 稿 日期 : 2 0 1 2 — 0 7 — 2 3 本文编辑 : 卫 轲)
【 6 】杨淑梅 , 陈艳芬 , 李新霞 , 等. 阿 莫 西 林 分 散 片 的溶 出 度 的 测 定 过 程
分析[ J 1 . 新疆医科大学学报, 2 0 1 0, 3 3 ( 6 ) : 6 3 1 — 6 3 3 . [ 7 】张娟 , 涂秋榕 , 陈艺娟. 泛昔 洛 韦 分散 片稳 定 性 的研 究 U 】 . 海峡药学 ,
3 . 2有效 期 内上 市 包装 的 可靠 性 问题 样 品模 拟 上市 包装 所 采用 的双 铝材 料 . 对 其 进行 加 速
量
试验 , 测 定其 各 项 质 量指 标 均 符 合 质 量标 准 要 求 , 说 明该 制剂 的 有效 期 限可初 步确 定 为 2 4个 月 。
利用球面对称设计法筛选泛昔洛韦分散片的优化处方

利用球面对称设计法筛选泛昔洛韦分散片的优化处方【摘要】这篇文章旨在探讨利用球面对称设计法筛选泛昔洛韦分散片优化处方的方法。
首先介绍了背景及研究目的,阐明了研究的重要性。
接着讲解了球面对称设计法的原理以及筛选分散片的步骤。
然后详细描述了泛昔洛韦分散片的制备过程,并探讨了优化处方设计的关键性。
最后展示了实验结果,验证了该方法的有效性。
结论部分总结了利用球面对称设计法筛选优化处方对泛昔洛韦分散片的意义,并展望了未来的研究方向。
这项研究为药物制剂设计领域提供了新的思路和方法,有望为相关领域的发展带来重要的贡献。
【关键词】球面对称设计法、泛昔洛韦分散片、优化处方、制备、实验结果、意义、未来展望、筛选、原理1. 引言1.1 背景介绍泛昔洛韦分散片是一种常用的药物制剂,常用于治疗病毒性感染,如带状疱疹等。
目前制备这种药物的过程存在一些挑战,如药物的稳定性、溶解度和生物利用度等问题。
为了解决这些问题,利用球面对称设计法筛选泛昔洛韦分散片的优化处方成为一种有效的途径。
通过球面对称设计法,可以针对药物分子的特性和结构进行优化设计,从而提高其药效和制备过程的效率。
利用这一方法,研究人员可以根据药物的物理化学性质和药效学特征,通过合理的实验设计和数据分析,筛选出最优的处方配方,以提高药物的稳定性、溶解度和生物利用度。
通过本研究,不仅可以优化泛昔洛韦分散片的制备工艺,提高药物的质量和疗效,还可以为相关药物的研发和生产提供重要的参考和指导。
利用球面对称设计法筛选泛昔洛韦分散片的优化处方具有重要的研究意义和应用前景。
1.2 研究目的通过利用球面对称设计法筛选泛昔洛韦分散片的优化处方,旨在寻找出最佳的药物配方,使其在分散片制备过程中具有更好的球面对称性。
通过优化处方设计,进一步提高分散片的药效和生物利用度,以实现更有效的治疗效果。
研究还旨在探究球面对称设计法在筛选药物分散片处方中的应用价值,为日后研究提供参考。
通过本研究,可以为泛昔洛韦分散片的制备工艺优化提供理论和实践基础,为相关药物研究领域的发展做出贡献。
利用球面对称设计法筛选泛昔洛韦分散片的优化处方重点

利用球面对称设计法筛选泛昔洛韦分散片的优化处方[ 07-11-12 15:27:00 ] 编辑:studa20作者:陈华土, 梁冬红, 张少春【关键词】泛昔洛韦;,,分散片;,,优化;,,球面对称设计摘要:目的:利用球面对称设计法对处方进行优化。
方法:以分散均匀性为考察指标,选择影响分散片质量的主要因素进行球面试验,进一步筛选优化处方。
结果:按优化处方制备的泛昔洛韦分散片,可在3min内完全崩解。
结论:优化处方的泛昔洛韦分散片的体外溶出度明显优于普通片剂。
关键词: 泛昔洛韦;分散片;优化;球面对称设计Optimization of the Formulae of Famciclovir Dispersible Tablet by Spherical Symmetric DesignAbstract: Objective: To optimize the formulae by Spherical Symmetric design test. Method: The formulae of Famciclovirdispersible tablet were optimized in terms of disintegrating time by Spherical Symmetric design test. Result: The optimized Famciclovir dispersible tablet disintegrated in 3min. Conclusion: The in-vitro dissolubility of the optimized dispersible tablet is better than that of common tablet.Key words: Famciclovir; Dispersibletablet; Optimization; Spherical Symmetric design泛昔洛韦具有广谱抗病毒作用,对疱疹病毒、乙肝病毒、巨细胞病毒、EB病毒等均有活性、临床上主要用于单纯性疱疹、带状疱疹、生殖器疱疹、乙型肝炎的治疗[1~3]。
HPLC法同时快速测定伐昔洛韦、泛昔洛韦和更昔洛韦含量

HPLC法同时快速测定伐昔洛韦、泛昔洛韦和更昔洛韦含量孔爱英;纪宏;韩杰;朱文凤【摘要】目的建立同时快速测定伐昔洛韦、泛昔洛书和更昔洛韦3种化合物含量的分析方法.方法采用C18色谱柱,流动相:甲醇-0.03mol/L磷酸二氢铵溶液(用磷酸调节pH值至3.0±0.1)(V∶V=35∶65);流速:1.0mL/min,柱温:35℃,检测波长为250nm,结果更昔洛韦、伐昔洛韦和泛昔洛韦浓度分别在9.88~59.28、9.48~56.88和20.08~120.48μg/mL范围内,与其峰面积呈良好线性关系,线性方程分别为:A=6.71×104C+7.91×104(R2=0.9997),A=4.89×104C+6.94×104(R2=0.999 7)和A=1.06×104C+3.82×104(R2=0.9995);加标回收率分别为99.7%(RSD为1.0%)、100.4%(RSD为1.2%)和9.3%(RSD为1.1%)(n=9);样品溶液在6h内稳定.结论建立的方法简便、准确,可同时测定核苷类抗病毒药物的含量.【期刊名称】《中国抗生素杂志》【年(卷),期】2015(040)008【总页数】4页(P607-610)【关键词】更昔洛韦;伐昔洛韦;泛昔洛韦;高效液相色谱法【作者】孔爱英;纪宏;韩杰;朱文凤【作者单位】总后卫生部药品仪器检验所,北京100166;北京市药品检验所,北京100035;北京师范大学分析测试中心,北京100875;总后卫生部药品仪器检验所,北京100166【正文语种】中文【中图分类】R978.7核苷类抗病毒药物是目前临床上治疗爱滋病、疱疹和肝炎等病毒性疾病的首选药物。
将核苷类药物制成其前药,可以提高生物利用度,也可以降低代谢速度,减少不良反应。
羧酸酯类前药包括伐昔洛韦、泛昔洛韦、更昔洛韦等。
伐昔洛韦是第一代核苷类抗病毒前药,与其原药阿昔洛韦相比,伐昔洛韦的口服生物利用度大大提高;泛昔洛韦、伐昔洛韦在临床主要用于抗疱疹类病毒;更昔洛韦尽管有很大的潜在毒性,但在抗巨细胞病毒和疱疹病毒更有优势,被用来治疗艾滋病人巨细胞病毒感染[1],伐昔洛韦、泛昔洛韦、更昔洛韦等药物是临床关注且常用药物。
利用球面对称设计法筛选泛昔洛韦分散片的优化处方

利用球面对称设计法筛选泛昔洛韦分散片的优化处方
陈华土;梁冬红;张少春
【期刊名称】《河北医学》
【年(卷),期】2006(012)007
【摘要】目的:利用球面对称设计法对处方进行优化.方法:以分散均匀性为考察指标,选择影响分散片质量的主要因素进行球面试验,进一步筛选优化处方.结果:按优化处方制备的泛昔洛韦分散片,可在3min内完全崩解.结论:优化处方的泛昔洛韦分散片的体外溶出度明显优于普通片剂.
【总页数】3页(P595-597)
【作者】陈华土;梁冬红;张少春
【作者单位】广东医学院附属医院,广东,湛江,524001;广东医学院附属医院,广东,湛江,524001;广东医学院附属医院,广东,湛江,524001
【正文语种】中文
【中图分类】R944.4
【相关文献】
1.球面对称设计筛选罗沙替丁缓释片的处方及其释放度考察 [J], 林志绣;陆洁;吴万征
2.正交试验设计法优化泛昔洛韦分散片处方的研究 [J], 陈华土;林志绣;张少春
3.正交试验设计法优化泛昔洛韦分散片处方的研究 [J], 于丽丽
4.球面对称设计法筛选青藤碱贴片中的透皮吸收促进剂 [J], 刘强;周莉玲;李锐
5.利用均匀设计筛选阿司匹林分散片处方 [J], 王卓;韩丽梅;张晓青;邓英杰;张艳华;王越
因版权原因,仅展示原文概要,查看原文内容请购买。
药物代谢稳定性筛选的研究进展

药物代谢稳定性筛选的研究进展
翁骏;吕秋军
【期刊名称】《国际药学研究杂志》
【年(卷),期】2006(033)003
【摘要】在药物发现过程中,药代动力学研究成本高、耗时长,已成为制约新药开发速度和成功的瓶颈.因此,有必要在药物发现过程的早期阶段进行代谢稳定性检测,及早淘汰代谢性质不良的化合物.随着组合化学和高通量药理活性筛选技术的发展,在药物发现早期阶段进行高通量代谢稳定性检测的需求日渐迫切,本文综述了新药筛选过程中代谢稳定性的研究进展.
【总页数】4页(P211-214)
【作者】翁骏;吕秋军
【作者单位】军事医学科学院放射与辐射医学研究所,北京,100850;军事医学科学院放射与辐射医学研究所,北京,100850
【正文语种】中文
【中图分类】R967;R969.1
【相关文献】
1.流动注射-串联质谱法快速筛选植物提取物对药物代谢酶的抑制潜性 [J], 郭宾;段俊敏;王美玲;王晓莹;陈波
2.VolSurf软件及其在药物代谢性质虚拟高通量筛选中的应用 [J], 庄笑梅;肖军海;张振清;阮金秀
3.提高蛋白质和多肽类药物代谢稳定性的研究进展 [J], 王宇新;周晓巍;党颖;黄培
堂
4.高通量药物代谢与毒性筛选平台研究进展 [J], 何小爱;刘智;程泽能
5.CYP2C19基因多态性在中草药物代谢性质筛选中的初步研究 [J], 陈旺;温纯洁;付利娟
因版权原因,仅展示原文概要,查看原文内容请购买。
泛昔洛韦治疗带状疱疹49例

泛昔洛韦治疗带状疱疹49例
姜景英;王松君
【期刊名称】《航空航天医学杂志》
【年(卷),期】2005(016)001
【摘要】自2001年以来应用泛昔洛韦治疗带状疱疹49例,均取得满意疗效,现将结果报告如下:
【总页数】1页(P28)
【作者】姜景英;王松君
【作者单位】271502,山东省东平县皮肤病防治所;150056,黑龙江省哈尔滨市第二医院
【正文语种】中文
【中图分类】R752.1+2
【相关文献】
1.糖皮质激素联合泛昔洛韦治疗带状疱疹疗效分析 [J], 马中原
2.氦氖激光治疗仪联合泛昔洛韦治疗带状疱疹老年患者的临床效果 [J], 王宇
3.泛昔洛韦联合外用重组人干扰素α-2b治疗带状疱疹的临床效果 [J], 吴利锋
4.复方倍他米松注射液联合泛昔洛韦胶囊、普瑞巴林胶囊治疗带状疱疹的临床疗效观察 [J], 陈婷婷;赖应庭;谢四荣
5.龙胆泻肝胶囊联合泛昔洛韦分散片治疗带状疱疹的效果探析 [J], 徐思思;高萌因版权原因,仅展示原文概要,查看原文内容请购买。
泛昔洛韦治疗慢性乙型肝炎的近期疗效

泛昔洛韦治疗慢性乙型肝炎的近期疗效陈新月;闵佳;李俊红;辛咏梅;汪俊韬【期刊名称】《首都医科大学学报》【年(卷),期】2002(023)002【摘要】为观察泛昔洛韦(FCV)对慢性乙型肝炎的近期治疗效果,并评估其安全性,将40例血清乙型肝炎病毒-脱氧核糖核酸(HBV-DNA)阳性的慢性乙型肝炎患者随机分成FCV治疗组(20例),一般药物(维生素C、复方益肝灵或葡醛内酯)对照组(20例),疗程均16周.定期检测血清乙型肝炎病毒标志物和肝功能.结果:疗程结束时FCV组ALT复常率为65%(13/20),治疗组明显高于对照组的35%(7/20),P<0.01.HBV-DNA定量明显下降(2个数量级)者,FCV 组为60%(12/20),高于对照组的10%(2/20), P< 0.01.另外,FCV 组有6例HBeAg 阴转,其中3例转为抗HBe 阳性,对照组无此现象(P<0.05).2组的不良反应发生率无显著性差异(P>0.05).结果提示:泛昔洛韦可明显降低血清HBV-DNA水平,促进肝功能恢复,不良反应轻微,耐受性良好.【总页数】3页(P145-147)【作者】陈新月;闵佳;李俊红;辛咏梅;汪俊韬【作者单位】北京佑安医院特需病房;北京佑安医院特需病房;北京佑安医院特需病房;北京佑安医院特需病房;北京佑安医院特需病房【正文语种】中文【中图分类】R512.6+2【相关文献】1.干扰素α、泛昔洛韦和参麦注射液联合治疗慢性乙型肝炎疗效观察 [J], 崔洪岭;胡文杰;封飞;刘景妨2.干扰素α、泛昔洛韦和参麦注射液联合治疗慢性乙型肝炎疗效观察 [J], 崔洪岭;胡文杰;封飞;刘景妨3.干扰素α、泛昔洛韦和薄芝糖肽注射液联合治疗慢性乙型肝炎疗效观察 [J], 崔洪岭;胡文杰;封飞;刘景妨4.泛昔洛韦治疗复发性生殖器疱疹的近期疗效观察 [J], 李红;伍建华;刁仕华5.泛昔洛韦治疗慢性乙型肝炎近期疗效观察 [J], 周红燕因版权原因,仅展示原文概要,查看原文内容请购买。
泛昔洛韦治疗带状疱疹50例

泛昔洛韦治疗带状疱疹50例
张群寿
【期刊名称】《华西药学杂志》
【年(卷),期】2008(0)2
【摘要】目的评价泛昔洛韦治疗带状疱疹的疗效。
方法100例带状疱疹患者随机均分为2组,治疗组口服0.25 g泛昔洛韦,tid,连用8 d;对照组口服0.2 g阿昔洛韦,每天5次,连服8 d。
结果治疗组的症状、体征、痊愈时间明显短于对照组,后遗神经痛发生率治疗组低于对照组。
结论泛昔洛韦治疗带状疱疹的疗效优于阿昔洛韦。
【总页数】1页(P243-243)
【关键词】泛昔洛韦;治疗;带状疱疹
【作者】张群寿
【作者单位】攀钢密地医院皮肤科
【正文语种】中文
【中图分类】R752.12
【相关文献】
1.Carnation22光子治疗仪联合泛昔洛韦治疗老年带状疱疹的疗效分析 [J], 田超群;陈恒君;袁睿
2.五味消毒饮加减加火针治疗对比西药用泛昔洛韦分散片治疗带状疱疹的临床效果观察 [J], 李锦亮; 钟金宝; 何伟强; 梁凤兴; 林日华
3.氦氖激光治疗仪联合泛昔洛韦治疗带状疱疹老年患者的临床效果 [J], 王宇
4.龙胆泻肝汤联合泛昔洛韦治疗带状疱疹的疗效 [J], 高鹏
因版权原因,仅展示原文概要,查看原文内容请购买。
伐昔洛韦 (Valacyclovir) 抗病毒治疗

伐昔洛韦 (Valacyclovir) 抗病毒治疗伐昔洛韦(Valacyclovir)抗病毒治疗伐昔洛韦(Valacyclovir)是一种常用的抗病毒药物,被广泛应用于治疗病毒感染性疾病。
本文将对伐昔洛韦的药理特性、临床应用以及副作用进行详细探讨,旨在帮助读者更好地理解和应用该药物。
一、药理特性伐昔洛韦是一种鸟苷类似物,其化学结构和活性主要与乙酰肼(Acyclovir)相似。
在体内,伐昔洛韦经过首次酶解转化为活性代谢物-阿昔洛韦(Acyclovir),然后通过磷酸化作用转化为更为活性的磷酸阿昔洛韦。
磷酸阿昔洛韦可与病毒DNA聚合酶竞争性结合,抑制病毒DNA的合成,从而起到抗病毒作用。
二、临床应用伐昔洛韦主要用于治疗疱疹病毒感染性疾病,包括单纯疱疹(HSV)、带状疱疹(HZV)及水痘(VZV)等。
其临床应用主要体现在以下几个方面:1. 单纯疱疹病毒感染:对于单纯疱疹病毒感染的治疗,伐昔洛韦可以缓解疱疹症状,减轻疼痛和瘙痒感,并促进病情的恢复。
对于初次感染者,常见的剂量为每天500mg,连续服用7-10天;对于复发性感染者,常见的剂量为每天500mg,连续服用3-5天。
2. 带状疱疹病毒感染:伐昔洛韦也广泛用于带状疱疹的治疗。
该药物可减轻疼痛、瘙痒感,并促进皮肤损伤的愈合。
常见的剂量为每天1000mg,分两次口服,疗程通常为7天。
3. 水痘病毒感染:对于儿童和成人的水痘感染,伐昔洛韦可缓解疱疹症状和瘙痒感,减少皮肤损伤,并预防或减轻后遗神经痛。
常见的剂量为每天3次口服,儿童为500mg/次,成人为1000mg/次,剂量和疗程依据患者的年龄和病情而定。
三、副作用虽然伐昔洛韦是一种有效的抗病毒药物,但在使用过程中也可能出现一些副作用。
常见的副作用有恶心、呕吐、腹泻、头痛、头晕以及皮疹等。
此外,极少数患者可能会出现过敏反应,表现为皮疹、瘙痒、呼吸困难等症状。
如果出现严重的过敏反应,应立即停药并就医治疗。
对于肾功能不全的患者,需要调整剂量以避免药物积累。
抗病毒药物联用问题分析

抗病毒药物联用问题分析发表时间:2017-08-03T14:55:08.043Z 来源:《心理医生》2017年13期作者:马勇[导读] 医院应加强药事质量管理工作,发挥药师在处方审核、处方点评、药学监护等合理用药管理中的作用[3],使临床用药更有效、更安全。
(四川省射洪县人民医院四川射洪 629200)【中图分类号】R97 【文献标识码】A 【文章编号】1007-8231(2017)13-0087-02 病毒为细胞内寄生的微生物,利用宿主细胞的代谢系统生成并增生复制[1]。
药品具有两重性,既能治疗疾病,又能导致疾病的发生,它与人们的生活生命紧密相关,不可缺少。
合理用药问题受到社会的广泛关注,党和政府高度重视,曾先后制定了一系列合理用药管理文件,各级医院贯彻执行在医疗卫生服务工作中,医疗质量与人们的健康水平都得到了很大提高。
为了进一步贯彻落实国家有关医药卫生政策,我院相应制度了合理用药管理制度,强化临床合理用药管理,每月开展处方点评工作,将点评结果进行通报,对于有用药问题的处方进行处理,使临床合理用药能力与医疗质量管理水平明显提升。
本文就处方点评中发现的抗病毒药物联用问题作一分析,希望有益于临床,共同关注临床合理用药问题。
1.处方实例患者就医首先在医院门诊,基础医疗首先在医院门诊,加强门诊处方用药管理尤为重要。
在门诊处方点评中发现了一些用药存在问题的处方,其中抗病毒药物联用不合理问题较为突出,处方点评专家组高度重视。
典型处方:如门诊号为20160726000717的处方,临床诊断为“扁桃腺炎、疱疹性口腔炎、哮喘”,共用9种药品,其中选用了“阿昔洛韦片、利巴韦林片、清开灵片”等3种药品;门诊处方号为20160819000468的处方,临床诊断为“结膜炎”,选择了泛昔洛韦分散片与阿昔洛韦片联合应用。
2.抗病毒药的药理作用抗病毒药在体外对单纯性疱疹病毒、水痘带状疱疹病毒、巨细胞病毒等具抑制作用,进入疱疹病毒感染的细胞后,与脱氧核苷竞争病毒胸苷激酶或细胞激酶,药物被磷酸化成活化型阿昔洛韦三磷酸酯,然后通过二种方式抑制病毒复制:(1)干扰病毒DNA多聚酶,抑制病毒的复制;(2)在DNA多聚酶作用下,与增长的DNA链结合,引起DNA链的延伸中断。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药布袋材料对其煎出率影响较小!从经济方面"耐用和环保方面考察#用自制的棉质布袋多次循环使用更为合理!同时在实际工作中由于每个病人处方稍有变化#煎药房人员应根据药味在原定条件上考虑煎煮时间的变化与否!本次实验只煎煮$次#从节约药材和发挥疗效考察应煎煮两次!但同时药液增多#患者最好每天服用%次!每个医院都有一些相对固定的处方!如果我们能对各类处方制备汤剂的条件进行规范化#那将极大地提高煎药效率和汤液质量#更好地为患者服务!参考文献&$’李彬(应用新型煎药机煎药时对加水量的实验研究&)’(天津医科大学学报#*++,#$+-$./01203(泛昔洛韦分散片稳定性的研究张娟#涂秋榕#陈艺娟-厦门星鲨制药有限公司厦门%0$+*0.摘要4目的考察泛昔洛韦分散片的稳定性!方法按药典规定的方法进行考察!结果在不同条件下泛昔洛韦的外观性状"含量"分散均匀性"溶出度及有关物质等均符合规定!结论泛昔洛韦分散片具有良好的稳定性!关键词4泛昔洛韦分散片5稳定性中图分类号463*7($$文献标识码48文章编号4$++09%70:-*++0.+%9++%$9+*泛昔洛韦-;<=>?>@A B?C#D E F.是新一代嘌呤核苷类抗病毒药物#是在喷昔洛韦-G E F.的结构基础上研制出的喷昔洛韦的前体药物!D E F具有广谱抗病毒作用#对疱疹病毒"乙型肝炎病毒"巨细胞病毒"H I病毒等均有活性!与普通片剂相比#分散片具有分散状态佳#崩解时间短#药物溶出迅速#吸收快#生物利用度高#不良反应少#服用方便等特点!将泛昔洛韦制成分散片#在药物的有效性及顺应性上都有所提高!本文着重介绍其稳定性考察及其结果!J仪器与试药J(J仪器8K?@L M N$$++高效液相色谱仪#工作站软件版本为6L B O8O+0O+$5分光光度计P Q R$3+$-北京普析通用仪器有限责任公司.5电子天平S<C N A C?T U I G*$$V-德国赛多利斯公司.J(W试药泛昔洛韦分散片-厂家4厦门星鲨制药有限公司.#批号4*++,+:$%"*++,+0+*"*++,+0+,-包薄膜衣.!W方法与结果W(J重点项目考察方法*($($外观及分散均匀性4样品的性状应为白色薄膜衣片5样品应符合中国药典*+++年版二部附录X8片剂项下对分散片分散均匀性的规定!*($(*有关物质4Y色谱条件4色谱柱4Z[\L C U?@]V S*E$1柱-*++==^,(0==.#大连依利特科学仪器有限公司5填充剂4用十烷基硅烷键合硅胶5流动相4乙腈9+(+*=A@_‘R$磷酸二氢钾-*+/1+.5流速4$(+=@_=?M R$5柱温4室温5进样量4 *+a‘5检测波长4**$M=!理论塔板数按泛昔洛韦峰计算应不低于*:++#泛昔洛韦峰与各杂质峰的分离度应符合要求!b检查方法5取本品的细粉适量#加流动相溶解#稀释#制成每$=‘含+($=K的供试品溶液和每$=‘含$(+a K的对照溶作者简介4张娟#女-$31+($+c.!中国药科大学生物制药专业!职称4助理工程师!联系电话4+:3*c0:$*%%%c$,$%液!照上述色谱条件#取对照溶液*+a‘注入液相色谱仪#调节检测灵敏度#使主成分峰高为满量程的*+d2*:d#再准确量取上述两种溶液各*+a‘分别注入色谱仪#记录色谱图至主成分峰保留时间的*(:倍#量取各杂质峰面积#供试品溶液的色谱图中各单个杂质峰的面积不得大于对照溶液主峰面积的$e*!*($(%含量测定4取本品$+片#精密称定#研细#精密称取适量-约相当于泛昔洛韦*:=K.#置:+=‘量瓶中#加流动相使溶解并稀释至刻度#精密量取$=‘#置$+=‘量瓶中#加流动相稀释至刻度#摇匀#滤过#得供试品溶液-每$=‘中含泛昔洛韦约:+a K.!另精密称取泛昔洛韦对照品约*:=K#同法操作得对照品溶液!照高效液相色谱法-中国药典*+++年版二部附录F V.试验#在%+:M=波长处测定吸收度#以外标法按峰面积计算#即得!*($(,溶出度测定4取本品#照溶出度测定法-中国药典*+++年版二部附录f E第一法.#以水1++=‘为溶剂#转速为每分钟$++转#依法操作#经%+=?M时取溶液#滤过#精密量取续滤液适量#加水稀释制成每$=‘中约含*:a K的溶液#作为供试品溶液!另取泛昔洛韦对照品适量#精密称定#加水制成每$=‘中约含*:a K的溶液#作为对照品溶液!取上述两种溶液#照分光光度法-中国药典*+++年版二部附录X F8.#在%+:M=的波长处测定吸收度5计算每片的溶出度!限度为标示量的1+d#应符合规定!W(W光照试验取泛昔洛韦分散片#批号为*++,+:$%-包衣.#置于装有日光灯的光照箱内#于光照强度为,:++2:+++@g条件下放置$+h#与第五"十天分别取样#观察片剂的外观性状#用Z G‘E法进行有关物质检查及含量测定#照分光光度法测定溶出度#并与+h的数据和图谱结果比较!结果-见表$.!_$%_S N C<?N G i<C=<>L T N?><@)A T C M<@F A@$1j A O%*++0表!强光照射对制剂的稳定性影响时间"#$性状含量"%$分散均匀性溶出度"%$有关物质&白色薄膜衣片剂’’()*符合规定’’+),&+-!.白色薄膜衣片剂’/(/)符合规定’’+.-&+)* !.白色薄膜衣片剂’’(),符合规定’’+!-&+.,结论0样品光照!&#后1与&#比较1其性状2含量及降解产物等指标均无明显变化1且检测合格34(5高温试验取泛昔洛韦分散片1批号为*&&)&.!-"包衣$1将其分置于)&6和7&6的恒温干燥箱中1分别于.2!&#取样1考察外观性状2含量2分散均匀性2有关物质及溶出度3并与&#的数据图谱结果比较3结果"见表*$3表*高温对制剂的稳定性影响温度时间"#$性状含量"%$分散均匀性溶出度"%$有关物质高湿&白色薄膜衣片剂’’+)*符合规定’’+),&+-! )&6.白色薄膜衣片剂’/+’/符合规定’’+&,&+)* !&白色薄膜衣片剂!&&+--符合规定’’+!&&+7!高温.白色薄膜衣片剂’’+7*符合规定’’+./&+)/7&6!&白色薄膜衣片剂’’+7.符合规定’’+7,&+7!结论0样品于7&6高温放置!与&#比较1降解产物无明显变化1在)&6高温放置!与&#比较1无明显变化1且各项指标均检测合格34(8高温度试验取泛昔洛韦分散片1批号为*&&)&.!-"包衣$1将其置于相对湿度的,.%2’*(.%的干燥器中1然后置于*.6恒温干燥箱中1分别于.2!&#取样1考察外观性状2含量2分散均匀性2有关物质及溶出度2片剂增重3并与&#的数据图谱结果比较3结果"见表-$3表-高湿度对制剂的稳定性影响湿度时间"天$性状增重"%$含量"%$分散均匀性溶出度"%$有关物质高温,.%高湿’*(.%&白色薄膜衣片剂9’’+)*符合规定’’+),&+-! .白色薄膜衣片剂1吸湿后有膨胀*(&’’’())符合规定!&&(*)&(.7 !&白色薄膜衣片剂1吸湿后衣膜破裂)(!,’’(/!符合规定’/(.&(.’.白色薄膜衣片剂1吸湿后有膨胀*(*!’’(!*符合规定’’(.&(.) !&白色薄膜衣片剂1吸湿后衣膜破裂.(**’’(!/符合规定’/(/*&(.7结论0样品于相对湿度为,.%2’*(.%的环境中放置!&#后1与&#比较1除片剂重量有明显增加外1其他各项指标无无明显变化34(:加速试验将样品"批号0*&&)&.-!1*&&)&7&*1 *&&)&7&)$在上市包装条件下1置于相对湿度为,.%的干燥器中1再置于)&6恒温干燥箱中1分别于&2!2*2-27月取样1考察外观性状2含量2分散均匀性2有关物质及溶出度3结果"见表)$3表)加速试验结果批号时间"月$外观含量"%$分散均匀性溶出度"%$有关物质*&&)&.-!&白色薄膜衣片’’()*符合规定’,(’.&()7!白色薄膜衣片’’(!,符合规定’,(!,&(.*白色薄膜衣片’’()-符合规定’,(..&(.!-白色薄膜衣片’’(.!符合规定’/(!/&(.)7白色薄膜衣片’’(.*符合规定’,(-/&(7-*&&)&7&*&白色薄膜衣片!&&(’/符合规定’/(’.&().!白色薄膜衣片!&!(--符合规定’/(.-&(.!*白色薄膜衣片!&&+’,符合规定’/+’/&+)’-白色薄膜衣片!&&+!.符合规定’/+-7&+),7白色薄膜衣片!&&+/符合规定’/+/,&+./*&&)&7&)&白色薄膜衣片!&!+,!符合规定’’+’&+).!白色薄膜衣片!&*+!,符合规定’’+,&+.*白色薄膜衣片!&!+))符合规定’’+*,&+.7-白色薄膜衣片!&!+-/符合规定’’+/!&+)77白色薄膜衣片!&!+*,符合规定’’+).&+7)结论0样品于温度为)&61相对湿度为,.%的环境中放置7个月后1与&#比较1泛昔洛韦含量基本不变1外观性状2分散均匀性2溶出度2有关物质检查均检查合格34(;长期试验将样品"批号0*&&)&.-!1*&&)&7&*1 *&&)&7&)$在上市包装条件下1于*.<*6下自然放置留样*)个月1分别于&2-27月取样1考察外观性状2含量2分散均匀性2有关物质及溶出度3结果"见表.$1其各项指标均检测合格3表.长期试验结果批号时间"月$外观含量"%$分散均匀性溶出度"%$有关物质*&&)&.-!&白色薄膜衣片’’()*符合规定’,+’.&+)7-白色薄膜衣片’’(*)符合规定’,+7-&+.’7白色薄膜衣片’’(.符合规定’,+7!&+.**&&)&7&*&白色薄膜衣片!&&(’/符合规定’/+’.&+).-白色薄膜衣片!&&(7!符合规定’/+,&+)77白色薄膜衣片!&!(&)符合规定’/+.-&+.-*&&)&7&)&白色薄膜衣片!&!(,!符合规定’’+’&+).-白色薄膜衣片!&&(’符合规定’’+,-&+).7白色薄膜衣片!&!(.!符合规定’’+7!&+.75小结泛昔洛韦分散片稳定性试验的影响因素考察结果表明0泛昔洛韦分散片在光照2高温2高湿的条件下在其外观性状2分散均匀性2含量2溶出度及有关物质检查中与&#相比无明显变化1各项指标均合格3加速试验和长期试验的结果进一步表明0泛昔洛韦分散片有很好的化学稳定性及物理稳定性3=*-=海峡药学*&&7年第!/卷第-期。
