用微型实验方法制备三苯甲醇
三苯甲醇

一、实验步骤及现象1 格氏试剂的制备步骤现象在三口瓶中放入0.4g镁,一粒碘,磁石;在滴液漏斗中装入2ml溴苯和7ml无水乙醚将1/3的混合液倒入溶液呈黄绿色(I2),无气泡生成开启搅拌器转动一会儿,再关闭有气泡产生继续搅拌溶液颜色逐渐变淡,最终呈无色将温度保持在32℃逐滴滴加溶液始终有汽包冒出,溶液呈微沸状态待加完溶液之后保持温度在34℃,待回流0.5h 溶液变成棕黄色从加热套中取出三口瓶让其自然冷却2 三苯甲醇的制备在滴液漏斗中装入1ml苯甲酸乙酯和2ml无水乙醚开动搅拌器滴加混合液溶液开始冒泡溶液颜色开始发生变化滴加完成后在将温度保持在34℃回流0.5h 溶液变为红色再变成黄色最终为灰绿色从加热套中取出三口瓶让其自然冷却在滴液漏斗中装入2g氯化铵和7-8ml水配成的混合溶液,并逐滴滴入三口瓶中溶液冒泡,呈绿色,混合后呈粘稠状放置一周3 水蒸气蒸馏放置一周后的溶液呈紫色安装蒸馏装置后,加热至微沸状态蒸馏有紫色的物质浮于溶液的表面一段时间后溶液呈棕黄色,在直型冷凝管中有白色的物质生成,同时再过一段时间之后,有多个黄色的球状的物质生成待直型冷凝管口的溶液出现的油状物质较少时停止蒸馏在空气中进行冷却,抽滤的粗样品。
称的出样品的质量为1.223g。
将粗产品研碎之后装入三口瓶中,向粗产品中加入8.5ml的95%乙醇,加热搅拌溶解溶液呈黄色加入活性碳溶液逐渐变为无色趁热进行过滤,放置在空气中让其自然结晶最后的看到棱状的晶体,在阳光的照射下折射出彩色的光芒待结晶完成之后进行过滤滤液仍呈黄色放置一周后称重得0.364g4 物理常数的测定取少量的晶体放到玻片上加热并记录晶体坍塌,初熔和全熔时的温度5 三苯甲醇的熔点测定数据记录熔点萎缩(℃)初熔(℃)全熔(℃)三苯甲醇1 157.8 161.3 1682 159.4 160.4 165.93 163.4 165.1二、实验步骤的图示三口瓶中放入0.4g镁,一粒碘,磁石→将1/3的混合液倒入→开启搅拌器→将温度保持在32℃逐滴滴加→待加完溶液之后保持温度在34℃,待回流0.5h→从加热套中取出三口瓶让其自然冷却→在滴液漏斗中装入1ml苯甲酸乙酯和2ml无水乙醚→开动搅拌器滴加混合液→滴加完成后在将温度保持在34℃回流0.5h→从加热套中取出三口瓶让其自然冷却→在滴液漏斗中装入2g氯化铵和7-8ml水配成的混合溶液,并逐滴滴入三口瓶中→放置一周→安装蒸馏装置→加热待直型冷凝管口的溶液出现的油状物质较少时停止蒸馏在空气中进行冷却,抽滤的粗样品→将粗产品研碎之后装入三口瓶中,向粗产品中加入8.5ml的95%乙醇,加热搅拌溶解→加入活性碳→趁热进行过滤,放置在空气中让其自然结晶→待结晶完成之后进行过滤→取少量的晶体放到玻片上加热并记录晶体坍塌,初熔和全熔时的温度三、实验结果的计算1三苯甲醇的产率以粗产品为参考,实验的产率=0.364∕1.223×100%=29.76%2 三苯甲醇的熔点熔程=(168-161.3+165.9-160.4+165.1-163.4)/3=4.63℃熔点在161.7℃到166.3℃之间四、讨论1 红色的中间产物应为。
有机化学实验三苯甲醇的制备

有机化学实验三苯甲醇的制备中山大学实验报告 2010-10-29学院: 专业: 学号: 姓名:实验题目:三苯甲醇一(实验目的:1,学习用格式试剂反应制备醇2,学习无水反应~水蒸气蒸馏~有机溶剂重结晶操作二(反应原理及反应方程式:概述:格式试剂与羰基化合物加成生成醇实验室制备醇的重要途径之一利用羰基化合物,醛>酮>酯,与格式试剂反应生成醇。
利用格式试剂与甲醛~环氧乙烷或者是卤代醇的反应制备一级醇,与醛或者甲酸酯,2倍格氏试剂,的反应制备二级醇,与酮~酯~酰氯~不饱和酸酯或者酸酐反应制备三级醇反应制备三级醇。
本实验采用格氏试剂与苯甲酸甲酯制备三苯甲醇~而格氏试剂则用镁和溴苯作为反应原料在无水乙醚的溶剂中~和一小粒碘来活化镁。
来反应制备格氏试剂。
1, 格氏试剂的制备格氏试剂很活泼可以与水和含有酸性氢的有机化合物,ROH,RSH,RCOH,RNHH,RCONHH,RCCH,RSOH,反应也可以和 2223氧发生反应。
反应式如下RMH+HOR-H+XMOH g2gRMH+[O] ROMXR—H+XMOH ggg反应之前需要通入氮气一赶走反应瓶中的空气。
乙醚则为反应溶剂严格不准见水~挥发性大~蒸气可赶走瓶中的空气~但是在需要较高温度下反应时也可以用四氢呋喃等。
镁则应用细小的镁屑或者是镁粉~事先可在60到80摄氏度下干燥30分钟~再经真空干燥保存于密闭的玻璃容器中。
必要时可用碘活化镁~将理论计算量的镁喝少量的碘放进反应瓶中~小火加热至瓶中充满碘蒸气~待冷却后再加入其它的试剂进行反应。
在制备格氏试剂的过程中注意滴加卤代烷的方法。
之前先加入少量的卤代烷乙醚溶液和镁作用~待反应引发之后~再将其他剩余的卤代烷缓慢的滴入~使乙醚保持微沸腾~若是一次加入太多的卤代烷反应剧烈且不易控制~也会有自身的耦合反应。
必要时可用冷水冷却~而对于引发反应很难可以适当的加热2, 三苯甲醇的制备格氏试剂与醛酮等形成的加成产物进行酸性水解的时候镁变为易溶于水的镁盐便于乙醚与水分层。
三苯甲醇的制备课件

三苯甲醇的制备
三苯甲醇的制备
Hale Waihona Puke 三苯甲醇的制备三苯甲醇的制备
三苯甲醇的制备
三苯甲醇的制备
三苯甲醇的制备
15
三苯甲醇的制备
(1)将制备好的苯基溴化镁乙醚溶液置于冰浴中,在搅拌下 滴加1.9 mL (0.013mol)的苯甲酸乙酯和无水乙醚的混合液。滴 加完毕后,继续反应5min,然后将反应混合物在水浴加热回流 0.5小时。(反应物明显分为两层) (2)慢慢从冷凝管上口加入配好的饱和的氯化铵水溶液,改 成蒸馏装置,蒸出乙醚。然后进行水蒸气蒸馏,蒸出溴苯及副 产物。 (3)瓶中的剩余物冷却,过滤收集。再用80%的乙醇重结晶。
三苯甲醇的制备
三苯甲醇的制备
三苯甲醇的制备
此课件下载可自行编辑修改,供参考! 感谢您的支持,我们努力做得更好!
三苯甲醇的制备
三苯甲醇的制备

蒸毕后冷至室温,加入10ml石油醚,析 出晶体,抽滤收集
3、三苯甲醇的分离提纯
95%乙醇重结晶,活性炭脱色 热溶液 热过滤
溶液
冷却 溶液中析出固体 抽滤、洗涤 产品
七、注意事项
1、加氯化铵溶液之前的步骤中所用仪器和药品必须严格干 燥处理。否则将不能反应或不能得到目标化合物。 2、镁条长期放置,表面常有一层氧化膜,可用细砂纸将其 擦亮,剪成小段。 3、引发反应时,碘的量不可多,否则碘颜色无法消失,得
,此实验很可能已失败。
八、思考题
1、在对格氏试剂过夜保存时须采取什么措施?在进行格氏反 应时是否需要特殊保护? 2、试述碘在本反应中的作用。 3、在制备苯基溴化镁时,为什么溴苯不宜加入过快?
4、在制备三苯甲醇时,加入饱和氯化铵的目的是什么?
5、本反应可能发生什么副反应? 6、反应结束,可用那些方法除去未反应完的溴苯及副产物?
银白色 固体
溶液呈 紫色 无色液 体 无色澄 清液体, 有芳香 气味
苯甲酸乙酯
150. 7
1.05
-34.6
212.6
微溶于热水,溶于乙醇、乙 醚、石油醚等
六、实验步骤
1、苯基格式试剂的制备
100mL三口烧瓶 搭建装置 0.4g (0.016mol) 镁 屑,5mL无水乙醚 1粒 碘 混合均匀 滴加剩余混合液,控制滴加 速度,保持微回流 滴加完毕得浊液 浴温45~50℃搅拌回流30min, 至镁屑作用完全 冷却
《有机化学实验》
三苯甲醇的制备
醇的制法:
1、羰基还原(醛、酮、羧酸和羧酸酯) 2、烯烃的硼氢化-还原水解
3、Grignard反应
一、实验目的
• 1.学习格氏试剂法制备三苯甲醇的原理方法; • 2.掌握Grignard试剂的制备操作及Grignard反应操作;
实验5:三苯甲醇的制备及结构表征

实验五 三苯甲醇的制备及结构表征一、实验目的1. 了解格氏试剂的制备、应用和进行格氏反应的条件。
2. 进一步掌握搅拌、回流、萃取蒸馏(包括低沸点物蒸馏)等操作。
二、反应原理三苯甲醇可通过格氏试剂与苯甲酸乙酯与苯基溴化镁的反应制备: Br Mg MgBr+ MgBr COC 2H 5O OMgBrOC 2H5O C 2H 5OMgBr+C C +OMgBr OMgBrC +C42OHC三、实验装置图接氯化钙干燥管四、试剂及仪器仪器:半微量有机合成玻璃仪器;电动搅拌器;旋转蒸发仪;数显式熔点测定仪;红外光谱仪试剂:镁屑,溴苯,苯甲酸乙酯,无水乙醚,氯化铵,乙醇五、操作步骤1. 苯基溴化镁的制备如图安装好反应装置,瓶内放置0.8g镁屑及一小粒碘片,在滴液漏斗中混合5g溴苯及13mL无水乙醚。
先将三分之一的混合液滴入烧瓶中,反应开始后开动搅拌,缓缓滴放其余的溴苯醚溶液,滴加速度保持溶液呈微沸状态。
加毕后,继续回流1.5h。
2. 三苯甲醇的制备将已制好的苯基溴化镁试剂置于冷水浴中,在搅拌下由滴液漏斗滴加1.9mL苯甲酸乙酯和5mL无水乙醚混合液,控制滴加速度保持反应平稳地进行。
滴加完毕后,继续回流0.5h。
将反应液改为冰水浴冷却,在搅拌下由滴液漏斗滴加由3.8g氯化铵配成的饱和溶液,分解加成产物。
在旋转蒸发仪上蒸去乙醚,再将残留物进行水蒸汽蒸馏。
残留物冷却后抽滤,得到三苯甲醇粗产品。
3. 重结晶法提纯粗产物用95%进行重结晶,得三苯甲醇产品。
4. 产品表征(1)测定产品熔点。
(2)测定产品的红外光谱图。
*废液和固体废弃物倒入指定容器中。
六、注意事项1. 所用仪器、药品必须经过严格的干燥处理,否则反应很难进行,并可使生成的格氏试剂分解。
2. 卤代烃与镁的作用很难发生通常温热或用一小粒碘作催化剂,以促使反应开始。
3. 滴加的速度太快,反应过于激烈,不易控制,并会增加副产物的生成。
4. 为了使反应易于发生,故搅拌应在反应开始以后进行,若5min后反应仍不开始,可用温水浴或直接加入一小粒碘促使反应开始。
有机化学实验实验二十三 三苯甲醇的制备

熔点 (℃) 164.2 沸点 (℃) 380 折光率 20 (n D )
d
1.509 1.199
溶 解 度 水 乙醇 乙醚 不溶 易溶 易溶 溶 ∞ ∞ ∞
比重 名 称 分子量 颜色形态 20 结构式或分子式 (d 4 )
(C6H5)3COH (C6H5)2CO C3CH2OH (C2H5)2O
C6H5MgBr,Et2O (C6H5)2C O
+
C6H5CO2C2H5
C2H5OMgBr
C6H5MgBr (C6H5)3COMgBr NH4Cl,H2O (C6H5)3COH
方法二:
主要的副反应:
MgBr
C6H5Br
三、物理常数
Name
C6H5COOEt (C6H5)3COH
M
150 260
b.p.或m.p.(℃)
260.34 无色晶体 1.199 182.21 无色晶体 1.0847
(α )48.1 305.9 1.6191 分解 (β )26 78.5 1.3611 ∞
46.07 无色液体 0.7893 -117.3
74.12 无色液体 0.71378 -116.2 34.51 1.3526 微溶 ∞
四、实验装置
二颈瓶要使 用平底烧瓶, 也可使用锥 形瓶加二口
电磁加热搅拌器
管
五、注意事项
1、反应不可过剧,否则乙醚会从冷凝管上口冲出。
2、乙醚的蒸馏一定要用热水浴,实验室不能有明火。
六、成功关键
1、仪器、药品要绝对干燥,否则格氏试剂水解。
2、加料要迅速,防止药品吸潮。
七、课后习题
1、本实验溴苯加入太快或一次性加入,会发生哪些
三苯甲醇的制备
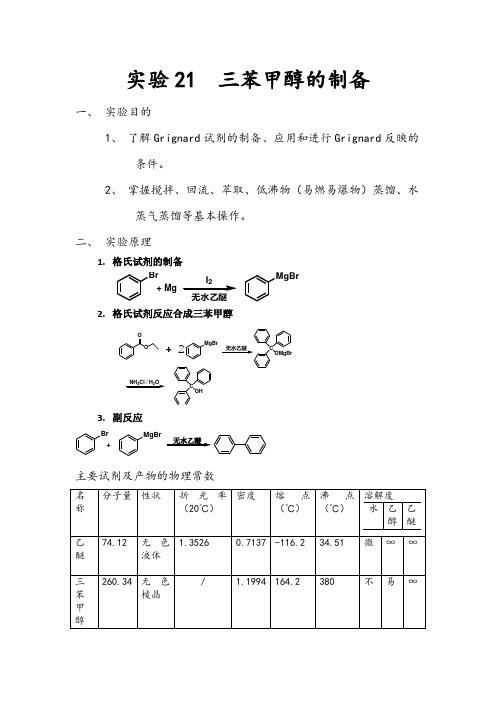
熔点:
48.5
305.4
不
溶
溶
联苯
154.21
无色片状晶体
1.5888
0.8660
71
255.9
不
溶
溶
三、实验内容
1、苯基溴化镁制备
2、 在100mL三颈烧瓶上分别装上恒压滴液漏斗、球形冷凝管(带无水CaCl2gan干燥管),放进磁石 向瓶中加入0.5g(0.02moL)剪碎的镁、一小粒碘 恒压漏斗中加入2.1mL(0.02mol)溴苯和15mL无水乙醚混合均匀 滴入约1-2mL混合液(浸没镁条),(数分钟后见溶液微沸,碘颜色消失) 开动搅拌器,继续滴加其余混合液(控制滴加速度),维持微沸状态(如果发现反应液粘稠,则补加适量乙醚) 滴完后,温水浴回流至镁条反应完全(约30min)
密度
熔点(℃)
沸点(℃)
溶解度
水
乙醇
乙醚
乙醚
74.12
无色液体
1.3526
0.7137
-116.2
34.51
微
∞
∞
三苯甲醇
260.34
无色棱晶
/
1.1994
164.2
380
不
易
∞
溴苯
157.02
无色液体
1.5597
1.4950
-30.82
156
不
易
易
二苯甲酮
182.22
白色至淡黄色结晶
1.6077
1.1146
4、引发反应时,所用碘量不能太大,以1/3粒大小为宜
5、制备格氏试剂时,溴苯和乙醚混合液滴加速度不能太快
6、所制备的格氏试剂是混浊有色液体,若为澄清可能瓶中进水没制好格氏试剂
实验七 三苯甲醇制备及其性质

酯层
(苯甲酸乙酯,水,少量乙醇、乙醚)
水层
(水,无机盐,苯甲酸乙酯) 加25ml乙醚萃取
合并有机液
1)加无水氯化钙,干燥除水 2)水浴蒸除乙醚
醚层
水层
3)减压蒸馏,10mmHg下收集 75~80℃馏分
苯甲酸乙酯
2012-12-21
福州大学 分子设计与合成研究中心
三苯甲醇的制备
反应混合物
1)加氯化铵饱和溶液至固体完全溶解,使三苯甲醇充分游离 2)水浴蒸除乙醚 3)水蒸气蒸馏,除苯甲酸乙酯、乙醚、联苯、溴苯、三苯甲醇
2012-12-21
福州大学 分子设计与合成研究中心
五、操作规程
制备苯甲酸乙酯
2012-12-21
福州大学 分子设计与合成研究中心
2012-12-21
福州大学 分子设计与合成研究中心
制备三苯甲醇
2012-12-21
福州大学 分子设计与合成研究中心
2012-12-21
福州大学 分子设计与合成研究中心
2012-12-21
分子设计与合成研究中心
+
0.1mol
EtOH
H2SO4
COOEt
0.4mol(过量)
Br
+
0.091mol
Mg
0.091mol
(CH3 CH2)2O
MgBr
O MgBr
+
0.045mol
C
OEt
(CH3 CH2)2O OEt C OMgBr
2012-12-21
福州大学 分子设计与合成研究中心
MgBr
2012-12-21
福州大学 分子设计与合成研究中心
12、根据道尔顿分压定律:整个体系的蒸气压力等于各
化学实验报告三苯甲醇的合成

三苯甲醇的合成实验目的和要求一、了解无水条件下的实验操作要求;1、掌握无水乙醚制备方法;2、3、了解Grignard反应;4、掌握水蒸气蒸馏操作;5、熟练掌握混合溶剂重结晶及熔点测定。
实验内容和原理二、结构复实验中,,称为RMgXGrignard试剂。
卤代烷在无水乙醚中和金属镁作用后生成的烷基卤化镁试剂来制备。
杂的醇通常由Grignard ROH(C)252ORX + Mg + 2(C)HMg225X)OH(C225X=Cl,Br,I芳香族氯化物和氯乙烯类型的化合物,Grignard试剂实际是烷基卤化镁与二烷基镁和卤化镁的混合物。
试剂。
但如果改用碱性比乙醚稍强,沸点较高的四氢在上述无水乙醚为溶剂的条件下,不易生成Grignard Grignard试剂,并且操作比较安全。
呋喃(沸点66℃)作溶剂,它们也能生成的条件下进行。
微量水的存在,不但会阻碍卤代烷和镁之间COGrignard反应必须在无水、无氧和无2试剂而影响产率。
因此,反应时最好用氮气赶走反应瓶中的空气。
一般在乙Grignard的反应,同时会破坏醚作溶剂时,由于乙醚的挥发性大,也可以借此赶走反应瓶中的空气。
反应中,有热量放出,所以反应液滴加速度不宜过快。
必要时反应瓶需要用冷水冷此外,在Grignard 却。
试剂与醛酮等形成的加成物,在酸性条件下可以进行水解反应。
如通常用稀盐酸或稀硫酸使Grignard产生的碱式卤化镁转变成易溶于水的镁盐,以便于乙醚溶液和水溶液分层。
由于水解时放热,因此要在冷却下进行。
对遇酸极易脱水的醇或易发生卤代反应的醇,最好用饱和氯化铵溶液进行水解。
反应式如下:ONHCl,H24OHOMgBr苯甲酸甲酯与苯基溴化镁的反应:OMCBrOOCHC+3OMgBr自动脱去ether OOMgBrMgBr副反应:Grignard试剂是一个强亲核试剂,除了与羰基化合物加成外,Grignard试剂中的烃基负离子还可以与CO、O等加成,能被活泼氢分解。
三苯甲醇的制备

Guangzhou UniversitySchool of Chemistry & Chemical Engineering广州大学化学化工学院实验报告专用日期12.18 气温20℃基础合成实验报告姓名学号班级指导老师成绩实验题目三苯甲醇的制备一、实验目的1. 学习和掌握叔醇的制备原理和方法;2. 进一步巩固Grignard试剂的制备、应用和进行Grignard 反应的条件;3. 掌握无水反应、回流、萃取、蒸馏(包括低沸点物蒸馏)、重结晶等操作。
二、实验原理三苯甲醇可以通过Grignard反应,用苯甲酸乙酯与苯基溴化镁反应而制取:主反应:副反应:格氏试剂很活泼(C-Mg 极性很强),遇含活泼氢的物质(如H2O、ROH)即被分解,也可与O2、CO2反应反应条件反应需在无水、无氧条件下进行;进行格氏反应的试剂要经过充分纯化,整个反应过程保持干燥极为重要,即使只有痕迹量的水存在也可抑制反应的进行,而发生反应试剂一生成就被分解成烃和碱性卤化镁。
研究工作中通常采用在惰性气体(如氮气、氦气)下反应,可防止氧气和二氧化碳与格氏试剂反应。
如果用乙醚作溶剂,由于乙醚具有很高的蒸气压,这样可以排除反应瓶中一部分空气,使反应顺利进行。
影响反应的主要因素:1.用于格氏反应的有机卤素化合物一般,碘代烃与金属镁作用最快,氯代烃最慢,而最常用的是溴代烃,因为其价格不像碘代烃那样昂贵,并且能与镁顺利进行反应。
碘化物虽然容易参加反应,但生成烃类副产物的速度也最快,其产率通常比用相应的溴化物或氯化物要差。
当然,使用溴苯制格氏试剂也存在生成联苯副产物的反应,而脂肪族溴化物比芳香溴化物更易反应。
在制备格氏试剂过程中,卤化物和镁之间引发反应是困难的,尤其是氯化物,通常是在反应中加入少量碘来引发反应,由于有少量卤化物转化为碘化物,故使反应变得更易进行。
镁有机化合物(格氏试剂)的产率一般为80~99%。
另外,格氏试剂与羰基进行加成时,如果羰基上有较大的两个基团,可因空间阻碍而使反应不能进行。
三苯甲醇的制备

三苯甲醇的制备注意:① 实验前一天,烘干仪器。
烘干仪器包括:100mL 三颈圆底烧瓶,恒压滴液漏斗(活塞取下,塑料不烘),空心塞(14# 2个;19# 1个),量筒(10mL ,25mL ),锥形瓶(19# 50mL ),干燥管,接头(14塞19口)放于600mL 烧杯中,以及球形冷凝管;【烧杯和冷凝管上贴标签】②本实验为实验期中考试,请大家提前做好预习,注意实验操作等。
[目标] 通过对高活性的金属有机试剂的制备让学生了解无水操作的技能,并掌握金属有机试剂的应用和反应的条件;复习回流、萃取、重结晶等基本实验操作;学习并掌握低沸点易燃液体的蒸馏技术和要领。
[重点] 掌握无水操作的技术;掌握低沸点易燃液体的蒸馏技术和要领。
[难点] 活泼金属有机试剂的应用和反应的条件【实验目的】了解格氏试剂的制备、应用和进行格氏反应的条件。
掌握搅拌、回流、重结晶、萃取等基本实验技能低沸点易燃液体的蒸馏技术和要领。
【实验原理】格式试剂是有机合成中应用最广泛的金属有机试剂。
其化学性质十分活泼,可以与醛、酮、酯、酸酐、酰卤、腈等多种化合物发生亲核加成反应,常用于制备醇、醛、酮、羧酸及各种烃类。
三苯甲醇是一种带有相同基团的第三醇,可以通过苯基溴化镁格式试剂和二苯甲酮或苯甲酸乙酯反应制备得到,本实验采用二苯甲酮和苯基溴化镁的反应制备。
Br I 2MgBr+ Mg无水乙醚MgBrOC OMgBr无水乙醚+COMgBrCOHNH 4Cl / H 2O副反应:MgBrBr无水乙醚+[演示] 【实验装置图】图1 反应装置 图2蒸馏装置 图3 重结晶装置【实验所用试剂及性质】试剂 分子量 沸点 (熔点 o C)比重 (g / cm 3)溴苯 157.01 156 1.49 镁条 24.30 651 1.74 碘 253.81 二苯酮 182.22 49~51 苯甲酸乙酯150.18 212 1.05 乙醚 74.12 34.6 0.7 乙醇 46.06 78 0.78 石油醚 60~90 氯化铵53.49340 (dec.)1.52【实验所用仪器及设备】100 mL 三颈圆底烧瓶,恒压漏斗,回流冷凝管,干燥管,圆底烧瓶,蒸馏头,直型冷凝管,尾接管,锥形瓶,温度计,分液漏斗,抽滤装置磁力搅拌器,搅拌子,量筒,电吹风【实验步骤】如图1所示,在100 mL三颈瓶上分别装置回流冷凝管和恒压滴液漏斗[1],在冷凝管的上口装置氯化钙干燥管[2]。
实验25 grignard反应合成三苯甲醇

实验目的
1.学习格式试剂制备三苯甲醇的原理方法
2.掌握无水条件下实验操作要求和无水乙醚的制备
3.掌握水蒸气蒸馏的操作方法
实验原理
反应方程式如下
反应中主要运用了格氏试剂的特殊化学性质,它的与金属相连的碳原子具有显著的亲核性,可发生许多与此相关的反应。
实验装置
三苯甲醇会成装置
水蒸气蒸馏装置
三苯甲醇
分子式:C19H16O;(C6H5)3COH
分子量:260.33
性质:片状晶体。
熔点164.2℃;
沸点380℃。
相对密度1.199。
折光率:1.1994
溶解性:不溶于水和石油醚,溶于乙醇、乙醚、丙酮、苯,溶于浓硫酸显黄色。
操作流程
实验结果
得到粗产物,未干燥,目测量较小。干燥后,称得产物质量是0.038g,产率为
4.用混合溶剂重结晶时,何时加入活性炭脱色?能否加入大量的不良溶剂使反应物全部析出?抽滤后的结晶应该用什么溶剂洗涤?
答:应该在完全溶解后加入活性炭脱色,这样可以保证溶解的完全性,缩短反应时间;
不能,这样做既不能形成良好的晶形,又造成了试剂与产物的浪费;
应该用乙醇洗涤,这样既能洗去有机物,又不会溶解过多产物。
答:这样做容易使溴苯发生耦合,产生副产物R-R。这样,生成的格氏试剂就少了。
3.如苯甲酸乙酯和乙醚中含有乙醇,对反应有何影响?
答:我么知道-OH也是很强的亲核基团,若混有乙醇,—OH可能取代-OC2H5,参与反应,使二苯酮难以生成,降低产率与速率。而乙醚的高蒸汽压可以排除反应中的大部分空气,混入乙醇可能减弱这种作用。
0.038/1.81*100%=2.10%
实验体会
三苯甲醇的制备

三苯甲醇的制备一、 实验目的1.了解格氏试剂的制备、应用和格氏反应的条件。
2.掌握制备三苯甲醇的原理和方法。
3.掌握搅拌、回流、萃取、蒸馏等基本操作。
二、 实验原理1. 格氏试剂的制备BrMgBr + Mg 2. 格氏试剂反应合成三苯甲醇 MgBr O OC OMgBr +C OH NH 4Cl / H 2O23. 副反应 MgBr Br无水乙醚+三、 试剂0.75g (0.032mol )镁屑,5g (3.5ml ,0.032mol )溴苯(新蒸),2g (1.9ml ,0.013mol )苯甲酸乙酯,无水乙醚,4g 氯化铵,乙醇。
四、物理参数1、三苯甲醇:英文名称:Triphenylmethanol, Triphenylcarbinol, Trityl alcohol Cas 号:【76-84-6】MDL 号:--MFCD00004445Beilstein 号:1460837 EINECS: --200-988-5分子式:C19H16O;(C6H5)3COH 结构式:分子量:260.33性质:片状晶体。
熔点164.2℃;沸点380℃。
相对密度1.199。
折光率:1.1994溶解性:不溶于水和石油醚,溶于乙醇、乙醚、丙酮、苯,溶于浓硫酸显黄色。
化学性质:羟基很活泼,与干燥氯化氢在乙醚中生成三苯氯甲烷。
与一级醇作用成醚。
用锌和乙酸还原得三苯甲烷。
由三苯氯甲烷水解,或溴化苯基镁(格利雅试剂)与二苯甲酮(或苯甲酸乙酯)制备。
用途:有机合成中间体。
市场价:65000元/吨顺强生物科技有限公司阿里巴巴-化工2012/3/14。
2、溴苯:中文名:溴苯外文名: bromobenzene别名:一溴代苯分子式: C6H5Br 结构式:相对分子质量: 157.02熔点(℃):—30.7沸点(℃):156.2相对蒸气密度(空气=1):5.41外观与性状:无色油状液体,具有苯的气味。
溶解性:不溶于水,溶于甲醇、乙醚、丙酮、苯、四氯化碳等多数有机溶剂。
三苯甲醇的制备

三苯甲醇的制备三苯甲醇的制备⼀、实验⽬的:1. 掌握制备三苯甲醇的原理和⽅法;2. 熟悉恒压漏⽃及磁⼒加热搅拌器的使⽤;3. 掌握⽔蒸⽓蒸馏装置的安装和使⽤以及其注意事项。
⼆、实验原理醇的制备:以提问的形式问学⽣常⽤的醇的制备⽅法有哪些?然后总结:(1)烯烃的⽔合(2)醛酮的还原(3)卤代烃的⽔解(4)⽤格⽒试剂我们今天就是⽤的格⽒试剂的⽅法,讲到格⽒试剂的制备,对反应原料进⾏选择(主要是看卤素,卤素的反应活性顺序:碘>溴>氯,但是碘的格⽒试剂价格较为昂贵,氯的反应活性太差,反应太慢。
因此选择溴的格⽒试剂),反应条件⽆⽔,⽤⽆⽔⼄醚或四氢呋喃作溶剂。
格⽒试剂的性质:(1)与羰基反应,(格⽒试剂有极性,烷基带负电荷,镁带正电荷,该反应具有亲核反应的⼀些特点)(2)与⼆氧化碳反应(3)与环氧⼄烷反应(考虑正电荷的稳定性)(4)与腈等反应然后联系到本实验,与⼆苯甲酮反应,就是亲核羰基反应。
写出反应⽅程式,说明采⽤的是哪种⽅法,与另⼀种⽅法的差别,我们⽤⽅法⼆,不⽤去制备⼆苯酮,⽤现成的。
格⽒试剂的制备要提到格⽒试剂易与⼆氧化碳、氧、卤代烃等耦合,有卤代烃后,卤代烃的耦合为主要副反应,格⽒试剂因此要控制温度、溴苯的滴加速度、充分搅拌降低溶液浓度(⼤量存在的⼄醚蒸汽可以排出反应体系中的⼤量空⽓减少对反应的影响,格⽒试剂的制备反应是⼀个放热反应,因此反应开始后为了控制反应速度,不要加热,甚⾄⽤冷⽔浴;开始如果反应较长时间没开始,就加⼊少量碘⽚,并⽤⼿或直接略微加热,开始反应⿎泡后就停⽌加热,滴加不能太快,否则副产物(以联苯为主)多。
)Br MgBrMg格⽒试剂反应合成三苯甲醇格⽒试剂与⼆苯酮反应,必须先⽤⽆⽔⼄醚将固体在恒压漏⽃⾥⾯混合,尽量溶解完,然后在冰⽔浴条件下滴加,控制滴加速度,这⼀步也是放热反应。
(加⼊氯化铵饱和溶液⽔解,相当于酸性⽔解,⼜不⾄于酸度太⼤使⼄醚也⽔解了)C O MgBrCOMgBrCOH提纯先⽤⽔浴的⽅式除去多余⼄醚,然后⽤⽔蒸⽓蒸馏的⽅式除去联苯、溴苯等副产物。
化学实验报告三苯甲醇的合成

三苯甲醇的合成实验目的和要求一、了解无水条件下的实验操作要求;1、掌握无水乙醚制备方法;2、3、了解Grignard反应;4、掌握水蒸气蒸馏操作;5、熟练掌握混合溶剂重结晶及熔点测定。
实验内容和原理二、结构复实验中,,称为RMgXGrignard试剂。
卤代烷在无水乙醚中和金属镁作用后生成的烷基卤化镁试剂来制备。
杂的醇通常由Grignard ROH(C)252ORX + Mg + 2(C)HMg225X)OH(C225X=Cl,Br,I芳香族氯化物和氯乙烯类型的化合物,Grignard试剂实际是烷基卤化镁与二烷基镁和卤化镁的混合物。
试剂。
但如果改用碱性比乙醚稍强,沸点较高的四氢在上述无水乙醚为溶剂的条件下,不易生成Grignard Grignard试剂,并且操作比较安全。
呋喃(沸点66℃)作溶剂,它们也能生成的条件下进行。
微量水的存在,不但会阻碍卤代烷和镁之间COGrignard反应必须在无水、无氧和无2试剂而影响产率。
因此,反应时最好用氮气赶走反应瓶中的空气。
一般在乙Grignard的反应,同时会破坏醚作溶剂时,由于乙醚的挥发性大,也可以借此赶走反应瓶中的空气。
反应中,有热量放出,所以反应液滴加速度不宜过快。
必要时反应瓶需要用冷水冷此外,在Grignard 却。
试剂与醛酮等形成的加成物,在酸性条件下可以进行水解反应。
如通常用稀盐酸或稀硫酸使Grignard产生的碱式卤化镁转变成易溶于水的镁盐,以便于乙醚溶液和水溶液分层。
由于水解时放热,因此要在冷却下进行。
对遇酸极易脱水的醇或易发生卤代反应的醇,最好用饱和氯化铵溶液进行水解。
反应式如下:ONHCl,H24OHOMgBr苯甲酸甲酯与苯基溴化镁的反应:OMCBrOOCHC+3OMgBr自动脱去ether OOMgBrMgBr副反应:Grignard试剂是一个强亲核试剂,除了与羰基化合物加成外,Grignard试剂中的烃基负离子还可以与CO、O等加成,能被活泼氢分解。
三苯甲醇制备

有机化学实验报告实验项目:三苯甲醇制备实验日期:2012年3月13日一.实验目的1:了解Grignard反应合成法制备各种结构复杂醇反应原理。
2:掌握搅拌,回流,重结晶等操作。
二.实验原理1:利用Grignard反应合成法制备各种结构复杂醇的重要方法。
卤代烷和卤代芳烃与金属镁在无水乙醚中反应生成烃基卤化镁,称为Grignard试剂。
碳-金属键是激化的,带有部分负电荷的碳具有显著的亲电性质,在增长碳链的方法中重要用途,其最重要的性质与醛、酮、酸的衍生物、环氧化合物等发生亲核加成,生成相应的醇、酸和酮等化合物。
2.反应式C6H5B r + Mg(无水乙醚)——>C6H5MgB r2C6H5MgBr + C9H10O2(无水乙醚)— C19H15OMgBrC19H15OMgBr + NH4Cl (H2O)——>C19H16O副反应: C6H5MgB r + C6H5B r ——>MgBr2 +C12H10三.试剂0.75g(0.032mol)镁屑,5g(3.5ml,0.032mol)溴苯(新蒸),2g(1.9ml,0.013mol)苯甲酸乙酯,无水乙醚,4g氯化铵,乙醇四.主要试剂及产物物理常数1.名称:溴苯 CAS号:108-86-1 分子式:C6H5Br分子量:157 熔点:- 30.7 沸点:156.2相对密度:1.48 折射率: 价格:6500元/吨供应商:上海佳美精细化工有限公司。
用途:农药原料、医药原料、用作压敏和热敏的染料的原料。
性质:不溶于水,溶于甲醇、乙醚、丙酮、苯、四氯化碳等多数有机溶剂2.名称:镁屑CAS号:7439-93-4分子式:Mg分子量:24.3熔点:651沸点:1107相对密度:1.73折射率: ------ 价格:1.00元/250g 供应商:广州易目化工有限公司。
用途:还原剂、脱氧剂、脱硫剂、格林试剂。
性质:银白色金属,具有延展性、有好的热消散性。
有机化学实验三苯甲醇的制备

有机化学实验三苯甲醇的制备中山大学实验报告 2010-10-29学院: 专业: 学号: 姓名:实验题目:三苯甲醇一(实验目的:1,学习用格式试剂反应制备醇2,学习无水反应~水蒸气蒸馏~有机溶剂重结晶操作二(反应原理及反应方程式:概述:格式试剂与羰基化合物加成生成醇实验室制备醇的重要途径之一利用羰基化合物,醛>酮>酯,与格式试剂反应生成醇。
利用格式试剂与甲醛~环氧乙烷或者是卤代醇的反应制备一级醇,与醛或者甲酸酯,2倍格氏试剂,的反应制备二级醇,与酮~酯~酰氯~不饱和酸酯或者酸酐反应制备三级醇反应制备三级醇。
本实验采用格氏试剂与苯甲酸甲酯制备三苯甲醇~而格氏试剂则用镁和溴苯作为反应原料在无水乙醚的溶剂中~和一小粒碘来活化镁。
来反应制备格氏试剂。
1, 格氏试剂的制备格氏试剂很活泼可以与水和含有酸性氢的有机化合物,ROH,RSH,RCOH,RNHH,RCONHH,RCCH,RSOH,反应也可以和 2223氧发生反应。
反应式如下RMH+HOR-H+XMOH g2gRMH+[O] ROMXR—H+XMOH ggg反应之前需要通入氮气一赶走反应瓶中的空气。
乙醚则为反应溶剂严格不准见水~挥发性大~蒸气可赶走瓶中的空气~但是在需要较高温度下反应时也可以用四氢呋喃等。
镁则应用细小的镁屑或者是镁粉~事先可在60到80摄氏度下干燥30分钟~再经真空干燥保存于密闭的玻璃容器中。
必要时可用碘活化镁~将理论计算量的镁喝少量的碘放进反应瓶中~小火加热至瓶中充满碘蒸气~待冷却后再加入其它的试剂进行反应。
在制备格氏试剂的过程中注意滴加卤代烷的方法。
之前先加入少量的卤代烷乙醚溶液和镁作用~待反应引发之后~再将其他剩余的卤代烷缓慢的滴入~使乙醚保持微沸腾~若是一次加入太多的卤代烷反应剧烈且不易控制~也会有自身的耦合反应。
必要时可用冷水冷却~而对于引发反应很难可以适当的加热2, 三苯甲醇的制备格氏试剂与醛酮等形成的加成产物进行酸性水解的时候镁变为易溶于水的镁盐便于乙醚与水分层。
三本甲醇的制备

三本甲醇的制备甲醇,又称甲醇酒精,是一种无色、易燃的液体,具有广泛的应用领域。
其中,三本甲醇是甲醇的一种同分异构体,具有优异的性能和广泛的用途。
本文将介绍三本甲醇的制备过程以及相关的反应机理。
三本甲醇的制备主要有以下几种方法:1. 甲醇脱水法:甲醇脱水法是最常用的三本甲醇制备方法之一。
该方法通过在适当的温度和压力下,将甲醇与脱水剂(如浓硫酸、浓磷酸等)进行反应,使甲醇分子中的一个或多个羟基(OH基)脱除,从而得到三本甲醇。
该方法操作简便、成本较低,因此被广泛应用于工业生产。
2. 甲醇氧化法:甲醇氧化法是另一种常用的三本甲醇制备方法。
该方法以甲醇为原料,在适当的催化剂存在下,通过氧化反应将甲醇转化为三本甲醇。
常用的催化剂有铜、铝、镉等。
该方法反应条件较为温和,产率较高,因此也被广泛应用于工业生产中。
3. 甲醇脱氢法:甲醇脱氢法是一种较为新颖的三本甲醇制备方法。
该方法通过在适当的温度和催化剂存在下,使甲醇分子中的一个或多个氢原子脱除,从而得到三本甲醇。
该方法具有反应效率高、产物纯度高等优点,但操作条件较为苛刻,需要较高的催化剂活性和选择性。
以上是三本甲醇的三种主要制备方法,每种方法都有其特点和适用范围。
在实际生产中,可以根据具体的需求和条件选择合适的制备方法。
除了制备方法,还有一些反应机理和条件需要注意。
例如,在甲醇脱水法中,脱水剂的选择和使用量对反应的效果有重要影响;在甲醇氧化法中,催化剂的选择和反应温度对反应的速率和产物选择性有重要影响;在甲醇脱氢法中,催化剂的选择和反应温度对反应的活性和选择性有重要影响。
三本甲醇的制备是一个复杂而重要的过程。
在实际生产中,我们需要根据具体的需求和条件选择合适的制备方法,并合理控制反应机理和条件,以获得高效、高纯度的三本甲醇产品。
希望通过本文的介绍,能对三本甲醇的制备有更深入的了解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
文献 [ ] 1 中三 苯 甲醇的 常量制 备是 通过 格利雅 ( r n r ) G i ad 反应 来 完成的 . g 首先 溴苯 与镁 在
绝 对 无 水 乙醚 中 反应 生 成 格 利 雅 试 剂 —— 溴 化 苯 基 镁 , 接 将 格 利 雅 试 剂 与 二 苯 甲 酮 进 行 亲 直
2 结 果 讨 论
/
2 1 微型 实 验 方 法 省 时 , . 操作 简 便 , 用低 , 率 高 费 产
由 于 格 刺 雅 试 剂 非 常 活 泼 , 与 空 气 中 的 二 氧 化 碳 和 水 发 生 反 应 , 响 格 刺 雅 试 剂 与 二 苯 易 影
甲酮 的亲 核加 成 反应 , 降低 产 率 . 微 型 实 验 中 , 微 量 注 射 器 向反 应 系 统 注 入 试 剂 或 溶 剂 , 在 用 避
节. 此 , 求 实 验 者 既 要 有 严 谨 的科 学 态 度 , 要 认 真 细 致 地 工 作 . 因 要 又 总 之 , 型 实验 方 法 优 点 很 多 , 得 在 有 机 化 学 实 验 教 学 中 推 广 . 微 值
参
考
文
献
i 曾 昭琼. 机 化学 实 验. 二 版. 京 : 等教 育 出版 杜 ,97 15 1 6 有 第 北 高 1 8. 1~ 1
e p rme s e s nd e o m i . e ye d o rp e y m e h n l b a n d t i y i 8 . x e i nti a y a c no c Th il ft ih n l t a o t i e h swa s 8 o K e wo ds m ir s ae e p rm e t y r c o e l x e i n Trp e y me h n l G rg a d r a e t p e a a in i h n l t a o ; i n r e g n ; r p r to Ya g Di g i o Le t De t o e . HN U ,H u ng h u 43 0 0 Ch n . n n qa c .; p . fCh m a z o 8 0 , i a
12 1 格制 雅试 科的制备 ..
在干 燥 的 1 试管 中加A . 0m o (8 6 ) 0mL 2 0 t l4 . 0mg 镁条 , 加入 0 2 o 再 . 2mL( 3 g 溴 3 0r ) a
苯 , 注射器 加入 10 用 . 0mL 绝 对 无 水 乙 醚 . 果 反 应 在 2 3ri 如 ~ a n内不 发 生 , 玻 璃 棒 轻 轻 撞 击 用 镁 条 , 导 反 应 发 生 ; 果 镁 条 表 面有 气 泡 产 生 , 明 反 应 已 开 始 . 诱 如 表 当溶 液 慢 慢 变 浑 浊 , 条 逐 镁 渐 消失 , 即形 成 格 利 雅 试 剂 一 1 2 2 三 苯 甲 醇 的 制 备 . 在 1 0mL 干 燥 的 试 管 中 , 1 0 用 — 0mL 绝 对 元 水 乙 醚 溶解 2 。 . Om to ( 6 a g 二 苯 甲酮 , o l3 4r ) 并 将 溶 液 逐 滴加 ^ 到 已 制 备 的格 利 雅 试 剂 中 ( 意 : 应放 热 , 液 变 成 浅 红 色 ) 用 4  ̄ 5 C 注 反 溶 ; 0 0
Com pan , 94 6g~ 371 y 19 .3
PR EPA R AT1 0N F 0 TR I PH EN YLM ETH A N 0 L
I M I R0SCA LE N C EXPER I EN T M
Ya i q ao ng D ng t
Ab ta t Trp e y me h n lc n b r p r d i h t o f mir s ae a p r t s Th sr c i h n l t a o a e p e a e n t e me h d o e o c l p a a u . e
维普资讯
第 l 9卷 弟 4期
19 9 9年 8月
黄
闭
师
范
学
院
学
报
V ol 19 N o _ I
J r a fHua g n r a n v r i ou n lo n ga g No m lU ie st y
Au 1 9 g. 9 9
维普资讯
黄
阿 9卷
温 水 浴 加 热 0 5h 使 反 应 完 全 ; 却 后 , . , 冷 小心 滴 加 2 0 . 0mL的 3to ・ l L o 滤, 缩, 浓 得粗 产 品三 苯 甲 醇. I 2 3 精 制 粗 产 品 ..
2 Ke n t n eh L l a ∞ n M a r s ae a d Mir s ae Or  ̄ i Ex e i n . e i g o : C He l n l i . c o c l n c o c l g . c n p rme t L xn t n D. . at a d h
免 了 空 气 中 水 分 的 进 入 . 型 仪 器 容 易 操 作 、 全 , 验 省 时 ( 3学 时 ) 原 料 损 耗 低 , 品 损 微 安 赛 约 , 产
失少 , 率 高 . 当 前 实 验 经 费 不 足 的 情 况 下 , 用 微 型实 验 方 法 制 备 三 苯 甲 醇 , 品 用 量 少 , 产 在 采 药 可节 省 经 费 , 对环 境 枵 染程 度 小 . 2 2 微型 实 验 有 利 于 培养 学 生严 谨 的 科学 态 度 . 在 微 型实 验 中 , 须严 格 掌 握 固 体 药 品 的 投 放 量 及 液 体 药 品 的取 用 量 , 握 好 每 一 操 作 环 必 把
1 实 验 部 分
1 1 仪 器 和 试 剂 . 仪 器 : 0mL试 管 , / 0 1 1 l0 0TN 型 扭 力 托 盘 天 平 , 棒 , 玻 1mL 注 射 器 , 头 , 型抽 滤 装 针 微 置 , 点 澍定仪. 熔
酸.
,
。
试 剂 : 析 纯是 溴 苯 、 条 、 分 镁 无水 乙醚和 二 苯 甲酮 ; 化学 纯 是 石 油 醚 、 5 矗 醇 、 丙 醇 和 盐 9 异 1 2 实验 步 骤 .
用 微 型 实 验 方 法 制 备 三 苯 甲 醇
杨 定 乔
( 学 系) 化
摘
要
用 饺 型 仪 器 制 备 三 苯 甲 醇 , 作 简 便 , 济 , 时 , 率 这 8 操 经 省 产 8
06 5 3 2. 4
关 键 词 微 型 实 验 ; 苯 甲 醇 ; 利 雅 试 弈 ; 备 三 格 j制
收 稿 日 期 ;9 8 0 — 4 1 9—91. 扬 定 乔 , ・ 教 授 ; 州 t 同 师 院 化 学 系 ( 3 0 0 男 剐 黄 黄 48 0 ) * 湖 北 省 普 通 高 等 学 校 数 学 研 究 项 目基 壹 资 助 课 题 ( 5 1 3 9 06 )
溴化 苯 基 镁 .
的 HC 溶 液 , 用 I 再
冰 水 冷 却 ; 乙醚 萃 取 三 次 ( 次 用 1 5 用 每 . 0mL 乙醚 ) 合 并 醚 层 , 无 水 硫 酸 钠 干 燥 1 n; , 用 0mi 过
先用 05 . 0mL 石 油 醚 洗 涤 粗 产 品 , 后 用 微 型 抽 滤 装 置 减 压 抽 滤 , 去 联 苯 副 产 物 ; 用 然 除 再 I5 ~ 2 0 .0 . 0mL 异 丙 醇 重 结 晶 , 却 , 滤 , 燥 , 无 色 片 状 结 晶 三 苯 甲 醇 0 4 产 率 达 冷 抽 干 得 . 6g, 8 , 点 为 I 3 1 4℃ . 8 熔 ~ 6 6
核 加 成 反 应 , 后 经 稀 酸 水 解 得 三 苯 甲醇 . 最
常量 法 制 备 三 苯 甲醇 , 仅 操 作 麻 烦 , 时 长 ( 需 6学 时 ) 丽且 产 率 低 ( 0 ~ 3 ) 丽 不 耗 约 , 2 O . 微 型 实 验 方 法 , 作 简 便 , 时 ( 3学 时 ) 而且 产 率 高 ( 达 8 ) 操 省 约 , 可 8 .
