ZrO2陶瓷
99陶瓷化学成分

99陶瓷化学成分
99陶瓷,又称氧化锆陶瓷,其主要化学成分是氧化锆(ZrO2)。
氧化锆陶瓷具有高硬度、高耐磨性、高耐高温性能、化学稳定性好等优点。
除了氧化锆,99陶瓷中还包含少量的氧化钇(Y2O3),以调整陶瓷的性能。
氧化锆陶瓷的制备过程通常包括以下步骤:
1. 采购原料:购买高纯度的氧化锆矿石作为主要原料。
2. 粉碎和混合:将氧化锆矿石进行粉碎,然后与氧化钇等其他原料混合。
混合过程中,加入一定的结合剂(如水玻璃)以提高陶瓷粉体的塑性。
3. 成型:将混合好的陶瓷粉体进行成型,常用的成型方法有注浆成型、压制成型、挤压成型等。
4. 烧结:将成型后的陶瓷件进行高温烧结。
烧结过程中,氧化锆矿石和氧化钇等原料发生化学反应,形成高密度的氧化锆陶瓷。
5. 加工:烧结后的氧化锆陶瓷件进行打磨、抛光等加工工序,
以满足不同的使用要求。
6. 检验和包装:对加工好的氧化锆陶瓷件进行性能检测,确保其质量合格。
合格的陶瓷件进行包装,准备发往市场。
99陶瓷广泛应用于航空航天、化工、电子、医疗等领域,因其优异的性能而受到关注。
95%氧化锆珠密度

95%氧化锆珠密度
氧化锆(ZrO2)是一种重要的陶瓷材料,其密度取决于晶体结
构和氧化锆的纯度。
一般来说,氧化锆的密度在5.68至6.09克/立
方厘米之间。
而氧化锆珠是由氧化锆制成的微小颗粒,通常用于研
磨和磨削应用中。
氧化锆珠的密度通常在3.7至3.9克/立方厘米之间,这也是其在研磨领域中被广泛应用的原因之一。
需要注意的是,具体的氧化锆珠密度可能会因制造工艺、粒径大小和添加物等因素
而略有不同。
因此,在使用氧化锆珠时,最好参考供应商提供的具
体技术参数以获取准确的密度数值。
总的来说,氧化锆珠的密度一
般在3.7至3.9克/立方厘米之间。
结构陶瓷1(ZrO2)

问题:
1 完全稳定 2 稳定机理 3 溶胶-凝胶法 4 应力诱导
Thank you!
缺点:硬度和强度偏低
• 多种稳定剂的氧化锆陶瓷:
在Y-TZP中添加适量的CeO2,利用Ce-TZP 良好的抗低温水热腐蚀性能 ,可以有效抑制 低温老化现象。
另一方面,向Ce-TZP中加入少量Y2O3可提 高材料的烧结致密度、细化晶粒并提高其硬 度。
➢ 氧化锆增韧陶瓷
如果在不同陶瓷基体中加入一定量的 ZrO2 并使亚稳四方氧化锆多晶体均匀的弥散分布在 陶瓷基体中,利用氧化锆相变增韧机制使陶瓷 的韧性得到明显的改善。这种氧化锆相变增韧 陶瓷称为氧化锆(相变)增韧陶瓷(Zirconia Toughened Ceramics,ZTC)。
(+H2O) ZrOCl2 氯氧化锆凝固150-180 ℃ ,与SiCl4分离
冷却结晶/焙烧
ZrO2(粉体) + Cl2 或,ZrOCl2 + 2NH3 + 2H2O Zr(OH)4 + 2NH4Cl
热分解分馏Z法rO2超细粉 150-180℃ ZrCl4
3.2 共沉淀法:
此法由于设备工艺简单,生产成本低廉,且易 于获得纯度较高的纳米级超细粉体,因而被广
内容提要
• 前言 • ZrO2的结构与性能 • ZrO2粉体制备工艺
什么是氧化锆
氧化锆是所有形式二氧化锆的统称,是一种
耐高温、耐磨损、耐腐蚀无机非金属材料。
世界上已探明的锆资源约为 1900 万吨(以金属锆计),矿石品 种约有20种,主要含有如下几种化合物:
氧化锆陶瓷原料

氧化锆陶瓷原料
氧化锆陶瓷原料一般是指用于制备氧化锆陶瓷制品的原始材料。
氧化锆是一种无机化合物,化学式为ZrO2,具有高熔点、硬
度高、耐腐蚀等优良性能,因此广泛应用于陶瓷工业中。
氧化锆陶瓷原料主要包括以下几种:
1. 氧化锆粉:一般为白色结晶粉末状,具有高纯度、细度、均匀性等特点。
2. 氧化锆球:通常为球状颗粒,用于制备高密度、高硬度的氧化锆陶瓷制品。
3. 氧化锆颗粒:多为不规则颗粒状,用于制备氧化锆薄膜、涂层等。
4. 氧化锆原料浆料:一般为浓度较高的氧化锆粉末悬浮液,用于注模、涂敷等工艺。
以上是常见的氧化锆陶瓷原料,根据不同的应用需求和工艺要求,氧化锆陶瓷原料的特性和形态也会有所不同。
zro2热膨胀系数

zro2热膨胀系数热膨胀系数是一个物质在温度变化下线性膨胀或收缩的程度的度量。
它描述了物质在单位温度变化下的长度、面积或体积的变化量。
热膨胀系数是一个重要的物理性质,在工程设计、材料科学、建筑工程等领域的研究和应用中具有重要的意义。
本文将介绍ZrO2的热膨胀系数,并提供一些相关参考内容。
ZrO2,化学名称为二氧化锆,是一种常见的无机化合物。
它具有高熔点、高硬度和良好的化学稳定性,是一种重要的结构陶瓷材料和功能陶瓷材料。
对于ZrO2的热膨胀系数的研究对于设计和应用各种基于ZrO2的材料和构件都至关重要。
热膨胀系数一般用线膨胀系数(α)来表示,即单位温度变化引起的长度、面积或体积变化与原来的长度、面积或体积之比。
对于固体材料而言,可以用线膨胀系数来描述长度的变化,即单位温度变化引起的长度变化与原来的长度之比。
ZrO2的热膨胀系数因材料的晶相结构、组分和制备工艺等因素而异。
根据文献资料记载,ZrO2的室温线膨胀系数为10~12×10^-6/℃。
其中,其晶体结构的相变也会对热膨胀系数产生影响,例如由单斜相到四方相的相变会引起热膨胀系数的显著变化。
对于ZrO2的热膨胀系数的研究,可以参考多种文献和研究成果。
下面列举几个常用的参考文献:1. Yunos, D.M., et al. (2014). "Thermal Expansion of ZirconiaCeramics: A Review." Ceramics International, 40(1), 1159-1165.这篇综述文章回顾了关于ZrO2陶瓷热膨胀系数的研究成果。
文章概述了影响ZrO2热膨胀系数的各种因素,包括晶相结构、晶胞结构、材料纯度等,并总结了各种测量方法和技术的优缺点。
2. Garvie, R., et al. (1966). "Thermal Expansion in the Ceria Zirconia Series." Journal of the American Ceramic Society, 49(8), 408-9.这篇文章研究了CeO2和ZrO2组成系列中的热膨胀系数。
氧化锆是什么材料

氧化锆是什么材料
氧化锆,化学式ZrO2,是一种重要的陶瓷材料,具有优异的物理化学性能,
被广泛应用于陶瓷、医疗器械、电子元器件等领域。
它具有高熔点、高硬度、优良的热稳定性和化学稳定性等特点,因此备受工业界的青睐。
首先,氧化锆在陶瓷领域有着重要的应用。
由于其高熔点和优良的热稳定性,
氧化锆被广泛用于制作高温陶瓷,如耐火砖、耐火涂料等。
此外,氧化锆陶瓷还具有优异的机械性能,硬度高、抗压强度大,因此在机械制造领域也有着广泛的应用,如轴承、阀门、刀具等。
其次,氧化锆在医疗器械领域也有着重要的地位。
由于氧化锆具有优良的生物
相容性和化学稳定性,被广泛用于制作人工假体,如人工关节、牙科修复材料等。
相比传统的金属材料,氧化锆具有更好的生物相容性和耐腐蚀性,能够更好地适应人体内环境,减少了人体对异物的排斥反应,因此在医疗器械领域有着广阔的市场前景。
此外,氧化锆还被广泛应用于电子元器件领域。
由于其优良的绝缘性能和化学
稳定性,氧化锆被用作电容器的介质材料,能够在高频和高温环境下保持稳定的电学性能。
同时,氧化锆还被用作电子陶瓷材料,制成的电子陶瓷具有优异的介电性能和压电性能,被广泛应用于电子元器件中。
总的来说,氧化锆是一种具有广泛应用前景的重要材料,其优异的物理化学性
能使其在陶瓷、医疗器械、电子元器件等领域都有着重要的应用。
随着科技的不断进步和人们对材料性能要求的提高,相信氧化锆将会有更广阔的发展空间,为各个领域带来更多的创新和发展。
§25ZrO2的晶型转变和陶瓷增韧ZrO2是最耐高温的氧化物之一,它的熔点
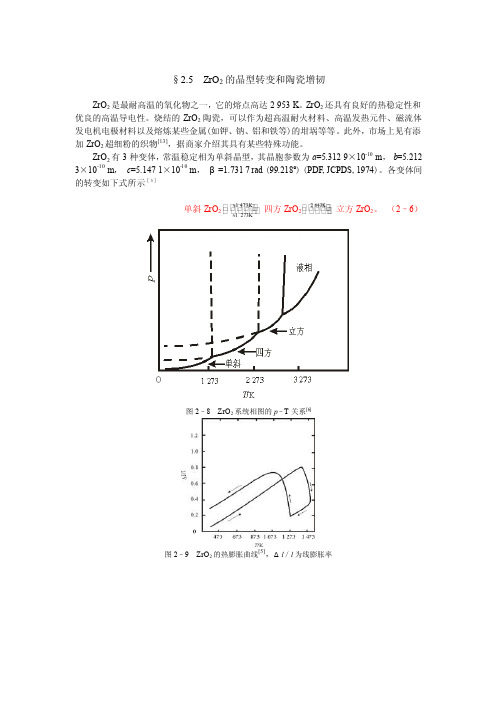
§2.5 ZrO 2的晶型转变和陶瓷增韧ZrO 2是最耐高温的氧化物之一,它的熔点高达2 953 K 。
ZrO 2还具有良好的热稳定性和优良的高温导电性。
烧结的ZrO 2陶瓷,可以作为超高温耐火材料、高温发热元件、磁流体发电机电极材料以及熔炼某些金属(如钾、钠、铝和铁等)的坩埚等等。
此外,市场上见有添加ZrO 2超细粉的织物[13],据商家介绍其具有某些特殊功能。
ZrO 2有3种变体,常温稳定相为单斜晶型,其晶胞参数为a =5.312 9×10-10 m , b =5.212 3×10-10 m , c =5.147 1×10-10 m , β=1.731 7 rad (99.218º) (PDF , JCPDS, 1974)。
各变体间的转变如下式所示[5]单斜ZrO 21473K 1273K ≈≈ 四方ZrO 22643K立方ZrO 2。
(2–6)图2–8 ZrO 2系统相图的p –T 关系[6]图2–9 ZrO 2的热膨胀曲线[5],Δl /l 为线膨胀率图2–10 ZrO2的差热曲线[5]ZrO2的晶型转变也可用相图(图2–8)来表示。
当温度升高到接近1 473 K时,单斜晶型会转变成四方晶型。
此转变伴随有7%~9%的体积收缩和1.8×104J·mol-1的吸热效应[6, 14](参见图2–9及图2–10)。
此转变属于位移式转变中的马氏体相变[2],转变速度很快。
从热膨胀曲线及差热曲线可以发现,在加热过程中由单斜转变成四方ZrO2的温度(≈1 473 K),和冷却过程中后者转化为前者的温度(≈1 273 K),并不一致。
也就是说,出现了多晶转变中常见的热滞现象。
由此可知,热滞现象不仅能在重构式转变中发生(这点似较易理解,详见上文§2.2中的机理三),也可以在转变速度很快的位移式转变中观察到。
ZrO2在发生位移式相变时,有较大的体积效应,因此它不能在高温下直接使用。
氧化锆的主要特点

氧化锆的主要特点
氧化锆(Zirconium dioxide,化学式:ZrO2)是一种重要的陶瓷材料,具有多种优异的物理和化学性质。
下面是一些氧化锆的主要特点:
1.高熔点和耐高温性:氧化锆具有极高的熔点(约2700°C)
和耐高温性,使其在高温环境下具有出色的稳定性和耐久
性。
2.高硬度和强度:氧化锆具有很高的硬度和强度,接近或超
过某些金属材料,因此在某些应用领域可以作为结构材料
使用。
3.优良的磨损和腐蚀抗性:氧化锆具有出色的耐磨损和耐腐
蚀性能,可以用于磨料、切削工具和耐腐蚀器件等。
4.高绝缘性:氧化锆是一种良好的绝缘体,具有高绝缘性能
和低电导率,可用于电气绝缘件和电子器件等。
5.优异的光学性能:氧化锆具有优异的光学特性,包括高透
明度、低散射和较高的折射率等。
这使得氧化锆广泛应用
于光学镜片、光纤窗口和光学涂层等领域。
6.热电性能:氧化锆具有良好的热电性能,表现为压电和热
释电效应,使其在传感器和热电设备等领域有一定的应用。
由于其诸多优良的性质,氧化锆被广泛应用于各个领域,包括航空航天、医疗器械、电子器件、化工和石油等。
它在这些领域中扮演着重要的角色,为现代科技的发展做出了重要贡献。
复方氧化锆结构

复方氧化锆结构
1. 简介
氧化锆(ZrO2)是一种高性能陶瓷材料,因其良好的机械性能、
化学稳定性、热稳定性和电学特性而被广泛应用。
复方氧化锆是一种
由不同材料组成的氧化锆复合材料,其结构更为复杂,性能更加出色。
下面将详细介绍复方氧化锆的结构。
2. 组成
复方氧化锆由氧化锆和其他一些材料组成,如钙、镁、铝、硅等。
不同组成的复方氧化锆具有不同的性能优点,可应用于不同的领域。
3. 结构
复方氧化锆的结构比氧化锆更为复杂,可以根据其组成元素的不
同分为以下几种:
3.1 晶体结构
复方氧化锆一般为立方晶系,其中石榴石型结构(ZrO2)和正交晶
型(Y2O3)是常见的两种结构,两者可混合形成不同的结构。
3.2 晶格缺陷
由于复方氧化锆中的杂质元素或氧化物含量较高,其晶格中常存
在一些缺陷,如点缺陷、位错、面缺陷等,这些缺陷使复方氧化锆的
性质更具多样性。
3.3 物相变
复方氧化锆可与其他材料形成不同的物相结构,如氧化锆和氧化铈合成的氧化铈氧化锆混合物(CeO2-ZrO2)具有良好的氧离子导电性能和催化活性等。
4. 应用
复方氧化锆由于其结构更复杂,性能更加出色,所以在各个领域都有广泛的应用。
在催化、电池、传感器等领域,常常采用复方氧化锆作为材料基础,制成高性能材料,满足不同领域的需求。
5. 总结
复方氧化锆的结构很复杂,包含了多种元素和化合物,不同结构和不同组分的复合材料具有不同的性能和功能。
由于其出色的性能表现,复方氧化锆在未来的科技研究和工程应用中,将继续扮演着非常重要的角色。
ZrO2陶瓷

烧结
T=1650-1800 ℃(保温2-4h) 粉料中粗颗粒多:体积收缩小 粉料中细颗粒多:产品密度高 热压烧结:可制得透明ZrO2陶瓷
氧化锆结构陶瓷
ZrO2结构陶瓷的性质与应用
1. 高耐火度,小比热和导热系数,ρ=1015Ωm(纯氧化锆) 高温绝缘材料 2. 化学稳定性好,抗酸性和中性物质腐蚀 熔炼坩埚,冶炼金属及合金,如Pt,Pd,Ru,Rh等 对钢水稳定,用作连续铸锭用的耐火材料 3. 高熔点( 2715 ℃)和抗氧化性 高温无机涂层,高温发热材料,高温电极材料 4. 莫氏硬度=7 陶瓷刀具及研磨材料 5.Zr02具有较高的折射率(N-21^22) 在超细的氧化锆粉末中添加一定的着色元素 (V205,Mo03,Fe203等),可将它制成多彩的半透明多晶Zr02 材料,像天然宝石一样绚丽多彩,可制成各种装饰品。
面整体还处于较落后的水平。今后的发展应朝着超细、高纯方向发展 ,产品制造方面应朝着新功能、新应用领域方向发展,不断扩大氧化
锆应用领域
The End
Thanks for your attention!
在未来需要解决如下问题:
1.关于Y-TZP
虽然Y-TZP烧结性能好,致密度高且具有优良的常温力学性能,抗弯强度高,断裂韧度高
, 但是,Y-TZP有一明显缺点,即在100~400℃的低温区长期使用时,材料表面向内部发生 t→m的等温相变,导致力学性能急剧下降,即发生低温性能老化。在200~300℃温度区间表现最 为突出,且在潮湿空气或有水的环境下,老化速度明显加快。这种低温性能老化现象严重地制约 着其应用,因此研究Y-TZP的低温老化机理和防止低温老化的途径逐渐成为近年来氧化锆陶瓷材 料研究的热点。
• 生物应用:研究表明, 氧化锆在人体口腔中无过敏现象, 在 合理设计的前提下, 可保证使用50年依然坚固. 氧化锆可以 用于几乎所有的义齿设计中, 它使牙桥制做的长度不再有 限制- 无论是螺栓固定式或粘接式,它 也是用于种植牙技术 的最好材料。
氧化锆

氧化锆氧量分析仪氧化锆氧量分析仪(Zirconia Oxygen Analyzer ,又称氧化锆氧分析仪、氧化锆分析仪、氧化锆氧量计、氧化锆氧量表),主要用于测量燃烧过程中烟气的含氧浓度,同样也适用于非燃烧气体氧浓度测量。
在传感器内温度恒定的电化学电池(氧浓差电池,也简称锆头)产生一个毫伏电势,这个电势直接反应出烟气中含氧浓度值。
氧化锆氧量分析仪广泛应用于多种行业的燃烧监视与控制过程,并且帮助各行业领域取得了相当可观的节能效果。
应用领域包括能耗行业,如钢铁业、电子电力业、石油化工业、制陶业、造纸业、食品业、纺织品业,还包括各种燃烧设备,如焚烧炉、中小型锅炉等。
将此分析仪应用于燃烧监视与控制,将有助于充分燃烧,减少CO2、SOx及NOx的排放,从而为防止全球变暖及空气污染做出贡献。
为何要进行氧含量监测随着人们环保和节能意识的逐渐提高,众多大中型企业如钢铁冶金、石油化工、火力发电厂等,已将提高燃烧效率、降低能源消耗、降低污染物排放、保护环境等作为提高产品质量和增强产品竞争能力的重要途径。
钢铁行业的轧钢加热炉、电力行业的锅炉等燃烧装置和热工设备,是各行业的能源消耗大户。
因此,如何测量和提高燃烧装置的燃烧效率、确定最佳燃烧点,是十分令人关心的。
确定最佳燃烧效率点供给加热炉、锅炉等加热设备的燃料燃烧热并不是全部被利用了。
以轧钢加热炉或锅炉为例,有效热是为了使物料加热或熔化(以及工艺过程的进行)所必须传入的热量,炉子烟气带走的物理热是热损失中主要部分。
当鼓风量过大时(即空燃比α偏大),虽然能使燃料充分燃烧,但烟气中过剩空气量偏大,表现为烟气中O2含量高,过剩空气带走的热损失Q1值增大,导致热效率η偏低。
与此同时,过量的氧气会与燃料中的S、烟气中的N2反应生成SO2、NOX等有害物质。
而对于轧钢加热炉,烟气中氧含量过高还会导致钢坯氧化铁皮增厚,增加氧化烧损。
当鼓风量偏低时(即空燃比α减小),表现为烟气中O2含量低,CO含量高,虽说排烟热损失小,但燃料没有完全燃烧,热损失Q2增大,热效率η也将降低。
二氧化锆带隙位置

二氧化锆带隙位置
【原创实用版】
目录
1.二氧化锆的概述
2.二氧化锆的带隙位置
3.二氧化锆带隙位置的重要性
4.二氧化锆的应用领域
正文
1.二氧化锆的概述
二氧化锆(ZrO2)是一种常见的陶瓷材料,具有高熔点、高硬度、高强度、化学稳定性好等优点。
它是一种四方晶体结构的化合物,由锆离子(Zr4+)和氧离子(O2-)组成。
由于其独特的物理和化学性质,二氧化锆被广泛应用于工业、航空航天、生物医疗等领域。
2.二氧化锆的带隙位置
二氧化锆是一种半导体材料,它的带隙位置决定了其导电性能。
在室温下,二氧化锆的带隙宽度约为 3.2 电子伏特。
这个带隙位置对于二氧化锆的电学性能有着重要的影响。
3.二氧化锆带隙位置的重要性
二氧化锆的带隙位置对于其应用领域有着重要的意义。
由于其带隙位置接近于一些常见氧化物的带隙位置,因此,二氧化锆可以被用作这些氧化物的替代品。
同时,二氧化锆的带隙位置也决定了其在光催化、电化学等方面的应用性能。
4.二氧化锆的应用领域
由于其独特的物理和化学性质,二氧化锆被广泛应用于各个领域。
其
中,最为人们所熟知的应用是作为牙科修复材料的锆瓷牙。
此外,二氧化锆还被用于制造电子元器件、光催化剂、传感器、生物医疗材料等。
共沉淀法制备zro2陶瓷

共沉淀法制备zro2陶瓷共沉淀法是一种常用的方法,用于制备高质量的ZrO2陶瓷材料。
ZrO2陶瓷具有广泛的应用前景,例如作为高温材料、催化剂和生物材料等。
本文将详细介绍共沉淀法的工艺流程,并探讨其在制备ZrO2陶瓷中的应用。
首先,我们来了解一下共沉淀法的原理。
共沉淀法是通过在溶液中同时加入适当的金属离子,使它们发生氧化沉淀反应,生成所需的陶瓷材料。
对于制备ZrO2陶瓷,我们可以选择含Zr离子的溶液和沉淀剂,如氨水或碳酸氢铵。
经过沉淀反应后,得到的沉淀物经过热处理和压制成型,最终得到高纯度的ZrO2陶瓷。
共沉淀法有很多优点。
首先,该方法可以制备出纯度高、颗粒均匀的ZrO2陶瓷。
其次,共沉淀法工艺简单,操作方便,成本较低。
此外,由于共沉淀法是在溶液中进行的,所以可以制备复杂形状的陶瓷制品。
在实际应用中,我们可以根据具体需求来进行共沉淀法的优化。
例如,可以调整沉淀剂的浓度和pH值,以控制颗粒大小和形貌。
此外,可以通过加入过渡金属离子或掺杂剂,来改变ZrO2陶瓷的性能。
例如,加入一定量的铒可以提高ZrO2的导电性能,使其用于固体氧化物燃料电池等电子器件中。
需要注意的是,共沉淀法还存在一些挑战和限制。
首先,沉淀过程中可能出现杂质的掺杂,影响ZrO2陶瓷的纯度和质量。
其次,共沉淀法制备的陶瓷材料可能存在晶型不均匀或结构缺陷等问题,影响其物理性能和化学稳定性。
因此,在制备过程中需要进行严格的控制和表征。
综上所述,共沉淀法是一种有效制备ZrO2陶瓷的方法,具有很大的应用潜力。
通过合理选择工艺条件和沉淀剂,可以得到高质量的ZrO2陶瓷材料。
随着科学技术的不断发展,共沉淀法在ZrO2陶瓷领域的应用前景将更加广阔,对于实现高性能材料的可持续发展具有重要的指导意义。
结构陶瓷1(ZrO2)
(3)四方相氧化锆在应力条件下,相变成单斜相 氧化锆。
➢裂纹的弯曲和偏转增韧(弥散增韧机理):
在裂纹的扩展路径上,放置一些障碍,阻碍 裂纹的运动,使裂纹扩展时须改变方向。这 些障碍可以是第二相粒子,也可以是第二相 产生的应力集中或残余应力等。
• Mg-PSZ:稳定剂MgO
优点:在相对较高的温度下具有优良的力 学性能和抗蠕变性能。
缺点:烧结温度很高(1700℃-1800℃), 高于1000℃时易产生晶相分解和大量四 方相失稳,致使材料性能衰退,严重制 约其在高温区的应用。
➢ 四方氧化锆多晶体陶瓷
当 ZrO2 中稳定剂加入量控制在适当量时可以使 tZrO2 以亚稳状态稳定保存到室温,那么块体氧化 锆陶瓷的组织结构是亚稳的 t- ZrO2 细晶组成的四 方氧化锆多晶体称之为四方氧化锆多晶体陶瓷 (tetragonal zirconia polycrystal,TZP)。在外力作用 下可相变 t-ZrO2发生相变,增韧不可相变的 ZrO2 基体,使陶瓷整体的断裂韧性改善。当加入的稳定 剂是Y2O3 、CeO2,则分别表示为 Y-TZP、Ce-TZP 等。
➢ 四方氧化锆多晶体陶瓷(tetragonal zirconia polycrystal,TZP)
➢ 氧化锆增韧陶瓷(Zirconia Toughened Ceramics,ZTC)
➢ 部分稳定氧化锆陶瓷
当 ZrO2 中稳定剂加入量在某一范围时,高温稳定的 cZrO2 通过适当温度下时效处理使 c-ZrO2 大晶粒(c 相) 中析出许多细小纺锤状的 t-ZrO2(t 相)晶粒,形成 c 相和 t相组成的双相组织结构。其中 c 相是稳定的而 t相 是亚稳定的并一直保存到室温。在外力诱导下有可能诱 发 t 相到 m 相的马氏体相变并伴随体积膨胀,耗散部分 能量、抵消了部分外力从而起到增韧作用,称为应力诱 导相变增韧。这种陶瓷称之为部分稳定氧化锆(partially stabilized zirconia, PSZ),当稳定剂为 CaO、MgO、 Y2O3 时,分别表示为 Ca-PSZ、Mg-PSZ、Y-PSZ 等。
氧化锆陶瓷的结构(1)

在转变过程中伴随着体积的变化,由单斜向四方转 变时,体积会收缩5%;的变化而粉化,所以制造较大的纯氧化锆体材料是 很困难的,有人提出可以利用这一相变改善氧化锆 陶瓷的强度和韧性。 在立方相基体中被约束的亚稳定四方相颗粒在扩展 的裂纹解除这一约束时能引起转变为单斜相的相变 。伴随着马氏体相变体积的变化和剪切应力能阻挡 裂纹的张开,从而增加陶瓷抵抗裂纹的扩展,即增 加了陶瓷的韧性。
氧化锆的结构
氧化锆存在三种稳定的同素异形体:单斜相(M) 立方相(C)和四方相(F)。 它们之间的转换关系如下:
单斜 (M)
1170℃
四方 (T)
2370℃
立方 (C)
2680℃ 液态
ZrO2三种晶体结构
ZrO2的四方晶型相当于萤石结构沿着C轴伸长而变形的晶 体结构;而单斜晶为沿着β角偏转一个角度而成的。
图1 四方晶内ZrO8在(100)平 面上投影
图2 立方晶内ZrO8在(100)平面 上投影
ZrO2晶体结构单胞参数和原子参数
在粉末混合物中,纯ZrO2的头同素异晶多型体能用X 射线衍射鉴别,Garvie和Nicholson和Schmid叙述了 用X射线衍射技术多氧化锆多型体混合物进行定量分 析的方法。不过,在立方、四方和单斜相的三元系 统中,不可能用XRD进行定量分析。在这种情况下, 唯一正确的方法是中子衍射。下表为不同情况下单 斜相ZrO2晶体结构原子参数。
氧化锆三相结构的特征
单斜结构如图所示,锆与氧离子是7个配位数,它一 方面被氧离子夹在四面体配位(OⅡ)的一边,另一 方面被氧离子夹在三角形配位(OⅠ)的另一边,他 们都有各自不同的键长和键角。由于晶体结构差异 很大,所以在外界应力作用下,将发生晶型转变。 四方晶ZrO2晶胞结构是Zr与O所处的位置类似于萤石 结构,Zr为8个O所包围,Zr 与其中四个O是等距离 配位,其距离是0.2455nm;另外四个O也是等距离 配位,Zr与O距离为0.2065nm。说明O是占有四方 的偏心位置,表明氧空位有利于阴离子转移(见图1 )。立方ZrO2晶格内每个Zr与8个O等距离配位,每 个Zr与4个O是四面体配位,如图2
氧化锆新型陶瓷

图1 四方晶内ZrO8在(100)平 面上投影
图2 立方晶内ZrO8在(100)平面 上投影
ZrO2晶体结构单胞参数和原子参数
• 在粉末混合物中,纯ZrO2的头同素异晶多型体能用X射 线衍射鉴别,Garvie和Nicholson和Schmid叙述了用X射 线衍射技术多氧化锆多型体混合物进行定量分析的方法。 不过,在立方、四方和单斜相的三元系统中,不可能用 XRD进行定量分析。在这种情况下,唯一正确的方法是中 子衍射。下表为不同情况下单斜相ZrO2晶体结构原子参 数。
2.2.5注射成型
• 注射成型是陶瓷可塑成型工艺中最普遍的一种方 法,在成形过程中,除了使用热塑性有机物或热 固性有机物或水溶性的聚合物作为主要的粘结剂 以外,还必须加入一定数量的增塑剂,润滑剂和
偶联剂等工艺助剂,以改善陶瓷注射悬浮体的流动 性,并保证注射成型坯体的质量。 • 缺点:生坯中有机物含量太高,排除时间太长,
4.烧结
• 分别采用一次烧结和两次烧结两种热处理方式, 在不同的烧结温度下烧结,对不同烧结方式和烧 结温度下材料的烧结密度、三点挠曲强度、维氏 硬度和断裂韧性进行测量分析,并通过扫描电镜 观察试件的断裂面形貌。
• 两次烧结与一次烧结相比,氧化锆陶瓷烧结体的 密度、三点挠曲强度、维氏硬度及断裂韧性存在 差异。在900 ℃/1 450 ℃烧结温度时,两次烧结 氧化锆陶瓷烧结体相对密度最高(98.49%),机 械性能最佳,三点挠曲强度、维氏硬度和断裂韧 性分别为1 059.08MPa±75.24MPa、1 377.00MPa±16.37MPa和5.92MPa·m1/2±0.37 MPa·m1/2。两次烧结使氧化锆陶瓷烧结体的内部 孔隙略有增多,部分晶粒长大且大小不均匀。
• 相变增韧ZrO2陶瓷具有优良的力学性能、低的导 热系数和良好的抗热震性,是一种极有发展前途 的新型结构陶瓷。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ΔH——单位体积的相变热
将ΔH=2.82108 J/m3、Tb=1170 ℃、t-ZrO2 和m-ZrO2的表面能1.46和0.55 J/m2代入公式 中,得到rc=15.3 nm。即t-ZrO2稳定存在的 临界尺寸为30.6 nm
表面能
使用Scherrer公式,由图5-4的XRD衍射谱可以计算晶粒尺寸。
2. 高温碱解法
3. 水热法
工艺流程:
– 锆盐溶液的水热处理→过滤→干燥(70 ℃ )
→ZrO2微粉/超细粉
水热反应条件:T>200℃,P=10MPa 设备:高压釜 原料:锆盐(ZrOCl2)溶液 化学反应: – ZrOCl2+H2O→ZrO2+HCl
4. 等离子体合成法
1)ZrSiO4粉体注入等离子弧反应室 ZrSiO4 ZrO2 + SiO2 + 2NaOH + H2O (煮沸) ZrO2 + Na2SiO3 洗涤 ZrO2粉体 2)等离子体加热粉体至2100-2300 ℃ ZrSiO4 c-ZrO2(10-100nm) + SiO2(liq) NaOH溶液处理 ZrO2粉体
3、单斜相和四方相之间相互转化
相变是无热的。即相变的量只随温度变化 而不随时间变化,为使相变进一步发生必 须增大相变驱动力,即进一步降低温度。 相变的结构转变是无扩散的。母相通过切 变来形成新相,通过原子的集体协调运动 来完成,相变后每个原子的近邻原子的种 类不变,原子的运动小于一个原子间距, 仅仅是Zr、O原子的较小的移动。 相变材料出现表面凸起。
正由于氧化锆有晶型转变和体积突变的特点, 因此单用纯氧化锆就很难制造出烧结且又不开裂的 制品。当向氧化锆中加入一些与Zr4+离子半径相差 在 12% 以 内 的 氧 化 物 , 如 CaO 、 MgO 、 Y2O3 、 CeO2 等,经高温处理后就可以得到从室温直至 2000℃以上都稳定的立方晶型的氧化锆固溶体,从 而消除了体积突变。
Tp1 (℃) Tp2 (℃)
8 305.13 528.02
10 316.62 534.91
12 321.21 544.10
15 332.70 553.30
Tp1: t-ZrO2析晶放热峰温度 Tp2: m-ZrO2析晶放热峰温度
析晶活化能
根据JMA方程,等温条件下析晶体积分数可描 述为: x =1-exp[-(kt)n] 式中x为结晶体积分数,k为析晶动力学参数,t 为等温时间,n是反映析晶机理的指数。一般 情况k可表示为: k =νexp(-E/RT) 式中ν为频率因子(s-1),E为析晶活化能,T 为开氏温度,R为气体常数
析晶活化能
在非等温条件下应用此式,需要对JMA 方程进行修正。由Bansal N P等人修正 后的方程为:
E ln 2 ln( E / R) ln RT p Tp
其中,Tp是DTA的峰值温度,β是升温速率
析晶活化能
以表5-2的数据代入方程中,分别绘制tZrO2和m-ZrO2的ln(β/Tp2)-1/Tp关系曲 线如图5-6(a)、(b)所示,由此直线的斜率 可得到溶胶-凝胶法制备的二氧化锆粉中 的t-ZrO2和m-ZrO2析晶活化能分别为 56.5kJmol-1和109.2kJmol-1。t-ZrO2析晶活 化能更低,即析出t-ZrO2所克服的能垒更 低,因此从二氧化锆凝胶粉中更易析出tZrO2并稳定存在。
析晶活化能
-10.0 -10.1 -10.2
-10.6 -10.7 -10.8
ln(/Tp )
ln(/Tp )
-10.3 -10.4 -10.5 -10.6 -10.7 1.64 1.66 1.68 1.70 -1 1000/Tp(K ) (a) 1.72 1.74
2
-10.9 -11.0 -11.1 -11.2 -11.3 1.21 1.22 1.23 1.24 -1 1000/Tp(K ) (b) 1.25 1.26
ZrO2陶瓷 ZIRCONIA CERAMICS
ZrO2陶瓷
4.1 概述 4.2 ZrO2的特征 4.3 ZrO2结构陶瓷 4.4 ZrO2气敏陶瓷 4.5 ZrO2导电陶瓷 4.6 ZrO2高温热敏陶瓷(NTC)
ZrO2的市场
2000 年世界ZrO2的销售额约为450 亿美元。
0.2
Temperature difference( C/mg)
316.62 C 534.91 C 0.1
o
o
10 C/min
o
o
0.0 128.6 C 0 200 400 600
o o
800
1000
Temperature ( C)
析晶活化能
表5-2 不同升温速率下凝胶粉的DTA数据
升温速率 (℃/min)
20
25
30 35 40 45 Degrees two theta (CuK)
50
55
图5-4 不同温度下二氧化锆凝胶粉的XRD衍射图
晶体结构
由图5-4可看出400℃时的ZrO2非晶馒头峰 峰顶与t-ZrO2的具有最大峰强的(111) 衍射峰相对应。表明非晶态的近程有序 结构与t-ZrO2的晶体结构类似。这种结构 相近性,使得非晶态ZrO2向t-ZrO2的转变 只需克服较小的晶格畸变能。因此, ZrO2凝胶中的非晶态更易向t-ZrO2转变
图5-6 DTA分析中ln(β/Tp2)与1/Tp关系曲线:(a)t-ZrO2,(b)m-ZrO2
2
小结
晶体结构、表面能及析晶活
化能三个方面均显示,低温 下纳米二氧化锆凝胶粉中的 亚稳t-ZrO2易先于m-ZrO2析 出并稳定存在
稳定的ZrO2
氧化锆的几个术语
PSZ:部分稳定氧化锆,又叫陶瓷钢 TZP:四方多晶氧化锆 Y-TZP:掺Y2O3稳定剂的四方多晶氧化锆
热处理温度 (℃)
t-ZrO2晶粒尺寸 (nm) m-ZrO2晶粒尺寸 (nm)
600
8.6 9.4
800
17 15.5
1000
- 33.8
从表5-1看到500、600和800 ℃热处理后tZrO2晶粒尺寸分别为5.1、8.6和17 nm, 处于表面能起决定作用的t-ZrO2稳定存在 的尺寸范围内,因此亚稳t-ZrO2可在低温 稳定存在。至1000 ℃热处理后,m-ZrO2 晶粒尺寸达到33.8 nm,而此时t-ZrO2已完 全消失,可知由于t-ZrO2此时晶粒尺寸已 大于30.6 nm的保持稳定的临界尺寸,所 以失稳并完全转变为m-ZrO2。
ZrO2的性质
含锆的矿石:斜锆石(ZrO2),锆英石 (ZrO2 · 2); SiO 颜色:白色(高纯ZrO2); 黄色或灰色(含 少量杂质的ZrO2),常含二氧化铪杂质; 密度:5.65~6.27g/cm3;
熔点:2715℃。
ZrO2的晶型及其转化
单斜、四方、立方晶系3种 1170 ℃ 2370 ℃ 2715 ℃ m-ZrO2 t-ZrO2 c-ZrO2 liq-ZrO2 d = 5.65 6.10 6.27 g/cm3 m-ZrO2 t-ZrO2 T=~1200 ℃ m-ZrO2 t-ZrO2 T=~1000 ℃ 3~5%的体积膨胀和7~8%的切应变 稳定ZrO2 稳定剂微裂纹 Y2O3,CaO,MgO et al.
氧化锆陶瓷
ZrO2结构陶瓷
ZrO2粉体的制备 ZrO2陶瓷的制备 ZrO2陶瓷的性质和用途
ZrO2粉体的制备
1. 锆英石加碳氯化法 ZrSiO4 + C + 4Cl2 ZrCl4 + SiCl4 + 4CO >300 ℃(升华) 57.6 ℃ (+H2O) ZrOCl2 氯氧化锆凝固150-180 ℃ ,与SiCl4分离 冷却结晶/焙烧 ZrO2(粉体) + Cl2 或,ZrOCl2 + 2NH3 + 2H2O Zr(OH)4 + 2NH4Cl 热分解 ZrO2超细粉
0.9 D cos
D ——平均晶粒尺寸(nm) ——衍射角
——2衍射峰的半高宽(弧度)
=0.15418 nm
表面能
t-ZrO2和m-ZrO2的主衍射峰t(111)和m(-111)所对应的2 衍射角分别为30.5°和28°,由这二个主衍射峰计算不同温度 下t-ZrO2和m-ZrO2平均晶粒尺寸如表5-1所示。 表5-1 不同温度下t-ZrO2与m-ZrO2的平均晶粒尺寸
5. 气相沉积法
Zr(OC3H7)4粉体蒸汽 320-450 ℃热分解 ZrO2超细粉
ZrO2陶瓷粉体制备
单纯ZrO2很难生产ZrO2陶瓷 原因:晶型转变体积变化制品开裂 途径:加入稳定剂 Y2O3 CaO MgO et al., 无异常膨胀/收缩稳定c-/t-ZrO2(Y2O3 8mol%) 抗折强度~35MPa Y2O3-PSZ (Y2O3 3-4mol%) 抗折强度~140MPa 良好ZrO2陶瓷 PSZ: Partially Stabilized Zirconia 稳定剂的阳离子半径与Zr4+离子半径相差小于12%
– 日本占41~42% – 美国占22%左右
氧化锆陶瓷的用途 结构材料:磨料磨具、耐火材料等 功能材料:
– 氧传感器
– 固体氧化物燃料电池 – 高温发热体
氧化锆陶瓷的研发历史
20世纪20年代开始就被用做熔化玻璃和冶炼钢铁等的 耐火材料; 1968年,日本松下电器公司开发出氧化锆非线性电阻 元件; 1973年,美国R. Zechnall制得电解质氧传感器,能正 确显示汽车发动机的空气/燃料比,1980年用于钢铁工 业; 1975年,澳大利亚R. G. Garvie以CaO为稳定剂制得部 分稳定的氧化锆,并首次利用陶瓷马氏体相变的增韧 效应,提高了其韧性和强度; 1982年,日本绝缘子公司和美国Cummins发动机公司 共同开发出节能柴油机缸套。 氧化锆陶瓷
