2014秋中国石油大学(北京)《普通化学》第二阶段在线作业答案
2014春中石油大学(北京)《有机化工工艺》第二阶段作业答案

第1题目前先进裂解炉的热效率是您的答案:C题目分数:0.5此题得分:0.5批注:裂解炉相关专业常识第2题脱乙烷塔的重关键组分是您的答案:E题目分数:0.5此题得分:0.5批注:深冷分离第3题脱乙烷塔的轻关键组分是您的答案:D题目分数:0.5此题得分:0.5批注:深冷分离第4题丙烷裂解时,产物含量最多的是您的答案:C题目分数:0.5此题得分:0.5批注:自由基链反应机理第5题乙烷裂解时,产物含量最多的是您的答案:C题目分数:0.5此题得分:0.5批注:自由基链反应机理第6题裂解炉的哪一段承担裂解反应的任务您的答案:B题目分数:0.5此题得分:0.5批注:裂解炉结构第7题裂解炉的排烟温度为您的答案:C题目分数:0.5此题得分:0.5批注:工艺条件第8题急冷锅炉出口的裂解气温度设计为您的答案:D题目分数:0.5此题得分:0.5批注:工艺条件第9题裂解气脱除酸性气的方法是您的答案:D题目分数:0.5此题得分:0.0批注:裂解气净化第10题裂解气脱水的方法是您的答案:A题目分数:0.5此题得分:0.5批注:裂解气净化第11题裂解气脱水所用的干燥剂为您的答案:C题目分数:0.5此题得分:0.5批注:裂解气净化第12题裂解气脱炔的方法是您的答案:D题目分数:0.5此题得分:0.5批注:裂解气净化第13题深冷分离是指分离温度低于您的答案:C题目分数:0.5此题得分:0.5批注:深冷分离的概念第14题根据热力学判断,裂解一次反应中的脱氢反应是不可逆的您的答案:错误题目分数:0.5此题得分:0.5批注:裂解一次反应的热力学分析第15题根据热力学判断,裂解一次反应中的断链反应是不可逆的您的答案:正确题目分数:0.5此题得分:0.5批注:裂解一次反应的热力学分析第16题最佳停留时间是指某反应温度下,反应系统给出最高乙烯收率所需的反应时间您的答案:正确题目分数:0.5此题得分:0.5批注:裂解反应的动力学,最佳停留时间第17题生成烯烃的反应为一次反应您的答案:正确题目分数:0.5此题得分:0.5批注:裂解反应分类第18题生成芳烃的反应为二次反应您的答案:错误题目分数:0.5此题得分:0.5批注:裂解反应分类第19题根据自由基链反应机理,异丁烯裂解不产生乙烯您的答案:正确题目分数:0.5此题得分:0.5批注:自由基链反应机理第20题根据自由基链反应机理,环烷烃裂解不产生乙烯您的答案:错误题目分数:0.5此题得分:0.5批注:自由基链反应机理第21题根据自由基链反应机理,环烷烃裂解产生丙烯较多您的答案:错误题目分数:0.5此题得分:0.5批注:自由基链反应机理第22题裂解反应是强吸热反应您的答案:正确题目分数:0.5此题得分:0.5批注:裂解工艺条件第23题裂解反应温度一般高于750℃您的答案:正确题目分数:0.5此题得分:0.5批注:裂解工艺条件第24题裂解时不可能同时获得最大的乙烯收率和最大的丙烯收率您的答案:正确题目分数:0.5此题得分:0.5批注:裂解反应深度第25题稀释水蒸汽的加入,加快了裂解反应速度您的答案:错误题目分数:0.5此题得分:0.5批注:裂解反应的动力学第26题稀释水蒸汽的加入,在热力学上有利于裂解的一次反应您的答案:正确题目分数:0.5批注:裂解一次反应的热力学分析第27题稀释水蒸汽的加入,在热力学上有利于裂解的二次反应您的答案:错误题目分数:0.5此题得分:0.5批注:裂解一次反应的热力学分析第28题裂解炉的类型有您的答案:A,B,C,D题目分数:0.5此题得分:0.5批注:裂解工艺第29题裂解气降温过程所用的冷却介质包括您的答案:A,B,C,D题目分数:0.5此题得分:0.5批注:裂解工艺第30题裂解气净化是指脱除您的答案:A,B,C题目分数:0.5此题得分:0.5批注:裂解气净化第31题裂解气净化过程所说的酸性气是指您的答案:A,B,C题目分数:0.5此题得分:0.0批注:裂解气净化第32题裂解过程中稀释蒸汽的作用是您的答案:A,C,D题目分数:0.5此题得分:0.0批注:裂解工艺条件第33题顺序分离流程中,脱甲烷塔塔底出料中的组分有您的答案:A,B,C,D题目分数:0.5批注:深冷分离第34题顺序分离流程中,脱甲烷塔塔顶出料中的组分有您的答案:A,B,C,D题目分数:0.5此题得分:0.0批注:深冷分离第35题顺序分离流程中,脱乙烷塔塔顶出料中的主要组分有您的答案:B,D,E题目分数:0.5此题得分:0.0批注:深冷分离第36题前脱乙烷流程中,脱乙烷塔塔顶出料中的主要组分有您的答案:A,B,C,D,E题目分数:0.5此题得分:0.5批注:深冷分离第37题前脱乙烷流程中,脱乙烷塔塔底出料中的主要组分有您的答案:A,B,C,D题目分数:0.5此题得分:0.5批注:深冷分离第38题乙烯精馏塔塔顶出料为您的答案:A,B题目分数:0.5此题得分:0.5批注:深冷分离第39题乙烯产品的出料位置可能为您的答案:A,D题目分数:0.5此题得分:0.5批注:深冷分离第40题裂解炉由哪几部分组成题目分数:0.5此题得分:0.5批注:裂解炉结构作业总得分:17.5 作业总批注:。
中国石油大学(北京)15秋《普通化学》第一阶段在线作业100分答案

第一阶段在线作业单选题(共22道题)1.(2.5分)等容热效应Qv的大小只与_____有关。
A、系统的始态B、系统的终态C、系统的始态和终态正确答案:C 此题得分:2.5分2.(2.5分)某反应在一定条件下转化率为25%,当有催化剂存在时,其平衡转化率_____ 25%。
A、大于B、等于C、小于正确答案:B 此题得分:2.5分3.(2.5分)催化剂能加快反应速率主要是因为______反应活化能。
A、增大B、减小C、不能改变正确答案:B 此题得分:2.5分4.(2.5分)催化剂加入使反应的热效应。
A、增大B、减小C、不能改变正确答案:C 此题得分:2.5分5.(2.5分)某反应的速率常数k为0.107 min-1,则反应物浓度从1.0 mol·L-1变到0.7 mol·L-1和浓度从0.01 mol·L-1变到0.007 mol·L-1所需时间的比值为A、10B、100C、0.01D、1正确答案:D 此题得分:2.5分6.(2.5分)在描述一级反应特征时,___ 是不正确的A、CA- t为一直线关系。
B、反应物消耗的百分数相同时所需的时间一样(同一反应)C、速率常数的单位为(时间)-1正确答案:A 此题得分:2.5分7.(2.5分)一定温度下化学反应体系的反应级数越小,一般反应速率随时间的延长______。
A、下降越快B、下降越慢C、升高越快D、升高越慢正确答案:B 此题得分:2.5分8.(2.5分)对两个活化能不同的反应,当温度同样从T1升至T2时,具有活化能高的反应,其反应速率增加的倍数比活化能低的反应增加的倍数。
普通化学全本部分习题答案

《普通化学》课程练习题使用教材 教材名称普通化学 编 者 史国纲出 版 社中国石油大学出版社第一章 物质及其变化的一些基本规律上交作业 3、7(1)(2)、8、113 NH 3的分压为: kpa n NH n p x p NH NH 47.3513370.018.032.032.0p )(333=⨯++=⨯==总 O 2的分压为:kpa n O n p x p O O 95.1913370.018.032.018.0p )(222=⨯++=⨯==总 N 2的分压为:kpa n N n p x p N N 95.1913370.018.032.018.0p )(222=⨯++=⨯==总7查出各物质及水合离子的标准生成焓标在反应方程式中各对应物质和水合离子化学式的下面,然后根据公式计算。
(1) )()(2)(2222g O g H l O H +=1/-⋅∆mol kJ H f θ -285.83 0 01122229866.577)83.285(200)](,[2)]}(,[)](,[2{--⋅=⋅-⨯-+=∆-∆+∆=∆mol kJ mol kJ l O H H g O H g H H H f f f θθθθ(2) )(4)()(4)(32432g H s O Fe l O H s Fe +=+1/-⋅∆mol kJ H f θ0 -285.83 -1118.4 011243229892.24]}0)83.285(4[)]4.1118(0{[)]}(,[3)](,[4{)]}(,[)](,[4{--⋅=⋅+-⨯--+=∆+∆-∆+∆=∆mol kJ mol kJ g Fe H l O H H g O Fe H g H H H f f f f θθθθθ8 )(21)(322g SO O g SO =+1/-⋅∆mol kJ H f θ -296.83 0 -395.721122329889.98)]83.296(0[72.395)]}(,[)](,[21{)](,[--⋅-=⋅-+--=∆+∆-∆=∆mol kJ mol kJ l O H H g O H g SO H H f f f θθθθ11 (1)反应速率表达式为:)()(22Cl c NO c k v ⋅⋅=(2)该反应对NO 为二级反应,对Cl 2的一级反应,总反应级数为3。
《油田化学》填空题总结及详细答案(word版可编辑修改)

《油田化学》-填空题总结及详细答案(word版可编辑修改)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(《油田化学》-填空题总结及详细答案(word版可编辑修改))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为《油田化学》-填空题总结及详细答案(word版可编辑修改)的全部内容。
中国石油大学(北京)《油田化学》填空题总结1.水和冰是属于两个 不同 的相,因为虽然两者的化学性质相同,但物理性质不同。
2.物质颗粒越小,分散度越 高 ,比表面越 大 。
3。
净吸力 的存在是表面张力产生的根本原因。
4。
液体接近临界温度时,液相与气相区别消失,界面消失,表面张力趋于 零 。
5.雨点落在荷叶上呈小球形,这是 润湿 现象。
6.润湿方程为:θσσσcos 液气固液固气---+=7.液体在固体表面上的润湿有三种:沾湿、浸湿和铺展。
8。
液体沾湿固体的条件是:沾湿功 ≥0,即接触角〈1800。
9。
浸湿功又叫 粘附张力。
10。
浸湿的条件是:浸湿功 ≥0,即接触角θ〈900。
11.当铺展系数S 大于或等于0 ,即 接触角≤00 时,液体可以在固体上铺展,此时,液—固粘附张力 大于或等于 液体表面张力。
12。
对于同一体系,沾湿功 〉 浸湿功 > 铺展系数,即如果液体能够在固体上铺展,那么它一定能沾湿和浸湿固体。
13。
由于表面张力的存在,而在弯曲液面上产生的附加的压力,称为 附加压力 .14.表面张力越 大 ,曲率半径越 小 ,附加压力越大.15。
球面的附加压力为:RP σ2=∆16。
毛细管半径越小,两相密度差越小,界面张力越大,则毛细管上升高度越 大 .17.液体在毛细管中是上升还下降,决定于 液体对毛细管管壁固体的润湿程度 。
2014年历年北京卷普通高等学校招生全国统一化学考试及答案

2014年普通高等学校招生全国统一考试(北京卷)化学1.下列试剂中,标签上应标注和的是A.B.C.D.解析:此题源自必修一中常见标签介绍。
非常简单。
答案: C2.下列金属中,表面自然形成的氧化层能保护内层金属不被..空气氧化的是A.B.C.D.解析:此题同样源自必修一种几种常见金属,非常简单。
答案: DA.选项:为正极。
B.选项:氢氧燃料电池,通氧气为正极,正确。
C.选项:为正极。
D.选项:我正极。
答案: B4.下列解释事实的方程式不正确...的是A.测氨水的pH为11:B.将块放入水中,产生气体:C.用溶液做导电实验,灯泡发光:D.片溶于溶液中,产生气体:解析:A 弱电解质电离平衡考查,正确。
B 金属性质考查,正确。
C 电解质电离考查:溶于水或熔化状态下可以导电的化合物。
电离不是通电。
D 金属性质考查,此离子方程式和化学方程式学生复习时必然多次重复,正确。
答案: C5.下列说法正确的是A.室温下,在水中的溶解度,丙三醇>苯酚>1-氯丁烷B.用核磁共振氢谱不能区分和C.用溶液不能区分和D.油脂在酸性或碱性条件下均能发生水解反应,且产物相同解析:此题考查有机化合物相关知识,难度:中等偏易A 选项:亲水基数目与溶解度关系考查,羟基越多越易溶,故正确。
B 选项:核磁共振概念考查:两物质峰个数分别为2种,3种,可以区分,故错误。
C 选项:官能团性质考查:羟基有酸性可以与碳酸钠反应,而酯基不可,可以区分,故错误。
D 选项:酯水解反应考查:酸性水解变羟酸和醇,碱性水解产物为钠盐和醇,产物不同,故错误。
答案: A6.用下图装置(夹持、加热装置已略)进行试验,有②种现象,不能..证实①中反应发生的是A 选项:选自必修一课本演示实验:铁粉和水蒸汽反应。
但肥皂水冒泡无法证明生成氧气,现象应为生成大量气泡并上浮,点燃有爆鸣声。
故错误B 选项:选自必修一课本实验:氨气的制备,正确C 选项:选自必修一课本实验:碳酸氢钠受热分解,正确D 选项:选自必修二课本实验:乙烯的制备,正确答案: A7.在一定温度下,溶液发生催化分解。
2014秋中国石油大学《油田化学》第二阶段在线作业

2014秋中国石油大学《油田化学》第二阶段在线作业
1.(
2.5分)硅酸钠(sodiumsilicate)俗名水玻璃、泡花碱,分子式为Na2O.nSiO2,n称为水玻璃的模数。
n值在3以上的称为
•A、酸性水玻璃
•B、中性水玻璃
•C、碱性水玻璃
•D、弱碱性水玻璃
我的答案:B此题得分:2.5分
2.(2.5分)无机物类缓凝剂主要以下面哪项机理起作用
•A、吸附理论
•B、沉淀理论
•C、晶核延缓结晶理论
•D、络合理论
我的答案:B此题得分:2.5分
3.(2.5分)现场采用的水玻璃密度约为1.5~1.6g/cm3,pH为多少,使她能溶于水和碱性溶液,能与盐水混溶,可用饱和盐水调节水玻璃的粘度。
•A、4~6
•B、5~7
•C、9~11
•D、11.5~12
我的答案:D此题得分:2.5分
4.(2.5分)决定水泥初凝和稠化时间的是
•A、硅酸二钙
•B、硅酸三钙
•C、铝酸二钙
•D、硅酸三钙
我的答案:C此题得分:2.5分
5.(2.5分)下面哪种主要用于温度低的浅井或深井导管、表层套管或高寒地区或挤水泥、打水泥塞时使用
•A、速凝剂
•B、降失水剂
•C、缓凝剂
•D、减阻剂
我的答案:A此题得分:2.5分
6.(2.5分)下面哪种降低水泥浆的表观粘度,有利于水泥在低压低速进入紊流状态,提高注水泥质量和驱替效率
•A、速凝剂
•B、降失水剂
•C、缓凝剂
•D、减阻剂
我的答案:D此题得分:2.5分
7.(2.5分)在高温、超深井中应慎用。
2014年中国石油大学北京化工热力学在线考试(主观题)答案

1.教材中给出了众多的状态方程,请根据本人的工作或者生活选择一个体系、选择一个状态方程、对其PVT关系的计算准确度进行分析,并提出改进的方向和意见。
丙烯的PVT状态分析近期我正在新疆五家渠一家焦化厂甲醇车间进行培训,在甲醇净化工段丙烯为利用最多的制冷剂,在学习丙烯压缩工段的同时对丙烯的物化性质也有了深入了解。
丙烯的理化学性质:丙烯是一种无色略带甜味的易燃气体,分子式为CH3CH=CH2,分子量为42.08,沸点-47.7℃,熔点为-185.25℃,其密度为空气的1.46倍,临界温度为91.8℃,临界压力为4.6Mpa,爆炸极限为2.0~11%(vol),闪点为-108℃。
(因此,丙烯在贮藏时要特别小心,如果发生泄漏,因为它比空气重,积聚在低洼处及地沟中,如在流动过程中遇到火星,则极易引起爆炸,酿成严重后果。
)选择用R-K状态方程计算对液态丙烯的PVT关系计算准确度进行分析,从《化工热力学、陈光进等编著》中查得丙烯的临界数据为Tc=364.9K;p=46.0*10-1MPa,c下面是上海焦化厂给定的丙烯性质数据。
为了计算方便,用excel换算和简单计算得到新的数据如下:温度-40 -30 -20 -10 0 10 20 30 40 50 (℃)压力1.4012.0973.0234.2575.772 7.685 10.046 12.911 16.307 20.299 (atm)体积12966 6404 4639 3423 2569 1957 1510 1510 1177 922 (mL/g)R-K 方程:()b v v T a b v RT p +--=5.0 ()25.0665.25.223409.16106.49.3643146.842748.042748.0-•••=⨯⨯⨯==mol K Pa m p T R a c c ()1356107145.5106.49.3643146.808664.008664.0--•⨯=⨯⨯⨯==mol m p RT b c c 由上表又知道摩尔体积v ,故根据R-K 方程,用excel 可分别计算得到各温度下的压力值P 1:温度(℃)-40-30 -20 -10 0 10 20 30 40 50 温度(K )233 243 253 263 273 283 293 303 313 323 压力P(1*10-1MPa )1.41962.12483.06314.31345.8485 7.7868 10.1791 13.0821 16.5231 20.5680 摩尔体积v(1*10-5m 3/mol) 54560.928 26948.032 19520.912 14403.984 10810.352 8235.056 6354.080 6354.080 4952.816 3879.776温度(℃)-40 -30 -20 -10 0 10 20 30 40 50 压力P(1*10-1MPa )1.41962.12483.06314.31345.8485 7.7868 10.1791 13.0821 16.5231 20.5680 计算压力P 1(1*10-1MPa) 1.0288 2.1706 3.1182 4.3903 6.0679 8.2505 11.0602 11.4412 15.1467 19.9288用R-K状态方程计算得数据与给定值比较可得如下数据图:通过计算和上图的数据对比,可得结论:利用《上海焦化厂给定丙烯性质数值》,代入v值,用R-K方程计算所得的压力值P1与给定的P值偏差很小。
奥鹏教育油田化学答案DOC

奥鹏教育远程油田化学答案第一次作业单选题 (共11道题)1.(2.5分)知道表面活性剂的HLB值,就可以大致估计该表面活性剂的用途。
HLB值在1~3时,可用作下列哪种?A∙A、消泡剂∙B、油包水型乳化剂∙C、润湿剂∙D、增溶剂2.(2.5分)质量分数法确定HLB值时,适用于哪种表面活性剂?C∙A、阴离子高分子活性剂∙B、阳离子高分子活性剂∙C、非离子高分子活性剂∙D、两性离子高分子活性剂3.(2.5分)蒙脱石的基本结构层属于哪种层型的粘土矿物。
B∙A、1:1∙B、2:1∙C、3:1∙D、4:14.(2.5分)伊利石的基本结构层属于哪种层型的粘土矿物。
B∙A、1:1∙B、2:1∙C、3:1∙D、4:15.(2.5分)阳离子交换容量是指1kg粘土矿物在哪种pH条件下被交换下来的阳离子总量。
B∙A、pH=6∙B、pH=7∙C、pH=8∙D、pH=96.(2.5分)油包水型乳化剂的HLB值在什么范围内?B∙A、1~3∙B、3~6∙C、5~7∙D、8~107.(2.5分)水包油型乳化剂的HLB值在什么范围内?D∙A、1~3∙B、3~6∙C、5~7∙D、8~108.(2.5分)以30%司盘一80(HLB值为4.3)和70%吐温一80(HLB值为15)混合使用,求该混合乳化剂的HLB值。
A∙A、11.79∙B、12.45∙C、12.77∙D、13.119.(2.5分)高分子化合物是指分子量大于多少的化合物。
D∙A、1000∙B、1500∙C、5000∙D、1000010.(2.5分)下列说法错误的是D∙A、少量存在就能降低水的表面张力的物质称为表面活性剂。
∙B、引起液体表面自动收缩的单位长度上的力称之为表面张力。
∙C、表面活性剂分子结构由亲油基和亲水基两部分结成。
∙D、阴离子表面活性剂在水中电离,起活性作用的部分为阳离子。
11.(2.5分)浊点法鉴别表面活性剂类型是哪种活性剂的特性?C∙A、阴离子高分子活性剂∙B、阳离子高分子活性剂∙C、非离子高分子活性剂∙D、两性离子高分子活性剂多选题 (共14道题)12.(2.5分)高分子表面活性剂包括以下哪几类ABCD∙A、阴离子高分子活性剂∙B、阳离子高分子活性剂∙C、非离子高分子活性剂∙D、两性离子高分子活性剂13.(2.5分)用基数法确定HLB值时,适合与哪种表面活性剂?AC∙A、阴离子高分子活性剂∙B、阳离子高分子活性剂∙C、非离子高分子活性剂∙D、两性离子高分子活性剂14.(2.5分)按合成高分子材料的性质、用途分,高分子化合物可分为:ABC∙A、塑料∙B、合成橡胶∙C、合成纤维∙D、元素高聚物15.(2.5分)下列说法正确的是ABCD∙A、加聚反应指单体加成而聚合起来的反应。
中国石油大学远程教育_(74925)《普通化学》第二阶段在线作业(自测)试卷

试题1.第1题单选题向0.1 mol·dm-3的氨水溶液中加入NH4Cl固体,使溶液中NH4Cl浓度为0.18 mol·dm-3。
已知:K(HAc) = 1.76×10-5,则溶液的pH值为()A、13B、5C、6D、9标准答案:D您的答案:题目分数:5此题得分:0.0批注:2.第2题单选题某元素的价电子结构为3d24s2,则该元素位于周期表中()A、四周期、ⅥA、s区B、四周期、ⅥB、s区C、四周期、ⅣB、d区D、四周期、ⅣA、d区标准答案:C您的答案:题目分数:5此题得分:0.0批注:3.第3题单选题决定多电子原子核外电子运动能量高低的两个主要因素是()A、电子层和电子的自旋状态B、电子云的形状和伸展方向C、电子层和电子亚层D、电子云的形状和电子的自旋状态标准答案:C您的答案:题目分数:5此题得分:0.0批注:4.第4题单选题AgCl在下列体系中溶解度最小的是()。
A、纯水B、0.1 mol·dm-3NH3·H2OC、0.1 mol·dm-3BaCl2D、0.1 mol·dm-3AgNO3标准答案:C您的答案:题目分数:5此题得分:0.0批注:5.第5题单选题在标准Cu电极和标准Zn电极组成的原电池中,如想使电动势增加,则采取()A、增大Zn2 浓度B、减小Cu2 浓度C、向Cu2 溶液中加氨水D、向Zn2 溶液中加氨水标准答案:D您的答案:题目分数:5此题得分:0.0批注:6.第6题单选题在某温度时,CaF2饱和溶液的浓度为2×10-4mol·dm-3,则CaF2的溶度积为()A、2.6×10-9B、4×10-8C、3.2×10-11D、8×10-12标准答案:C您的答案:题目分数:5此题得分:0.0批注:7.第7题单选题若某反应在一定条件时,反应商Q=1,则此时下列等式成立的是()A、ΔG=0B、C、D、标准答案:D您的答案:此题得分:0.0批注:8.第8题单选题下列离子中外层d轨道达到半充满状态的是()A、Cr3B、Fe3C、Co3D、Cu标准答案:B您的答案:题目分数:5此题得分:0.0批注:9.第9题单选题在下列氧化剂中,其氧化性强弱与c(H )无关的是()。
2014年北京石油大学普通化学第一阶段作业答案

第1题对于反应PCl5(g) ═PCl3(g) + Cl2 (g),恒压条件下升高温度,会增大PCl5的分解率。
则判断该反应为______。
您的答案:A题目分数:0.5此题得分:0.5批注:温度对化学平衡的影响第2题在刚性密闭容器中,有下列理想气体的反应达到平衡:A(g)+B(g)=C(g) ,若在恒温下加入一定量的惰性气体,则平衡将。
您的答案:C题目分数:0.5此题得分:0.5批注:总压对化学平衡的影响第3题如果体系经过一系列变化后,又回到初始终态,则体系的。
您的答案:C题目分数:0.5此题得分:0.5批注:热力学第一定律和状态函数的性质第4题H2的燃烧焓等于。
您的答案:A题目分数:0.5此题得分:0.5批注:燃烧焓的定义第5题下列反应中表达式正确的是。
您的答案:A题目分数:0.5此题得分:0.5批注:生成焓和燃烧焓的定义第6题已知反应2NH3=N2+3H2 在等温条件下,标准平衡常数为0.25,那么,在此条件下,氨的合成反应0.5N2+1.5H2=NH3的标准平衡常数为。
您的答案:D题目分数:0.5此题得分:0.5批注:多重平衡规则第7题理想气体化学反应A(g)=C(g)+D(g),在恒温下增大总压时(改变体积),反应物转化率。
您的答案:B题目分数:0.5此题得分:0.5批注:总压对化学平衡的影响第8题下列叙述不正确的是。
您的答案:C题目分数:0.5此题得分:0.5批注:平衡移动原理第9题关于功W符号的判断,下列说法是准确的。
您的答案:B题目分数:0.5此题得分:0.5批注:功符号的规定第10题等容热效应Qv的大小只与有关。
您的答案:C题目分数:0.5此题得分:0.5批注:Qv和内能的关系第11题某反应在一定条件下转化率为25%,当有催化剂存在时,其平衡转化率25%。
您的答案:B题目分数:0.5此题得分:0.5批注:催化剂的特性第12题催化剂能加快反应速率主要是因为反应活化能。
您的答案:B题目分数:0.5此题得分:0.5批注:催化剂的特性第13题催化剂加入使反应的热效应。
普通二化学2013-2014学年度第二学期期中考试化学试题及答案测试
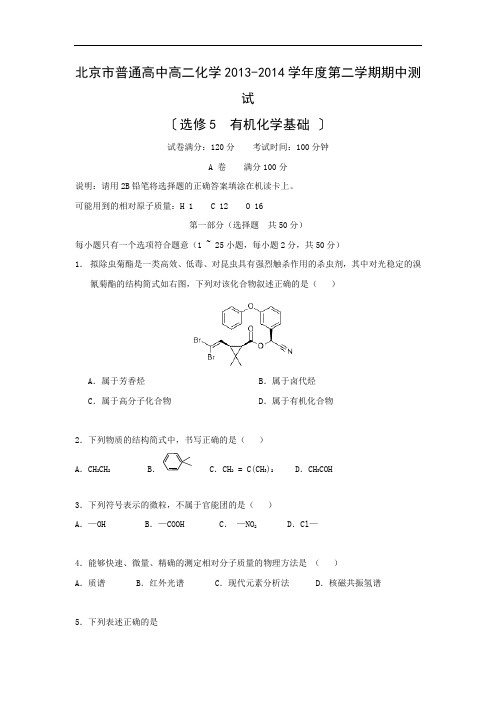
北京市普通高中高二化学2013-2014学年度第二学期期中测试〔选修5 有机化学基础〕试卷满分:120分考试时间:100分钟A 卷满分100分说明:请用2B铅笔将选择题的正确答案填涂在机读卡上。
可能用到的相对原子质量:H 1 C 12 O 16第一部分(选择题共50分)每小题只有一个选项符合题意(1 ~ 25小题,每小题2分,共50分)1.拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如右图,下列对该化合物叙述正确的是()A.属于芳香烃 B.属于卤代烃C.属于高分子化合物 D.属于有机化合物2.下列物质的结构简式中,书写正确的是()A.CH2CH2 B. C.CH2 = C(CH3)2 D.CH3COH3.下列符号表示的微粒,不属于官能团的是()A.—OH B.—COOH C.—NO2 D.Cl—4.能够快速、微量、精确的测定相对分子质量的物理方法是()A.质谱 B.红外光谱 C.现代元素分析法 D.核磁共振氢谱5.下列表述正确的是A.醛基的结构简式—COH B.聚丙烯的结构简式C.四氯化碳分子的电子式 D.丙烷分子的球棍模型6.下列物质可用重结晶法提纯的是()A.含杂质的工业酒精 B.含杂质的粗苯甲酸C.从溴水中提纯溴 D.苯中混有少量苯酚7.下列有机化合物分子中,所有碳原子不可能处于同一平面的是()8.下列各组物质中,互为同系物的是A.乙醇、乙二醇、丙三醇 B.苯、甲苯、二甲苯C.一氯甲烷、氯苯、氯乙烯 D.乙烷、乙烯、乙炔9.下列有机物的系统命名中正确的是()A.3-甲基-4-乙基戊烷 B.3,3,4-三甲基己烷C.3,4,4-三甲基己烷 D.3,5-二甲基己烷10.下列物质沸点的比较,正确的是()A.乙烷>丙烷 B.正戊烷>异戊烷C.丙烷>乙醇 D.乙醇>乙二醇11.在乙醇发生的各种反应中,断键方式不正确的是()A .与金属钠反应时,键①断裂B .与醋酸、浓硫酸共热时,键②断裂C .与浓硫酸共热至170℃时,键②和④断裂D .与HCl 反应生成氯乙烷时,键②断裂12.下列反应中,属于加成反应的是( )A .甲烷与氯气反应制取一氯甲烷B .乙酸与乙醇反应制取乙酸乙酯C .苯酚与饱和溴水反应生成三溴苯酚D .乙烯与氯化氢反应制取氯乙烷13.某单烯烃与H2加成后的产物是 则该烯烃的结构式可能有多少种( )A .1B .2C .3D .414.为检验某卤代烃中的卤元素,进行如下操作,正确的顺序是( )①加热 ②加入AgNO3溶液 ③取少量该卤化物 ④加入足量稀硝酸酸化⑤加入NaOH 溶液 ⑥冷却A .③①⑤⑥②④B .③⑤①⑥④②C .③②①⑥④⑤D .③⑤①⑥②④15.下列分子式只表示一种纯净物的是( )A .C 3H 6B .C C .C 4H 10D .CH 2Br 216.下列物质中,既能发生消去反应生成烯烃,又能氧化成醛的是( )A .B .C .D . CH 3CH CH 3CH 2OHCH 3OH CH 3C CH 3CH 3CH 3CH 2CH CH 3OH17.3-甲基戊烷的一氯代物有()A.3种 B.4种 C.5种 D.6种18.下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是()A.CH3CH2CH3 B.CH3 CH2CO CH2CH3C.CH3OCH3 D.CH3CH2OH19.某有机物完全燃烧只生成CO2和H2O,两者的物质的量之比为2∶3,可以说()A.该有机物中含C、H、O三种原子B.该化合物是乙烷C.该化合物中C、H原子个数比为1∶3D.该化合物中含2个C原子、6个H原子,但一定不含有O原子20.下列各组物质在一定条件下反应,可以制得较纯净的1,2-二氯乙烷的是()A.乙烷和氯气混合 B.乙烯的氯化氢混合C.乙烯和氯气混合 D.乙烯通入浓盐酸21.只用一种试剂鉴别正己烷、1-己烯、乙醇、苯酚水溶液4种无色液体,应选用()A.酸性KMnO4溶液 B.饱和溴水 C.NaOH溶液 D.AgNO3溶液22.下列物质中,互为同分异构体的是A.①② B.①⑤ C.①④ D.①③④23.下列说法中,正确的是()A .醛类催化加氢后都得到饱和一元醇B .甲醛、乙醛、丙醛都没有同分异构体C .将2%的稀氨水逐滴加入2%的AgNO 3溶液中,至沉淀恰好溶解为止,可制得银氨溶液D .将2%的NaOH 溶液4~6滴,滴入2mL 10%的CuSO 4溶液中制得Cu(OH)2悬浊液,用作检验醛基的试剂24.从柑桔中炼制萜二烯,下列的有关它的推测,不正确的是( )A .分子式为C 10H 16B .常温下为液态,难溶于水C .它不能使酸性高锰酸钾溶液褪色D .与过量的溴的四氯化碳溶液反应后产物为25.将用于2008年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE ,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成全氟乙丙烯。
完整word版2016中国石油大学北京化工热力学第二阶段在线作业

第二阶段在线作业共道题18)单选题 (收起T、P)经节流膨胀后,流体的温度1.(2.5分)流体(11 ?、不变A?不能有两个以上的数值内能只能有一数值, B、对应于某一状态,?内能也一定跟着变化C、状态发生变化,?的关系为和U分)对于一均匀的物质,其H3.(2.5?li=\>H<u< A、?UH> B、:对于同样的气体压缩终态和始态2.5分)4.(?、等温压缩过程所需要的压缩功小于绝热压缩过程A?、等温压缩过程所需要的压缩功大于绝热压缩过程B?、等温压缩过程所需要的压缩功等于绝热压缩过程C5.(2.5分)蒸汽经过不可逆绝热透平膨胀后?△S=0A、?△H=0、B?△G=0C 、)来定义的.6.(2.5分)纯物质的偏心因子是根据(?、分子的对称性A?、蒸汽压的性质B?、分子的极性 C21环的热效率。
?、前者大于后者A?、两者相等B?、前者小于后者 C?)的条件下,等熵膨胀与节流膨胀两种方案相比,)和膨胀压力(P 分)在相同的初态(T ,P8.(2.500 哪种方案的降温大??、前者 A:?方程能同时应用于汽、液两相计算,准确度较高R -K B 、?1也可小于、活度系数可以大于1 C10.(2.5分) 经历一个实际热机的循环过程,体系工质的熵变?0> A 、?0、< B(2.5分) 以下措施中既能提高蒸汽朗肯循环的热效率,又提高汽轮机出口乏气的干度的是11. ?、提高汽轮机进汽温度A?、提高汽轮机进汽压力B?、提高汽轮机乏汽压力 C高压氮气从同一始态出发,分别经历两个不同的膨胀过程达相同的终态。
其中已知一个可(2.5分)12.(kg.K)。
),另一个不可逆过程的工质熵变逆过程的工质熵变为20KJ/(kg.K KJ/?20、大于A?20、小于B?20、等于C?13.(2.5分)冬天要给-10℃房间供热取暖,消耗500W的功率给房间供热,采用可逆热泵循环、电热器两种供热方式,哪种供热方式的供热量多?、前者A分)14.2.5(?.A、D我的答案:分2.5此题得分:C15.(2.5分)?.、A?D我的答案:分2.5此题得分:D 分)16.2.5(?.A、D我的答案:分2.5此题得分:C 17.(2.5分)?.、A?D我的答案:分2.5此题得分:A (2.5分)18.?.A、C?.、D我的答案:D 此题得分:2.5分多选题 (共7道题)收起19.(2.5分)非理想气体的熵与什么有关??、温度A?、压力B?、体积C?、偏心因子D我的答案:ABCD 此题得分:2.5分20.(2.5分)对于dG=-SdT+Vdp等热力学基本方程,说法错误的是?、只能用于气体,不能用于液体或固相A?、只能用于可逆过程,不能用于不可逆过程B?、既可用于可逆过程,又可用于不可逆过程C?:任何过程的发生和进行必定要符合2.5分)21.(?、热力学第一定律A?、热力学第二定律B?、热力学第三定律C?定律、Raoult D下列哪些热力学性质无法直接测量分)22.(2.5?HA、?TB、?S、C流体经过节流膨胀后2.5(分)23.?、压力减小A ?、温度降低B?、熵增加C?、焓减小D24.(2.5分)理想气体的节流膨胀过程?△H=0A、?△H>0、B2.525.(分)?.A 、?.B、?.C、?.、D我的答案:ACD 此题得分:2.5分判断题 (共15道题)收起26.(2.5分)对于一个绝热不可逆过程,其熵变可以设计一个可逆过程来计算。
石油大学远程教育 必修课 化学反应工程 在线作业二

石油大学远程教育必修课化学反应工程第二阶段在线作业单选题(共8道题)收起1.(2.5分)答题要求:1.严禁抄袭、雷同,一经发现,成绩为0;2.如果题目要求“结合自己的理解”、“结合自己的观点”等字样,一定要有自己观点的阐述,否则不及格。
"按钮上传作业文件!下列参数中,_______能够判断出转化率的大小。
A、DamkÖhler准数B、Thiele模数C、Mears准数D、Weisz-Prater准数我的答案:A 此题得分:2.5分2.(2.5分)答题要求:1.严禁抄袭、雷同,一经发现,成绩为0;2.如果题目要求“结合自己的理解”、“结合自己的观点”等字样,一定要有自己观点的阐述,否则不及格。
"按钮上传作业文件!对于在多个CSTR进行的一级反应,DamkÖhler准数为_______,则串联所需的反应器个数越多。
A、0.1B、0.5C、1D、2我的答案:A 此题得分:2.5分3.(2.5分)答题要求:1.严禁抄袭、雷同,一经发现,成绩为0;2.如果题目要求“结合自己的理解”、“结合自己的观点”等字样,一定要有自己观点的阐述,否则不及格。
"按钮上传作业文件!下列属于均相反应的是_______。
A、煤炭燃烧B、氢气燃烧C、离子交换D、石油裂解我的答案:B 此题得分:2.5分4.(2.5分)答题要求:1.严禁抄袭、雷同,一经发现,成绩为0;2.如果题目要求“结合自己的理解”、“结合自己的观点”等字样,一定要有自己观点的阐述,否则不及格。
"按钮上传作业文件!下列属于非均相反应的是_______。
A、乙酸乙酯水解B、氢气燃烧C、HCL和NaOH中和D、石油裂解我的答案:D 此题得分:2.5分5.(2.5分)答题要求:1.严禁抄袭、雷同,一经发现,成绩为0;2.如果题目要求“结合自己的理解”、“结合自己的观点”等字样,一定要有自己观点的阐述,否则不及格。
2014年秋季第二阶段考试高二化学试题含答案(鲁科版选修四)

鸿图中学2014年秋第二阶段考试高二化学(理科)试题考试范围:《化学反应原理》第1~2章考试时间:90分钟满分:100分可能用到的相对原子质量:H:1 O:16 Fe:56 Cu:64一、选择题(每小题只有一个正确选项,每小题2分,共46分)1.下列说法中正确的是()A.在化学反应过程中,发生物质变化的同时不一定发生能量变化B.ΔH >0表示放热反应,ΔH <0表示吸热反应C.ΔH的大小与热化学方程式中的计量数无关D.反应产物的总焓大于反应物的总焓时,ΔH >02.已知反应A+3B2C+D在某段时间内以A的浓度变化表示的化学反应速率为1.0mol·L-1·min-1,则此段时间内以C的浓度变化表示的化学反应速率为()A.0.5mol·L-1·min-1 B. 1.0mol·L-1·min-1C.2.0mol·L-1·min-1 D. 3.0mol·L-1·min-13. 在2A + B 3C + 4D 反应中,表示该反应速率最大的是()A. v(A)=0.5 mol/(L·s)B. v(B)=0.3 mol/(L·s)C. v(C)=0.8 mol/(L·s)D. v(D)=1 mol/(L·s)4. 某温度下,反应SO2(g)+ (1/2) O2(g) SO3 (g) 的平衡常数K1=50,在同一温度下,反应SO3(g) SO2(g) + (1/2)O2(g)的平衡常数K2的值为()A.2500 B. 100 C. 0.02 D. 0.0015.下列关于电解法精炼粗铜的叙述中不正确的是()A.粗铜板作阳极,纯铜片作阴极,CuSO4溶液作电解液B.电解时,阳极发生氧化反应,而阴极发生的反应为:Cu2++2e-CuC.粗铜中所含Ni、Fe、Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥D.电解铜的纯度可达99.95% ~99.98%6.根据反应:2Ag++Cu = Cu2++2Ag,设计如图所示的原电池,下列说法错误的是()A.X可以是银或石墨B.Y是硫酸铜溶液C.电子从铜电极经外电路流向X电极D.X极上的电极反应式为:Ag++e- = Ag 7. 用铂电极电解下列溶液,阴极和阳极上的主要产物分别为H2和O2的是()A.稀NaOH溶液B.HCl溶液C.CuSO4溶液D.AgNO3溶液8. 在合成氨工业中,为增加NH3的日产量,下列措施中与平衡移动无关的是()A. 不断将氨分离出来B. 使用催化剂C. 采用500℃左右的高温D. 采用2×107~5×107Pa的压强9. 在密闭容器中进行如下反应:H2(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如图所示。
中国石油大学远程教育_(74925)《普通化学》第二阶段在线作业(自测)试卷

B、减小Cu2浓度
C、向Cu2溶液中加氨水
D、向Zn2溶液中加氨水
标准答案:D
您的答案:
题目分数:5
此题得分:0.0
批注:
6.第6题单选题在某温度时,CaF2饱和溶液的浓度为2×10-4mol·dm-3,则CaF2的溶度积为()
A、2.6×10-9
B、4×10-8
C、3.2×10-11
标准答案:C
您的答案:
题目分数:5
此题得分:0.0
批注:
4.第4题单选题AgCl在下列体系中溶解度最小的是()。
A、纯水
B、0.1 mol·dm-3NH3·H2O
C、0.1 mol·dm-3BaCl2
D、0.1 mol:5
此题得分:0.0
批注:
5.第5题单选题在标准Cu电极和标准Zn电极组成的原电池中,如想使电动势增加,则采取()
试卷总批注:
标准答案:正确
您的答案:
题目分数:5
此题得分:0.0
批注:
15.第15题判断题主族元素的原子半径随原子序数的递增呈现周期性变化,同一周期从左到右逐渐减小,同一主族从上到下逐渐增大。
标准答案:正确
您的答案:
题目分数:5
此题得分:0.0
批注:
16.第16题判断题同一能级组中的原子轨道都是等价轨道。
标准答案:错误
您的答案:
题目分数:5
此题得分:0.0
批注:
17.第17题判断题一定温度下,AgCl水溶液中,Ag与Cl-浓度的乘积是一个常数。
标准答案:错误
您的答案:
题目分数:5
此题得分:0.0
批注:
18.第18题判断题原电池工作时,体系的DG增大,而电动势E减小。
2014高考全国理综化学II卷[附答案解析]
![2014高考全国理综化学II卷[附答案解析]](https://img.taocdn.com/s3/m/121ce479ec3a87c24128c40b.png)
. .WORD.格式整理. ^2021年高考全国理综化学II 卷可能用到的相对原子质量: H 1 C 12 N 14 O 16 F 19 Na 23 Al 27 S 32 Cl 35.5 K 39 Ca 40 Cr 52Fe 56 Ni 59 Cu 64 Zn 65一、选择题:此题共 7小题,每题6分.在每题给出的四个选项中,只有一项为哪一项符合题目要求的.7.在一定条件下,动植物油脂与醇反响可制备生物柴油,化学方程式如下:B.苯乙烯在适宜条件下催化加氢可生成乙基环己烷C.乙烯和澳的四氯化碳溶液反响生成 1, 2—二澳乙烷D.甲苯与氯气在光照下反响主要生成2, 4—二氯甲苯9. N 0为阿伏伽德罗常数的值.以下表达正确的选项是 A. 1.0L1.0mol• L -1的NaAl .水溶液中含有的氧原子数为2N 0B. 12g 石墨烯(单层石墨)中含有六元环的个数0.5N .C. 25 c 时pH= 13的NaOH§液中含有 OH 的数目为0.1N .D. 1mol 的羟基与1mol 的氢氧根离子所含电子数均为 9N b10. 能正确表不以下反响的离子方程式 A. 浓盐酸与铁屑反响:2Fe + 6H + = 2Fe 3+ + 3H 2 T B. 钠与 CuSO 溶液反响:2Na + Cu 2+ = Cu J + 2Na +C. NaHCO 3 溶液与稀 HaSQ 反响:CQ 2 + 2H + = H 2O + CO 2 TD.向 FeCl 3溶液中参加 Mg(OH>: 3Mg(OH> + 2Fe 3+ = 2Fe(OH) 3 + 3Mg 2+11. “ZEBRA 蓄电池的结构如下图,电极材料多孔 Ni/NiCl 2和金属钠之间由钠离子导体制作的陶瓷管相隔.以下关于该电池的表达错误..的是A.电池反响中有NaCl 生成B.电池的总反响是金属钠复原三价铝离子C.正极反响为:NiCl 2 + 2e = Ni + 2ClD.钠离子通过钠离子导体在两电极间移动.专业.知识.分享.OHCOUCOBCOHC ouconc生物柴油CH j OH ICH-OH ICH 广 OH 甘以下表达错误.的是A. 生物柴油由可再生资源制得 C.动植物油脂是高分子化合物8.以下表达中,错俣.的是A.苯与浓硝酸、浓硫酸共热并保持B. 生物柴油是不同酯组成的混合物 D.“地沟油〞可用于制备生物柴油55〜60 c 反响生成硝基苯 NIAIC .妥孔Ni/NiC1a龄离于学体液体命属幡C.分〕正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反响如下:工机0】0了CH J CH J CH J CI^OH -------- ——► CHCHKHKHOH 3SO 4 A反响物和产物的相关数据列表如下:沸点/ c密度/g - cm 3水中溶解性 止」醇 117.2 0.8109 微溶 止」醛75.70.8017微溶实验步骤如下:将6.0gNa 2Cr 2O 放入100mL 烧杯中,加30mL 水溶解,再缓慢参加5mL 浓硫酸,将所得溶液小心转移至 B 中.在A 中参加4.0g 正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加 B 中溶液.滴加过程中保持反响温度为90〜95 C,在E 中收集90c 以上的微分...专业.知识.分享.^..WORD.格式整理. 12.在1200时,天然气脱硫工艺中会发生以下反响: H 2s(g) + 3/2O 2(g) = SO 2(g) + H 2O(g) AHi2H 2s(g) + SO 2(g) = 3/2S 乂g) + 2H 2O(g)△ H 2H 2s(g) +1/2O 2(g) = S(g) + H 2O(g) AH^ 2S(g) = S 2(g)△ H那么4 H 的正确表达式为A. = 2/3( AH. + AH 2 - 3 △H)B.△ H4 = 2/3(3 △ H J - AHi - △■) C. = 3/2( AH. + AH 2 - 3 △H) D.△ H4 = 3/2( AHi - AHa - 3 AH s )13. 室温时,M(OH )(s) = M 2+(aq) + 2OH (aq) K sp = aC (M 2+) = b mol • L -1时,溶液的pH 等于A J'IB.D.26. (15.WORD.格式整理. ^将储出物倒入分液漏斗中,分去水层,有机层枯燥后蒸储,收集 75〜77c 微分,产量2.0g .答复以下问题:(1)实验中,能否将 NaCrzQ 溶液加到浓硫酸中,说明理由 .(2)参加沸石的作用是,假设加热后发现未参加沸石,应采取的正确方法 (3)上述装置图中,B 仪器的名称是 , D 仪器的名称是(4)分液漏斗使用前必须进行的操作是 (填正确答案标号). a. 润湿 b. 枯燥 c. 检漏 d. 标定(5)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上〞或“下〞). (6)反响温度应保持在 90〜95 C,其原因是 . (7)本实验中,正丁醛的产率为 %.27. (14分)氧化锌为白色粉末, 可用于湿疹、癣等皮肤病的治疗. 纯化工业级氧化锌(含有Fe(II) 、Mn(II)、Ni(II)等杂质)的流程如下:工八.嗫浸蹄葛骤枭 ②提示:在本实验条件下, Ni(II)不能被氧化;高镒酸钾的复原产物是 MnO .答复以下问题:(1)反响②中除掉的杂质离子是 ,发生反响的离子方程式为;在加高镒酸钾溶液前,假设 pH 较低,对除杂的影响(2)反响③的反响类型为 ,过滤得到的滤渣中,除了过量的锌外还有 . (3)反响④形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是 .(4)反响④中产物的成分可能是 ZnCO • xZn(OH 〞.取枯燥后的滤饼11.2g ,锻烧后可得到产品 8.1g ,那么x 等于.反响时间(t )与容器内气体总压强(p )的数据见下表:答复以下问题:.专业.知识.分享.28.(14分)在1.0L 密闭容器中放入 A(g)—B(g) + C(g ) 0.10molA(g),在一定温度进行如下反响:-1△ H =+85.1kJ • mol.WORD.格式整理.(1)欲提升A 的平衡转化率,应采取的举措为(2)由总压强p 和起始压强P 0计算反响物A 的转化率a (A)的表达式为, 平衡时A 的转化率为,列式并计算反响的平衡常数K .(3)①由总压强 p和起始压强 p o 表示反响体系的总物质的量 n 总和反响物 A 的物质的量 n (A) , n 总=mol, n (A) =mol .②下表为反响物 A 浓度与反响时间的数据,计算:a =.反响时间t/h 0 4 8 16 c (A)/(mol - L -1)0.10a0.0260.0065分析该反响中反响物的浓度 C (A)变化与时间间隔(A t )的规律,得出的结论是由此规律推出反响在 12h 时反响物的浓度 c (A)为 mol •L -1.36.〔化学一一选修 2:化学与技术〕(15分)锌镒电池(俗称干电池)在生活中的用量很大.两种锌镒电池的构造如图(a)所示.一破修普通伴智电池图两种干电池的结构示意图答复以下问题:(1)普通锌镒电池放电时发生的主要反响为: Zn + 2NH4Cl + 2MnO 2 = Zn(NH 3)Z C1 2 + 2MnOOH①该电池中,负极材料主要是 ,电解质的主要成分是 ,正极发生的主要反响_________________________________________________________________________________________________________________________________________________________________________________________ O②与普通锌镒电池相比,碱性锌镒电池的优点及其理由是 .(2)图(b)表示回收利用废旧普通锌镒电池工艺(不考虑废旧电池中实际存在的少量其他金属) ..专业.知识.分享.-二氧化隹糊毒化技制伴的金属外壳L 锌粉和狙氧化伴~的混合物—二氧化候医旧桂售电池机械别离ii m KCOs- KOH,焙融始块b.溶廨.通CO 〞过海化合物A 化合物B 化合物C 化合物D①图〔b 〕中产物的化学式分别为 KdMnQ 操彳b 中,绿色的K a MnO 溶液反响生成紫色溶液和一种黑褐色固体,该反响的离子方程式为 .③采用惰性电极电解 KMnO 溶液也能得到化合物 D,那么阴极处 得到的主要物质是_________________ 〔填化学式〕.37 .〔化学一一选修 3:物质结构与性质〕〔15分〕前四周期原子序数依次增大的元素 A 、B 、C 、D 中,A 和B 的价电子层中未成对电子均只有一个,并且A 和B +的电子数相差为8;与B 位于同一周期的 C 和D,它们价电子层中的未成对电子数分别 为4和2,且原子序数相差为 2.答复以下问题:(1) 炉的价层电子排布图为 .(2) 四种元素中第一电离能最小的是 , 电负性最大的是 .〔填元素符号〕(3) A 、B 和D 三种元素组成的一个化合物的晶胞如下图.①该化合物的化学式为 ; D 的配位数为3②列式计算该晶体的留度 g - cm .溶解.法缩结晶;令却酒液浓缩结晶(b>一种回收利用废旧普通锌桂电池的工艺.WORD.格式整理.稀裾酸 黑色固体混合物水浸、过滤锌.铜.碟棒等 I 分类回收〕浓缩结晶, itae固体国体OAOB •D②操作a 中得到熔块的主要成分是灼烧固体—400pm ―叱.专业.知识.分享.. .WORD.格式整理. ^(4)'、B +和C 3+三种离子组成的化合物的 RCA,其中化学键的类型有 ;该化合物中存在一个复杂离子,该离子的化学式为 , 配位体是.38 .[化学一一选修5:有机化学根底〕(15分)化合物I(C 11H2Q )是制备液晶材料的中间体之一,其分子中含有醛基和酯基. I 可以用E 和H 在一定条件下合成:以下信息:①A 的核磁共振氢谱说明其只有一种化学环境的氢;③化合物F 苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成厥基. 答复以下问题:(1) A 的化学名称为 . (2) D 的结构简式为 . (3) E 的分子式为.(4) F 生成G 的化学方程式为 ,该反响类型为 . (5) I 的结构简式为 .(6) I 的同系物J 比I 相对分子质量小14, J 的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反响,又能与饱和NaHCO§液反响放出CO,共有 种(不考虑立体异构).J 的一个同分异构体发生银镜反响并酸化后核磁共振氢谱为三组峰, 且峰面积比为2 : 2 : 1 ,写出J 的这种同分异构体的结构简式 ..专业.知识.分享.R-CH=CH. ①巳2Hg '®H :OyOHf R CHCHOH ■-' 一 i ・一■(1)升高温度、降低压强(2) (£-0*100% 94.1%%A(g) / B(g)OJO 0030x(1-941%) 0J0 K 94.1%-ML』…t 0.0059 mol V1(3)①.4Ox 二.:;OxQ-/-)Po P.② 0.051 到达平衡前每间隔4h, c(A)减少约一半.专业.知识.分享.〔2分〕〔每空I分,共2分〉弥00.10x911%〔3分〕〔每空】分,共2分〕〔2分〕〔2分〕.WORD.格式整理.2021年高考全国理综化学II卷参考答案第I卷一、选择题7.C 8.D 9.B 10.D 11.B 12.A 13.C第II卷26.(15 分)(1)不能,易迸溅(2)预防暴沸冷却后补加(3)分液漏斗直形冷凝管(4) C(5)下(6)既可保证正丁醛及时蒸出,又可尽量预防其被进一步氧化⑺5127.(14 分)(1)Fe2+和MrTMnO 4 + 3Fe 2+ + 7H2O = 3Fe(OH) 3 J + MnQ J + 5H +2 MnO 4 + 3Mn 2+ + 2H2O = 5MnQ J + 4H +铁离子和镒离子不能生成沉淀,从而无法除去铁和镒杂质〔2〕置换反响馍〔2分〕〔每空1分,共2分〕〔每空1分,共2分〕〔2分〕〔2分〕〔2分〕〔2分〕〔2分〕〔2分〕〔2分〕〔2分〕〔每空1分,共2分〕〔3〕取少量水洗夜于试管中,滴入1〜2滴稀硝酸,再滴入硝酸钢溶液,假设无白色沉淀生成,那么说明沉淀已经洗涤干净(2分)(4) 1(2分)28. (14 分). .WORD.格式整理.0.013 36.〔化学一一选修2:化学与技术〕(15分)(1)① Zn NH^CIMnO 3 + NH ; +e' = MnOOH + NH,碱性电池使用寿命较长.由于金属材料在碱性电解质中比在酸性电解成中 的稳定性提升.〔答对一条即可,其他合理答案也给分〕 〔2分〕 ①ZnC" NH4CI 〔每空2分,共4分〕〔2分〕〔2分〕〔每空2分,共4分〕 〔2分, I 分•共3分〕〈2分〕C2分,I 分, 1分,共4分〕.专业.知识.分享.② 麒性电池不易发生电解质的泄 由于消耗的负极改装在电池的内部:〔1分〕〔每空I 分,共2分〕〔2〕3MnO ;_ + 2CO : 2MnO/ + MnO 21+2CO ;-〔3分〕 ③—37.〔化学一一选修3:物质结构与性质〕〔15分〕3d⑵K F (3)① KjNiF. 6否 39x4+59x2 + 19x8, 3 --------------------------- = 3/6.02x1^x40(^x008x10(4)离子键.配位键便叫「 f38.[化学一一选修5:有机化学根底〕(15分).WORD.格式整理.根据企业开展战略的要求,有方案地对人力、资源进行合理配置,通过对企业中员工的招聘、培训、使用、考核、评价、鼓励、调整等一系列过程,调发动工地积极性,发挥员工地潜能,为企业创造价值,保证企业战略目标的实现. 读书是一种感悟人生的艺术读杜甫的诗使人感悟人生的辛酸,读李白的诗使人领悟官场的腐败,读鲁迅的文章使人认清社会的黑暗,读巴金的文章使人感到未来的希望每一本书都是一个朋友,教会我们如何去看待人生读书是人生的一 门最不缺少的功课,阅读书籍,感悟人生,助我们走好人生的每一步.专业.知识.分享.〔1〕工-甲基2氯丙烷〔或叔丁基氯〕M 9 CH-C-H H 3CC 4H (O 20 IICHj-CH-C'O CHjCH 2CHO取代反响〔2分〕?2分〕<1分〕12分.】分,共3分〕〔2分〕〔4分.1分,共5分〕(5) ⑹18 HOOCHjC+ 2HCI。
中石油《普通化学》2020年秋季学期在线作业(二)

一、判断题共20题,100分15分状态函数的变化值只取决于体系的始终态,而与变化的途径无关。
A错误B正确我的得分:5分我的答案:B解析:暂无内容25分对于某电极,如果有H+或OH- 参加反应,则溶液的pH值改变将使其电极电势也发生改变。
A错误B正确我的得分:5分我的答案:B解析:暂无内容35分中心离子的配位数为四的配离子,其结构都是四面体型。
A错误B正确我的得分:5分我的答案:A解析:暂无内容45分升高温度,使吸热反应的反应速率增大,放热反应的反应速率减小。
A错误B正确我的得分:5分我的答案:A解析:暂无内容55分配合物中,配位数就是与中心离子结合的配位体的个数。
A错误B正确我的得分:5分我的答案:A解析:暂无内容65分在NaCl晶体中不存在NaCl分子。
A错误B正确我的得分:5分我的答案:A解析:暂无内容75分Fe (s)和Cl2 (l)的ΔfHӨ都为零。
A错误B正确我的得分:5分我的答案:A解析:暂无内容85分在氧化还原反应中,失电子的物质叫做还原剂,它使另一种物质还原,本身被氧化;得电子的物质叫做氧化剂,它使另一种物质氧化,本身被还原。
A错误B正确我的得分:5分我的答案:B解析:暂无内容95分主量子数n 为3 时有3s,3p,3d,3f 四条轨道。
东大14秋学期《普通化学》在线作业2答案

B. 4.82
C. 3.46
D. 2.35
?
正确答案:D
14. NaCl结构是阴离子排成最紧密堆积,阳离子则占据()
A.
所有八面体空穴
B.
所有四面体空穴
C.
二分之一的八面体空穴
D.
四分之一的八面体空穴
?
正确答案:A
15.下列各组物质中,沸点高低次序不正确的是( )
A.
HF>NH
B.
S2(g)>O2
A.
Ag+和Cd2+
B.
Cd2+和Pb2+
C.
Ag+和Pb2+
D.
Pb2+和Sr2+
?
正确答案:C
12.在0.10 L 0.10 mol·L-1 HAc溶液中,加入少量NaAc晶体,溶液的pH值将会()。
A.升高
B.降低
C.不变
D.无法判断
?
正确答案:A
13.等体积混合pH=2.00和pH=11.00的强酸和强碱溶液,所得溶液的pH值为()。
A.
Cu(OH)2
B.
Pb(OH)2
C.
Al(OH)3
D.
AgCl
?
正确答案:A
4.下列电极反应中,离子浓度减小一半,其他条件不变,j值增加的是()。
A.
Cu2++2 e-=Cu
B.
Fe3++e-=Fe2+
C.
2 H++2 e-=H2
D.
I2+2 e-=2 I-
?
正确答案:D
5.下列元素中原子外层电子构型为ns2np5的是()
A. 0
B.
1 J·mol-1·K-1
C.
> 0
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
作业第1题在相同浓度的Pb2+、Ba2+(均为0.1mol/L)的混合溶液中逐滴加入K2CrO4溶液(溶液体积变化忽略不计),先沉淀的物质是。
已知Kspθ(PbCrO4)= 2.8×10-13,Kspθ(BaCrO4)=1.17×10-10。
您的答案:A题目分数:0.5此题得分:0.5批注:分步沉淀第2题利用溶度积规则可以判断沉淀转化的方向,对于反应 2AgCl + CrO42-=Ag2CrO4 + 2Cl-,Kspθ(AgCl)=1.56×10-10,Kspθ( Ag2CrO4 )=9.0×10-12,则标准态下该反应应向方向进行。
您的答案:B题目分数:0.5此题得分:0.5批注:沉淀转化第3题向带有PbCl2沉淀的饱和溶液中加入少量NH4Cl晶体,则PbCl2的溶解度将。
您的答案:B题目分数:0.5此题得分:0.5批注:难溶盐的同离子效应第4题25℃时,Mg(OH)2的K spθ为1.2×10-11,在0.01mol · L-1的NaOH溶液中的溶解度为。
您的答案:C题目分数:0.5此题得分:0.5批注:AB2型溶解度计算第5题将某氧化还原反应组成原电池,下列说法正确的是()您的答案:B题目分数:0.5此题得分:0.5批注:氧化还原反应和原电池第6题对原电池(-)Fe|Fe2+ || Cu2+|Cu (+)随反应的进行,电动势将()您的答案:B题目分数:0.5此题得分:0.5批注:原电池电动势第7题在标准条件下,下列反应均向正方向进行:2Fe3++Sn2+=2Fe2++Sn4+;Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O ,它们中间最强的氧化剂为,最强的还原剂为。
您的答案:A题目分数:0.5此题得分:0.5批注:氧化剂、还原剂的判断:强氧化剂和强还原剂生成弱氧化剂和弱还原剂第8题反应: Zn + 2H+ (x mol·dm-3) = Zn2+(1mol·dm-3) + H2(100kPa) 构成的原电池的电动势为0.46V,Φθ (Zn2+ / Zn ) =-0.76V, 则pH值为。
您的答案:D题目分数:0.5此题得分:0.5批注:电动势的能斯特方程第9题现有原电池(-)Pt | Fe3+,Fe2+ || Ce4+,Ce3+ | Pt (+),则氧化还原反应为。
您的答案:C题目分数:0.5此题得分:0.5批注:根据原电池符号写氧化还原反应第10题反应Ag+(0.01mol/L)+Fe2+(1.0mol/L)=Ag+Fe3+(1.0mol/L)的反应方向是。
已知Φθ (Ag+ / Ag ) =0.799 V,Φθ (Fe3+ / Fe2+ ) =0.771 V您的答案:B题目分数:0.5此题得分:0.5批注:根据氧化还原反应写原电池符号第11题将下列电极反应中有关离子浓度减小一半,而E值增加的是您的答案:C题目分数:0.5此题得分:0.5批注:电极电势的能斯特方程第12题将下列两个反应设计成原电池: Zn + Cd2+= Zn2+ + Cd-----①; 2 Zn+ 2 Cd2+=2 Zn2+ +2 Cd---------② ,两电池标准电动势的关系为,两电池标准电动势的关系为。
您的答案:A题目分数:0.5此题得分:0.5批注:利用吉布斯函数的关系推导第13题已知原电池:(?)Zn| ZnSO4 (1mol·L-1)║CuSO4(1mol·L-1)| Cu (+) ;若增加ZnSO4溶液的浓度,电池电动势;往CuSO4溶液中通入H2S,电池电动势。
您的答案:B题目分数:0.5此题得分:0.5批注:电动势的能斯特方程第14题在298 K下,若使电池(-)Pt | H2(g,p1) | HCl (cmol·L-1) | H2(g,p2) | Pt(+)的电动势为正值,则必须使_________。
您的答案:B题目分数:0.5此题得分:0.5批注:电动势的能斯特方程第15题难溶电解质AgCl(s)在中溶解度最小。
您的答案:D题目分数:0.5此题得分:0.5批注:难溶盐的同离子效应第16题下列电对中,若降低pH值,其氧化性改变的是。
您的答案:C题目分数:0.5此题得分:0.5批注:电极电势的能斯特方程第17题下列电池的电动势与氯离子浓度无关的是。
您的答案:C题目分数:0.5此题得分:0.5批注:电动势的能斯特方程第18题电对H+/H2,其电极电势随溶液的pH上升而;电对O2/OH-,其电极电势随溶液的pH上升而。
您的答案:B题目分数:0.5此题得分:0.5批注:电极电势的能斯特方程第19题将下列反应设计成原电池时,不用惰性电极的是。
您的答案:C题目分数:0.5此题得分:0.5批注:电极种类的书写规则第20题若计算得到电池反应的电池电动势为负值,表示此电池反应是。
您的答案:B题目分数:0.5此题得分:0.5批注:氧化还原反应方向的判断第21题对于分步沉淀,下列叙述正确的是。
您的答案:B题目分数:0.5此题得分:0.5批注:分步沉淀的判断第22题下列原电池符号正确的是。
您的答案:D题目分数:0.5此题得分:0.5批注:原电池符号的书写规则第23题已知原电池反应:Cu (s) + Cl2 (g)=?Cu2+ (aq) + 2Cl- (aq)?。
?当增大Cl2 (g) 压力,原电池的电动势变_______;当增大Cu2+ (aq) 浓度,原电池的电动势变 __________。
您的答案:A题目分数:0.5此题得分:0.5批注:电动势的能斯特方程第24题有一组成为A2B的难溶强电解质,若在水溶液中达沉淀-溶解平衡时c(A+)=x mol·L-1,c(B2-)=y mol·L-1,则A2B的标准溶度积常数= 。
您的答案:A题目分数:0.5此题得分:0.5批注:溶度积第25题若计算得到电池反应的电池电动势为负值,表示此电池反应是。
您的答案:B题目分数:0.5此题得分:0.5批注:原电池与反应方向第26题一元弱碱溶液,加水稀释,则弱碱的解离度将,溶液的c(H+)将,弱碱的解离常数。
您的答案:A题目分数:0.5此题得分:0.5批注:稀释定律第27题在温度T时,某反应的速率常数k为4.62×10-2 (min)-1,则可判断该反应为级反应。
您的答案:B题目分数:0.5此题得分:0.5批注:反应级数的判断和半衰期第28题根据酸碱质子理论,HPO42-、H2O的共轭碱分别是。
您的答案:A题目分数:0.5此题得分:0.5批注:酸碱质子理论第29题已知反应 A- + H2B+ = HA + HB标态下向右进行。
根据酸碱质子理论,反应中较强的酸是,较强的碱是。
您的答案:A题目分数:0.5此题得分:0.5批注:酸碱质子理论第30题一封闭系统经一循环过程热和功分别为Q和W,则(Q+W) ______0。
您的答案:B题目分数:0.5此题得分:0.5批注:热力学第一定律第31题氧化还原电对的标准电极电势越高,表示该电对氧化态的氧化能力越强。
您的答案:正确题目分数:0.5此题得分:0.5批注:电极电势的大小与优化还原反应性能的判断第32题原电池电动势与电池反应的书写无关,而标准平衡常数却随反应式的书写而变化。
您的答案:正确题目分数:0.5此题得分:0.5批注:电动势与方程式写法无关,平衡常数则与方程式写法有关第33题氧化还原反应达到平衡时。
标准电动势和标准平衡常数均为零。
您的答案:正确题目分数:0.5此题得分:0.5批注:标准电动势不能用来判断反应是否已经达到平衡第34题难溶电解质离子浓度的乘积就是该物质的标准溶度积常数。
您的答案:错误题目分数:0.5此题得分:0.5批注:标准容度积的概念第35题在氧化还原反应中,正极发生还原反应,负极发生氧化反应。
您的答案:正确题目分数:0.5此题得分:0.5批注:原电池中正负极的化学反应第36题在AgCl的水溶液中加入固体NaCl,会降低AgCl的溶解度。
您的答案:正确题目分数:0.5此题得分:0.5批注:难溶盐的同离子效应第37题在一定温度下,原电池的标准电动势只取决于原电池的两个极,与电池中各物质的浓度无关。
您的答案:正确题目分数:0.5此题得分:0.5批注:标准电动势第38题 CaCO3和CaF2的标准溶度积相近,两者在水中的溶解度(mol·L-1)相近。
您的答案:错误题目分数:0.5此题得分:0.5批注:标准溶度积与溶解度第39题同类型难溶电解质的溶度积常数越小,溶解度S越小。
您的答案:正确题目分数:0.5此题得分:0.5批注:标准溶度积与溶解度第40题已知在一定的温度下,CdCO3的标准溶度积为 4.0×10-12,Cd(OH)2的标准溶度积为3.2×10-14,那么它们在水中的溶解度(mol/L)关系为CdCO3>Cd(OH)2。
您的答案:错误题目分数:0.5此题得分:0.5批注:标准溶度积与溶解度作业总得分:20.0作业总批注:。
