第三章不饱和烃剖析
第三章不饱和烃

到含氢较多的双键C原子上,而带负电荷的部分加到含
氢较少或不含氢的双键碳原子上,这一规则简称为马氏
规则。★★★★★
利用马氏规则,可以预测反应的主产物。
⑷ 过氧化物效应——在利用马氏规则时要注意,当反
应条件改变时,例如在ROOR存在下,烯烃和HBr加成 的取向正好和马尔科夫尼科夫规律相反,叫做烯烃与 HBr加成的过氧化物效应。 ★★★★★
⑵ SP2杂化轨道的形状:和SP3杂化轨道 相似,也是不对称的葫芦形,一头大一 头小,只是大的一头比SP3 杂化轨道更 大,小的一头比 SP3杂化轨道更小。
⑶ SP2杂化轨道的空间取向:三个SP2杂 化轨道的对称轴分布在同一平面上,并以 C原子为中心分别指向正三角形的三个顶 。 点,夹角互成120 ;未参加杂化的 2P轨道, 仍然保持原来的形状,其对称轴垂直于三 个SP2 轨道对称轴所在的平面。
只有HBr有过氧化物效应
4、加硫酸 ⑴ 与浓硫酸反应,生成烷基硫酸(或叫酸性硫酸酯) CH2=CH2 + HO-SO2-OH ⑵ 符合马尔科夫尼科夫规则 CH3-CH2-OSO3H
2-甲基丙烯
叔丁基硫酸
⑶ 烷基硫酸的水解(烯烃的间接水合)--制醇 CH3-CH2-OSO3H + H2O
H2SO4
3、顺反异构
条件:—任何一个双键碳原子上所连接的两个原子或原 子团都要不同。 注意: 只要任何一个双键碳原子所连接的两个取代基 是相同的,就没有顺反异构。
二、烯烃的命名 (一)系统命名法原则与烷烃相似 1、选主链:选择含有双键在内的最长碳链为主链, 支链作为取代基,按主链碳原子数称为某烯或某碳烯。 碳原子数在十以下的,用天干表示,在十个以上的用中 文数字表示十一、十二……表示,称为某碳烯。
有机化学--第三章 不饱和烃:烯烃和炔烃

碳碳双键不能绕键轴自由旋转。因此,当两个双键碳 原子各连有两个不同的原子或基团时,可能产生两种不同 的空间排列方式。
一些烯烃的物理性质
构型:(I)和(Ⅱ)的分子式相同,构造亦相同,但分子中的原子在空间 排列不同。分子中原子在空间的排列形式称为构型。 构型异构体:(I)和(Ⅱ)是由于构型不同而产生的异构体,称为构型异 构体(configurational isomers)。构型异构体具有不同的物理性质。
3.1.1 碳原子轨道的sp2杂化
H
H
CC
H
Hale Waihona Puke H1/3s +2/3p
3.1.2 碳碳双键的组成
在乙烯中,成键的两碳原子各以一个sp2杂化轨道彼 此交盖形成一个C—C σ键,并各以两个sp2杂化轨道分 别与两个氢原子的1s轨道形成两个C—H σ键,这样形成 的五个σ键其对称轴都在同一平面内。
由于每个碳原子上余下的p轨道的对称轴垂直于同一 平面,且彼此平行,这样两个p轨道就从侧面相互平行交 盖成键,组成新的轨道,称为π轨道。处于π轨道的电子称 为π电子,这样构成的共价键称为π键。
含一个碳碳三键者称为炔烃(alkynes),通式为CnH2n-2, 碳碳三键(一C≡C一)是炔烃的官能团。分子中既含有碳碳 双键,又含有碳碳三键者称为烯炔。
3.1 烯烃和炔烃的结构
碳碳双键是由两对共用电子构成,通常用两条短线表 示:C=C。碳碳三键由三对共用电子构成,通常用三条 短线表示:C≡C。但实验事实表明,它们都不是由两个 或三个σ键加合而成:
与烷基相似,一个不饱和烃从形式上去掉两个氢原 子也构成亚基。最常见的不饱和亚基有—CH=CH—, 称为1,2-亚乙烯基。
第三章不饱和烃烯烃和炔烃

第三章不饱和烃烯烃和炔烃第三章不饱和烃:烯烃和炔烃本章重点内容一、命名1、烯烃和炔烃构造异构体的命名1)选择含双键或三键在内的最长碳链为主链。
2)靠近双键或三键一端编号,重键的位次用数字标明(标号较小的碳原子)。
3)书写:与烷烃书写格式相同(当主链碳原子数大于十时,命名时汉字数字与烯或炔字之间应加一个“碳”字)。
3H3CCH3CH3H3CCCH34,4-二甲基-2-戊烯 3-甲基-1-丁炔通常将碳碳双键处于端位的烯烃,统称α-烯烃。
碳碳三键处于端位的炔烃,一般称为端位炔烃。
2、烯烃顺反异构体的命名顺反命名法:两个相同原子或基团处于双键碳原子同一侧的称为顺式,反之称为反式。
但当两个双键碳原子所连接的四个原子或基团都不相同时,则难用顺反命名法命名。
Z,E—命名法:依据次序规则比较出两个双键碳原子所连接取代基优先次序。
当较优基团处于双键的同侧时,称Z式;处于异侧时,称E式。
BrClCCClHH3CCH3CH2CCH2CH2CH3CH(CH3)2反-1,2-二氯溴乙烯(Z)-3-甲基-4-异丙基-3-庚烯3、烯炔的命名1)选择含有双键和叁键在内的最长碳链为主链;2)在满足最低系列原则下,优先考虑双键,使其具有较小编号; 3)书写:称某碳“烯”某“炔”;4)若双键和三键处于相同的位次供选择时,优先给双键较低编号。
HCCCH2CH2CH21-己烯-5-炔二、结构与性质1、结构:烯烃为sp2杂化,余下一个未参与杂化的p轨道,垂直与三个杂化轨道对称轴所在的平面。
炔烃为sp杂化,未参与杂化的两个p轨道的对称轴互相垂直且都垂直于sp杂化轨道对称轴所在直线。
2、性质物理性质电负性:三键碳原子>双键碳原子>饱和碳原子;沸点:烯烃顺式异构体>反式异构体。
顺式异构体具有弱极性,分子间作用力增大,故沸点较高。
熔点:反式异构体>顺式异构体。
反式异构体对称性教好,晶格紧密,故熔点较高。
化学性质 1)加成反应加氢:炔烃比烯烃更容易进行催化氢化(与分子形状有关,炔烃为线型结构,易吸附)。
有机化学第3章 不饱和烃

Cl
Br
CC
H
Cl
(Z)-1,2-二氯-1-溴乙烯 (反-1,2-二氯-1-溴乙烯)
Cl C
H
Cl C
Br
(E)-1,2-二氯-1-溴乙烯 (顺-1,2-二氯-1-溴乙烯)
28
6. 烯炔的命名
第三章 烯烃和炔烃 (三、烯烃和炔烃的命名)
• 编号时尽可能使重键的位次之和最低。 • 当双键和三键处于两头相同的位次时,
反式:两个取代基在环异侧 顺式:两个取代基在环同侧
15
第三章 烯烃和炔烃 (二、烯烃和炔烃的同分异构)
问题:下列化合物是否存在顺反异构?
CH3
C2H5 D
C=C
H
Cl H
H C=C
CH3
CH2-CH-CH3 CH-CH3
16
第三章 烯烃和炔烃 (三、烯烃和炔烃的命名)
三、烯烃和炔烃的命名
1. 简单的烯烃常用普通命名法
98
7
CH3
CH2CH3
10,10-二甲基-3-乙基-9-异丙基-4-十一碳烯
例3
4 CH3 3 CH2CH3
4 –甲基–3–乙基环庚烯
12
例4 CH3CC CCH2CH3 2 –甲基–3–己炔
CH3
19
4. 烯基与炔基
第三章 烯烃和炔烃 (三、烯烃和炔烃的命名)
CH2 CH
乙烯基 (vinyl)
3. 烯烃的比重都小于1,都是无色物质,溶于有机溶剂,不溶于水。
CH3 C C CH3
H
H
沸点(bp): 3.7℃ 熔点(mp): -138.9℃
CH3
H
CC
H
CH3
0.88℃
第三章不饱和烃(UnsaturatedHydrocarbons剖析

顺-2-丁烯
CH3 H
H C H3C
反-2-丁烯
CH3 C H
当双键碳原子上各连有两个不相同的原子或基 团时,由于双键不能自由旋转,在空间就会形成不 同的排列方式,形成顺反异构(也叫几何异构)。
烯烃顺反异构体的命名 顺/反标记法
H3C CH2 C C H H
顺-2-戊烯
CH3
(Z)-1-氯-2-溴丙烯
(Z)-3-甲基-4-异丙基-3-庚烯
H3C C CH3CH2CH2
CH3 CH2 CH2 (CH3)2 CH
CH2CH2CH3 C CH(CH3)2
> CH3 > CH3 CH2 CH2
(Z)-4-甲基-5-异丙基-4-辛烯
(反-4-甲基-5-异丙基-4-辛烯)
3.1.3 烯烃的物理性质
D
顺式加成,定量完成;从位阻小的一面进行。
亲电加成反应
亲电加成反应:
由亲电试剂的作用而引起加 成反应。 亲电试剂: 在反应中,具有亲电性能的 试剂。亲电试剂通常为带正电 的离子(如H+、X+等)或为在 反应中易被极化带正电荷的分 子(如X2)。
加 卤 素 加卤化氢 加 硫 酸 加 水
加次卤酸
C
C
C
C
键能为: 610.9-347.3 =263.6KJ/mol
键能为: 347.3 KJ/mol
π 键只有对称面没有对称轴。所以,双键碳原子之 间不能以两碳核间联线为轴自由旋转
C
C
σ键可绕键轴自由旋转
Байду номын сангаас
π键
σ键
π 键电子云比较分散,有较大的流动性,容易极化 变形,化学反应性较强
第六讲 第三章 不饱和烃:烯烃和炔烃(2)
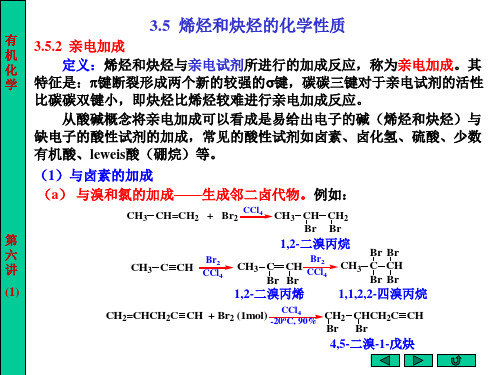
C C
+
H-X
-X -
C=C H
+
+X快
C=C X H
乙烯基碳正离子
由于卤素的吸电子作用, 阶段。 几 1 由于卤素的吸电子作用,反应能控制在加一分子 HX 阶段。 加成, 加成 常用汞盐和铜盐做催化剂。 点 2 与HCl加成,常用汞盐和铜盐做催化剂。 讨 3 与卤化氢的加成,在相应卤离子(如:(CH3 )4N+Cl-)存在下, 与卤化氢的加成,在相应卤离子( 存在下, 论 通常进行反式加成。例如: 通常进行反式加成。例如:
*1. Markovnikov规则 不对称烯烃与氯化氢等极性试剂进行加成反应时, 规则 不对称烯烃与氯化氢等极性试剂进行加成反应时, 氢原子总是加到含氢较多的双键碳原子上, 氢原子总是加到含氢较多的双键碳原子上,氯原子或其它原子或基团则加 到含氢较少的或不含氢的双键碳原子上。这条经验规则简称马氏规则。 到含氢较少的或不含氢的双键碳原子上。这条经验规则简称马氏规则。 例如
CH3CH2CH=CH2 + HBr HAc 80% (CH3)2C=CH2 + HCl CH3CH2CH2CH2Br
~100%
(CH3)2C CH3 Cl
第 六 讲 (6)
*2. 不对称炔烃与卤化氢等极性试剂进行加成反应时,也符合马氏规则。 不对称炔烃与卤化氢等极性试剂进行加成反应时,也符合马氏规则。 Br 例如 (CH3)2CHC CH HBr (CH3)2CHC=CH2 HBr (CH3)2CH C CH3
NaCl CH2=CH2 + Br2 水溶液
Br H2C CH2 Br 1,2-二溴乙烷 二溴乙烷
Cl H2C CH2 Br 1-氯-2-溴乙烷 氯 溴乙烷
有机复习提纲第3章不饱和烃

有机复习提纲第3章不饱和烃第3章不饱和烃3.1烯烃⼀、⼄烯的结构⼆、烯烃的同分异构现象1.位置异构(构造异构)——官能团位置不同⽽产⽣的异构2.顺反异构(⽴体异构)产⽣顺反异构的条件:①刚性结构(脂环、C=C) ,具有阻碍旋转的因素②刚性结构中同⼀个碳上所连的原⼦(基团)不同3.2 烯烃和炔烃的同分异构3.3 烯烃和炔烃的命名3.3.1 烯基与炔基(1)衍⽣命名法(2)系统命名法3.3.2 烯烃的命名(1) 顺,反–标记法(2) Z,E–标记法次序规则: 相连原⼦的⼤⼩,⼤者为“优先”基团。
依照相对原⼦质量:I > Br > Cl > S > O > N > C同位素依照相对原⼦质量:D > H未共⽤电⼦:最⼩较“优先”基团在双键的同侧, 标记为Z式;较“优先”基团在双键的异侧, 标记为E式。
如果直接相连的第⼀个原⼦相同,继续逐个⽐较。
对于含重键的基团,将其视为两个或三个单键3.3.4 炔烃的命名编号时尽可能使重键的位次低。
当双键和三键处于相同的位次时,优先给予双键较低的位次。
3.4 烯烃和炔烃的物理性质简单炔烃的沸点、熔点以及密度⽐碳原⼦数相同的烷烃和烯烃⾼⼀些炔烃分⼦极性⽐烯烃稍强炔烃不易溶于⽔,⽽易溶于⽯油醚、⼄醚、苯和四氯化碳中3.5 烯烃和炔烃的化学性质由于π键易于断裂,加成反应是烯烃和炔烃的主要反应⼀、加成反应总述(1)碳正离⼦1.反应活性烷基供电⼦,增加双键上的电⼦云密度,利于亲电加成反应;羧基吸电⼦,降低双键上的电⼦云密度,不利于亲电加成反应。
双键碳上的电⼦密度越⾼则容易⽣成稳定碳正离⼦,亲电加成活性越⼤。
烷基给电⼦作⽤,增加中⼼碳原⼦上正电荷分散程度,提⾼碳正离⼦的稳定性。
2.性质作⽤a. 碳正离⼦的重排b.⼆、反应类型(1)加氢(催化氢化反应,反应放热)催化剂:Pt, Pd, Ni催化剂的表⾯对重键、氢分⼦的吸附,使π键和H-H键松驰,降低价键断裂的离解能,从⽽降低反应活化能。
第3章不饱和脂肪烃

1.4.1.1 加氢反应(又称之为催化氢化)
催化剂:Pd、Pt、Ni(需高温) 产物:烷烃
RCH=CHR'
催化剂
H2
RCH2CH2R'
反应可以定量进行,因此可以根据所用的H2气的体积 来定量地分析烯烃。
无Cat. E活 E CH2 CH2 E活 H CH3CH3
一个反应能否进行,并不取决于
加Cat. 反应是放热还是吸热,而是取决于
两个甲基在双 键的不同侧, 叫反式异构体
H CH3
H C C
(Ⅳ)
H CH3
CH3 C
(Ⅴ)
CH3
C
H
这种异构现象叫顺反异构或叫几何异构
产生几何异构体的条件:
I.分子中必须具有限制旋转的因素;
II.满足条件I的两个碳原子必须和两个不 同的原子或基团相连。
H2C=CH-CH2-CH3
H2C C CH3 CH 3
C C + A-B C A C B
象这样的反应叫亲电加成反应。
1.4.1 1.4.2 1.4.3
加成反应 氧化反应 聚合反应
1.4.4
a-H的卤代反应
1.4.1 加成反应
1 . 加氢反应 2 . 加卤素(Cl2、Br2、I2)
3 . 加卤化氢HX (HCl、HBr、HI)
4 . 加水 5 . 加硫酸 6 . 加次卤酸 7. 加烯烃 8. 硼氢化反应
子与水加成,最后脱质子。
CH2=CH2 + Cl2 + H2O HOCl
CH3CH=CH2 + Br-OH
ClCH2CH2OH
CH3CHCH2Br OH
1.4.1.7 加烯烃 * 需要酸催化
第三章 不饱和烃ppt课件

C Cቤተ መጻሕፍቲ ባይዱ
• ②充分条件:同一双键碳原子上连有两不同原 子或基团
c a CC b d
a ≠ b ,c ≠ d
若 a 优 于 b c 优 于 d 则 为 Z 型 ; 反 之 , 若 优 先 基 团 在 双 键 两 侧 , 则 为 E 型
C H ( C H ) H C 3 2 3 C C C H C H C H C H 2 5 2 2 3 ( E )
2 、与X2加成
F2,Cl2,Br2,I2都能与烯烃加成。F2加成比较激烈, I2加 成又比较缓慢,最常用的是Cl2和Br2的加成。
+r H C C H 2 2 2 B
C H B r C H B r 2 2
用 于 定 性 检 查
C C
+
B r B r
C C B r
B r
C C
B r B r C C B r
顺位规则
1、
2、
3、
二 命名
普通命名法:
H C C C H 3 2 H C C H 2 2 H
乙烯 丙烯
H C C C H 3 2 C H 3
异丁烯
C C H 2 H
乙烯基
C C C H 3 HH
丙烯基
H 2 H 2C C C H
烯丙基
系统命名法
a) 选择包括双键在内最长碳键做主键, 根据主键碳原子个数称做xx烯。 b) 从靠近双键一端对主键碳编号, 双键位置与号数的双键依次表示,写在母体之 前。 c) 支键处理方法同烷烃命名。
与烷烃相似,顺反异构体,反式异构体对称性较 好,分子极性比顺式体小,b.p.,m.p.比顺式体 略低。
有机化学 第三章讲解

CH 2 =CH 2
+ HO Cl
Cl-CH 2 -CH 2 -OH
-氯乙醇
实际操作时,常用氯和水直接反应。例:
Cl CH 2 =CH 2
Cl 2 -Cl
-
CH 2 Cl
+
CH 2
H 2O -H
+
CH 2
CH 2 (主) OH
Cl -
Cl CH 2
-氯乙醇
CH 2 (副) Cl
33
b a CH 3 -CH=CH
CH 3 CH 3 -C CH-CH 3
30
3 碳正离子
。
H
Cl H
重 排 产 物 (主 )
(d) 过氧化物效应
但有过氧化物存在时:
CH 3 -CH=CH
2
+ HBr
hor
过氧化物
CH 3 CH 2 CH 2 Br (反马)
只能是HBr (HCl、HI都不反马)
31
(丙) 与硫酸加成
烯烃与H2SO4的加成反应也是亲电加成反应,加成方向 遵循马氏规则。例:
2
+ HCl
CH 3 -CH-CH Cl
2-氯丙烷 主要产物
乙酸 80%
3
+ CH 3 CH 2 CH 2 Cl
1-氯丙烷 次要产物
CH 3 CH 2 CH=CH
2
+ HBr
CH 3 CH 2 CH CH Br
HBr
2
H
2-溴丁烷
Br
CH 3 CH 2 CH 2 C CH
HBr
CH 3 CH 2 CH 2 C=CH 2 Br
2
(一) 烯烃和炔烃的结构
《有机化学》第三章 不饱和烃

吸电子基团: +NR3>NO2>CN>COOH>F>Cl>Br>I>COOR>OR>
COR>SH>OH> C CR>C6H5>CH=CH2>H
诱导效应的特点:
(1)诱导效应的强弱取决于原了或基团的电负性的大小
的两原子可相对的自由旋转。 能相对自由旋转。Βιβλιοθήκη c.键的可极化度:较小。 较大
1.2 单烯烃的异构现象
1.2.1 结构异构
CH3 CH2 CH CH2 CH3 CH CH CH3
1-丁 烯
2-丁 烯
官能团碳碳双键 位置异构
CH3 C CH2 2-甲 基 丁 烯 CH3
碳链异构
结构异构是由于分子中各原子的结合顺序不同而引起的, 位置异构和碳链异构均属于结构异构。
(2) 与卤化氢的加成
CH3CH CHCH3 + HCl CH3CH2CHCH3
2–丁烯
HBr CH3CH2CH CH2
Markovnikov规则
Cl
2–氯丁烷
Br
CH3CHCH CH3
80 %
CH3CHCH2 CH2Br 20 %
当不对称的烯烃与卤化氢等极性试剂加成时,氢原总
是加到含氢较多的双键碳原子上,卤原子(或其子或
上相互重叠。
从侧面重叠。
电子云的分布情况 a. 电子云集中于两原子 电子云分布在 键所
核的连线上,呈圆柱形分布。 在平面的上下两方,呈块
状分布。
第3章 不饱和烃
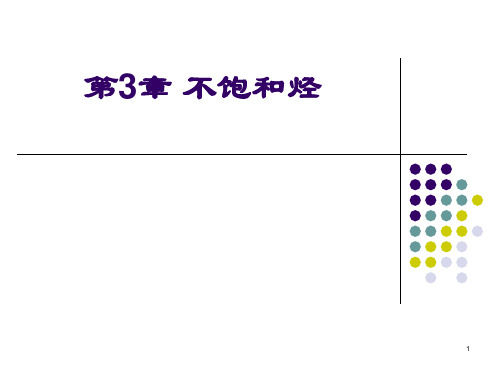
CH3-C=CH2
CH3
19
三、烯烃的性质
(一)物理性质
烯烃在物理性质上与相应的烷烃相似,但 它们的沸点低些,而相对密度稍高。 C2~C4 是气体,C5~C18是液体,C19 以上是固体。 所有烯烃的相对密度都小于1,并有特殊 气味。 烯烃难溶于水而能溶于有机溶剂,如乙醚、 四氯化碳等。
n CH CH2 AlR3 TiCl4 1MPa , 50℃ CH3
[ CH CH2 ]
CH3
聚丙烯
n
30
作业
p39 一、1、2、3、6、11、13、14、15 二、6 四、3、4
第2节 二烯烃
一、二烯烃的分类和命名 二、共轭二烯烃的结构和共轭效 应 三、共轭二烯烃的化学性质
H2C=CH2+H2O
H3PO4
300℃,7~8MPa
H3C-CH2OH
H3PO4/硅藻土 CH3CH2CH=CH2+H2O 300℃
CH3CH2CHCH3 OH
27
(二)化学性质
2.氧化反应
(1)碱性或中性高锰酸钾氧化
室温 CH2-CH2+KOH+MnO2 ↓
CH2=CH2+KMnO4+H2O
38
三、共轭二烯烃的化学性质
1.加成反应
共轭二烯烃与一分子卤素、卤化氢等亲电试剂进行加 成反应,产物通常有1,2-加成和1,4-加成两种。
低温及非极性溶剂中以1,2-加成为主 高温及极性溶剂中以1,4-加成为主。 与卤化氢加成符合马氏规则
1,2-加成
CH2BrCHBrCH=CH2 CH2=CH-CH=CH2+Br2-1,4-加成 CH2BrCH=CHCH2Br
有机化学 第三章 不饱和烃讲解

(7)与烯烃加成
“异辛烷”
二聚异丁烯
(8)硼氢化反应
3 CH3CH
CH2 + BH3 甲硼烷
OH(CH3CH2CH2)3B + 3 H2O2
(CH3CH2CH2)3B 三烷基硼
3 CH3CH2CH2 OH + B(OH)3
从形式上看是反马氏规律的,可用来合成烯烃水合等其它 方法不能得到的醇
反应机理
65 4
CH3CH=CH
3 21
CH=CHCH3
2,4-已二烯
烯基
烯烃分子中去掉一个H 原 子,剩下的 基团称 “某烯基”
2. 烯烃的异构
画出丁烯的同分异构体
2. 烯烃的异构
顺-反异构
顺式:相同基团在双键同侧 反式:相同基团在双键两侧
顺-反异构产生的条件
E-Z异构
次序规则
H3C CH3CH2
(2)与卤素(Cl2, Br2)加成
红棕色
无色
双键的两侧分别加到两 个碳原子上的,为反式加成。
溴鎓离子
(3)与卤化氢加成
加成取向
电子效应
烷基排斥电子,H+进攻电子云密度大 的碳原子,(这种由于电子云密度分 布对性质产生的影响叫电子效应)
CH2CH2CH3 CH2CH3
Br Cl
Cl
H
顺-3-甲基-4-乙基-3-庚烯 (E)-3-甲基-4-乙基-3-庚烯
反-1,2-二氯-1-溴乙烯 (Z) -1,2-二氯-1-溴乙烯
如果烯烃分子中有一个以上双键,而且每个双 键上所连基团都有Z,E两种构型时,在必要时 则需标明所有这些双键的构型。
ex.
碳正离子稳定性
课堂练习
(4)与水加成
《有机化学》第三章 不饱和烃
第三章 不饱和烃不饱和烃是指分子结构中含有碳碳双键或三键的烃。
不饱和烃中含有碳碳双键的叫烯烃,含有碳碳三键的称为炔烃。
含有两个或多个碳碳双键的不饱和烃称为二烯烃和多烯烃。
一个不饱和烃分子结构中同时含有碳碳双键和三键则称为烯炔。
不饱和烃的双键和三键不太牢固,容易发生亲电加成反应、取代反应及氧化反应。
烯烃是指含有碳碳双键的不饱和烃,包括链状烯烃和环状烯烃,其官能团为碳碳双键。
链状烯烃的通式为C n H 2n (n ≥2)。
相对于饱和烷烃,烯烃分子结构中每增加1个双键则减少2个氢原子。
一、烯烃的结构和异构现象 (一)烯烃的结构烯烃的结构中主要特征部分为碳碳双键,以最简单的烯烃-乙烯为例来了解双键的结构,乙烯的分子式为C 2H 4,乙烯的两个C 原子和四个氢原子均在同一个平面上,每个碳原子只和3个原子相连,为平面型分子。
碳碳双键由1个σ键和1个π键构成,而不是两个单键构成。
乙烯的平面构型如图3-1(a )所示,分子模型见图3-1(b )和3-1(c )。
CCH HH H121.7°117°0.108nm(a)乙烯的平面构型 (b)球棍模型 (c)比例模型图3-1 乙烯分子的结构拓展阅读碳原子的sp 2杂化和π键杂化轨道理论认为,乙烯分子中的碳原子在成键过程中,处于激发态的1个2s 轨道和2个2p 轨道进行杂化,形成3个能量相同的sp 2杂化轨道,称为sp 2杂化,其杂化过程可表示为:2s 2p激发sp 2杂化sp 2杂化轨道2p2s 2p基态激发态杂化态形成的3个sp 2杂化轨道中每个含有1/3的s 轨道成分和2/3的p 轨道成分,形状是一头大一头小;3个sp 2杂化轨道的对称轴分布在同一平面上,夹角为120°,呈平面三角形,每个碳原子还有一个2p z 轨道未参与杂化,其对称轴垂直于3个sp 2杂化轨道的对称轴所形成的平面,见图3-2。
由此可见,乙烯分子中碳碳双键是由1个σ键和1个π键组成的,π键是由2个p 轨道侧面重叠形成的,电子云分布于键轴上下,键能较小,同时由于π键电子云离核较远,受原子核束缚力较弱,容易被外电场极化,所以π键不稳定,比σ键容易断裂。
大学有机化学第三章不饱和脂肪烃

01
绿色合成
发展绿色合成方法,减少不饱和脂肪烃 合成过程中的环境污染和资源浪费,是 可持续发展的重要方向。
02
03
循环经济
通过循环利用不饱和脂肪烃,实现资 源的最大化利用,同时降低对环境的 负面影响。
跨学科研究的趋势与展望
化学与其他学科的交叉
不饱和脂肪烃的研究涉及到化学、生物学、医学、材料科学等多个学科领域,跨学科合作将有助于推动不饱和脂肪烃 的深入研究和发展。
烯烃的化学性质主要取决于碳碳双键,可以发生 加成、氧化、聚合等反应。
炔烃
01
炔烃的通式为CnH2n-2,其中含有两个碳碳三键。
02
炔烃的稳定性比烯烃更低,因为碳碳三键更容易受到亲电攻 击。
03
炔烃的化学性质与烯烃相似,但三键的反应活性更高,可以 发生加成、氧化、聚合等反应。
共轭二烯烃
01
02
03
烯烃的合成与转化
烷烃的热裂
在加热条件下,烷烃可以发生热裂反 应,生成烯烃和氢气。
醇的脱水
在酸催化下,醇可以发生脱水反应, 生成烯烃和水。
烯烃的合成与转化
• 炔烃的还原:通过还原炔烃的碳碳三键, 可以得到相应的烯烃。
烯烃的合成与转化
加氢反应
烯烃可以与氢气在催化剂的作用下发生加氢反应,生 成相应的烷烃。
烯烃的1,2-加成反应:在催化剂的作用 下,两个烯烃分子可以发生1,2-加成反 应,生成共轭二烯烃。
共轭二烯烃的转化
04 不饱和脂肪烃在工业和生 活中的应用
工业应用
01 02
塑料和合成橡胶生产
不饱和脂肪烃,如乙烯和丙烯,是塑料和合成橡胶的主要原料。它们通 过聚合反应形成高分子聚合物,广泛应用于包装、建筑材料、汽车部件 等领域。
第三章不饱和烃

还原水解可以避免产物的进一步氧化
常用的还原剂: 1)Zn/H2O 2)H2,Pd
臭氧化还原水解产物:
推测烯烃 的结构
CH2= RR'C=
CH2O , RCH= RR'C=O
RCHO
C
C
(i) O3 (ii) Zn, H2O
C
O
O
C
NO OVEROXIDATION
烯烃的臭氧化反应的应用
(1)测定烯烃的结构
nH2C=CH2
乙烯(单体)
TiCl4-Al(C2H5)3 0.1-1MPa 60-75 C
( CH2 CH2 )
聚乙烯(高分子)
n
练
+
CH3 CH CH3 CH Cl2 高 温
习
CH
CH3
+
Br2
高 温
NBS法(烯丙位的溴化)
O
Br
NBr
(C6H5COO)2
CCl4 ,
O
+
+
O
NH O
NBS
CH3 CH2 CH CH2 CH3 CH CHCH3 CH3 C CH3 H3 C C H C CH3 H CH2
H3 C C H C
CH3 H
产生顺反异构的必要条件:
不饱和双键的两个碳原子各连有不同的原 子或基团
当分子中含有两个或多个双键,且符合产 生顺反异构的条件时,顺反异构体数小于或 等于2n
“Them that has, gets!” “The richer get richer!”
(V. W. Markovnikov -- 1838 - 1904)
CH2 + HCl
有机化学:第三章 不饱和烃

CC
CH3
CH3
CC
H
CH2CH3 H
CH2CH3
E型
E型 13
Xiamen University of China
3.3 烯烃的命名
• 主链应含双键(不一定是最长) • 主官能团的位号尽可能小 • 如烯烃存在位置异构,母体名称前要加官能团 位号(三个碳原子以上) • 取代基的位置、数目、名称按“次序规则”顺 序写在母体前面 • Z或E加圆括号,写在化合物名称最前面
Xiamen University of China
Example
Br CH3
1-甲基-6-溴环己烯
17
Xiamen University of China
Example
CH(CH3)2
3-异丙基环己烯
18
Xiamen University of China
Example
5
6
1 23 4
CH2CH2CH=CH2
烯烃的反应活性
(CH3)2C CH2 > CH3CH CHCH3 > CH3CH CH2 > CH2 CH2 > CF3CH CH2
电子效应
给电子基-增加双键碳上电子云密度,有利于 亲电加成反应
吸电子基-降低双键碳上电子云密度,不利于
亲电加成反应
30
Xiamen University of China
2. 烯烃的自由基加成
3. 硼氢化反应
4. 催化氢化
5. 烯烃的氧化
6. 烯烃的卤化
7. 聚合反应
24
Xiamen University of China
亲电子试剂:电负性高,缺电子的试剂。 如:卤素、无机酸(H2SO4、HCl、HBr、HI、 HOCl、HOBr)及有机酸等(路易斯酸)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章不饱和烃3.1用系统命名法命名下列化合物a. b.c.(CH 3CH 2)2C=CH 2CH 3CH 2CH 2CCH 2(CH 2)2CH 3CH 2CH 3C=CHCHCH 2CH 3C 2H 5CH 3d.(CH 3)2CHCH 2CH=C(CH 3)2答案:a.2-乙基-1-丁烯2-ethyl -1-buteneb.2-丙基-1-己烯2-propyl -1-hexenec.3,5-二甲基-3-庚烯3,5-dimethyl -3-heptened.2,5-二甲基-2-己烯2,5-dimethyl -2-hexene3.2写出下列化合物的结构式或构型式,如命名有误,予以更正。
a.2,4-二甲基-2-戊烯b.3-丁烯c.3,3,5-三甲基-1-庚烯d.2-乙基-1-戊烯e.异丁烯f.3,4-二甲基-4-戊烯g.反-3,4-二甲基-3-己烯h.2-甲基-3-丙基-2-戊烯 答案:a.b.错,应为1-丁烯c.d.e. f.错,应为2,3-二甲基-1-戊烯g.h.错,应为2-甲基-3-乙基-2-己烯3.3写出分子式C 5H 10的烯烃的各种异构体的结构式,如有顺反异构,写出它们的构型式,并用系统命名法命名。
pent-1-ene (E)-pent-2-ene (Z)-pent-2-ene3-methylbut-1-ene2-methylbut-2-ene 2-methylbut-1-ene3.4用系统命名法命名下列键线式的烯烃,指出其中的sp2及sp3杂化碳原子。
分子中的σ键有几个是sp2-sp3型的,几个是sp3-sp3型的?3-ethylhex-3-ene3-乙基-3-己烯,形成双键的碳原子为sp2杂化,其余为sp3杂化,σ键有3个是sp2-sp3型的,3个是sp3-sp3型的,1个是sp2-sp2型的。
3.5写出下列化合物的缩写结构式答案:a 、(CH 3)2CHCH 2OH ;b 、[(CH 3)2CH]2CO ;c 、环戊烯;d 、(CH 3)2CHCH 2CH 2Cl3.6将下列化合物写成键线式A 、O ;b 、;c 、Cl;d、;e、3.7写出雌家蝇的性信息素顺-9-二十三碳烯的构型式。
(CH 2)11CH 33.8下列烯烃哪个有顺、反异构?写出顺、反异构体的构型,并命名。
a. b. c.d.CH 2=C(Cl)CH 3C 2H 5CH=CHCH 2ICH 3CH=CHCH(CH 3)2CH 3CH=CHCH=CH2CH 3CH=CHCH=CHC 2H 5CH 3CH 2C=CCH 2CH 3CH 3C 2H 5e.f.答案:c,d,e,f 有顺反异构c.C 2H 5CHCCH 2IH( Z )-1-碘-2-戊烯( E )-1-碘-2-戊烯C C 2H 5CCH 2I HHd.C HCCH(CH 3)2H( Z )-4-甲基-2-戊烯H 3CCHCHCH(CH 3)2H 3C ( E )-4-甲基-2-戊烯e.C H 3CCH C H( Z )-1,3-戊二烯H CH 2C HCH C H( E )-1,3-戊二烯H 3CCH 2f.C H 3CCHC( 2Z,4Z )-2,4-庚二烯HCH HC 2H 5C H 3CCHCH CH C 2H 5H( 2Z,4E )-2,4-庚二烯C HCHCH 3CCH C 2H 5H( 2E,4E )-2,4-庚二烯C HCH C( 2E,4Z )-2,4-庚二烯H 3CCH HC 2H 53.9用Z 、E 确定下来烯烃的构型答案:a 、Z ;b 、E ;c 、Z3.10有几个烯烃氢化后可以得到2-甲基丁烷,写出它们的结构式并命名。
2-methylbut-1-ene2-methylbut-2-ene 3-methylbut-1-ene3.11完成下列反应式,写出产物或所需试剂.a.CH 3CH 2CH=CH 2H 2SO 4b.(CH 3)2C=CHCH 3HBrc.CH 3CH 2CH=CH 2CH 3CH 2CH 2CH 2OHd.CH 3CH 2CH=CH 2CH 3CH 2CH-CH 3OHe.(CH 3)2C=CHCH 2CH 3O 3Zn H 2O,f.CH 2=CHCH 2OHClCH 2CH-CH 2OHOH答案:a.CH 3CH 2CH=CH 2H 2SO 4CH 3CH 2CH CH 3OSO 2OHb.(CH 3)2C=CHCH 3HBr(CH 3)2C-CH 2CH 3Brc.CH 3CH 2CH=CH 2BH 3H 2O 2OH -CH 3CH 2CH 2CH 2OHd.CH 3CH 2CH=CH 2H 2O / H+CH 3CH 2CH-CH 3OHe.(CH 3)2C=CHCH 2CH 3O 3Zn H 2O ,,CH 3COCH 3+CH 3CH 2CHOf.CH 2=CHCH 2OHCl 2 / H 2OClCH 2CH-CH 2OHOH1).2).1).2).3.12两瓶没有标签的无色液体,一瓶是正己烷,另一瓶是1-己烯,用什么简单方法可以给它们贴上正确的标签?答案:1-己烯正己烷Br 2 / CCl 4or KMnO 4无反应褪色正己烷1-己烯3.13有两种互为同分异构体的丁烯,它们与溴化氢加成得到同一种溴代丁烷,写出这两个丁烯的结构式。
答案:CH 3CH=CHCH 3CH 2=CHCH 2CH 3或3.14将下列碳正离子按稳定性由大至小排列:CCH 3H 3C C HCH 3CH 3++C CH 3H 3C CH CH 3CH 3CCH 3H 3C CH 2CH 2CH 3+答案:稳定性:CCH 3H 3C CHCH 3CH 3++>CCH 3H 3C CHCH 3CH 3>CCH 3H 3C CH 2CH 2CH 3+3.15写出下列反应的转化过程:C=CHCH 2CH 2CH 2CH=CH 3C H 3CCH 3CH 3H+C=CH 3C H 3CC CH 2CH 2H 2CCH 2H 3C CH 3答案:C=CHCH 2CH 2CH 2CH=CH 3C H 3CH+CH 3CH 3C-CH 2CH 2CH 2CH 2CH=CH 3C H 3CCH 3CH 3++H+H_3.16分子式为C 5H 10的化合物A ,与1分子氢作用得到C 5H 12的化合物。
A 在酸性溶液中与高锰酸钾作用得到一个含有4个碳原子的羧酸。
A 经臭氧化并还原水解,得到两种不同的醛。
推测A 的可能结构,用反应式加简要说明表示推断过程。
答案:or3.17命名下列化合物或写出它们的结构式: a.CH 3CH(C 2H 5)C CCH 3 b.(CH 3)3CC CC(CH 3)3CCc.2-甲基-1,3,5-己三烯d.乙烯基乙炔 答案:a.4-甲基-2-己炔4-methyl -2-hexyneb.2,2,7,7-四甲基-3,5-辛二炔2,2,7,7-tetramethyl -3,5-octadiyneCHCd.c.3.18写出分子式符合C5H8的所有开链烃的异构体并命名。
2-methylbuta-1,3-diene 3-methylbuta-1,2-diene 3-methylbut-1-ynepenta-1,4-diene (E )-penta-1,3-diene (Z )-penta-1,3-dienepent-1-ynepent-2-yne penta-1,2-diene3.19以适当炔烃为原料合成下列化合物:a. CH 2=CH 2b. CH 3CH 3c. CH 3CHOd. CH 2=CHCle. CH 3C(Br)2CH 3f. CH 3CBr=CHBrg. CH 3COCH 3h. CH 3CBr=CH 2i. (CH 3)2CHBr答案:a.HC CH Lindlar catH 2C CH 2 b.HC CHNi / H 2CH 3CH 3c.HC CH+H 2OHgSO 4H 2SO 4CH 3CHOd.HC CH +HCl HgCl 2CH 2=CHCle.H 3CC CHHgBr 2HBrCH 3C=CH 2BrHBrCH 3-C Br BrCH 3f.H 3CC CH+Br 2CH 3C=CHBrBrg.H 3CC CH +H 2OHgSO 4H 2SO 4CH 3COCH 3+ H 2Lindlar catH 3CC CH +H 2h.H 3CC CH+HBrHgBr 2CH 3C=CH 2Bri.CH 3CH=CH 2HBr(CH 3)2CHBr3.20用简单并有明显现象的化学方法鉴别下列各组化合物: a.正庚烷1,4-庚二烯1-庚炔b.1-己炔2-己炔2-甲基戊烷 答案:正庚烷1,4-庚二烯1-庚炔Ag(NH 3)2+灰白色无反应1-庚炔正庚烷1,4-庚二烯Br 2 / CCl 4褪色无反应正庚烷1,4-庚二烯a.b.2-甲基戊烷2-己炔1-己炔Ag(NH 3)2+灰白色无反应1-己炔2-己炔Br 2 / CCl 4褪色无反应2-己炔2-甲基戊烷2-甲基戊烷3.21完成下列反应式:HgSO 4H 2SO 4a.CH 3CH 2CH 2C CHHCl (过量)b.CH 3CH 2C CCH 3+KMnO 4H+c.CH 3CH 2C CCH 3+H 2Od.CH 2=CHCH=CH 2+CH 2=CHCHOe.CH 3CH 2C CH+HCN答案:a.CH 3CH 2CH 2C CHHCl (过量)CH 3CH 2CH 2CClClCH 3b.CH3CH 2C CCH 3+KMnO 4H+CH 3CH 2COOH+CH 3COOHHgSO 4H 2SO 4c.CH 3CH 2C CCH 3+H 2OCH 3CH 2CH 2COCH 3+CH 3CH 2COCH 2CH 3d.CH 2=CHCH=CH 2+CH 2=CHCHO CHOe.CH 3CH 2C CH+HCNCH 3CH 2C=CH 2CN3.22分子式为C 6H 10的化合物A ,经催化氢化得2-甲基戊烷。
A 与硝酸银的氨溶液作用能生成灰白色沉淀。
A 在汞盐催化下与水作用得到CH 3CHCH 2CCH 3CH 3O。
推测A 的结构式,并用反应式加简要说明表示推断过程。
答案:CH 3CHCH 2C CH H 3C3.23分子式为C 6H 10的A 及B ,均能使溴的四氯化碳溶液褪色,并且经催化氢化得到相同的产物正己烷。
A 可与氯化亚铜的氨溶液作用产生红棕色沉淀,而B 不发生这种反应。
B 经臭氧化后再还原水解,得到CH 3CHO 及HCOCOH (乙二醛)。
推断A 及B 的结构,并用反应式加简要说明表示推断过程。
