SINO 管理体系文件策划表(一级、二级、三级文件互引)瑞普
APQP全套表格

APQP 项目资料清单项目名称:项目编号:项目组长:序号项目文件或记录主导部门责任人计划完成日期备注0 概念提出/批准:项目开始阶段市场调查表营销顾客的呼声市场调研报告营销产品建议书营销APQP 产品建议计划周期:市场营销计划-营销功能计划提APQP 会议记APQP 项目开发时间进度表第页,共页项目编号:产品名称:型式规格:客户名称:编制日期:APQP工作保证计划(项目责任矩阵表)第一阶段:计划和项目确定日期:年月日页页供方概况登记表-供方评价和选择中文送样通知书-供方评价和选择通知日期联系电话供货厂商早期供方名单-供方评价和选择APQP 初始过程流程图日期:年月日项目编号:工序名称:APQP 初始特殊特性清APQP 初始材料清APQP 初始设备、工装清单APQP 工作保证计划(项目责任矩阵表)第二阶段:产品设计和开发日期:年月日APQP 项目开发培训方案APQP 顾客样品评审确认书评审日期: 编号: 顾客APQP -A-2设计信息检查清单(新产品开发可行性评估表)APQP 设备需求表(主要设备盘点清单)APQP 工装需求表(工装盘点清单)APQP工装夹治具验收单APQP 量具试验装备要求(主要量仪盘点清单)APQP -A-3新设备、工装和试验装置检查清单APQP新产品成本预估表修订日期:APQP 新产品成本预算报告APQP 小组可行性承诺顾客:日期:零件编号:零件名称:可行性的考虑产品质量策划小组并不打算在进行可行性评价时面面俱到,但已考虑了以下问题。
所提供的图样和/或规范已被用来作为分析满足所有规定要求能力的基础。
对于所有否定答案要识别所关注事项和/或所提出更改,以满足特定要求的小组成员/职务/日期小组成员/职务/日期小组成员/职务/日期小组成员/职务/日期小组成员/职务/日期小组成员/职务/日期QR-2-13报价管理表-合同评审合同评审记录表-合同评审。
质量管理体系职能分配表格.

质量管理系统职能分派表管投企物幼商财人劳行党标准总理资业业托业务力政委服工内容经者发管管管服审资办办公会条款理代展理理理务计源公公司表部部部部部部部室室4质量管理系统★▲▲▲▲▲▲▲▲▲▲▲▲整体要求文件要求★文件控制▲▲▲▲▲▲▲▲★▲▲记录控制▲▲▲▲▲▲▲▲★▲▲5管理职责★▲▲▲▲▲▲▲▲▲▲▲▲管理承诺以顾客为关注焦点★▲▲▲▲▲▲▲▲▲▲▲▲质量目标★▲▲▲▲▲▲▲▲▲▲▲▲策划★★▲▲▲▲▲▲▲▲▲▲▲质量目标质量管理系统策划★▲▲▲▲▲▲▲▲▲▲▲职责、权限和交流★▲▲▲▲▲▲▲▲▲▲▲职责与权限管理者代表★内部交流★▲▲▲▲▲▲▲▲▲▲▲管理评审★▲▲▲▲▲▲▲▲▲▲▲▲6资源管理★资源供给人力资源★★★★★基础设备▲★工作环境▲★7产品实现★▲▲▲▲产品实现的策划与顾客相关的过程管投企物幼商财人行党标准劳总理资业业托业务力政委内容经者发管管管服审资服办办工条款公理代展理理理务计源公公会表部部部部部部部司室室与产品相关的要求确实▲★★★定与顾客相关的要求的评▲★★★审顾客交流▲▲★★★设计和开发▲★★★★采买▲▲★★★★生产和服务供给★★★★生产和服务供给的控制生产和服务供给过程的★★★★确认表记和可追忆性★顾客财富▲★▲▲产品防备8监督和丈量装置的控制★★★★丈量、剖析和改良总则★▲▲▲▲▲监督和丈量▲★★★★顾客满意内部审查▲▲▲▲▲▲▲▲★▲▲过程的监督和丈量★▲▲▲▲▲产品的监督和丈量★▲★★★★★▲不合格品的控制★▲★★★★▲数据剖析▲▲▲▲★改良★▲▲▲▲▲▲连续改良纠正举措▲▲▲▲▲★预防举措▲▲▲▲▲★★-------责任部门▲--------辅助部门。
9000 14001 45001 三体系管理表格汇编(doc 97页)

XX有限公司MS-CARE-01三体系管理表格汇编(ISO9001:2015,ISO14001:2015,ISO45001:2018全套表格记录97页)制订:审批:2020-1-1发布2020-1-1实施XX有限公司管理手册/程序文件受控版本发放范围编制: 审核:日期:年月日XX有限公司受控文件清单编制: 审核:日期:年月日文件发放记录编制: 审核: 日期:年月日编制: 审核: 日期:年月日部门及发放数量版次编号文件名称编制: 审核: 日期:年月日技术文件发放范围表部门及发放数量版次编号文件名称编制: 审核: 日期:年月日管理文件汇编发放范围表部门及发放数量版次编号文件名称编制: 审核: 日期:年月日文件回收记录编号文件编号文件名称版次份数页/份回收日期销毁日期备注编制: 审核: 日期:年月日XX有限公司文件更改单申请部门申请人文件编号版次文件名称申请日期更改理由:更改内容:编制: 审批: 日期: 年月日XX有限公司文件更改记录文件编号文件名称更改人更改日期批准人批准日期序号更改说明更改页数XX有限公司文件/记录作废清单序号文件/记录名称文件/记录编号版次受控编号作废日期编制:批准:日期:年月日XX有限公司文件/记录作废申请单编号名称版次申请部门申请人批准人申请原因原文件/记录内容页次(可附页)发放部门及份数审查意见签字:日期:年月日批准意见签字:日期:年月日XX有限公司文件领用申请表申请部门申请人文件名称文件编号版次申请数量申请原因审查意见签字:日期:年月日批准意见签字:日期:年月日XX有限公司文件领用申请表申请部门申请人文件名称文件编号版次申请数量申请原因审查意见签字:日期:年月日批准意见签字:日期:年月日XX有限公司外来文件接收登记表序号接收日期文件编号文件名称接收人收到份数备注文件/记录借阅申请表借阅部门申请人文件名称文件编号版次申请数量预计归还日期年月日~ 年月日批准人批准日期XX有限公司文件/记录借阅申请表借阅部门申请人文件名称文件编号版次申请数量预计归还日期年月日~ 年月日批准人批准日期XX有限公司文件/记录借阅申请表借阅部门申请人文件名称文件编号版次申请数量预计归还日期年月日~ 年月日批准人批准日期记录清单序号表格编号表格名称保存期限归口部门编制: 审批: 日期: 年月日管理评审计划评审目的评审内容评审时间年月日~ 年月日参加人员:评审准备工作备注编制: 审批: 日期: 年月日管理评审会议记录会议时间会议地点主持人记录人参与评审人员姓名部门职务姓名部门职务会议内容编制: 审核: 日期: 年月日管理评审报告评审时间评审地点评审目的评审输入内容评审内容三、评审结论本报告副本分发给:总经理、管理者代表及各职能部门编制:审批:日期:年月日XX有限公司年度培训计划序号培训时间培训项目培训课程名称讲师培训对象培训方式地点备注编制:审核:日期:年月日XX有限公司培训申请表申请部门申请人申请时间培训项目名称培训名称培训时间讲师培训方式培训课时申请原因训练的目标审核人批准人批准时间XX有限公司培训申请表申请部门申请人申请时间培训项目名称培训名称培训时间讲师培训方式培训课时申请原因训练的目标审核人批准人批准时间培训签到表培训项目名称培训课程名称培训讲师培训对象培训时间培训地点培训方式签到处序号部门姓名签到时间序号部门姓名签到时间培训记录表培训主题时间地点培训讲师培训方式参加培训人员签到:培训内容摘要(可附件):考核方式及成绩(可附件):□提问/考核□试卷考试□合格□不合格合格率:培训效果评价:记录人:审核:日期:年月日XX有限公司设备台帐序号内部编号设备名称规格型号生产厂家出厂编号单位数量功率kW安装地点进厂日期设备状态备注编制:审核:日期:年月日XX有限公司设备履历表设备编号名称制造厂商压造力吨制造年份冲程数出厂编号每分钟最大产能次/分型号最大切断直径mm购置日期最大切断长度Mm所属单位主马达KW重量Kg附属设备或其他记录(备份件. 辅助专用夹具等)保修记录日期保养或维修内容更换零件名称数量效果确认确认人编制: 审核: 日期: 年月日XX有限公司设备日常保养检点表日序项期号目1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 311转动部分机床转动声音2 主马达运转3 转键4润滑部分铜套部分5 滑块6 油路畅通7 球头有规定油量8 电路部分工作灯9 控制开关10 卫生各部位清洁检查保养人监督人符号说明正常状态“√”不正常状态“×”编制审核日期设备报废申请单申请部门申请人填表日期设备编号设备名称规格型号出厂日期使用日期已使用年限原值(万元)数量(可另附纸说明)设备状况报费原因部门负责人:日期:制造中心部门负责人:日期:采购部签名:日期:财务中心意见部门负责人:日期:总经理意见签名:日期:编制审核日期设备/仪器验收记录设施名称到货数量规格型号到货日期验收日期检查验收内容序号项目检查验收记录检查结果1 设备名称□正确□不正确2 规格型号□正确□不正确3 供应商□正确□不正确4 到货数量□正确□不正确5 外包装完好性□完好□破损6 设施本身完好性□完好□破损锈蚀7 随机备件□符合□不符合8 技术资料□符合□不符合9 其它□符合□不符合检查验收结论:验收人验收部门主管(如有破损、锈蚀情况,应照相并粘贴于此处)编制审核日期XX有限公司设备报修单设备编号设备名称使用部门故障时间报修人报修时间接受人故障现象备注维修的,则在此栏填写相应的处理结果。
质量体系文件结构一览表-P

手册过程作业规范#记录表格备注责任人完成日期质1《文件发放记录表》吴春伟量2《文件更改通知单》吴春伟手3《文件控制清单》吴春伟册4《外来文件清单》吴春伟5《文件评审记录》吴春伟6《销毁报告单》吴春伟bCX4.2-02质量记录管理程序7《质量记录明细表》吴春伟8《长期业务计划》喻蕙兰潘越9《年度业务计划》喻蕙兰潘越10《部门年度目标》潘越11《业务计划评审记录》潘越12《业务目标实施统计台帐》(附《业务目标实施统计台帐分析》)潘越13《公司级数据报表》潘越14《公司级数据和资料》(附《公司级数据统计分析》)潘越15《质量成本帐》高亚红16《质量成本分析表》高亚红17《废品损失统计表》高亚红内部沟通fCX5.5-01内部沟通程序18《管理评审计划表》潘越19《管理评审记录》潘越20《管理评审报告》潘越任职要求21《员工培训申请》许静洁22《年度员工培训计划》许静洁23《培训记录》许静洁24《员工培训档案》许静洁25《岗位人员评定记录》许静洁程序文件质量体系文件结构一览表体系文件:质量手册、程序文件、三级文件;文件和记录控制文件控制程序业务计划管理公司级数据管理程序人力资源管理程序人力资源管理质量成本管理质量成本控制程序CX8.4-01acdegCX4.2-01CX5.4-02hCX6.2-01CX5.6-02CX5.6-01管理评审管理业务计划管理程序管理评审程序26《合格专业人员名册》许静洁质27《员工技能矩阵图》许静洁量28《员工满意度调查表》许静洁手29《员工满意度分析报告》许静洁册30《员工奖励统计表》许静洁设备维护保养细则31《采购申请单》吴春伟32《设备台帐》吴春伟33《设备日常点检表》吴春伟34《设备检修计划》吴春伟35《设备定期检修记录》《设备维修记录》吴春伟36《设备布局多方论证记录》吴春伟37《设备易损件清单》吴春伟38《设备停机率分析报告》吴春伟突发事件控制措施39《突发事件情况记录表》刘林鹏40《突发事件总结分析报告》刘林鹏41《订货合同台帐》喻蕙兰42《口头(电函)合同记录表》喻蕙兰43《合同评审会签表》喻蕙兰44《月份要货计划》喻蕙兰45《市场调研报告》喻蕙兰46《可行性分析报告》喻蕙兰lCX7.3-01产品质量先期策划控制程序刘林鹏m CX7.3-04潜在失效模式及后果分析控制程序刘林鹏nCX7.3-05特殊特性管理程序刘林鹏质量保证协议48《供应商调查表》陆文婷49《样品认定报告》陆文婷50《供应商确认表》陆文婷ko见APQP计划表供应商评定供应商评定和监控管理程序47人力资源管理程序人力资源管理设备管理及预防维护程序应急计划管理程序hijCX6.2-01CX6.3-01合同评审产品质量先期策划CX7.4-01设施管理CX6.3-02CX7.2-01合同评审管理程序质量手77《用户服务登记表》喻蕙兰量具校准方法;78《量具校准记录》刘林鹏自制验具校准方法79《自制验具校准记录》刘林鹏80《实验检测原始记录》刘林鹏81《实验检测结果报告》刘林鹏82《检验、测量和试验设备台帐》刘林鹏83《检验、测量和试验设备周期检定计划》刘林鹏84《检验、测量和试验设备周期检定记录表》刘林鹏85《年度测量系统分析计划》刘林鹏86《量具重复性和再现性报告》刘林鹏87《量具重复性和再现性数据表》刘林鹏88《重复性极差控制图》刘林鹏质89《零件评价人平均值图》刘林鹏量90《计数型量具(小样法)数据表》手进货检验zeCX8.2-01进料检验和试验管理程序采购产品验收规范91《原材料、外协件、外购件进厂检验单》刘林鹏册92《产品首尾件交验单》刘林鹏93《巡检记录》刘林鹏产品标准94《产品检验记录》刘林鹏95《全尺寸测量报告》刘林鹏96《型式实验报告》刘林鹏97《顾客满意度调查表》刘林鹏98《顾客满意度评价报告》刘林鹏99《过程审核年度计划》潘越吴春伟100《过程审核计划》潘越吴春伟101《检查表》潘越吴春伟102《过程审核报告》潘越吴春伟103《产品审核年度计划》潘越刘林鹏zfzgzhziza产品检验工序间检验管理程序测量设备管理CX7.6-03zbzc检验指导书CX8.2-02最终检验和试验管理程序服务管理服务管理程序检验、测量和试验设备的控制程序顾客满意度评价顾客满意度评价管理程序过程审核程序zd实验室控制程序测量系统分析控制程序CX8.2-03CX8.2-03CX8.2-05CX7.5-09CX7.6-01CX7.6-02104《产品审核计划》潘越刘林鹏105《检查表》潘越刘林鹏106《产品审核报告》潘越刘林鹏107《审核方案》潘越108《内部质量体系审核实施计划》潘越109《检查表》潘越110《不符合报告》潘越111《不合格项分布情况表》潘越112《内部质量体系审核报告》潘越113《不合格品评审表》刘林鹏质114不合格品统计分析表刘林鹏量115《纠正预防措施报告》刘林鹏116《质量信息反馈单》刘林鹏手117《质量信息台账》刘林鹏册118《持续改进项目申请表》潘越119《年度持续改进的计划》潘越120《项目持续改进方案》潘越121《持续改进效果验证记录》潘越zkzlz mznzj持续改进持续改进控制程序不合格品控制不合格品控制程序CX8.3-07CX8.5-01纠正预防措施纠正和预防措施管理程序CX8.5-02产品审核程序CX8.2-06内部质量体系审核程序内部审核CX8.2-07。
质量管理体系职能分配表格新版

东莞 XXXX有限企业
质量管理系统职能分派表:
管销技客采生资品管行标准条款理售术服购产材管理政
层部部课课部课课部课4 组织环境 /4.1 理解企业及其环境▲△△△△△△△△△
理解有关方的需乞降希望▲△△△△△△△△△质量管理系统的范围▲
质量管理系统及其过程▲△△△△△△△△△5 领导作用 /5.1 领导作用和承诺▲
目标▲△△△△△△△△△
组织的岗位、职责的权限▲△△△△△△△△△6 策划 /6.1 应付风险和机会的举措▲△△△△△△△△△
质量、目标及其实现的策划▲△△△△△△△△△改正的策划▲△△△△△△△△△
▲△△△△△△△△△
人员▲△△△△△△△△△基础设备△△△△△▲△△△△
△△△△△▲△△△△
△△△△△△△▲△△
△△△△△△△△△▲能力△△△△△△△△△▲
意识△△△△△△△△△▲
交流△△△△△△△△▲△
形成文件的信息△△△△△△△△▲△8 运转 /8.1 运转策划和控制△△▲△△△△△△△
产品和服务要求△▲△△△△△△△△产品和服务的设计和开发删减
外面供给过程、产品和服务的控制△△△△▲△△△△△
△△△△△▲△△△△
△△△△△▲△△△△
△▲△△▲△△△△△
△△△△△△▲△△△
△△△▲△△△△△△改正控制△△△△△▲△△△△产品和服务的放行△△△△△△△▲△△不合格输出的控制△△△△△△△▲△△
▲△△△△△△△▲△
△△△▲△△△△△△
△△△△△△△▲△△内审审查▲△△△△△△△△△管理评审▲△△△△△△△△△10 连续改良 /10.1 总则▲△△△△△△△△△
不合格与纠正举措△△△△△△△▲△△
连续改良▲△△△△△△△△△注:▲代表主控部门△代表辅助部。
三体系通用表格

文件审批表WD—JL—01 NO:文件控制清单文件更改申请单文件销毁记录质量记录清单记录销毁登记表年度管理评审方案管理评审报告年度培训计划培训效果考核表生产设备台账设备检修记录表设备报废申请质量计划用户来电、来函记录表合同更改单供方评价记录表合格供方名单采购产品验证和检验记录校准记录用户质量异议表用户(单位):联系人:联系电话:填写日期:顾客档案WD—JL—31 NO:请在下面您认为正确的括号中打“√”并提出您的意见和看法。
1.产品净重:满意()一般()不满意()建议或意见:2.产品质量:满意()一般()不满意()建议或意见:3.产品使用后的色泽与性能:满意()一般()不满意()建议或意见:4.销售的程序:满意()一般()不满意()建议或意见:5.销售管理:满意()一般()不满意()建议或意见:6.售后服务:满意()一般()不满意()建议或意见:客户(单位):联系方法:填表日期:制表人:制表日期:内部信息联络单年度内部审核计划内审日程安排表签到表内审检查表不合格报告内部审核报告工作检查与考评表不合格品评审处置表不合格品通知单WD—JL—41 NO:车间(部门):你部门生产(购进)的,经检验项指标不合格,请做好标识,以便处置。
生产部20 年月日纠正和预防措施通知单文件借阅/复印记录编号:表号:QP01-09员工技能一览表编号:表号:QP05-05服务要求评审表编号:表号:QP06-01服务质量检查与考评表表号:QP12-01部门:公司于年月日对你部门工作以公司质量管理体系各文件、工作要求为依据进行检查后,记录如下:填写人:日期:年度内部质量审核计划编号:表号:QP13-01编制:审核:批准:日期:日期:日期:设计开发信息联络单项目设计开发任务书设计开发评审记录表。
2020年 质量管理体系--一体化管理体系文件总览表-三级文件清单

一体化管理体系文件总览表
序号
文件名称
1
《特采作业管理办法》
2
《停线异常管理办法》
3
《物料检验规范》
4
《物料代用管理办法》
5
《抽样计划作业办法》
6
《QA作业指导办法》
7
《品质异常作业管理办法》
8
《签样作业管理办法》
9
《客退品处理办法》
10
《IQC作业指导办法》
11
《IPQC巡检作业指导办法》
版本 B0 B0 B0 B0 B0 B0 B0 B0 B0 B0 B0 B0 A0 B0 B0 B0 B0 B0 B0 B0 B0 B0 B0 B0
生效日期 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 2013/11/4 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14 202x/3/14
24
《特殊出货管理办法》
25
26
27
文件编号 SL-WI-QA-01 SL-WI-QA-02 SL-WI-QA-03 SL-WI-QA-04 SL-WI-QA-05 SL-WI-QA-06 SL-WI-QA-07 SL-WI-QA-08 SL-WI-QA-09 SL-WI-QA-10 SL-WI-QA-11 SL-WI-QA-12 SL-WI-QA-13 SL-WI-ENG-01 SL-WI-ENG-02 SL-WI-ENG-03 SL-WI-ENG-04 SL-WI-WH-01 SL-WI-WH-02 SL-WI-PMC-01 SL-WI-HRD-01 SL-WI-MKT-01 SL-WI-MKT-02 SL-WI-MKT-03
三体系认证全套表格(很全实用)

受控文件清单一式两份,一份申请部门留存,一份报审核部门.记录清单填表人: 年月日审核(管理者代表): 批准:审核(管理者代表): 批准:实用文档文案大全年度培训计划编制; 日期:审核: 日期:批准: 日期:培训记录表设备台帐设备维修记录表车间:MZFL /JL-13设施报废单合同要求评审表批准: 年月日定单确认表合同登记台帐供方评定记录表实用文档文案大全合格供方名录编制:日期: 批准:日期:采购计划编制:日期: 批准:日期: 文案大全生产计划编制:日期: 批准:日期: 文案大全监视测量设备台帐编制: 日期:监视测量设备周期检定记录表编制: 日期:顾客满意度调查表填表人: 年月日年度内审计划审核实施计划内审检查表单位:MZFL /JL-31不符合报告内审不符合项分布表内审报告内审首(末)次会议签到表时间:MZFL /JL-35实用文档文案大全进货物资验证单2、g项(验证结果)应填写“合格”或“不合格”,其余各项合格者划符号√,否则×。
3、企业能出具检测结果者,验证d.、e、f项合格,则g项填合格,否填不合格。
4、如供方(或委托方)提供a、b、c项之一者,并经企业验证d、f项通过,即视为合格。
5、不合格品应在“备注”栏中注明拒收或退回。
不合格品报告单MZFL /JL-39纠正预防措施表统计技术应用记录外部投诉处理报告表MZFL /JL-42环境适用法律法规和其他要求清单文案大全职业健康安全适用法律法规和其他要求清单文案大全实用文档环境因素清单编制:审核:批准:实用文档年月日年月日年月日实用文档文案大全环境因素评价表重大环境因素清单编制:审核:批准:年月日年月日年月日可望施加影响的环境因素清单说明:第7项、第10项经评价为重要环境因素,不另列文。
编制:审核:批准:危险源辨识评价表辨识人:年月日文案大全重大危险源清单编制:审核:批准:年月日年月日年月日文案大全环保设备表信息交流记录表废弃物处理统计表填表:负责人:年月日环境、职业健康安全运行检查记录注:公司本部每季检查一次。
某公司质量管理体系文件表格

********有限公司质量管理体系文件表格********有限公司目录1、文件编制申请表........................2、制度执行情况检查记录..................3、供货方汇总表..........................4、供货方质量体系调查表..................5、合格供货方档案表......................6、药品采购计划表........................7、购进质量验收药品目录..................8、药品质量档案表........................9、药品购进、质量验收纪录................10、药品储存、陈列环境检查记录...........11、环境温湿度监测记录...................12、近效期药品催销表.....................13、药品拆零销售记录.....................14、处方药销售调配销售记录...............15、中药饮片装斗复核记录.................16、中药方剂调配销售记录.................17、顾客意见征询表.......................18、药品质量问题查询表...................19、药品质量问题投诉、质量事故调查处理报告20、药品质量信息汇总分析表...............21、药品销售分析表.......................22、药品质量异常情况报告表...............23、不合格药品确认、报告、报损、销毁表……24、药品购进退出、销后退回记录…25、药店员工花名册 ............26、企业年度培训计划表 ........27、药店员工个人培训教育档案……28、药店员工个人建康档案 ......29、企业设施设备一览表 ........30、首营企业审批表 ............40、设施设备一览表 ............41、养护设备检修维护记录 ......43、缺货登记表 ................44、投诉客户信息登记表 ........45、销售记录表 ................46、不合格药品处理情况汇总分析表47、药品拒收报告单 ............文件编制申请批准表申请人(部门):制度执行情况检查记录检查日期:年月日检查人:供货方汇总表供货方质量体系调查表营业执照编号许可证编号生产经营范围经营方式年销售额质量认证情况业务联系人电话传真E-mail主要产品依法经营状况综合评价经审核符合规定,可以列为合格供货方。
三合一整合管理体标准对应表2015
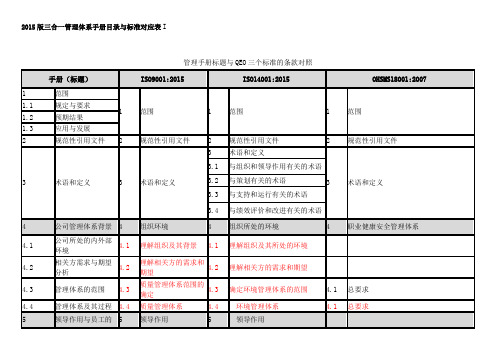
2015版三合一管理体系手册目录与标准对应表I管理手册标题与QEO 三个标准的条款对照手册(标题)ISO9001:2015ISO14001:2015OHSMS18001:20071 范围 1范围1范围1范围1.1 规定与要求 1.2 预期结果 1.3 应用与发展 2规范性引用文件2规范性引用文件2 规范性引用文件 2规范性引用文件3术语和定义3术语和定义3 术语和定义3术语和定义 3.1与组织和领导作用有关的术语 3.2 与策划有关的术语 3.3 与支持和运行有关的术语 3.4与绩效评价和改进有关的术语 4 公司管理体系背景 4 组织环境 4 组织所处的环境 4 职业健康安全管理体系 4.1 公司所处的内外部环境4.1理解组织及其背景4.1理解组织及其所处的环境 4.2 相关方需求与期望分析4.2理解相关方的需求和期望4.2理解相关方的需求和期望 4.3 管理体系的范围4.3质量管理体系范围的确定4.3确定环境管理体系的范围 4.1 总要求 4.4 管理体系及其过程 4.4 质量管理体系 4.4 环境管理体系 4.1 总要求 5领导作用与员工的5领导作用5领导作用参与协商5.1领导作用及其承诺5.1领导作用和承诺5.1领导作用与承诺5.1.1总则5.1.2以顾客为关注焦点5.2管理方针5.2方针 5.2环境方针. 4.2职业健康安全方针5.2.1制定质量方针5.2.2沟通质量方针5.3组织的岗位、责任、职责和权限5.3组织的作用、职责和权限5.3组织的岗位、职责和权限 4.4.1资源、作用、职责和权限5.4职业健康安全管理的参与和协商4.4.3沟通、参与和协商5.4.1总则5.4.2应特别重视并管理非管理人员的参与5.4.3应特别重视并管理非管理人员的协商6策划6策划6策划 4.3策划(仅标题)6.1风险与机遇的应对措施6.1风险和机遇的应对措施6.1应对风险和机遇的措施6.1.1总则 6.1.1总则6.1.2环境因素 6.1.2环境因素6.1.3危险源辨识与职业健康安全风险评估4.3.1危险源辨识、风险评价和控制措施的确定6.1.4合规义务 6.1.3合规义务 4.3.2法律法规和其他要求6.1.5控制措施的策划 6.1.4措施的策划6.2目标及其实现的策划6.2质量目标及其实施的策划6.2环境目标及其实现的策划4.3.3目标、指标和方案6.2.1环境目标6.2.2实现环境目标措施的策划6.3体系变革计划 6.3变更的策划7支持7支持7支持 4.4实施与运行(仅标题)7.1资源7.1资源7.1资源 4.4.1资源、作用、职责和权限7.1.1总则7.1.1总则7.1.2人员7.1.2人员7.1.3基础设施与维护保养7.1.3基础设施7.1.4过程运行环境7.1.4过程环境 9.1 9.2 9.37.1.5 监视和测量资源7.1.5监视和测量资源9.1.1总则 4.5.1检查7.1.6组织知识7.1.6组织知识7.2能力7.2能力7.2能力4.4.2能力、培训和意识7.3意识7.3意识7.3意识7.4沟通7.4沟通7.4沟通4.4.3沟通、参与和协商7.4.1总则7.4.2内部信息交流7.4.3外部信息交流7.5形成文件的信息控制7.5形成文件的信息7.5文件化信息 4.4.4文件7.5.1总则7.5.1总则7.5.1总则 4.4.4文件7.5.2创建和更新7.5.2编制和更新7.5.2创建和更新 4.4.54.5.4文件控制记录控制7.5.3文件控制7.5.3文件控制7.5.3文件化信息的控制8运行8运行8运行 4.4实施与运行(仅标题)8.1产品和服务提供的运行策划与控制8.1运行的策划和控制8.1运行策划和控制 4.4.6运行控制8.2产品和服务的要求8.2市场需求的确定和顾客沟通8.2.1客户沟通8.2.1顾客沟通8.2.2与产品、服务有关要求的确定、评审与更改8.2.2与产品和服务有关要求的确定8.2.3与产品和服务有关要求的评审8.2.4产品和服务要求的变更8.3设计和开发8.3产品和服务的设计和开发8.3.1总则8.3.2设计和开发策划8.3.3设计和开发输入8.3.4设计和开发控制8.3.5设计和开发输出8.3.6设计和开发变更8.4外部提供的过程、产品和服务的控制8.4外部提供的过程、产品和服务的控制8.4.1总则8.4.2控制类型和程度8.4.3提供外部供方的文件信息8.5服务的提供8.5生产和服务的提供8.5.1产品和服务提供的控制8.5.1生产和服务提供的控制8.5.2标识和可追溯性8.5.2标识和可追溯性8.5.3顾客或外部供方的财产8.5.3顾客或外部供方的财产8.5.4防护8.5.4防护8.5.5交付后的活动(售后服务)8.5.5交付后活动8.5.6变更控制8.5.6变更的控制8.6产品和服务的放行8.6产品生产和服务提供8.7不合格输出的控制8.7不合格输出的控制8.8环境与职业健康安全体系的运行策划与控制8.1运行策划和控制 4.4.6运行控制8.8.1总则8.8.2层级控制8.8.3外包8.8.4基于生命周期观点的环境管理8.8.4采购与承包方的运行控制8.9环境与职业健康安全管理的变更控制8.10应急准备和响应8.2应急准备和响应 4.4.7应急准备和响应9绩效评价9绩效评价9绩效评价 4.5检查(仅标题)9.1监视、测量、分析和评价9.1监视、测量、分析和评价9.1监视、测量、分析和评价 4.5.1绩效监视和测量9.1.1总则9.1.1总则9.1.1总则 4.5.1绩效监视和测量9.1.3数据分析与评价9.1.2顾客满意9.1.2顾客满意9.1.3合规性评价9.1.2合规性评价 4.5.2合规性评价9.2内部审核9.2内部审核9.2内部审核4.5.5内部审核9.2.1总则9.2.2内部审核方案9.3管理评审9.3管理评审9.3管理评审 4.6管理评审9.3.1总则9.3.2管理评审输入9.3.3管理评审输出10改进10改进10改进10.1总则10.1总则10.1总则10.2事件、不符合和纠正措施10.2不符合和纠正措施10.2不符合和纠正措施4.5.3事件调查、不符合、纠正措施和预防措施4.5.3.1事件调查4.5.3.2不符合、纠正措施和预防措施10.3持续改进10.3持续改进10.3持续改进 4.5.4。
质量管理体系文件一览表
人事行政部
7
7 人事行政部 PY-PD-027 绩效和监视测量控制程序
8
8
人事行政部
PY-PD-029
危险源辨识、风险评价和 风险控制程序
人事行政部
人事行政部
人事行政部
9
9
国贸部
PY-PD-004
订单管理控制程序
国贸部
国贸部
10
10
国贸部
PY-PD-005
合同评审程序
国贸部
国贸部
国贸部
11
11
国贸部
149 25
56 26 PY-HR-026
年度月考核指标、权重
57 27 PY-HR-027
##制度
58 28 PY-HR-028
####制度
沟通控制程序 环境因素识别和评价控制
程序
150 26 151 27 152 28
合规性评价控制程序
153 29
记录编号 QS-QA-001 QS-QA-003 QS-QA-026 QS-QA-025 QS-QA-005 QS-QA-004 QS-HR-001 QS-HR-002 QS-HR-003 QS-HR-004 QS-HR-005 QS-HR-006 QS-HR-010 QS-HR-011 QS-HR-012 QS-HR-013 QS-HR-014 QS-HR-015 QS-HR-016 QS-HR-017 QS-HR-018 QS-HR-008 QS-HR-019 QS-HR-009 QS-HR-020
三级文件名称(支持性文件) 出差管理暂行规定
总序号 序号 125 1
32 2 PY-HR-002
费用报销流程
126 2
33 3 PY-HR-003
最新ISO质量管理体系全套实用表格
标准要求
检验结果
合格否
检验结论:
合格 ( ) 不合格 ( )
检验员: 日期: 年 月 日
不合格处置:
让步接收( ) 返工/返修 ( ) 降级 ( )
批准: 日期: 年 月 日
成品检验记录
产品名称
型号规格
生产车间
生产日期
生产数量
检验数量
检验方式
检验项目
标准要求
检验结果
合格否
检验结论:
合格 ( ) 不合格 ( )
文 件 审 批 表
文件名称
文 件 编 号
编制
审批
会审部门
签字
会审部门
签字
发 放 范 围
分发号
发放部门
分发号
发放部门
受控文件清单
编号: JL-4.2.3-02
序号
文件编号
文 件 名 称
版本
主管部门
编制: 审批:
文件更改申请(通知)单
文件名称
文件编号
申 请 人
日 期
更改原因
更改前内容
更改后内容
审批意见
签名:
备注
编制: 审批: 日期: 年 月 日
顾客满意程度调查表
顾客名称
地址
电话、传真
联系人
订购产品的时间、订购方式、产品型号、规格、数量;
对本厂产品的满意程度:
质量: □很满意 □一般 □不满意
价格: □很满意 □一般 □不满意
交货期: □很满意 □一般 □不满意
可分别说明原因:
对本厂服务的满意程度:
售后服务: □很满意 □一般 □不满意
对上述观察结果要求
原因分析
纠正
质量管理体系策划程序(体系过程文件-含附件表单)

××××××有限公司企业标准程序文件拟制:批准:受控状态:□受控□非受控发放编号:2017-7-1 发布 2017-7-1实施××××××有限公司发布质量管理体系策划程序文件编号:IQM01-2017B1 目的为确保公司质量管理体系得到有效运行及实施,使其符合GB9001:2016和GJB9001C:2017质量管理体系要求,公司在实施和执行质量管理体系之前,需要对其进行策划。
2. 范围适用于本公司质量管理体系覆盖产品所涉及到的所有过程和环节。
3 职责3.1总经理:负责制定质量方针和目标;公司组织架构的确定、职能部门的职责确定。
3.2体系中心:负责质量管理体系的策划、建立和完善以及质量管理体系所需资源的配备和确定;负责过程的识别和确定、数据的收集和分析。
3.3各部门:负责质量管理体系的实施、贯彻和落实;负责部门目标的建立和测量;负责过程目标的建立和监测。
3.4全体员工:负责质量管理体系文件各项规定的执行。
4 工作程序4.1 公司组织架构的建立和部门职能的确定4.1.1 为了质量管理体系的顺利推进,总经理依据公司经营的要求建立组织架构。
并赋予各职能部门的职责和权限并发布。
4.2质量方针和目标的建立4.2.1 为了更好的实施质量管理体系,总经理制定了质量方针和目标,各部门依据公司的总的质量目标制定本部门的质量目标并实现这个目标。
每年12月在召开管理评审会议时必须对各部门建立的目标进行全面的检讨,为下年度制定质量目标提供可靠的依据。
4.3质量管理体系和过程的策划4.3.1体系中心根据公司实际的生产和经营状况识别和建立公司质量管理体系所需要的过程,并识别这些过程先后顺序和其相互作用以及其在整个组织中的应用。
本公司质量管理体系所需的过程包括三类过程:COP顾客导向的过程 MP管理过程 SP支持过程4.3.2各部门建立和本部门相关的过程目标、测量方法、频次。
质量体系全套文件包含1-3阶文件
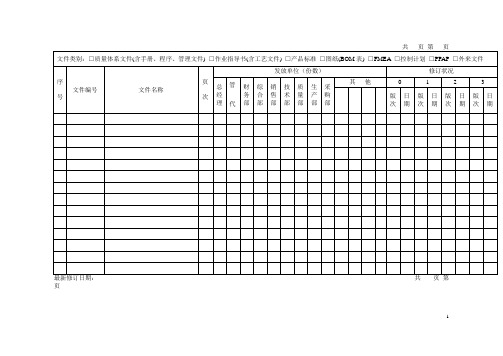
页1文件控制流程图1. 目的对质量体管理系中的文件进行规范和控制,确保文件的充分性与适宜性,确保各相关场所使用有效文件。
2. 适用范围适用于与质量管理体系有关的文件和资料的控制。
3. 职责3.1质量部负责编制质量手册,管理者代表审核,总经理批准。
3.2各相关业务主管部门负责编制相关的质量管理体系程序文件,相关部门主管审核、签字,质量部审定,管理者代表批准。
3.3各相关业务主管部门负责编制其他管理性文件,相关部门主管审核、签字,综合部审定,管理者代表批准。
3.4技术部和相关部门负责编制主管的技术文件、支持性文件,包括《工序标准操作卡》、《作业指导书》、《设备操作规程》、《检验指导书》等,并由部门主管领导审核批准。
3.5各部门设兼职文件管理员,负责本部门文件和资料的管理工作。
4. 工作程序和要求4.1文件的分类4.1.1受控文件凡质量管理体系运行的部门(含提供认证机构)、场所、班次,使用的文件均为受控文件,包括:a.质量体系文件:如质量手册、程序文件和其它质量文件(表格、报告等)。
b.管理文件:如制度等。
c.技术、支持性文件:如工程图样、工程标准、数据资料、检验指导书、试验程序等。
d.外来文件:国家标准、行业标准、法律法规、顾客工程规范、供方记录等。
4.1.2非受控文件凡于质量管理体系运行无关联的文件属于非受控文件,如行政任命、事务性通知等。
a.盖“非受控”章的文件为非受控文件,供有关人员参考用。
b.因评审、考察等用的,向上级机关或顾客提供的质量体系文件,均为非受控文件。
c.“非受控”文件,更改不通知,作废不回收。
4.1.3文件管理a.质量体系文件、管理性文件由综合部归档、控制、分发和回收。
b.技术文件由技术部归档、控制、分发和回收。
c.外来文件由各相关部门接受后进行识别,对需执行的文件按受控文件进行控制和管理。
d.各相关部门文件由各部门进行控制和管理。
4.2 文件编号4.2.1 质量手册B版文件顺序号质量手册组织简称4.2.2程序文件和管理规定/规则/细则/工作标准文件顺序号文件代号组织简称文件性质规定编码如下:程序文件-QP;管理文件-GL;支持性文件-WI;外来文件-WL。
新16949文件策划

IATF16949质量管理体系文件策划一览表ISO9001+IATF16949标准条文新标准评审意见与建议措施(某文件名称责任部门备注0.1 总则关注并理解0.2 质量管理原则正确理解七大质量管理原则,作为体0.3 过程方法关注并理解0.3.1 总则关注并理解0.3.2 PDCA 循环关注并理解0.3.3 基于风险的思维关注并理解0.4 与其他管理体系标准的关系 关注并理解1. 范围关注并理解1.1 范围——汽车行业对 ISO 9001:2015 的补充本汽车QMS标准规定了汽车相关产品(包括装有嵌入式软件的产品)的设计和开发、生产,以及(相关时) 装配、安本汽车QMS标准适用于制造顾客指定生产件、服务件和/或配件的组织的现场。
应当在整个汽车供应链中实施本汽车QMS标准。
2 规范性引用文件2.1 规范性引用标准和参考性引用标准附录A (控制计划)为本汽车QMS标准的规范性部分。
关注并理解附录B (参考书目——汽车行业补充)为参考性部分,提供了有助于理解或使用本汽车QMS标准的附加信息。
识别适用要求并转化为本公司的——附录B给出了参考书3 术语和定义修订质量手册中的部分术语(补充特定的部分《质量手册》3.1 汽车行业的术语和定义4 组织环境4.1 理解组织及其环境1.修订《经营计划控制程序》、《产品规划控制程序》,细化公司内外部环境分析要求2.修订《管理评审控制程序》,增加组织及其环境的监视和评审要求《经营计划控制程序》《产品规划控制程序》组织应确定与其宗旨和战略方向相关并影响其实现质量管理体系预期结果的能力的各种外部和内部因素。
组织应对这些外部和内部因素的相关信息进行监视和评审。
注1:这些因素可能包括需要考虑的正面和负面要素或条件。
注 2:考虑来自于国际、国内、地区或当地的各种法律法规、技术、竞争、市场、文化、社会和经济环境的因素,《管理评审控制程序》注3:考虑与组织的价值观、文化、知识和绩效等有关的因素,有助于理解内部环境。
三体系认证全套表格(很全实用)

受控文件清单一式两份,一份申请部门留存,一份报审核部门.记录清单填表人: 年月日审核(管理者代表): 批准:审核(管理者代表): 批准:实用文档文案大全年度培训计划编制; 日期:审核: 日期:批准: 日期:培训记录表设备台帐设备维修记录表车间:MZFL /JL-13设施报废单合同要求评审表批准: 年月日定单确认表合同登记台帐供方评定记录表实用文档文案大全合格供方名录编制:日期: 批准:日期:采购计划编制:日期: 批准:日期: 文案大全生产计划编制:日期: 批准:日期: 文案大全监视测量设备台帐编制: 日期:监视测量设备周期检定记录表编制: 日期:顾客满意度调查表填表人: 年月日年度内审计划审核实施计划内审检查表单位:MZFL /JL-31不符合报告内审不符合项分布表内审报告内审首(末)次会议签到表时间:MZFL /JL-35实用文档文案大全进货物资验证单2、g项(验证结果)应填写“合格”或“不合格”,其余各项合格者划符号√,否则×。
3、企业能出具检测结果者,验证d.、e、f项合格,则g项填合格,否填不合格。
4、如供方(或委托方)提供a、b、c项之一者,并经企业验证d、f项通过,即视为合格。
5、不合格品应在“备注”栏中注明拒收或退回。
不合格品报告单MZFL /JL-39纠正预防措施表统计技术应用记录外部投诉处理报告表MZFL /JL-42环境适用法律法规和其他要求清单文案大全职业健康安全适用法律法规和其他要求清单文案大全实用文档环境因素清单编制:审核:批准:实用文档年月日年月日年月日实用文档文案大全环境因素评价表重大环境因素清单编制:审核:批准:年月日年月日年月日可望施加影响的环境因素清单说明:第7项、第10项经评价为重要环境因素,不另列文。
编制:审核:批准:危险源辨识评价表辨识人:年月日文案大全重大危险源清单编制:审核:批准:年月日年月日年月日文案大全环保设备表信息交流记录表废弃物处理统计表填表:负责人:年月日环境、职业健康安全运行检查记录注:公司本部每季检查一次。
物业管理ISO 三级文件清单
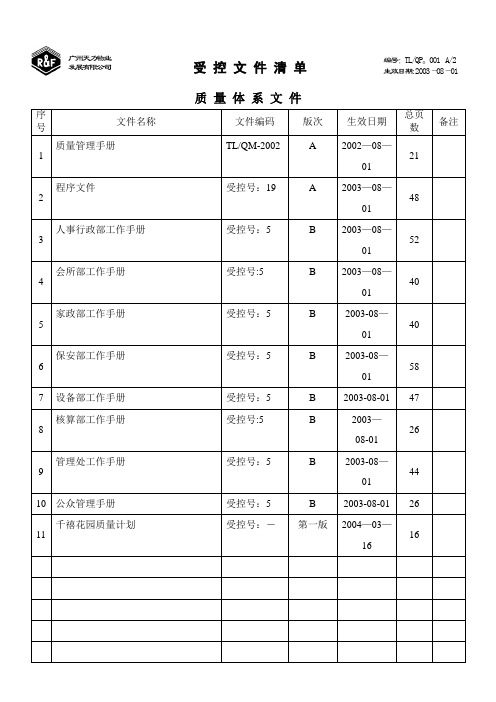
广州天力物业发展有限公司受控文件清单编号:TL/QP。
001 A/2生效日期:2003—08—01质量体系文件序号文件名称文件编码版次生效日期总页数备注1 质量管理手册TL/QM-2002 A 2002—08—01212 程序文件受控号:19 A 2003—08—01483 人事行政部工作手册受控号:5 B 2003—08—01524 会所部工作手册受控号:5 B 2003—08—01405 家政部工作手册受控号:5 B 2003-08—01406 保安部工作手册受控号:5 B 2003-08—01587 设备部工作手册受控号:5 B 2003-08-01 478 核算部工作手册受控号:5 B 2003—08-01269 管理处工作手册受控号:5 B 2003-08—014410 公众管理手册受控号:5 B 2003-08-01 2611 千禧花园质量计划受控号:-第一版2004—03—1616编制人/日期:毛桂萍/2004。
5。
15 审核人/日期:广州天力物业发展有限公司受控文件清单编号:TL/QP.001 A/2生效日期:2003—08—01序号文件名称文件编码版次生效日期备注1 文件和资料管理程序TL/QP—001 A/2 2003—08—012 内部沟通管理程序TL/QP—002 A/1 2003-08—013 基础设施控制程序TL/QP—003 A/2 2003-08-014 人力资源控制程序TL/QP-004 A/2 2003—08-015 服务要求评审控制程序TL/QP-005 A/1 2003-08—016 采购控制程序TL/QP—006 A/2 2003—08—017 标识和可追溯性控制程序TL/QP—007 A/2 2003—08—018 产品防护控制程序TL/QP-008 A/1 2003—08—019 监视和测量装置控制程序TL/QP-009 A/1 2003—08—0110 顾客满意度评价控制程序TL/QP-010 A/2 2003—08—0111 顾客满意率、满意度的计算方法TL/QP-010—01A/2 2003—08-0112 内部审核控制程序TL/QP—011 A/1 2003-08—0113 服务的监视和测量控制程序TL/QP—012 A/1 2003-08—0114 不合格品控制程序TL/QP-013 A/1 2003—08—0115 数据分析和改进控制程序TL/QP—014 A/2 2003—08-0116 质量记录管理程序TL/QP—015 A/0 2003-08—01编制人/日期:毛桂萍/2004。
管理体系文件的分类、管理、审批关系表
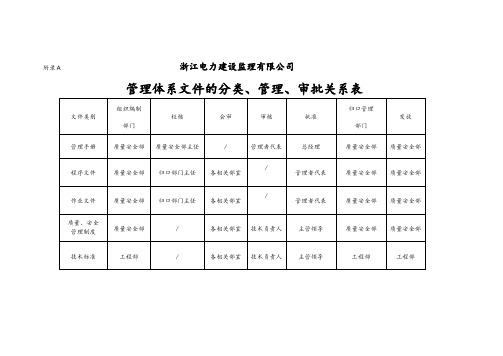
管理体系文件的分类、管理、审批关系表
工程项目监理文件的分类、管理、审批关系表
P002—R001 浙江电力建设监理有限公司
文件发放/回收记录表
文件名称文件编号版次/状态
审核:制表:共页第页注:当此表用于各部门管理体系文件分发及回收时,应同时抄送质量安全部一份.
P002-R002 浙江电力建设监理有限公司
受控文件清单
审核:编制:年月日
P002-R003 浙江电力建设监理有限公司
文件修改通知单
编号:
现对管理手册/程序文件/作业文件的部分内容进行修改:
1.共修改页,同时发送,请立即自行更换。
2.请将修改情况登记在修改记录页上.
年月日
P002-R004 浙江电力建设监理有限公司
施工图纸接收记录
审核:制表日期
P002—R005 浙江电力建设监理有限公司
施工图纸分发记录
分发单位:
审合:制表:日期:
浙江电力建设监理有限公司
受控文件作废、销毁清单
注:数量单位可为册、本、张。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验室分析结 QC SOP 035 果超出规格调 查程序
QC STP 003 支架质量标准 带药支架药物 QC STP 004 溶出度质量标 准 QC STP 005 QC STP 006 QC STP 007 QC STP 008 QC STP 009 QC STP 010 QC STP 011 QC STP 012 QC STP 013 QC STP 014 QC STP 015 QC STP 016 注射用水质量 标准 底部涂层支架 质量标准 喷涂溶液质量 标准 去污液的质量 标准 预电解溶液的 质量标准 药物涂层支架 质量标准 成型后球囊质 量标准 焊接后的球囊 导管质量标准 球囊导管组装 后质量标准 产品无菌检测 质量标准 产品细菌内毒 素检测质量标 准 底部涂层溶液 的质量标准 QC VAL 001 QC VAL 002 QC VAL 005 QC VAL 006
QC REC 016 试液配制记录 QC REC 017 注射用水细菌内毒 素检验记录 颈缩保护丝检验记 录 焊接保护丝检验记 录
QC REC 018
QC REC 019
QC REC 020 球囊管检验记录 QC REC 021 球囊外管检验记录 QC REC 022 热缩管检验记录
QC REC 023 海波管检验记录 防折金属管检验记 录
7.6
7.6
第八章
——
QDF-2A型热球 QC SOP 020 式风速仪标准 操作程序
Monitoring And Measuring Equipment EMS-9A型加 QC SOP 021 热磁力搅拌器 标准操作程序 SNUGⅢ3000 QC SOP 022 型精密天平标 准操作程序 QC SOP 023 通风橱标准操 作程序 90C-1型净化 作程序 QL-901型漩涡 QC SOP 025 混合器标准操 作程序 GMSX-208型 QC SOP 026 压力蒸汽消毒 器标准操作程 序 GW-CJ医用型 QC SOP 027 洁净工作台标 准操作程序 SK3200H型超 QC SOP 028 声波清洗器标 QC SOP 029 准操作程序 低温保存箱标 准操作程序 DRP-9082电热 准操作程序 QC SOP 031 干热灭菌器标 准操作程序
QC REC 002
QC REC 003 纯化水检验报告 QC REC 004 QC REC 005 QC REC 006 QC REC 007 QC REC 008 工序控制分析申请 及结果 纯化水电导率日常 检验记录 支架抛光后检验记 录-尺寸 支架抛光后检验记 录-外观 支架抛光后检验记 录-重量
QC STP 022
QC STP 023 QC STP 024 QC STP 025 QC STP 026
QC STP 027
QC STP 029
QC STP 030
QC STP 031 QC STP 032 QC STP 033
QC STP 034 QC STP 035 QC STP 036 QC STP 037
QC REC 063 压握检测原始记录
QC REC 064
BuMA支架药物定性 定量检测原始记录 BuMA支架涂层
QC REC 065
微粒级别检测 原始记录
BuMA支架药物涂溶 出度检测原始记录 丙酮残留量检测原 始记录 DMF残留量检测原 始记录 氯仿残留量检测原 始记录
QC REC 066 QC REC 067 QC REC 068 QC REC 069
QC REC 040 冰箱/冰柜使用记录 QC REC 041 QC REC 042 培养基增殖能力测 定记录 生化培养箱使用记 录
QC REC 043 菌种接种记录 QC REC 044 生物指示剂使用记 录
QC REC 045 菌种使用记录 QC REC 046 鲎试剂灵敏度复核 记录
QC REC 047 干扰试验记录 QC REC 048 QC REC 049 QC REC 050 洁净区沉降菌检测 记录 洁净设备沉降菌检 测记录 洁净区换气次数检 测记录表 产品初始污染菌修 正系数检测记录 产品初始污染菌检 测记录 原材料初始污染菌 检测记录 洁净区操作人员手 菌检测记录 洁净设备浮游菌检 测记录
质量管理体系文件策划表
过程对应文件 (二层文件) No. 一层文件 First level 文件编号 文件名称 ISO9001 ISO13485 规范 MDD 93/42/EEC 文件编号 QC SOP 045 Second level documents SOP 文件名称 检验和试验规 定 文件编号 QC STP 002 STP 文件名称 带药支架残留 溶剂质量标准 文件编号 标准&条款Standards & terms 三层文件 Third level documents
QC SOP 024 工作台标准操
QC SOP 030 恒温培养箱标
Sotax CE7溶 QC SOP 032 出系统标准操 作规程 赛多利斯分析 QC SOP 033 天平标准操作 QC SOP 034 程序 DDS-307型电 导率仪标准操 作程序
QC SOP 036 QC SOP 037
培养基灵敏度 检查方法 理化分析实验 室管理程序
四层文件 Fourth level documents shall be established VAL 文件名称 记录编号 记录名称 部门、车间内部文件
QC REC 001 干热灭菌器的 验证方案 高压蒸汽灭菌 锅验证方案 BuMA支架输 送器溶剂残留 BuMA支架输 送器溶剂残留
纯化水理化实验记 录 纯化水微生物限度 检验记录
热缩管质量标 准 海波管质量标 准 防折金属管质 量标准 保护丝质量标 准
QC STP 038 手柄质量标准 QC STP 039 QC STP 040 球囊保护鞘管 质量标准 Marker质量标 准
QC STP 041 内管质量标准 QC STP 042 QC STP 043 QC STP 044 QC STP 045 QC STP 046 环形保护套质 量标准 压握保护管质 量标准 洁净区浮游菌 检测试法 焊接保护管质 量标准 内包装袋-1 质 量标准
QC REC 009 注射用水检验报告 QC REC 010 QC REC 011 QC REC 012 注射用水电导率日 常检验记录 注射用水微生物限 度检验记录 注射用水理化实验 记录
QC REC 013 天平使用记录
QC REC 014 QC REC 015
高压蒸汽灭菌锅使 用记录 干热灭菌器使用记 录
PHSJ-3F型PH QC SOP 038 计标准操作规 程 鲎试剂灵敏度 QC SOP 039 复核及干扰实 验方法 Checkpoint 便 QC SOP 042 携式/在线TOC 分析仪标准操 作程序 MAS-100NT QC SOP 043 微生物空气采 样器标准操作 程序 Handheld QC SOP 044 3016型悬浮粒 子计数器标准 操作程序
QC STP 018 QC STP 019 QC STP 020 QC STP 021
初始污染菌检 测质量标准 洁净区悬浮粒 子测试法 洁净区沉降菌 测试法 洁净区操作人 员手菌检测质 量标准 西罗莫司质量 标准 生物降解药物 涂层冠脉支架 系统产品质量 产品说明书质 量标准 产品包装用纸 盒质量标准 产品标签质量 标准 产品外包装箱 质量标准 颈缩保护丝质 量标准 焊接保护丝质 量标准 球囊管质量标 准 316L不锈钢管 质量标准 球囊外管质量 标准
QC SOP 009 显微镜标准操
梅特勒XS205 QC SOP 010 分析天平操作 规程 Leica MZ95 显 QC SOP 011 微镜标准操作 程序 岛津LCQC SOP 012 2010AHT型高 效液相色谱标 准操作程序 3173R型电导 QC SOP 013 率仪标准操作 程序 DDB-303A型 QC SOP 014 便携式电导率 仪标准操作程 序 GWF-8JA型微 QC SOP 015 粒分析仪标准 操作程序 岛津FTIRQC SOP 016 8400s红外光 谱仪标准操作 程序 Alpha-Step IQ QC SOP 017 型台阶仪标准 操作规程 JSM-6510 型 QC SOP 018 扫描电子显微 镜标准操作程 序 BCJ-1型尘埃 监视和测量设备 管理程序 Management 34 EM QSMP 002 Procedure of Monitoring And Measuring QC SOP 019 粒子计数器标 准操作程序
生物指示剂无 QC STP 047 菌检测质量标 QC STP 048 QC STP 049 准 压缩空气检测 质量标准 支架压握后质 量标准
环氧乙烷残留 QC STP 050 量测定质量标 QC STP 051 准 内包装袋-2 质 量标准
QC STP 053 喷涂支架过程 检测质量标准 洁净区换气次 QC STP 054 数检测质量标 QC STP 055 准 BuMA支架系统 微粒污染质量
岛津GC-2010 QC SOP 001 Plus型气相色 QC SOP 002 QC SOP 003 谱仪标准操作 SPX-80型生化 培养箱标准操 Leica M80显微 镜标准操作程 序 立式透明门药 QC SOP 004 品冷藏箱标准 操作程序 SK2200型超声 QC SOP 005 波清洗器标准 操作程序 岛津UV-1800 QC SOP 006 型紫外分光光 度计标准操作 程序 QC SOP 007 QC SOP 008 YX280A座式电 热蒸汽压力消 岛津UV-2550 型紫外分光光 Leica M205A 作程序
QC REC 052
QC REC 053 QC REC 054 QC REC 055 QC REC 056
QC REC 057 悬浮粒子检测记录 QC REC 058 压缩空气监测报告 QC REC 059 QC REC 060 QC REC 061 QC REC 062 底涂溶液检测原始 记录 预电解溶液检测原 始记录 喷涂溶液检测原始 记录 喷涂支架过程检测 原始记录
