药品质量管理各种表格
新版药店GSP质量管理表格大全

新版药店GSP质量管理表格大全背景临床药师是医药行业中的重要职业之一,其工作内容主要包括药品的临床应用、药品质量管理、药物治疗监护等。
在医院药房及零售药店等药品销售场所,临床药师和其他药剂师在工作中要保证药品的质量和安全性,遵循国家和地方相关法规和标准。
在国内药店的质量管理中,GSP(Good Supply Practice)是一种被广泛接受的药品质量管理标准,旨在保证药品在整个存储、运输、销售和监管过程中保持适当的质量和安全性。
GSP的主要内容GSP主要包含以下内容:1.药品存储环境的控制:为确保药品质量,需要控制药品的存储环境,如温度、湿度、采光等,以保证产品的稳定性和质量。
2.药品采购、销售和运输的过程中需要进行质量控制:在药品采购、销售和运输的过程中要保证适当的质量控制,防止药品的变质和过期。
3.药品的安全管理:注重安全措施和安全管理,防止财产和人员的伤害。
4.对员工进行专业培训和技能加强:为了保证员工的专业素质和能力,要加强对员工的专业培训和技能加强。
5.药品的质量管理和监控:运用相关质量管理工具,提高药品质量管理的水平和质量控制的可靠性。
6.建立健全的药品质量管理体系:建立药品质量管理体系,保证每一个环节的质量管理都可靠有效。
GSP的核心要求GSP的核心要求主要包括以下内容:1.药品的存储环境和仓库的设施应符合规划要求。
2.建立药品的质量保证和控制体系,确保药品的管理规程符合规定。
3.验证员工的药品知识水平,并建立相应的岗位安排,确保员工的技能能够胜任相关的工作。
4.严格遵守药品交易记录和审计,防止假冒和伪劣药品的使用和流通。
5.在运输和储存过程中,要对温度、湿度、采光等方面严格控制。
6.进口药品要依据药品的相关法规验货并拥有合法的报关资料。
GSP常用的质量管理表格在GSP质量管理过程中,常用的质量管理表格主要包括以下内容:药品配送清单药品配送清单主要记录药品配送的信息,包括药品名称、批号、规格、数量、有效期等信息,以供库存管理和盘点。
药品质量信息汇总报表

占季末库存金额百分比;C、“占总销金额%”为售后查询(结案)有质量问题金额占本季总销金额百分比。
药品质量信息汇总报表
编号:填报单位:年季
药品
类别
入库验收
在库检查
售后质量查询
备注
本季
总购
进金额
ห้องสมุดไป่ตู้验收
批数
有质量问题
季末库存金额
检查
品规数
有质量问题
本季总销金额
有质量问题(结案)
批数
金额
占总购
金额%
品规数
金额
占库存金额%
笔数
金额
占总销金额%
负责人:
注:①总购进金额内包括纯购、调入和进口;总销售金额内包括纯销售、调出;总购进金额、季末库存金额、总销售金额均以统计数字为准。
药店GSP管理表格全套
编号:
通用名称
商品名称
剂 型
规 格
产品批号
有效期至
生产企业
批准文号
供货企业
购进日期
进货数量
验收人员
验收日期
不合格数量
不合格情况发现地点
不合格情况发现日期
不合格原因
保 管 员: 年 月 日
不合格情况复 查
负 责 人: 年 月 日
质量管理部意 见
负 责 人: 年 月 日
主管负责人审批意见
综
合
评
价
经审核符合规定,可以列为合格经营品种。
主管负责人: 年 月 日
备
注
填表人:
药品拒收报告单
编号:
通用名称
商品名称
检查验收人
剂 型
单 位
数 量
规 格
批 号
有效期至
生产企业
供货企业
验收时间
质量问题
保 管 员: 年 月 日
业务部门意 见
负 责 人: 年 月 日
质量管理部门意见
负 责 人: 年 月 日
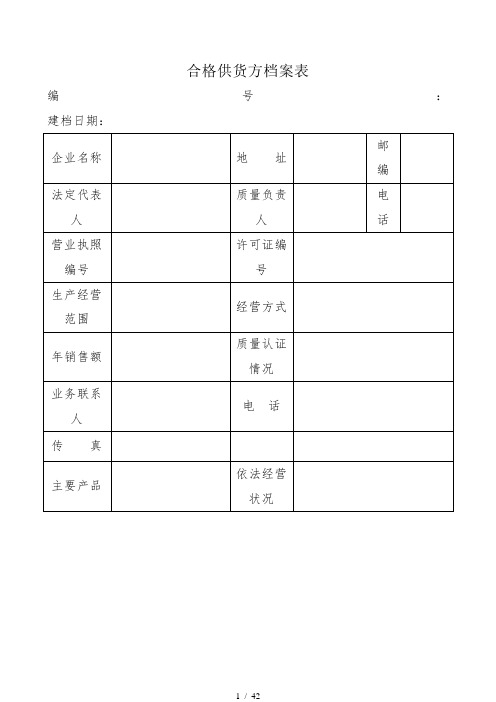
合格供货方档案表
编号: 建档日期:
企业名称
地 址
邮编
法定代表人
质量负责人
电话
营业执照编号
许可证编号
生产经营范围
经营方式
年销售额
质量认证情况
业务联系人
电 话
传 真
主要产品
依法经营状况
综
合
评
价
经审核符合规定,可以列为合格供货方。
该供货方企业编码为:
主要负责人: 质管部负责人:
年 月 日 年 月 日
备
注
药品质量档案表
GSP认证表格大全(内含31个)
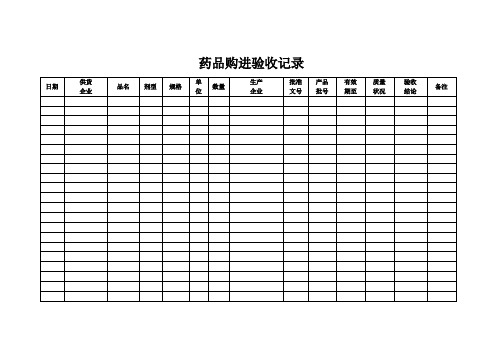
药品购进验收记录库存药品质量养护检查记录编号:检查日期:备注:1.进库达一个季度以上的药品方列入养护之列。
2.如检查中无质量问题,在质量情况一栏中,填写“正常”即可。
3.数量栏填写库存实际数量。
不合格药品报销销毁记录药品购进记录年月日药品储存记录表药品出库复核、配送记录药品质量查询、投诉、抽查情况记录库房温湿度记录表(常温库□阴凉库□冷库□)药品购进退出记录药品销后退回验收记录计量器具检定记录表制表人:年月日质量事故报告书报告单位(人):质量管理制度执行情况检查考核记录处方药留存和处方药销售记录枣庄康维药业连锁有限公司销售凭证枣庄康维药业连锁有限公司销售凭证药品缺货记录表顾客意见簿员工健康检查档案员工培训档案编号:药品质量档案表药品养护档案质量问题,应填写质量问题状况。
处理措施栏:有质量问题应填写具体处理措施,无质量问题填写“——”。
供货方档案表设施和设备及定期检查、维修、保养档案计量器具管理档案供货企业资质审批表药品资质审批表注:本表附药品生产许可证、营业执照、批准文件、质量标准、出厂检验报告书、样品、价格批文、GMP证书以及临床总结报告等资料。
不合格药品报损审批表编号:报告时间:年月日药品质量信息汇总表药品质量问题查询追踪记录表近效期药品催销表药品不良反应 / 事件报告表新的□严重□一般□医疗卫生机构□生产企业经营企业□个人□编码□□□□□□□□□□□□□□□□□□□单位名称:部门:电话:报告日期:年月日。
药品经营各环节质量风险管理评价与控制表格

环节
风险因素
产生原因
风险后果
风险评估
风险控制
药品采购
供应商问题
供应商质量管理体系不健全
药品质量不合格
高风险
严格供应商审计,确保供应商质量合规
药品储存
温度、湿度不适宜
设备故障、人员操作不当
药品效价降低、变质
中风险
定期检查储存设备,培训操作人员
药品配送
运输不当
配送车辆不符合要求,配送员操作不规范
药品损坏、变质
中风险
规范配送车辆,培训配送员
药品销售
销售假劣药品
内部管理漏洞,被不法分子渗透
对患者造成危害,企业声誉受损
高风险
加强内部管理,开展员工培训,防止假冒伪劣药品流入市场
药品退货
退货药品管理不当
退货流程不规范,退货药品未得到妥善处理
药品质量受损,可能再次流入市场
中风险
规范退货流程,确保退货药品得到正确处理
药品销毁
销Hale Waihona Puke 不彻底销毁设备不完善,操作人员不专业
药品残留可能对环境、人体造成危害
高风险
采用专业销毁设备,培训专业操作人员,确保药品彻底销毁
以上表格列出了药品经营各环节的质量风险管理评价与控制内容。在实际操作中,企业应结合自身情况和监管部门的要求,制定更详细的风险控制措施,确保药品经营过程中的质量安全。
药品质量管理制度档案表格

首营品种审批表
附表2
编号:填写日期:
合格供货方档案表
编号:建档日期:
编号:
近效期药品催销表
不合格药品台帐质量负责人:验收员:
不合格药品报损审批表
编号:日期:
不合格药品销毁台帐
批准人:经手人:
药品质量档案表
编号:建档日期:
职工健康检査档案
编号:建档日期:
( )员工培训计划
注:将培训材料、考试试卷附于表
后
培训档案表
记录人:
设施设备一览表
注:将设施设备合格证、说明书、发票附于表后
养护设备检修维护记录
:
药品质量事故报告表
附表28
附表27
顾客意见及投诉受理记录
拆零销售药品记录表原装药品名称规格包1数量单位生产日期批」
日期总量拆零量剩余量拆零人复核人
1、2、
3
、4、
5、拆零药品以最小计
拆零药品原包装在
拆零药品销完后,
拆零药品销售应有
拆零销售药品应认
I内容应填写完整;
6、原包装标签,拆零。
某药房有限公司质量管理规范全套表格模板

XXX 药房有限企业质量管理规范全套表格目录(一)、制度执行情况检查记录 (1)(二)、供货方汇总表 (3)(三)、供货方质量系统检查表 (4)(四)、合格供货方档案表 (5)(五)、药品采买计划表 (6)(六)、购进、质量查收药品目录 (7)(七)、药质量量档案表 (8)(八)、药品查收记录 (10)(九)、药品存储、摆设环境检查记录 (11)(十)、环境温湿度监测记录 (12)(十一)、近效期药品催销表 (13)(十二)、药品拆零销售记录 (15)(十三)、处方药销售分派记录 (17)(十四)、中药饮片装斗复核记录 (18)(十五)、中药方剂分派销售记录表 (20)(十六)、顾客建议征询表 (21)(十七)、药质量量问题盘问表 (22)(十八)、药质量量问题投诉、质量事故检查办理报告 (23)(十九)、药质量量信息汇总剖析表 (24)(二十)、药品销售剖析 (25)(二十一)、药质量量异常情况报告表 (26)(二十二)、不合格药品确认、报告、报损、销毁表 (27)(二十三)、药品购进退出、销退后回记录 (28)(二十四)、药品不良反响报告表 (29)(二十五)、药店员工花名册 (30)(二十六)、企业年度培训计划表 (31)(二十七)、药店员工个人培训教育档案 (32)(二十八)、药店员工个人健康档案 (33)(二十九)、企业设施设施一览表 (34)(三十)、设施、设施档案表 (35)(一)、制度执行情况检查记录检查日期:年月日检查人:序检查内容检查结果与问题采用措施复查结果号质量管理系统文件1检核查查制度2药品采买管理制度3药品查收管理制度4药品摆设管理制度5药品销售管理制度供货单位和采买品6种审察管理制度7处方销售管理制度8药品销售管理制度含麻黄碱类复方制9剂质量管理制度1记录和凭证管理制0度序检查内容检查结果与问题采用措施复查结果号1收集和盘问质量信1息管理制度1药质量量事故、质2量投诉管理制度1中药饮片处方审3核、分派、核对管1药品有效期管理制4度1不合格药品、药品5销毁管理制度1环境卫生管理制度61人员健康管理制度71供应用药咨询、指8导合理用药等药学1人员培训及核查管9理制度2药品不良反响报告0管理制度2计算机系统管理1制度2执行药品电子看守2规定管理制度(二)、供货方汇总表评为合格供货方序号供货方名称建档日期销售员姓名联系电话时间(三)、供货方质量系统检查表企业名称地址邮编法定代表人质量负责人电话营业执照编号同意证编号生产经营范围经营方式质量认证情年销售额况业务联系人电话传真E-mail主要产品依法经营状况实地察看经营场所与设施情况记录质量管理机构制度建设运输保障能力察看者:日期:综合讨论签字:日期(四)、合格供货方档案表编号:建档日期:企业名称地址邮编法定代表人质量负责人电话营业执照编号同意证编号生产经营范围经营方式年销售额质量认证情况业务联系人电话传真E-mail依法经营状主要产品况经审察切合规定,可以列为合格供货方。
药品质量不合格产品管理规程(含表格)

药品质量不合格产品管理规程(ISO9001-2015/GMP)1.0总则1.1目的:本文件规定了不合格品产生的原因、处理方式,保证产品生产质量。
1.2范围:本文件适用各种质量不符合要求的成品、中间产品、待包装产品、原辅材料、包装材料等不合格品的管理。
1.3责任:本文件由化验室负责起草,化验室主任负责审核,生产负责人负责批准;仓库保管员,化验室人员、各车间负责实施。
2.0不合格品的来源2.1.不合格品的产生主要包括两个方面:➢物料和产品的拒收➢产品的退回或召回2.2.不合格品可能来自于企业的产品放行和拒收系统。
当物料和产品不符合标准,有可能被化验室拒收而产生不合格品。
2.3造成不合格的原因造成物料和产品不符合标准的原因很多,这些原因都可能涉及质量体系的偏离。
例如:➢供应商的原因,➢运输的原因,➢贮存的原因,➢生产操作的原因,➢检验过程的原因。
3.0不合格品的标识不合格的每件物品上均应有明显的“不合格”红色标识。
由保管人员将物品搬进不合格品专门存放区域同时采取稳妥的方式挂在物品表面明显位置处。
4.0不合格品的贮存不合格品应该采取有效物理隔断与其他物品隔离存放,一般采取设置单独不合格区这种物理隔离的方式来实现隔离。
不合格物料、成品只有在化验室出具不合格报告书以后,才能将其隔离存放于不合格区域内。
并改变其质量状态为不合格。
5.0不合格成品5.1.不合格成品是指在生产过程中、仓库贮存中、市场销售环节中因运输、贮存等条件不当,造成产品内在质量不合格或外包装破损;或在生产、检验中发生重大失误造成产品内在质量不合格;或在生产过程中外包装物使用错误;批号、有效期打印错误造成不符合要求。
5.2.不合格成品的来源5.2.1.生产过程中产生的异常—由于设备清洁或清洁程序的不到位,以致于产品或产品生产之间导致交叉污染,从而影起产品质量不合格;—没有严格的按照注册工艺或规定的更衣程序生产产品,导致产品不合格。
5.2.2.中间产品或产品在最后的检验过程中,出现检验项目不合格,即超出检验标准。
药品经营质量管理记录表格完整打印版

药品经营质量管理记录表格完整打印版有效期生产厂商供货单位事故发生时间事故原因影响范围处理情况处理人签名备注药品零售企业的质量管理记录表格目录:一、药品采购记录表二、药品验收记录表三、药品陈列检查记录表四、药品养护记录表五、药品销售记录表六、中药饮片处方审核、调配核对记录表七、中药饮片清斗装斗记录表八、药品拆零销售记录表九、温湿度监测记录表十、药品质量投诉和质量事故处理记录表十一、药品不良反应报告记录表十二、不合格药品处理记录表十三、首营企业审核记录表十四、首营品种审核记录表药品采购记录表购货日期通用名称剂型规格生产厂商供货单位数量价格(中药)产地备注采购人主管负责人药品验收记录表到货日期通用名称剂型规格批准文号批号生产日期有效期生产厂商供货单位到货数量验收合格数量验收结果验收人主管负责人中药饮片验收记录表到货日期品名规格批号产地生产日期生产厂商供货单位到货数量批准文号验收合格数量验收结果验收人主管负责人药品陈列检查记录表检查日期通用名称剂型规格批号生产日期有效期生产厂商供货单位陈列数量检查合格数量检查结果陈列环境和药品摆放检查情况检查人主管负责人药品养护记录表养护日期通用名称剂型规格批号生产日期有效期生产厂商供货单位库存数量外观检查情况包装检查情况养护措施养护情况的总结分析养护人主管负责人药品销售记录表销售日期通用名称剂型规格批号生产日期有效期生产厂商购货单位经营地址联系方式销售数量单价金额记录人主管负责人中药饮片处方审核、调配核对记录表核对日期处方详情处方出具单位处方提供人员及联系方式处方审核情况审核药师签名调配情况调剂药师签名备注中药饮片清斗装斗记录表品名规格批号产地生产日期生产厂商供货单位斗内剩余数量清斗时间装斗数量装斗时间质量情况养护人主管负责人药品拆零销售记录表拆零日期通用名称剂型规格批号生产日期有效期生产厂商销售数量销售日期分拆情况复核人员签名温湿度监测记录表监测日期监测时间监测场所实时湿度实时温度异常情况处理监测人员签名备注药品质量投诉处理记录表投诉时间投诉单位基本信息投诉内容接收人处理签名时间情况核实处理结果处理人签名药品质量事故处理记录通用名称剂型规格批号生产日期有效期生产厂商供货单位事故发生时间事故原因影响范围处理情况处理人签名备注药品不良反应报告记录表通用名称:未填写剂型规格:未填写批号:未填写生产日期:未填写有效期:未填写生产厂商:未填写不良反应发生时间:未填写不良反应过程描述:未填写不良反应处理措施:未填写不良反应处理结果:未填写记录人:未填写签名:未填写不合格药品处理记录表通用名称:未填写剂型规格:未填写批号:未填写生产日期:未填写有效期:未填写生产厂商:未填写不合格原因:未填写发现时间:未填写处置措施:未填写处置时间:未填写处置结果:未填写记录人:未填写主管负责人:未填写日期:未填写首营企业审核记录表供货企业名称:未填写经营或生产地址:未填写统一社会信用代码:未填写药品经营或生产许可证号:未填写有效期限:未填写经营范围及方式:未填写代表品种质量状况:未填写相关印章及随货同行单的审核情况:未填写银行开户信息审核结果:未填写审核人:未填写主管负责人:未填写日期:未填写首营品种审核记录表品种通用名称:未填写剂型规格:未填写批准文号:未填写生产日期:未填写有效期:未填写批号:未填写以上记录表存在大量未填写的信息,无法提供有效的记录和参考。
零售药店GSP质量管理表格(全套药监版)

零售药店GSP质量管理表格(全套药监版)为了加强药品质量管理,保障公众健康,药品监管机构制定了一系列药品质量管理规范,其中包括药品经营质量管理规范(GSP)。
药品经营企业需按照规范制定和执行相应的管理制度和标准操作规程,确保符合药品质量管理要求。
本文将分享一份零售药店GSP质量管理表格(全套药监版),希望有所帮助。
表格说明该表格为零售药店GSP质量管理表格(全套药监版),共包括以下9个部分:1.企业概况及管理2.人员管理3.质量管理制度4.财务管理5.订单及采购管理6.库存管理7.营业管理8.药品安全技术管理9.环境卫生管理这份表格包含了零售药店质量管理的方方面面,涉及企业概况、人员管理、质量管理制度、财务管理、订单及采购管理、库存管理、营业管理、药品安全技术管理和环境卫生管理等多个方面,是一份实用性很高的表格。
使用这份表格可以让零售药店更好地遵守药品质量管理规范,提升经营管理水平,保障药品质量和公众健康。
GSP质量管理表格(全套药监版)内容预览以下是GSP质量管理表格(全套药监版)的内容预览,其中每个部分又包含若干小项,具体内容可参考表格。
1. 企业概况及管理•企业基本情况•药品经营许可证及资质证书•组织机构及管理人员•药品储存条件及设施2. 人员管理•岗位职责分工•员工资格证书及考核情况•员工培训记录3. 质量管理制度•质量保证体系文件•质量手册•SOP制度文件•质量监控体系文件4. 财务管理•资产清查记录•投资决策记录•财务预算•账目核对5. 订单及采购管理•采购计划和订单•采购员资格证书及考核情况•采购记录•采购验收记录6. 库存管理•记录及清点流程、频次•库存盘点记录•贮藏条件及环境记录•库存商品销毁记录7. 营业管理•市场定位及推广•营业额及毛利分析•客户投诉记录•售后服务记录8. 药品安全技术管理•药品质量安全管理制度•环境检测及相关记录•药品检验记录•不良反应监测及记录9. 环境卫生管理•环境卫生及清洁制度•废弃物管理及相关记录•消毒记录及消毒剂配制记录•安全管理制度及相关记录如何使用GSP质量管理表格(全套药监版)该表格可以按照企业实际情况进行填写和使用,以达到质量管理的目的。
药剂科药品质量管理检查表

相关管理记录
1、温湿度记录是否完整。
2、近效期记录是否完整。
3、出入库记录是否完整.
4、报损记录是否完整.
5、调剂差错记录是否完整.
6、麻精空安瓿回收及销毁记录是否完整。
7、验收记录是否完整。
卫生管理
1、在岗人员是否穿戴整洁、佩戴胸卡。
2、手卫生是否符合规范。
3、摆药架是否整洁,药品外、墙角、窗台、电脑等无积尘。
6、中药药斗是否清洁,无散落药粉。
岗位检查
1、在岗人员是否按排班表上岗。
2、是否有迟到、早退、擅自离岗等行为。
处方调剂检查
1、有无用药交代,是否详尽。
2、药师审核、调配、发药程序是否符合规范。
药剂科药品质量与安全管理检查表
检查项目
检 查 细 项
检查结果
意见及整改措施
安全管理
1、门、窗、监控等安防设施是否正常
2、消防器材是否正常。
药品储存管理
1、药品存放是否符合规定
2、药品储存条件(避光、冷藏等)是否符合规定。
3、药品是否按“先产先出,近效先出”摆放.
4、摆药架有无过期、破损等药品.
5、中药材是否有质量问题(如虫蛀,霉变等)
3、中药分剂量是否按称量减重法,差异为±5%。
4、是否注明患者姓名、药名,用法用量、有效期、注意事项等
5、合理用药咨询服务情况
拆零药品管理
1、拆零药品区域是否整洁,无杂物
2、拆零用具(药匙、药袋等)是否洁净。
3、拆零药品是否标明药名、规格、效期等内容.
4、拆零记录是否完整。
检查人年月日
零售药店质量管理制度及各种表格

______药店质量管理体系文件——————药店质量管理体系文件使用说明1、该书仅作为巴南区药品零售企业建立质量管理体系文件的参考文件。
2、该书不作为GSP认证的标准,药品零售企业必须根据企业实际情况对文件进行修改。
3、企业必须根据组织机构职能框架图和GSP规定,合理设置本企业的各岗位。
4、企业认为该文件可行的,可根据实际情况对文件的相关内容进行增减后,将相关内容修改完成后签发,作为企业内部的质量管理体系文件。
目录一、质量管理制度1、质量管理体系文件管理制度2、质量管理体系文件检查考核制度3、药品采购管理制度4、药品验收管理制度5、药品陈列管理制度6、药品销售管理制度7、供货单位和采购品种审核管理制度8、处方药销售管理制度9、药品拆零管理制度10、含麻黄碱类复方制剂质量管理制度11、记录和凭证管理制度12、收集和查询质量信息管理制度13、药品质量事故、质量投诉管理制度14、中药饮片处方审核、调配、核对管理制度15、药品有效期管理制度16、不合格药品、药品销毁管理制度17、环境卫生管理制度18、人员健康管理制度19、药学服务管理制度20、人员培训及考核管理制度21、药品不良反应报告规定管理制度22、计算机系统管理制度23、执行药品电子监管规定管理制度二、各岗位管理标准1、企业负责人岗位职责2、质量管理人员岗位职责3、药品采购人员岗位职责4、药品验收人员岗位职责5、营业员岗位职责6、处方审核、调配人员岗位职责三、操作程序1、质量体系文件管理程序2、药品采购操作规程3、药品验收操作规程4、药品销售操作规程5、处方审核、调配、审核操作规程6、中药饮片处方审核、调配、核对操作规程7、药品拆零销售操作规程8、含麻黄碱类复方制剂销售操作规程9、营业场所药品陈列及检查操作规程10、营业场所冷藏药品存放操作规程11、计算机系统操作和管理操作规程四、质量记录表格1、文件编制申请表2、制度执行情况检查记录3、供货方汇总表4、供货方质量体系调查表5、合格供货方档案表6、采购计划表7、购进质量验收药品目录8、药品质量档案表9、药品购进、质量验收纪录10、药品储存、陈列环境检查记录11、环境温湿度监测记录12、近效期药品催销表13、药品拆零销售记录14、处方药销售调配销售记录15、中药饮片装斗复核记录16、中药方剂调配销售记录17、顾客意见征询表18、药品质量问题查询表19、药品质量问题投诉、质量事故调查处理报告————————药店管理文件1、目的:规范本企业质量管理体系文件的管理。
