武汉化学2011分析和无机化学
化学专业无机化学教材及主要参考书

化学专业《无机化学》主要参攻读物配套教材1、北京师大,华中师大,南京师大.无机化学(第四版) .北京:高等教育出版社.2003.1. (面向21世纪课程教材,获优秀教材一等奖,针对高等师范院校编写的教材,理论阐述深度适当,讲解清楚;并注意运用基本理论去解释无机物质的变化规律。
)2、申泮文.近代化学导论.北京:高等教育出版社.2002.1(面向21世纪课程教材,共有四部分: 基本化学原理;溶液平衡和化学分析;元素化学;近代化学热点。
)3 、武汉大学,吉林大学.无机化学(第二版).北京:高等教育出版社.(获国家优秀教材一等奖,高等教育出版社。
内容覆盖面较广,知识点讲解详细,条理清晰,有利于学生自学,有利于学生今后报考综合性大学研究生时,用做复习资料。
)4、傅献彩.大学化学.北京:高等教育出版社.1999.9(化学理科,面向21世纪课程教材,“九五”国家级重点教材,面向21世纪课程教材.将无机化学和化学分析的教学内容融合,上册以化学原理为主,将定量分析纳入化学平衡;下册以元素化学为主。
)5、天津大学.无机化学 (第三版).北京:高等教育出版社.2002.7(面向21世纪课程教材)6、史启祯.无机化学与化学分析(第二版).北京:高等教育出版社.2005.5.(1992年由教育部化学教学指导委员会立项, 列为国家“八五”重点教材.1998年由高教社出版, 2000年被列为国家“面向21世纪课程教材”)7、唐宗熏.中级无机化学.北京:高等教育出版社.2003.(普通高等教育“十五”国家级规划教材,介于无机化学和高等无机化学之间的中级水平的无机化学教材。
系统介绍了现代无机化学所涉及的新理论、新领域、新知识和无机新型化合物。
)8、傅献彩.大学化学.北京:高等教育出版社.(面向21世纪课程教材.将无机化学和化学分析的教学内容融合,上册以化学原理为主,将定量分析纳入化学平衡;下册以元素化学为主)9、申泮文.无机化学. 北京:化学工业出版社. 2002.(面向21世纪课程教材. 编写者均为名校专家,以专题形式撰写无机化学的近代成就与发展现状,各专题选录文献水平为当代国际前沿。
无机及分析化学实验教学大纲

《无机及分析化学实验》教学大纲【课程编号】【学时学分】120 学时;【开课模式】必修【实验学时】36 学时【上机学时】【课程类型】专业课【考核方式】考试【先修课程】【开课单位】石油化工学院【授课对象】石油化工生产技术、精细化学品生产技术、有机化学品分析、煤化工一、教学目的与任务无机化学和分析化学是一门实验科学为主的基础课程。
实验是无机化学不可缺少的一个重要组成部分,是培养学生独立操作、观察记录、分析归纳、撰写报告等多方面能力的重要环节。
学生通过无机及分析实验课的学习,不仅加深对分析化学基础理论的理解,而且学习和掌握分析化学实验的基本知识、基本操作和基本技能,树立严格的“量”的概念。
培养学生实事求是的科学态度和严谨的科学作风、良好的实验室工作习惯,使其初步具备作为高级工程技术应用型人才的要求。
掌握常量组分定量分析的基础知识和基本操作。
1、掌握常用仪器分析的基本知识和基本操作技术。
2、掌握实验数据的误差分析和统计处理方法。
实验是化学与材料科学学院各专业本科生的一门必修的、独立的基础实验课。
课程的安排服从“一体化、渐定式、多层次、开放式”的教学体系和模式。
着力于培养学生具有宽广的基础知识和熟练的基本技能、能够适应未来社会发展需要的专业人才。
教学内容着眼于为学生今后的发展奠定基础。
学生在学习无机化学专业理论知识的同时,通过实验研究活动,学习和掌握无机化学专业的基本实验技术,研究元素的单质及其化合物的重要性质,熟悉重要无机化合物的制备方法;加深理解和掌握无机化学基本理论和基础知识;比较牢固地掌握化学实验的基本知识和操作技能;培养学生严谨的科学态度;培养学生准确观察化学反应现象,处理实验数据的能力,达到训练学生基本理论知识的综合应用能力。
课程的任务包括:(一)实验室一般知识介绍1.在全部教学过程中,应始终坚持对学生进行实验室安全和爱护公物的教育。
2.简介有效数字和误差理论。
3.介绍正确书写实验记录和实验报告的方法。
无机化学

Ø 系统状态发生任何的变化称为过程; Ø 实现一个过程的具体步骤称途径。
思考:过程与途径的区别。
始态
恒温过程
25℃ ,105 Pa
25℃ ,5×105 Pa
恒压过程
恒压过程
100℃ ,105 Pa
100℃ ,5×105 Pa
恒温过程
终态
附图1.3 不同途径的示意图
37
四、热和功
体系和环境之间的两种能量传递形式。单位:kJ或J。 1. 定义 热:在物理或化学变化的过程中,体系与环境之间因温差而传 递的能量。 功:在物理或化学变化的过程中,体系与环境之间除热之外以 其他形式传递的能量。
24
二、反应进度( ξ )
反应进度ξ 的定义:对于反ห้องสมุดไป่ตู้0=ΣνBB
d dnB B
nB 为物质B的物质的量,d nB表示微小的变化量。 或定义
nB()nB(0) B
25
由上式可见: ⑴对于一定的计量方程式,νB为定值,所以ξ随物质B的物质的 量变化ΔnB而变化。ξ可以反映反应的程度,所以称为反应进度。
5
(3)单位换算
英文 中文 符号 举例
103 kilo
千
k
kg
10-3 milli 毫
m ml,mg
10-6 micro 微
u ug,ul
10-9 nano 纳
n nm,ng
6
2. 有效数字 (1)有效数字的含义:有效数字是指实际测量得到 的数值,允许最后一位是估计数值。 例如:分析天平的最小刻度为0.0001g,读数必须精 确到0.0001g,没有估读。
1. 本门课程常用的计量单位 (1)基本单位: 长度l(m);时间t(s);质量m(kg);电流强度I(A);热力学温度 T(K);物质的量n(mol)。 (2)常用的导出单位: 频率v(Hz=s-1);压强p(Pa= N·m-2);能量、功、热(J=N·m);电 压、电动势E(V=J•C-1);体积V (m3=103dm3);密度ρ(kg•m-3); 物质的量浓度c(mol•L-1)
《无机化学》习题解析和答案

1、教材《无机化学》北京师范大学、华中师范大学、南京师范大学无机化学教研室编,高等教育出版社,2002年8月第4版。
2、参考书《无机化学》北京师范大学、华中师范大学、南京师范大学无机化学教研室编,高等教育出版社,1992年5月第3版。
《无机化学》邵学俊等编,武汉大学出版社,2003年4月第2版。
《无机化学》武汉大学、吉林大学等校编,高等教育出版社,1994年4月第3版。
《无机化学例题与习题》徐家宁等编,高等教育出版社,2000年7月第1版。
《无机化学习题精解》竺际舜主编,科学出版社,2001年9月第1版《无机化学》电子教案绪论(2学时)第一章原子结构和元素周期系(8学时)第二章分子结构(8学时)第三章晶体结构(4学时)第四章配合物(4学时)第五章化学热力学基础(8学时)第六章化学平衡常数(4学时)第七章化学动力学基础(6学时)第八章水溶液(4学时)第九章酸碱平衡(6学时)第十章沉淀溶解平衡(4学时)第十一章电化学基础(8学时)第十二章配位平衡(4学时)第十三章氢和稀有气体(2学时)第十四章卤素(6学时)第十五章氧族元素(5学时)第十六章氮、磷、砷(5学时)第十七章碳、硅、硼(6学时)第十八章非金属元素小结(4学时)第十九章金属通论(2学时)第二十章s区元素(4学时)第二十一章p区金属(4学时)第二十二章ds区元素(6学时)第二十三章d区元素(一)第四周期d区元素(6学时)第二十四章d区元素(二)第五、六周期d区金属(4学时)第二十五章核化学(2学时)1 .化学的研究对象什么是化学?●化学是研究物质的组成、结构、性质与变化的一门自然科学。
(太宽泛)●化学研究的是化学物质(chemicals) 。
●化学研究分子的组成、结构、性质与变化。
●化学是研究分子层次以及以超分子为代表的分子以上层次的化学物质的组成、结构、性质和变化的科学。
●化学是一门研究分子和超分子层次的化学物种的组成、结构、性质和变化的自然科学。
无机及分析化学第一章 气体、溶液和胶体

设有一混合气体,有 i个组分,pi和ni分别表示各组 分的分压力和物质的量,V为混合气体的总体积,则
pi=(ni/V) ·RT p=pi=(ni/V)·RT =(n/V)·RT pi/p=ni/n pi = ( ni/n )·p
第二节 溶 液
第一章第二节
广义地说,两种或两种以上的物质均匀混合而且彼 此呈现分子(或离子或原子)状态分布者均称为溶液, 溶液可以气、液、固三种聚集状态存在。
ppb(十亿分浓度):表示溶质的质量占溶液质量 的十亿分之几,即每kg溶液中所含溶质的g数。如:
1ppb:1g/1,000,000,000g溶液=1g溶质/1kg溶液。 8ppb:8g/1,000,000,000g溶液=8g溶质/1kg溶液。
例 题 1-1
第一章第二节
在100 mL水中,溶解17.1 g蔗糖(C12H22O11),溶液 的密度为1.0638 g ·mL1,求蔗糖的物质的量浓度、质 量摩尔浓度、摩尔分数各是多少?
LOGO
无机及分析化学第一章 气体、溶液和胶体
化学学科的分类
1. 无机化学 2. 分析化学 3. 有机化学 4. 物理化学 5. 高分子化学
化学学科的重要性
化学学科与其它学科的相互渗透,形成新 的学科,如生物化学、环境化学、环境分析化 学、食品化学、农药化学、土壤化学、植物化 学、配位化学、放射化学等。
第一章第二节
在100 mL水中,溶解17.1 g蔗糖(C12H22O11),溶液 的密度为1.0638 g ·mL1,求蔗糖的物质的量浓度、质 量摩尔浓度、摩尔分数各是多少?
解:
( 2 )b ( C 1 2 H 2 2 O 1 1 )= n ( C m 1 ( 2 H H 2 2 O 2 O ) 1 1 ) 1 0 0 0 .0 1 5 0 3 0 .5 m o lk g 1
学生学习座谈会问题归纳

部学生学习座谈会问题归纳:会议时间:2011年11月24日会议主持:应用化学系教学副主任李继睿与会人员:应用化学系系主任兰立新、系部教学干事徐佳生化教研室主任刘军冶金教研室主任刘勇刚等辅导员:张渺岚、钟娜学生代表:各班班长、学习委员、考勤副班长等为了配合学院期中教学检查工作,我系于2011年11月24日,召开了全系学生学习座谈会。
会议由教学副主任李继睿主持,我系系主任、教师代表、各班学生代表共70余人参加。
会上,同学们针对在学习中、生活中遇到的各种问题纷纷发表了自己的意见与建议,现将大家反映比较集中的问题总结归纳如下:一、课堂教学方面:1、有些教师使用方言授课,学生难以理解授课内容,学习兴趣大大降低。
2、少数教师教学不够灵活,内容空洞、课堂气氛沉闷,课堂纪律不好。
3、分析2011级新生班反映专业基础课授课进度太快,如无机化学课,希望授课老师结合班级同学实际情况适当调整授课进度。
4、制药2010级学生反映,他们班周课时超30节,课程开设太多、试验多,学生学习压力过大,学习效率较低。
5、英语课程教学方面,某些教师授课中语法内容所占比例太大,不注重口语教学,对于学生英语A级报名,授课教师未能及时通知及推荐班级学生参加,延误了学生的报名。
6、某些教师在课堂上推销个人编写的教材,强行要求学生购买,如就业指导课。
7、实验室天枰称量不精准,学生在称量过程中需要花费大量的时间,试验数据容易出现误差。
8、某些实验室老师,在学生做实验的过程中,指导不够耐心,试验药品用完未及时添加。
二、外出实习及学生就业方面1、学生外出实习的安排未提前告知学生,导致班上学生议论纷纷,错以为学校未安排其专业外出实习。
2、对于学生外出实习,希望系部相关负责的老师能够对实习情况进行具体的讲解并及早通知。
如:实习时间、实习安排、实习单位情况、实习要求等。
3、部分学生就业方向不明确,对所学专业的就业情况不了解。
就业信心不足。
三、学生餐饮方面1、学生在学校食堂就餐,经常会碰到吃到异物的的现象,如:螺丝钉等。
无机与分析化学

无机及分析化学
课程代码 81049001
课程名称无机及分析化学
英文名称Inorganic and analytical chemistry
学分:4.5 开课学期:第1 学期
授课对象:生物科学、生物技术专业先修课程:高中化学
课程主任:张英珊副教授硕士
课程简介
《无机及分析化学》是生物科学及生物技术专业学生学习的第一门基础化学课。
本课程以化学的基本原理如原子和分子结构理论、化学热力学、化学动力学以及化学平衡为主线,将平衡理论与相应的滴定分析方法融合在一起,把主族元素及其化合物的性质和过渡金属作为元素周期表的应用来讨论。
最后还介绍了仪器分析的基本方法,如电化学和光谱法。
这种编排方法的优点是:使难点得以分散,理论与实际结合的更为紧密,使学生对所学理论的实际应用之认识更加清晰、透彻;与无机及分析化学实验课匹配更加容易。
这对增加学生对化学学科的全面认识,以及增加他们学习化学的兴趣将起到重要的作用。
实践教学环节:
课程考核:课程最终成绩=期末考试成绩
指定教材
[1]General Chemistry, ZHANG Yingshan, Beijing, Chemical Industry Press,2005.
[2 ] 无机及分析化学(Ⅲ)南京大学“无机及分析化学”编写组,高等教育出版社
分析化学武汉大学主编,高等教育出版社
参考书目
[1 ] Contemporary Instrumental Analysis Kenneth A Rubinson
[2 ] 化学原理华彤文方锡义等译,北京大学出版社
[3 ] 无机化学大连理工大学无机教研室编,北京,高等教育出版社,2001。
《分析化学C》课程教学指导大纲

精心整理《分析化学C》教学大纲一、课程基本信息1、掌握酸碱滴定、沉淀滴定、重量分析、氧化还原滴定、配位滴定基本原理和分析方法;理解实验中的数据记录、处理和误差分析;2、与分析化学实验相结合,使学生初步建立起严格的“量”的概念;具备化学实验操作的基本能力和化学分析与检测的初步能力;3、通过本课程的学习,培养学生观察、分析、解决问题的能力;4、培养学生严肃认真、实事求是的良好作风。
三、课程目标、教学目标与毕业要求对应关系(一)绪论与滴定分析概述1、基本要求了解分析化学的任务、作用,明确本课程的学习要求,熟悉分析方法的分类法、滴定分析的基本概念和滴定分析的基本计算。
2、主要内容:滴定分析基本概念;滴定分析法分类;滴定分析对化学反应的要求;标准溶液的配制与标定;滴定分析计算。
3、重点与难点重点:滴定分析基本概念、滴定分析法分类、滴定分析对化学反应的要求、标准溶液的配制与标定、滴定分析计算。
4、作业或报告作业1:滴定分析计算3~4题。
(二)误差和数据处理1、基本要求熟悉误差产生原因、分类及消除方法;了解随机误差的正态分布;理解测定值的准确度与精密度概念及其表征;熟悉提高分析结果准确度的方法;掌握有效数字及其修约规则。
2、主要内容341~2题12(碱)分步滴定的条件;酸碱滴定法的应用及计算。
3、重点与难点(1)重点:酸碱溶液pH的计算;酸碱滴定曲线;滴定突跃;指示剂的选择;一元弱酸(碱)准确滴定和多元弱酸(碱)分步滴定的条件;酸碱滴定法的应用及计算。
(2)难点:酸碱溶液pH的计算;酸碱滴定法的应用及计算。
4、作业或报告作业3:分布系数1题,溶液平衡基本关系1题,pH计算2~3题,酸碱滴定及其应用3~5题。
(四)配位滴定法1、基本要求了解EDTA及其与金属离子配合的特点;掌握稳定常数、不稳定常数累积稳定常数和逐级稳定常数的概念和关系;熟悉副反应系数和条件常数的计算;理解配位滴定原理;理解配位滴定的酸效应曲线;了解金属指示剂的作用原理;掌握金属离子准确滴定的判据,了解提高配位滴定选择性的方法;掌握配位滴定的应用和计算。
无机化学实验 武汉大学化学与分子科学学院

无机及分析化学实验无机化学实验参考讲义2011级 下学期目录第一部分 无机化学实验室基本知识、操作技能与常用仪器设备的使用.........1 第二部分 实验部分 (13)实验1 由粗实验制备试剂级氯化钠 (13)实验2 五水硫酸铜的制备及其医药学用途 (18)实验3 由废白铁制备硫酸亚铁和硫酸亚铁铵 (21)实验4 未知物鉴别实验I (24)实验4 未知物鉴别实验II (28)实验 6 茶叶中无机微量元素的分离及鉴别 (31)* 碳酸钠制备实验见《无机及分析化学实验》教材 P139* 如果你对实验讲义有任何意见和建议,欢迎提出来,我们会积极改进。
可与指导老师交流也可写邮件至kaihu@邮箱。
谢谢!第一部分 无机化学实验室基本知识、操作技能与常用仪器设备的使用一常用玻璃仪器的洗涤:1. 洗涤干净的标准除水分子以外无其它任何杂物,洁净透明;附在仪器壁的水不成股流,器壁不挂水珠,表面留有一层均匀而薄的水膜。
2. 洗涤方法(1)用水刷洗:用毛刷刷洗仪器,可以去掉附着的尘土、可溶性物质和易脱落的不溶性杂质。
根据仪器的大小和形状选择合适的毛刷,注意避免毛刷前端的铁丝撞破或损伤仪器。
(2)用去污粉或合成洗涤剂刷洗:去污粉是由碳酸钠、白土、细沙等混合而成的。
它是利用碳酸钠的碱性、细沙的磨擦作用和白土的吸附作用,实现对仪器的清洗。
使用时先将待洗容器用水湿润(必需用少量水),然后用打湿的毛刷沾取少量去污粉擦洗。
仪器内、外壁经擦洗后,先用自来水洗去粘附的去污粉颗粒,然后用蒸馏水洗三次,洗去自来水中带来的钙、镁、铁、氯等离子。
每次蒸馏水的用量要少些,注意节约(采取“少量多次”的原则)。
用合成洗涤剂刷洗玻璃仪器的方法类似。
(3)用洗液洗:在进行精密的定量实验时,对仪器洁净的程度要求很高,或所用仪器容积精确、形状特殊、不能用刷子刷洗时,可用洗液清洗。
通常用的洗液有铬酸洗液、碱性高锰酸钾洗液和以氢氧化钠或碳酸钠为主要成分的强碱洗液。
河南大学硕士研究生考试大纲材料学院(学硕)
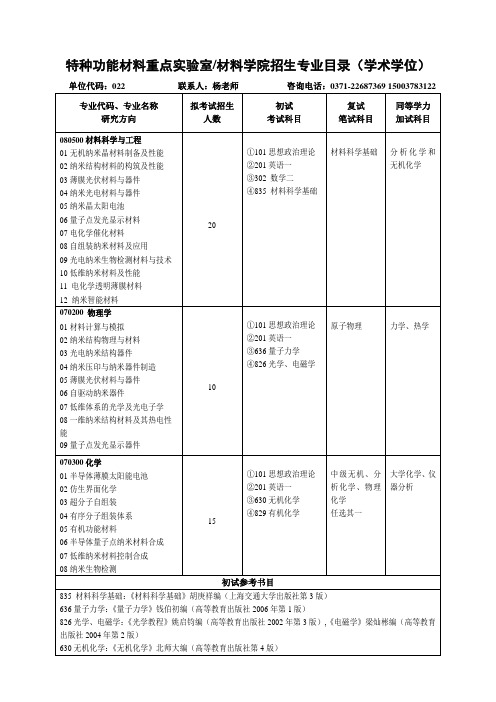
特种功能材料重点实验室/材料学院招生专业目录(学术学位)单位代码:022联系人:杨老师咨询电话:0371-2268736915003783122专业代码、专业名称研究方向拟考试招生人数初试考试科目复试笔试科目同等学力加试科目080500材料科学与工程01无机纳米晶材料制备及性能02纳米结构材料的构筑及性能03薄膜光伏材料与器件04纳米光电材料与器件05纳米晶太阳电池06量子点发光显示材料07电化学催化材料08自组装纳米材料及应用09光电纳米生物检测材料与技术10低维纳米材料及性能11电化学透明薄膜材料12纳米智能材料20①101思想政治理论②201英语一③302数学二④835材料科学基础材料科学基础分析化学和无机化学070200物理学01材料计算与模拟02纳米结构物理与材料03光电纳米结构器件04纳米压印与纳米器件制造05薄膜光伏材料与器件06自驱动纳米器件07低维体系的光学及光电子学08一维纳米结构材料及其热电性能09量子点发光显示器件10①101思想政治理论②201英语一③636量子力学④826光学、电磁学原子物理力学、热学070300化学01半导体薄膜太阳能电池02仿生界面化学03超分子自组装04有序分子组装体系05有机功能材料06半导体量子点纳米材料合成07低维纳米材料控制合成08纳米生物检测15①101思想政治理论②201英语一③630无机化学④829有机化学中级无机、分析化学、物理化学任选其一大学化学、仪器分析初试参考书目835材料科学基础:《材料科学基础》胡庚祥编(上海交通大学出版社第3版)636量子力学:《量子力学》钱伯初编(高等教育出版社2006年第1版)826光学、电磁学:《光学教程》姚启钧编(高等教育出版社2002年第3版),《电磁学》梁灿彬编(高等教育出版社2004年第2版)630无机化学:《无机化学》北师大编(高等教育出版社第4版)829有机化学:《有机化学》胡宏纹编(高等教育出版社第2版或第3版)复试笔试科目参考书材料科学基础:《材料科学基础》胡庚祥编(上海交通大学出版社第3版)原子物理:《原子物理学》褚圣麟编(高等教育出版社第4版)中级无机:《中级无机化学》朱文祥编(高等教育出版社2004版)分析化学:《分析化学》武汉大学编(高等教育出版社第6版)物理化学:《物理化学》傅献彩编(高等教育出版社第5版)同等学力加试参考书无机化学:《无机化学》北师大编(高等教育出版社第4版)分析化学:《分析化学》武汉大学编(高等教育出版社第6版)力学:《力学》漆安慎、杜婵英编(高等教育出版社2012年第3版,十二五普通高等教育本科国家级规划教材)热学:《热学》秦允豪编(高等教育出版社2011年第3版,十二五普通高等教育本科国家级规划教材)大学化学:《新大学化学》周伟红编(科学出版社第4版)仪器分析:《仪器分析》胡坪编(高等教育出版社第5版)。
《无机及分析化学》课程教学大纲

《无机及分析化学》课程教学大纲一、课程简介
二、 课程目标
本课程的课程目标如表1
所示:
三、
课程目标与毕业要求对应关系
本课程的课程目标对毕业要求指标点的支撑情况如表2所示:
四、 课程目标与教学内容和方法的对应关系
五、实践环节及要求(无)
详细说明每个实践环节主要内容和基本要求两方面。
六、学时分配
各章节的学时分配如表4所示。
七、课程学生成绩评定方法
1.课程考核与成绩评定方法
各部分的具体评价环节、关联课程目标、评价依据及方法和在总成绩中的占比,如表5所示。
八、教学资源
九、课程目标达成情况评价
在课程结束后,需要对每一个课程目标(含思政课程目标)进行达成情况进行定性和定量评价,用以实现课程的持续改进。
其中课程目标达成情况的定量评价算法如下:
1.使用教学活动(如课程思政实践、课后作业、课堂练习、单元测验、实验验收、演讲、课堂讨论、互动、阅读报告、大作业等等)成绩或期末考试部分题目得分率作为评价项目,来对某个课程目标进行达成情况的定量评价;
2.为保证考核的全面性和可靠性,要求对每一个课程目标的评价项目选择超过两种;
3.根据施教情况,评价项目可以由教师自行扩展,权重比例可以由教师自行设计;
4.对某一个课程目标有支撑的各评价项目权重之和为1;
5.使用所有学生(含不及格)的平均成绩计算。
十、说明
本课程大纲自2020级开始执行,生效之日原先版本均不再使用。
无机及分析化学-PPT课件精选全文

溶液的浓度 0.02080 mol/L
四位有效数字
溶液的浓度 0.10 mol/L
二位有效数字
被测物含量 56.12%
四位有效数字
平衡常数 K=1.8x10
二位有效数字
pH值(注) 12.08
二位有效数字
pH值
5.1
一位有效数字
注:
考虑pH值的有效数字时,因为pH值是氢离子浓度 的负对数,所以pH值的有效数字位数只考虑小数点后 数字个数,小数点前面的数字不是有效数字,因为它实 际上只反映了氢离子浓度的数量级。
化学是一门以实验为基础的科学:Chem-is-try
化学在21世纪焕发着新的青春
20世纪化学的标志性成果 1. 合成氨技术 2.三大合成高分子材料:塑料、橡胶、纤维。 3.药物的发明
化学发展的现状( 21世纪)
化学和其他学科交叉,形成了许多新兴学科:
如地球化学、环境化学、化学生物学、药物化学等 化学已经成为生命、农业、医学、材料、环境等学科 的基础。
(±0.2)+(±0.0002)≈±0.2
所以计算结果的正确表示应为 36.5 。有效数字36.5 正好 与0.2的绝对误差相匹配。
(2)乘除法 例如,以下三个有效数字进行乘除法运算时 0.024×8.156 12.576 =0.015564885…… 因为每个数据的最后一位数字均为可疑数字,若最后一位有1
在有效数字中,数字“0”具有双重意义:(1)作为普通 数字使用,它是有效数字;(2)只起定位作用,它不是有效 数字。
例如,测得以下数据:
试剂的体积 12mL (量筒量取)
二位有效数字
试样的质量 0.6283g (分析天平称取) 四位有效数字
滴定液体积 23.58mL (滴定管读取) 四位有效数字
《无机及分析化学一》课程教学大纲

《无机及分析化学一》课程教学大纲课程名称(中文):无机及分析化学一课程名称(英文):Inorganic Chemistry and Analytical Chemistry (I)课程性质:(专业必修)学分: 2.5学时:54 ,其中理论学时: 36 ,实践(实验)学时:18授课对象:环境科学与工程类、生态学类大学一年级本科生授课语言:中文开课院系:生态与环境科学学院课程网址:无撰写人:邓晶晶审定人:一、课程简介(中文)无机化学是化学及相关专业本科生的一门专业基础课程。
它主要介绍无机化学的基本理论、原理及应用,包括气体和溶液的基本性质,化学热力学和动力学及化学平衡移动原理等相关知识。
在宏观方面,主要介绍“四大平衡”理论 (酸碱解离平衡,沉淀溶解平衡,氧化还原平衡,配位解离平衡);在微观方面,对原子结构也做了详尽的介绍。
此外,为了实现理论与实际相结合,本门课程还针对理论课程的不同章节开设了相应的实验课程,为学生更好地理解无机化学知识提供了保证。
课程简介(英文)Inorganic chemistry is an important and professional basic course for undergraduate students of chemistry and related majors. In this course, we would introduce the basic theory, principle and application of inorganic chemistry, including the basic properties of gas and liquid, chemical thermodynamics and chemical kinetics, the principle of the movement of chemical equilibrium, and so on. In the macroscopic aspect, “four major equilibriums”(Acid-base dissociated equilibrium, Precipitation and dissolution equilibrium, Redox equilibrium, Coordination equilibrium) are briefly introduced, while in microcosmic aspect, the atomic structure is introduced in details. Moreover, for integrating the theory with practice, we establish experimental course according to different chapter of inorganic chemistry, which is of great importance for a better understanding of basic knowledge of inorganic chemistry.二、课程目标无机化学是化学的一个分支,也是其它各门化学的入门课程,因而本课程被定位为环境科学与工程类、生态学类专业学生的专业必修课。
2064无机及分析化学.doc

2064⽆机及分析化学.doc湖北省⾼等教育⾃学考试⼤纲课程名称:⽆机及分析化学课程代码:2064第⼀部分课程性质与⽬标⼀、课程性质与特点《⽆机及分析化学》是⾮化学类理⼯科相关专业的⼀门专业基础课。
化学是研究物质的组成、结构、性质及其变化规律和变化过程中能量关系的科学。
本课程的主要内容是⽆机化学和分析化学的基础理论和基本知识。
系统介绍原⼦结构和分⼦结构理论、元素性质;酸碱反应、沉淀反应、配位反应和氧化还原反应;在分析化学⽅⾯主要介绍定量分析化学的基本概念,常⽤滴定分析法、重量分析法、分光光度分析法等,分析研究化学中常⽤的分离法。
对仪器分析法作简单介绍。
本课程将⽆机化学和分析化学的内容有机地结合起来讨论。
⼆、课程⽬标与基本要求随着科学技术和⽣产的发展,各门学科之间的相互渗透⽇益增强,并出现了许多边缘学科。
⼈们⾯临的研究课题,往往需要综合运⽤多学科的知识才能解决。
本课程的⽬标和要求是:掌握必需的化学基本理论、基本知识和基本技能,了解这些化学理论、知识和技能在相关科学研究和科学技术及⼯程⽅⾯的应⽤。
三、与本专业其他课程的关系化学是⼀门基础科学,⽆机及分析化学是最基础的课程。
通过本课程的学习使学⽣掌握最基本的化学原理和定量分析⽅法,为今后从事环境⼯程和管理等⼯作和研究打下基础,为后续专业课程的学习打下良好的基础。
第⼆部分考核内容与考核⽬标第⼀章酸碱反应⼀、学习⽬的与要求通过本章学习,了解酸碱电离理论,酸碱溶剂理论,酸碱质⼦理论,酸碱电⼦理论及软硬酸碱理论的基本内容;缓冲溶液的概念及其重要作⽤;理解酸碱反应的本质和基本规律。
掌握酸碱溶液,缓冲溶液中pH的计算原理和⽅法。
⼆、课程内容酸碱理论概述酸碱平衡中有关浓度的计算缓冲溶液三、考核知识点与考核⽬标(⼀)重点(1)识记:酸碱电离理论,酸碱质⼦理论,酸碱电⼦理论的基本概念;弱酸弱碱溶液的电离特征;缓冲溶液的概念。
(2)理解:酸碱电离理论基础,酸碱质⼦理论基础,酸碱电⼦理论的基本内容,各理论的主要优点和应⽤范围,各理论所存在的局限性,⼏种理论对酸碱的说明。
《分析化学》课程教学大纲

《分析化学》课程教学大纲一、课程基本信息课程名称:分析化学(Anal ytical Chemistry)课程代码:08S1107B课程性质:专业核心课程课程类别:必修适用专业:化学专业课程学时:总学时60(理论60学时实践0学时)课程学分:总学分4(理论4 实践0)先修课程:无机化学、无机化学实验、有机化学、有机化学实验选用教材:《分析化学》上册(第6版)[M].武汉大学主编.北京:高等教育出版社,2016.参考书目:1.《分析化学》上册(第4版)[M].华中师范大学等编.北京:高等教育出版社,2011.2.《分析化学习题解答》上册(第6版)[M].曾百肇,赵发琼编.北京:高等教育出版社,2018.二、课程目标(一)课程具体目标通过本课程的学习,学生达到以下目标:1.了解分析化学的目的、任务和方法分类,明确滴定分析要求,掌握滴定分析的主要方法和方式。
了解分析过程和结果表示的方法,学会溶液的配制与标定,能根据化学计量比进行滴定分析计算,并把分析结果表示成相应的形式,建立起严格的“量”的概念。
掌握酸碱滴定、配位滴定、氧化还原滴定、沉淀滴定、重量分析法、吸光光度法的基本概念、原理、计算和操作方法。
【毕业要求3学科素养】2.了解分析过程中的误差来源、表示方法及提高分析结果准确度的方法,学会实验数据的统计处理,能够认识到实验前的准备工作、实验中的严格操作、数据记录及处理等过程应该遵循的原则和重要性,灵活掌握各种基本运算,给出正确的分析结果。
善于反思、发现问题,并从实验设计和操作中改进。
【毕业要求3学科素养】【毕业要求7学会反思】3.结合试样的处理方法,能独立完成采样和制样,能根据试样的特点提出主要采取的措施、方法及注意事项。
熟悉常用的分离和富集方法,理解分析全过程的质量保证与质量控制。
理解课堂内外自学、小组讨论式学习的作用,既能独立思考,又具备初步的团队合作精神。
结合课程思政教育,在校园生活和学习中践行爱国主义、环保教育、“原创性”科研、食品安全、平衡心态等理念。
