化合物溶解性全表
常用化合物在不同温度下的溶解度
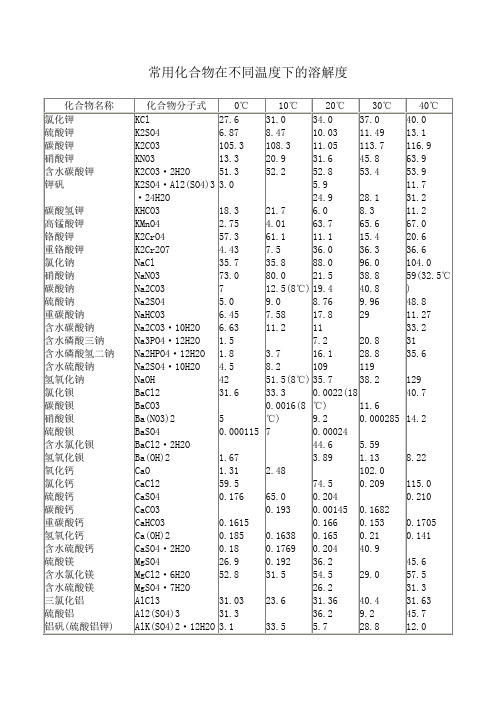
K2CrO4
25.9 31.2 36.2 41.1 45.2 50.5
K2Cr2O7
37.0 37.3 37.8 38.4 39.0 39.8
NaCl
114.0 124.0 135.0 148.0 162.0 180.0
NaNO3
45.4
Na2CO3
46.7 45.3 44.1 43.7 42.9 42.5
FeCl2
34.4
FeCl3
73.1
FeSO4
315.1
FeCl2·4H2O
48.6
FeCl3·6H2O
42.2
FeSO4·7H2O
75.9
CuSO4
32.3
CuSO4·5H2O
33.3
NH4Cl
25.1
NH4NO3
50.4
(NHห้องสมุดไป่ตู้)2SO4
NH4HCO3
(NH4)2HPO4
(NH3)2SO4·Al2
KNO3
85.5 110.0 138.0 169.0 202.0 246.0
K2CO3·2H2O
54.8 55.9 57.1 58.3 59.6 60.9
K2SO4·Al2(SO4)3
24.75
71.0 109.0
·24H2O
34.2 37.5
KHCO3
14.4 18.0
KMnO4
69.0 72.8
(SO4)3·24H2O
0.86 136.8 0.205
0.1750 0.116
55.0 61.0 35.5 31.73 59.2 26.1
37.1 78.3
57.0 43.9
35.5 40.0 28.1 55.2 421.0 88.0
常见有机溶剂的溶解性汇总

也有一定的刺激性。不同有机溶剂其作用的主要靶*****和作用的强弱也不同,这决定于每一种有机溶剂 的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。 毒性 ①神经毒性。以脂肪烃(正己烷、戊烷、汽油)、芳香烃(苯、苯乙烯、丁基甲苯、乙烯基甲苯)、氯化烃(三 氯乙烯、二氯甲烷),以及二硫化碳、磷酸三邻甲酚等脂溶性较强的溶剂为多见。有机溶剂对神经系统的损 害大致有三种类型:第一种为中毒性神经衰弱和植物神经功能紊乱。病人可有头晕、头痛、失眠、多梦、 嗜睡、无力、记忆力减退、食欲不振、消瘦,以及多汗、情绪不稳定,心跳加速或减慢、血压波动、皮肤 温度下降或双侧肢体温度不对称等表现;第二种为中毒性末梢神经炎。大部分表现为感觉型,其次为混合 型。可有肢端麻木、感觉减退、刺痛、四肢无力、肌肉萎缩等表现;第三种为中毒性脑病,比较少见,见 于二硫化碳、苯、汽油等有机溶剂的严重急、慢性中毒。 ②血液毒性。以芳香烃,特别是苯最常见。苯达到一定剂量即可抑制骨髓造血功能,往往先有白细胞减少, 以后血小板减少,最后红细胞减少,成为全血细胞减少。个别接触苯的敏感者,可发生白血病。 ③肝肾毒性。多见于氯代烃类有机溶剂,如氯仿、四氯化碳、三氯乙烯、四氯乙烯、三氯丙烷、二氯乙烷 等中毒。中毒性肝炎的病理改变主要是脂肪肝和肝细胞坏死。临床上可有肝区痛、食欲不振、无力、消瘦、 肝脾肿大、肝功能异常等表现。有机溶剂引起的肾损害多见为肾小管型,产生蛋白尿,肾功能呈进行性减 退。 ④皮肤粘膜刺激。多数有机溶剂均有程度不等的皮肤粘膜刺激作用,但以酮类和酯类为主。可引起呼吸道 炎症、支气管哮喘、接触性和过敏性皮炎、湿疹、结膜炎等。 防治 生产和使用有机溶剂时,要加强密闭和通风,减少有机溶剂的逸散和蒸发。采用自动化和机械化操 作,以减少操作人员直接接触的机会。应使用个人防护用品,如防毒口罩或防护手套。皮肤粘膜受污染时, 应及时冲洗干净。勿用污染的手进食或吸烟。勤洗手、洗澡与更衣。应定期进行健康检查,及早发现中毒 征象时,进行相应的治疗和严密的动态观察。
溶解性表详解

部分酸、碱和盐的溶解性表(室温)
阳 离
阴离子 OH - (氢氧根) NO3 - (硝酸根) Cl- (盐酸根)
子
H+
NH
+ 4
1.写出所有的阳离子与CO32-结合所生成的
K+
化合物的化学式和名称。
Na + 2.生成的化合物有什么共性?什么是盐酸
Ba2+
盐?
Ca 2+ Mg2+
3.共有几种?几种可溶、几种微溶、几种 不溶?
Fe2+
3.除BaSO4不溶,CaSO4、Ag2SO4微
Fe3+
溶,11种硫酸盐可溶。
Cu2 +
Ag +
SO4 2- (硫酸根) CO32 - (碳酸根)
H2SO4 (硫酸) (NH4)2SO4(硫酸铵) K2SO4 (硫酸钾) Na2SO4 (硫酸钠) BaSO4 (硫酸钡) CaSO4 (硫酸钙) MgSO4 (硫酸镁) Al2(SO4)2 (硫酸铝) MnSO4 (硫酸锰) ZnSO4 (硫酸锌) Fe SO4 (硫酸亚铁) Fe2(SO4)3 (硫酸铁) CuSO4 (硫酸铜) Ag2SO4 (硫酸银)
Ag +
AgCl(氯化银)
SO4 2- (硫酸根) CO32 - (碳酸根)
2.它们的阴离子全部是Cl - , 酸根离子全部是Cl- 离子的 化合物叫盐酸盐。 3.除AgCl不溶,12种盐酸 盐可溶。
部分酸、碱和盐的溶解性表(室温)
阳 离
阴离子 OH - (氢氧根) NO3 - (硝酸根) Cl- (盐酸根)
NH
+ 4
K+
NH 3.H2O (铵水) KOH (氢氧化钾)
溶解性口诀总汇(附溶解性表)

溶 解 性硝酸盐,Fra bibliotekO₃~都易溶。
亚硝酸盐,NO₂ˉ
除AgNO₂难溶外都易溶。
醋酸盐,C₂H₃O₂ˉ
除Ag⁺,Hg₂²⁺,Bi³⁺⁵等盐难溶外都易溶。
氯化物,Cl⁻
除Ag⁺,Hg₂²⁺,Pb²⁺,Cu²⁺⁶等盐难溶外都易溶。
溴化物,Br⁻
除Ag⁺,Hg₂²⁺,Pb²⁺,Pt²⁺÷等盐难溶外都易溶。
碘化物,I⁻
除Ag⁺,Hg₂²⁺,Pb²⁺,Cu²⁺,Bi³⁺⁶等盐难溶外都易溶。
硫酸盐,so₄²⁻
除Pb²⁺,Ba²⁺,Sr²⁺,Ca²⁺等盐难溶外都易溶。
亚硫酸盐,so₃²⁻
除Na⁺,K⁺,NH₄⁺³等盐难溶外都易溶。
硫代硫酸盐,S₂O₃²⁻
除Ba²⁺,Pb²⁺,Ag⁺≤等盐难溶外都易溶。
硫化物,s²⁻
砷酸盐,AsO₄³⁻
除Na⁺,K⁺,NH₄⁺等盐难溶外都难溶。
草酸盐,C₂O₄²⁻
除Na⁺,K⁺,NH₄⁺等盐难溶外都难溶。
硫代氰酸盐,SCN⁻
除Pb²⁺,Cu²⁺Ag⁺,Hg₂²⁺,Cd²⁺等盐难溶外都易溶。
氧化物,o²⁻
除Na⁺,K⁺,Ba²⁺,Sr²⁺,Ca²⁺等盐难溶外都难溶。
氢氧化物, OH⁻
除Na⁺,K⁺,Ba²⁺,等的氢氧化物外都难溶, Sr²⁺,Ca²⁺的氢氧化物微溶。
除Na⁺,K⁺,NH₄⁺,Ca²⁺,sr²⁺,Ba²⁺⁵等盐难溶外都难溶。
磷酸盐,PO₄³⁻
除Na⁺,K⁺,NH₄⁺等盐难溶外都难溶。
亚砷酸盐,AsO₄³⁻
除Na⁺,K⁺,NH₄⁺¹等盐难溶外都难溶。
碳酸盐,CO₃²⁻
除Na⁺,K⁺,NH₄⁺等盐难溶外都难溶。
(完整)初中化学溶解性表
1.2Mg+O2点燃或Δ2MgO化学反应现象:剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟应用:白色信号弹2.2Hg+O2点燃或Δ2HgO化学反应现象:银白液体、生成红色固体应用:拉瓦锡实验3.4Al+3OΔ2Al2O3化学反应现象:银白金属变为白色固体4.3Fe+2O2点燃Fe3O4化学反应现象:剧烈燃烧、火星四射、生成黑色固体、放出大量热5.C+O2点燃CO2化学反应现象:剧烈燃烧、白光、放热、使石灰水变浑浊6.S+O2点燃SO2化学反应现象:剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰7.2H2+O2点燃2H2O化学反应现象:淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)应用:高能燃料8.4P+5O2点燃2P2O5化学反应现象:剧烈燃烧、大量白烟、放热、生成白色固体应用:证明空气中氧气含量9.CH4+2O2点燃2H2O+CO2化学反应现象:蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)应用:甲烷和天然气的燃烧10.2KClO3 MnO2Δ 2KCl +3O2↑化学反应现象:生成使带火星的木条复燃的气体应用:实验室制备氧气11.2KMnO4Δ K2MnO4+MnO2+O2↑化学反应现象:紫色变为黑色、生成使带火星木条复燃的气体应用:实验室制备氧气12.2HgOΔ2Hg+O2↑化学反应现象:红色变为银白、生成使带火星木条复燃的气体应用:拉瓦锡实验13.2H2O通电2H2↑+O2↑化学反应现象:水通电分解为氢气和氧气应用:电解水14.Cu2(OH)2CO3Δ2CuO+H2O+CO2↑化学反应现象:绿色变黑色、试管壁有液体、使石灰水变浑浊气体应用:铜绿加热15.NH4HCO3ΔNH3↑+ H2O +CO2↑化学反应现象:白色固体消失、管壁有液体、使石灰水变浑浊气体应用:碳酸氢铵长期暴露空气中会消失16.Zn+H2SO4=ZnSO4+H2↑化学反应现象:有大量气泡产生、锌粒逐渐溶解应用:实验室制备氢气17.Fe+H2SO4=FeSO4+H2↑化学反应现象:有大量气泡产生、金属颗粒逐渐溶解18.Mg+H2SO4 =MgSO4+H2↑化学反应现象:有大量气泡产生、金属颗粒逐渐溶解19.2Al+3H2SO4=Al2(SO4)3+3H2↑化学反应现象:有大量气泡产生、金属颗粒逐渐溶解20.Fe2O3+3H2Δ 2Fe+3H2O化学反应现象:红色逐渐变为银白色、试管壁有液体应用:冶炼金属、利用氢气的还原性21.2Na+Cl2Δ或点燃2NaCl化学反应现象:剧烈燃烧、黄色火焰应用:离子化合物的形成、22.H2+Cl2点燃或光照 2HCl化学反应现象:点燃苍白色火焰、瓶口白雾应用:共价化合物的形成、制备盐酸23.CuSO4+2NaOH=Cu(OH)2↓+Na2SO4化学反应现象:蓝色沉淀生成、上部为澄清溶液应用:质量守恒定律实验24.2C +O2点燃2CO应用:煤炉中常见反应、空气污染物之一、煤气中毒原因25.2CO+O2点燃2CO2化学反应现象:蓝色火焰应用:煤气燃烧26. C + CuO 高温2Cu+ CO2↑化学反应现象:黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体应用:冶炼金属27.2Fe2O3+3C 高温4Fe+ 3CO2↑Fe3O4+2C高温3Fe + 2CO2↑应用:冶炼金属28. C + CO2高温2CO29.CO2 + H2O = H2CO3化学反应现象:碳酸使石蕊变红应用:证明碳酸的酸性30.H2CO3ΔCO2↑+ H2O化学反应现象:石蕊红色褪去31.Ca(OH)2+CO2= CaCO3↓+ H2O化学反应现象:澄清石灰水变浑浊应用:应用CO2检验和石灰浆粉刷墙壁32.CaCO3+H2O+CO2 = Ca(HCO3)2化学反应现象:白色沉淀逐渐溶解应用:溶洞的形成,石头的风化33.Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑化学反应现象:白色沉淀、产生使澄清石灰水变浑浊的气体应用:水垢形成.钟乳石的形成34.2NaHCO3ΔNa2CO3+H2O+CO2↑化学反应现象:产生使澄清石灰水变浑浊的气体应用:小苏打蒸馒头35.CaCO3高温 CaO+ CO2↑应用:工业制备二氧化碳和生石灰36.CaCO3+2HCl=CaCl2+ H2O+CO2↑化学反应现象:固体逐渐溶解、有使澄清石灰水变浑浊的气体应用:实验室制备二氧化碳、除水垢37.Na2CO3+H2SO4=Na2SO4+H2O+CO2↑化学反应现象:固体逐渐溶解、有使澄清石灰水变浑浊的气体应用:泡沫灭火器原理38.Na2CO3+2HCl=2NaCl+ H2O+CO2↑化学反应现象:固体逐渐溶解、有使澄清石灰水变浑浊的气体应用:泡沫灭火器原理39.CuO +CO Δ Cu + CO2化学反应现象:黑色逐渐变红色,产生使澄清石灰水变浑浊的气体应用:冶炼金属40.Fe2O3+3CO高温 2Fe+3CO2应用:冶炼金属原理41.C2H5OH+3O2点燃2CO2+3H2O化学反应现象:蓝色火焰、产生使石灰水变浑浊的气体、放热应用:酒精的燃烧42.Fe+CuSO4=Cu+FeSO4化学反应现象:银白色金属表面覆盖一层红色物质应用:湿法炼铜、镀铜43.Mg+FeSO4= Fe+ MgSO4化学反应现象:溶液由浅绿色变为无色44.Cu+2AgNO3=2Ag+ Cu(NO3)2化学反应现象:红色金属表面覆盖一层银白色物质应用:镀银45.Zn+CuSO4= Cu+ZnSO4化学反应现象:青白色金属表面覆盖一层红色物质应用:镀铜46.Fe2O3+6HCl=2FeCl3+3H2O化学反应现象:铁锈溶解、溶液呈黄色应用:铁器除锈47.Al2O3+6HCl=2AlCl3+3H2O化学反应现象:白色固体溶解48.CuO+2HCl=CuCl2+H2O化学反应现象:黑色固体溶解、溶液呈蓝色49.MgO+2HCl=MgCl2+ H2OCaO+2HCl=CaCl2+ H2O共同的化学反应现象:白色固体溶解50.NaOH+HCl=NaCl+ H2O化学反应现象:白色固体溶解51.Cu(OH)2+2HCl=CuCl2+2H2O化学反应现象:蓝色固体溶解52.Mg(OH)2+2HCl=MgCl2+2H2O化学反应现象:白色固体溶解53.Al(OH)3+3HCl=AlCl3+3H2O化学反应现象:白色固体溶解应用:胃舒平治疗胃酸过多54.Fe(OH)3+3HCl=FeCl3+3H2O化学反应现象:红褐色沉淀溶解、溶液呈黄色55.Ca(OH)2+2HCl=CaCl2+2H2O56.HCl+AgNO3= AgCl↓+HNO3化学反应现象:生成白色沉淀、不溶解于稀硝酸检验Cl—的原理57.Fe2O3+3H2SO4= Fe2(SO4)3+3H2O化学反应现象:铁锈溶解、溶液呈黄色铁器除锈58.Al2O3+3H2SO4= Al2(SO4)3+3H2O化学反应现象:白色固体溶解59.CuO+H2SO4=CuSO4+H2O化学反应现象:黑色固体溶解、溶液呈蓝色60.2NaOH+H2SO4=Na2SO4+2H2O61.Cu(OH)2+H2SO4=CuSO4+2H2O化学反应现象:蓝色固体溶解62.2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O化学反应现象:白色固体溶解63.2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O化学反应现象:红褐色沉淀溶解、溶液呈黄色64.Ba(OH)2+ H2SO4=BaSO4↓+2H2O化学反应现象:生成白色沉淀、不溶解于稀硝酸检验SO42—的原理65.BaCl2+ H2SO4=BaSO4↓+2HCl化学反应现象:生成白色沉淀、不溶解于稀硝酸检验SO42—的原理66.Ba(NO3)2+H2SO4=BaSO4↓+2HNO3化学反应现象:生成白色沉淀、不溶解于稀硝酸检验SO42—的原理67.CuO+2HNO3=Cu(NO3)2+H2O化学反应现象:黑色固体溶解、溶液呈蓝色68.NaOH+HNO3=NaNO3+ H2O69.Cu(OH)2+2HNO3=Cu(NO3)2+2H2O化学反应现象:蓝色固体溶解70.Fe(OH)3+3HNO3=Fe(NO3)3+3H2O化学反应现象:红褐色沉淀溶解、溶液呈黄色71.2NaOH+CO2=Na2CO3+ H2O化学反应现象:吸收CO、O2、H2中的CO2、72.2NaOH+SO2=Na2SO3+ H2O2NaOH+SO3=Na2SO4+ H2O处理硫酸工厂的尾气(SO2)73.FeCl3+3NaOH=Fe(OH)3↓+3NaCl化学反应现象:溶液黄色褪去、有红褐色沉淀生成74.AlCl3+3NaOH=Al(OH)3↓+3NaCl化学反应现象:有白色沉淀生成75.MgCl2+2NaOH = Mg(OH)2↓+2NaCl76.CuCl2+2NaOH = Cu(OH)2↓+2NaCl化学反应现象:溶液蓝色褪去、有蓝色沉淀生成77.CaO+ H2O = Ca(OH)2化学反应现象:白色块状固体变为粉末生石灰制备石灰浆78.Ca(OH)2+Na2CO3=CaCO3↓+2NaOH化学反应现象:有白色沉淀生成工业制烧碱、实验室制少量烧碱79.Ba(OH)2+Na2CO3=BaCO3↓+2NaOH化学反应现象:有白色沉淀生成80.Ca(OH)2+K2CO3=CaCO3↓ +2KOH化学反应现象:有白色沉淀生成81.CuSO4+5H2O= CuSO4·H2O化学反应现象:白色粉末变为蓝色检验物质中是否含有水82.CuSO4·H2OΔ CuSO4+5H2O化学反应现象:蓝色晶体变为白色粉末83.AgNO3+NaCl = AgCl↓+NaNO3化学反应现象:白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子84.BaCl2 + Na2SO4 = BaSO4↓+2NaCl化学反应现象:白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子85.CaCl2+Na2CO3= CaCO3↓+2NaCl化学反应现象:有白色沉淀生成86.MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓化学反应现象:有白色沉淀生成87.CaCO3+2HCl=CaCl2+H2O+CO2↑88.MgCO3+2HCl= MgCl2+H2O+ CO2↑89.NH4NO3+NaOH=NaNO3+NH3↑+H2O化学反应现象:生成使湿润石蕊试纸变蓝色的气体应用:应用于检验溶液中的铵根离子90.NH4Cl+ KOH= KCl+NH3↑+H2O化学反应现象:生成使湿润石蕊试纸变蓝色的气体。
常用试剂的溶解性

常用试剂的溶解性常用试剂的溶解性1 . 二甲胺:有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂,强烈刺激性。
2 . 石油醚:不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶,与低级烷相似。
3 . 乙醚:微溶于水,易溶与盐酸,与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶。
麻醉性4 . 戊烷:与乙醇、乙醚等多数有机溶剂混溶,低毒性。
5 .二氯甲烷:与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶。
低毒性,麻醉性强7 . 二硫化碳:微溶与水,与多种有机溶剂混溶。
麻醉性,强刺激性8 .丙酮:与水、醇、醚、烃混溶。
低毒,类乙醇,但较大9 . 1,1-二氯乙烷:与醇、醚等大多数有机溶剂混溶。
低毒、局部刺激性10 . 氯仿:与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶。
中等毒性,强麻醉性11 . 甲醇:与水、乙醚、醇、酯、卤代烃、苯、酮混溶。
中等毒性,麻醉性12 . 四氢呋喃:优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃。
吸入微毒,经口低毒。
13 . 己烷:与甲醇部分溶解,与比乙醇高的醇、醚、丙酮、氯仿混溶。
低毒,麻醉性,刺激性14 . 三氟代乙酸:与水、乙醇、乙醚、丙酮、苯、四氯化碳、己烷混溶,溶解多种脂肪族、芳香族化合物。
15 . 1,1,1-三氯乙烷:与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶。
低毒类溶剂16 . 四氯化碳:与醇、醚、石油醚、冰醋酸、二硫化碳、氯代烃混溶。
氯代甲烷中毒性最强。
17 . 乙酸乙酯:与醇、醚、氯仿、丙酮、苯等大多数有机溶剂互溶,能溶解某些金属盐。
低毒,麻醉性18 . 乙醇:与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶。
微毒类,麻醉性19 . 丁酮:与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶。
低毒,毒性强于丙酮20 . 苯:难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶。
化合物溶解性全表

HCl
不溶
HCl
HCl
HCl
HCl
略溶
HCl
HCl
微溶
水
水
水
水
水
水
水
水
水
水
水
水
水
略溶,HCl
略溶,HCl
Sr2+
HCl
HCl
HCl
HCl
HCl
HCl
HCl
略溶
HCl
HCl
不溶
略溶
水
水
水
水
水
水
水
水
水
水
水
水
HCl
略溶,HCl
Ba2+
HCl
HCl
略溶
HCl
HCl
HCl
HCl
HCl
HCl
HCl
不溶
HCl
-
-
-
-
-
HCl
水解,HCl
水解,HCl
水
-
略溶,HNO3
HNO3
HCl
Hg2+
HCl
HCl
水
HCl
HCl
HCl
HCl
-
-
HCl
略溶
HCl
王水
水
-
不溶
-
水
HCl
水
水
水
水
水
HCl
-
Pb2+
HNO3
HNO3
略溶,HNO3
HNO3
HNO3
HNO3
HNO3
HNO3
HNO3
HNO3
HNO3
HNO3
不同温度下常见无机化合物的溶解度

氯酸钡
Ba(ClO2)2
铬酸钡
BaCrO4
氰化钡
Ba(CN)2
亚铁氰化钡 Ba2Fe(CN)6
氟化钡
BaF2
氟硅酸钡
BaSiF6
甲酸钡
Ba(HCO2)2
磷酸氢钡
BaHPO4
亚磷酸氢钡 BaHPO3
氢氧化钡
Ba(OH)2· 8H2O
0°C
58.8 12.5 0.29
98 20.3 31.2 43.9
26.2
3.144×10-4
3.622×10-4
7.998×10-2
物质 一氧化氮 一氧化二氮
化学式 NO N2O
Dy2(CrO4)3 铬酸镝(III) ·10H2O
铒
0°C
10°C
20°C 5.6×10-3
0.112
0.663
物质 氢氧化铒 (III)
化学式 Er(OH)3
钒
物质
化学式
五氧化二钒 V2O5
135
135
2.2×10-2
8.736×10-5
4
11.1
14.4
2.697×10-4
9.7×10-2
84.7
136 6.046×10-3
180
188
6.235×10-6
68.4
64
76
76.6
1.292×10-12 4.642×10-2
124
130
123
130
220
硫酸铬 叠氮化亚汞 溴化亚汞 碳酸亚汞 氯化亚汞 铬酸亚汞 氰化亚汞 高氯酸亚汞 硫酸亚汞 乙酸汞
砷酸二氢钾 磷酸二氢钾 铁氰化钾 亚铁氰化钾 氟化钾 甲酸钾 碳酸氢钾 磷酸一氢钾 硫酸氢钾 氢氧化钾 碘酸钾 碘化钾 硝酸钾 亚硝酸钾 草酸钾 高氯酸钾 高碘酸钾 高锰酸钾 过二硫酸钾 磷酸钾 硒酸钾 硫酸钾 四苯硼钾 硫氰酸钾 硫代硫酸钾 钨酸钾 三氯化金 三碘化金 草酸金(V)
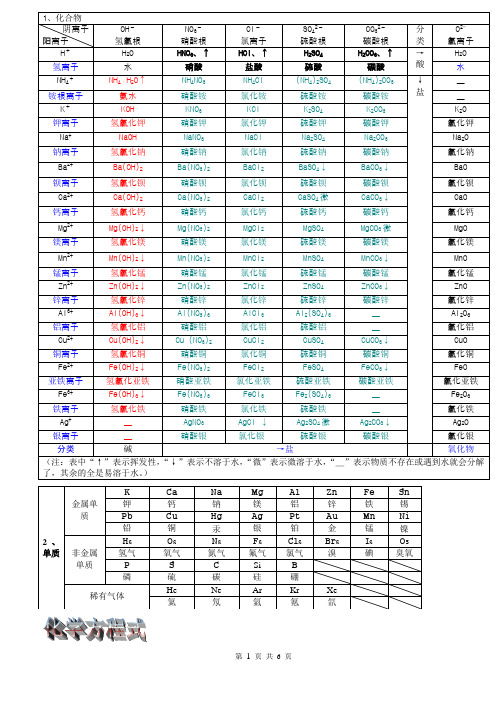
物质溶解性表及沉淀颜色

物质溶解性表及沉淀颜色1.Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解溶液呈黄色铁器除锈2.Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解3.CuO+H2SO4=CuSO4+H2O 黑色固体溶解溶液呈蓝色4.ZnO+H2SO4=ZnSO4+H2O 白色固体溶解5.MgO+H2SO4=MgSO4+H2O 白色固体溶解6.2NaOH+H2SO4=Na2SO4+2H2O7.Cu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解8.Ca(OH)2+H2SO4=CaSO4+2H2O9.Mg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解10.2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解11.2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解溶液呈黄色12.Ba(OH)2+ H2SO4=BaSO4+2H2O 生成白色沉淀不溶解于稀硝酸检验SO42的原理13..BaCl2+ H2SO4=BaSO4+2HCl 生成白色沉淀不溶解于稀硝酸检验SO42的原理14.Ba(NO3)2+H2SO4=BaSO4+2HNO3 生成白色沉淀不溶解于稀硝酸检验SO42的原理15.Na2O+2HNO3=2NaNO3+H2O 白色固体溶解16.CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解溶液呈蓝色17.ZnO+2HNO3=Zn(NO3)2+ H2O 白色固体溶解18.MgO+2HNO3=Mg(NO3)2+ H2O 白色固体溶解19.CaO+2HNO3=Ca(NO3)2+ H2O 白色固体溶解20.NaOH+HNO3=NaNO3+ H2O21.Cu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解22.Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解23.Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解24.Ca(OH)2+2HNO3=Ca(NO3)2+2H2O25.Fe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解溶液呈黄色26.3NaOH + H3PO4=3H2O + Na3PO427.3NH3+H3PO4=(NH4)3PO428.2NaOH+CO2=Na2CO3+ H2O 吸收COO2H2中的CO229.2NaOH+SO2=Na2SO3+ H2O2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气(SO2)30.FeCl3+3NaOH=Fe(OH)3+3NaCl 溶液黄色褪去有红褐色沉淀生成1.碳与氧气(不足)的反应2C+O2==== 2CO 碳与氧气(充足)的反应C+O2==== CO22.一氧化碳与氧气的反应2CO+O2==== 2CO23.二氧化碳与碳的反应CO2+C==== 2CO4.碳酸氢钠与盐酸的反应NaHCO3+HCl==== NaCl+H2O+CO2↑5.碳酸钠与盐酸的反应Na2CO3+ 2HCl==== 2NaCl+ H2O+ CO2↑6.碳酸钙与盐酸的反应CaCO3+2HCl==== CaCl2+ H2O+ CO2↑7.碳酸氢钠与氢氧化钠的反应NaHCO3+NaOH==== Na2CO3 +H2O8.碳酸钠与氢氧化钙的反应Na2CO3+Ca(OH)2==== CaCO3↓+2NaOH9.碳酸氢钠(少量)与氢氧化钙的反应NaHCO3+ Ca(OH)2==== CaCO3↓+NaOH+ H2O碳酸氢钠(过量)与氢氧化钙的反应2NaHCO3+ Ca(OH)2==== C aCO3↓+Na2CO3+2H2O10.碳酸氢钠加热的反应2NaHCO3==== Na2CO3+ H2O+CO2↑11.碳酸氢钙加热的反应Ca(HCO3)2==== CaCO3↓+H2O+CO2↑12.碳酸钙加热的反应CaCO3==== CaO+CO2↑13.二氧化碳(过量)通入氢氧化钙溶液中的反应Ca(OH)2+2CO2= === Ca(HCO3)2二氧化碳(少量)通入氢氧化钙溶液中的反应Ca(OH)2+CO2==== CaCO3↓+H2O14.氮气与氧气的反应N2+O2==== 2NO15.一氧化氮与氧气的反应2NO+O2==== 2NO216.二氧化氮与水的反应3NO2+ H2O==== 2HNO3+ NO17.氮气与氢气的反应N2+3H2========= 2NH318.氨气与水的反应NH3+H2O==== NH3•H2O19.氨气与盐酸的反应NH3+HCl==== NH4Cl20.氨气与硫酸的反应2NH3+H2SO4==== (NH4)2SO421.氨气与强酸的离子的反应NH3+H+==== NH4+22.氨的催化氧化的反应4NH3+5O2====== 4NO+6H2O23.碳酸氢铵加热的反应NH4HCO3==== NH3↑+CO2↑+H2O24.氯化铵加热的反应NH4Cl==== NH3↑+HCl↑25.碳酸铵加热的反应(NH4)2CO3==== 2NH3↑+CO2↑+H2O26.氯化铵与氢氧化钙的反应2NH4Cl+ Ca(OH)2==== CaCl2+2 NH3↑+2H2O27.氯化铵与氢氧化钠的反应NH4Cl+ NaOH==== NaCl+NH3↑+H2O28.碳酸氢铵与氢氧化钠的反应NH4HCO3+2NaOH==== Na2C O3+NH3↑+2H2O29.碳酸氢铵与氢氧化钙的反应NH4HCO3+Ca(OH)2==== CaC O3↓+NH3↑+2H2O30.硝酸的分解的反应4HNO3========= 4NO2↑+O2↑+2H2O31.铜与浓硝酸的反应Cu+4HNO3(浓)==== Cu(NO3)2+2NO2↑+ 2H2O32.铜与稀硝酸的反应3Cu+8HNO3(稀)==== 3Cu(NO3)2+2NO↑+4H2O33.铁与浓硝酸的反应Fe+6HNO3(浓)==== Fe(NO3)3+3NO2↑+ 3H2O34.铁与稀硝酸的反应Fe+4HNO3(稀)==== Fe(NO3)3+NO↑+2H 2O35.碳与浓硝酸的反应C+4HNO3(浓)==== CO2↑+4NO2↑+2H2 O36.一氧化氮与一氧化碳的反应2NO+2CO====== N2+2CO237.一氧化氮与氧气和水的反应4NO+3O2+2H2O==== 4HNO338.二氧化氮与氧气和水的反应4NO2+O2+2H2O==== 4HNO339.氢氧化钠吸收二氧化氮和一氧化氮的反应2NaOH+NO2+NO= === 2NaNO2+ H2O40.氨气(过量)与氯气的反应8NH3+3Cl2==== 6NH4Cl+N2氨气(少量)与氯气的反应2NH3+3Cl2==== 6HCl+N241.二氧化氮生成四氧化二氮的反应2NO2==== N2O442.硫与铜的反应S+2Cu==== Cu2S43.硫与铁的反应S+Fe==== FeS44.硫与钠的反应S+2Na==== Na2S45.硫与铝的反应3S+2Al==== Al2S346.硫与汞的反应S+Hg==== HgS47.硫与氧气的反应S+O2==== SO248.硫与氢气的反应S+H2==== H2S49.硫与氢氧化钠的反应3S+6NaOH==== 2Na2S+Na2SO3+3H2O50.硫与浓硫酸的反应S+2H2SO4(浓)==== 3SO2+2H2O51.黑火药点燃S+2KNO3+3C==== K2S+3CO2↑+N2↑52.二氧化硫(少量)与氢氧化钠的反应SO2+2NaOH==== Na2SO3+ H2O二氧化硫(过量)与氢氧化钠的反应SO2+NaOH==== NaHSO3 53.二氧化硫与氢氧化钙的反应SO2+Ca(OH)2==== CaSO3↓+H2O54.二氧化硫与亚硫酸钙溶液的反应SO2+CaSO3+H2O ==== Ca (HSO3)255.二氧化硫与水的反应SO2+H2O==== H2SO356.二氧化硫与硫化氢的反应SO2+2H2S==== 3S↓+2H2O57.二氧化硫与氧气的反应2SO2+O2====== 2SO358.二氧化硫与过氧化钠的反应SO2+Na2O2==== Na2SO459.二氧化硫与氯水的反应SO2+ Cl2+2H2O==== H2SO4+2HCl60.三氧化硫与水的反应SO3+H2O==== H2SO461.亚硫酸与氧气的反应2H2SO3+O2==== 2H2SO462.亚硫酸钠与氧气的反应2Na2SO3+O2==== 2Na2SO463.浓硫酸与铜的反应2H2SO4(浓)+Cu==== CuSO4+SO2↑+2H2 O64.浓硫酸与碳的反应2H2SO4(浓)+C==== CO2↑+2SO2↑+2H2O 寿65.工业制备硫酸(初步) 4FeS2+11O2==== 8SO2+2Fe2O366.实验室制备硫酸(初步) Na2SO3+H2SO4(浓)==== Na2SO4+SO 2↑+H2O67.硫化氢(少量)与氢氧化钠的反应H2S+2NaOH==== Na2S+2H2O硫化氢(过量)与氢氧化钠的反应H2S+NaOH==== NaHS+H2O 68.硫化氢(少量)与氨气的反应H2S+2NH3==== (NH4)2S硫化氢(过量)与氨气的反应H2S+NH3==== NH4HS69.硫化氢与氧气(不足)的反应2H2S+O2==== 2S↓+2H2O 2H2S+ O2==== 2S+2H2O硫化氢与氧气(充足)的反应2H2S+3O2==== 2SO2+2H2O70.硫化氢与氯气的反应H2S+Cl2==== 2HCl+S↓71.硫化氢与浓硫酸的反应H2S+H2SO4(浓)==== S↓+SO2↑+2H2 O72.硫化氢的制备FeS+H2SO4==== FeSO4+H2S↑73.电解饱和食盐水(氯碱工业) 2NaCl+2H2O==== 2NaOH+H2↑+C l2↑74.电解熔融状态氯化钠(制单质钠) 2NaCl==== 2Na+Cl2↑75.海水制镁(1) CaCO3==== CaO+CO2 (2) CaO+H2O==== Ca (OH)2(3) Mg2++2OH2-==== Mg(OH)2↓(4) Mg(OH)2+2HCl==== MgC l2+2H2O(5) MgCl2==== Mg+Cl2↑76.镁在空气中燃烧(与氧气的反应) 2Mg+O2==== 2MgO(与氮气的反应) 3Mg+N2==== Mg3N2(与二氧化碳的反应) 2Mg+CO2==== 2MgO+C77.镁与氯气的反应Mg+Cl2==== MgCl278.镁与水的反应Mg+2H2O==== Mg(OH)2+H2↑79.镁与盐酸的反应Mg+2HCl==== MgCl2+H2↑80.镁与氢离子的反应Mg+2H+==== Mg2++H2↑81.二氮化三镁与水的反应Mg3N2+6H2O==== 3Mg(OH)2↓+2NH3↑82.镁与溴水的反应(颜色退去) Mg+Br2==== MgBr2(产生气泡) Mg+2HBr==== MgBr2+H2↑83.溴与水的反应Br2+H2O==== HBr+HBrO84.溴与氢氧化钠的反应Br2+2NaOH==== NaBr+NaBrO+H2O85.溴与氢气的反应Br2+H2==== 2HBr86.溴与铁的反应3Br2+2Fe==== 2FeBr387.碘与铁的反应I2+Fe==== FeI288.溴与碘化钾的反应Br2+2KI==== 2KBr+I289.氯气与溴化钾的反应2KBr+Cl2==== 2KCl+Br290.硅与氧气的反应Si+O2==== SiO291.硅与氯气的反应Si+2Cl2==== SiCl492.硅与氢气的反应Si+2H2===== SiH493.二氧化硅与氟的反应Si+2F2==== SiF494.硅与碳的反应Si+C==== SiC95.硅与氢氧化钠溶液的反应Si+2NaOH+H2O==== Na2SiO3+2H2↑96.硅与氢氟酸的反应Si+4HF==== SiF4+2H2↑97.单质硅的制备(1.制备)SiO2+2C==== Si+2CO(2.提纯)Si+2Cl2==== SiCl4(3.提纯)SiCl4+2H2==== Si+4HCl98.二氧化硅与氢氧化钠的反应SiO2+2NaOH==== Na2SiO3+H2O99.二氧化硅与氧化钠的反应SiO2+Na2O==== Na2SiO3100.二氧化硅与碳酸钠的反应SiO2+Na2CO3==== Na2SiO3+ CO2↑101.二氧化硅与氧化钙的反应SiO2+CaO==== CaSiO3102.二氧化硅与碳酸钙的反应SiO2+CaCO3==== CaSiO3+CO2↑103.二氧化硅与氢氟酸的反应SiO2+4HF==== SiF4+2H2O104.硅酸的制备Na2SiO3+ CO2+H2O==== H2SiO3↓+ Na2CO3 105.硅酸加热分解H2SiO3==== SiO2+H2O106.铝与氧气的反应4Al+3O2==== 2Al2O3107.铝与氯气的反应2Al+3Cl2==== 2AlCl3108.铝与盐酸的反应2Al+6HCl==== 2AlCl3+3H2↑109.铝与氢氧化钠的反应2Al+2NaOH+6H2O==== 2Na[Al(OH)4]+3 H2↑110.铝与水的反应2Al+6H2O==== 2Al(OH)3+3H2↑111.铝与三氧化二铁的反应(铝热反应)2Al+Fe2O3==== 2Fe+Al2O3112.铝与二氧化锰的反应(铝热反应)4Al+3MnO2==== 3Mn+2AlO3 113.氧化铝与盐酸的反应Al2O3+6HCl==== 2AlCl3+3H2O114.氧化铝与氢氧化钠的反应Al2O3+2NaOH+3H2O==== 2Na[Al (OH)4]115.电解氧化铝2Al2O3==== 4Al+3O2↑116.硫酸与与一水合氨的反应Al2(SO4)3+6NH3•H2O==== 2Al(OH) 3↓+3(NH4)2SO4117.氯化铝与一水合氨的反应AlCl3+3NH3•H2O==== Al(OH)3↓+3NH4Cl118.氯化铝与氢氧化钠(少量)的反应AlCl3+3NaOH==== Al(OH)3↓+3NaCl119.氢氧化铝与氢氧化钠的反应Al(OH)3+NaOH==== Na[Al(OH)4]120.氯化铝与氢氧化钠(过量)的反应AlCl3+4NaOH==== Na[Al(OH) 4]+3NaCl121.四羟基合氯酸钠与盐酸(少量)的反应Na[Al(OH)4]+HCl==== Al (OH)3↓+NaCl+H2O122.氢氧化铝与盐酸的反应Al(OH)3+3HCl==== AlCl3+3H2O 123.四羟基合氯酸钠与盐酸(过量)的反应Na[Al(OH)4]+4HCl==== A lCl3+NaCl+4H2O124.四羟基合氯酸钠与氯化铝的反应3Na[Al(OH)4]+AlCl3==== 4Al (OH)3↓+3NaCl125.向四羟基合氯酸钠中通入过量二氧化碳Na[Al(OH)4]+CO2==== Al(OH)3↓+NaHCO3126.铜在潮湿空气中被腐蚀2Cu+O2+H2O+CO2==== Cu2(OH)2C O3127.铜与氧气的反应2Cu+O2==== 2CuO128.铜与氯气的反应Cu+Cl2==== CuCl2129.铜氧化在高温下转化4CuO==== 2Cu2O+O2↑130.硫酸铜与水的反应CuSO4+5H2O==== CuSO4•5H2O1.与碱反应产生气体 (1)(2)铵盐:O H NH NH 234+↑−→−+碱2.与酸反应产生气体(1) (2)()()()2332222332HH HCO HCO CO S HS HS SO HSO SO +++------⎧−−→↑⎪⎪−−→↑⎨⎪−−→↑⎪⎩化合物3.Na 2S 2O 3与酸反应既产生沉淀又产生气体:S 2O 32-+2H +=S ↓+SO 2↑+H 2O4.与水反应产生气体(1)单质 (2)化合物5.强烈双水解⎪⎪⎩⎪⎪⎨⎧↑+=++↑+=++↑−−→−-232222222232222H SiO Na O H NaOH Si H NaAlO O H NaOH Al H Si Al OH 、单质⎪⎪⎪⎪⎪⎩⎪⎪⎪⎪⎪⎨⎧⎪⎪⎩⎪⎪⎨⎧⎪⎩⎪⎨⎧↑↑−−→−↑−−−→−⎪⎩⎪⎨⎧↑↑−−→−↑↑−−−→−⎪⎩⎪⎨⎧↑↑−−→−↑−−−→−↑−−→−2222222222342342342NO SO SO S CO NO CO SO C NO NO SOH HNO SO H HNO SOH HNO SO H HCl 、、、非金属、金属单质浓浓浓浓浓⎪⎩⎪⎨⎧↑+=+↑+=+22222422222O HF O H F H NaOH O H Na()()()⎪⎪⎩⎪⎪⎨⎧↑+=+↑+↓=+↑+↓=+↑+=+22222232323222322222326233422H C OH Ca O H CaC S H OH Al O H S Al NH OH Mg O H N Mg O NaOH O H O Na ()()⎪⎧↓+↑−−→−----+232323322OH Al CO HCO CO O H OH6.既能酸反应,又能与碱反应(1)单质:Al (2)化合物:Al 2O 3、Al(OH)3、弱酸弱碱盐、弱酸的酸式盐、氨基酸。
溶解性表详解讲解

NH 3.H2O (溶、挥) KOH (溶)
NaOH (溶) Ba(OH )2(溶) Ca(OH)2 (微) Mg(OH)2(不) Al(OH )3 (不) Mn(OH )2(不) Zn(OH)2(不) Fe(OH)2(不)
Na2SO4 (溶)
Na2CO3 (溶)
BaSO4
CaSO4
(不)
(微)
BaCO3
SO4 2- (硫酸根) CO32 - (碳酸根)
H2SO4 (硫酸) H2CO3 (溶) (NH4)2SO4(硫酸铵) K2SO4 (硫酸钾) (NH4)2CO3(溶) K2CO3 (溶)
H+ NH 4+ K+ Na + Ba2+ Ca 2+ Mg2+ Al 3+ Mn2+ Z n2+ Fe2+ Fe3+ Cu2 + Ag +
H+ NH 4+ K+ Na + Ba2+ Ca 2+ Mg2+ Al 3+ Mn2+ Z n2+ Fe2+ Fe3+ Cu2 + Ag +
NH 3.H2O (铵水) KOH (氢氧化钾)
NaOH (氢氧化钠) Ba(OH )2(氢氧化钡) Ca(OH)2 (氢氧化钙) Mg(OH)2(氢氧化镁) Al(OH )3 (氢氧化铝) Mn(OH )2(氢氧化锰) Zn(OH)2(氢氧化锌) Fe(OH)2( 氢氧化亚铁)
(不)
(不) (微) ——
CaSO4
(硫酸钙)
Mg(NO3)2(硝酸镁)
MgSO4 (硫酸镁) Al2(SO4)2 (硫酸铝) MnSO4 (硫酸锰)
700种无机有机化合物溶解度

叠氮化钙 Ca(N3)2
磷酸二氢 钙 Ca(H2PO4)2 氟化钙 CaF2
氟硅酸钙 CaSiF6
甲酸钙
Ca(HCO2)2
16.1
16.6 4.303×10-3
17.1
磷酸氢钙 CaHPO4 氢氧化钙 Ca(OH)2 碘酸钙 碘化钙 钼酸钙 硝酸钙 Ca(IO3)2 CaI2 CaMoO4 Ca(NO3)2 · 2O 4H Ca(NO2)2 亚硝酸钙 · 2O 4H 草酸钙 CaC2O4 高氯酸钙 Ca(ClO4)2 高锰酸钙 Ca(MnO4)2 磷酸钙 硒酸钙 硫酸钙 钨酸钙 氟化锆 硫酸锆 砷酸镉 溴酸镉 溴化镉 碳酸镉 氯酸镉 氯化镉 Ca3(PO4)2 CaSeO4· 2O 2H CaSO4· 2O 2H CaWO4 ZrF4 Zr(SO4)2· 2O 4H Cd3(AsO4)2 Cd(BrO3)2 CdBr2 CdCO3 Cd(ClO3)2 CdCl2 299 100 308 135 56.3 75.4 9.73 0.223 9.77 0.244 63.9 102 115 0.189 9×10-2 64.6 0.182
4.642×10-2 124 123 130 130 220 2.727×10-2 1.352×10-6 4.351×10-7 3.246×10-5 2.313×10-3 2.266×1012
152
高氯酸铬 Cr(ClO4)3
325
407 4.277×10 25 1.1 0.08
-2
455
499
0.4 4.82
0.56 25 6.57 9.3 2.372×10-3 6×10-3
0.66 8.34
0.91 10.2
草酸汞 硫化汞
HgC2O4 HgS Co(BrO3)2
初中九年级化学溶解性表巧用

Cl- 氯离子 HCl↑ NH4Cl
KCl NaCl
变化一下,直接看矩形对角线:
NaOH + NH4Cl
△ =====
NaCl + NH3 ↑+ H2O
左上角的氨水不稳定易分解,受热挥发出氨气。
例 2:氢氧化钡和硝酸镁能否发生反应? NaOH Ba(OH)2
Ca(OH)2 Mg(OH)2↓ 变化一下,直接看矩形对角线:
根据溶解性或对反应物可溶性要求,可直接画矩形看对角,进行反应判断。
6、金属氧化物、非金属氧化物的有关反应。
非金属氧化物
金属氧化物
(1)大多数可与水反应生成酸
(1)少数可与水反应生成碱
1. CO2+H2O== H2CO3
Na2O +H2O== 2NaOH
2. SO2+H2O== H2SO3
K2O +H2O== 2KOH
一张溶解性表格的使用拓展
1、基础知识回顾
1.1 酸:解离时生成的阳离子部是氢离子(H+)的化合物叫做酸;
1.2 碱:解离时所有阴离子都是氢氧根离子(OH-)的化合物叫做碱;
1.3 盐:是指一类金属离子或铵根离子(NH4+)与酸根离子结合的化合物;
1.4 氧化物:由两种元素组成的化合物,其中一种是氧元素。
Al(OH)3↓ Cu(OH)2↓ Fe(OH)2↓
3.2 蓝色区域:酸
Fe(OH)3↓
3.3 红色区域:盐
HNO3↑ HCl↑
H2SO4
H2CO3↑
NH4NO3 KNO3
NH4Cl KCl
(NH4)2SO4 K2SO4
(NH4)2CO3 K2CO3
NaNO3 Ba(NO3)2 Ca(NO3)2 Mg(NO3)2
溶解性表详解

Al2(SO4)2 (硫酸铝)
——
MnSO4 (硫酸锰) ZnSO4 (硫酸锌)
MnCO3 (不) ZnCO3 (不)
Fe2+
Fe(OH)2( 氢氧化亚铁) Fe(NO3)2 (硝酸亚铁) FeCl2 (氯化亚铁) Fe SO4 (硫酸亚铁) FeCO3 (不)
Fe3+
Fe(OH )3(氢氧化铁) Fe2(NO3)3(硝酸铁) FeCl3(氯化铁)
Ag +
AgCl(氯化银)
SO4 2- (硫酸根) CO32 - (碳酸根)
2.它们的阴离子全部是Cl - , 酸根离子全部是Cl- 离子的 化合物叫盐酸盐。 3.除AgCl不溶,12种盐酸 盐可溶。
部分酸、碱和盐的溶解性表(室温)
阳 离
阴离子 OH - (氢氧根) NO3 - (硝酸根) Cl- (盐酸根)
NH4NO3(硝酸铵)
KOH (氢氧化钾) KNO3 (硝酸钾)
Na +
NaOH (氢氧化钠) NaNO3(硝酸钠)
Ba2+
Ba(OH )2(氢氧化钡) Ba(NO3)2 (硝酸钡)
Ca 2+
Ca(OH)2 (氢氧化钙) Ca(NO3)2 (硝酸钙)
Mg2+
Mg(OH)2(氢氧化镁) Mg(NO3)2(硝酸镁)
Mg(NO3)2(硝酸镁)
Al2(NO3)3 (硝酸铝)
Mn(NO3)2 (硝酸锰) 2.除HNO3外,13种盐的阴离子全部是NO3 - , Zn(NO3)2 (硝酸锌) 酸根离子全部是NO3 - 离子的化合物叫硝酸盐。
Fe(NO3)2 (硝酸亚铁) 3.13种硝酸盐全溶。
Fe2(NO3)3(硝酸铁)
溶解性表

1、每一个空格代表一种化合物,参照例子完成其它空格。
2、化合物
根据酸、碱、盐离子构成的特点,分别从表中画出酸、碱、盐区域 3、盐的数量比较多,经常把含有某种相同离子的盐称为某盐。
例:KNO 3、KCl 、K 2SO 4、K 2CO 3都含有钾离子K +,称为钾盐
KNO 3、NaNO 3、Mg(NO 3)2、Ca(NO 3)2等都含有硝酸根NO 3-,称为硝酸盐。
根据规律,你还能找出其它某盐吗?如铵盐、钠盐、硫酸盐、碳酸盐在哪里?
酸:由H +与酸根离子(NO 3-、Cl -、SO 42-、CO 32-等)构成的化合物。
读作某酸
碱:由金属离子与OH -构成的化合物。
读作氢氧化某
盐:由金属离子(或铵根离子NH 4+)与酸根离子构成的化合物。
读作某酸某 氧化物:两种元素组成,其中一种是氧元素的化合物。
常用化合物在不同温度下的溶解度
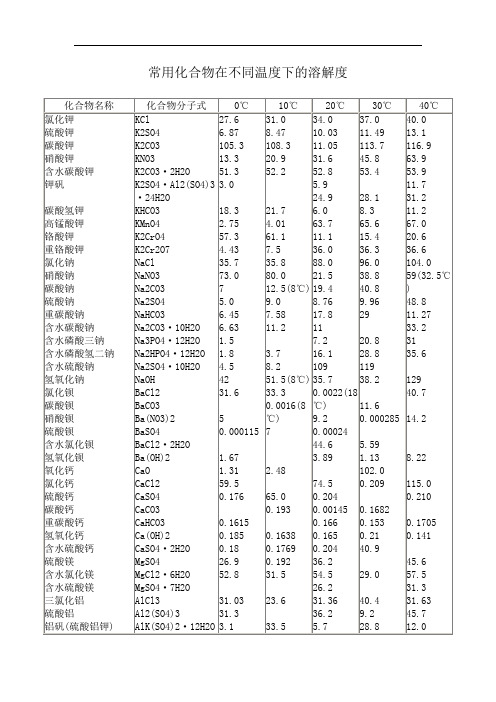
33.2
Na3PO4·12H2O 1.5
7.2
20.8
31
Na2HPO4·12H2O 1.8
3.7
16.1
28.8
35.6
Na2SO4·10H2O 4.5
8.2
109
119
NaOH
42
51.5(8℃) 35.7
38.2
129
BaCl2
31.6
33.3
0.0022(18
40.7
BaCO3
0.0016(8 ℃)
53.4
53.9
K2SO4·Al2(SO4)3 3.0
5.9
11.7
·24H2O
24.9
28.1
31.2
KHCO3
18.3
21.7
6.0
8.3
11.2
KMnO4
2.75
4.01
63.7
65.6
67.0
K2CrO4
57.3
61.1
11.1
15.4
20.6
K2Cr2O7
4.43
7.5
36.0
36.3
36.6
BaCl2
43.6 46.4
58.8
BaCO3
27
Ba(NO3)2
17.1 20.3
34.2
BaSO4
0.00033
0.00041
BaCl2·2H2O
0.210
CaCO3
0.193 0.00145 0.1682
CaHCO3
0.1615
0.166 0.153 0.1705
Ca(OH)2
0.185 0.1638 0.165 0.21
化合物溶解度表(很实用)

6
263
磷
酸 氢
BaHPO4
钡
1.3×10
-2
亚 磷 酸 BaHPO3 氢 钡
0.687
氢
氧 化
Ba(OH)2· 1.
8H2O
67
2.4 8
3.89
钡
5.59 8.22
20. 9
101
碘 酸 Ba(IO3)2 钡
3.5×10 4.6× 5.7×
-2
10-2
10-2
碘 化 BaI2 钡
18 2
201
1.096× 10-10
1.561× 10-20
3.109× 11
1.352× 10-7
3.144× 10-4
(II I)
氟 化 钚 PuF4 (IV )
碘 酸 钚 Pu(IO3)4 (IV )
3.622× 10-4
7.998× 10-2
[编辑] 氮、镝
物 质
化学式
0° 10 C °C
20°C
NH4I
155 163 172 182 191
209
229
250
硝酸 铵
NH4NO3
118 150 192 242 297
421
580 740 871
高碘 酸铵
(NH4)5IO6
2.7
草酸 铵
(NH4)2C2O
4
2.2
3.21 4.45
6.09 8.18
高氯 酸铵
NH4ClO4
12
16.4 21.7 37.7 34.6
173
铵
氟硅 (NH4)2Si 酸铵 F6
18.6
甲酸 铵
NH4HCO2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
陽離子
鹼 金 屬 鹼
H+ Na+ K+ Mg2+
反應
[1]
土
Ca2+
HCl
HCl
不溶
水
水
水
反應
[1]
微溶
HCl
水
HCl
HCl
HCl
略溶
HCl
HCl
水
水
水
水
水
水
水
水
略溶, HCl
略溶, HCl 略溶, HCl
解
水
水
水
金
Sr2+
HCl
HCl
Байду номын сангаас
HCl
水
水
水
微溶
[2]
不溶
HCl
水
HCl
HCl
HCl
略溶
HCl
水 - 不溶 不溶 水 不溶 不溶 - 不溶 不溶
水 水 水 水 水 水 水 不溶 HNO3 水
水 水 水 水 水 水 水 解 水 水
水 - 水 - 水 水 水 - 水 水
水 水 水 水 水 水 水 水 水 水
HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl
HCl HCl HCl HCl HCl HCl HCl 不溶 HCl HCl
HCl HCl HCl HCl HCl HCl HCl - HCl HCl
HCl 水 略溶, HCl HCl 水 水 HCl - 水 HCl
HCl HCl 略溶, HCl 氧還 水 HCl HCl - 水 水
略溶, HCl HCl HCl 不溶 - HNO3 HNO3 不溶 HCl HCl
水 - HCl 不溶 不溶 不溶 不溶 - 不溶 不溶
HCl - 水 水 - 水 水 - - 水
HCl HCl HCl HCl HCl HCl HCl - HCl HCl
HCl - HCl HCl HCl HCl HCl - HCl HCl
HCl HCl HCl HCl HCl HCl HCl - HCl HCl
HCl HCl HCl HCl HCl HCl HCl - HCl HCl
陰離子
碳 CO32 − NH4+ 水 弱、揮 水 水 略溶 C2O42 − 水 水 水 水 水 水 弱、揮 水 水 HCl F− 水 溶、揮 水 水 水 Cl −
鹵素 Br − 水 溶、揮 水 水 水 水 水 水 水 水 I− 水 水 水 水 S2 − SO42 − 水 水 水 水 水
硫 SO32 − 水 水 水 水 水 S2O32 − 水 水 水 水 水 AsO43 − 水 水 水 水 HCl AsO33 − 水 水 水 水 HCl PO43 − 水 水 水 水 HCl BO2 − 水 水 水 水 HCl SiO32 − 水 水 水 水 HCl C4H4O62 − 水 水 水 水 水 CrO42 − 水 水 水 水 水 水 水 水 水 水 CN − [Fe(CN) [Fe(CN) 6]4 − 6]3 − 水 水 水 水 水 水 水 水 水 水 SCN − 水 水 水 水 水 CH3COO − 水 水 水 水 水 NO2 − 水 水 水 水 水 NO3 − 水 水 水 水 水 解 弱 水 水 HCl O2 − 水 弱 水 水 HCl OH − H− 本身不穩 定 不溶 解 解 解 ClO4 − 水 水 水 水 水 MnO4 − 略溶 水 水 水 水 N3 − 幾乎不溶 水 水 水 水
解 解 解 解 解 解 解
水 水 水 水 水 水 水 水 水 水
微溶 水
水 - HNO3 HNO3 HNO3 HNO3 HNO3 HNO3 HNO3 HNO3
氧還
[3] 水 水 水 水 水 水 水
金
Cu+ Cu2+ Zn2+
氧還
[4] 略溶, HCl HCl
水
水 水
[5]
水 HCl HCl
不溶
[6][7] - 解
HCl
略溶
水
水
水
水
水
水
水
HCl
解
水
水
水
屬 過 第 一 過 渡 渡 系
Ba2+ Cr3+ Mn2+ Fe2+ Fe3+ Co2+ Ni2+
HCl - HCl HCl 解 HCl HCl 不溶
HCl HCl HCl HCl HCl HCl HCl - HCl HCl
略溶 水 HCl 略溶, HCl 略溶, HCl HCl HCl
HCl[8]
HCl
屬
第 二 過 渡 第 三 過 渡 系 Hg22+ Hg2+ Al3+ HNO3 HCl 解 HNO3 HCl HCl 水 水 水 HNO3 水 水 HNO3 水 水 HNO3 HCl 水 王水 王水 水解, HCl 略溶 略溶 水 HNO3 HCl HCl - - 水 HNO3 HCl HCl HNO3 HCl - HNO3 HCl HCl - - HCl - - HCl 略溶, HNO3 HCl 水 HNO3 HCl - - 水 - - - - - 不溶 - HNO3 水 水 水 水 水 水 水 - 略溶, HNO3 水 水 HNO3 HCl HCl Au3+ 不溶 略溶 Cd2+ HCl HCl 略溶, HCl 水 水 水 HNO3 水 HCl 水 HCl HCl HCl HCl HCl HCl HCl HCl 不溶 不溶 HCl 水 水 水 HCl Ag+ HNO3 HNO3 水 不溶 不溶 不溶 HNO3 略溶 HNO3 HNO3 HNO3 HNO3 HNO3 HNO3 HNO3 HNO3 HNO3 不溶 不溶 不溶 不溶 略溶 熱水 水 HNO3
水
水
水
不溶
水
不溶
水
-
-
不溶
-
-
-
水
-
-
-
-
-
水
水
-
不溶
-
水
水
不溶
族 碳 金 族
Tl+ C4+ Sn2+ Sn4+
水
水
微溶 微溶 水解, HCl 水解, HCl 沸水 水解, HCl 水解, HCl 水解, HCl 略溶
微溶 微溶 水解, HCl 水解, HCl 不溶 水解, HCl 水解, HCl 水解, HCl 弱、揮
水 水 水 水 水 水 水 微溶 水 水
水 水 水 水 水 水 水 HCl 水 水
水 水 水 水 水 水 水 不溶 略溶 水
反應
[1] 水解, HCl HCl HCl HCl HNO3 HNO3 微溶, HCl HNO3 HCl
不溶 水 水 水 水 水 水
HCl - HCl HCl 解 HCl HCl
不溶
[9][10] HCl
不溶
水
解[11]
水
HNO3
-
水
HNO3
水
[12]
水
微溶
不溶
不溶
水
-
-
-
-
不溶
-
-
-
-
熱水
-
-
-
-
水
水
HCl
酸
- - HCl
[13]
-
水
水
-
不溶 - 解
水 水 水
水 水 水
- HNO3 不溶
主
硼
族
Ga3+
不溶
略溶
酸, 氧還
[14] 微溶 微溶 水 水 略溶, HNO3 [17]
