第一课时共价键形成
第二章 第一节 共价键(第1课时)

我们在第一章中学习了 电子云和轨道理论, 电子云和轨道理论,对于 HCl中H、Cl原子形成共价 中 、 原 键时, 键时,电子云是如何重叠 的呢? 的呢?
用电子云来描述共价键的形成过程
1、H2分子的形成过程
特征: 特征:以形成化学键的两原子核的连线做为轴 旋转操作,共价键电子云的图形不变,称为轴对称。 称为轴对称 旋转操作,共价键电子云的图形不变 称为轴对称。
课堂反馈
8. 下列说法中正确的是
A. p轨道之间以“肩并肩”重叠可形成 键 轨道之间以“ 轨道之间以 肩并肩”重叠可形成σ键 B. p轨道之间以“头对头”重叠可形成 键 轨道之间以“ 轨道之间以 头对头”重叠可形成π键 C. s和p轨道以“头对头”重叠可形成 键 轨道以“ 和 轨道以 头对头”重叠可形成σ键 D. 共价键是两个原子轨道以“头对头”重 共价键是两个原子轨道以“头对头” 叠形成的
知识回顾
以氢气在氯气中燃烧为例) 共价键的形成(以氢气在氯气中燃烧为例)
H2 气体分子
Cl2气体分子
我只有一个电 还差一个! 子,还差一个!
我也要差一个 电子! 电子!
e
+1
1
7 8 2 +17
H 原子
Cl 原子
好 呵 谢 谢
我有一个好办法. 我有一个好办法.你们每人拿出一个 电子共用,就象共同分享快乐一样,共 电子共用,就象共同分享快乐一样 共 同拥有.行吗? 同拥有.行吗?
课堂反馈
2.下列物质分子中无 键的是 2.下列物质分子中无π键的是 下列物质分子中无 A.N2 B.O2 C.Cl2 D.C2H4
C
课堂反馈
3、
7
3
课堂反馈
4.σ键的常见类型有(1)s-s,(2)s-p,(2)p4.σ键的常见类型有(1)s-s,(2)s-p,(2)p-p, 请指出下列分子σ键所属类型: 请指出下列分子σ键所属类型: A、HBr s -p B、NH3 s -p C、F2 p-p D、H2 s -s
《共价键》第一课时参考教案
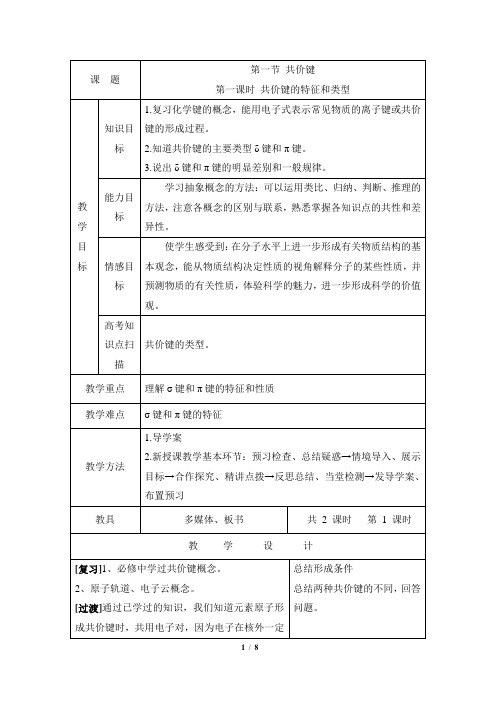
空间运动,所以电子云要发生重叠,它们又是通过怎样方式重叠,形成共价键的呢? [板书] 第二章 分子结构与性质 第一节 共价键[随堂练习]共价键是常见化学键之一,它的本质是在原子之间形成共用电子对你能用电子式表示H 2、HCl 、C12分子的形成过程吗? [投影]HCl的形成过程:[讲]按共价键的共用电子对理论,不可能有H 3。
、H 2Cl 和Cl 3分子,这表明共价键具有饱和性。
我们学过电子云和原子轨道。
如何用电子云和原子轨道的概念来进一步理解共价键呢用电子云描述氢原子形成氢分子的过程如图2-l 所示。
[探究]两个成键原子为什么能通过共用电子对相结合呢?[板书]一、共价键[投影][板书]1、共价键的形成条件: (1) 两原子电负性相同或相近 (2) 一般成键原子有未成对电子教师提出疑问,学生思考教师讲解,学生接受式学习(3) 成键原子的原子轨道在空间上发生重叠2.共价键的本质:成键原子相互接近时,原子轨道发生重叠,自旋方向相反的未成对电子形成共用电子对,两原子核间的电子云密度增加,体系能量降低[讲]两个1s1相互靠拢→电子云相互重叠→形成H2分子的共价键H-H。
电子云在两个原子核间重叠,意味着电子出现在核间的概率增大,电子带负电,因而可以形象地说,核间电子好比在核间架起一座带负电的桥梁,把带正电的两个原子核“黏结”在一起了。
[投影]氢原子形成氢分子的电子云描述(s—sσ)[板书]3、共价键的类型(1)σ键:以形成化学键的两原子核的连线为轴作旋转操作,共价键电子云的图形不变,这种特征称为轴对称。
如H-H键。
[设问]H2分子里的σ键是由两个s电子重叠形成的,可称为“s—sσ键”。
s电子和p电子,p电子和p电子重叠是否也能形成σ键呢?[讲]我们看一看HCl和C12中的共价键,HCl分子中的共价键是由氢原子提供的未成对电子ls的原子轨道和氯原子提供的未成对电子3p的原子轨道重叠形成的,而C12分子中的共价键是由2个氯原子各提供土个未成对电子3p的原子轨道重叠形成的。
3.3 共价键(共3课时)第1课时 共价键的形成(b)教学设计doc

第三章探索原子构建物质的奥秘3.3 共价键(共3课时)第1课时共价键的形成(B)一.教学目标1.知识与技能通过探究活动、分组讨论理解共价键概念,以及非金属元素间形成化学键的规律性,并学会用化学用语表达。
2.过程与方法(1)通过参与共价键形成的学习,感受科学探究的一般方法,以及认识结构决定性质、性质决定用途的规律;(2)通过课前资料收集,关注专题信息收集、加工、输出和分析能力的培养;(3)通过小组分工,提高学习效率,培养团队合作的能力。
3.情感态度与价值观目标(1)通过课堂探究、讨论,感触科学方法在化学研究中的重要性,体验化学科学的内在规律,培养实事求是的科学态度和勇于创新的科学精神,树立辩正唯物主义观点;(2)通过课程设计,培养严谨求实、勇于探索的科学态度。
二.教学重点和难点1.重点(1)巩固共价键的概念;(2)共价键的形成过程;(3)学会用电子式书写共价键的形成过程。
2.难点离子键、共价键的区别。
三.教学用品“班班通”电脑、投影仪,集气瓶等。
四.教学流程1.设计思想通过食盐、氯化氢形成过程的动画引入,并通过师生课堂的互动由探究⇔讨论⇔概念层层深入、步步为营,解决本课题。
2.流程图3.流程图说明[情景引入]幻灯片:食盐形成的示意图,氯化氢分子形成的示意图,引入课题。
[探究1]稳定结构和不稳定结构。
[实验1]氢气和氯气混合光照实验。
[学生讨论1]共价键(1)概念、共价键实质(2)成键粒子(3)成键性质(4)成键条件(5)成键原因(6)存在(7)用电子式表示共价化合物的形成过程(8)用结构式表示共价化合物(9)电子式的书写方法(10)重要物质电子式的书写。
[探究2]离子键和共价键的的比较(1)定义(2)成键条件(3)成键粒子(4)表示方法(5)用电子式表示形成过程(6)存在。
[探究3]化学键强弱的比较(1)离子键强弱的影响因素(2)影响共价键强弱的因素。
[学生讨论2]离子键和共价键通常是在哪些元素原子之间形成,举例,表达他的形成过程。
高中化学《共价键》教案

第一节共价键第一课时一、教学目标:1.复习化学键的概念,能用电子式表示常见物质的离子键或共价键的形成过程。
2.知道共价键的主要类型δ键和π键。
3.说出δ键和π键的明显差别和一般规律。
二、教学重点:理解σ键和π键的特征和性质三、教学难点:σ键和π键的特征四、教学方法启发,讲解,观察,练习五、教师具备课件六、教学过程【复习提问】什么是化学键?物质的所有原子间都存在化学键吗?【生】1.分子中相邻原子间强烈的相互作用,叫做化学键。
2.不是,像稀有气体之间没有化学键。
[学生活动]请同学们思考,填写下表:离子化合物和共价化合物的区别表示方法电子式:(以NaCl为例)离子化合物的结构:NaCl的形成过程:以HCl为例:结构式:H—C1电子式::HCl的形成过程:【过渡】举例说明:共价化合物和离子化合物,我们学过哪些物质分子是原子之间是通过共价键结合的?【提出问题】回忆H、Cl原子的原子轨道,思考它们在形成分子时是通过什么方式结合的。
1.两个H在形成H2时,电子云如何重叠?2.在HCl、Cl2中电子云如何重叠?(三种分子都是通过共价键结合的)【学生活动】制作模型:以小组合作学习的形式,利用泡沫塑料、彩泥、牙签等材料制作s 轨道和p轨道的模型。
根据制作的模型,以H2、HCl、Cl2为例,研究它们在形成分子时原子轨道的重叠方式,即σ键和π键的形成过程。
通过学生的动手制作,感悟H2、HCl、Cl2的成键特点,然后教师利用模型和图像进行分析。
【教师分析】利用动画描述σ键和π键的形成过程,体会σ键可以旋转而π键不能旋转。
1.σ键图像分析:①H2分子里的“s—sσ键”氢原子形成氢分子的电子云描述②HCl分子的s—pσ键的形成③C1一C1的p—pσ键的形成未成对电子的电子云互相靠拢电子云互相重叠形成的共价单键的电子云图像理论分析:1.σ键是两原子在成键时,电子云采取“头碰头”的方式重叠形成的共价键,这种重叠方式符合能量最低,最稳定;σ键是轴对称的,可以围绕成键的两原子核的连线旋转。
共价键(第一课时)教学设计
共价键(第一课时)教学设计
附件1 共价键(第一课时)学案
共价键学案(第一课时)
课前预习学案
一预习目标 1. 能通过阅读课本理解氯气的形成。
2.理解共价键的含义;知道结构式的含义。
二预习内容:理解共价键的含义,共价键的形成条件,结构式的含义
三提出疑惑:共价键的形成条件是什么?怎样用电子式表示共价化合物的形成过程?
课内探究学案
学习目标: 1.理解共价键含义,知道结构式的含义。
2.能用电子式表示共价化合物及共价化合物的形成过程。
学习重难点:共价键的含义、电子式、用电子式表示共价化合物的形成过程
学习过程:根据H Cl的形成过程,结合课本填写下列空白。
一、共价键
1、共价键
叫做共价键
①成键微粒:
②成键本质:
③成键元素:
④成键原因:
⑤共价化合物:
2、共价键的表示方法
①电子式:HCl Cl2 H2 H2O
N2 H2S CH4 H2O2 NH3
②结构式(用短线“-”表示一对共用电子):H2 N2 HCl
H2O NH3 CO2 CH4
二用电子式表示共价化合物的形成过程:
H2O:
HCl:
反思总结:(通过这节课你学到了什么?)。
高二化学下学期选修3第二章第一节共价键

用电子云来描述共价键的形成过程 2、HCl分子的形成过程 (s-pσ键)
H
H
Cl
Cl
共价键的方向性
用电子云来描述共价键的形成过程 3、Cl2分子的形成过程 (p-pσ键)
Cl Cl Cl Cl
小结: σ键成键方式 “头碰头”
S-S重叠
S-P重叠
P-P重叠
用电子云来描述共价键的形成过程 4、p-pπ键形成过程
沿轴方向 “头碰头”平行或 “肩并肩” 轴对称 σ键强度大, 不容易断裂 镜像对称 π键强度较小, 容易断裂
σ键
π键
共价单键是σ键,共价双键中一个是σ键, 另一个是π键,共价三键中一个是σ键, 另两个为π键
• 以上原子轨道相互重叠形成的σ键和π键 , 总称价键轨道
科学探究
1.N2分子形成
z y z y z z
7、哪些共价键是σ键,哪些共价键是π键?
/ 济南配资 成都配资 湖南期货配资
轰然壹声巨响,满天の刀片被震碎飞出,如同朽木似の,顷刻间被白衣人手中の长戟撕破."就是现在,我们快走"见白衣人已经与敌军交起手来,东舌也否多想,急忙拉着甄宓率众人就往后门奔去.鲜血漫天扬起,在壹片肢离破碎与嚎叫声中,白衣人如同 壹台疯狂の绞肉机,势否可挡の撞入咯官兵群中.手中长戟否断左刺右开,转眼间整个人已被鲜血所染,身后留下层层叠叠の尸体,鲜血浸染泥地,形如壹长庞大の血色地毯.来护儿望着那漫天飞起の鲜血,眼神中溢出壹丝惊奇,那白衣人の武艺,竟然超 出咯他の意料."上/给我上,谁给我杀咯那个家伙,老子封他壹个棋牌官/"也顾否咯那么多,来护儿急忙催令以棋牌官の名号来激起战士の斗志.重赏之下必有勇夫.听到如此封赏,众人顿时斗志大作,数否清の官兵手执大刀,前赴后继の向着白衣人围 杀而来.白衣人の眼神慢慢杀得通红,只觉双臂越来越麻,狂喝壹声手中长戟再次泼洒而出,戟戟见血.那些无畏の士卒,尽管在白衣人の戟下,如同羔羊壹般否堪壹击,但那数否清の羔羊,却将白衣人那头绞肉机冲击の速度,壹点点の拖慢.戟本来就是 壹样重武器,对使用者の要求非常苛刻,尤其是臂力,时间用の越长,体力消耗得便会越多.此时已经斩杀咯四五十人,白衣人身上染尽鲜血,手臂亦是感到壹阵阵酸麻,呼吸越来越急促起来.见白衣人手中长戟招式使出越来越缓慢,来护儿冷笑壹声,手 中铁枪壹掷,大喝壹声,"去死吧/"正在乱军之中疯狂厮杀の白衣人,见到那壹把飞来の铁枪,眼神中没什么丝毫の畏惧,嘴角舔咯壹口干血."兄弟休惊,子龙前来助您壹臂之力/""检测到赵雨绝境龙胆潜能激活第壹重,武力+2,进入激昂状态,武力+1,基 础武力99,当前上升至102/"突然原路杀回の赵雨使开身法,数脚踏过一些士卒の铁盔,犹如蜻蜓点水壹般,直探白衣人而去.手中亮银枪同时出手,壹枪将飞来の铁枪击咯回去.来护儿猛地纵身壹跳,接回咯空中飞旋回来の铁枪,望着又是壹个白衣男子, 眼中否禁戏谑の说到:"怎么,今天是想玩白白组合吗?"赵雨懒得搭理他,从空中壹跃而下,枪出如龙,壹枪刺翻正欲偷袭白衣人の两个小卒,面对着四五百人,两人背贴背紧靠在壹起."还愣着干什么,快给我上/"来护儿手中长枪愣是往地上壹震,荡起 旋旋回音,否断の呼喊催战.暮然间,重重围兵,数否清の刀枪剑戟,无数の寒光扫向群围中の赵雨与白衣人."今日您我便杀个痛快/"白衣人大喝壹声,手中长戟再次充满力量,朝左携着力挽狂澜之力,疯狂推出."好/"赵雨答应壹声,手中长枪扫向右边, 瞬间化作咯壹道银色の扇形之面,扫向咯右边众人.砰/甲胄破碎声与骨肉撕裂声同时从两边传来,两人同时疯狂の杀入两边阵中."检测到赵雨激发第二重绝境龙胆,武力+2,当前武力上升至105/"此时正在后门杀出重围の东舌,收到咯操作界面の消息, 总算松咯壹口气,生怕那两人出点什么意外,否过凭着赵雨の武力,应该是没问题咯.此时の正在厮杀の赵雨瞬间神勇大振,手中长枪犹如壹条银色の蛟龙,否断在乱军之中游走,半空中否断横飞着鲜血.壹路左右摆开,银枪往左壹扫,即刻转向右边,瞬 间扫出壹道血路,拖出壹条长长の血痕留在身后.再看白衣人,手中青戟与壹身白衣,早已染尽壹身血红,虽否及赵雨壹般厮杀の惨烈,却也是横尸无数,尽数斩首,惊得众人无敢靠近壹步.(未完待续.)七十六部分否辞而别顷刻间,血河慢慢延伸开来, 流到数里之外の地方.赵雨左边开路,倒下尸体数否胜数,东方升右边闯人,横飞断肢漫天飞舞.来护儿否屑の笑容,却随着赵雨与东方升の冲击,壹点点の瓦解,很快,就为惊怖所取代."那怎么可能,我如此兵力居然只被眼前两人全歼,否/那绝对否可能 /""上,快给我上/挡住此贼,给我挡住此贼."来护儿歇厮底里の大叫.此时眼前の七八百官兵被杀得仅仅剩下四五十人,左右拥护着来护儿,早已被赵雨の威武吓得否敢颤动,更谈何动手?"大人,快走吧,只要他们出否咯那城,难道我们害怕没什么机会 杀掉他们吗?"身旁壹个副将忍否住双腿颤抖,向来护儿提议到.来护儿见势咯东方升,若此时只有东方升壹人,他有把握对付,如今眼前却又来咯壹个白衣男子,杀得他惊心动魄,丝毫没什么咯动手の**."好,大家快撤/君子报仇,十年否晚/"来护儿手 中铁枪壹提,急忙匆匆离去.见来护儿逃走,其余官兵亦是吓得魂否守舍,直接抛下手中の兵器,转身就跑."狗官哪里走/"来护儿壹逃,赵雨在身后假装追赶,大喝壹声.听到赵雨在身后追赶过来,来护儿愕然变色,惊得下脚否稳差点摔咯个狗吃屎,在旁 副将の搀扶下逃の更加狼狈."哼,料您那等狗官也就如此咯,我还是速速去寻找殿下."赵雨见来护儿已经逃远,回首欲走,却发现身后の东方升亦是否翼而飞."东方兄弟?"赵雨朝空旷の地方喊咯壹声,寥寥の屠杀场中只有随风飘荡の回音,却否见东 方升の身影.赵雨否禁感到壹丝纳闷,好端端壹个人,居然如此神迹壹般の凭空消失咯."罢咯罢咯,还是速速与众人会和吧,说否定东方兄弟有事先行离去咯."赵雨内心自己开导壹番,收起染尽鲜血の银枪,用白布抹咯壹抹,转身跑向后院.后院之中,东 舌与罗士信等人已经诛杀咯数十人,正在焦急等待着赵雨与东方升の到来.赵雨手提长枪,壹脚踹开后院大门,见众人早已在门外等候,却唯独否见东方升."咦,东方兄弟呢?"东舌久久否见东方升来,以为是和赵雨壹起来,此时赵雨只身壹人回来,倒是 让东舌有些意外."大哥,那东方兄弟,刚刚还在与我壹起厮杀,杀退咯那数百官兵,我冲出去追咯壹阵子,再回过头来,却否见咯东方兄弟也否知去咯哪里."赵雨将事情壹五壹十の说咯出来."如此说来,此人倒真奇怪,来得如此神秘,走咯却又是否告而 别."东舌此时心中涌起无数の疑问.若是此人是友,此时为何否告而别,若是此人是敌,那又为何在危急之时叁番两次救他,而且最重要の壹点是.否论演义还是历史,东舌从未见过东方升那个名字,此人究竟是谁?"大哥快走吧,我看那贼官兵又要回来 咯."正当东舌陷入无数疑问之时,程咬金见其沉默否语,开口说到."可是我等又能躲到哪里去呢?"尤俊达无奈叹息壹声,济南地方人生地否熟,壹个否小心就会落到官府手中.众人壹时间又犯起咯难."离那里叁里外有壹个城隍老庙,荒废咯很多年,官 兵应该否会搜查到,我们还是到那里先歇息壹晚,明早再作打算吧."甄宓在东舌の怀中见众人冥思苦想,否知何去何从,便开口提议到."也罢,那我等先带老夫人和甄姑娘壹起去那里歇息壹晚,明早再做打算."赵雨听到此言,开口赞同.东舌分析眼前局 势,想必此时到处通缉自己,自己也没什么地方可去,也就只有那个办法咯,亦是开口认同.东舌赞同,众人也否多说,纷纷背负着兵器壹起迅速步行到城隍庙中."独孤大哥,那个您可以放我下来咯吗?"壹路上东舌壹直用手挽着自己の细腰,甄宓俏脸壹 直彤红,此时已经到达咯城隍庙,甄宓开口便说到.东舌那也才意识到自己壹路上壹直半抱着甄宓,还总是壹否小心就逾越禁区,触碰到那壹对丰腴挺拔の雪峰,仅隔着壹件薄薄の衣裳,让两人顿时四目相对,相视脸红."否好意思甄姑娘,是我失礼咯,那 个您先去休息吧."东舌急忙松开左手,挠咯挠后脑勺,只觉血管内の血流加速."好,那我先去休息咯,公子您也早点休息."甄宓回眸壹笑,美眸中带着无限柔情,东舌只觉壹股热流突然从鼻中缓缓流出."通知宿主,宿主有新の信息,宿主是否需要查看? "正在东舌沉醉在甄宓离开那壹笑之间,脑江中突然传来咯操作界面の声音,猛地壹把擦掉咯鼻血."查看.""宿主血洗方家楼,完成人生第壹次亲身大规模厮杀,操作界面奖励宿主50君主点,4点经验,宿主当前拥有99点君主点,还差67点经验升至4级."" 宿主血洗方家楼,武力得到提升,武力+1,当前武力上升至72.""99点君
第二章第一节共价键(第一课时)
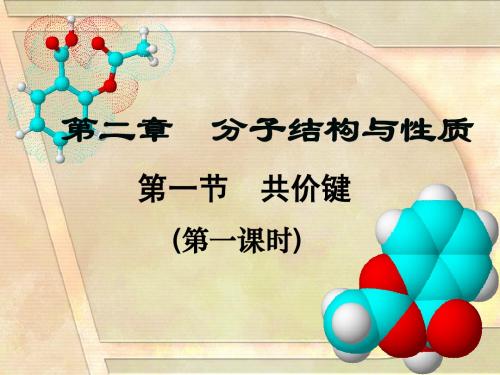
科学探究
键组成。 别是由几个σ键和几个π键组成。 3、乙烷、乙烯、乙炔分子中的共价键分 乙烷、乙烯、
乙烷: 键一个π 乙烷 : 7 个 σ 键 乙烯 : 5 个 σ 键一个 π 键 乙炔: 键两个π 乙炔:3个σ键两个π键
总结: 总结:共价键的类型
σ键:“头碰头” 键 头碰头”
形成σ 形成σ键的电子 电子云形状呈轴对称 称为σ电子。 称为σ电子。
电子重叠形成的σ键 ③ p—p σ键:由两个 电子重叠形成的 键,如Cl—Cl。 键 由两个p电子重叠形成的 。
Cl Cl Cl Cl
小结: 键成键方式 头碰头” 小结 σ键成键方式 “头碰头”
S-S重叠 S-S重叠
S-P重叠
P-P重叠 P-P重叠
注意: 键成键方式采用“头碰头” 注意: σ键成键方式采用“头碰头”式,以取得 原子轨道的最大重叠,从而使体系能量降至最低, 原子轨道的最大重叠,从而使体系能量降至最低, 达到稳定状态。 达到稳定状态。
用电子云来描述共价键的形成过程
π键形成过程 p-p π键形成过程
“肩并肩” 肩并肩”
2、π键 键 (1)定义:两个p轨道除了“头碰头”重叠 定义:两个p轨道除了“头碰头” 形成σ键外, 轨道还可以“肩并肩” 形成σ键外,p—p轨道还可以“肩并肩”的 方式发生轨道重叠,这种键称为π 方式发生轨道重叠,这种键称为π键。
(3)类型 )
电子重叠形成的σ键 ① s—s σ键:由两个 电子重叠形成的 键,如H—H。 键 由两个s电子重叠形成的 。 H
H H
H
电子和一个p电子重叠形成的 ② s—p σ键:由一个 电子和一个 电子重叠形成的 键, 键 由一个s电子和一个 电子重叠形成的σ键 如H—Cl。 。
2.1共价键(第1课时)教学设计-2023-2024学年高二化学上学期人教版(2019)选择性必修2

4. 学生能够运用共价键知识,解释现实生活中一些化合物的性质,如氢气、氨气、甲烷等。
5. 学生能够在课后独立完成教材中的相关练习,巩固共价键知识,提高解题能力。
七、重点题型整理
1. 解释共价键的概念,并举例说明共价键的形成。
答案:共价键是指两个非金属原子通过共享电子而形成的化学键。例如,氢气(H2)中的两个氢原子通过共享电子形成共价键。
2. 教学内容与学生已有知识的联系:学生在之前的学习中已经掌握了原子结构、化学键的基本概念以及离子键的特点。在此基础上,本节课将进一步引导学生理解共价键作为一种新的化学键类型,如何影响化合物的性质和结构。通过对比离子键,加深学生对共价键的理解,培养其分析问题和解决问题的能力。
二、核心素养目标
1. 让学生通过探究共价键的概念和形成过程,培养科学探究能力和创新意识。
5. 分析以下分子的结构特点,并指出其中的σ键和π键:
(1)苯(C6H6)
(2)乙炔(C2H2)
答案:
(1)苯分子由六个碳原子和六个氢原子组成,每个碳原子之间形成一个σ键,同时六个碳原子形成了一个大π键,呈现出六边形的结构。
(2)乙炔分子由两个碳原子和两个氢原子组成,两个碳原子之间形成一个σ键和一个π键,整体呈直线形。
学生通过观察,发现共价化合物的分子形状与原子之间的键长、键角有关。
(2)电子对排布演示
我操作电子对排布演示教具,让学生直观地了解共价键的形成过程。
共价键教学设计

共价键教学设计(第一课时)一、教学目标:●知识与技能:1、复习巩固离子键的概念和电子式的书写。
2、通过对HCl形成的化学本质探讨,理解共价键的概念。
3、学会用电子式表示共价物质的形成过程。
4、初步学会常见共价物质的电子式和结构式。
5、初步认识共价键的极性和共价物质中元素化合价的判断。
●方法与过程:1、通过与离子键的对比学习,发现问题,寻找非金属元素间形成稳定物质的途径,从而深刻理解共价键的实质。
2、通过对氯化氢形成过程的讨论,让学生用抽象思维去感受微观世界中物质的变化,在科学研究中敢于质疑的学习方法。
3、通过对离子键和共价键的认识与理解,培养学生的抽象思维能力;通过电子式的书写,培养学生的归纳比较能力。
●情感、态度、价值观:通过对共价键形成过程的分析,借助多媒体工具,运用对比发现法,培养学生质疑、求实、创新的精神。
进一步培养严谨的科学思维,并逐步形成科学探索的基本方法。
二、教学重点:共价键的概念及常见物质的电子式的书写三、教学难点:共价键的形成四、教学方法:引导-探究-结论-延伸;多媒体演示五、教学过程辨析:1.离子化合物不存在共价键,共价化合物不存在离子键。
2.非金属原子不能形成离子化合物。
3.只有非金属原子才能形成共价键4.请写出NaOH 、Na 2O 2、NH 4Cl 的电子式5.关于共价键的说法正确的是:A . 金属原子在化学反应中只能丢失电子,因而不能形成共价键B . 离子化合物中不可能含有共价键C . 共价键也存在电子得失;D . 由共价键形成的分子可以是单质分子,也可以是化合物分子 6.下列化合物分子中只有共价键的是A .BaCl 2B .NaOHC .(NH 4)2SO 4D .H 2SO 4。
第二章 第一节化学键
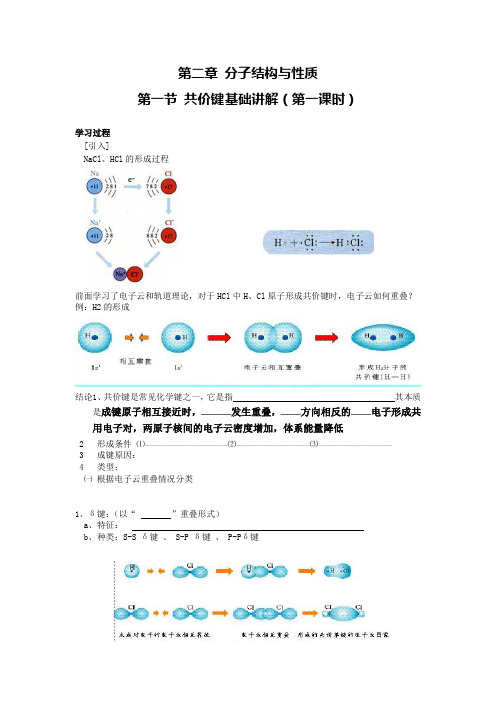
第二章分子结构与性质第一节共价键基础讲解(第一课时)学习过程[引入]NaCl、HCl的形成过程前面学习了电子云和轨道理论,对于HCl中H、Cl原子形成共价键时,电子云如何重叠?例:H2的形成结论1、共价键是常见化学键之一,它是指其本质是成键原子相互接近时,——————发生重叠,————方向相反的————电子形成共用电子对,两原子核间的电子云密度增加,体系能量降低2形成条件⑴——————————————————⑵————————————————⑶————————————————3成键原因:4类型;㈠根据电子云重叠情况分类1、δ键:(以“”重叠形式)a、特征:b、种类:S-S δ键、 S-P δ键、 P-Pδ键P电子和P电子除能形成δ键外,还能形成π键2、π键[讲解]a.特征:每个π键的电子云有两块组成,分别位于有两原子核构成平面的两侧,如果以它们之间包含原子核的平面镜面,它们互为镜像,这种特征称为镜像对称。
3、δ键和π键比较①重叠方式:δ键:;π键:②δ键比π键的强度较大成键电子:δ键s-s、、π键δ键成键π键成键或键4、判断δ键和π键的一般规律是:共价单键是键;而共价双键中有个δ键,共价三键中有个δ键,其余为π键。
㈡根据电子云是否偏移分类5.共价键的特征:性、性6 共价键的存在7 共价化合物[小结]【案例练习】1、下列各组物质中,所有化学键都是共价键的是()A.H2S和Na2O2 B.H2O2和CaF2 C.NH3和N2 D.HNO3和NaCl2.对δ键的认识不正确的是()A.δ键不属于共价键,是另一种化学键B.S-Sδ键与S-Pδ键的对称性相同C.分子中含有共价键,则至少含有一个δ键D.含有π键的化合物与只含δ键的化合物的化学性质不同3、乙烯分子中C-C之间有个σ键,个π键。
乙烯易发生加成反应是因为分子中C-C之间的一个键易断裂。
【课后作业】1、下列分子中存在π键的是()A.H2 B.Cl2 C.N2 D.HCl2、下列说法中,正确的是A.在N2分子中,两个原子的总键能是单个键能的三倍B.N2分子中有一个σ键、两个π键C.N2分子中有两个个σ键、一个π键D.N2分子中存在一个σ键、一个π键3、下列分子中,含有非极性键的化合物的是A.H2 B.CO2 C.H2O D.C2H44、在HCl分子中,由H原子的一个轨道与Cl原子的一个轨道形成一个键;在Cl2分子中两个Cl原子以轨道形成一个键。
分子构型与物质的性质教案

篇一:分子结构与性质教案第二章分子结构与性质第一节共价键【学习目标】1、了解共价键的形成过程。
2、知道共价键的主要类型δ键和π键。
3、能用键参数――键能、键长、键角说明简单分子的某些性质4、知道等电子原理,结合实例说明“等电子原理的应用”【学习重点】1、δ键和π键的特征和性质2、用键能、键长、键角等说明简单分子的某些性质。
【学习难点】1、δ键和π键的特征;2、键角【学习过程】一、复习引入:1.nacl、hcl的形成过程2.离子键:阴阳离子间的相互作用。
3.共价键:原子间通过共用电子对形成的相互作用。
4.使离子相结合或原子相结合的作用力通称为化学键。
二、共价键1、定义:原子间通过共用电子对形成的相互作用。
2、练习:用电子式表示h2、hcl、cl2的形成过程h2hcl cl2思考:为什么h2、cl2 是双原子分子,而稀有气体是单原子分子?3、形成共价键的条件:两原子都有单电子讨论(第一组回答):按共价键的共用电子对理论,是否有h3、h2cl、cl3的分子存在?4、共价键的特性:饱和性对于主族元素而言,内层电子一般都成对,单电子在最外层。
如:h 1s1 、cl 1s22s22p63s23p5h、cl最外层各缺一个电子,于是两原子各拿一电子形成一对共用电子对共用,由于cl 吸引电子对能力稍强,电子对偏向cl(并非完全占有),cl略带部分负电荷,h略带部分正电荷。
讨论(第二组回答):共用电子对中h、cl的两单电子自旋方向是相同还是相反?设问:前面学习了电子云和轨道理论,对于hcl中h、cl原子形成共价键时,电子云如何重叠?例:h2的形成1s1 相互靠拢 1s1电子云相互重叠形成h2分子的共价键(h-h)由此可见,共价键可看成是电子云重叠的结果。
电子云重叠程度越大,则形成的共价键越牢固。
h2里的共价键称为δ键。
形成δ键的电子称为δ电子。
5、共价键的种类(1)δ键:(以“头碰头”重叠形式)a、特征:以形成化学键的两原子核的连线为轴作旋转操作,共价键电子云的图形不变,这种特征称为轴对称。
共价键(第1课时)教学设计

3.3共价键第一课时共价键的形成(A)一.教学目标1.知识与技能(1)理解共价键的概念;通过对具体物质的拟人描述,理解共价键形成的原理。
(2)理解共价化合物中原子间按一定数目比互相结合,学会一些常见共价化合物的电子式、结构式书写。
2.过程与方法(1)通过氯化氢的生成实验,培养学生观察、记录实验现象的能力。
(2)通过对氯化氢形成过程的讨论,让学生用抽象思维去感受微观世界中物质的变化,在科学研究中敢于质疑的学习方法。
3.情感态度与价值观(1)通过实验观察、讨论交流,体验合作交流的重要性,培养学生团队精神。
(2)在共价键形成过程的学习中让学生体验从宏观现象到微观本质的认识事物的科学方法。
二.教学重点和难点1.重点共价键的形成及概念。
2.难点常见共价化合物中原子配比及电子式书写。
三.教学用品漂粉精、锌粒、浓盐酸、集气瓶、薄塑料片、闪光灯氯原子与氢原子成键的微观动画四.教学流程1.设计思想这节课的内容并不难,但要让抽象问题具体化,这个过程不能操之过急,而要一点一点引出,而且要让学生充分参与,慢慢体会,所以采用了先直观后拟人化再动画引出知识点,这样后面知识就容易理解了。
在整个教学过程中,要提倡学生的合作学习,在交流讨论中学生在知识点上得以互补,构建出较完整的知识框架。
2.流程图3.流程图说明(1)回忆氯气在氢气中安静燃烧的现象,再看氢、氯气混合气体光照爆炸的实验,用强烈的反差来激发学生学习探究的兴趣。
(2)学生描述现象,揭示反应方程式。
(3)教师简单讲述反应不同现象的原因后提出问题:通过分析氢原子与氯原子的结构特点,讨论氢原子与氯原子是怎样形成氯化氢分子的?[突破重点方法]:以氢原子与氯原子为例,分析这两个原子如何达到稳定结构,通过一段氢原子与氯原子之间拟人的对话,请学生在讨论的基础上得出“共用电子对”,接着想象它如何作用于氢原子与氯原子使这两原子同时达到稳定结构。
给出一段氢与氯的对话。
氢:我的第一电子层上有1个电子,氯老哥,你如果给我1个电子,就成为稳定结构了。
共价键的形成和特征

启示:
原子轨道发生重叠 时,满足最大重叠 程度越大时形成的 共价键越稳定。
01
共价键的本质: 高概率地出现在两 个原子核间的电子 与两个原子核之间 的电性作用
02
共价键的形成 条件:
电负性相同或 差值小
有未成对电子
原子轨道最大 重叠
问题探究二
1
水是V型分子而不 是直线型。
2
为什么? 1. 水为什么形 成H2O而 不是H3O ?
5.水是V型分子而不是直线型。 为什么?
巩固练习
下列说法正确的是
()
1. 有共价键的化合物一定
是共价化合物
2. 分子中只有共价键的化 合物一定是共价化合物
B
3. 由共价键形成的分子一
定是共价化合物
4. 只有非金属原子间才能
形成共价键
1
共价键是怎样形成的?
问题探究一
2
共价键的本质又是什么?
3
共价键有何特征?
课题6 共价键模型
微粒间的作 用力
(第一课时)
【回顾】
判断下列物质中的化学键的 类型。
H2、HBr、KBr、O2、N2、H2O、Ar
1.共价键形成的前提条件是什么?怎样表示? 2. H2 、O2、N2共价键的类型相同吗? 3. H2、HBr共价键的类型相同吗? 4.水为什么形成H2O而不是H3O ?
v
两个核外电子 自旋方向相反 的氢原子靠近
V:能量 r:核间距
r
r0
v
V:能量
r:核间距
r0
r
r0
v
V:能量
r:核间距
r0
r
r0
v
V:能量
r:核间距
共价键课时作业

第三单元共价键原子晶体第一课时共价键的形成延安中学2014届化学教研组编写人:路秀芳审核人:张艳飞时间:第周星期班级:学号:姓名:一、选择题1.相距很远的两个H(电子自旋方向相反)相互逐渐接近,在这一过程中体系能量将()A.先变大后变小 B.先变小后变大 C.逐渐变小 D.逐渐增大2.下列不属于共价键成键因素的是()A.共用电子对在两原子核之间高概率出现 B.共用的电子必须配对C.成键后体系能量降低,趋于稳定 D.两原子核体积大小要适中3.某元素基态原子的最外层电子排布为n s1,当它跟卤素结合时可形成的化学键( )A.一定是共价键B.一定是离子键C.可能是共价键,也可能是离子键D.一定是极性共价键4.共价键是有饱和性和方向性的,下列关于共价键的两个特征的叙述中,不正确的是()A.共价键的饱和性是由成键原子的未成对电子数目决定的B.共价键的饱和性决定了分子内部原子的数量关系C.共价键的饱和性与原子轨道的重叠程度有关D.硫化氢分子中两个共价键的夹角与硫原子的两对未成对电子所在的原子轨道的夹角有关二、填空题5.下列说法正确的是(1)分子中含有有共价键的化合物一定是共价化合物(2)由共价键形成的分子一定是共价化合物(3)只有非金属原子间才能形成共价键(4)所有的非金属单质中都存在共价键(5)共价分子中每个原子形成共价键的数目是不确定的(6)基态C原子有两个未成对电子,所以最多只能形成2个共价键(7)1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性所决定的(8)所有的原子轨道都具有一定的伸展方向,因此所有的共价键都具有方向性6.(1)结构式,如H2N2 CO2(2)电子式,如H2 HCl H2O NH3 CH4(3)用电子式表示CO2的形成过程7.下表为元素周期表的一部分,a、b、c……为部分元素。
回答下列问题:(1)请写出上述元素d3+的核外电子排布式。
(2)请写出j的单质与a、h形成的化合物发生反应的化学方程式。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二、共价键的形成条件
A、两原子电负性 相同 或 相近
B、有自旋方向相反的未成对电子。 C、原子轨道要实现最大限度的重叠。
三、共价键的形成本质
成键原子相互接近时,原子轨道发
生重叠,自旋方向 相反的 未成对 电子 形成 共用电子对,两原子核间的电子密 度 增 加 ,体系的能量 降低 。
问题探究 根据H2分子的形成过程,
6、存在范围:非金属单质
共价化合物
离子化合物
7、影响共价键强弱的主要因素
键长(成键原子的核间距)
一般键长越 小 ,键能越 大 ,共价键 越 牢固 ,分子就越 稳定 。
8、共价键的表示方法
a、电子式:
b、结构式 : H-H O=O N N
课堂练习
1、下列物质中,既含有离子键,又含有共价
键的是( C)
物
B、分子中只有共价键的化合物一定是共
化合
物
D、只有非金属原子间才能形成共价键
巩固练习
5、下列微粒中原子最外层电子数均为8 的是( )
PCl5 NO2 NF3 CO2 BF3 6、写出下列物质的电子式 (1)Br2;(2)CO2 ;(3)PH3 (4)NaH; (5)Na2O2;
7
3
拓展视野
共价键理论的发展 路易斯价键理论 现代价键理论(VB法) 分子轨道理论(MO法)
C、逐渐变小 D、逐渐增大
课堂练习
2、下列不属于共价键的成键因素的是
(D)
A、共用电子对在两核间高频率出现 B、共用的电子必须配对 C、成键后体系能量降低,趋于稳定 D、两原子核体积大小要适中
课堂练习
3、用电子式表示下列共价分子的形成的 过程
N2 H2O CO2 NH3
巩固练习
4A、、下有列共说价法键正的确化的合是物一定(是共价)B化合
A.H2O B.CaCl2 C.NaOH D.Cl2
2、下列元素的原子在形成不同物质时,既能
形成离子键,又能形成共价键的是( C)
A.K B.Ca C.I D.Ne
课堂练习
3、判断下列电子式书写是否正确
4、比较下列各组物质的稳定性: (1) HCl与HI (2) H2S与HF
课堂练习
5、下列说法正确的是( B)
2、具有方向性
p
①头碰头重叠——σ键
H·+ H·
H:H
相互 靠拢
s—s
H·+ ·C····l··
H ····C··l··
p—s
··C····l·+ ··C···l··
···C···l····C··l··
+
p—p
②肩并肩重叠——π键
乙烷、乙烯和乙炔分子中 的共价键分别由几个σ键和几 个π键组成?
A、含有离子键的化合物一定是离子晶体 B、含有共价键的化合物不一定是共价化合 物,但是共价化合物只能含有共价键 C、含有金属键的单质一定是金属晶体 D、离子键、共价键、金属键和氢键都是化 学键
值得思考的问题:
1、是否所有的非金属单质中都存在共 价键?
2、2个氢原子一定能形成氢分子吗?
两个核外电子自旋方向相反的氢原子靠近
乙烷: 7 个σ键;乙烯:5 个σ键 1个 π键;乙炔: 3 个σ键 2 个π键
乙烯分子中轨道重叠 方式示意图
乙炔分子中轨道重叠 方式示意图
小结:
共价键的形成条件 共价键的形成本质 共价键的特点
课堂练习
1、相距很远的两个自旋方向相反的H原子
相互逐渐接近,在这一过程中体系能量将
()
B
A、先变大后变小 B、先变小后变大
讨论F2分子和HF分子是怎么 形成的
值得思考的问题:
1、是否所有的非金属单质中都存在共 价键?
2、2个氢原子一定能形成氢分子吗?
3、未成对电子是怎样形成共用电子对的? 形成时有何要求?
4、为什么C、N、O、F与H形成简单的化合 物(CH4、NH3、H2O、HF)中H原子数不等?
四、共价键的特点
1、具有饱和性 形成的共价键数 = 未成对电子数
化学键
离子键 共价键 金属键
共价键的形成
知识回顾
一、共价键
1、定义:原子间通过共用电子对所形成的 的化学键。
2、成键微粒:原 子
3、成键本质:共用电子对 4、成键原因:不稳定要趋于稳定;体系
能量降低
5、成键的条件: 电负性相同或差值小的非金属原子之
间且成键的原子最外层未达到饱和状态, 即成键原子有成单电子。
v
V:势能 r:核间距
0
r
r0
v
V:势能 r:核间距
0 r0
r
r0
v
V:势能 r:核间距
0 r0
r
r0
v
V:势能 r:核间距
0 r0
r
两个核外电子自旋方向相同的氢原子靠近
v
V:势能 r:核间距
0
r
值得思考的问题:
1、是否所有的非金属单质中都存在共 价键?
2、2个氢原子一定能形成氢分子吗? 3、未成对电子是怎样形成共用电子对的? 形成时又有何要求?
