高一下学期化学期末常考知识点
高一年级化学必修二知识点综合考点2024

高一年级化学必修二知识点综合考点2024
以下是2024年高一年级化学必修二的知识点综合考点:
1. 化学反应:了解化学反应的定义、反应类型(如氧化还原反应、酸碱中和反应、置
换反应等)以及反应方程式的写法和平衡。
2. 酸碱理论:了解酸碱的定义、酸碱指示剂、pH值的计算以及酸碱中和反应。
3. 氧化还原反应:了解氧化还原反应的定义、氧化剂和还原剂的概念,以及常见的氧
化还原反应(如金属与酸反应、金属与非金属的反应等)。
4. 原子结构与元素周期表:了解原子结构、元素周期表的组成和特点,以及元素周期
表中元素的分类和周期趋势。
5. 化学键与分子结构:了解化学键的类型(如离子键、共价键、金属键等)及其特点,了解分子的立体结构和分子间力的影响。
6. 化学计量与化学反应速率:了解化学计量的基本概念与计算方法,了解化学反应速
率的影响因素和速率方程式的推导。
7. 物质的组成与性质:了解物质的组成方式(如纯物质、混合物等)及其与性质的关系,了解共振结构、构象异构和环状共轭体系等概念。
8. 化学能量与化学热力学:了解化学能量的转化与热力学定律,包括焓、焓变、内能
等概念的理解和计算。
这些是综合了2024年高一年级化学必修二的知识点考点,希望对你有帮助。
2023-2024学年北京市朝阳区高一下学期期末考试化学试题+答案解析

2023-2024学年北京市朝阳区高一下学期期末考试化学试题一、单选题:本大题共14小题,共42分。
1.下列碳原子相互结合的方式中,碳骨架类型与其他三种不一致...的是A.B.C.D.2.下列关于乙烯的叙述中,不正确...的是A.属于饱和烃 B.官能团为碳碳双键C.难溶于水D.能使酸性溶液褪色3.下列关于物质用途的说法中,不正确...的是A.液氨作制冷剂 B.二氧化硅作半导体C.用油脂生产肥皂D.用二氧化硫漂白纸浆4.下列做法的主要目的与调控化学反应速率无关..的是A.食物存放在冰箱里 B.糕点包装内放置除氧剂C.食盐中添加碘酸钾D.煤块粉碎后燃烧5.一种简单的原电池装置如图所示,下列说法不正确...的是A.该装置能将化学能转化为电能B.电子从Cu 经导线流向ZnC.Cu 片上有气泡产生:D.氧化反应和还原反应分别在两个不同的区域进行6.下列关于化学反应的说法中,不正确...的是A.煤的干馏属于化学变化B.与生成和HCl 的反应属于取代反应C.工业上冶炼钠、镁、铝等活泼金属的反应均属于置换反应D.晶体与晶体的反应属于吸热反应7.下列解释事实的反应方程式不正确...的是A.利用铝热反应冶炼铁:B.碳酸氢铵作食品膨松剂:C.用铜和稀硝酸制备D.用稀硫酸和从含的海带灰滤液中提取碘:8.用溶液和溶液探究催化剂和浓度对化学反应速率的影响。
实验编号溶液的体积的体积溶液/滴ⅰ200ⅱ202ⅲ112下列分析不正确...的是A.通过观察产生气泡的快慢,比较反应速率的大小B.对比ⅰ和ⅱ,可研究催化剂对分解速率的影响C.对比ⅱ和ⅲ,可研究对分解速率的影响D.实验ⅲ加入试剂的顺序是溶液、溶液、水9.利用“空气吹出法”从海水中提溴的工艺流程如下。
下列说法不正确...的是A.“空气吹出法”从海水中提溴利用了溴单质的挥发性B.经过“吹出”、“吸收”过程后,溴元素得到了富集C.“吸收”过程的化学方程式:D.第一次通入的目的是氧化,第二次通入的目的是氧化过量的10.用化学沉淀法去除粗盐水中的、和等杂质离子,过程如下。
高一下化学原电池知识点

高一下化学原电池知识点电池是我们日常生活中经常使用的电源装置之一,它能够将化学能转化为电能,并为我们的电子设备提供稳定可靠的能量。
而要了解电池的原理,就需要掌握一些基础的化学知识。
本文将为大家介绍高一下学期化学中关于原电池的知识点。
1. 电池的基本结构电池的基本结构包括两个电极和电解质。
其中正极是指能够供给电子的电极,通常由金属或其化合物构成;而负极则是指能够接受电子的电极,也可由金属或其化合物组成。
电解质则是指能够提供离子,并在电池中维持电中性的物质。
2. 氧化还原反应与电池电池的工作原理与氧化还原反应密切相关。
在电池中,正极发生氧化反应,负极发生还原反应。
通常情况下,正极的反应是氧化反应,而负极的反应则是还原反应。
这两个半反应之间通过电子流相连,形成了电路。
3. 电池的电动势电动势是电池输出电流的推动力,是衡量电池正负极之间电能转化效果的物理量。
它通常以电势差的形式进行表示,单位是伏特(V)。
电动势取决于电池中发生的化学反应特性,可以通过标准电极电势来计算。
4. 电池的使用寿命与容量电池的使用寿命是指电池能够持续供电的时间,取决于电池内的活性物质耗尽程度。
而容量则是指电池能够存储的电荷量,通常以安时(Ah)为单位。
一般来说,电池的容量越大,使用时间越长。
5. 常见的原电池在日常生活中,我们常见的原电池有铅酸蓄电池、锌-碳干电池和碱性电池。
铅酸蓄电池主要用于汽车起动等高功率设备;锌-碳干电池常用于手电筒、遥控器等低功率设备;碱性电池则是目前应用最广泛的一种常规电池,适用于各种电子设备。
6. 原电池的环保问题尽管原电池在我们的生活中发挥着重要的作用,但同时也产生了一系列的环保问题。
原电池中的重金属如铅、汞等对环境具有一定的污染作用,因此在使用后需要进行妥善处理,不可随意丢弃。
总结:原电池是常用的电源装置,利用氧化还原反应将化学能转化为电能。
了解电池的基本结构、电动势、使用寿命和容量等知识,对于我们合理使用和处理电池具有重要意义。
第八章化学与可持续发展高一化学下学期期末专题复习(人教版2019)(原卷版)
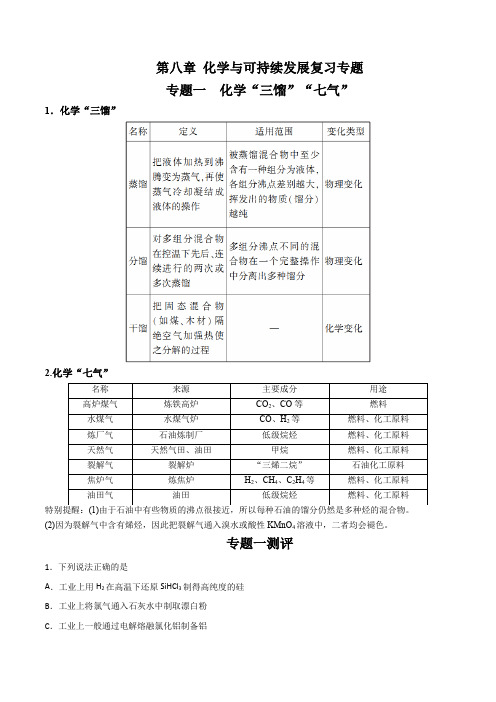
2.化学“七气”D .通过石油分馏可以得到乙烯、丙烯等重要的基本化工原料2.硫铁矿焙烧取硫后烧渣(主要成分为23Fe O 、2SiO 、23Al O ,不考虑其他杂质)可用于制取七水合硫酸亚铁(42FeSO 7H O ⋅),流程如下。
已知:[][]3263623Fe 2Fe(CN)Fe Fe(CN)-++=↓(蓝色沉淀),下列说法不正确的是 A .操作1、2、3的名称均为过滤B .固体1和固体2都可以和NaOH 溶液反应C .向溶液2中加入3~5滴()36K Fe CN ⎡⎤⎣⎦(铁氰化钾)溶液,可观察到有蓝色沉淀生成D .操作3须控制条件防止其氧化和分解3.化学与人类生产、生活密切相关,下列叙述中正确的是 A .在葡萄酒酿制过程中,添加适量二氧化硫可以起到杀菌作用B .京东方生产的可折叠柔性屏中的灵魂材料——纳米银与硝酸不会发生化学反应C .硅是制作光导纤维的主要材料D .海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化4.空气吹出法工艺,是目前“海水(呈弱碱性)提溴”的最主要方法之一,其工艺流程如图所示。
下列说法错误的是A .“吹出塔”步骤中利用了溴的挥发性B .“吸收塔”内发生反应的离子方程式为Br 2+SO 2+2H 2O=SO 24-+2Br -+4H + C .工业溴中含少量Cl 2,可用NaOH 溶液除去D .在该流程中,每提取1mol 溴,理论上至少消耗氯气44.8L(标准状况) 5.在给定条件下,下列选项所示的物质间转化均能实现的是22HgO 2Hg O +2Al+高温2O 2Cu 高温D .步骤Ⅱ吹出的溴也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏9.海水综合利用的工艺流程如图所示(粗盐中的可溶性杂质有MgCl 2、CaCl 2、Na 2SO 4),下列说法不正确...的是A .过程①加入的药品顺序为Na 2CO 3溶液→BaCl 2溶液→NaOH 溶液→过滤后加盐酸B .过程②中所加的试剂是盐酸C .过程④的离子方程式:SO 2+Br 2+2H 2O=SO 24+2Br -+4H + D .在过程③或⑤反应中每氧化-需消耗标况下2 10.下列说法不正确...的是 A .26C H 与512C H 互为同系物B .正丁烷和异丁烷互为同分异构体C .石油的分馏和煤的干馏都是化学变化D .符合分子式612C H 的烃不一定是烯烃11.下列表述正确个数是①煤的干馏、煤的液化、石油的裂化都是化学变化;②检验亚硫酸钠溶液在空气中放置是否变质可以通过先加稀硝酸,再加氯化钡溶液的方法; ③汽车尾气中NO 主要来自燃油中氮元素的不完全燃烧;④足量的铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe 2+; ⑤工业上,通过电解NaCl 溶液的方法可以获取金属Na ; ⑥高炉炼铁中利用焦炭直接将铁矿石还原为铁单质;⑦二氧化硫能使紫色石蕊试液褪色,可用于漂白纸浆、编织物; ⑧S 与非金属单质反应时,S 均作还原剂;⑨普通玻璃是由石灰石、石英砂、纯碱为原料烧制而成的; ⑩制造太阳能电池板的二氧化硅属于新型无机非金属材料。
高一下学期必修二化学知识点总结

高一下学期必修二化学知识点总结【篇一:高一下学期必修二化学知识点总结】第一章物质结构元素周期律1原子结构1. 注意:质量数(a)=质子数(z)+中子数(n)原子序数=核电荷数=质子数=原子的核外电子数熟背前20号元素,熟悉1~20号元素原子核外电子的排布:h he li be b c n o f ne na mg al si p s cl ar k ca2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(k层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
3.元素、核素、同位素元素:具有相同核电荷数的同一类原子的总称。
核素:具有一定数目的质子和一定数目的中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。
(对于原子来说)2 元素周期表1.编排原则:①按原子序数递增的顺序从左到右排列②将电子层数相同的各元素从左到右排成一横行。
(周期序数=原子的电子层数)③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行。
主族序数=原子最外层电子数2.结构特点:3 元素周期律1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。
元素性质的周期性变化实质是元素原子核外电子排布的周期性变化的必然结果。
2.同周期元素性质递变规律第三周期元素11na12mg13al15p16s17cl18ar(1)电子排布电子层数相同,最外层电子数依次增加(2)原子半径原子半径依次减小—(3)主要化合价+1+2+3+4-4+5-3+6-2+7-1—(4)金属性、非金属性金属性减弱,非金属性增加—(5)单质与水或酸置换难易冷水剧烈热水与酸快与酸反应慢———(6)氢化物的化学式——ph3h2shcl—(7)与h2化合的难易——由难到易—(8)氢化物的稳定性——稳定性增强—(9)最高价氧化物的化学式na2omgoal2o3sio2p2o5so3cl2o7—最高价氧化物对应水化物(10)化学式naohmg(oh)2al(oh)3h2sio3h3po4h2so4hclo4—(11)酸碱性强碱中强碱两性氢氧化物弱酸酸强酸很强的酸—(12)变化规律碱性减弱,酸性增强—第Ⅰa族碱金属元素:li na k rb cs fr(fr是金属性最强的元素,位于周期表左下方)第Ⅶa族卤族元素:f cl br i at(f是非金属性最强的元素,位于周期表右上方)判断元素金属性和非金属性强弱的方法:(1)金属性强(弱)——①单质与水或酸反应生成氢气容易(难);②氢氧化物碱性强(弱);③相互置换反应(强制弱)fe+cuso4=feso4+cu。
高一下学期化学期末复习知识点

高一下学期化学期末复习知识点1.高一下学期化学期末复习知识点篇一常见的酸和碱1、酸:由H+和酸根离子构成的化合物。
如:H2SO4、HCl、HNO3、H2CO3等。
2、碱:由OH—和金属离子构成的化合物。
如:KOH、NaOH、Ca(OH)2、Al (OH)3等。
3、酸碱指示剂:紫色石蕊和无色酚酞能使酸碱溶液显不同的颜色,叫做酸碱指示剂。
可用于检验酸碱溶液。
①石蕊遇酸变红色,遇碱变蓝色;②酚酞遇酸不变色,遇碱变红色。
2.高一下学期化学期末复习知识点篇二原电池电极反应的书写方法:(i)原电池反应所依托的化学反应原理是氧化还原反应,负极反应是氧化反应,正极反应是还原反应。
因此书写电极反应的方法归纳如下:①写出总反应方程式。
②把总反应根据电子得失情况,分成氧化反应、还原反应。
③氧化反应在负极发生,还原反应在正极发生,反应物和生成物对号入座,注意酸碱介质和水等参与反应。
(ii)原电池的总反应式一般把正极和负极反应式相加而得。
3.高一下学期化学期末复习知识点篇三1.区分元素、同位素、原子、分子、离子、原子团、取代基的概念。
正确书写常见元素的名称、符号、离子符号,包括IA、IVA、VA、VIA、VIIA族、稀有气体元素、1~20号元素及Zn、Fe、Cu、Hg、Ag、Pt、Au等。
2.物理变化中分子不变,化学变化中原子不变,分子要改变。
常见的物理变化:蒸馏、分馏、焰色反应、胶体的性质(丁达尔现象、电泳、胶体的凝聚、渗析、布朗运动)、吸附、蛋白质的盐析、蒸发、分离、萃取分液、溶解除杂(酒精溶解碘)等。
常见的化学变化:化合、分解、电解质溶液导电、蛋白质变性、干馏、电解、金属的腐蚀、风化、硫化、钝化、裂化、裂解、显色反应、同素异形体相互转化、碱去油污、明矾净水、结晶水合物失水、浓硫酸脱水等。
(注:浓硫酸使胆矾失水是化学变化,干燥气体为物理变化)3.理解原子量(相对原子量)、分子量(相对分子量)、摩尔质量、质量数的涵义及关系。
高一下学期化学主要知识点归纳

高一下学期化学主要知识点归纳
下学期化学的主要知识点主要包括有机化学、化学反应动力学、化学
平衡和电化学等内容。
下面对这些知识点进行归纳总结。
1.有机化学:
有机化学是化学的一个重要分支,主要研究有机化合物的合成、结构、性质和反应机理。
主要涉及的知识点包括:
(1)有机化合物的命名和分类;
(2)有机化合物的结构与性质;
(3)有机反应的机理和应用。
2.化学反应动力学:
化学反应动力学是研究反应速率和反应机理的分支学科,主要关注以
下内容:
(1)反应速率与反应机理的关系;
(2)反应速率的影响因素;
(3)反应速率方程和速率常数的确定;
(4)反应活化能和反应速率的关系。
3.化学平衡:
化学平衡研究在封闭系统中化学反应达到动态平衡的条件和性质,包
括以下知识点:
(1)化学反应的平衡状态;
(2)化学平衡常数和平衡常数表达式;
(3)平衡常数与反应条件的关系;
(4)利用平衡常数计算平衡浓度。
4.电化学:
电化学是研究电和化学变化之间相互关系的学科,主要包括以下内容:(1)电化学反应动力学;
(2)著名的电化学反应,如氧化还原反应、电解反应、电池等;
(3)电解质溶液中的电解质行为和电导性;
(4)电解质浓度与电势的关系。
此外,还有一些辅助性知识点需要掌握:
(1)化学键的类型和强度;
(2)化学方程式的平衡及其应用;
(3)化学式、化学方程式的写法和读法;
(4)溶液的浓度和计算(摩尔浓度、质量浓度等);
(5)酸碱中的pH值、pOH值和离子产生的计算。
高一下学期化学期末复习学案:离子反应

离子反应一、离子反应1.电解质与非电解质在_______________ 中或____________ 状态下能够 ____________ 的化合物叫电解质,女口:____________ 、________ 、及_______________________。
而在上述条件下________________ 化合物称非电解质,如CH4、CO2、NH3等。
离子化合物溶解.或熔化都可电离出自由离子,共价化合物只有在水分子的作用..下才电离。
2.常见离子反应可分为两大类:⑴ 离子互换形式的复分解反应。
如:碳酸钙溶于盐酸:CaCO3 + 2H+ = Ca2+ + CO2T + HO⑵ 有离子参与的氧化还原反应。
如:铁与硫酸铁溶液反应:Fe + 2Fe3+ = 3Fe2+3.离子反应发生的条件⑴在溶液中进行的离子互换形式的复分解反应发生的条件:实质上就是 _______ 反应物的某些离子浓度的条件。
总起来讲,具备下列条件之一就可以使反应物的某些离子浓度减小。
①生成 ____________的物质(如BaSO4、CaCO3、AgCI、Mg (OH )2、Al (OH ) 3 等);②生成 ____________的物质(如弱酸、弱碱、水等);③生成 __________________ 物质(如CO2、SO2、NH3等)。
⑵ 对于氧化还原反应类型的离子反应发生的条件:生成相对弱的氧化产物和还原产物。
2Fe3+ + Cu = 2Fe2+ + Cu2+CI2 + 2Fe2+ = 2Fe3+ + 2CI-二、离子方程式书写的一般步骤1 离子方程式:用实际参加反应的__________________________________ 的符号表示__________________ 的式子。
不仅表示化学反应,且能表示___________________________ 的离子反应。
2.离子方程式的书写步骤⑴写出反应的_________________________ 。
高一化学知识点大全

高一化学知识点大全1、Na2O2是淡黄色固体,与水反应放出使带火星的木条复燃的气体,离子方程式是2Na2O2+2H2O=4Na++4OH-+2H2↑。
反应后溶液中滴入酚酞的现象是先变红后褪色。
2、Na2CO3、NaHCO3的鉴别除了观察是否细小,加水是否结块的物理方法外,还可以①加热固体质量减轻或放出气体能使澄清的石灰水变浑浊的是NaHCO3。
②在其溶液中滴入CaCl2或BaCl2溶液由白色沉淀的是Na2CO3。
③加等浓度的HCl放出气体快的是NaHCO3。
3、焰色反应是物理性质,钠元素为黄色,钾元素为紫色(透过蓝色的钴玻璃观察的原因是滤去黄色焰色);钠单质或其化合物焰色均为黄色。
4、焰色反应的操作为,先用盐酸洗净铂丝或无锈的铁丝,然后在火焰外焰上灼烧至与原来的火焰焰色相同为止,再蘸取溶液灼烧并观察焰色。
5、由可溶性可溶性铝盐制Al(OH)3沉淀选用试剂是氨水,离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+。
6、铝片放入NaOH溶液开始无现象是因为表面氧化铝先与氢氧化钠溶液反应、然后有气体逸出且逐渐加快是因为铝与碱溶液反应使溶液温度升高,加快了反应速度,最后生成气体的速度又慢下来(仍有铝片)原因是OH-浓度逐渐减小,速度变慢。
2molAl完全反应放出标况下气体是67.2L。
7、明矾和FeCl3都可净水,原理是:溶于水后生成的胶体微粒能吸附水中悬浮的杂质一起沉淀。
8、Al3+溶液中渐渐加入NaOH溶液或AlO2-溶液中渐渐加入HCl溶液的现象都是:白色沉淀渐多又减少至澄清;NaOH溶液渐渐加入Al3+溶液或H+溶液渐渐加入NaAlO2溶液的现象都是:开始无沉淀,后来沉淀迅速增加至定值。
9、铁的三种氧化物化学式分别是FeO、Fe2O3、Fe3O4。
其中磁性氧化铁和盐酸反应的离子方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O。
10、FeSO4加入NaOH溶液的现象是有白色沉淀生成,迅速变成灰绿色,最后变成红褐色。
高一化工流程题必背知识点

高一化工流程题必背知识点化工流程题是高一化学中的重要内容之一,解题需要具备一定的理论知识。
下面将列出高一化工流程题必背的知识点,以供学习和复习使用。
一、化学物质的性质与用途1. 酸和碱的性质及其中和反应:酸与碱的定义、常见酸碱的性质和用途、酸碱中和反应的化学方程式。
2. 氧化还原反应:氧化还原反应的概念、氧化还原反应的判定方法、常见氧化剂和还原剂的性质和用途。
二、化工原料与生产过程1. 常见化工原料:如硫酸、氯气、氢气等原料的性质、产地和主要用途。
2. 常见化工生产过程:如硫酸的制备、硝酸的制备、氨的制备等。
要了解生产过程的原理、反应方程式和工艺条件。
三、工业流程中的关键步骤1. 精制过程:如溶剂的蒸馏、气体的吸收与析出等。
2. 分离过程:如固液分离、液液分离、气液分离等常见分离过程。
3. 反应过程:如常温、高温、加压等特殊条件下的反应过程。
4. 吸收与析出:了解吸收过程中物质的吸附和释放,析出过程中溶质的析出与分离。
四、常见化工装置与设备1. 反应设备:如反应釜、反应塔等。
2. 分离设备:如蒸馏塔、萃取塔等。
3. 储存设备:如容器、槽车等。
五、安全与环保1. 化学品的安全储存和运输:了解化学品的危险性和安全措施,学会正确存储和运输化学品。
2. 环境保护:了解化工生产中的环境问题,掌握常见的环保技术和方法。
以上是高一化工流程题必背的知识点,掌握这些知识将有助于解答化工流程题目。
在学习过程中,理论知识的掌握是基础,结合实际工业流程的例子进行练习,可以更好地理解和应用知识。
希望通过学习和复习,能够提高解题水平,取得好成绩!。
高一下学期硫的知识点

高一下学期硫的知识点高一下学期化学课程中,硫元素是一个重要的学习内容。
硫是自然界中的一种常见元素,它在我生活中起着重要作用。
在下面的文章中,我们将探讨硫的性质、应用以及环境问题。
硫是一种非金属元素,化学符号为S,原子序数为16,是含氧族元素的第一位。
硫的原子结构包括6个价电子,外层电子结构为2s22p4。
硫的电负性较大,属于活泼的元素。
在自然界中,硫以多种形式存在,常见的有硫酸盐、硫酸和硫化物等。
硫的物理性质与化学性质关系密切。
在常温下,硫呈黄色固体,具有强烈的臭味。
它是一种非金属半导体,属于明亮金黄色的晶体。
当硫被加热时,会发生物理变化,由固体转变为液体,并伴随着颜色的变浅。
这叫做硫的熔化点。
硫的熔化点是115.2摄氏度,熔化后的硫呈深黄色的液体状态。
此外,硫还具有很强的化学活性。
硫和氧气可以发生反应生成二氧化硫,化学方程式为S + O2 -> SO2。
硫还可以与金属元素形成硫化物,例如铁和硫反应可以生成硫化铁,方程式为Fe + S -> FeS。
硫还是一种重要的催化剂,可以促使某些化学反应发生。
硫在生活和工业中有着广泛的应用。
最常见的应用是制造硫酸。
硫酸是一种重要的化工原料,广泛用于制造肥料、洗涤剂、染料和燃料电池等。
此外,硫还被用于制造橡胶、纸张、药品和杀虫剂等产品。
在能源行业中,硫常被用作燃料的添加剂,可以减少燃烧过程中产生的有害物质。
尽管硫在生活和工业中有重要的应用,但是它也存在一些环境问题。
硫氧化物在大气中会与水蒸气反应形成硫酸和硫酸盐,导致酸雨的形成。
酸雨对环境和生态系统造成严重的破坏,对土地和水资源的污染是需要关注和解决的问题。
为了减少硫对环境的影响,我们可以采取一些措施。
例如,在工业生产中使用低硫燃料,减少硫氧化物的排放。
同时,科学合理地利用化工废料,例如含硫废水的处理,可以减少硫的排放和环境污染。
总结起来,硫是我们高一下学期化学课程中需要学习的一个重要元素。
我们掌握了硫的性质、应用以及环境问题,也意识到了硫带来的环境问题并提出了相应的解决办法。
第八章知识串讲-高一化学下学期期末复习大串讲(人教版必修第二册)(解析版)

第八章化学与可持续发展(知识串讲)【网络构建】【知识梳理】一.自然资源的开发利用(一)金属的冶炼大多数金属的化学性质活泼,在自然界中主要以化合态形式存在(金、铂等少数金属例外),使用的金属大多数是人工制得的。
金属冶炼是工业上将金属从含有金属元素的矿石中还原出来的生产过程。
金属的性质越稳定,越容易将其从化合物中还原出来。
金属的活动性不同,可以采用不同的冶炼方法。
金属冶炼的方法主要有:(1)热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来,例如:2HgO2Hg+O2↑2Ag2O4Ag+O2↑(2)热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来,例如:Fe2O3+3CO2Fe+3CO2 WO3+3H2W+3H2O (3)电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属,例如:2NaCl(熔融)2Na+Cl2↑4NaOH(熔融)4Na+O2↑+2H2O附:金属活动性与冶炼方法的关系金属的活动顺序:K Ca Na MgAlZn Fe Sn Pb(H)CuHg Ag金属原子失电子能力强→弱金属离子得电子能力弱→强2、铝热反应(1)原理:Al是还原剂,另一种氧化物是氧化剂。
(2)铝热反应的实质是铝将氧化物中的化合态金属还原为金属单质。
(3)反应特点是在高温下进行,反应迅速并放出大量的热,新生成的金属单质呈液态且易与Al2O3分离。
(4)铝热剂是指铝粉和某些金属氧化物组成的混合物。
(5)应用:冶炼难熔金属,如V、Cr、Mn等;焊接钢轨等。
3、回收金属的意义(1)节约矿物资源;(2)节约能源;(3)减少环境污染。
(二)海水资源的开发利用1、从海水中提取淡水——海水淡化海水淡化的方法主要有蒸馏法、电渗析法、离子交换法、冷冻法等。
2、从海水中提取溴的主要工艺流程①用蒸馏法将海水浓缩,用硫酸将浓缩的海水酸化。
高一年级化学科目知识点下学期

高一年级化学科目知识点下学期(实用版)编制人:__审核人:__审批人:__编制单位:__编制时间:__年__月__日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如教案大全、书信范文、述职报告、合同范本、工作总结、演讲稿、心得体会、作文大全、工作计划、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of practical materials for everyone, such as lesson plans, letter templates, job reports, contract templates, work summaries, speeches, reflections, essay summaries, work plans, and other materials. If you want to learn about different data formats and writing methods, please stay tuned!高一年级化学科目知识点下学期本店铺为大家整理的,在高一下学期,我们会学习新的化学知识,必修二的化学内容也是我们每个学生都必须要掌握好的。
高一化学知识点复习笔记下学期

高一化学知识点复习笔记下学期(实用版)编制人:______审核人:______审批人:______编制单位:______编制时间:__年__月__日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如教案大全、书信范文、述职报告、合同范本、工作总结、演讲稿、心得体会、作文大全、工作计划、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of practical materials for everyone, such as lesson plans, letter templates, job reports, contract templates, work summaries, speeches, reflections, essay summaries, work plans, and other materials. If you want to learn about different data formats and writing methods, please stay tuned!高一化学知识点复习笔记下学期本店铺为各位同学整理了《高一化学知识点复习笔记下学期》,希望对你的学习有所帮助!1.高一化学知识点复习笔记下学期篇一物质的量的单位――摩尔1.物质的量(n)是表示含有一定数目粒子的集体的物理量.2.摩尔(mol):把含有6.02X1023个粒子的任何粒子集体计量为1摩尔.3.阿伏加德罗常数:把6.02X1023mol-1叫作阿伏加德罗常数.4.物质的量=物质所含微粒数目/阿伏加德罗常数n=N/NA5.摩尔质量(1)定义:单位物质的量的物质所具有的质量叫摩尔质量.(2)单位:g/mol或g..mol-1(3)数值:等于该粒子的相对原子质量或相对分子质量.6.物质的量=物质的质量/摩尔质量(n=m/M)2.高一化学知识点复习笔记下学期篇二氨气及铵盐氨气的性质:无色气体,刺激性气味、密度小于空气、极易溶于水(且快)1:700体积比。
专题03 硫酸和硝酸专讲(专题过关)高一化学下学期期中期末考点大串讲(必修第二册)(原卷版)

专题03硫酸和硝酸专讲【专题过关】1.下列说法正确的是()A .蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生B .钠、铝、铁、铜在空气中都会氧化变质生成相应的金属氧化物C .可直接向铜与浓硫酸反应后溶液中加入水来证明该反应有硫酸铜生成D .实验室中蔗糖遇浓硫酸炭化,过程中浓硫酸表现出脱水性2.某同学设想用如图装置来验证浓硫酸的某些性质,其中不能达到目的的是()AB C D 实验目的吸水性脱水性溶解放热强氧化性实验装置3.下列有关硝酸化学性质的叙述中,正确的是()A .浓、稀硝酸都能使蓝色石蕊试纸最终变为红色B .硝酸能与FeO 反应,只表现氧化性C .硝酸可与Na 2S 反应制得H 2S 气体D .浓硝酸因分解放出的NO 2又溶解于硝酸而呈黄色4.下列过程中,最终的白色沉淀物不一定是BaSO 4的是()A .Fe(NO 3)2溶液―――――――――――――――――→+过量盐酸,+过量SO 2,+BaCl 2溶液白色沉淀B .Ba(NO 3)2溶液―――――――――――――――→+过量盐酸,+少量Na 2SO 3溶液白色沉淀C .无色溶液―――――――――――――→+稀HNO 3,+BaCl 2溶液白色沉淀D .无色溶液――――→+过量盐酸无色溶液――――――→+BaCl 2溶液白色沉淀5.下列有关实验操作、现象和解释或结论都正确的是()序号实验操作现象解释或结论①过量的Fe 粉中加入稀HNO 3,充分反应后,滴入KSCN 溶液溶液呈红色稀HNO 3将Fe 氧化为Fe 3+②浓HNO 3久置或光照变黄色HNO 3不稳定易分解③Al 箔插入稀HNO 3中无现象Al 箔表面被HNO 3氧化,形成致密的氧化膜④用玻璃棒蘸取浓HNO 3点到蓝色石蕊试纸上试纸先变红色后褪色浓HNO 3具有酸性和强氧化性A.①②B .③④C .②③④D .②④6.推理是一种重要的能力。
打开分液漏斗活塞,进行如图所示的探究实验,对实验现象的预测及分析错误的是()A .试管内CCl 4层溶液褪色,说明Br 2具有氧化性B .试管中的红色花瓣褪色,说明SO 2具有漂白性C .试管中产生大量气泡,说明Na 2SO 3被氧化产生SO 3D .一段时间后试管内有白色沉淀,说明有SO 2-4生成7.将相同质量的铜分别与足量的浓硝酸、稀硝酸反应,下列叙述正确的是()A .硝酸浓度越大消耗的硝酸越少,产生的有毒气体也越少B .反应中转移的电子总数:稀硝酸少于浓硝酸C .试管内壁上的铜用浓硝酸除去比用稀硝酸好,因为反应速率快D .两者用排水法收集的气体的体积相同8.炭跟浓硫酸共热产生的气体X 和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是A .洗气瓶中产生的沉淀有碳酸钡B .Z 导管口无红棕色气体出现C .洗气瓶中产生的沉淀是亚硫酸钡D .Z 导管出来的气体中有二氧化碳9.用以下三种途径来制取相同质量的硝酸铜:①铜跟浓硝酸反应,②铜跟稀硝酸反应,③铜跟氧气反应生成氧化铜,氧化铜再跟硝酸反应。
专题04 化工生产-高一化学下学期期中期末考点大串讲(沪科版2020)(解析版)

专题04化工生产1.工业制硫酸反应原理(1)主要原料:硫磺或硫铁矿,其中硫磺制酸具有生产流程短,“三废”治理量较少等优势,因而今后以硫磺制取酸为主要发展趋势。
(2)根据工业制硫酸的反应原理,生产过程通常可以分为造气、转化、吸收三个主要阶段2.接触法制硫酸(1)接触法制硫酸:主要阶段造气-硫铁矿煅烧制造SO2转化-SO2接触氧化吸收-SO3的吸收主要设备沸腾炉转化器吸收塔化学反应4FeS2+11O2高温=Fe2O3+8SO22SO2(g)+O2(g)催化剂⇌△2SO3(g)SO3+H2O=H2SO4A.转化器出来的气体主要包括:二氧化硫、氧气、氮气,原料气要通过除尘、干燥等净化处理,目的是___防止催化剂中毒________________________________________。
B.使用98.3%的硫酸而不是直接用水来吸收三氧化硫的原因:_使用水吸收三氧化硫会导致大量酸雾妨碍吸收_________________。
化学反应方程式压强温度催化剂SO2的氧化2SO2+O2催化剂⇌△2SO30.1MPa(常压)400℃~500℃V2O5等3.硫酸工业中热能的合理利用及三废处理硫酸生产过程中的三个反应都是放热反应,为了充分利用这些热量,在生产过程中,沸腾炉外设置废热锅炉回收高温废热,把热交换器和转化器合为一体,将二氧化硫转化为三氧化硫时放出的热量及时导出用来预热进入转化器的原料气。
(1)废气:硫酸工业的尾气中含有的有毒气体是SO2,用氨酸法处理尾气的化学方程式分别为:________________________________、________________________________、________________________________。
①NH3+H2O=NH3•H2O②SO2+2NH3•H2O=(NH4)2SO3+H2O③(NH4)2SO3+SO2+H2O=2NH4HSO3(2)废水:没有被污染的冷却水可以被循环利用;若排出的是酸性废水,一般使用石灰乳等中和处理,反应的离子方程式为2H++Ca(OH)2==Ca2++2H2O。
高一下学期化学章节知识点

高一下学期化学章节知识点化学是学习物质的性质、组成、结构以及变化的一门科学。
在高一下学期的化学课程中,有许多重要的知识点,下面将对一些主要的知识点进行介绍。
一、化学反应化学反应是指物质变化的过程,它描述了物质之间的转化和原子之间的重组。
其中,化学方程式是描述化学反应的符号表示法。
化学方程式由反应物、产物和状态符号组成。
反应物是参与反应的物质,产物是反应后形成的物质。
状态符号表示物质的物态,如(s)表示固体,(l)表示液体,(g)表示气体,(aq)表示溶液。
化学方程式还包括反应的平衡问题。
平衡是指在一定条件下,正向反应和逆向反应速率相等,系统处于稳定状态。
平衡反应可由平衡常数(K)进行描述,K的大小决定了反应的方向。
二、酸碱中和反应酸碱中和反应是指酸和碱反应生成盐和水的过程。
其中,酸是指能产生H+离子的物质,碱是指能产生OH-离子的物质。
中和反应可表示为酸+碱→盐+水。
酸碱中和反应还可用酸度和碱度来描述。
酸度指的是溶液中酸性物质的含量,碱度指的是溶液中碱性物质的含量。
pH值是一种表示酸碱性的指标,pH= -log[H+]。
除了酸碱中和反应,还存在其他一些特殊的酸碱反应。
例如,酸氧化性反应是指酸和氧化剂反应生成产物的过程;自然酸碱指的是酸碱性质由于物质的自身特性而产生。
三、氧化还原反应氧化还原反应描述了物质中电子转移的过程。
其中,氧化是指物质失去电子,还原是指物质获得电子。
氧化剂是可以接受电子的物质,还原剂是可以提供电子的物质。
氧化还原反应可以用电子转移的方式表示。
例如,A→A+ + e-表示A物质被氧化得到正离子,B+ e-→B表示B物质被还原得到负离子。
将这两个反应方程相加得到:A+B→A++B-氧化还原反应也可以用氧化数来描述。
氧化数指的是原子在化合物中带电的正负值。
在氧化还原反应中,正离子的氧化数会增大,负离子的氧化数会减小。
四、化学平衡化学平衡是指反应物和产物在一定条件下达到稳定状态的过程。
高一化学下学期生物知识点

高一化学下学期生物知识点生物是高一化学下学期中的一大知识点,学习生物可以帮助我们更好地了解生命的起源、结构和功能。
下面是一些重要的生物知识点,希望对大家的学习有所帮助。
一、细胞与组织1. 细胞结构:细胞膜、细胞质、细胞核、线粒体等。
2. 细胞生理:细胞的呼吸作用、分裂作用和合成作用等。
3. 细胞分化:原始细胞经过分化形成各种特定功能细胞。
二、生物的分类1. 生物分类的原则:根据生物的形态、结构、生活习性等进行分类。
2. 生物分类的目的:便于研究和了解生物的规律性,方便教学和科研。
三、遗传与变异1. 遗传的基本规律:孟德尔的遗传定律、基因的概念和遗传物质的分子组成。
2. 数量性状遗传规律:卡方检验及其应用。
3. 变异与进化:突变、突变的意义和影响。
四、生态学1. 生态系统的组成及相互关系:生物、非生物环境和生物之间的相互作用。
2. 环境保护与资源利用:保护生态平衡、节约资源、可持续发展等。
五、植物学1. 植物的形态结构:根、茎、叶及其特点和功能。
2. 植物的生理功能:光合作用、呼吸作用、植物激素的作用等。
六、动物学1. 动物的形态结构:动物的对称性、体腔和体节等特点。
2. 动物的生理功能:摄食、呼吸、循环、排泄和运动等。
七、生活中的化学与生物生活中的化学与生物相互关联,例如:1. 蛋白质、糖类和脂肪在人体中的作用。
2. 酶在食物消化和代谢过程中的作用。
3. 细胞膜的构成及传递物质的方式。
八、生物技术与人类生活1. 基因工程:重组DNA技术和转基因技术的应用。
2. 细胞工程:组织细胞培养和克隆技术的应用。
以上是一些高一化学下学期涉及的生物知识点,希望同学们能够通过学习和掌握这些知识,加深对生物的理解并应用到实际生活中。
生物是非常有趣和实用的学科,希望大家能够保持对生物学的兴趣,不断探索和发现生命的奥秘。
加油!。
高一化学下学期期末考试分类汇编常见物质间的转化关系新人教版必修第二册202207261125

专题01常见物质间的转化关系一、硫及其化合物1、(2021·黑龙江省哈尔滨市·期末试卷)在给定条件下,下列选项所示的物质间转化均能实现的是()A. B.C. D.【答案】C【解析】A.因为氯气具有强氧化性,则铁与氯气反应生成氯化铁,而不是氯化亚铁,故A错误;B.硫与氧气反应生成二氧化硫,而不是三氧化硫,故B错误;C.CaC O3高温分解生成CaO,CaO与二氧化硅在高温条件下反应生成硅酸钙,故C正确;D.氨气催化氧化生成NO,NO和水不反应,不能生成硝酸,故D错误。
故选C。
2、(2021·甘肃张掖期末)硫在自然界的循环过程如下图所示。
下列说法中,不正确的是¿ ¿A. 火山喷发、森林火灾会产生S O2B. 氢、氧两种元素没有参与硫的循环C. 工厂产生的烟气应经脱硫处理后再排放D. 硫在自然界的循环过程中,涉及了氧化还原反应【答案】B【解析】略3、(2021·广东省东莞市·期末考试)核心元素的化合价及类别是研究物质性质的两个重要视角。
硫及其化合物的分类与相应硫元素的化合价关系如图所示。
下列说法错误的是()A. 适量的c可作为葡萄酒的添加剂B. 常温下,a与f的浓溶液反应可生成b和cC. 将c通入紫色石蕊试液中,溶液先变红后褪色D. 在自然界中,部分的c会转化成d,最后转化为f或h【答案】C【解析】由图可知,a为−2价S的氢化物,a为H2S;b为单质,b为S;c为+4价S的氧化物,c为S O2;d为+6价S的氧化物,d为S O3;e、f分别为+4价、+6价含氧酸,则e、f分别为H2SO3、H2SO4;g、h分别为+4价、+6价S的正盐,如亚硫酸钠、硫酸钠等,以此来解答。
A.c为S O2,具有还原性,可作抗氧化剂,适量的S O2可作为葡萄酒的添加剂,故A正确;B.常温下H2S能与浓硫酸发生氧化还原反应生成S和S O2,故B正确;C.c为S O2,为酸性氧化物,将c通入紫色石蕊试液中,溶液变红,但不褪色,故C错误;D.自然界中,部分的S O2在飘尘的作用下会催化氧化转化成S O3,最后转化为硫酸或硫酸盐,故D正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高一下学期化学期末常考知识点知识点在不断更新的同时也需要及时的归纳总结,才能更好的掌握,接下来查字典化学网给大家整理高一下学期化学期末常考知识点,供大家参考阅读。
高一化学下册知识点(三)
1、元素周期表的编排原则:
①按照原子序数递增的顺序从左到右排列;
②将电子层数相同的元素排成一个横行——周期;
③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行——族
2、如何精确表示元素在周期表中的位置:
周期序数=电子层数;主族序数=最外层电子数
3、元素金属性和非金属性判断依据:
①元素金属性强弱的判断依据:
a.单质与水或酸反应置换氢的难易或与氢化合的难易及气态氢化物的稳定性
b.最高价氧化物的水化物的碱性或酸性强弱
c.单质的还原性或氧化性的强弱(注意:单质与相应离子的性质的变化规律相反)
(2)元素性质随周期和族的变化规律
a.同一周期,从左到右,元素的金属性逐渐变弱
b.同一周期,从左到右,元素的非金属性逐渐增强
c.同一主族,从上到下,元素的金属性逐渐增强
d.同一主族,从上到下,元素的非金属性逐渐减弱
4、核素:具有一定数目的质子和一定数目的中子的一种原子。
①质量数==质子数+中子数:A==Z+N
②同位素:质子数相同而中子数不同的同一元素的不同原子,互称同位素。
(同一元素的各种同位素物理性质不同,化学性质相同)
现在是不是感觉查字典化学网为大家推荐的高一下学期化学期末常考知识点很关键呢?欢迎大家阅读与选择。
