无机化学试卷A(8)
《无机化学》期末考试试卷

《无机化学》期末考试试卷一、单选(共40小题,每题2分,共80分。
)(题下选项可能多个正确,只能选择其中最佳的一项。
)1.下列溶液中与血浆等渗的是:() [单选题] *A.90g/L的NaCl溶液B.9g/L的NaCl溶液(正确答案)C.100g/L的葡萄糖溶液D.50g/L的NaHCO3溶液E.20g/L的乳酸钠溶液2.下列溶液能使红细胞发生皱缩的是:() [单选题] *A.1.5g/L的NaHCO3溶液B.1.0 g/L的NaCl溶液C.9g/L的NaCl溶液D.100g/L的葡萄糖溶液(正确答案)E.20g/L的乳酸钠溶液3.欲使半透膜两侧的溶液不发生渗透现象的条件是:() [单选题] *A.两溶液酸度相等B.两溶液体积相等C.两溶液的物质的量浓度相等D.两溶液的渗透浓度相等(正确答案)E.两溶液温度一致4.配制300ml、0.10mol/L的NaOH溶液,需要称取固体NaOH(M=40)的质量为:() [单选题] *A.1.2g(正确答案)B.1.2mgC.4.0gD.4.0mgE.40g5.在下列单位中,哪一个是物质的量浓度的单位:() [单选题] *A.g·LB.g·molC.g·mLD.mol·L(正确答案)E.16.对于物质的体积分数,下列表示正确的是:() [单选题] *A.φ=VB/V(正确答案)B.ρ=mB/VC.wB=mB/mD.CB= nB/VE.E.xB=mB/M7.在生活中,常用75℅酒精消毒,这个浓度是指:() [单选题] *A.物质的量浓度B.质量浓度C.体积分数(正确答案)D.质量分数E.摩尔质量浓度8.溶液、胶体和悬浊液这三种分散系的根本区别是() [单选题] *A.是否是大分子或离子的聚集体B.能否透过滤纸或半透膜C.是否均匀、稳定、透明D.分散质微粒直径的大小(正确答案)E.没有区别9.胶粒稳定的主要原因是:() [单选题] *A.布朗运动B.胶粒带电(正确答案)C.溶剂化膜D.丁达尔现象E.渗透现象10.某可逆反应的正反应为吸热反应,欲使平衡向逆反应方向移动,可采取的措施是:() [单选题] *A.升高温度B.降低温度(正确答案)C.加催化剂D.加压E.减压11.有关催化剂的叙述不正确的是() [单选题] *A.能改变化学反应的历程B.能降低反应的活化能C.能使不反应的物质相互发生反应(正确答案)D.反应前后质量没有发生变化E.催化作用是化学作用12.增加气体反应物的压强能加快化学反应速率的原因是() [单选题] *A.增加了反应体系内分子总数B.增加了反应体系内活化分子数C.降低了化学反应的活化能D.增加了单位体积的活化分子数(正确答案)E.减少了单位体积的活化分子数13.一些药物需要保存在冰箱中,以防其变质,其主要作用是() [单选题] *A.避免与空气接触B.保持药物干燥C.避免药物受光照D.降低温度,减缓药物变质的反应速率(正确答案)E.以上都不对14.若用NH3和HCl来配置缓冲溶液,缓冲溶液的抗碱成分是:() [单选题] *B.HClC.NH4Cl(正确答案)D.NH3E.OH-15.人体血液中最重要的缓冲对的抗酸成分是:() [单选题] *A.H3PO4B.H2PO4-C.HCO3-(正确答案)D.H2CO3E.H2O16.正常人血浆的pH范围是:() [单选题] *A.7~8B.7~7.5C.7.5~8D.7.45~7.55E.7.35~7.45(正确答案)17.下列化合物中,属于两性物质的是:() [单选题] *A.HClB.NaOHC.H2O(正确答案)D.NH4Cl18.根据酸碱质子理论,下列叙述不正确的是:() [单选题] *A.H2CO3和CO32-不是共轭酸碱对B.酸越强,其共轭碱也越强(正确答案)C.酸失去质子转变成共轭碱D.酸碱反应的实质是质子的转移E.碱得到质子生成其共轭酸19.当pH=4的时候,则 [H+]的浓度为:() [单选题] *A.5B.104C.10-4(正确答案)D.4E.1020.下列酸中,属于一元弱酸的是:() [单选题] *A.HAc(正确答案)B.H2CO3C.H3PO4D.H3BO3E.H2SO321.同离子效应将使弱电解质的电离平衡:() [单选题] *A.左移(正确答案)C.不移动D.无法确定E.以上都对22.室温下,1.0mol/L氨水中,水的离子积常数为() [单选题] *A.1.0×10-10B.1.0×10-4C.1.0×10-14(正确答案)D.1.0×10-7E.2.0×10-723.下列溶液中酸性最强的是() [单选题] *A.pH=5B.pH=2C.[H+]=0.1mol/L(正确答案)D.[OH-]=10-2mol/LE.[OH-]=10-7mol/L24.在含有CrO42-和Cl-的混合溶液中加入AgNO3溶液,先有白色沉淀生产,后有砖红色沉淀生成,这种现象称为:() [单选题] *A.分步沉淀(正确答案)B.沉淀的生成C.沉淀是转化D.沉淀的溶解E.以上都不对25.在AgCl饱和溶液中加入NaCl,使其溶解度减小的现象称为() [单选题] *A.盐效应B.同离子效应(正确答案)C.缓冲效应D.配位效应E.沉淀效应26.沉淀生成的必要条件是() [单选题] *A.Ip>Ksp(正确答案)B.加入强电解质C.加入与难溶强电解质具有相同离子的盐D.Ip<KspE.加入氧化剂或还原剂27.下列化合物中,S的氧化数为+4的是:() [单选题] *A.H2SB.Na2S2O3C.Na2SO3(正确答案)D.Na2SO4E.S28.在原电池中, 发生氧化反应的是:() [单选题] *A.正极B.负极(正确答案)C.正极和负极D.正极或负极E.以上都对29.13号元素在元素周期表的位置是:() [单选题] *A.4周期ⅠA族B.4周期ⅡA族C.3周期ⅢA族(正确答案)D.4周期ⅥA族E.4周期ⅢA族30.某元素处在元素周期表的第三周期,该元素原子的电子层数为:() [单选题] *A.1B.2C.3(正确答案)D.4E.531.水的沸点“反常”,这是由于分子间存在着:() [单选题] *A.范德华力B.共价键C.氢键(正确答案)D.离子键E.E.配位键32.配合物中特征化学键是:() [单选题] *A.离子键B.共价键C.配位键(正确答案)D.氢键E.化学键33.下列盐中,难溶于水的是:() [单选题] *A.Ca(HCO3)2B.CaCO3(正确答案)C.Na2CO3D.(NH4)2CO3E.NH4Cl34.下列物质中,不能用做消毒剂的是:() [单选题] *A.氯水B.臭氧C.双氧水D.蒸馏水(正确答案)E.都不能做消毒剂35.H2O2不具备的性质是:() [单选题] *A.氧化性B.还原性C.不稳定性D.酸性E.既没有氧化性也没有还原性(正确答案)36.下列物质中与Cl2 作用能生成漂白粉的是:() [单选题] *A.CaCO3B.CaSO4C.Mg(OH) 2D.Ca(OH) 2(正确答案)E.MgSO437.下列化学药品在实验室常作氧化剂的是:() [单选题] *A.硫酸铜B.活泼金属C.高锰酸钾(正确答案)D.氯化钠E.水38.用自来水养金鱼时,通常先将自来水日晒段时间后,再注入鱼缸,其目的是()[单选题] *A.利用紫外线杀死水中的细菌B.提高水温,有利于金鱼生长C.增加水中氧气的含量D.促进水中的次氯酸分解(正确答案)E.以上说法均不正确39.下列关于Al(OH) 3性质的叙述错误的是() [单选题] *A.Al(OH) 3是两性的,其酸性与碱性相当B.可溶于酸C.Al(OH) 3是两性的,其酸性弱于碱性(正确答案)D.可溶于过量的强碱E.Al(OH) 3是碱性的40.参与构成人体和维持机体正常生理功能的元素称为:() [单选题] *A.人体微量元素B.人体常量元素C.人体必需元素(正确答案)D.人体有益元素E.人体有害元素二、是非(共10小题,每题1分,共10分。
中南大学2020年《无机化学》考试试题及答案

---○---○--- ---○---○--- 学 院专业班级学 号姓 名任课教师………… 评卷密封线 ……………… 密封线内不要答题,密封线外不准填写考生信息,违者考试成绩按0分处理 ……………… 评卷密封线 ………… 中南大学考试试卷(A 卷) 2019~2020 学年 1 学期 无机化学 课程 时间110分钟 56 学时, 闭 卷,总分 100 分,占总评成绩 70 % 题 号 一 二 三 四 五 合 计 得 分 评卷人 复查人 一、单选题(本题40分,每小题2分,请将答案填入下表中) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 1.在一定温度下,某容器中充有质量相等的下列气体,其中分压最小的是( ) (A )N 2 (B )CO 2 (C )O 2 (D )He 2.反应CaCO 3(s) CaO(s) + CO 2(g) 在高温时正反应自发进行,其逆反应在298 K 时为自发的,则逆反应的 Δr H m ө 和 Δr S m ө 是( ) (A )Δr H m ө > 0和 Δr S m ө > 0 (B )Δr H m ө < 0和 Δr S m ө > 0 (C )Δr H m ө < 0和 Δr S m ө < 0 (D )Δr H m ө > 0和 Δr S m ө < 0 3.670 K 时,H 2(g) + D 2(g) 2HD (g) 的平衡常数K ө = 3.78,同温下反应HD (g) 1/2 H 2(g) + 1/2 D 2(g) 的平衡常数K ө 为( ) (A )0.514 (B )0.265 (C )1.94 (D )0.133 4.将0.01 mol·L –1的某一元弱酸溶液稀释一倍时,下列因素将不变的是( ) (A )H 3O + 的浓度 (B )pH (C )解离度 α (D )解离常数K a ө 5.将pH=5.00的强酸和pH=13.00的强碱溶液等体积混合,则混合溶液的pH 为( ) (A )5.00 (B )8.00 (C )9.00 (D )12.70 6.向饱和AgCl 溶液中加水,下列叙述正确的是( ) (A )AgCl 的溶解度增大 (B )AgCl 的K sp ө 增大 (C )AgCl 的溶解度、K sp ө 均不变 (D )AgCl 的溶解度、K sp ө 均增大 7.下列有关分步沉淀的叙述正确的是( ) (A )溶度积小的物质先沉淀出来 (B )沉淀时所需沉淀试剂浓度小的先沉淀出来 (C )溶解度小的物质先沉淀出来 (D )被沉淀离子浓度大的先沉淀 8.由反应Fe(s) + 2Ag +(aq) Fe 2+(aq) + 2Ag(s) 组成的原电池,若将Ag +浓度减小到原来的1/10,则原电池电动势的变化为( )(A )增加0.0592 V (B )降低0.0592 V (C )降低0.118 V (D )增加0.118V 得 分 评卷人10.根据分子轨道理论,O 2的最高占有轨道(HOMO )是( )(A )σ2p (B )σ2p * (C )π2p (D )π2p *11.利用价层电子对互斥理论推测ClO 2– 的几何构型为( )(A )直线型 (B )V 型 (C )T 型 (D )三角形12.下列各组物质熔点高低判断错误的是( )(A )SiO 2 > CO 2 (B )CaO > KCl (C )NaCl < NaBr (D )MgO > Al 2O 313.下列各分子中,偶极距不为零的是( )(A )BeCl 2 (B )BF 3 (C )NF 3 (D )CH 414.下列关于配合物的叙述错误的是( )(A )高自旋配合物的晶体场分裂能小于电子成对能(B )通常情况下內轨型配合物比外轨型配合物稳定(C )中心离子的未成对电子数愈多,配合物磁矩愈大(D )第一过渡系金属离子[M(H 2O)6]n + 的水溶液均具有一定的颜色15.在氯的含氧酸中,氧化能力最强的是( )(A )HClO (B )HClO 2 (C )HClO 3 (D )HClO 416.下列叙述正确的是( )(A )H 2O 2分子构型为直线型 (B )H 2O 2既有氧化性又有还原性(C )H 2O 2 是非极性分子 (D )H 2O 2与K 2CrO 7的酸性溶液反应生成稳定的CrO 517.下列含氧酸中属于一元中强酸的是( )(A )H 3PO 2 (B )H 3PO 3 (C )H 3BO 3 (D )H 3AsO 318.下列化合物中属于离子型化合物的是( )(A )ZnCl 2 (B )CuCl 2 (C )FeCl 3 (D )HgCl 219.下列物质不易被空气所氧化的是( )(A )Fe 2+ (B )Mn(OH)2 (C )Ni(OH)2 (D )[Co(NH 3)6]2+20.仅用一种试剂即能将Fe 3+、Ni 2+、Zn 2+、Ag + 和Hg 2+五种离子区分开,这种试剂是( )(A )NH 3·H 2O (B )NaOH (C )H 2S (D )Na 2S 二、是非题(对,打“√”;错,打“×”每小题1分,共10分) 1.冬天公路上撒盐以使冰融化,此时Δr G m 的符号为负,Δr S m 的符号为正。
无机化学考试试卷

无机化学考试试卷一、选择题(每题2分,共20分)1. 以下哪种元素的原子序数是11?A. 氢B. 钠C. 铝D. 硅2. 元素周期表中的第18族元素被称为:A. 碱土金属B. 卤素C. 稀有气体D. 过渡金属3. 以下化合物中,哪个是共价化合物?A. NaClB. CaOC. H2OD. LiI4. 以下哪个反应是氧化还原反应?A. 2H2O → 2H2 + O2B. CaO + H2O → Ca(OH)2C. 2Na + Cl2 → 2NaClD. CO2 + H2O → H2CO35. 以下哪个不是碱金属元素?A. 锂B. 钠C. 钾D. 铯6. 什么是原子的电子亲和能?A. 原子获得电子的能力B. 原子失去电子的能力C. 原子形成化学键的能力D. 原子形成离子的能力7. 以下哪个是金属元素的典型特性?A. 良好的电导性B. 良好的热塑性C. 良好的光合作用D. 良好的热分解性8. 以下哪个是正确的化学方程式?A. 2H2 + O2 → 2H2OB. 2H2 + O2 → H2OC. 2H2 + O2 → H2O2D. 2H2O → 2H2 + O29. 以下哪个是正确的离子方程式?A. NaCl → Na+ + ClB. H2O → H+ + OH-C. CaCO3 → Ca2+ + CO3D. Mg(OH)2 → Mg2+ + 2OH-10. 以下哪个是正确的化学式?A. 氧气 O2B. 水 H2OC. 二氧化碳 CO2D. 所有选项都是正确的二、填空题(每空1分,共20分)11. 原子的核外电子排布遵循______原理。
12. 元素的化学性质主要由其原子的______决定。
13. 元素周期表中的第1族元素被称为______。
14. 离子键是由______和______之间的相互作用形成的。
15. 一个原子的电子亲和能越大,它获得电子的能力越______。
三、简答题(每题10分,共20分)16. 描述什么是离子键,并给出一个例子。
无机化学实验试卷A

1. 标定氢氧化钠溶液的浓度时,不能用作基准试剂的物质是A.邻苯二甲酸氢钾B.草酸C.盐酸D.苯甲酸2. 使用下列仪器时需要润洗的是A.容量瓶B.移液管C.锥形瓶D.量筒3. 用已知标准浓度的NaOH溶液滴定HCl溶液达终点时,若滴定管尖还挂有一滴碱液,则A.估计出这一滴碱液的体积B.直接读数C.将此一滴碱液靠入锥形瓶后读数D.滴定失败,重新滴定4. 下列物质不能用来标定EDTA浓度的是A.Ca B.Zn C.CaO D.ZnO5. 欲取20.00mLEDTAD溶液于锥形瓶中,最合适的仪器是A.移液管B.量筒C.酸式滴定管D.碱式滴定管6. 用K2Cr2O7标定Na2S2O3的浓度,滴定终点时溶液的颜色为A.红色B.蓝色C.绿色D.无色7. 下列操作不属于固液分离方法的是A.过滤B.离心C.倾析D.蒸发8. 某同学取10.00mL的Fe2+于锥形瓶中,用0.01667mol/L的K2Cr2O7标定至终点,用了10.00mL,则Fe2+的浓度(mol/L)为A.0.01667 B.0.1000 C.0.002778 D.0.050019. 我国食盐中加有碘,该碘的存在形式是A.I2B.KI C.KIO3D.KIO10.测定胃舒平中的铝含量,最简单的方法是A.直接滴定B.置换滴定C.返滴定D.重量法1. 蒸发硫酸亚铁铵溶液时,溶液出现黄褐色的原因是。
2. 明矾能作为净水剂是因为。
3. 三草酸合铁(III)酸钾能作为感光材料是因为。
4. 硫代硫酸钠不能用作基准试剂,原因有三:硫代硫酸钠含有杂质;硫代硫酸钠易风化和潮解;。
5. 用重铬酸钾标定硫代硫酸钠,到终点后溶液又变蓝色的原因有二:;。
6. 食盐中的抗结剂是,水中的溶解氧以形式存在。
7. 工业废水中若有苯酚,在酸性条件下加入溴酸钾-溴化钾,会出现色沉淀。
8. 氯化铵是一种速效化肥,生产和实验中,广泛采用测定其氮含量。
9. 测定工业用水的硬度时,须在溶液中加入来消除Fe3+离子干扰。
《无机化学》考试试卷及答案

《无机化学》考试试卷及答案一、选择题(在下列各题中,选出符合题意的1个答案,写在括号中,每题1.5分,共24分)1.下列说法正确的是( )A.放热反应均为自发反应B.r S m为正的反应均为自发反应H m为负的反应均为自发反应C.r S m为正、rH m为正的反应均为自发反应D.r S m为负、r2.升高温度可以加快反应速率,其主要原因是( )A.降低了反应的活化能B.增加了活化分子百分数C.增加了活化分子总数D.增加了分子的碰撞次数3.下列各组量子数,不合理的是( ) (按n、l、m的顺序)A.(2,2,–1)B.(3,1,–1)C.(1,0,0)D.(4,3,1)4.分子中有极性键且偶极矩不等于零的是( )A.CO2B.BF3C.CH4D.CH2Cl25.室温下,稳定状态单质的标准摩尔熵是( )A.0B.1C.>0D.<06.既能用浓H2SO4干燥,又能用碱石灰干燥的物质是 ( )A.NH3B.H2C.SO2D.Cl27.已知H2S的=1.0×10–7,=1.0×10–13,在1L饱和的H2S水溶液中通0.1mol的HCl气体,c(S2–)为( )mol·L-1A.1.0×10–13B.1.0×10–4C.1.0×10–20D.1.0×10–198.将pH=5.0 与pH=9.0的两种强电解质溶液等体积混合,其pH值为( )A.1.0B.13.0C.7.0D.1.59.既溶于过量氨水,又溶于过量NaOH溶液的是( )A.Ca(OH)2B.Fe(OH)3C.Zn(OH)2D.Al(OH)310.配制I2溶液时,加入固体KI,目的是为了( ),增大I2的溶解度。
A.增加盐效应B.利用同离子效应C.降低水分子极性D.生成I3-离子11.在Al2(SO4)3溶液中加入Na2CO3,其主要产物是( )。
A.Al2(CO3)3+Na2SO4B.Al3++CO32-C.Al(OH)3+CO2D.Al2(CO3)3+CO212.40mL0.1mol·L–1HAc与20mL0.1mol·L–1NaOH混合后,溶液的pH值为( )A.3.1B.9.25C.4.75D.5.313.已知(Fe3+/Fe2+)=0.77V,(Fe2+/Fe)= –0.44V,则(Fe3+/Fe)=( )A.–0.037VB.0.55VC.0.40VD.1.65V14.27元素Co的[Co(NH3)6]3+是内轨型配合物,则中心离子未成对电子数和杂化轨道类型是( )A.4,sp3d2B.0,sp3d2C.4,d2sp3D.0,d2sp315.下列分子或离子中含有键的是( )A.SO2B.NO3-C.NO2D.NO2+三、是非题(判断下列叙述是否正确,在正确的答案后打√,在错误的答案后打×,共10分,每题1分。
无机化学试题

无机化学试题一、选择题1. 下列化合物中,具有最高氧化数的是:a) KClO4b) NaNO3c) LiClO4d) Ca(NO3)22. 下列元素中,不属于第三周期的是:a) 氮b) 氧c) 硫d) 钠3. 以下离子中,半径最大的是:a) Mg2+b) Na+c) Al3+d) F-4. 化合物XY4的结构是:a) 三角双锥b) 正方形c) 八面体d) 正四面体5. 下列化合物中,属于强酸的是:a) HClb) H2SO3c) CH3COOHd) H2SO4二、填空题1. 氮气的化学式是________。
2. 一氧化碳的化学式是________。
3. 碳的原子序数是_______。
4. 氯化钠的化学式是________。
5. 硝酸的化学式是________。
三、解答题1. 现有一物质X,被氧化剂Y氧化,生成了化合物Z和水。
写出反应方程式,并指名X、Y、Z的化学式。
2. 铝的原子序数是13,氧的原子序数是8,将它们的电子排布写出来。
3. 硒是一种非金属元素,它的原子序数是34,写出硒的化学式以及它的主要化合物。
四、综合题1. 对于以下离子:SO4^2-、CO3^2-、PO4^3-,写出它们的键合结构以及它们的分子式。
2. 举例说明一种金属和非金属的化合物,并写出化学式。
3. 解释强酸和强碱的概念,分别给出一种强酸和一种强碱的例子。
以上是无机化学试题的内容,希望对你的学习有所帮助。
祝你取得好成绩!。
无机化学试题及答案

无机化学试题及答案公司内部档案编码:[OPPTR-OPPT28-OPPTL98-OPPNN08]2009-2010无机化学考试试卷(A )一、选择题:本大题共25个小题,每小题1分,共25分.选择出符合题意的一个答案,将其字母填在题后的括号内.1.下列物质碱性的大小顺序正确的是 [ ] A. NH 3<N 2H 4<NH 2OH B. NH 3>N 2H 4<NH 2OH C. N 2H 4>NH 3 >NH 2OH D. NH 3>N 2H 4>NH 2OH2.熔点最高的金属是 [ ] A. Cr B. W C. Au D. Tc3.现有ds 区某元素的硫酸盐 A 和另一元素氯化物 B 水溶液,各加入适量KI 溶液,则 A 生成某元素的碘化物沉淀和 I 2。
B 则生成碘化物沉淀,这碘化物沉淀进一步与KI 溶液作用,生成配合物溶解,则硫酸盐和氯化物分别是 [ ]A. ZnSO 4, Hg 2Cl 2B. CuSO 4, HgCl 2C. CdSO 4, HgCl 2D. Ag 2SO 4,Hg 2Cl 23.下列不属于二元质子酸的是 [ ]A. H 3PO 3B. H 2SO 4C. H 3PO 2D. NaH 2PO 44.既能溶于NaOH 又能溶于NH 3·H 2O 的氢氧化物是 [ ]A. Fe(OH)3B. Zn(OH)2C. Al(OH)3D. Cd(OH)25.AgBr 晶体在1L 1 mol/L 氨水中的饱和溶液浓度为(mol/L) (已知Ag(NH 3)2+的稳定常数为×107,AgBr 的K sp =×10-13). [ ]A. ×10-3B. ×10-3C. ×10-3D. ×10-26.PCl3和水反应的产物是 [ ],HCl B. H3PO3,HCl C. H3PO4,HCl D. PH3,HClO7.下列难溶于水的硫化物中,不溶于硝酸但可溶于Na2S溶液的是[ ]A. CuSB. ZnSC. MnSD. HgS8.将过量SiF4通入NaOH溶液中,主要产物是 [ ]A. H4SiO4,NaF B. Na2SiO3,NaF C. Na2SiO3,Na2SiF6D. SiO2,HF10. 下列含氧酸的氧化性顺序正确的是 [ ]A. HClO>HBrO>HIOB. HIO>HBrO> HclOC. HClO4>HClO3>HClO D. HClO3>HClO> HClO411.下列各组元素中,性质最相似的两个元素是 [ ]A. Zr和HfB. Mg和AlC. Ag和AuD. Fe和Co12.下列物质的强氧化性与惰性电子对效应无关的是 [ ]A. PbO2 B. NaBiO3C. K2Cr2O7D. TlCl313.下列那种分子不含桥链结构 [ ]A. AlCl3 B. FeCl3C. CuCl2D. FeCl214.仅一种试剂,即可将Ag+, Hg2+, Zn2+, Fe3+, Ni2+五种离子区分开,可选用 [ ]15.A. NH3·H2O B. NaOH C. H2S D. Na2S16.含有下列离子的溶液,与Na2S溶液反应不生成黑色沉淀的一组是[ ]A. Fe2+, Bi3+B. Cd2+, Zn2+C. Fe3+, Cu2+D. Mn2+, Pb2+17.下列含氧酸中属于一元酸的是[ ]A. H3BO3B. H3AsO3C. H3PO3D. H4SiO418.下列物质与盐酸反应,能生成三价氯化物的是 [ ]A. Co2O3B. Fe2O3C. Ni2O3D. Pb3O419.下列碳酸盐中,热稳定性最好的是 [ ]A. BeCO3 B. MgCO3C. SrCO3D. BaCO320.通常鉴定镍离子的试剂是 [ ]A.硫脲B.二苯基联苯胺C.硝基苯偶氮间苯二酚D.丁二酮肟21.向Hg2Cl2溶液中加入过量的氨水后生成的产物是 [ ]A. Hg2(OH)42- B. [Hg(NH3)4]2+ C. Hg↓+ HgNH2Cl↓ D.HgNH2Cl↓22.含有П46离域大п键的是 [ ]A. ClO3- B. SO32- C. SO3(g) D. SOCl223.在HCl、 HBr 、HI 、HF中,沸点最低的是 [ ]A. HFB. HClC. HBrD. HI24.在Cr2(SO4)3溶液中,加入Na2S溶液,其沉淀产物为 [ ]A. Cr2S3(OH)325.在NaH2PO4溶液中加入AgNO3溶液后,主要产物是 [ ]B. AgOHC. AgH 2PO 4D. Ag 3PO 426. 在酸性介质中,欲使Mn 2+氧化为MnO 4-,可加下列哪种氧化剂[ ]A. KClO 3B. K 2Cr 2O 7C. 王水D. PbO 2 二、用化学反应方程式说明下列现象(要求配平,每小题2分,共10分)27. HgS 溶解于王水 28. CuO与氢碘酸反应29. 铜器在潮湿空气中缓慢生成一层绿色的铜锈 30. 铅制品中硫化铅黑斑可用过氧化氢处理去除 31. 热分解CuCl 2·2H 2O 产生黑色物质三、填空题(每空1分,共20分)32. 要除去N 2O(g)中的NO(g), 选用的试剂是( )。
广东医学院2020级本科《无机化学》期终考试试卷 (A)

广东医学院2020级本科《无机化学》期终考试试卷(A)二、填空题(共10分,每空1分)1.指出下列配合物的中心原子的单电子数、杂化类型、空间构型、内轨或外轨性三、计算题(共30分,每题10分)1. 某水溶液的凝固点是-0.85℃,试计算:(1)此溶液的沸点。
(2)27℃时的渗透压。
(已知水的K f = 1.86K·kg·mol-1,K b =0.512K·kg·mol-1)2. 计算下列溶液的pH值:(1)0.10 mol·L-1NH3·水溶液与0.050 mol·L-1HCl溶液等体积混合。
(2)0.10 mol·L-1NH3水溶液与0.10 mol·L-1HAc溶液等体积混合。
(已知:NH3:Kb =1.76×10-5, HAc:Ka=1.79×10-5,不考虑离子强度)3. 已知φθ(Cu2+/Cu)=+0.34V,φθ(Ag+/Ag)=+0.80V。
现将反应2Ag+ + Cu = 2Ag + Cu2+ 设计成原电池,若[Cu2+]=0.1mol·L-1,[Ag+]=0.01mol·L-1。
(1)写出该电池的组成式。
(2)计算此电池的电动势E并判断该反应进行的方向。
(3)计算标准状态下反应的平衡常数K⊖。
广东医学院2020级本科《无机化学》期终考试试卷(A)(客观题部分,答在答题卡上)一、选择题(共60分,每小题1.5分,只有一个正确答案)(1)答第一题前,考生务必先将考试科目、专业、年级和姓名用黑色签字笔写在答题卡上,同时一定要把学号用2B铅笔涂写在考号处。
考试结束,将试卷与答题卡一并交回。
(2)每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号,不能答在试题卷上。
1.红细胞在下列哪一种溶液中可保持正常状态( )A. 310m mol·L-1NaClB. 150m mol·L-1NaClC. 100m mol·L-1NaHCO3D. 0.380 mol·L-1葡萄糖2. 欲使被半透膜隔开的两种稀溶液间不发生渗透,应使两溶液(A,B中的基本单元均以溶质分子式表示)( )A. 物质的量浓度相同B. 质量摩尔浓度相同C. 质量浓度相同D. 渗透浓度相同3. 下列四种溶液(浓度都是0.1 mol·L-1)的凝固点最低的是( )A. Al2(SO4)3B. CaCl2C. MgSO4D. C6H5SO3H4. 盐碱地的农作物长势不良,甚至枯萎,其主要原因为( )A. 天气太热B. 很少下雨C. 肥料不足D. 水分从植物向土壤倒流5. 根据酸碱质子理论,下列物质中属于两性物质的是( )A. H2SB. CH3COO-C. NH2CH2COOHD. NH4+ .6. 已知HF的Ka =3.35 x 10-4, NH3的Kb=1.79 x 10-5,由此可知F- 与NH3.H2O相比,其碱性( )A. 比NH3.H2O 的强B. 比NH3.H2O弱C.与NH3.H2O的碱性相等D.无法比较7. 0.1 mol·L-1的H2S溶液中[S2-]是( )(已知H2S的Ka1=8.91×10-8, Ka2=1.12×10-12)A. 8.91×10-8B. 1.12×10-12C. 9.97×10-12D. 4.46×10-88. 已知固体K sp[Mn(OH)2]=2.06×10-14,0.01 mol·L-1MnCl2固体溶于1L pH=10的溶液中,则下列说法正确的是( )A. 溶液刚好饱和,无Mn(OH)2沉淀生成B. 溶液未达到饱和,无Mn(OH)2沉淀生成C.有Mn(OH)2沉淀生成D. 与溶液pH无关,无Mn(OH)2沉淀生成9. 在AgCl的饱和溶液中,有AgCl固体存在,当加入等体积的下列哪一种溶液会使AgCl的溶解度更大一些( )A. AgCl的饱和溶液B. 1mol.L-1NaClC. 1mol.L-1AgNO3D. 2mol.L-1NaNO3;10. HgCl2的Ksp = 4×10-15,则HgCl2饱和溶液中,Cl-离子的浓度是( )A. 4×10-8B. 2×10-15C. 1×10-15D. 2×10-511. 列关于电极电势φ 的叙述中,正确的是( )A. 电对的φ 越小,表明该电对的氧化态得电子倾向越大,是越强的的氧化剂B. 电对的φ 越大,其还原态越易得电子,是越强的的还原剂C. 电对的φ 越小,其还原态越易失去电子,是越强的的还原剂D. 电对的φ 越大,其氧化态是越弱的的氧化剂12. 利用离子电子法配平反应方程式Mn2++BiO3-=MnO4-+Bi3++H2O (酸性介质)配平后,H2O的系数应为( )A. 3B. 7C. 11D. 1613. 由标准锌半电池和标准银半电池组成原电池:(-) Zn(s) | ZnSO4(a=1)‖AgNO3(a=1) | Ag(s) (+)若在AgNO3溶液中加入氨水,电池电动势将( )A. 变大B. 变小C. 不变D. 无法判断14. 根据公式lgK = nEө / 0.0592 ,可以看出溶液中氧化还原反应的平衡常数K(严格地说应为Kө)应( )A. 与温度无关B. 与浓度无关C. 与反应本性无关D.与反应方程式的书写无关15. 己知ϕθCu 2+/ Cu= 0.34伏,ϕθSn4+ / Sn2+= 0.15伏,ϕθFe3+/ Fe2+= 0.77伏,判断标准状态时还原性从强到弱的顺序是( )A. Sn4+, Fe3+,Cu2+B. Cu2+ ,Sn4+ ,Fe3+C. Fe2+ ,Cu ,Sn2+D. Sn2+,Cu ,Fe2+16. 原子基态的电子构型为[Ar] 3d104s1 ,它在元素周期表中的位置是( )A. s区B. p区C. d区D. ds区17. 下列离子的电子构型可以用[Ar]3d5 表示的是( )A. Mn2+B. Fe2+C. Co2+D. Ni2+18. 下列各组量子数中,合理的一组是( )A. n=3,l=1,m1 =+1,m s=+1/2B. n=4,l=5,m1 =-1,m s= +1/2C. n=3,l=3,m1 =+1,m s=-1/2D. n=4,l=2,m1 =+3,m s= -1/219. Cu2+的电子排布式为( )A. [Ar] 3d8 4s1B. [Ar] 3d94s1C. [Ar] 3d94s0D. [Ar] 3d10 4s020. 描述一确定的电子运动状态,需用以下参数( )A. n.lB. n.l.mC. n.l.m.m sD. 只需n21. 下列说法不正确的是( )A. 氢原子中,电子的能量只取决于主量子数nB. 多电子原子中,电子的能量不仅与n有关,还与l有关C. 波函数由四个量子数确定D. m s=±½表示电子的自旋有两种方式22. H2S分子的空间构型、中心原子的杂化方式分别为:( )A. 直线形、sp等性杂化B. V形、sp2不等性杂化D. V形、sp3不等性杂化 D. V形、sp3等性杂化23. 在酒精的水溶液中,分子间主要存在的作用力为( )A. 取向力B. 诱导力C. 色散力和诱导力、取向力D. 取向力、诱导力、色散力、氢键24. BF3 分子中,N 原子与三个氯原子成键所采用的轨道是( )A. 二个sp轨道,一个p轨道成键B. 三个sp3 轨道成键C. p x p y p z 轨道成键D. 三个sp2 轨道成键25. 下列离子或分子有顺磁性的是( )A. O22-B. N2C. NOD. NO+26. 在[Co(en)2(NH3)Cl]2+中,Co3+的配位数是( )A. 4B. 5C. 6D.727. AgCl的Ksp=a,[Ag(NH3)2]+的Ks=b,则下列反应AgCl +2 NH3-↔[Ag(NH3)2]++Cl-的平衡常数为( )A. abB. a+bC. b/aD.a/b28. Na2S2O3可作为重金属中毒时的解毒剂,这是利用它的( )A. 还原性B. 氧化性C. 配位性D. 与重金属离子生成难溶物。
无机化学期末考试试题库

无机化学期末考试试题库一、选择题(共10题,每题2分)1. 以下哪一种金属是常温下液体状态的?- A. 铜- B. 铁- C. 汞- D. 铝2. 对于下列化学式,哪一种物质是无机化合物?- A. C6H12O6- B. CH4- C. NaCl- D. C2H5OH3. 水在常温常压下的沸点是多少?- A. 100℃- B. 0℃- C. -273℃- D. 25℃4. 下面哪种元素在元素周期表上属于卤素族?- A. 氢- B. 氮- C. 氧- D. 氯5. 以下哪种物质不属于无机盐?- A. NaCl- B. CaCO3- C. H2SO4- D. NH4OH6. MgO是什么化合物的化学式?- A. 氧化锌- B. 氧化铝- C. 氧化钠- D. 氧化镁7. Fe2O3是以下哪种化合物?- A. 二氧化铁- B. 三氧化铁- C. 二氧化氮- D. 二氧化氢8. 下列哪种金属属于贵金属?- A. 铜- B. 银- C. 铝- D. 铁9. 化学式KCl表示什么物质?- A. 氯化钠- B. 氯化氢- C. 氧化钠- D. 氯化钾10. 以下哪种物质适合用于蓄电池?- A. 铝- B. 锌- C. 铁- D. 银二、填空题(共5题,每题2分)1. N2是________化合物的化学式。
2. 水的化学式是________。
3. 氧元素的化学符号是________。
4. 具有相同电子层结构的元素属于同一________。
5. NaOH的化学名是________。
三、问答题(共5题,每题10分)1. 解释离子化合物的概念。
2. 什么是氧化还原反应?举一个例子。
3. 请解释一下溶液的概念。
4. 简要介绍一下主族元素和过渡元素的区别。
5. 为什么金属导电性强?。
复旦大学《无机化学》2023-2024学年第一学期期末试卷

7. 以下哪种化合物属于酸式盐? A. NaCl B. NaNO₃ C. Na₂ SO₃ D. Na₂ CO₃
8. 下列哪种元素属于过渡元素? A. 碳
B. 氮 C. 磷 D. 锌
9. 在化合物中,以下哪种键属于金属键? A. 氢键 B. 离子键 C. 金属键 D. π 键
复旦大学《无机化学》2023-2024 学年第一学期期末试卷
考试课程:无机化学 考试时间:120 分钟 专业:化学 总分:100 分
一、单项选择题(每题 2 分,共 20 分)
1. 以下哪种化合物属于酸式盐? A. NaCl B. NaNO₃ C. Na₂ SO₃ D. Na₂ CO₃
2. 下列哪种元素属于主族元素? A. 碳 B. 氮 C. 磷 D. 锌
子键。 27. 无机化合物的命名规则有_____________________。 28. 在化合物中,_____________________键是指原子之间的金
属键。 29. 氧化还原反应的类型有_____________________。 30. 无机化合物的性质有_____________________。
四、简答题(每题 10 分,共 40 分) 31. 请简述酸式盐和碱式盐的区别及其在化学反应中的应用。 32. 试述氧化还原反应的基本原理及其在化学反应中的应用。 33. 请简述无机化合物的命名规则及其在化学反应中的应用。 34. 试述金属键的特点及其在化合物中的应用。
考试说明: 1. 答题前请务必将姓名、学号及班级填写在答题纸上。 2. 所有答案必须写在答题纸上,不能在试卷上作答。 3. 本试卷共 100 分,考试时间为 120 分钟。
无机化学试题
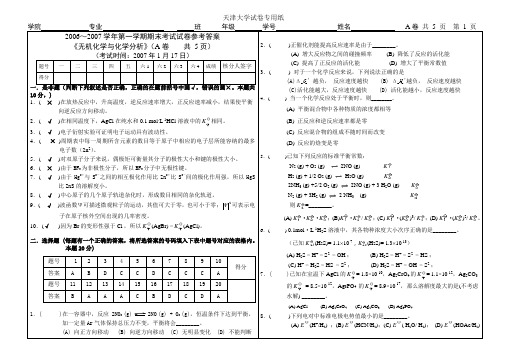
1 0 0
1-
n(总)=1+
=
=68.7%
天津大学试卷专用纸
学院专业班年级学号姓名共5页第5页
3.含有FeCl2和CuCl2的溶液,两者的浓度均为0.10 mol·L-1,通H2S至饱和(饱和H2S溶液的浓度为0.1mol·L-1),通过计算说明是否会生成FeS沉淀?
4.( )当一个化学反应处于平衡时,则________。
(A)平衡混合物中各种物质的浓度都相等
(B)正反应和逆反应速率都是零
(C)反应混合物的组成不随时间而改变
(D)反应的焓变是零
5.( )已知下列反应的标准平衡常数:
N2(g) + O2(g) 2NO (g)K
H2(g) + 1/2 O2(g) H2O (g)K
2.( )正催化剂能提高反应速率是由于________。
(A)增大反应物之间的碰撞频率(B)降低了反应的活化能
(C)提高了正反应的活化能(D)增大了平衡常数值
3.( )对于一个化学反应来说,下列说法正确的是
(A)ΔrGmθ越负,反应速度越快(B)ΔrHmθ越负,反应速度越快
(C)活化能越大,反应速度越快(D)活化能越小,反应速度越快
(C)分子间力和氢键能同时存在于分子之间;
(D)大多数分子的分子间力以色散力为主;
三.填空题(本题共22分)
1.50号元素的电子排布式为[Kr]4d105s25p2,该元素属五周期,IVA族,P区元素.
2.在乙醇的水溶液中,分子间存在的分子间力的种类有色散力、诱导力、
取向力和氢键。
3.KCN, NH4F, NH4OAc, NH4NO3, Na2CO3,各溶液浓度均为0.1 mol·L-1,按pH值从小到大顺序排列NH4NO3, NH4F, NH4OAc, KCN, Na2CO3。(已知Kθ(NH3·H2O)=1.8×10-5,Kθ(HF)=6.6×10-4,Kθ(HCN)=6.2×10-10,Kθ(HOAc)=1.8×10-5, (H2CO3)=4.4×10-7, (H2CO3)=4.8×10-11)
无机化学试题及答案

⽆机化学试题及答案⽆机化学试题及答案公司内部档案编码:[OPPTR-OPPT28-OPPTL98-OPPNN08]2009-2010⽆机化学考试试卷(A )⼀、选择题:本⼤题共25个⼩题,每⼩题1分,共25分.选择出符合题意的⼀个答案,将其字母填在题后的括号内.1.下列物质碱性的⼤⼩顺序正确的是 [ ] A. NH 3N 2H 4NH 3 >NH 2OH D. NH 3>N 2H 4>NH 2OH2.熔点最⾼的⾦属是 [ ] A. Cr B. W C. Au D. Tc3.现有ds 区某元素的硫酸盐 A 和另⼀元素氯化物 B ⽔溶液,各加⼊适量KI 溶液,则 A ⽣成某元素的碘化物沉淀和 I 2。
B 则⽣成碘化物沉淀,这碘化物沉淀进⼀步与KI 溶液作⽤,⽣成配合物溶解,则硫酸盐和氯化物分别是 [ ]A. ZnSO 4, Hg 2Cl 2B. CuSO 4, HgCl 2C. CdSO 4, HgCl 2D. Ag 2SO 4,Hg 2Cl 23.下列不属于⼆元质⼦酸的是 [ ]A. H 3PO 3B. H 2SO 4C. H 3PO 2D. NaH 2PO 44.既能溶于NaOH ⼜能溶于NH 3·H 2O 的氢氧化物是 [ ]A. Fe(OH)3B. Zn(OH)2C. Al(OH)3D. Cd(OH)25.AgBr 晶体在1L 1 mol/L 氨⽔中的饱和溶液浓度为(mol/L) (已知Ag(NH 3)2+的稳定常数为×107,AgBr 的K sp =×10-13). [ ]A. ×10-3B. ×10-36.PCl3和⽔反应的产物是 [ ],HCl B. H3PO3,HCl C. H3PO4,HCl D. PH3,HClO7.下列难溶于⽔的硫化物中,不溶于硝酸但可溶于Na2S溶液的是[ ]A. CuSB. ZnSC. MnSD. HgS8.将过量SiF4通⼊NaOH溶液中,主要产物是 [ ]A. H4SiO4,NaF B. Na2SiO3,NaF C. Na2SiO3,Na2SiF6,HF10. 下列含氧酸的氧化性顺序正确的是 [ ]A. HClO>HBrO>HIOB. HIO>HBrO> HclOC. HClO4>HClO3>HClO D. HClO3>HClO> HClO411.下列各组元素中,性质最相似的两个元素是 [ ]A. Zr和HfB. Mg和AlC. Ag和AuD. Fe和Co12.下列物质的强氧化性与惰性电⼦对效应⽆关的是 [ ]A. PbO2 B. NaBiO3C. K2Cr2O7D. TlCl313.下列那种分⼦不含桥链结构 [ ]A. AlCl3 B. FeCl3C. CuCl14.仅⼀种试剂,即可将Ag+, Hg2+, Zn2+, Fe3+, Ni2+五种离⼦区分开,可选⽤ [ ]15.A. NH3·H2O B. NaOH C. H2S D. Na2S16.含有下列离⼦的溶液,与Na2S溶液反应不⽣成⿊⾊沉淀的⼀组是[ ]A. Fe2+, Bi3+B. Cd2+, Zn2+C. Fe3+, Cu2+D. Mn2+, Pb2+17.下列含氧酸中属于⼀元酸的是[ ]A. H3BO3B. H3AsO3C. H3PO3D. H4SiO418.下列物质与盐酸反应,能⽣成三价氯化物的是 [ ]A. Co2O3B. Fe2OO3D. Pb3O419.下列碳酸盐中,热稳定性最好的是 [ ]A. BeCO3 B. MgCO3C. SrCO3D. BaCO320.通常鉴定镍离⼦的试剂是 [ ]A.硫脲B.⼆苯基联苯胺C.硝基苯偶氮间苯⼆酚D.丁⼆酮肟21.向Hg2Cl2溶液中加⼊过量的氨⽔后⽣成的产物是 [ ]A. Hg2(OH)42- B. [Hg(NH3)4]2+ C. Hg↓+ HgNH2Cl↓ D.HgNH2A. ClO3- B. SO32- C. SO3(g) D. SOCl223.在HCl、 HBr 、HI 、HF中,沸点最低的是 [ ]A. HFB. HClC. HBrD. HI24.在Cr2(SO4)3溶液中,加⼊Na2S溶液,其沉淀产物为 [ ]A. Cr2S3(OH)325.在NaH2PO4溶液中加⼊AgNO3溶液后,主要产物是 [ ]B. AgOHC. AgH 2PO 4D. Ag 3PO 426. 在酸性介质中,欲使Mn 2+氧化为MnO 4-,可加下列哪种氧化剂[ ]A. KClO 3B. K 2Cr 2O 7C. 王⽔D. PbO 2 ⼆、⽤化学反应⽅程式说明下列现象(要求配平,每⼩题2分,共10分)27. HgS 溶解于王⽔ 28. CuOCuCl 2·2H 2O 产⽣⿊⾊物质三、填空题(每空1分,共20分)32. 要除去N 2O(g)中的NO(g),选⽤的试剂是( )。
一学期无机化学期中考试试卷(A卷)
⼀学期⽆机化学期中考试试卷(A卷)杭州师范⼤学化材学院2014-2015学年⼀学期⽆机化学期中考试试卷(B卷)班级:___________学号:___________姓名:___________得分:___________题⽬部分,(卷⾯共有51题,100.0分,各⼤题标有题量和总分)⼀、是⾮题(16⼩题,共16.0分)(1分)[1]p原⼦轨道的⾓度分布图是两个外切的等径圆,图中的正、负号代表电荷符号。
()(1分)[2] 原⼦的s轨道⾓度分布图是球形对称的。
()(1分)[3] 电⼦在原⼦核外运动的能级越⾼,它与原⼦核的距离就越远。
因为E (1s) < E (2s),所以任何时候1s电⼦⽐2s电⼦靠近原⼦核。
( )(1分)[4] 在周期系第三周期中,Si、P、S、Cl 的原⼦半径依次减⼩。
因此,Si4-、P3-、S2-、Cl-的离⼦半径也依次减⼩。
( ) (1分)[5] 在CS2、C2H2分⼦中,均有σ键和π键。
( )(1分)[6] 某原⼦所形成共价键的数⽬,等于该原⼦基态时未成对电⼦的数⽬。
( )(1分)[7] 相同原⼦间双键的键能等于单键键能的两倍,叁键键能等于单键键能的三倍。
( )(1分)[8] 烷烃分⼦中C - C 键的键长是炔烃分⼦中C≡C 键长的三倍。
( )(1分)[9] 原⼦轨道发⽣杂化后可以增强成键能⼒。
( )(1分)[10]SnCl2分⼦和H2O 分⼦的空间构型均为V 型,表明它们的中⼼原⼦采取相同⽅式的杂化轨道成键。
( )(1分)[11] 含有奇数电⼦的分⼦是顺磁性分⼦。
( )(1分)[12] 由分⼦轨道理论可推知O2、O2-、O22-键能的⼤⼩顺序为O2 > O2- > O22-。
( )(1分)[13] 分⼦中的共价键有极性,分⼦不⼀定是极性分⼦。
( ) (1分)[14]H2的极化率⽐He 的⼩。
( )(1分)[15] 对由⾮极性分⼦组成的物质来说,其沸点越⾼,则极化率越⼤。
《无机化学》期末考试试卷及参考答案
《无机化学》期末考试试卷适用专业:相对原子质量:H :1 O :16 C :12 N :14 Na ;23 Cl :35.5 S:32 Mg:24一、选择题(每小题只有一个正确的答案,请将其代码填入括号中;每小题2分,共60分) 1.下列物质中,属于无机化合物.....的是 ( ) A .葡萄糖 B .淀粉 C . 酒精 D . 食盐3.下列元素符号中,不属于卤族元素....的是 ( ) A .I B . F C .Cl D . Al4.表示摩尔的符号是 ( ) A .ml B .mg C .m D .mol5.右图是元素周期表中的一格,依据图中信息, 得到的下列认识中错误的是( )A .该元素原子的原子序数为16B . 该元素名称叫硫元素C .该元素的元素符号是SD .该元素的原子质量为32.06Kg 6.下列各能级中,符合能量由低到高的排列顺序的是 ( ) A . 3d2p4p1s2s B . 1s2s2p4p3d C . 1s2s2p3d4p D . 2p2s4p3d1s题号 一 二 三 四 总分 积分人 分数裁划玻璃A .B 菠萝榨汁C .磨制石器D .蜡烛照明2.人类的下列活动中不属于物理变化的是 ( ) 阅卷人班级 学号 姓名 - -------------------------------------装--------------------------------------------订---------------------------------------线-------------------------------------7. 5.5 mol 水的质量是 ( ) A . 18g B . 9g C . 99g D . 108g( )9.在标准状况下,任何气体的标准摩尔体积都是 ( ) A . 2.24L B . 11.2L C . 22.4L D . 224L10.下列物质的分子中属于极性分子的是 ( ) A . CO 2 B . O 2 C . HCl D . I 211.NaOH 的摩尔质量是 ( ) A . 4g B . 40 g/mol C . 40 Kg D . 28 mol12.在0.0001 mol/L 的NaOH 溶液中H +浓度为 ( ) A .10-4 mol/L B .10-10 mol/L C . 10-14 mol/L D .10-7mol/L14. 196g H 2SO 4的物质的量是 ( ) A .1mol B .2mol C .3mol D . 0.2mol 15. 浓度为0.01 mol/L 的稀盐酸的pH 是 ( ) A . 7 B . 2 C . 4 D . 816. 在标准状况下44.8L N 2气体的物质的量是 ( ) A .2mol B .1mol C .0.5mol D . 0.2mol17.配制250mL0.1mol/L 的NaOH 溶液需要NaOH 的质量是 ( ) A . 1g B . 10g C . 0.1g D .4gA . 试管B .烧瓶 D . 锥形C .容量瓶8.配制一定物质的量的浓度的溶液应选用的主要仪器是13.下列图像中不是..p 亚层电子云的是 ( ) A.C .B.D.19.配制250mL0.1mol/L 的NaCl 溶液应该选用的容量瓶的规格是 ( ) A . 250 mL B .200mL C . 100mL D . 500mL 20. 0.5mol 的水中含有的水分子个数是 ( ) A .3.01×1023B .6.02×1023C . 1.8×1023D .6.02×102221.标准状况下,与6.4gO 2的分子数目相同的CO 2气体的体积是 ( ) A . 22.4L B .11.2L C .4.48L D .2.24L22.在纯水中pH=7的原因是纯水 ( ) A . [H +]﹥[OH -] B . [H +]﹤[OH -] C . [H +]=[OH -] D .只有[H +] 无[OH -] 23.阿伏伽德罗常数是 A .5×1026B . 3.01×1022C . 6.02×1023D .3.01×1022.24.食盐属于 ( ) A .分子晶体 B .原子晶体 C . 离子晶体 D . 金属晶体 25.物质的量的国际单位是 ( ) A .千克 B .克 C .摩尔 D . 米27.非极性分子与非极性分子之间的作用力主要是 ( ) A .取向力 B .诱导力 C .色散力 D . 氢键28.在通常情况下,水的离子积常数.....是 ( ) A . 1×10-8B .1×10-7C .1×10-14D .1×10-1018.下图是元素周期表中某元素的原子结构示意图, ( ) 依据图中信息所得的结论错误的是 A .该元素的原子很容易得到电子 B .C. 该元素在第一主族 D . 该元素是碱金属元素v26.如图表示某可逆反应的化学平衡建立过程,下 列对于图像中的意义分析有错误的是A . 正反应速率在不断的减小B . 逆反应速率不断增大C .达到平衡时正反应和逆反应都停止,速率都为零D .达化学平衡时正、逆反应速率相等,29.某可逆反应的逆反应的平衡常数K 逆为4,则正反应的平衡常数K 正为( ) A .0.25 B .10 C .2 D .530. 金属铝属于 ( ) A . 原子晶体 B . 分子晶体 C .金属晶体 D .离子晶体 二、判断题(正确的打“√”,错误的打“×”;每小题1分,共10分)31.元素周期表中同一周期的元素随着原子序数的递增原子的半径由大变小 ( ) 32.元素周期表中同一主族的元素原子的最外层电子数一定相等 ( ) 33.分子是否有极性取决于整个分子中正负电荷的重心是否重合 ( ) 34.氧化还原反应的特征是有元素化合价的升降 ( ) 35. 强酸弱碱盐水解,溶液呈酸性 p H ﹤7 ( ) 36. 原电池是一种将电能转变为化学能的装置 ( ) 37. 物质的量就是指物质的质量 ( )38. 酸性溶液中[OH -]﹥[H +]﹥1×10-7mol/L ( ) 39.电子云图中的一个小黑点就代表一个电子. ( )40. 在NaAc-HAc 组成的缓冲溶液 中抗酸成分是HAc ( ) 三、填空题(每空1分,共10分)41. 硫酸四氨合铜(Ⅱ)的化学式是 。
无机化学试卷A

3、路易斯酸碱定义
4、酸碱指示剂
四、计算题(共20分)
1、按照电子论的观点,在以下两个反应中,哪些物种是酸?哪些物种是碱?
BF3+ F-BF4-
SO32-+S S2O32-
2、在298.2 K,10.0 L的容器中含有1.00 mol N2和3.00 mol H2,设气体为理想气,试求容器中的总压和两种气体的分压?
3、已知下列反应CO (g) + H2O(g) =CO2(g) + H2(g)在1000K时,平衡常数Kθ=1.43,若反应在压力600kPa下进行,试计算:(1)当原料气中CO:H2O =1:1时,CO的平衡转化率。(2)若CO:H2O =1:5时,CO的平衡转化率是多少?
4、用草酸标定NaOH溶液的准确浓度,称取0.2250 gH2C2O4•2H2O,溶于水后,用NaOH溶液滴定直到加入30.12 ml到达终点,求NaOH溶液的浓度。
2、系统和环境之间可以交换和,根据它们的交换情况,可以把系统分为:
、、。
3、5个热力学函数之间的关系为、、、、。
4、化学反应进行方向的判据
△rGm<0,;
△rGm>0,;
△rGm=0,。
二、解释下列名词(共20分)
热力学第一定律:
热力学能:
盖斯定律:
标准摩尔生成焓:
化学平衡:
三、简答题(共20分)
1、什么是标准状态?
2010---2011学年度第二学期《无机化学》考试试卷(A)
化生系20级化生( ຫໍສະໝຸດ 班学号:姓名:注意:考生答题不能超过装订线(含背面),否则该题无效!
题号
一
二
三
四
五
无机化学课程试卷_(A卷)

无机化学(一) 课程试卷(A卷)一、选择题( 共16题32分)1. 2 分(4653)下列四种绿色溶液,加酸后,溶液变为紫红色并有棕色沉淀产生的是………………()(A) NiSO4(B) CuCl2(浓)(C) NaCrO2(D) K2MnO42. 2 分(7459)对于H2O2和N2H4,下列叙述正确的是………………………………………………()(A) 都是二元弱酸(B) 都是二元弱碱(C) 都具有氧化性和还原性(D) 都可与氧气作用3. 2 分(3776)市场上供应的干电池中有MnO2,它的主要作用是…………………………………()(A) 导电(B) 吸收产生出来的水分(C) 参加正极反应(D) 参加负极反应4. 2 分(4392)下列各组物质的性质递变顺序正确者为……………………………………………()(A) FeCl2 < FeCl3 (熔点) (B) Pb(II) > Pb(IV) (稳定性)(C) Si < P4 (硬度) (D) Na > Al (密度)5. 2 分(3747)下面氧化还原电对的电极电势不随酸度变化的是…………………………………()(A) NO-3- HNO2(B) SO-24- H2SO3(C) Fe(OH)3 - Fe(OH)2(D) MnO-4- MnO-246. 2 分(6707)某氢电极与饱和甘汞电极(ϕ= +0.240 V)组成原电池,如若使电池电动势达到+0.299 V,则溶液的pH值是………………………………………………………………………()(A) 1 (B) 2 (C) 3 (D) 47. 2 分(1101)[Ni(en)3]2+离子中镍的价态和配位数是………………………………………………()(A) +2,3 (B) +3,6 (C) +2,6 (D) +3,38. 2 分(4545)已知:K sp(AgSCN) = 1.1 ⨯ 10-12,K sp(AgI) = 1.5 ⨯ 10-16,K sp(Ag2CrO4) = 1.0 ⨯ 10-11;则上述难溶盐与其金属组成的电对的ϕ值大小顺序为…………………………………()(A) AgSCN > AgI > Ag2CrO4(B) AgI > AgSCN > Ag2CrO4(C) Ag2CrO4 > AgSCN > AgI (D) Ag2CrO4 > AgI > AgSCN9. 2 分 (0703)在酸性溶液中用K 2Cr 2O 7溶液将10cm 3 0.10 mol ·dm -3 KI 溶液完全氧化成I 2,需消耗 K 2Cr 2O 7(式量为294) 的质量(mg)为………………………………………………………( ) (A) 49 (B) 98 (C) 0.049 (D) 0.09810. 2 分 (3797)在由Cu 2+/Cu 和Ag +/Ag 组成的原电池的正负极中,加入一定量的氨水,达平衡后[NH 3·H 2O] = 1mol ·dm -3,则电池的电动势比未加氨水前将…………………………… ( )(Cu(NH 3)+24的K 稳 = 2.1 ⨯ 1013,Ag(NH 3)+2的K 稳 = 1.1 ⨯ 107) (A)变大 (B)变小 (C) 不变 (D) 无法判断11. 2 分 (1699)CrO 5中Cr 的氧化数为 ………………………………………………………………( ) (A) 4 (B) 6 (C) 8 (D) 1012. 2 分 (3796)已知: ϕ(Fe 3+/Fe 2+) = 0.77 V , ϕ(Br 2/Br -) = 1.07 V , ϕ(H 2O 2/H 2O) = 1.78 V ,ϕ(Cu 2+/Cu) = 0.34 V , ϕ(Sn 4+/Sn 2+) = 0.15V则下列各组物质在标准态下能够共存的是……………………………………………… ( )(A) Fe 3+,Cu (B) Fe 3+,Br 2 (C) Sn 2+,Fe 3+ (D) H 2O 2,Fe 2+13. 2 分 (0720)已知 M +21+ 2e -M 1 ϕ= -2.0 V ;M +2+ e-M 2 ϕ= 0.5 VM +31+ e - M +21 ϕ= -1.0 V ; M +22+ e -M +2ϕ= 1.0 VM +41+ e -M +31 ϕ= 0.5 V ; M +32+ e -M +22 ϕ= 1.9 V下列情况中,不可能反应的是………………………………………………………………( ) (A) M 1 投入水中(B) M +21离子加到水中(C) 1 mol M +31离子加到1 dm 3的1 mol ·dm -3 M +2离子溶液中 (D) M +32离子加到含M +2离子的溶液中去14. 2 分 (1141)不具有空间异构体的是……………………………………………………………… ( )(A) [PtCl 2(NH 3)4]2+ (B) [PtCl 3(NH 3)3]+(C) [PtCl(NO 2)(NH 3)4]2+(D) [PtCl(NH 3)5]3+15. 2 分 (1454)下列各组化合物热稳定性关系正确的是…………………………………………… ( ) (A) Na 2CO 3 > Na 2SO 4 (B) K 2CO 3 > Ag 2CO 3 (C) NaHCO 3 > Na 2CO 3 (D) (NH 4)2CO 3 > ZnCO 316. 2 分 (1421)将NCl 3通入碱性溶液,其水解产物是……………………………………………… ( ) (A) NH 3和ClO - (B) NH 3和Cl -(C)NO 2-和Cl - (D)NH 4+和Cl -二、填空题 ( 共 7题 15分 )17. 2 分 (1131)已知铁的原子序数为 26,则Fe 2+在八面体场中的晶体场稳定化能(以△0 =10 Dq 表示)在弱场中是_____________ Dq ,在强场中是______________ Dq 。
无机化学试卷及答案A

线内不要答题☆《无机化学》试题(A 卷)(答案)题号一二三四五总分得分阅卷人本套试卷共3 页一、填空题(每题2分,共20分)1、根据系统与环境之间有无物质和能量的交换,可把系统分为三类,分别为敞开系统、封闭系统、孤立系统。
2、描述电子运动态的函数是波函数,又称为原子轨道。
3、共价键的类型有两种,一种以“头碰头”的方式进行轨道重叠的叫σ键,另一种是以“肩并肩”的方式进行重叠的,其重叠部分呈镜面对称,这样的键称为π键。
4.所谓的标准态指的是标准压力等于100KPa,标准浓度等于1mol/L。
5、若一系统由A态变为B态,吸热100J,对外做功50J,那么系统的热力学能变为50J 。
6、判断反应方向的热力学判据是ΔG,判断反应达到平衡的热力学条件是ΔG=0。
7、已知反应2NO(g)+O2(g) = 2NO2,其反应速率方程式为v = k[c(NO)]2[c(O2)], 当其他条件不变,将NO的浓度增加到原来的2倍,反应速率将变为原来的4;若体积扩大到原来的2倍,则反应速率变为原来的1/8 。
8、24Cr的核外电子排布式是1s22s22p63s23p63d54s1;Cr3+的外层电子排布式是1s22s22p63s23p63d3。
9、量子力学中用来描述原子核内电子运动的状态的四个量子数为主量子数、角量子数、磁量子数、自旋量子数;10、根据组成晶体的粒子的种类和粒子间作用力的不同,可以把晶体分为四种类型,分别为:金属晶体、离子晶体、分子晶体、原子晶体。
二、选择题(每题2分,共20分)1、SP2杂化轨道是指(B)。
A、分子轨道;B、原子轨道;C、化学键;D、反健;2、催化剂是通过改变反应进行的历程来加快反应速度,则催化剂的作用是(A)。
A、降低活化能;B、减小速率常数;C、增大平衡常数;D、增大碰撞频率;3、能使反应2X(g)+Y(g)→2Z(g)(ΔHθ=45KJ·mol-1)的平衡向左移动的条件是(D)A、高温低压;B、低温高压;C、高温高压;D、低温低压;4、已知反应H2O H+ + OH―的K w 和HAc H+ + Ac―的K a (HAc),则反应Ac―+H2O HAc + OH―的K(Ac―)为(C)A、K W-K a(HAc);B、K W+K a(HAc);C、K W/K a(HAc);D、K a(HAc)/K W;5、对于某吸热且熵增的反应,下述说法正确的是(A)A、高温下能自发;B、低温下可能自发;C、都不能自发;D、都能自发;6、一个可逆化学反应达到平衡的标志是(D)A.各反应物和生成物的浓度相等;B.各反应物和生成物的浓度是常数;C.生成物浓度大于反应物的浓度;D.生成物和反应物浓度不再随时间的变化而改变;线内不要答题☆7、质量作用定律适用于(C)A.任意反应; B.复杂反应;C.基元反应; D.吸热反应;8、对于一个化学反应,下列说法正确的是(D)A.θmrS∆越小,反应速率越快;B. θmrH∆越小,反应速率越快;C.活化能越大,反应速率越快;D.活化能越小,反应速率越快;9、在水溶液中,配位解离平衡与沉淀溶解平衡竞争反应的平衡常数是( C )A. θSK/θfK B.θfK/θSK C.θfK·θSK10、NH3是四面体构型,它的轨道模型属于(B)A.SP杂化;B.SP3不等性杂化;C.SP2杂化;D.SP3等性杂化;四、判断下列各题是否正确,若正确请在题后的( )里打“√”若错误请在( )里打“x”(每题1分,共10分)1、选择合适的催化剂,提高活化能,加快反应速率。
南京晓庄学院无机化学课程期末考试试卷A

南京晓庄学院⽆机化学课程期末考试试卷A南京晓庄学院⽆机化学课程考试试卷A2006–2007学年度第⼀学期化学院(系)06 级化本(2)共8页教研室主任审核签名:院(系)主任审核签名:命题教师:郑波校对⼈:班级姓名学号得分⼀、选择题(每题2分,共计30分)1、相同的温度、压⼒条件下,1g下列各种物质,占体积最⼤的是 ( ) (原⼦量∶H 1,C 12,O 16,Ne 20,S 32)(A) ⼄烷(B) 氖(C) 氧(D) 硫化氢2、H2 (g)+1/2O2 (g) →H2 O(l) T=298K的Q p与Q v 之差(kJ·mol-1 )是 ( )(A) -3.7 (B) 3.7 (C) 1.2 (D) -1.23、在标准压⼒和 373 K下,⽔蒸⽓凝聚为液态⽔时体系中应是( )(A) ΔH = 0 (B) ΔS = 0 (C) ΔG = 0 (D) ΔU = 04、反应速率常数 k 的量纲为 dm3·mol-1·s-1时,反应是( )(A) 2 级反应 (B) 1 级反应(C) 1/2 级反应(D) 1.5 级反应5、⼀级反应 A → B的半衰期(t 1/2)在300K时是1.00×10-4 s,在400K时是1.00×10-5 s,该反应的活化能(J·mol-1 )是( )(A) 2.29×104(B) 5.29×104(C) 9.97×103 (D) 19.16、298 K 时,反应BaCl2 ·H2O(s) =BaCl2 (s) + H2O(g) 达平衡时p(H2O)= 330 Pa,反应的△r GФm为 ( )(A)-14.3kJ ·mol -1(B)+14.3kJ ·mol -1(C)+139kJ ·mol -1 (D)-141kJ ·mol -17、已知 CO(g)=C(s)+21 O2 (g) 的△r H Фm >0,△r S Фm <0,则此反应( ) (A) 低温下是⾃发变化(B) ⾼温下是⾃发变化 (C) 低温下是⾮⾃发变化,⾼温下是⾃发变化 (D) 任何温度下都是⾮⾃发的8、已知0.01 mol ·dm -3的弱酸HA 溶液有 1 %的电离,它的电离常数约为 ( )(A) 10-2(B) 10-6(C) 10-4 (D) 10-59、在反应 BF 3 + NH 3 → F 3 BNH 3中,BF 3为 ( )(A) Arrhenius 碱(B) Bronsted 酸(C) Lewis 碱(D) Lewis 酸10、已知 K Фsp[ Mg(OH)2]=1.2×10-11、K Фb (NH 3)= 1.76×10-5,要使0.40mol ·dm -3 MgCl 2与 0.20 mol ·dm -3氨⽔等体积混合后不产⽣沉淀,其混合液中需 NH 4Cl 最⼩的浓度为 ( )(A) 4.4 mol ·dm -3(B) 0.44 mol ·dm -3(C) 2.3 mol ·dm -3(D) 0.23 mol ·dm -311、某溶液中含有 KCl ,KBr 和K 2 CrO 4其浓度均为 0.010 mol ·dm -3,向该溶液中逐滴加⼊0.010 mol ·dm -3的AgNO 3溶液时,最先和最后沉淀的是 ()(已知: K Фsp (AgCl )=1.56×10-10,K Фsp (AgBr )=7.7×10-13, K Фsp ( Ag 2CrO 4)=9.0×10-12)(A) AgBr 和Ag 2CrO 4 (B) Ag 2CrO 4和AgCl (C) AgBr 和AgCl (D)⼀齐沉淀12、⽤Nernst ⽅程式计算Br 2/Br -电对的电极电势,下列叙述中正确的是( ) (A) Br 2的浓度增⼤,?增⼤(B) Br -的浓度增⼤,?减⼩(C) H +浓度增⼤,?减⼩(D) 温度升⾼对?⽆影响13、由下列锰元素的电势图判断其中不能稳定存在,可发⽣岐化反应的物是()MnO 4—V56.0MnO 42—V26.2MnO 2V95.0Mn3+V51.1 Mn2+V18.1-Mn(A ) Mn 3+和Mn 2+(B ) Mn 3+和MnO 42—(C ) Mn 3+和MnO 2(D ) MnO 2和MnO 42—14、下列各组量⼦数中错误的是()(A ) n=3, l=2, m=0, m s =+21(B) n=2, l=2, m=-1, m s =﹣21 (C) n=4, l=1, m=0, m s =﹣21(D) n=3, l=1, m=-1, m s =+2115、下列反应中,△r H m 与产物的△f H m 相同的是()(A)2H 2(g)+O 2(g)→2H 2O(l) (B)NO(g)+1/2O 2(g) →NO 2(g) (C)C(⾦刚⽯)→C(⽯墨) (D) H 2(g)+1/2O 2(g) →H 2O(g)⼆、填空题(每题2分,共计30分)1、在_____________________条件下绝⼤多数⽓体接近理想状态。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
无机化学试卷A(8)班级姓名分数一、选择题( 共14 题28 分)1. 2 分(0806)0806某化学反应的速率常数的单位是mol·dm-3·s-1时,则该化学反应的级数是……()2. (A) 3/22 分(3879)(B) 1 (C) 1/2 (D) 03879对于一个确定的化学反应来说,下列说法中正确的是………………………………((A) r G m 越负,反应速率越快(B) r H m 越负,反应速率越快(C) 活化能越大,反应速率越快(D) 活化能越小,反应速率越快)3. 2 分(0904)0904下列各组量子数中,相应于氢原子Schrödinger 方程的合理解的一组是………… ()n l m m s(A)(B)(C)(D) 3245232+1-4+2- 12+ 12- 12+ 124. 2 分(0592)0592当一个化学反应处于平衡时,则………………………………………………………((A) 平衡混合物中各种物质的浓度都相等(B) 正反应和逆反应速率都是零(C) 反应混合物的组成不随时间而改变(D) 反应的焓变是零)5. 2 分(0597)0597N2(g) + 3H2(g) 2NH3(g),反应达到平衡后,把p NH 3,p H 2各提高到原来的2 倍,p N 2不变,则平衡将会………………………………………………………………………()(A) 向正反应方向移动(C) 状态不变(B) 向逆反应方向移动(D) 无法确知已知:Cu 2+────Cu +────Cu6.2 分 (3665) 3665pH 为 9.40 的溶液中氢氧根离子浓度为………………………………………………( )(A) 4.0 ⋅ 10-10 mol·dm -3(C) 4.0 ⋅ 10-6 mol·dm -3(B) 2.5 ⋅ 10-9 mol·dm -3 (D) 2.5 ⋅ 10-5 mol·dm -37.2 分 (0698) 0698某溶液中含有 0.01 mol·dm -3 AgNO 3、0.01 mol·dm -3 Sr(NO 3)2 和 0.01 mol·dm -3 Pb(NO 3)2、 0.01 mol·dm -3 Ba(NO 3)2 四种盐,向该溶液中逐滴加入 K 2CrO 4 溶液时,则沉淀的先后顺序 是…………………………………………………………………………………………… ((A) Ag 2CrO 4,PbCrO 4,SrCrO 4,BaCrO 4 (B) PbCrO 4,Ag 2CrO 4,SrCrO 4,BaCrO 4 (C) SrCrO 4,PbCrO 4,Ag 2CrO 4,BaCrO 4 (D) PbCrO 4,Ag 2CrO 4,BaCrO 4,SrCrO 4(注:K sp (Ag 2CrO 4) =1.1 ⋅ 10-12,K sp (PbCrO 4) = 1.8 ⋅ 10-14K sp (BaCrO 4) = 1.2 ⋅ 10-10,K sp (SrCrO 4) = 2.2 ⋅ 10-5))8.2 分 (0713) 0713A 、B 、C 、D 四种金属,将 A 、B 用导线连接,浸在稀硫酸中,在 A 表面上有氢气放 出,B 逐渐溶解;将含有 A 、C 两种金属的阳离子溶液进行电解时,阴极上先析出 C ;把 D置于 B 的盐溶液中有 B 析出。
这四种金属还原性由强到弱的顺序是………………() (A) A > B > C > D (C) C > D > A > B (B) D > B > A > C (D) B > C > D > A9.2 分 (6704) 67040.15 V 0.52 V则 在水 溶液 中 Cu 2+、 Cu + 的 稳定 性大 小为…………………………………………………………………………………………… ( )(A) Cu 2+ 大,Cu + 小 (C) 两者稳定性相同 (B) Cu + 大,Cu 2+ 小 (D) 无法比较*.2 分 (1003) 1003极化能力最强的离子应具有的特性是……………………………………………… ( )(A) 离子电荷高、离子半径大 (C) 离子电荷低、离子半径小11. 2 分 (4030) 4030(B) 离子电荷高、离子半径小 (D) 离子电荷低、离子半径大关于晶格能,下列说法中正确的是……………………………………………………( (A) 晶格能是指气态阳离子与气态阴离子生成 1 mol 离子晶体所释放的能量 (B) 晶格能是由单质化合成 1 mol 离子化合物时所释放的能量)=CO(g) (2)C(金刚石)+O(g)=CO(g)m / =CO(g) (C) 晶格能是指气态阳离子与气态阴离子生成离子晶体所释放的能量 (D) 晶格能就是组成离子晶体时,离子键的键能12.2 分 (0199) 0199在 标 准 状 态 下 , 50 dm 3 某 气 体 为 100 g, 则 该 气 体 的 相 对 分 子 质 量 为 ---------------------()13. (A) 342 分 (0178) (B) 45(C) 56(D) 900178在等温条件下, 1.00 dm 3 密闭容器中装有 A 和 B 的混合气体 , 其总压力为 100 kPa, 气体 A 的分压为 50 kPa, 则下列说法中不正确的是---------------------------------------()(A) A 的摩尔分数为 0.50(B) A 与 B 的物质的量相等(C) A 的分体积为 0.50 dm2 分 (0408) 14. 0408在一定温度下:3(D) A 与 B 物质的量之比为 1∶2(1) C(石墨) + O 2(g) 2ΔH 12 2(3) C(石墨)= C(金刚石)ΔH 2ΔH 3 = 1.9 kJ·mol -1其中ΔH 1 和ΔH 2 的关系是…………………………………………………………………()(A) ΔH 1>ΔH 2 (C) ΔH 1=ΔH 2二、填空题 ( 共 7 题20 分 )(B) ΔH 1<ΔH 2 (D) 不能判断 15. 2 分 (3127) 3127在标准状况下, 气体 A 的密度为 0.08 g·dm -3, 气体 B 的密度为 2 g·dm -3,则气体 A 对气体 B 的相对扩散速率为__________________ 。
16. 34232 分 (3423) 已知在 25℃时CO(g)CO 2(g) H 2O(g) f GkJ·mol -1-137.2-394.4-228.6则反应:CO(g) + H 2O(g)2+ H 2(g),在 25℃和 101.3 kPa 下的 r G m 为___________________________________。
17.2 分 (0594)=HO(g)一定温度下,反应 PCl 5(g)PCl 3(g) + Cl 2(g)达到平衡后,维持温度和体积不变, 向容器中加入一定量的惰性气体,反应将___________ 移动。
18.2 分 (6639)6639选择以下正确答案,填入相应的空格内: (A) 弱酸及其盐的浓度 (C) 弱酸及其盐的浓度比 (B) 弱酸盐浓度 (D) 弱酸的 K a 值对于 HAc-NaAc 缓冲体系:(1) 决定体系 pH 值的主要因素是________________________________________; (2) 影响上述体系 pH 值变动 0.1 ~ 0.2 个单位的因素是______________________; (3) 影响缓冲容量的因素是______________________________________________; (4) 影响对外加酸缓冲能力大小的因素是_________________________________。
19. 07725 分 (0772) 将 Ni + 2Ag += 2Ag + Ni氧化还原反应设计为一个原电池。
则电池的负极为__________________________,正极为______________________________, 原电池符号为________________________________________________________。
已知 ∏ (Ni 2+ / Ni) = -0.25 V , ∏ (Ag + / Ag) = 0.80 V ,则原电池的电动势 E 为 ___________, r G m 为______________,该氧化还原反应的平衡常数为________________。
20.2 分 (0938) 0938第 50 号元素的原子的电子排布是_____________________________________________ 它位于第_______周期____________族,其化学符号是________。
21.5 分 (0981) 098124 号元素 Cr 的电子构型为___________________________, 价层电子的四个量子数分 别是_______________________________________________________________________。
三、计算题 ( 共 4 题30 分 ) 22. 5 分 (3451) 3451已知下列数据(298 K)H 2(g) + 12 O 2(g)2r H m 1 = -242 kJ·mol -1 ① H 2(g) ↓ 2H(g) r Hm 2 = 436 kJ·mol -1 ②O 2(g) ↓ 2O(g)r Hm 3= 498 kJ·mol-1③通过计算确定反应 H 2O(g) ↓ 2H(g) + O(g) 是吸热还是放热?PCl 3(g)+Cl 2(g)的K p =11.5。
取2.00molPCl 5与1.00=;2FeO(s)+H(g)=2Fe(s)+3HO(g)。
23. 10 分 (0524) 0524300℃ 时反应 PCl 5(g)mol PCl 3 相混合,在总压为 200 kPa 下反应达平衡,求平衡混合物中各组分的分压。
24.5 分 (3624) 3624试用近似计算说明在 0.1 mol·dm -3 醋酸溶液中通入 H 2S 达饱和(约 0.1 mol·dm -3 H 2S), 能否使溶液中 0.1 mol·dm -3 Mn 2+ 以 MnS 形式沉淀出来? (已知:K (HAc) = 1.8 ⋅ 10-5;K sp (MnS) = 1.4 ⋅ 10-15,H 2S 的 K 1 = 1.1 ⋅ 10-8,K 2 = 1.0 ⋅ 10-14 )25. 10 分 (0727) 0727若溶液中 [ MnO 4 ]= [Mn 2+] 问:(1) pH = 3.00 时, MnO 4 能否氧化 Cl ,Br ,I ? (2) pH = 6.00 时, MnO 4 能否氧化 Cl ,Br ,I ?已知: ∏ ( MnO 4 / Mn 2+) = 1.51 V , ∏ (Cl 2 / Cl ) = 1.36 V∏ (Br 2 / Br ) = 1.08 V , ∏ (I 2 / I ) = 0.54 V四、问答题 ( 共 5 题25 分 ) 26. 5 分 (3436) 3436某教科书中有这样一道题:由铁矿石生产铁有两种可能的途径:(1) Fe 2O 3(s) + 32 C(s)32(2)2 3 2 2 请通过热力学计算说明上述反应,哪个可以在较低温度下进行? 有某学生通过热力学计算得到:第一途径: r H m = 231.93 kJ·mol -1, r S m = 276.32 J·mol -1·K -1, r G m =149.43 kJ· mol -1;第二途径: r H m = 96.71 kJ·mol -1, r S m = 138.79 J·mol -1·K -1, r G m = 55.23 kJ·mol -1。
