芳香化合物概念
第十章 芳香族化合物

芳基 (Aryl)
1、普通命名法
邻氯苯甲醚 间甲苯酚 对甲苯甲酸 连三甲苯 偏三甲苯 间三甲苯
2、系统命名法
1,2-二溴苯
3-硝基溴苯
3-硝基苯甲醛
2-氨基-5-羟基苯甲醛 3-氨基-5-溴苯酚
三、单环芳烃的物理性质
一般为无色有芳香气味的液体,不溶于水,相对密度在 0.86-0.93之间,燃烧时火焰带有较浓的黑烟。沸点随相对 分子质量升高而升高。熔点除与相对分子质量有关外,还 与结构有关,通常对位异构体由于分子对称,熔点较高。 芳烃是一种良好的溶剂,但具有一定的毒性。常见单环 芳烃的物理常数P455表11-1
代反应等。
第三阶段:将具有芳香特性的化合物称为芳香化合物。
非苯芳香烃
3、苯及苯的表达方式
• 1825年 • 1857年 • 1858年
法拉第发现了苯。 凯库勒提出碳四价。 凯库勒提出苯分子具有环状结构。
勇于开始,才能找到成 功的路
Kekule’式
问题?
实际得到三种化合物
1865年 提出摆动双键学说
2°当引入的烷基为三个碳以上时,引入的烷基会发 生碳链异构现象。
3°烷基化反应不易停留在一元阶段,通常在反应中 有多烷基苯生成。
4°苯环上已有–NO2、-SO3H、-COOH、-COR等取 代基时,烷基化反应不在发生。因这些取代基都是 强吸电子基,降低了苯环上的电子云密度,使亲电 取代不易发生。例如,硝基苯就不能起付—克反应 ,且可用硝基苯作溶剂来进行烷基化反应。 5°烷基化试剂也可是烯烃或醇。
TNT十分稳定。与硝酸甘油不同,它对于摩擦、震动等 都不敏感。需要雷管引爆。每公斤TNT炸药可产生4200 千焦的能量。虽然,它的燃烧热低于脂肪和糖,但由于 能够迅速地释放能量,同时不需要消耗额外的氧气。从 而引发爆炸。现在常用吨TNT的爆炸当量来衡量核爆炸 、地震、行星撞击等大型反应时的能量。
有机化学基础知识点芳香性与芳香烃的性质

有机化学基础知识点芳香性与芳香烃的性质有机化学基础知识点——芳香性与芳香烃的性质有机化学是研究有机物质及其反应机理的一门学科,其中芳香性与芳香烃是其中重要的知识点之一。
本文将着重介绍芳香性以及芳香烃的性质,帮助读者更好地理解有机化学中的这一概念。
一、芳香性的定义与特点芳香性是指具有特殊结构和性质的有机化合物所表现出的香味和稳定的π电子结构。
根据芳香性的定义,芳香性化合物需要满足以下几个条件:1. 分子结构中含有一个或多个芳环(由6个共轭π电子组成的环状结构);2. 芳环中每个原子都以杂化sp2形式存在,磁性势能相对稳定;3. 芳环中的每个杂化的p轨道上都有一个未被配对的π电子。
值得注意的是,非芳香性化合物虽然可能具有香味,但其分子结构不符合芳香性的定义。
二、芳香烃的分类与性质芳香烃是一类基础的有机化合物,其分子中至少含有一个芳环。
根据芳香烃分子中芳环的个数及其它官能团,芳香烃可以分为以下几类:1. 单核芳香烃:只含有一个芳环的芳香烃。
例如,苯(C6H6)是最简单的芳香烃,其分子结构中含有一个六元环。
2. 多核芳香烃:含有两个或多个连接在一起的芳环的芳香烃。
最常见的多核芳香烃是萘(C10H8),它由一个苯环和一个呈共轭连结的五元环组成。
3. 取代芳香烃:分子中的芳环上存在取代基的芳香烃。
通过对芳环中的氢原子进行取代,可以获得各种不同性质和用途的化合物。
芳香烃的一些重要性质包括:1. 稳定性:芳香烃具有相对较高的稳定性,这是因为芳香烃分子中的共轭π电子系统能够稳定结构和分子。
2. 可溶性:大多数芳香烃在非极性溶剂中具有较好的溶解性,但在水中溶解度较低。
3. 反应性:芳香烃在化学反应中常常表现出亲电取代反应、脱氢反应等特性。
三、应用与实际意义芳香烃是有机化学中重要的化合物类别之一,其应用领域非常广泛。
以下是一些芳香烃的应用和实际意义:1. 燃料:芳香烃类化合物广泛应用于燃料行业,用作汽车燃料和燃气等能源。
5芳香族化合物

2) 苯本身不能和酸性 KMnO4 溶液反应,不会与高锰酸钾反应褪色,与溴水混合只会发生萃取,而苯 及其衍生物中,只有在苯环侧链上的取代基中与苯环相连的碳原子与氢相连的情况下才可以使高锰酸
钾褪色(本质是氧化反应),这一条同样适用于芳香烃(取代基上如果有不饱和键则一定可以与高锰 酸钾反应使之褪色)。 注意:①是仅当取代基上与苯环相连的碳原子; ②这个碳原子要与氢原子相连 (成键) 。 至于溴水, 苯及苯的衍生物以及饱和芳香烃只能发生萃取 (条 件是取代基上没有不饱和键,不然依然会发生加成反应)。 1、能证明苯分子中不存在单双键交替的理由是 ( ) A 苯的邻位二元取代物只有一种 B 苯的间位二元取代物只有一种 C 苯的对位二元取代物只有一种 D 苯的邻位二元取代物有二种 ) 2、苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( ①苯不能使溴水褪色 ②苯不能使酸性高锰酸钾溶液褪色 ③苯在一定条件下既能发生取代反应,又能发生加成反应 ④经测定,邻二甲苯只有一种结构 ⑤经测定,苯环上碳碳键的键长相等,都是1.40× 10-10m A.①②④⑤ B.①②③⑤ C.①②③ 3、下列物质中所有原子都有可能在同一平面上的是 ( )
8. 甲苯的化学性质:化学性质活泼,与苯相像。可进行氧化、磺化、硝化和歧化反应,以及侧链氯化 反应。甲苯能被氧化成苯甲酸。 (1) 硝化反应: CH3 CH3 +3HO-NO2 O2N-NO2+3H2O NO2 甲苯与浓硝酸在浓硫酸的催化( 100 摄氏度)下可发生反应,生成三硝基甲苯。又名 TNT ,是一种黄 色针状晶体。不溶于水。它是一种烈性炸药。用于国防、开矿、筑路等。 (2) 取代反应: (3) 加成反应: 课外小阅读(一) :苯的历程 苯最早是在 19 世纪初研究将煤气作为照明用气时合成出来的。 1803 年 -1819 年 G.T.Accum 采用同样方法制出了许多产品,其中一些样品用现代的分析方法检测 出有少量的苯。然而,一般认为苯是在 1825 年由麦可 · 法拉第发现的。他从鱼油等类似物质的热裂解 产品中分离出了较高纯度的苯,称之为 “ 氢的重碳化物 ” ( Bicarburetofhydrogen )。并且测定了苯的一 些物理性质和它的化学组成,阐述了苯分子的碳氢比。 1833 年, Milscherlich 确定了苯分子中 6 个碳和 6 个氢原子的经验式( C 6 H 6 )。弗里德里希 · 凯库 勒于 1865 年提出了苯环单、双键交替排列、无限共轭的结构,即现在所谓 “ 凯库勒式 ” 。 据称他是因为梦到一条蛇咬住了自己的尾巴才受到启发想出 “ 凯库勒式 ” 的。他又对这一结构作出 解释说环中双键位置不是固定的,可以迅速移动,所以造成 6 个碳等价。他通过对苯的一氯代物、二 氯代物种类的研究,发现苯是环形结构,每个碳连接一个氢。 1845 年德国化学家霍夫曼从煤焦油的轻馏分中发现了苯,他的学生 C.Mansfield 随后进行了加工 提纯。后来他又发明了结晶法精制苯。他还进行工业应用的研究,开创了苯的加工利用途径。 1861 年,化学家约翰·约瑟夫·洛斯密德( Johann Jasef Loschmidt )首次提出了苯的化学键,双 键交替结构,但他的成果未受到重视。 1865 年, 弗里德里希 · 凯库勒在论文 《关于芳香族化合物的研究》 中, 再次确认了四年前苯的结构, 为此,苯的这种结构被命名为 “ 凯库勒式 ” 。他对这一结构作出解释说环中双键位置不是固定的,可以 迅速移动,所以造成 6 个碳等价。他通过对苯的一氯代物、二氯代物种类的研究,发现苯是环形结构, 每个碳连接一个氢。 此外,詹姆斯 · 杜瓦发现了一种苯的类似物;命名为 “ 杜瓦苯 ” ,现已被证实,可由苯经光照得到。 大约从 1865 年起开始了苯的工业生产。最初是从煤焦油中回收。随着它的用途的扩大,产量不断 上升,到 1930 年已经成为世界十大吨位产品之一。 课外小阅读(二):苯的工业制备 苯可以由含碳量高的物质不完全燃烧获得。自然界中,火山爆发和森林火险都能生成苯。苯也存 在于香烟的烟中。煤干馏得到的煤焦油中,主要成分为苯。 直至二战, 苯还是一种钢铁工业焦化过程中的副产物。 这种方法只能从 1 吨煤中提取出 1 千克苯。 1950 年代后,随着工业上,尤其是日益发展的塑料工业对苯的需求增多,由石油生产苯的过程应运而生。 现在全球大部分的苯来源于石油化工。工业上生产苯最重要的三种过程是催化重整、甲苯加氢脱烷基 化和蒸汽裂化。 从煤焦油中提取:在煤炼焦过程中生成的轻焦油含有大量的苯。这是最初生产苯的方法。将生成 的煤焦油和煤气一起通过洗涤和吸收设备, 用高沸点的煤焦油作为洗涤和吸收剂回收煤气中的煤焦油, 蒸馏后得到粗苯和其他高沸点馏分。粗苯经过精制可得到工业级苯。这种方法得到的苯纯度比较低, 而且环境污染严重,工艺比较落后。 从石油中提取:在原油中含有少量的苯,从石油产品中提取苯是最广泛使用的制备方法。
第七章 芳香烃(2)
定位效应包括两方面:(1)基团所进入的位置; (2)反应的速度快慢。
42
CH3
H2SO4+ HNO3
30 ℃
CH3 NO2
( O + P = 96.5 %)
56.5 %
CH3
NO2
40 %
NO2
H2SO4+ HNO3
90~100 ℃
(O + P = 6.7%)
NO2
NO2
93.2%
NO2 NO2
6.4%
结构特点:与苯环直接相连的原子多数含有未共用 电子对。
44
2. 间位定位基—第二类定位基(钝化 苯环)
强致钝基:-N+R3, -NO2, -CX3 中等致钝基: -CN, -SO3H, -COR(H), -CO2H, -CCl3 弱致钝基:-COOR,-CONHCH3, -CONH2, -NH3, etc.
H
O
X
CR
卤代反应 NO2
SO3H
R 酰基化 反应
硝化反应
20
磺化反应 烷基化反应
反应机理: 亲电取代反应
sp2 + E+
E+ 慢
sp3
H -H+
+
E
sp2 E
亲电试剂 络合物
络合物
产物
用极限式表示中间体 络合物 :
H
H
E
E
+
+
21
+H E
1.卤代反应
卤 素:Cl2 、Br2 催化剂:FeX3 AlCl3 ZnCl2或 Fe
具有三个相同烃基的取代苯也有三种异构体。如:
CH3 CH3
芳香性化合物精华版

2
芳香性是指芳香族化合物所特有的性质。芳香 族化合物是指苯和类苯化合物,这是一类具有 高度不饱和性的环状化合物。芳香性的含义是 在不断发展的,经过一个由浅到深的过程。
1. 最初芳香性的定义着重于苯一类的环状共轭 体系的化学性质,这类化合物它们具有特殊的 稳定性,不易发生氧化或加成反应,容易发 生亲电取代反应。
芳香性
2014-4-21
22
22
2. 芳性离子 某些环烃没有芳香性,转变成离子(正或负离子) 后,有可能具有芳香性.
2K 2e
π 电子数
2
2
6
芳香性
6
6
2014-4-21
23
23
3.非苯稠环
蓝烃:天蓝色晶体,是一种稳定的化合物。它是五 元环的环戊二烯和七元环的环庚三烯稠合而成的, 分子结构中不含有苯环。结构如下: 它含有10个π 电子,符合休克尔规则, 所以有芳香性。 实际上,它的七元环带有 正电荷,五元环带有负电 荷,是一个典型的极性分 子,结构也可以表示如下:
2014-4-21 14
轮 烯
CmHm的 环状烯烃。 当m=2k+1(奇数)时,为自由基,不稳定。 当m=2k(偶数)时,是稳定的环状共轭多烯
具有C2kH2k分子式的环状共轭多烯称:轮烯。
多环芳烃电子数的计算方法 1954年,Platt提出了周边修正法,对于多环芳烃 可以忽略中间的双键而直接计算外围的电子数。 对休克尔规则进行了完善和补充。 (1) 经典结构式的写法 画经典结构式时,应使尽量多的双键处在轮烯上, 处在轮烯内外的双键写成其共振的正负电荷形式, 将出现在轮烯内外的单键忽略后,再用休克尔规 则判断。
NH2 + H 2N C
NH2 C + NH2
芳香族和脂肪族的化学式

芳香族和脂肪族的化学式1. 引言在有机化学中,芳香族和脂肪族是两个重要的化学类别。
它们具有不同的结构和性质,对于理解有机化合物的特性和反应机理至关重要。
本文将从以下几个方面对芳香族和脂肪族进行详细介绍:定义、结构、性质以及常见的化学反应。
同时,我们还将给出一些具体的例子来帮助读者更好地理解这两个概念。
2. 芳香族化合物2.1 定义芳香族化合物是一类具有特殊稳定性和独特电子结构的有机分子。
它们通常含有一个或多个苯环(由六个碳原子构成)。
苯环中每个碳原子与相邻碳原子共享一个π电子。
2.2 结构芳香族化合物可以通过以下结构式表示:C6H6这里,六个碳原子形成一个环状结构,并且每个碳原子上都连接一个氢原子。
2.3 性质芳香族化合物具有以下特点:•稳定性:芳香族化合物的稳定性比脂肪族化合物高,这主要归因于苯环中的共轭π电子体系。
这种稳定性使得芳香族化合物在许多有机反应中能够起到重要的催化剂和中间体的作用。
•不饱和性:芳香族化合物由于含有共轭π电子体系,因此具有较高的不饱和度。
这也使得它们在一些加成反应中表现出与脂肪族化合物不同的行为。
•溶解性:由于芳香族化合物通常是非极性分子,它们在非极性溶剂(如苯、甲苯等)中溶解度较高,而在极性溶剂(如水)中溶解度较低。
2.4 化学反应芳香族化合物可以参与多种重要的有机反应,其中一些包括:•取代反应:芳香族化合物可以通过取代反应引入新的基团。
例如,苯可以与卤代烷发生取代反应生成取代苯衍生物。
•加成反应:尽管芳香族化合物通常不会发生加成反应,但通过使用适当的反应条件和催化剂,它们也可以参与加成反应。
例如,芳香烃可以与亚硝酸盐反应生成芳香族亚硝基化合物。
•氧化反应:芳香族化合物可以通过氧化反应引入氧原子。
例如,苯可以与过氧化氢反应生成苯酚。
3. 脂肪族化合物3.1 定义脂肪族化合物是指由碳和氢组成的有机分子。
它们通常是直链或支链状的,并且不含苯环。
3.2 结构脂肪族化合物的结构式通常表示为:CnH2n+2这里,n代表碳原子的数量,每个碳原子上连接两个氢原子。
芳香族化合物

芳香族化合物1.芳香族化合物:分子中含有苯环的有机化合物叫做芳香族化合物。
历史上曾将一类从植物胶中取得的具有芳香气味的物质称为芳香族化合物。
但根据气味分类并不科学,现在是指分子中至少含有一个苯环,具有与开链化合物或脂环烃不同的独特性质的一类化合物。
如苯、萘、蒽及其衍生物。
它包括芳香烃及其衍生物,如卤代芳香烃、芳香族硝基化合物、芳香醇、芳香酸等。
最初是指分子中含有苯环的化合物。
19世纪中叶,化学工作者发现有相当多的有机化合物具有一些特别的性质,它们的分子式中氢原子与碳原子之比往往小于1,但是它们的化学性质却不像一般的不饱和化合物。
例如它们不容易起加成反应而容易起取代反应,这些化合物中许多有芳香气味,有些是从香料中提取出来的,因此当时称它们为芳香族化合物。
后来发现芳香族化合物是苯分子中一个或多个氢原子被其他原子或原子团取代而生成的衍生物。
有些化合物可以看作是由苯通过两个或两个以上的碳原子并连起来的多环体系,它们也属于芳香族化合物,如萘和蒽等。
20世纪30年代以后,芳香族化合物的含义又有了进一步的发展。
有些化合物不含苯环,但具有芳香族化合物的某些性质,例如:酚酮、二茂铁等都能发生取代反应,这些化合物是非苯芳香族化合物。
2.芳香烃:简称“芳烃”,通常指分子中含有苯环结构的碳氢化合物。
是闭链类的一种。
具有苯环基本结构,历史上早期发现的这类化合物多有芳香味道,所以称这些烃类物质为芳香烃,后来发现的不具有芳香味道的烃类也都统一沿用这种叫法。
例如苯、萘等。
芳香烃根据结构的不同可分为三类:①单环芳香烃即苯的同系物;②稠环芳香烃,如萘、蒽、菲等;③多环芳香烃,如联苯、三苯甲烷。
主要来源于石油和煤焦油。
芳香烃在有机化学工业里是最基本的原料。
现代用的药物、炸药、染料,绝大多数是由芳香烃合成的。
燃料、塑料、橡胶及糖精也用芳香烃为原料。
3.苯(C6H6)在常温下为一种无色、有甜味的透明液体,并具有强烈的芳香气味。
苯可燃,有毒,也是一种致癌物质。
有机化学 8
H
H
H
H
H H
H
H
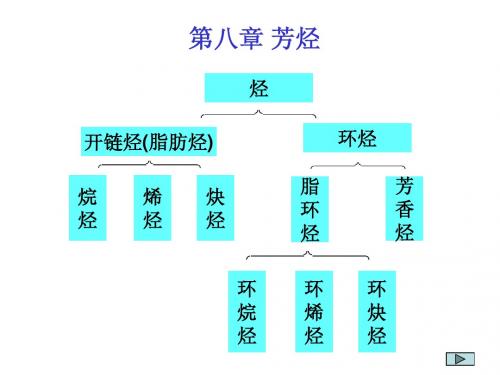
KekuléFormulation of Benzene
However, this proposal suggested isomers of the kind shown were possible. Yet, none were ever found. X X X H
H
H
H
H
E
20%
如果不考虑取代基的影响,仅从统计规律的角度来分 析,邻对位产物应为60%,间位产物为40%。
邻对位定位基:邻对位产物>60%, G为邻对位定位基。
间 位 定 位 基:间位产物>40%, G为间位定位基。
取代基的定位效应:已有的基团对后进入基团进 入苯环的位置产生制约作用,这种制约作用称为 取代基的定位效应。
为芳香化合物。
第三阶段:将具有芳香特性的化合物称
为芳香化合物。
芳香性的概念
1 C/H的比例高。 2 具有平面和接近平面的环状结构。
3 键长接近平均化。
4 在核磁共振谱中,环外氢的化学位移明显移向低 场,环内氢的化学位移明显移向高场。 5 化学性质稳定,易发生亲电取代而不易发生加成。
第二节 芳香烃的来源 干馏
第三节 苯及其衍生物的分类和命名
苯 (Benzen)
苯基 (phenyl) 苯基 (Ph) (C6H5-)
苄基 (benzyl)
芳基 (Aryl)
1. 单环芳香烃 分子内只含有一个苯环。 命名原则:
(1). 苯的同系物时以苯做母体;
甲苯
乙苯
异丙苯
(2). 苯环上连有不饱和基团,以苯环做取代基;
CHO
COOH
芳香化合物

AlCl3,C uCl C H O
+C O+H C l
+ H C l
△
21
Organic Chem
University of Science and Technology of China
二、苯的加成反应:
1. 加H2:
Ni +3 H2
180~250C
OH
OH
H2
用于制备环己烷衍生物
O NH2OH
2.硝化
浓 H 2SO 4
+ HNO3
浓 H 2SO 4
+发烟 HNO3
CH3 浓 H 2SO 4 O 2N
+ HNO3
进攻质点:
NO2
NO2
NO3 CH3
NO2
TNT NO2
HONO2 +2H2SO4
H3O++2HSO4- ++NO2 硝鎓离子
NO2+BF4- , NO2+CLO4-, CH3COO-NO2+ 等也可以作为硝化剂
二、苯的结构的现代理论:
分子轨道理论:
H H 139 sp2 H
120o
H
H
H
六个p原子轨道线性组合成分子轨道:
Ψ6=0.408(-φ1+φ2-φ3+φ4-φ5+φ6) Ψ5=0.500(φ2-φ3+φ5-φ6) Ψ4=0.289(-2φ1+φ2+φ3-2φ4+φ5+φ6) Ψ3=0.289(2φ1+φ2-φ3-2φ4-φ5+φ6) Ψ2=0.500(φ2+φ3-φ5-φ6) Ψ1=0.408(φ1+φ2+φ3+φ49+φ5+φ6)
芳香烃与芳香化合物的合成与反应

医药领域
芳香烃在药物合 成中具有重要作
用
● 02
第2章 芳香烃的合成方法
传统芳烃合成方 法
传统芳烃的合成方法 涵盖了煤焦油提取、 芳香烃氢化和芳香化 等过程。然而,这些 方法存在效率低、环 境污染等问题,需要 进一步改进和优化。
现代芳烃合成技术
催化裂解
高效分解原料
芳香硫醚
含硫芳香化合物 的合成
应用实例
01 医药化学
药物合成
02 材料科学
新材料研究
03
● 04
第四章 芳香化合物的物理性 质
芳香化合物的熔点和沸点
分子结构影 响
熔点和沸点相关 性
分子间作用 力
相互作用对性质 影响
芳香化合物的溶 解性
芳香化合物在不同溶 剂中的溶解度受分子 大小和极性等因素影 响,这一性质对其在 实际应用中的溶解和 反应提供了重要参考。
总结
随着科学技术的不断进步,芳烃的合成方法不断 创新,新型技术的应用将促进芳烃产业的发展, 带来更多的经济与社会效益。
● 03
第3章 芳香烃的反应及应用
电子亲近取代反应
芳香烃中含有亲电位的原子或基团 01 会发生取代反应
亲电位
02 反应通常在亲电试剂的作用下进行
亲电试剂
03
亲核取代反应
芳香烃可以 发生亲核试 剂的亲核取
芳香化合物的光学性质
旋光仪测定
测量方法 结果解读
手性分析
手性异构体 对称性问题
反应性影响
化学反应性 生物活性
应用范围
有机合成 材料科学
芳香化合物的光谱性质
01 紫外-可见光谱
吸收峰分析
02 红外光谱
波谱图解读
芳香化合物定义

芳香化合物定义
芳香化合物是一種具有濃郁芳香氣味的一種化合物,其化學式通常為C6H5,其中C代表碳,H代表氫,C6H5中的6表示碳原子有6個,5表示氫原子有5個。
芳香氣味是由其
中的芳香環構成的,芳香環指的是一種由分子碳原子環組合而成的環形結構,裡面任何一
個碳原子都接著兩個不同的半環(極性單體或雙鍵),與其他碳原子連接。
由於芳香環屬
於敏感結構,其中碳原子會進行環加成,導致非常濃郁的嗅覺效果。
芳香化合物可分為有機芳香化合物和無機芳香化合物。
有機芳香化合物通常以烴基為
最明顯的特征,例如環己烴、二甲苯和環己烯,能夠極易形成芳香環,同時也能夠溶於水,也就是說它們具有很好的水溶性,是自然界中很多生物基礎以及營養來源,因此它們可以
有著非常多的用途。
而無機芳香化合物,則以汞系等重金屬製成,這些芳香化合物通常相
對於有機芳香化合物而言會有更多的氣味,例如汞氰化物、汞腈等,因此它們可以用來調
整香料的濃度。
芳香化合物在生活中被廣泛使用,它們不僅可以用於調食物的香味,更可以用於製造
清新的植物香味。
通常,芳香香味是由迎接受者的嗅覺而評價的,因此芳香化合物對於人
類的影響非常大,尤其是對於心情和情緒的改善上,對於產品的影響也是非常大的,產品
很多時候依賴於它們的香味或者對芳香化合物有某種特殊要求,例如香味薰衣草、小麥草、甘草等等獨特的植物香味,香水等產品更是依賴對芳香化合物的調控。
有机化学基础知识点整理芳香化合物的结构和性质

有机化学基础知识点整理芳香化合物的结构和性质有机化学基础知识点整理芳香化合物的结构和性质一、介绍在有机化学中,芳香化合物是一类具有特殊结构和性质的有机分子。
芳香化合物由苯环或其类似的环结构构成,它们具有稳定的共轭π电子体系和特有的芳香性质。
本文将介绍芳香化合物的结构和性质的基础知识点。
二、芳香化合物的结构特征1. 苯环结构芳香化合物的基本结构是苯环,苯环由六个碳原子组成,形成一个平面结构。
每个碳原子上有一个氢原子,分子中共有6个碳-碳单键和3个碳-碳双键。
2. 共轭π电子体系芳香化合物中,苯环上的碳-碳双键形成了共轭π电子体系。
这种共轭结构使得苯环中的π电子能够自由运动,增强了分子的稳定性。
3. 非局域化电子由于芳香化合物中的π电子呈现共轭结构,电子能在整个分子中自由运动,不局限于特定的化学键。
这种非局域化电子是芳香化合物具有特殊性质的重要原因之一。
三、芳香化合物的性质1. 芳香性芳香化合物的最重要性质是芳香性。
它指的是芳香化合物具有较强的香味或特殊的芳香气味。
这种芳香性与芳香化合物的共轭π电子体系有关,电子能在分子中自由运动并吸收特定波长的光子。
2. 稳定性芳香化合物的共轭π电子体系使其具有较高的稳定性。
这种稳定性来源于共轭体系的电子共享和共轭结构的共鸣效应。
相对于非芳香化合物,芳香化合物更不容易发生化学反应。
3. 光谱性质芳香化合物的结构和性质可以通过各种光谱技术进行分析。
紫外可见光谱和红外光谱是常用的分析手段,可以用来研究芳香化合物的电子跃迁和化学键振动。
4. 反应性虽然芳香化合物由于其稳定性而不容易参与化学反应,但它们仍然可以进行芳香亲核取代反应、芳香亲电取代反应等。
这些反应通常需要在适当的条件下进行,如使用强酸或强碱催化剂。
5. 变性物质芳香化合物和一些物质反应能够产生变性作用。
比如,苯环上的碳原子可以被氢气加氢反应,形成环己烷等非芳香化合物。
四、典型的芳香化合物1. 苯苯是最简单的芳香化合物,由六个碳原子和六个氢原子组成。
芳香化合物的同分异构体

芳香化合物的同分异构体
芳香化合物是一类具有芳香性质的有机化合物,它们的分子中含有一个或多个芳环。
由于芳环结构的特殊性质,芳香化合物具有很多独特的物理和化学性质。
其中,同分异构体是指分子式相同但结构不同的化合物,它们具有相同的化学计量学式,但在分子结构上却有所不同。
在芳香化合物中,同分异构体的存在很常见。
同分异构体的存在会影响化合物的物理性质和化学性质,因此对其进行分析和研究非常重要。
芳香化合物的同分异构体可以从分子结构上进行分类。
最常见的同分异构体是位置异构体,即分子中不同的基团在芳环上的位置不同。
例如,苯甲醛和间甲醛就是一对位置异构体。
此外,还有一类同分异构体是环式异构体,即分子中不同的基团在芳环上的位置相同,但它们的环式结构不同。
例如,萘和苯并[α]芘就是一对环式异构体。
同分异构体的存在会导致化合物的物理性质和化学性质发生变化。
例如,位置异构体的沸点和熔点会因为分子结构不同而有所不同,不同的同分异构体可能对光、电、磁场的响应也不同。
化学性质方面,同分异构体的反应性也会有所不同。
例如,位置异构体的亲电性和核磁共振谱也会因为分子结构不同而有所不同,从而影响其反应性能。
总之,芳香化合物的同分异构体的存在是非常常见的,其对化合物的物理性质和化学性质都会产生影响。
因此,对同分异构体的分析和研究是化学领域中非常重要的一项工作。
- 1 -。
芳香化合物的结构和反应

芳香化合物的结构和反应芳香化合物是碳原子排列成环状结构的有机化合物,具有天然香气或气味,化学性质稳定,是化学工业中广泛应用的有机化学品。
芳香化合物的结构和性质芳香化合物的分子结构特点就是一个或多个苯环,苯环由6个碳原子构成,每个碳原子上都连接一个氢原子。
苯环具有高度稳定性和共轭特性,可形成共轭体系,使芳香化合物具有特殊的化学性质。
首先,在苯环上,由于环上的所有碳原子均含有一个孪生电子或一个孪生原子,因此它们形成3对π电子,这些π电子可以通过苯环的所有碳原子移动。
因此,苯环是稳定的, 这是因为π电子在共轭体系中具有更低的能量状态。
苯环的稳定性也能够使其形成共轭结构。
特别是当苯环上连接了异构烷基或覆以芳香性团时,还会使其性质变得更加稳定。
其次,芳香化合物之间的氢键也具有特殊性质。
由于苯环及其衍生物分子中的π电子受到许多化学团的作用,因此,其内部存在许多云电子密度波(π电子)模式,这些模式是共轭的。
对于相邻苯环之间的电子云密度波通过π-π作用方式得到加强。
此外,随着苯环上的化学基团数量和多样性增加,共轭电子流的强度和空间活性也会增加。
这意味着主要由共轭π键组成的芳香化合物的空间构型可以通过一种反应模式来预测,即通过推导其分子中的电子云密度波方法,以确定其空间形状和化学反应方式。
芳香化合物的反应芳香化合物的氢原子很难脱离,因此其氧化或还原反应中极少有涉及氢的通道。
在许多化学反应中,芳香化合物的分子被改变其化学键而不破坏苯环的共轭π键,可以通过取代反应来引起改变。
取代反应可以用强氧化剂和烷基烯来进行。
例如可以将苯甲醛通过氧化加热形成苯甲酸。
还可以使用磺酸、氧化合物、烷基烯和投入性反应来进行芳香化合物的取代反应。
此外,芳香化合物也可以发生重排和分解反应。
重排反应是指原本芳香化合物分子内部的化学键,发生重排造成结构的变化。
例如烷基苯和取代苯甲酸甲酯均可经过重排反应(通常是催化剂和高温热弱反应)形成对应的酰氯。
芳香化合物的定义(精)PPT课件

第一节 芳香化合物的定义
第一阶段:从植物胶中取得的具有芳香气味 的物质称为芳香化合物。 第二阶段:将苯和含有苯环的化合物称为芳 香化合物。 第三阶段:将具有芳香特性的化合物称为芳 香化合物。
3
芳香性的概念 1 C/H的比例高。 2 具有平面和接近平面的环状结构。 3 键长接近平均化。 4 化学性质稳定,易发生亲电取代而不易 发生加成。
每个C=C的平均氢化热 119.5
115.9
119.5
69.5
(kJ / mol)
从整体看: 苯比环己三烯的能量低 苯比环己二烯的能量低
358.5 - 208.5 = 150 kJ / mol (苯的共振能) 231.8 - 208.5 = 23.3 kJ / mol
13
4 难以发生加成反应
(1) 其它不饱和键优先发生加成
4
第二节 芳香烃的物理性质
芳香烃不溶于水,但溶于有机溶 剂。一般芳香烃均比水轻。沸点随相 对分子质量升高而升高。熔点除与相 对分子质量有关外,还与结构有关, 通常对位异构体由于分子对称,熔点 较高。
5
历史上苯的表达方式
Kekul’e式
双环结构式 杜瓦苯
棱形结构式 棱晶烷
向心结构式
对位键 结构式
余价 结构式
Br
快
+ H+ + Br3-
30
*4 常用的卤化试剂
氟化(XeF2 , XeF4 , XeF6) 氯化(Cl2+FeCl3 , HOCl) 溴化(Br2 , Br2 + Fe , Br2 + I , HOBr , CH3COOBr) 碘化(ICl , I2 + HNO3 , I2 + HgO, KI)
