北方学院实验水的汽化热
试验12水的汽化热测定

实验3 水的汽化热测定[实验目的]1.测定水的汽化热.2.学习用冷热补偿法减少系统误差的方法.[实验仪器]量热器 水的汽化热测定装置 酒精灯 支架 温度计[实验原理]物质由液态向气态转化的过程称为汽化.在一定压强下,单位质量的液体汽化为同温 度的蒸气所吸收的热量为汽化热.物质由气态向液态转化的过程称为凝结.凝结时要放出 在同一条件下汽化时所吸收的热量.由于直接测水的汽化热不容易,所以本实验采用测量 凝结时放出热量的方法来测定水的汽化热.实验装置如图12—1图12—1从沸水器(蒸汽发生器)出来的水蒸汽在冷凝器中凝结成水,放出热量。
使量热器内 筒和筒里的水温升高.若系统达到平衡时则可列出下列热平衡方程式:lm+mc(t 2-T)=m 1c(T-t 1)+m 2c 1(T- t 1)=( m 1c+ m 2c 1)(T- t 1) (12-1)l=m1[( m 1c+ m 2c 1)(T- t 1) –mc(t 2-T)] (12-2) l ——水的汽化热;m ——凝结成水的蒸气的质量;c ——水的比热;m 1——量热器中液 体的质量;c 1——量热器内筒的比热;m 2——量热器内筒的质量;t 1——量热器中水的初 温;t 2——蒸气的温度;T ——通人蒸气后量热器中水的终温.由于蒸气通过导气管时会有少量凝结,其中一部分会随蒸气一同送人冷凝器,这部分已凝结的水不再提供汽化热.因此对(12-2)中的m 进行修正,设随同蒸气带人冷凝 器中水质量为m ’,则(12-2)式为l='1m m -[( m 1c+ m 2c 1)(T- t 1) –mc(t 2-T)] (12-3) 用本实验的装置,m '不好测定,因此我们仍用(12-2)式进行计算.为了减少实验误差,适当控制实验条件,采用冷热补偿法修正系统误差,使系统的初 温低于室温,终温高于室温,使它们尽量满足如下关系:T -θ=θ- t 1 ,式中θ为室温. 从而使系统在前段时间由环境吸收的热量与后段时间向环境散失的热量可大体上互相抵消.[实验内容〕1.按图(12-1)装好仪器,但不要先把量热器放在导气管下面.2. 向沸水器中注水180-200毫升(为了缩短加热时间,最好是注热水),在沸水器下 面点燃酒精灯.3.测出量热器内筒质量m 2,随后将150毫升左右、低于室温的水注入内筒,测出它们的总质量,从而求出筒里水的质量m 1.4.等到沸水器中的水沸腾,有大量的蒸气从导气管喷出,读出水的沸点温度t 25.测出量热器内衡水的初温t 1。
水的汽化热的测量
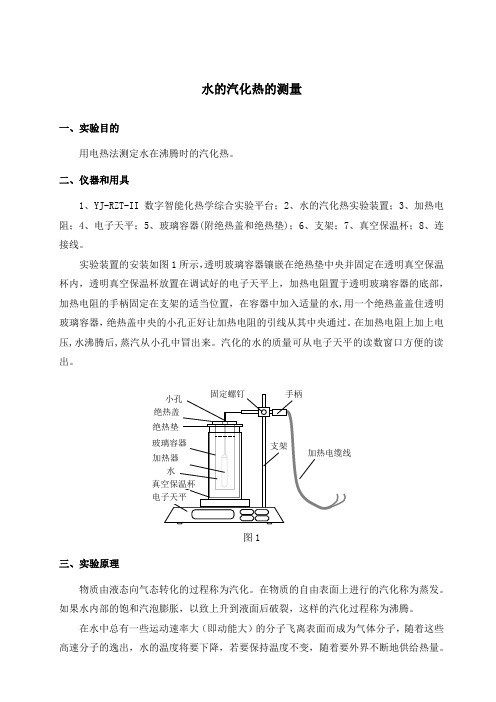
水的汽化热的测量一、实验目的用电热法测定水在沸腾时的汽化热。
二、仪器和用具1、YJ-RZT-II数字智能化热学综合实验平台;2、水的汽化热实验装置;3、加热电阻;4、电子天平;5、玻璃容器(附绝热盖和绝热垫);6、支架;7、真空保温杯;8、连接线。
实验装置的安装如图1所示,透明玻璃容器镶嵌在绝热垫中央并固定在透明真空保温杯内,透明真空保温杯放置在调试好的电子天平上,加热电阻置于透明玻璃容器的底部,加热电阻的手柄固定在支架的适当位置,在容器中加入适量的水,用一个绝热盖盖住透明玻璃容器,绝热盖中央的小孔正好让加热电阻的引线从其中央通过。
在加热电阻上加上电压,水沸腾后,蒸汽从小孔中冒出来。
汽化的水的质量可从电子天平的读数窗口方便的读出。
图1三、实验原理物质由液态向气态转化的过程称为汽化。
在物质的自由表面上进行的汽化称为蒸发。
如果水内部的饱和汽泡膨胀,以致上升到液面后破裂,这样的汽化过程称为沸腾。
在水中总有一些运动速率大(即动能大)的分子飞离表面而成为气体分子,随着这些高速分子的逸出,水的温度将要下降,若要保持温度不变,随着要外界不断地供给热量。
1kg 的水汽化时所吸收的热量就是该物质的汽化热。
汽化热与汽化时的温度有关,温度升高时汽化热减小。
因为随着温度的升高,液相与气相之间的差别将逐渐减小。
如图1所示,在容器中加入了适量的水,加热电阻丝加上直流工作电压,水沸腾后,蒸汽从出汽口冒出来。
测出加热电阻丝上两端的电流I 和电压U ,以及通电时间t 和t 时间内汽化的水的质量M ,则:h ML UIt +=式中:L 为水蒸气的比汽化热:h 为水的汽化热实验装置总的散失的热量。
假定在相同的时间间隔t 里,水的汽化热实验装置散失的热量h 相等,则可得到下列等式:h L M t I U +=111h L M t I U +=222由两等式得:212211)(M M t I U I U L --= (1) 式中, I 1、U 1及I 2、U 2为相同条件下,两次不同电流和电压的实验数据。
水的汽化实验

水的汽化实验水的汽化是一种非常常见的现象,在我们日常生活和科学实验中都可以观察到。
这篇文章将探讨水的汽化实验以及背后的科学原理。
首先,我们需要准备以下材料和设备:一只玻璃杯、一小瓶水、一块光滑的玻璃板和一块布。
实验步骤如下:1. 将玻璃杯中放入一些水,并确保水面平稳且不会溢出。
2. 将玻璃板小心地覆盖在玻璃杯上,确保两者之间没有间隙。
3. 用布轻轻地擦拭玻璃板上的水滴,以确保板面的干燥。
接下来,我们可以开始观察实验过程中的一些现象和变化。
当我们将玻璃板覆盖在玻璃杯上时,水会从玻璃杯中蒸发到玻璃板上,形成雾气。
这是因为水分子在热量作用下变得更加活跃,从液态转变为气态。
这个实验中涉及的科学原理是水的汽化。
水的汽化是指水分子从液态转变为气态的过程。
在常温下,水分子的平均动能不足以克服分子间的吸引力,因此处于液态。
但当水受到热量传递时,水分子的平均动能会增加,这使得一部分水分子获得足够的能量以克服分子间的吸引力,并转变为气态。
这个过程也被称为蒸发。
而玻璃板的作用是提供一个平滑的表面,以便水分子能够聚集在上面形成雾气。
当空气中的水分子与玻璃板上的水分子发生碰撞时,水分子会凝结成微小的水滴,导致玻璃板上出现雾气。
此外,我们还可以通过改变实验条件来观察水的汽化过程的变化。
例如,我们可以加热玻璃杯中的水,以增加水分子的平均动能,从而促进水的汽化。
也可以在不同的环境温度下进行实验,以观察不同温度对水汽化速率的影响。
水的汽化实验不仅可以帮助我们更好地理解水的性质,也可以应用到日常生活和实际应用中。
例如,当我们在炒菜时,可以通过观察水的汽化来判断锅底温度是否适宜,以保证食物的烹饪效果。
在工业生产中,了解水的汽化原理也可以帮助我们控制和优化一些工艺过程。
总之,水的汽化是一种普遍存在的现象,通过实验我们可以更好地了解和观察这个过程。
通过实验,我们不仅可以观察到水的蒸发现象,还可以深入探索其背后的科学原理,并将这些知识应用到日常生活和实际应用中。
水的比汽化热实验报告

一、实验目的1. 通过实验,学习使用混合量热法测定水的比汽化热。
2. 了解实验误差产生的原因及减小误差的方法。
3. 培养实验操作技能和数据处理能力。
二、实验原理在一定的外部压强下,液体总是在一定的温度下沸腾。
在沸腾过程中,虽然对它继续加热,但液体的温度并不升高。
可见,在把液体变成汽体时,要吸收热量。
为此引进汽化热这个物理量,来表示在一定温度及压强下,单位质量的液体变成同温度的汽所需要的热量,即比汽化热。
本实验通过测定出水蒸汽在常压条件下凝结热,从而根据公式间接得到水在沸点(100℃)时的比汽化热。
三、实验仪器与材料1. XJ-TQ-2型液体汽化热测定仪2. WL-1物理天平3. 秒表4. 烧杯5. 温度计6. 玻璃棒7. 铝箔8. 水和酒精四、实验步骤1. 将XJ-TQ-2型液体汽化热测定仪的量热器清洗干净,并用蒸馏水冲洗干净,将烧杯和温度计也清洗干净。
2. 用物理天平称量量热器、烧杯和水的总质量m0,记录数据。
3. 将水倒入烧杯中,用温度计测量水的初温t1,记录数据。
4. 将烧杯放入量热器中,用温度计测量量热器、烧杯和水的总质量m1,记录数据。
5. 将酒精倒入烧杯中,用玻璃棒搅拌均匀,使酒精与水充分混合。
6. 用酒精灯加热烧杯中的混合液体,直至水沸腾,用秒表记录加热时间t,记录数据。
7. 当水沸腾后,立即用铝箔覆盖在烧杯上,防止热量散失。
8. 用温度计测量混合液体的温度t2,记录数据。
9. 用物理天平称量量热器、烧杯和水的总质量m2,记录数据。
10. 重复步骤6-9,进行三次实验,记录数据。
五、数据处理1. 计算每次实验中水的质量m = m2 - m1,记录数据。
2. 计算每次实验中加热时间t的平均值t_avg,记录数据。
3. 计算每次实验中混合液体的温度变化Δt = t2 - t1,记录数据。
4. 根据公式Q = m ΔH,计算每次实验中水的比汽化热ΔH,记录数据。
5. 计算三次实验中水的比汽化热的平均值ΔH_avg,记录数据。
实验二十五_水的汽化热的测定

实验二十五水的汽化热的测定[目的]1.学习测定水的汽化热的方法。
2.学会使用量热器及水银温度计。
3.学习选定实验条件和选择实验仪器。
4.学习系统误差的修正方法。
[仪器和用具]量热器,水银温度计,冷凝器,滤汽室,蒸汽发生器,支架,夹子,天平,烧杯及秒表等。
[实验内容和要求]测定水的汽化热,进行三次测量。
第一次测量为初测。
主要目的是摸清实验条件,以估计冷热补偿的控制条件,保证在第二次的正式测量中取得满意的实验结果。
测试的内容应包括:⑴冷水的初始温度的选择;⑵水的质量的选择;⑶通入蒸汽过程中系统的温度变化情况以及因漏热而引起的水的温度及系统温度的变化情况。
与此同时,熟悉实验操作,保证在第二次正式实验时,一切操作都准确无误。
为保证取得数据的可靠性,初测时的实验条件应在预习时事先设计好。
第二,三次测量是正式测量。
是在根据第一次测量的结果重新调整实验条件和设计更完美的实验步骤和方法之后进行的。
将实验数据描点作图,用外推法确定冷水的初始温度及系统的末温的值,计算水的汽化热及相应的测量不确定度。
附:在完成上面的实验后,可利用本实验的仪器设计测量冰块的溶解热。
[注意事项]1.向冷凝器通入蒸汽后立即充分搅拌,但不要将水溅出筒外。
2.进行第二,三次实验时,应将冷凝器中水倒掉并吹干。
3.为画出准确的实验进程温度曲线,读取温度和时间的数值时要对应读取。
[预习和思考题]1.在了解实验原理和方法的基础上,设计出初测的实验条件及方法。
2.设计实验步骤及记录表格。
3. 设计出测量冰的溶解热的实验方案。
[课后作业题]请定性或定量说明课本156页的问题讨论。
水的比汽化热测定实验报告

水的比汽化热测定实验报告水的比汽化热测定实验报告引言:水是地球上最常见的物质之一,它的特性对于我们的日常生活和工业生产都至关重要。
而水的比汽化热则是描述水从液态转变为气态所需的能量,它在热力学和化学领域中具有重要的意义。
本实验旨在通过测定水的比汽化热,深入了解水的性质以及热力学原理。
实验目的:1. 了解水的比汽化热的定义和意义;2. 学习使用实验装置和测量方法,进行水的比汽化热的测定;3. 掌握实验数据的处理和结果分析方法。
实验原理:水的比汽化热是指单位质量的水从液态转变为气态所需的能量。
在实验中,我们使用加热器加热水,使其温度升高,直至沸腾。
当水沸腾时,温度不再升高,而是保持恒定,这是因为水的沸点温度与外界压强有关。
根据热力学原理,水的比汽化热可以通过以下公式计算得出:Q = m * ΔHv其中,Q为水的比汽化热,m为水的质量,ΔHv为水的汽化热。
实验步骤:1. 准备实验装置:将加热器连接到恒温水槽中,加热器上方放置一个温度计,确保温度计能够准确测量水的温度。
2. 将一定质量的水倒入加热器中,并记录水的质量。
3. 打开加热器,逐渐加热水,同时用温度计测量水的温度变化。
当水开始沸腾时,记录下此时的温度,并保持恒定。
4. 关闭加热器,等待水冷却至室温,并记录下此时的温度。
5. 根据实验数据计算水的比汽化热。
实验数据:通过实验记录的数据,我们可以计算出水的比汽化热。
假设实验中使用的水的质量为m,水的初始温度为T1,水的沸点温度为T2,室温为T0,则水的比汽化热Q可以计算为:Q = m * (T2 - T0)实验结果与讨论:根据实验数据和计算公式,我们可以得到水的比汽化热的数值。
在实验过程中,我们发现水的沸点温度与外界压强有关,当压强增加时,水的沸点温度也会相应升高。
这是因为增加压强会增加水分子之间的相互作用力,使得水分子更难从液态转变为气态,所需的能量也会增加。
此外,实验中我们还发现,水的比汽化热是一个固定的数值,与水的质量无关。
实验三 b 水的汽化热的测定(用杜瓦瓶测)

实验三(b ) 水的汽化热的测定(用杜瓦瓶测)实验目的1.测定水在大气压下的汽化热。
2.学会测定杜瓦瓶的有效热容量。
实验仪器煮水器,电热器,杜瓦瓶,0.1℃刻度的温度计,物理天平,蒸馏水,输入水蒸汽的导管等。
实验原理单位质量的液体在温度不变的条件下变成水蒸汽时所吸收的热量,叫做液体的汽化热,常以γ表示,单位为卡/克。
当水蒸汽凝结时,则放出与汽化热等量的热量。
汽化热的数值与汽化时的温度有关。
本实验测定水在常沸点(与常压强相对应)时的汽化热。
为此,把煮水器中质量为m d 的饱和水蒸汽引入盛有水的量热器中。
本实验用一只杜瓦瓶来替换一般的量热器,引入的蒸汽和瓶中的水混合并在水中凝结。
设引入的蒸汽温度为1T (100℃),以1T ′、2T 分别表示在量热器中水的初始温度和终止温度,以m w 表示量热器内原先水的质量,C ′表示量热器连同质量为m w 的水的有效热容量(略去搅拌器)。
蒸汽凝结时放出热量γ・m d 。
这凝结成水后又冷却到终温2T ,在这个过程中,它又放出热量w C ・m d ·(1T -2T ),而量热器则吸收热量C ′・(2T -1T ′)。
根据热平衡原理有 γ・m d +w C ・m d ・(1T -2T )=C ′・(2T -1T ′) 所以)()(2112T T C T T m C w d −−′−′=γ (3-3b -1) 因为是采取杜瓦瓶来替换量热器,待测量物质同周围介质的热交换非常小,所以1T ′和2T 可能直接测量而无需要进行散热校正,也能达到测量的准确度要求。
现在来讨论杜瓦瓶以及它内部装有水的有效热容量C ′。
由于玻璃的导热率很小,只有容器的内壁的温度才会升高到与水相同的温度。
因此,在C ′内不应当算进量热器的全部热容量。
为此,可用下述方法就能准确地求出有效热容量C ′:首先,用与实验时相等量的温度为室温的水注入量热器,使容器的温度有一个确定的值。
经过一段时间后,直到容器内水的温度稳定在∗1T 时为止。
实验三 水的汽化热的测定

实验三 水的汽化热的测定一、实验目的1、学习用混合量热法测定水的汽化热。
2、了解一种粗略修正散热的方法——抵偿法。
二、实验仪器1、XJ-TQ-2型液体汽化热测定仪;2、WL-1物理天平;3、秒表。
三、实验原理在一定的外部压强下,液体总是在一定的温度下沸腾,在沸腾过程中,虽然对它继续加热,但液体的温度并不升高。
可见,在把液体变成汽体时,要吸收热量。
为此引进汽化热这个物理量,来表示在一定温度及压强下,单位质量的液体变成同温度的汽所需要的热量,即:L Q m =反过来,当汽体重新凝结成液体时就会放出热量。
所放出的热量跟等量的液体在同一条件下汽化时所吸收的热量相同。
即:汽化热=凝结热。
由此,本实验通过测定出水蒸汽在常压条件下凝结热,从而根据上式,间接得到水在沸点(100℃)时的汽化热。
蒸汽从发生器出来,经玻璃管进入量热器内筒中凝结成水,放出热量,使量热器内筒和水的温度由初温1t 升到θ,设凝结成水的蒸汽质量为m ,蒸汽由2t ℃变到θ℃的有个中间转化过程,那就是2t ℃的水蒸气首先转化成2t ℃的水,这时要放出热量,即凝结热mL ;然后2t ℃的水再与冷水混合,最终达到热平衡,平衡温度为θ℃,这时要放出热量2()c m t θ-水,则总的放热量就是 2()Q mL c m t θ=+-放水 设量热器和水的质量分别为1m 、M ,比热分别为1c 、c 。
则量热器、水所得到的热量(不考虑系统的对外散热): 111()()Q m c M ct θ=+-吸 式中由热平衡方程式 吸放Q Q =θ t 1 则 1112()()()m c cM t mc t L m θθ+---= (1)【散热修正】:上述讨论是假定量热器与外界无热量交换时的结论.实际上只要有温度的差异就必然要有热交换存在,因此必须考虑如何防止散热或对散热进行修正。
本实验中热量的散失主要是蒸汽通入盛有水的量热器中,混合过程中量热器向外散失的热量,由此造成混合前水的初温与混合后水的终温不易测准.为此,根据牛顿冷却定律来修正温度。
