高分子化学第六章.ppt
合集下载
高分子化学 第6章 配位聚合
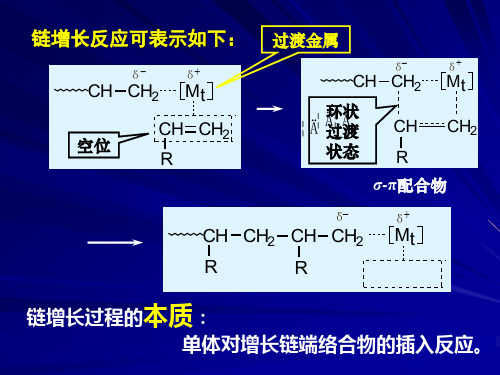
对于合成橡胶,希望得到高顺式结构。
(3)立构规整度的测定 聚合物的立构规整性用立构规整度表征。 立构规整度:是立构规整聚合物占总聚合物的分数。 ----是评价聚合物性能、引发剂定向聚合能力的一 个重要指标。 结晶 比重 根据聚合物的物 熔点 理性质进行测定 溶解行为 化学键的特征吸收 全同聚丙烯的立构规整度(全同指数、等规度): 常用沸腾正庚烷的萃取剩余物所占百分数表示
-烯烃聚合物的Tm大致随取代基增大而升高。 HDPE 全同PP 聚3-甲基-1-丁烯 聚4-甲基-1-戊烯 Tm 120 175 300 235 ( ℃)
②二烯烃聚合物 如:丁二烯聚合物 1, 2聚合物都具有较高的熔点
全同 Tm = 128℃ 间同 Tm = 156℃
1, 4聚合物
反式1, 4聚合物 Tg = -80℃, Tm = 148℃ 较硬的低弹性材料 顺式1, 4聚合物 Tg = -108℃, Tm = 2 ℃ 是弹性优异的橡胶
直接证据:
用含标记元素的终止剂终止增长链
14CH OH 3
14CH3O- + H+
得到的聚合物无14C放射性,表明加上的是H+, 证明链端是阴离子。
因此,配位聚合属于配位阴离子聚合。 ③增长反应是经过四元环的插入过程
δδ+
增长链端阴离 子对烯烃双键 碳原子的亲 核进攻
CH CH2 ¦Ä¦Ä¦Ä
高分子化学导论第6章 阴离离子聚合与阳离子聚合
S:苯乙烯链段,B:丁二烯链段
在室温条件下它的性能与一般硫化橡胶并 无差别,但却可以方便地采用一般塑料的 加工方法如熔融注射挤压成型进行生产。
制备嵌段共聚物的关键
不同单体加料的先后次序 并非所有活性聚合物都能引发另一种单体 聚合。活性聚合物能否引发另一单体聚合, 取决于M1和M2的相对碱性: pKa。
pKa=-logKa,Ka:电离平衡常数
pKa值:St 40-42 ; MMA 24
6.6 工业生产
理论上:对分子链结构有较强的控 制能力,可获得“活性聚合物”,可进 行分子设计,合成预定结构和性能的聚 合物;
工业生产中:可生产许多性能优良的 聚合物,如丁苯橡胶、异戊橡胶、SBS 热塑性橡胶等。
自由阴离子引发体系
形成单阴离子
金属烷基化合物 ——最常用的阴离子聚合引发剂
引发活性与金属电负性有关,若Mt-C的 极性愈强,引发活性愈大。 丁基锂(Butyllithium,BuLi)是最常见的阴 离子聚合引发剂之一,它以离子对的形式 引发丁二烯、异戊二烯聚合。
阴离子聚合机理
(1)链引发:
Bu来自百度文库Li + CH2 CH C CH2 CH3
慢增长是相对于引发而言较慢,其实 它的增长较自由基聚合要快得多。
溶剂对聚合反应的影响
质子型:ROH;H2O 不能作为阴离子聚合的溶剂
极性:四氢呋喃 非质子型
在室温条件下它的性能与一般硫化橡胶并 无差别,但却可以方便地采用一般塑料的 加工方法如熔融注射挤压成型进行生产。
制备嵌段共聚物的关键
不同单体加料的先后次序 并非所有活性聚合物都能引发另一种单体 聚合。活性聚合物能否引发另一单体聚合, 取决于M1和M2的相对碱性: pKa。
pKa=-logKa,Ka:电离平衡常数
pKa值:St 40-42 ; MMA 24
6.6 工业生产
理论上:对分子链结构有较强的控 制能力,可获得“活性聚合物”,可进 行分子设计,合成预定结构和性能的聚 合物;
工业生产中:可生产许多性能优良的 聚合物,如丁苯橡胶、异戊橡胶、SBS 热塑性橡胶等。
自由阴离子引发体系
形成单阴离子
金属烷基化合物 ——最常用的阴离子聚合引发剂
引发活性与金属电负性有关,若Mt-C的 极性愈强,引发活性愈大。 丁基锂(Butyllithium,BuLi)是最常见的阴 离子聚合引发剂之一,它以离子对的形式 引发丁二烯、异戊二烯聚合。
阴离子聚合机理
(1)链引发:
Bu来自百度文库Li + CH2 CH C CH2 CH3
慢增长是相对于引发而言较慢,其实 它的增长较自由基聚合要快得多。
溶剂对聚合反应的影响
质子型:ROH;H2O 不能作为阴离子聚合的溶剂
极性:四氢呋喃 非质子型
《高分子化学》PPT课件

应用领域
共混改性技术广泛应用于塑料、橡胶、涂料等领域,如增韧塑料、阻燃塑料、导电塑料等 。
填充改性技术
01
填充剂种类与特性
填充剂包括无机填充剂和有机填充剂。无机填充剂如碳酸钙、滑石粉等
,具有来源广泛、价格低廉、稳定性好等优点;有机填充剂如木粉、废
纸粉等,具有可再生、可降解等优点。
02
填充改性效果
填充改性可以改善高分子材料的力学性能、热稳定性、尺寸稳定性等,
加工成型过程中的影响因素
加工成型过程中,温度、压力、时间等因素对高分子材料的性能和制品质量有重要影响 。合理的控制这些因素可以获得优质的制品。
应用领域
加工成型技术是高分子材料制品生产的关键环节,广泛应用于塑料、橡胶、涂料、胶粘 剂等领域。
05
高分子材料应用领域及发展趋势
塑料领域应用及发展趋势
包装材料
同时还可以降低成本。但填充剂的加入也可能对材料的加工性能和某些
物理性能产生负面影响。
03
应用领域
填充改性技术广泛应用于塑料、橡胶、复合材料等领域,如填充聚乙烯
、填充聚丙烯、填充橡胶等。
纤维增强技术
增强纤维种类与特性
增强纤维包括玻璃纤维、碳纤维、芳纶纤维等。这些纤维 具有高强度、高模量、耐高温等优点,可以有效提高高分 子材料的力学性能和耐候性能。
服装纺织
合成纤维如涤纶、锦纶、腈纶等广泛应用于服装纺织品中。
共混改性技术广泛应用于塑料、橡胶、涂料等领域,如增韧塑料、阻燃塑料、导电塑料等 。
填充改性技术
01
填充剂种类与特性
填充剂包括无机填充剂和有机填充剂。无机填充剂如碳酸钙、滑石粉等
,具有来源广泛、价格低廉、稳定性好等优点;有机填充剂如木粉、废
纸粉等,具有可再生、可降解等优点。
02
填充改性效果
填充改性可以改善高分子材料的力学性能、热稳定性、尺寸稳定性等,
加工成型过程中的影响因素
加工成型过程中,温度、压力、时间等因素对高分子材料的性能和制品质量有重要影响 。合理的控制这些因素可以获得优质的制品。
应用领域
加工成型技术是高分子材料制品生产的关键环节,广泛应用于塑料、橡胶、涂料、胶粘 剂等领域。
05
高分子材料应用领域及发展趋势
塑料领域应用及发展趋势
包装材料
同时还可以降低成本。但填充剂的加入也可能对材料的加工性能和某些
物理性能产生负面影响。
03
应用领域
填充改性技术广泛应用于塑料、橡胶、复合材料等领域,如填充聚乙烯
、填充聚丙烯、填充橡胶等。
纤维增强技术
增强纤维种类与特性
增强纤维包括玻璃纤维、碳纤维、芳纶纤维等。这些纤维 具有高强度、高模量、耐高温等优点,可以有效提高高分 子材料的力学性能和耐候性能。
服装纺织
合成纤维如涤纶、锦纶、腈纶等广泛应用于服装纺织品中。
高分子化学-第六章 逐步聚合

r=
Na Na+NC
q=
NC Na
37
• 二、控制产物聚合度的方法
通常是在两官能团等当量的基础上, 使某种单体稍过量或另外加入某种单 官能度的物质。
38
•思考:
1.对于逐步聚合反应,为什么不 用P、K来控制产物的聚合度?
39
2.为什么缩聚物的分子量一般都不高 (小于105)?
3.采取何措施,才能得到尽可能大分 子量的高聚物?
4
• RCOOH+R´OH
RCOOR´+ H2O
• RCOOH+ HOR´OH
RCOO R´OH + H2O
RCOO R´OH + RCOOH RCOO R´OCOR + H2O
5
• HOCORCOOH+ HOR´OH
HOCORCOO R´OH + H2O
• HOCORCOOR´OH + HOR´OH
• 设t=t´时,体系中的分子数为N,消 耗官能团总数2(N0–N)
• 则P=2(N0–N)/(N0• f ) 又Xn=N0/N
得到:P=
2 f
(1–
1 Xn
)
62
假设凝胶点时Xn→∝。
卡洛基斯方程:Pc=
2 f
63
• (2)官能团非等摩尔比投料时 平均官能度f:
高分子化学第六章配位聚合

HH HH HH HH
全 同 立 构
H R H R H R H R
H R H H H R H H
H H H H H H H H
H H H R H H H R
HHHHHHHH HR HR HR HR
HR R H HR R H C C C C C C C C
HHHR HHHR HR HHHR HH
HH HH HH HH
H H C * C* R1 R2
18.03.2019
它们以不同的组合方 式排列,可以形成四种立 构规整性聚合物。
高分子化学
6.2.2 顺反异构 聚合物的顺反异构或称几何异构是由于分子链中的双键上取代 基在空间上排列不同而造成的。 典型的例子是1,3-丁二烯进行1,4-聚合时,形成带双键的重复 单元,该双键便是一立体异构中心,有顺式构型和反式构型:
18.03.2019
高分子化学
H2C
CH CH
CH2
1,4-聚合
CH2 CH
CH CH2 n
CH2 C C H
CH2CH2 C C H H
CH2CH2 H H C C
CH2 H
CH2 C C H
H
H C C
CH2CH2 C C H H
H CH2
CH2CH2
CH2 C C H
CH2 H
CH2 C C H
第六章 配位聚合 高分子化学PPT课件

K为仪器常数
16 62/16
6.2 聚合物的立体规整性
二烯烃聚合物的立构规整度用某种立构体的 百分含量表示,可用IR、NMR测定。
聚丁二烯IR吸收谱带
全同1, 2: 991、694 cm-1 间同1, 2: 990、664 cm-1 顺式1, 4: 741 cm-1 反式1, 4: 964 cm-1
15 62/15
6.2 聚合物的立体规整性
全同聚丙烯的立构规整度(全同指数、等规度) 常用沸腾正庚烷的萃取剩余物所占百分数表示。
沸腾正庚烷萃取剩余物重 聚丙烯的全同指数 (I I P) = 未萃取时的聚合物总重
也可用红外光谱的特征吸收谱带测定
I I P = K A975 A1460
全同螺旋链段特征吸收,峰面积 甲基的特征吸收,峰面积
6 62/6
6.2 聚合物的立体规整性
立体异构 由于分子中的原子或基团的空间构 型和构象不同而产生的异构
构象异构 Conformation 立体异构 Stereo-isomer
构型异构 Configuration
手性异构 Chiral
几何异构 Geometrical
R右 S左
Z顺 E反
7 62/7
1954年,意大利人Natta 采用TiCl3/Al(C2H5)3 为引发剂,实现了丙烯的聚合,产物具有高度的 等规度,熔点达175 ℃。
《高分子化学》PPT课件

连锁聚合的产品占聚合物总量的60%以 上,可见其重要性。聚乙烯,聚氯乙烯、聚 苯乙烯、聚丙烯酸酯类、聚丙烯腈、聚乙烯 醇以及各类合成橡胶。
完整版课件ppt
16
一、连锁聚合的单体
单烯类、共轭二烯类、炔烃、羰基化合 物和一些杂环化合物都是热力学上可连锁聚 合的单体。
单烯类、共轭二烯类是最常用的单体。
这些单体对于连锁聚合中的不同引发类 型的选择性不同,如氯乙烯只能自由基聚合, 异丁烯只能阳离子聚合,而苯乙烯自由基、 阳离子和阴离子聚合都可进行。
如尼龙66,聚酯等
在缩聚物中有官能团反应产生的一些基团, 如酰胺键、酯键、醚键等。大部分缩聚物是 杂链聚合物。这些键结构很容易被水、醇、 酸等药品所水解、醇解或酸解。
完整版课件ppt
9
随着高分子化学的发展,出现了很多新的合成方法,如 开环聚合、异构化聚合、分子间氢转移等
环氧乙烷开环合成聚环氧乙烷
聚丙烯酰胺异构化(分子内氢转移)生成尼龙3
完整版课件ppt
2
在聚合物中重复单元和原单体,除电子结构变 化外,原子种类、数量和排列都不变的,这种重复 单元又可称单体单元。
[NH(CH2)6NH·CO(CH2)4CO]n 结构单元 结构单元
[
重复单元
]
(CH2CH OCOCH3)n 单体单元=重复单元
完整版课件ppt
3
2、聚合物的分类
完整版课件ppt
16
一、连锁聚合的单体
单烯类、共轭二烯类、炔烃、羰基化合 物和一些杂环化合物都是热力学上可连锁聚 合的单体。
单烯类、共轭二烯类是最常用的单体。
这些单体对于连锁聚合中的不同引发类 型的选择性不同,如氯乙烯只能自由基聚合, 异丁烯只能阳离子聚合,而苯乙烯自由基、 阳离子和阴离子聚合都可进行。
如尼龙66,聚酯等
在缩聚物中有官能团反应产生的一些基团, 如酰胺键、酯键、醚键等。大部分缩聚物是 杂链聚合物。这些键结构很容易被水、醇、 酸等药品所水解、醇解或酸解。
完整版课件ppt
9
随着高分子化学的发展,出现了很多新的合成方法,如 开环聚合、异构化聚合、分子间氢转移等
环氧乙烷开环合成聚环氧乙烷
聚丙烯酰胺异构化(分子内氢转移)生成尼龙3
完整版课件ppt
2
在聚合物中重复单元和原单体,除电子结构变 化外,原子种类、数量和排列都不变的,这种重复 单元又可称单体单元。
[NH(CH2)6NH·CO(CH2)4CO]n 结构单元 结构单元
[
重复单元
]
(CH2CH OCOCH3)n 单体单元=重复单元
完整版课件ppt
3
2、聚合物的分类
高分子化学第六章+离子聚合

分子量分布:
服从Poisson分布,即x-聚体的摩尔分率为:
ν:动力学链长,即每个引发剂分子所引发的单体分子数。 若引发反应包括一个单体分子,则:
当很大时,接近于1 由萘钠-THF引发得的聚苯乙烯,接近单分散性,这种 聚苯乙烯可用作分子量及其分布测定的标样。
D. 活性聚合的应用
合成均一分子量的聚合物 这是目前合成均一特定分子量的唯一方法,为GPC 提供标准样品
紧离子对有利于单体定向配位,形成立构规整聚合 物,但聚合速率较低;松离子对和自由离子聚合速 率较高,却失去定向能力。单体-引发剂-溶剂配合 得当,兼顾聚合活性和定向能力。
溶剂的介电常数和电子给予指数
溶剂 己烷 苯 二氧六环 乙醚 四氢呋喃 丙酮 硝基苯 二甲基甲酰胺
介电常数 2.2 2.2 2.2 4.3 7.6 20.7 34.5 35
CH2 CH A + MMA CH2 CH CH2 C A COOCH3
CH3 CH2 C A + COOCH3
CH2 CH
不能
pKd值同一级别的单体也有方向性 St-能引发B,反之相对困难,因B-比St-更稳定
制备星型聚合物
通过偶联剂将聚合物链阴离子 连接起来,可获得星型聚合物
Mn
Mn A + SiCl4
先制成一种单体的“活的聚 合物”,再加另一单体共聚, 制得任意链段长度的嵌段共 聚物。如合成SBS热塑性橡 胶。
高分子化学ppt幻灯片课件

高分子化学ppt幻灯片课件
•高分子化学概述
•高分子化合物结构与性质•高分子合成方法与反应机理•高分子材料制备与加工技术•高分子材料性能与应用领域•高分子化学前沿研究领域与展望
目录
CONTENTS
01
高分子化学概述
高分子化学定义与特点
定义
高分子化学是研究高分子化合物的
合成、结构、性能及其应用的科学。
特点
高分子化学涉及的高分子化合物具
有分子量高、分子结构复杂、性能
多样等特点。
高分子化学发展历史
早期阶段
天然高分子的利用和改性,如橡胶、
纤维素等。
合成高分子阶段
20世纪初合成第一个高分子化合物—
—酚醛树脂,之后合成橡胶、塑料等
高分子材料。
高分子科学建立
20世纪30年代,高分子科学作为一门独立学科得以建立,高分子化学作为高分子科学的重要分支得到迅速发展。
材料领域生物医学领域环保领域
其他领域
高分子化学研究意义
合成具有优异性能的高分子材料,满足航空航天、汽车、建筑等领
域对高性能材料的需求。开发可降解高分子材料,解决传统塑料带来的环境污染问题。
研究生物相容性高分子材料,用于医疗器械、药物载体等方面,提高医疗水平。高分子化学在能源、信息、农业等领域也有广泛应用,推动相关
产业的发展。
02
高分子化合物结构与性质
由长链分子组成,链上原子以共价键连接,形成线性或支链结构。
链状结构
由三维空间的分子链交织而成,具有高度的交联性和空间稳定性。
网状结构
高分子链在空间中的排列和堆砌方式,包括晶态、非晶态、液晶态等。
聚集态结构
高分子化合物基本结构
非晶态结构
高分子链在空间中无规则排列,呈现无序状态。非晶态高分子具有较好的柔韧性和加工性能。
高分子化学第6章-聚合物的化学反应

CH2 CH OH + C COCl CH2 CH CH2 CH CH2 CH OH OH O CO
7
b. 静电效应:邻近基团的静电效应可降低或提高功能基的反 静电效应 效应: 应活性。 应活性。 如聚丙烯酰胺的水解反应速率随反应的进行而增大, 如聚丙烯酰胺的水解反应速率随反应的进行而增大,其原 因是水解生成的羧基与邻近的未水解的酰胺基反应生成酸酐环 状过渡态,从而促进了酰胺基中-NH2的离去加速水解。 的离去加速水解。 状过渡态,从而促进了酰胺基中
14
醋酸纤维
浓硫酸/醋酸 浓硫酸 醋酸 溶胀、 溶胀、催化剂 用途 二醋酸和三醋酸纤维素:人造丝、 二醋酸和三醋酸纤维素:人造丝、薄膜 一醋酸纤维素:透明高强度塑料、胶卷、 一醋酸纤维素:透明高强度塑料、胶卷、录像带
脱水
15
纤维素醚类
Cell-OR:
R:甲基,乙基,通过与碘甲烷,溴乙烷反应制备。 甲基,乙基,通过与碘甲烷,溴乙烷反应制备。 甲基 -CH2CH2OH:与环氧乙烷反应制备; OH:与环氧乙烷反应制备 与环氧乙烷反应制备; -CH2COOH:与氯乙酸反应制备,得到羧甲基纤维素。 :与氯乙酸反应制备,得到羧甲基纤维素。 水溶性高分子,用做表面活性剂,食品工业, 水溶性高分子,用做表面活性剂,食品工业,纺 织品工业中常用。 织品工业中常用。
19
(2) 聚乙烯醇的缩醛化: ) 聚乙烯醇的缩醛化:
7
b. 静电效应:邻近基团的静电效应可降低或提高功能基的反 静电效应 效应: 应活性。 应活性。 如聚丙烯酰胺的水解反应速率随反应的进行而增大, 如聚丙烯酰胺的水解反应速率随反应的进行而增大,其原 因是水解生成的羧基与邻近的未水解的酰胺基反应生成酸酐环 状过渡态,从而促进了酰胺基中-NH2的离去加速水解。 的离去加速水解。 状过渡态,从而促进了酰胺基中
14
醋酸纤维
浓硫酸/醋酸 浓硫酸 醋酸 溶胀、 溶胀、催化剂 用途 二醋酸和三醋酸纤维素:人造丝、 二醋酸和三醋酸纤维素:人造丝、薄膜 一醋酸纤维素:透明高强度塑料、胶卷、 一醋酸纤维素:透明高强度塑料、胶卷、录像带
脱水
15
纤维素醚类
Cell-OR:
R:甲基,乙基,通过与碘甲烷,溴乙烷反应制备。 甲基,乙基,通过与碘甲烷,溴乙烷反应制备。 甲基 -CH2CH2OH:与环氧乙烷反应制备; OH:与环氧乙烷反应制备 与环氧乙烷反应制备; -CH2COOH:与氯乙酸反应制备,得到羧甲基纤维素。 :与氯乙酸反应制备,得到羧甲基纤维素。 水溶性高分子,用做表面活性剂,食品工业, 水溶性高分子,用做表面活性剂,食品工业,纺 织品工业中常用。 织品工业中常用。
19
(2) 聚乙烯醇的缩醛化: ) 聚乙烯醇的缩醛化:
高分子化学全套PPT课件-2024鲜版

包装薄膜
高分子包装薄膜具有优异的阻隔性能、耐 候性能和加工性能,广泛应用于食品、药
品、日用品等领域。
2024/3/28
包装容器
高分子材料制成的包装容器具有重量轻、 耐冲击、不易破碎等优点,如PET塑料瓶、 高分子复合材料包装罐等。
发展趋势
随着环保意识的提高,可降解高分子包装 材料、生物基高分子包装材料等将成为未 来包装领域的发展重点。
高分子化学全套PPT课 件
2024/3/28
1
目
录
2024/3/28
• 高分子化学概述 • 高分子合成方法 • 高分子结构与性能 • 高分子物理与化学性质 • 高分子材料制备与加工 • 高分子材料应用领域及发展趋势
2 contents
01
高分子化学概述
2024/3/28
3
高分子化学定义与发展
高分子化学定义
塑料原料选择与预处理
包括合成树脂、填料、增塑剂、稳定剂等原料的 选择及预处理方法。
塑料加工设备与模具
介绍塑料加工中常用的设备如注塑机、挤出机、 吹塑机等,以及模具的设计与制造。
ABCD
2024/3/28
塑料成型工艺
详细阐述注塑、挤出、吹塑、压延等成型工艺的 原理、特点及应用。
塑料制品质量控制与检测
分析塑料制品常见的质量问题,提出相应的控制 措施及检测方法。
高分子包装薄膜具有优异的阻隔性能、耐 候性能和加工性能,广泛应用于食品、药
品、日用品等领域。
2024/3/28
包装容器
高分子材料制成的包装容器具有重量轻、 耐冲击、不易破碎等优点,如PET塑料瓶、 高分子复合材料包装罐等。
发展趋势
随着环保意识的提高,可降解高分子包装 材料、生物基高分子包装材料等将成为未 来包装领域的发展重点。
高分子化学全套PPT课 件
2024/3/28
1
目
录
2024/3/28
• 高分子化学概述 • 高分子合成方法 • 高分子结构与性能 • 高分子物理与化学性质 • 高分子材料制备与加工 • 高分子材料应用领域及发展趋势
2 contents
01
高分子化学概述
2024/3/28
3
高分子化学定义与发展
高分子化学定义
塑料原料选择与预处理
包括合成树脂、填料、增塑剂、稳定剂等原料的 选择及预处理方法。
塑料加工设备与模具
介绍塑料加工中常用的设备如注塑机、挤出机、 吹塑机等,以及模具的设计与制造。
ABCD
2024/3/28
塑料成型工艺
详细阐述注塑、挤出、吹塑、压延等成型工艺的 原理、特点及应用。
塑料制品质量控制与检测
分析塑料制品常见的质量问题,提出相应的控制 措施及检测方法。
高分子化学 第六章 离子聚合

38
五、影响阳离子聚合速率常数 的因素
~~CH2–CH–A X ~~CH2–CH+A– X
共价键化合物
~~CH2–CH+┆┇A– X
紧密离子对
~~CH2–CH+ + A– X
松散离子对
自由离子
39
1.溶剂
溶剂的极性和溶剂化能力越大,则聚合 体系中自由离子和松散离子对的比例就越高, 结果会使聚合速率和聚合度增大,而产物的 规整性下降。
• 二、同一对单体采用不同机理进行共聚,竞 聚率和共聚物组成有较大差别。 • 二、离子共聚的单体极性往往相近,有理想 共聚的倾向。 • 三、离子共聚时,溶剂、反离子、温度等对 单体的活性和竞聚率有较大影响。
46
47
一、聚异丁烯
CH3 CH2─C CH3
n
48
聚异丁烯分子量在1.5×104才显示出一定的 强度和弹性,可作橡胶使用。 其主链、侧基均不含不饱和键,化学稳定 性和耐老化性良好,适宜用作化工设备及 管道衬里。
53
四、聚甲醛
• n H-C-H O=
] -CH2-O-n [
• 聚甲醛是一种工程塑料,产量居第三位。它 具有优良的耐磨性、耐疲劳性、耐蠕变性, 较高的刚性、耐冲击性能,尺寸稳定性好、 电绝缘性能优良,耐有机溶剂性能突出。但 热稳定性较差。
54
• 代替金属铜、锌、铝等制造各种零件,例 如齿轮、轴承等,用于汽车工业、机械制 造、电子、精密仪器等。
相关主题
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020/10/20
(1) 电子转移引发——碱金属(alkali metal) 如 Li、Na、K等。 • 电子直接转移引发。
碱金属将最外层的一个价电子直接转移给单体, 生成自由基-阴离子,自由基末端很快偶合终止, 生成双阴离子,而后引发聚合。
M + CH 2 CH X
M CH 2 CH X
M CH CH 2 X
H2N CH2 C C6H5
金属烷基化合物
引发活性与金属电负性有关,若M—C的 极性愈强,引发活性愈大。 丁基锂(butyllithium) 是最常见的阴离子 聚合引发剂,它以离子对的形式引发丁二 烯、异戊二烯聚合,并有缔合现象 (association phenomenon)。
2020/10/20
2020/10/20
化学计量(stoichiometric)聚合具有以下特点: • 引发剂很快形成阴离子活性中心,至单体耗尽仍 保持活性,即形成活性聚合物; • 聚合物分子量均一; • 聚合度与引发剂浓度、单体浓度有关,可定量计 算。
2020/10/20
§6. 2.6 无终止阴离子聚合反应动力学(书P172) (1)聚合速率:
第六章 离子聚合
(ionic polymerization) §6. 1引言(introduction)(书P156)
离子聚合的活性中心——离子(ion)或离子对(ionpair)
离子聚合
根据活性中心 的电荷性质
阳离子聚合 阴离子聚合
离子聚合机理和动力学研究不及自由基聚合成熟。
2020/10/20
离子聚合的特点: • 对单体的选择性高; • 聚合条件苛刻; • 聚合速率快,需在低温下进行; • 许多引发体系为非均相; • 反应介质对聚合有很大影响。
一些重要的聚合物,如丁基橡胶、异戊橡胶、聚 甲醛、聚氯醚等只能通过离子聚合制得。
2020/10/20
§6. 1 阴离子聚合(anionic polymerization) (P168)
反应通式:
A B +M
BM A
M Mn
B :阴离子活性中心,一般由亲核试剂(nucleophile) 提供;
A :为反离子,一般为金属离子(metallic ion)。
2020/10/20
微量杂质如水、氧、二氧化碳等都易使 碳阴离子终止。
阴离子聚合必须在高真空或惰性气氛下, 试剂和玻璃器皿非常洁净的条件下进行。
在无终止聚合的情况下,当单体全部作用 以后,常加入水、醇、酸、胺等链转移剂 使活性聚合物终止。
阴离子聚合机理的特点:
2020/10/20
快引发、慢增长、无终止
§6. 2.3 阴离子聚合引发剂和单体的匹配(书P170) (matching)
与自由基聚合相比,阴离子聚合的单体对 引发剂有较强的选择性,只有当引发剂与 单体活性相匹配才能得到所需的聚合物。 匹配情况见表6-2,表中按引发剂活性由 强到弱、单体聚合活性由弱到强的次序排 列。箭头连接的单体和引发剂都可以进行 阴离子聚合。
2020/10/20
§6.2.1 阴离子聚合的烯类单体(书P168) 烯类、基化合物、含氧三元杂环以及含氮杂环的 单体。
以烯类单体为例:
含吸电子基的烯类单体原则上都可以进行阴离子 聚合。 • 吸电子基能使 C=C上的电子云密度降低,有 利于阳离子的进攻;
• 吸电子基也使碳阴离子增长种的电子云密度 分散,能量降低而稳定。
• 环氧乙烷、环氧丙烷、己内酰胺等杂环化合 物,可由阴离子催化剂开环聚合。
2020/10/20
§6. 2.2 阴离子聚合的引发剂和引发反应
阴离子聚合引发剂——电子给体,即亲核试剂, 属于碱类。 按引发机理分为: • 电子转移引发,如碱金属、碱金属芳烃引发剂; • 阴离子加成引发,如有机金属化合物。
2020/10/20
(2) 有机金属化合物——阴离子加成引发 ——最常用的阴离子聚合引发剂。
主要有金属氨基化合物、金属烷基化合物、 格利雅试剂等。
金属胺基化合物的引发过程如下:
2K NH 3 2KNH 2 H 2
KNH2
K + NH2
形成单阴离子
NH2 + CH2=CH
2020/10/20
C6H5
2020/10/20
§6. 2. 4 活性聚合(living polymerization) (书P171) (1) 定性描述 离子聚合无双基终止,阴离子聚合主要通过向单体转移终止; 阴离来自百度文库聚合,尤其是非极性的共轭烯烃,链转移都不易,成 为无终止聚合,形成“活”的聚合物。 阴离子聚合无终止的主要原因: • 活性链上脱负氢离子困难。 • 反离子一般为金属阳离子,无法从其中夺取某个原子或 H+ 而终止。
无终止的阴离子聚合速率可以简单地由增长速率表 示:
2M CH CH2
X 钠引发丁二烯生产丁钠橡胶 (bun2a02r0u/1b0b/2e0r),属此类。
M CH CH2 CH2 CH M
X
X
双阴离子
• 电子间接转移引发
碱金属—芳烃复合引发剂 碱金属将最外层的一个价电子转移给中间体,使 中间体变为自由基—阴离子,再引发单体聚合。 同样形成双阴离子。 典例:钠萘在四氢呋喃(THF)中引发苯乙烯聚合。
2020/10/20
表6-2
书P169
• A类单体:非极性共轭烯烃,用a类强的阴离子引发剂才能引发聚合; • B类单体:极性单体,用格利雅在非极性溶剂中可制得立体规整聚合物; • C类单体:主要以自由基机理聚合,也可用b、c类引发剂引发阴离子聚合; • D类单体:阴离子聚合活性很高,引发剂和单体活性基团易起反应而失活。
( 2) 活性聚合物和化学计量聚合
活性聚合物:
1956年对萘钠在THF中引发
苯乙烯聚合时首先发现的。
主要特征:分子量分布很窄,即具有单分散性。
形成过程:引发剂先定量地形成阴离子活性中 心,然后以相同的速率链增长,直至单体全部 消耗,使每个活性链以相同几率分享全部单体, 生成的聚合物分子量非常接近。
2020/10/20
• In fact,具有π-π共轭体系的烯类单体才能 进行阴离子聚合,如苯乙烯、丁二烯、丙烯腈、 硝基乙烯及丙烯酸酯类。
• 氯乙烯、醋酸乙烯酯等单体,它们的P-π共 轭效应与诱导效应相反,减弱了双键电子云密 度下降的程度,不利于阴离子聚合。
• 甲醛既能阳离子聚合,又能阴离子聚合。
(1) 电子转移引发——碱金属(alkali metal) 如 Li、Na、K等。 • 电子直接转移引发。
碱金属将最外层的一个价电子直接转移给单体, 生成自由基-阴离子,自由基末端很快偶合终止, 生成双阴离子,而后引发聚合。
M + CH 2 CH X
M CH 2 CH X
M CH CH 2 X
H2N CH2 C C6H5
金属烷基化合物
引发活性与金属电负性有关,若M—C的 极性愈强,引发活性愈大。 丁基锂(butyllithium) 是最常见的阴离子 聚合引发剂,它以离子对的形式引发丁二 烯、异戊二烯聚合,并有缔合现象 (association phenomenon)。
2020/10/20
2020/10/20
化学计量(stoichiometric)聚合具有以下特点: • 引发剂很快形成阴离子活性中心,至单体耗尽仍 保持活性,即形成活性聚合物; • 聚合物分子量均一; • 聚合度与引发剂浓度、单体浓度有关,可定量计 算。
2020/10/20
§6. 2.6 无终止阴离子聚合反应动力学(书P172) (1)聚合速率:
第六章 离子聚合
(ionic polymerization) §6. 1引言(introduction)(书P156)
离子聚合的活性中心——离子(ion)或离子对(ionpair)
离子聚合
根据活性中心 的电荷性质
阳离子聚合 阴离子聚合
离子聚合机理和动力学研究不及自由基聚合成熟。
2020/10/20
离子聚合的特点: • 对单体的选择性高; • 聚合条件苛刻; • 聚合速率快,需在低温下进行; • 许多引发体系为非均相; • 反应介质对聚合有很大影响。
一些重要的聚合物,如丁基橡胶、异戊橡胶、聚 甲醛、聚氯醚等只能通过离子聚合制得。
2020/10/20
§6. 1 阴离子聚合(anionic polymerization) (P168)
反应通式:
A B +M
BM A
M Mn
B :阴离子活性中心,一般由亲核试剂(nucleophile) 提供;
A :为反离子,一般为金属离子(metallic ion)。
2020/10/20
微量杂质如水、氧、二氧化碳等都易使 碳阴离子终止。
阴离子聚合必须在高真空或惰性气氛下, 试剂和玻璃器皿非常洁净的条件下进行。
在无终止聚合的情况下,当单体全部作用 以后,常加入水、醇、酸、胺等链转移剂 使活性聚合物终止。
阴离子聚合机理的特点:
2020/10/20
快引发、慢增长、无终止
§6. 2.3 阴离子聚合引发剂和单体的匹配(书P170) (matching)
与自由基聚合相比,阴离子聚合的单体对 引发剂有较强的选择性,只有当引发剂与 单体活性相匹配才能得到所需的聚合物。 匹配情况见表6-2,表中按引发剂活性由 强到弱、单体聚合活性由弱到强的次序排 列。箭头连接的单体和引发剂都可以进行 阴离子聚合。
2020/10/20
§6.2.1 阴离子聚合的烯类单体(书P168) 烯类、基化合物、含氧三元杂环以及含氮杂环的 单体。
以烯类单体为例:
含吸电子基的烯类单体原则上都可以进行阴离子 聚合。 • 吸电子基能使 C=C上的电子云密度降低,有 利于阳离子的进攻;
• 吸电子基也使碳阴离子增长种的电子云密度 分散,能量降低而稳定。
• 环氧乙烷、环氧丙烷、己内酰胺等杂环化合 物,可由阴离子催化剂开环聚合。
2020/10/20
§6. 2.2 阴离子聚合的引发剂和引发反应
阴离子聚合引发剂——电子给体,即亲核试剂, 属于碱类。 按引发机理分为: • 电子转移引发,如碱金属、碱金属芳烃引发剂; • 阴离子加成引发,如有机金属化合物。
2020/10/20
(2) 有机金属化合物——阴离子加成引发 ——最常用的阴离子聚合引发剂。
主要有金属氨基化合物、金属烷基化合物、 格利雅试剂等。
金属胺基化合物的引发过程如下:
2K NH 3 2KNH 2 H 2
KNH2
K + NH2
形成单阴离子
NH2 + CH2=CH
2020/10/20
C6H5
2020/10/20
§6. 2. 4 活性聚合(living polymerization) (书P171) (1) 定性描述 离子聚合无双基终止,阴离子聚合主要通过向单体转移终止; 阴离来自百度文库聚合,尤其是非极性的共轭烯烃,链转移都不易,成 为无终止聚合,形成“活”的聚合物。 阴离子聚合无终止的主要原因: • 活性链上脱负氢离子困难。 • 反离子一般为金属阳离子,无法从其中夺取某个原子或 H+ 而终止。
无终止的阴离子聚合速率可以简单地由增长速率表 示:
2M CH CH2
X 钠引发丁二烯生产丁钠橡胶 (bun2a02r0u/1b0b/2e0r),属此类。
M CH CH2 CH2 CH M
X
X
双阴离子
• 电子间接转移引发
碱金属—芳烃复合引发剂 碱金属将最外层的一个价电子转移给中间体,使 中间体变为自由基—阴离子,再引发单体聚合。 同样形成双阴离子。 典例:钠萘在四氢呋喃(THF)中引发苯乙烯聚合。
2020/10/20
表6-2
书P169
• A类单体:非极性共轭烯烃,用a类强的阴离子引发剂才能引发聚合; • B类单体:极性单体,用格利雅在非极性溶剂中可制得立体规整聚合物; • C类单体:主要以自由基机理聚合,也可用b、c类引发剂引发阴离子聚合; • D类单体:阴离子聚合活性很高,引发剂和单体活性基团易起反应而失活。
( 2) 活性聚合物和化学计量聚合
活性聚合物:
1956年对萘钠在THF中引发
苯乙烯聚合时首先发现的。
主要特征:分子量分布很窄,即具有单分散性。
形成过程:引发剂先定量地形成阴离子活性中 心,然后以相同的速率链增长,直至单体全部 消耗,使每个活性链以相同几率分享全部单体, 生成的聚合物分子量非常接近。
2020/10/20
• In fact,具有π-π共轭体系的烯类单体才能 进行阴离子聚合,如苯乙烯、丁二烯、丙烯腈、 硝基乙烯及丙烯酸酯类。
• 氯乙烯、醋酸乙烯酯等单体,它们的P-π共 轭效应与诱导效应相反,减弱了双键电子云密 度下降的程度,不利于阴离子聚合。
• 甲醛既能阳离子聚合,又能阴离子聚合。
