Fenoprofen Calcium_34597-40-5_DataSheet_MedChemExpress
分可靖

分可靖这是一个重定向条目,共享了醋氯芬酸的内容。
为方便阅读,下文中的醋氯芬酸已经自动替换为分可靖,可点此恢复原貌,或使用备注方式展现目录1 分可靖说明书1.1 药品名称1.2 英文名称1.3 别名1.4 分类1.5 剂型1.6 分可靖的药理作用1.7 分可靖的药代动力学1.8 分可靖的适应证1.9 分可靖的禁忌证1.10 注意事项1.11 分可靖的不良反应1.12 分可靖的用法用量1.13 药物相互作用1 分可靖说明书1.1 药品名称分可靖1.2 英文名称Aceclofenac1.3 别名爱芬;贝速清;醋氯芬酸;风宁;俊能;莱亿芬;美诺芬;舒力;维朴芬;喜力特;乙酰氯芬酸;Airtal;Biofenac1.4 分类神经系统药物> 解热镇痛药> 其他1.5 剂型1.50mg,100mg。
贮法:遮光、密闭、干燥处保存。
2.分可靖胶囊:50mg,100mg。
贮法:遮光、密闭、干燥处保存。
3.分可靖肠溶片:25mg,100mg。
贮法:密闭、阴凉、干燥处保存。
4.分可靖肠溶胶囊:100mg。
贮法:密闭保存。
1.6 分可靖的药理作用分可靖为非甾体类抗炎药(NSAIDs),作用类似于双氯芬酸,可抗炎、镇痛。
其作用机制主要是通过抑制环加氧酶活性而减少前列腺素的合成。
此外,分可靖尚可促进软骨修复。
1.7 分可靖的药代动力学据国外文献报道,分可靖口服后吸收迅速而完全,1.25~3h达血药浓度峰值,生物利用度接近100%,血浆蛋白结合率大于99.7%,在滑膜液中的浓度为血药浓度的60%,分布容积约30L。
分可靖在肝脏代谢为双氯芬酸及活性极微的4-羟基分可靖,约2/3的药物主要以结合形式的羟基化代谢物随尿排泄,尿中原型药物仅占给药量的1%,消除率约为6L/h,平均消除半衰期为4~4.3h。
1.8 分可靖的适应证用于骨性关节炎、类风湿性关节炎和强直性脊椎炎等引起的疼痛和炎症的症状治疗。
1.9 分可靖的禁忌证1.对分可靖及其他NSAIDs过敏者。
凯纷氟比洛芬酯注射液说明书

氟比洛芬酯注射液窗体顶端药品名称:通用名称:氟比洛芬酯注射液英文名称:FlurbiprofenAxetilInjection商品名称:凯纷成份:氟比洛芬酯适应症:术后及癌症的镇痛。
规格:5ml:50mg用法用量:通常成人每次静脉给予氟比洛芬酯50mg,尽可能缓慢给药(1分钟以上),根据需要使用镇痛泵,必要时可重复应用。
并根据年龄、症状适当增减用量。
一般情况下,本品应在不能口服药物或口服药物效果不理想时应用。
不良反应:1.严重不良反应:罕见休克、急性肾衰、肾病综合征、胃肠道出血、伴意识障碍的抽搐。
2.在氟比洛芬的其他制剂的研究中还观察到以下严重不良反应:罕见再生障碍性贫血、中毒性表皮坏死症(Lyell综合症)、剥脱性皮炎。
3.一般的不良反应:1.注射部位:偶见注射部位疼痛及皮下出血;2.消化系统:有时出现恶心、呕吐,转氨酶升高,偶见腹泻,罕见胃肠出血;3.精神和神经系统:有时出现发热,偶见头痛、倦怠、嗜睡、畏寒;4.循环系统:偶见血压上升、心悸;5.皮肤:偶见瘙痒、皮疹等过敏反应;6.血液系统:罕见血小板减少,血小板功能低下。
禁忌:1.已知对本品过敏的患者。
2.服用阿司匹林或其他非甾体类抗炎药后诱发哮喘、荨麻疹或过敏反应的患者。
3.禁用于冠状动脉搭桥手术(CABG)围手术期疼痛的治疗。
4.有应用非甾体抗炎药后发生胃肠道出血或穿孔病史的患者。
5.有活动性消化道溃疡/出血,或者既往曾复发溃疡/出血的患者。
6.重度心力衰竭患者、高血压患者。
7.严重的肝、肾及血液系统功能障碍患者。
8.正在使用依诺沙星、洛美沙星、诺氟沙星的患者。
警告:以下患者禁用:1.已知对本品过敏的患者。
2.服用阿司匹林或其他非甾体类抗炎药后诱发哮喘、荨麻疹或过敏反应的患者。
3.禁用于冠状动脉搭桥手术(CABG)围手术期疼痛的治疗。
4.有应用非甾体抗炎药后发生胃肠道出血或穿孔病史的患者。
5.有活动性消化道溃疡/出血,或者既往曾复发溃疡/出血的患者。
盐酸非索非那定片说明书

核准日期:2021年4月12日修改日期:2021年6 月8日盐酸非索非那定片说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:盐酸非索非那定片英文名称:Fexofenadine Hydrochloride Tablets汉语拼音:Yansuan Feisuofeinading Pian【成份】本品主要成份为盐酸非索非那定。
化学名称:2-[4-[(1RS)-1-羟基-4-(4-羟基二苯甲基)–哌啶-1-基)丁基]苯基]-2-甲基丙酸盐酸盐化学结构式:分子式:C32H39NO4·HCl分子量:538.13【性状】本品为浅红色胶囊型薄膜包衣片,一面刻有数字“012”,另一面刻有字母“e”,除去包衣后显白色。
【适应症】适用于缓解成人和12岁及12岁以上儿童的季节性过敏性鼻炎的相关症状。
如打喷嚏,流鼻涕,鼻、上腭、喉咙发痒,眼睛发痒、潮湿、发红。
【规格】120mg【用法用量】成人、12岁及12岁以上儿童:口服,一日一次,一次120mg,用水送服。
肾功能不全患者的推荐起始剂量为60mg,一日一次。
【不良反应】以下列出的不良反应的发生率采用如下定义:十分常见(≥10%);常见(≥1%,<10%);偶见(≥0.1%,<1%);罕见(≥0.01%,<0.1%);十分罕见(<0.01%);未知(依据现有数据而不能确定)。
在对季节性过敏性鼻炎等适应症进行的安慰剂对照临床研究中,与安慰剂相比,报告了以下不良事件,其发生率与安慰剂相当:各类神经系统疾病:常见:头痛(>3%),嗜睡(1-3%),头晕(1-3%)胃肠系统疾病:常见:恶心(1-3%)在对季节性过敏性鼻炎等适应症进行的所有对照临床研究中,报告了以下不良事件,其发生率低于1%且与安慰剂相似:胃肠系统疾病:未知:口干全身性疾病及给药部位各种反应:偶见:疲乏在成人中,在上市后监测期间报告了以下不良事件。
发生率未知,无法从现有数据中确定。
免疫系统疾病:已报告过敏反应,包括面部和颈部突然肿胀(血管神经性水肿),胸闷,呼吸困难,潮热和其它全身性速发过敏反应。
依达拉奉分子量

依达拉奉分子量一、什么是依达拉奉依达拉奉(Ibuprofen)是一种非处方药,也是一种非甾体抗炎药(NSAID)。
它主要用于缓解轻度至中度的疼痛和发热,例如头痛、牙痛、关节痛、肌肉痛、感冒和流感引起的发热等。
二、依达拉奉的分子量依达拉奉的化学式为C13H18O2,分子量为206.29克/摩尔。
它是一种白色结晶性固体,熔点为76-77℃。
三、依达拉奉的化学结构依达拉奉的化学结构如下所示:H H| |H - C = C - C - C - O - CH3| |H CH3四、依达拉奉的药理作用依达拉奉通过抑制前列腺素合成酶(COX)的活性来发挥其药理作用。
COX是一种酶,参与合成前列腺素,而前列腺素是一种促炎症物质。
通过抑制COX的活性,依达拉奉可以减少前列腺素的合成,从而减轻炎症反应和疼痛。
五、依达拉奉的药代动力学1. 吸收依达拉奉在口服后很快被吸收,达到峰值浓度的时间约为1-2小时。
2. 分布依达拉奉主要分布在体内组织和液体中,包括血浆、肺、肝脏、肾脏和关节液。
3. 代谢依达拉奉在肝脏中经过代谢,主要通过氧化和脱甲基化反应进行。
4. 排泄依达拉奉的代谢产物主要通过肾脏排泄,小部分通过粪便排泄。
六、依达拉奉的副作用依达拉奉在使用过程中可能会出现一些副作用,包括但不限于:1.胃肠道反应:例如胃痛、恶心、呕吐、腹泻、消化不良等。
2.肝脏损害:长期大剂量使用可能导致肝功能异常。
3.皮肤反应:例如皮疹、荨麻疹等。
4.过敏反应:包括呼吸困难、喉咙肿胀、药物热等。
七、依达拉奉的禁忌症和注意事项依达拉奉有一些禁忌症和注意事项需要特别注意,包括但不限于:1.对依达拉奉过敏的患者禁用。
2.曾经出现哮喘、鼻窦炎、荨麻疹等过敏反应的患者慎用。
3.孕妇、哺乳期妇女、儿童和老年人需在医生指导下使用。
4.心脏病、肝脏病、肾脏病、高血压等患者需在医生指导下使用。
八、依达拉奉的药物相互作用依达拉奉可能与其他药物发生相互作用,包括但不限于:1.抗凝血药物:与依达拉奉合用可能增加出血风险。
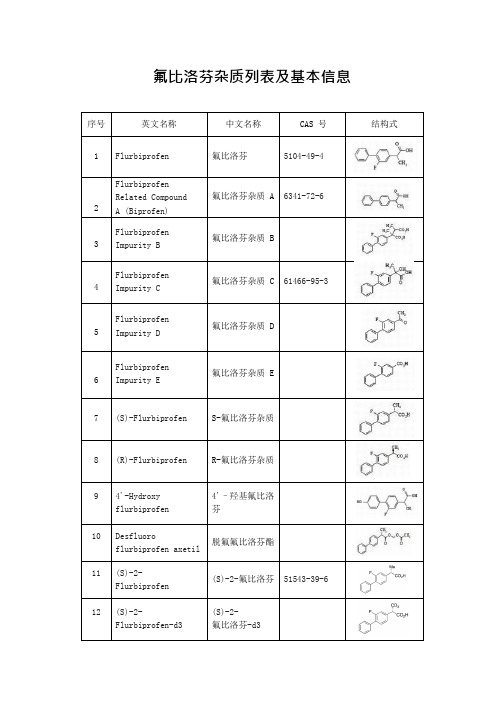
氟比洛芬杂质列表及基本信息
24
(R)-2-Flurbiprofen
(R)-2-氟比洛芬
51543-40-9
25
(R)-2-Flurbiprofen- d3
(R)-2-氟比洛芬
-d3
26
FlurbiprofenAcyl-β-D-glucuronide AllylEster(Mixture
of Diastereomers)
31
3’,4’-Dihydroxy Flurbiprofen
3’,4'–二羟基氟比洛芬
66067-41-2
氟比洛芬酯(Flurbiprofenaxetil)由日本科研制药株式会社研发,于1992年在日本首次上市,适用于术后及癌症的镇痛。卓越生物全面提供氟比洛芬酯研发用杂质对照品和标准品。
序号英文名称中文名称cas号结构式1flurbiprofen氟比洛芬51044942flurbiprofenrelatedcompoundabiprofen氟比洛芬杂质a63417263flurbiprofenimpurityb氟比洛芬杂质b4flurbiprofenimpurityc氟比洛芬杂质c614669535flurbiprofenimpurityd氟比洛芬杂质d6flurbiprofenimpuritye氟比洛芬杂质e7sflurbiprofens氟比洛芬杂质8rflurbiprofenr氟比洛芬杂质94hydroxyflurbiprofen4羟基氟比洛芬10desfluoroflurbiprofenaxetil脱氟氟比洛芬酯11s2flurbiprofens2氟比洛芬5154339612s2flurbiprofend3s2氟比洛芬d313flurbiprofensulfate硫酸氟比洛芬1159977373144hydroxyflurbiprofend34羟基氟比洛芬d3154methoxyflurbiprofen4甲氧基氟比洛芬4163583016methylflurbiprofen甲基氟比洛芬6620286617methylflurbiprofend3甲基氟比洛芬d318sflurbiprofenacyldglucuronides氟比洛芬酰基d葡萄糖19rflurbiprofenacyldglucuronider氟比洛芬酰基d葡萄糖20flurbiprofend3氟比洛芬d3118513381621flurbiprofen13cd3氟比洛芬13cd322flurbiprofenaxetilmixtureofdiastereomers氟比洛芬酯对映异构体的混合物9150379623flurbiprofenacylglucuronideracemicmixture氟比洛芬酰基葡萄糖外消旋混合物24r2flurbiprofenr2氟比洛芬5154340925r2flurbiprofend3r2氟比洛芬d326flurbiprofenacyldglucuronideallylestermixtureofdiastereomers氟比洛芬酰基d葡萄糖烯丙基酯对映异构体的混合物27flurbiprofenacyldglucuronided3mixtureofdiastereomers氟比洛芬酰基d葡萄糖d3对
洛索洛芬(氯索洛芬)杂质种类整理列表

xy Loxoprofen 83599-40-0 10mg-25mg-50mg-100mg
项目报批 纯度高于99.89%
武汉斯坦德供应各种杂质对照品:泊沙康唑杂质、替卡格雷杂质、索拉非尼杂质、索拉菲尼相关杂质、去氧肾上腺素杂质、维生素BI杂质
中文名称英文名称cas规格用途结构式洛索洛芬loxoprofen6876714610mg25mg50mg100mg项目报批纯度高于9989洛索洛芬开环杂质loxoprofenringopeningimpurity109162161210mg25mg50mg100mg项目报批纯度高于9989洛索洛芬相关化合物1loxoprofenrelatedcompound1na10mg25mg50mg100mg项目报批纯度高于9989洛索洛芬相关化合物2loxoprofenrelatedcompound2109162162310mg25mg50mg100mg项目报批纯度高于9989顺羟基洛索洛芬cishydroxyloxoprofen8359940010mg25mg50mg100mg项目报批纯度高于9989武汉斯坦德供应各种杂质对照品
项目报批 纯度高于99.89%
洛索洛芬相关化合 Loxoprofen Related
物1
Compound 1
N/A
10mg-25mg-50mg-100mg
项目报批 纯度高于99.89%
洛索洛芬相关化合 物2
Loxoprofen Related Compound 2
1091621-62-310mg-25mg-50mg-100mg
、马来酸氯苯那敏杂质、瑞格列奈杂质等;并提供COA、NMR、HPLC、MS等图谱。详情请点用户名。
专注各种杂质对照品
代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌
酮替芬成分

酮替芬成分酮替芬是一种非处方药,常用于缓解头痛、发热和关节疼痛等症状。
它的药物成分主要包括酮替芬本身以及辅助成分。
在本文中,我们将详细介绍酮替芬的成分及其作用。
一、酮替芬的主要成分1. 酮替芬(Ketoprofen):它是一种非甾体抗炎药(Nonsteroidal Anti-Inflammatory Drug,简称NSAID),属于苯丙酸类药物。
酮替芬通过抑制体内的环氧化酶(Cyclooxygenase,简称COX)活性,从而减少前列腺素的合成,进而起到抗炎、镇痛和退热作用。
二、辅助成分1. 羟丙基甲基纤维素(Hydroxypropyl methylcellulose):它是一种多聚物,常用作药片的包衣剂或胶囊的填充剂。
羟丙基甲基纤维素具有良好的溶解性和稳定性,并能增加药片的可溶性和延缓释放速度。
2. 硬脂酸镁(Magnesium stearate):它是一种常见的润滑剂,用于减少药片在生产过程中的粘附性,并提高药片的流动性。
硬脂酸镁还能防止药物与机器设备之间的摩擦,从而减少不必要的磨损。
3. 纤维素(Cellulose):纤维素是一种天然聚合物,常用作药片的填充剂和稳定剂。
它具有良好的溶解性和可压缩性,在制造过程中能够提供药片所需的稳定性和均匀性。
4. 玉米淀粉(Corn starch):玉米淀粉是一种常用的填充剂和稳定剂,用于增加药片的质量和体积。
它具有良好的可溶性和流动性,并且容易与其他成分相容。
5. 聚乙二醇(Polyethylene glycol):聚乙二醇是一种多功能辅助成分,常用于调节药物的释放速度、改善口感以及增加药品稳定性。
它具有良好的溶解性,并能与其他成分形成均匀混合物。
6. 二氧化钛(Titanium dioxide):二氧化钛是一种常用的药片着色剂,常用于使药片呈现白色或其他特定颜色。
它具有良好的不溶性和稳定性,并且对人体无毒。
7. 聚山梨酸酯(Polysorbate):聚山梨酸酯是一种表面活性剂,常用于改善药物的可溶性和稳定性。
卡泊芬净说明书

类别:抗微生物药物卡泊芬净药品中文名称:卡泊芬净药品英文名称:Caspofungin本品主要成份:醋酸卡泊芬净..化学名称:1-4R;5S-5-2-氨乙酸氨基-N2-10;12-二甲基-1-羰基十四烷基-4-羟基-L-鸟氨酸-5-3R-3-羟基-L-鸟氨酸肺白菌素B0二乙酸盐..化学结构式:分子式:C52H88N10O152C2H4O2分子量:1 213.42性状本品注射剂为白色或类白色饼状固体..药理毒理1.药理作用:醋酸卡泊芬净是一种由Glarea Lozoyensis发酵产物合成而来的半合成脂肽Echinocandin化合物..卡泊芬净能抑制1;3-β-D-葡聚糖合成酶..该酶作用于细胞膜;可催化转运尿苷二磷酸中的葡聚糖基生成1;3-β-D-葡聚糖..为真菌生长所必需;抑制该酶可使细胞壁结构异常;致使细胞破坏;细胞内容物渗漏..哺乳类动物的细胞中不存在1;3-β-D-葡聚糖..体外药理学研究显示;卡泊芬净对许多种致病性曲霉菌属和念珠菌属真菌具有抗菌活性..目前尚未建立针对1;3-β-D-葡聚糖合成抑制剂检测的标准药物敏感性试验方法..而且药物敏感性试验的结果也不一定与临床结果有必然联系..卡泊芬净是新一类的抗真菌药;具有广谱抗真菌活性;对耐氟康唑的念珠菌、曲霉菌、孢子菌等真菌均有较好的活性..尤其对氟康唑、伊曲康唑耐药的上述病原菌也具抗真菌活性..应用本品治疗上述敏感菌所致的侵袭性曲霉病和念珠菌感染均获较满意疗效..在有限的安全性评价病例中;其不良反应发生率明显低于两性霉素B..2.临床试验:1侵袭性曲霉菌病:在一项开放、无对照组的研究中;对患有肺部或肺部以外侵袭性曲霉菌病IA的病人年龄18~80岁进行了使用本品的安全性、耐受性和疗效的研究..这些病人是对其它抗真菌治疗无效采用其它疗法病情继续发展或没有改善;或者是不能耐受肾脏毒性、与药物输注有关的反应或其他急性反应的病人..患肺部曲霉菌病的病人其诊断是确定的;或者是很可能的..而肺部以外曲霉菌病的病人其诊断都是确定的..病人在接受单剂量70mg的负荷剂量后;每日给药50mg..平均持续的治疗时间为31.1天范围:1~162天..81%的病人为对既往抗真菌治疗无效的病人;而且他们中的大多数病人患有血液系统恶性肿瘤;或者接受了同种异基因骨髓移植..由一个独立的专家小组对病人的资料进行了分析..在接受了至少一剂本品治疗的病人中;有41%的病人22/54治疗有效..即所有体征和症状以及有关的放射学表现彻底消失完全有效或者出现临床意义的改善部分有效..病情稳定、又未表现出现恶化被认为是治疗无效..在接受了7天以上本品治疗的病人中;有49%的病人22/45治疗有效..对于既往治疗无效或不能耐受的病人;本品治疗的有效率分别为34%15/44和70%7/10..另外;还对206名患侵袭性曲霉菌病的病人与上述研究较好地匹配的医疗记录进行了回顾;以便分析标准治疗非研究性的疗效..与本品在开放、无对照组设计的研究中的有效率41%22/54相比;既往标准治疗的有效率为17%35/206..多变量分析的结果显示;本品的比值比大于3;而且95%可信限大于1;提示使用本品治疗将是有益的;2发烧、中性粒细胞减少病人中的经验性治疗:共1 111名持续发热和中性粒细胞减少病人入组的一项临床试验使用的治疗药为本品用药方式为首剂70mg负荷剂量;随后每日1次50mg或两性霉素B脂质体用药方式为3mg/kg d..合适入选的病人接受了恶性肿瘤的化疗或造血干细胞移植;都是抗生素治疗无效的中性粒细胞减少者持续96小时小于500个细胞/mm3和发烧者>38.0°C..病人接受治疗直至中性粒细胞恢复正常;治疗期最长28天..然而;已确诊为真菌感染的病人可以延长治疗期..如果病人对药物耐受性良好;但在治疗5天后发烧仍持续和临床症状加重;可以将用药剂量提高至70mg/d对本品而言和5mg/kg d对两性霉素B脂质体而言..总体有效要符合以下5个标准:①成功治疗任何基线的真菌感染;②用药期间或治疗结束7日内无复发的真菌感染;③治疗结束后存活7日;④没有因为与药物有关的毒性或缺乏疗效导致的停药;⑤在中性粒细胞减少期间发烧症状消退..总体来看;本品33.9%和两性霉素B脂质体33.7%一样有效0.2%的差异95.2%CI-5.6;6..本品在成功治疗任何基线的真菌感染方面比两性霉素B脂质体治疗有效率有明显的增高本品组51.9%14/27;两性霉素B脂质体组25.9%7/27 ;没有因为与药物有关的毒性或缺乏疗效导致的停药的病人的百分数本品组89.7%499/556;两性霉素B脂质体组85.5%461/539;本品和两性霉素B脂质体对曲霉菌引起的真菌感染的治疗有效率分别为41.7%5/12和8.3%1/12;对念珠菌引起的真菌感染的治疗有效率分别为66.7%8/12和41.7%5/12;3侵袭性念珠菌病:在一项比较本品和两性霉素B治疗侵袭性念珠菌病的研究中;共入选了239名病人..最常见的诊断是经血流的感染念珠菌菌血症占83%和念珠菌腹膜炎占10%..本品的用药方式为首剂70mg负荷剂量;随后每日一次50mg..而两性霉素B的用药方式为非中性粒细胞减少症的病人0.6~0.7mg/kg d;中性粒细胞减少症的病人0.7~1mg/kg d..同时达到症状消失和念珠菌感染的微生物检测阴性;可判定为治疗有效..共有224名病人纳入了主要疗效分析..其结果显示本品和两性霉素B治疗侵袭性念珠菌病的疗效相当..其中使用本品的有效率为73%80/109;两性霉素B的有效率为62%71/115..为支持此项主要疗效分析研究;对185名静注用药至少5天的病人进行了预定义的疗效分析;结果本品的疗效有效率81%71/88在统计学意义上要优于两性霉素B的疗效65%63/97..对患念珠菌菌血症的病人;主要疗效分析研究显示本品的有效率为72%66/92;两性霉素B的有效率为63%59/94;预先定义的疗效分析研究显示本品有效率为80%57/71;两性霉素B的有效率为65%51/79..针对此两项分析研究;本品和两性霉素B治疗念珠菌菌血症的疗效相当;4食道念珠菌病:大量的临床研究对本品用于治疗食道念珠菌病的疗效进行了评价..在这些临床研究中;所有病人都有食道念珠菌病的症状和微生物学检查结果;多数病人患有严重的艾兹病CD4计数小于50/mm3..在一项大型、随机双盲的研究中;对患有食道念珠菌病的病人持续给予本品每天50mg或静注的氟康唑每天200mg;给药时间为7~21天..两药的整体疗效包括症状消除和内窥镜下病变有所改善相当:本品的有效率为82%;氟康唑为85%..另外两项剂量范围研究评价了本品的3种不同的剂量每天35mg;50mg;70mg和两性霉素B0.5mg/kg d..在第一项研究中;本品每天50mg的总有效率为74%34/46;两性霉素B为63%34/54..在第2项研究中;本品每天50mg的总有效率为90%18/20;两性霉素B为61%14/23..给予本品高于50mg的剂量对食道念珠菌没有更好的疗效;5口咽念珠菌:本品治疗口咽念珠菌的疗效结果是从上述临床研究中入选病人的治疗情况中总结得来..在所有病人中;有效性被定义为所有口咽部症状和可见口咽病变的完全消除..一组病人只患有口咽念珠菌病n=52;另一组病人同时患有口咽念珠菌病和食道念珠菌病n=173..在只患有口咽念珠菌病的病人中;持续治疗7~10天;有14名病人用本品推荐剂量每天50mg治疗;其治疗有效率为93%13/14;而两性霉素B0.5mg/kg d为67%8/12..同时患有口咽念珠菌病和食道念珠菌病的病人的治疗结果;进一步证实本品每天50mg治疗口咽念珠菌的有效性..本品的疗效与两性霉素B和氟康唑相当..本品高于每天50mg的剂量对治疗口咽念珠菌没有更好的疗效..3.毒大约介于25mg/kg 理研究:在小鼠和大鼠中..由静脉注射卡泊芬净;其LD50至50mg/kg之间..尚未在动物中进行长期研究以评估卡泊芬净致癌的可能性..在一系列的体外研究中;未发现卡泊芬净有致突变或具有遗传毒性..另外;在小鼠体内进行的骨髓染色体试验中;当经静脉注射的卡泊芬净剂量高达12.5mg/kg;也没有发现有遗传毒性..药代动力学单剂量卡泊芬净经一小时静脉输注后;其血浆浓度下降呈多相性..输注后立即出现一个短时间的α相..接着出现一个半衰期为9~11小时的β相..另外还会出现一个半衰期为27小时的γ相..影响卡泊芬净血浆清除的主要机制是药物分布而不是排出或生物转化..大约75%放射性标记剂量的药物得到回收;其中有41%在尿中;34%在粪便中..卡泊芬净在给药后的最初30个小时内;很少有排出或生物转化..卡泊芬净与白蛋白的结合率很高大约97%..通过水解和N–乙酰化作用卡泊芬净被缓慢地代谢..有少量卡泊芬净以原型药形式从尿中排出大约为给药剂量的1.4%..原型药的肾脏清除率低..卡泊芬净有两条代谢途径:化学降解为一种开环的缩氨酸复合物;水解为氨基酸和其降解物;包括去氢单氨L747969酪氨酸和N–乙酰基–氢单氨酪氨酸..卡泊芬净的分布容积为9.67升;血浆消除半衰期为9~11小时;主要在肝脏内代谢为非活性产物;中度肝功能不全的患者需调整剂量..适应症用于食管念珠菌病;以及其它药物如两性霉素B、两性霉素B指质体、伊曲康唑等治疗无效或不耐受的侵入性曲霉病..用法用量不可静脉推注;仅供缓慢静脉滴注;持续一小时以上..1.侵入性曲霉病患者:第一天应给予70mg的负荷剂量;随后一日50mg;当剂量增加到一日70mg时;耐受性良好;但是超过此剂量;其安全性和有效性尚未进行充分研究..2.食管念珠菌病患者:一日50mg;由于HIV感染者易发生口咽念珠菌病;可以考虑口服治疗..3.肝脏功能不全的病人:对轻度肝脏功能不全Child-Pugh 评分5~6的病人无需调整剂量..但是对中等程度肝脏功能不全Child-Pugh 评分7~9的病人;推荐在给予首次70mg负荷剂量之后;将本品的每日剂量调整为35mg..对严重肝脏功能不全Child-Pugh 评分大于9的病人;目前尚无用药的临床经验..不良反应1.在临床研究中已有1 440人使用过单剂量或多剂注射用醋酸卡泊芬净:564名发热性中性粒细胞减少的病人经验治疗研究;125名侵袭性念珠菌病病人;285名患有食道念珠菌病和/或口咽念珠菌病的病人;72名侵袭性念珠菌病的病人和394名一期临床的参加者..在经验治疗研究中病人均接受过恶性肿瘤的化疗或进行过造血干细胞的移植..在有明确诊断的念珠菌感染的病人进行的研究中;大多数病人的病情非常严重例如血液系统恶性肿瘤或其他肿瘤;近期大的手术、爱滋病;需要同时进行多种治疗手段..在无对照的曲霉菌病研究中;病人的病情均严重;而且原有的疾病又复杂例如骨髓或外周血干细胞移植;血液恶性肿瘤;实体瘤或器官移植;需要同时进行多种治疗手段..2.在所有接受本品治疗的病人总数989人中;已报告与药物有关的临床和实验室检查异常一般都是轻微的;而且极少导致停药..常见>1/100:1一般情况:发热、头痛、腹痛、寒战;2胃肠:恶心、腹泻、呕吐;3肝脏:肝酶水平升高天冬氨酸转氨酶;丙氨酸转氨酶;碱性磷酸酶;直接胆红素和总胆红素;4肾:血清肌酐增高;5血液:贫血血红蛋白和红细胞压积降低;6心脏:心动过速;7周围血管:静脉炎/血栓性静脉炎;8呼吸系统:呼吸困难;9皮肤:皮疹、瘙痒症、发汗..已报告的可能的组胺介导的症状包括皮疹、面部肿胀、瘙痒、温暖感或支气管痉挛..有使用本品发生过敏性反应的报道..3.上市后经验:已报道有下列上市后不良事件的发生:1肝胆:罕见的肝脏功能失调;2心血管:肿胀和外周浮肿;3实验室异常:高钙血症..4.实验室检查发现:已报告与药物有关的其它实验室检查异常有:低白蛋白、低钾、低镁血症、白细胞减少、嗜酸性粒细胞增多、血小板减少、中性白细胞减少、尿中红细胞增多、部分凝血激酶时间延长、血清总蛋白降低、尿蛋白增多、凝血酶原时间延长、低钠、尿中白细胞增多以及低钙..禁忌对本品中任何成份过敏的病人禁用..注意事项1.不建议将本品与环孢霉素同时使用..已在健康受试者和患者中评价过本品与环孢霉素合用的情况..一些健康受试者在接受2次剂量为3mg/kg的环孢霉素且使用本品治疗后;丙氨酸转氨酶ALT和天冬氨酸转氨酶AST出现不到或等于3倍正常上限ULN水平的一过性升高..但停药后又恢复正常..当本品与环孢霉素同时使用时;本品的曲线下面积AUC会增加大约35%;而血中环孢霉素的水平未改变..在一项40名患者使用本品和环孢霉素1~290天不等平均17.5天的回顾性研究中;没有发现严重的肝脏不良事件..在进行同种异基因造血干细胞移植和实体器官移植的患者中;象事先预期的一样;肝酶异常经常发生;然而;没有患者ALT的升高被认为与用药有关..5名患者AST的升高被认为可能与使用本品或环孢霉素有关;但所有的升高低于正常上限的3.6倍..4名患者由于各种原因引起的实验室肝酶异常停药;其中2名患者被认为可能与使用本品或环孢霉素有关;也可能有其它原因..在前瞻性的侵袭性曲霉菌病和同时使用的研究中;6名患者同时使用本品和环孢霉素2~56天不等;没有发现患者肝酶升高的情况..所有这些结果显示可能的益处超过可能的风险时可以将本品给予接受环孢霉素治疗的患者使用..2.注射用醋酸卡泊芬净的溶解:1不得使用任何含有右旋糖α-D-葡聚糖的稀释液;因为本品在含有右旋糖的稀释液中不稳定..不得将本品与任何其它药物混合或同时输注;因为尚无有关本品与其它静脉输注物;添加物或药物的可配伍性资料..应当用肉眼观察输注液中是否有颗粒物或变色;2第一步;溶解药物中的药物:溶解粉末状药物时;将储存于冰箱中的本品药瓶置于室温下;在无菌条件下加入10.5ml的无菌注射用水、或含有对羟基苯甲酸甲酯和对羟基苯甲酸丙酯的无菌注射用水、或含有0.9%苯甲醇的无菌注射用水..溶解后瓶中药液的浓度将分别为7mg/ml每瓶70mg装或5mg/ml每瓶50mg装..白色至类白色的药物粉末会完全溶解..轻轻地混合;直到获得透明的溶液..应对溶解后的溶液进行肉眼观察是否有颗粒物或变色..保存于25°C或以下温度的此溶液;在24小时之内可以使用;3第二步;配置供病人输注的溶液:配置成供病人输注用溶液的稀释剂为:无菌注射用生理盐水或乳酸化的林格氏溶液..供病人输注用的标准溶液应在无菌条件下将适量已溶解的药物见下表加入250ml的静脉输注袋或瓶中制备..如医疗上需要每日剂量为50mg或35mg;可将输注液的容积减少到100ml..溶液浑浊或出现了沉淀;则不得使用..如输注液储存于25°C或以下温度的环境中;必须在24小时内使用;如储存于2~8°C的冰箱中;必须在48小时内使用..输注液须在大约一小时内经静脉缓慢地输注..3.病人静脉输注液的制备:孕妇及哺乳期妇女用药1.目前尚无有关妊娠妇女使用卡泊芬净的临床资料..在大鼠中;当给母鼠5mg/kg d的申毒剂量时;卡泊芬净导致了胎鼠体重下降;并使头颅和躯干不完全骨化的发生率上升..另外;在此剂量下;大鼠中颈肋的发生率升高..动物试验发现;卡泊芬净能穿过胎盘屏障..除非一定必要;本品不得在妊娠期间使用..2.尚不清楚本药物是否能由人类乳汁排出..因此接受本品治疗的妇女不应哺乳..儿童用药尚未在儿童病人中对醋酸卡泊芬净进行过研究..不推荐18岁以下的病人使用..老年患者用药老年病人65岁或以上无需调整药物刑量..与健康年轻男性相比;健康老年男性和女性65岁或65岁以上的血浆卡泊芬净浓度略有升高AUC大约升高28%..在感染真菌的病人中;年龄不是影响卡泊芬净药代动力学的主要决定因素..CYP 药物相互作用1.体外试验显示;醋酸卡泊芬净对于细胞色素P450系统中任何一种酶都不抑制..在临床研究中;卡泊芬净不会诱导改变其它药物经CYP3A4代谢..卡泊芬净不是P-糖蛋白的底物..对细胞色素P而言;450卡泊芬净是一种不良的底物..2.在2项临床研究中发现;环孢素4mg/kg一次给药;或3mg/kg两次给药能使卡泊芬净的AUC增加大约35%..AUC增加可能是由于肝脏减少了对卡泊芬净的摄取所致..本品不会使环孢素的血浆浓度升高..当与环孢素同时使用时;会出现肝酶ALT和AST水平的一过性升高..在一项40名患者使用本品和环孢素1~290天不等平均17.5天的回顾性研究中;没有发现严重的肝脏不良事件见“注意事项”..3.在健康受试者中进行的临床研究中显示;本品的药代动力学不受伊曲康唑、两性霉素B、麦考酚酸盐、奈非那韦或他克莫司的影响..本品对伊曲康唑、两性霉素B、利福平或有活性的麦考酚酸盐代谢产物的药代动力学也无影响..4.本品能使他克莫司FK-506的12小时血浓度C12h下降26%..对于同时接受这2种药物治疗的病人;建议对他克莫司的血浓度进行标准的检测;同时适当地调整他克莫司的剂量..5.两项药物相互作用的临床研究显示利福平既诱导又抑制卡泊芬净的消除;稳态显示净诱导作用..在其中一项研究中;同一天开始给予利福平和卡泊芬净合用14天..在第二项研究中;单独给予利福平14天使其诱导作用达到稳态;然后再给予利福平和卡泊芬净合用14天..当利福平的诱导作用达到稳态时;卡泊芬净AUC或输注末浓度变化很小;但卡泊芬净谷浓度减少了约30%..利福平的抑制作用表现在当同一天开始使用利福平和卡泊芬净时;卡泊芬净血浆浓度在第一天有短暂的升高AUC升高约60%..当卡泊芬净加至已进行的利福平治疗中;没有发现这种抑制作用;卡泊芬净的浓度没有升高..6.另外;群体药代动力学检查的结果提示;当本品与其它药物清除诱导剂依非韦伦、奈韦拉平、苯妥英、地塞米松或卡马西平同时使用时;可能使卡泊芬净的浓度产生有临床意义的下降..目前获得的数据显示;在卡泊芬净消除中的可诱导药物清除机理更象一种摄取运转过程;而不是代谢..因此;当本品与药物清除诱导剂如依非韦伦、奈韦拉平、利福平、地塞米松、苯妥英或卡马西平同时使用时;应考虑给予本品每日70mg的剂量见“用法用量”..药物过量临床研究中;已使用过的最大剂量为210mg;这一剂量曾在6名健康受试者中单次给予过;耐受良好..另外;每日100mg连续给予21天曾在15名健康受试者使用过;结果耐受良好..卡泊芬净不能由透析清除..规格注射剂:50mg、70mg..贮藏未开封瓶的贮藏:密闭的瓶装冻干粉末应储存于2~8°C..药瓶中溶解液的贮藏:在制备病人的输注液之前;溶解液可储存在25°C或25°C以下维持24小时..稀释后用于病人的输注液:在静注袋或瓶中的最终用于病人的输注液可储存在25°C或25°C以下维持24小时..而在2~8°C的冰箱中可维持48小时..。
米非司酮

药物相互作用
不能与利福平、卡马西平、灰黄霉素、巴比妥类、苯妥英钠、非甾体抗炎药、阿司匹林、肾上腺皮质激素并 用。
安全信息
安全术语
风险术语
安全术语
S22:Do not breathe dust. 不要吸入粉尘。 S36/37/39:Wear suitable protective clothing, gloves and eye/face protection. 穿戴适当的防护服、手套和眼睛/面保护。 S45:In case of accident or if you feel unwell, seek medical advice immediately (show the lable where possible). 发生事故时或感觉不适时,立即求医(可能时出示标签)。 S53:Avoid exposure - obtain special instructions before use. 避免接触,使用前获得特别指示说明。
化合物简介
基本信息 理化性质
计算化学数据 用途
基本信息
化学式:C29H35NO2 分子量:429.594 CAS号:-65-3
理化性质
密度:1.18g/cm3 熔点:195-198°C 沸 点 : 6 2 8 . 6 ºC 闪 点 : 3 3 4 ºC 折射率:1.623 外观:淡黄色结晶性粉末 溶解性:在甲醇或二氯甲烷中易溶,在乙醇或乙酸乙酯中溶解,在水中几乎不溶
鉴别
1、取本品,加乙醇溶解并稀释制成每1mL中约含10μg的溶液,照紫外-可见分光光度法(通则0401)测定, 在304nm与260nm的波长处有最大吸收。
2、本品的红外光吸收图谱应与对照的图谱(光谱集1141图)一致。
布洛芬 有关物质 薄层

布洛芬有关物质薄层摘要:1.布洛芬的基本信息2.布洛芬的相关物质3.薄层色谱法在布洛芬分析中的应用正文:布洛芬(Ibuprofen)是一种非处方药,属于非甾体抗炎药(NSAIDs)类药物,广泛应用于缓解轻至中度疼痛、降低发热和消炎等方面。
其化学名称为2-(4-异丙基苯基)丙酸,化学式为C13H18O2。
布洛芬具有良好的药理作用和广泛的临床应用,但在生产和储存过程中可能会产生一些相关的杂质,这些杂质对药物的安全性和有效性具有重要影响。
布洛芬的相关物质主要包括两个方面:1.生产过程中的副产物,如异丙基苯酚、对异丙基苯酚等。
这些副产物可能由于生产工艺、反应条件等因素而产生。
2.储存过程中产生的降解产物,如布洛芬酸、4-异丙基苯酚等。
这些降解产物可能由于光照、高温、湿度等环境因素影响而导致布洛芬质量变化。
为了确保布洛芬的质量和安全性,需要对其中的相关物质进行分析和控制。
薄层色谱法(Thin Layer Chromatography,TLC)是一种常用的药物分析方法,具有操作简便、分离效果好、灵敏度高等优点。
在布洛芬的相关物质分析中,薄层色谱法可以有效地实现对杂质成分的定性、定量分析。
具体操作过程如下:1.制备薄层板:选用合适的固定相和流动相,将二者按一定比例涂布在玻璃板上,干燥后备用。
2.样品处理:将布洛芬样品进行粉碎、提取、浓缩等处理,获得待测样品溶液。
3.点样:将待测样品溶液分别点在薄层板上,形成斑点。
4.展开:将薄层板放入展开槽中,加入流动相,展开一定时间。
5.显色:将薄层板放入显色槽中,加入显色剂,显色一定时间。
6.观察:用紫外灯或碘蒸气对薄层板进行观察,分析布洛芬样品中的相关物质。
综上所述,布洛芬作为一种广泛应用的药物,其相关物质分析是保证药物质量和安全性的重要环节。
精氨酸布洛芬分子量

精氨酸布洛芬分子量
精氨酸布洛芬的英文名是(S)-2-AMINO-5-GUANIDINOPENTANOIC ACID COMPOUND WITH 2-(4-ISOBUTYLPHENYL)PROPANOIC ACID (1:1),CAS号是57469-82-6,其分子量为380.48200。
精氨酸布洛芬是一种药物,主要用于治疗关节痛、牙痛、痛经和因创伤引起的疼痛等,也可缓解感冒时的发热和头痛症状。
其具体的分子量信息对于普通用户来说可能并不直接相关,但对于药物研发、生产以及质量控制等环节却是至关重要的。
如需更多关于精氨酸布洛芬的信息,建议咨询医疗专家或查阅相关医学文献。
在使用任何药物时,都应遵循医生的指导和建议,确保用药的安全性和有效性。
(凯纷) 氟比洛芬酯注射液说明书

氟比洛芬酯注射液窗体顶端药品名称:通用名称:氟比洛芬酯注射液英文名称:FlurbiprofenAxetilInjection商品名称:凯纷成份:氟比洛芬酯适应症:术后及癌症的镇痛。
规格:5ml:50mg用法用量:通常成人每次静脉给予氟比洛芬酯50mg,尽可能缓慢给药(1分钟以上),根据需要使用镇痛泵,必要时可重复应用。
并根据年龄、症状适当增减用量。
一般情况下,本品应在不能口服药物或口服药物效果不理想时应用。
不良反应:1.严重不良反应:罕见休克、急性肾衰、肾病综合征、胃肠道出血、伴意识障碍的抽搐。
2.在氟比洛芬的其他制剂的研究中还观察到以下严重不良反应:罕见再生障碍性贫血、中毒性表皮坏死症(Lyell综合症)、剥脱性皮炎。
3.一般的不良反应:1.注射部位:偶见注射部位疼痛及皮下出血;2.消化系统:有时出现恶心、呕吐,转氨酶升高,偶见腹泻,罕见胃肠出血;3.精神和神经系统:有时出现发热,偶见头痛、倦怠、嗜睡、畏寒;4.循环系统:偶见血压上升、心悸;5.皮肤:偶见瘙痒、皮疹等过敏反应;6.血液系统:罕见血小板减少,血小板功能低下。
禁忌:1.已知对本品过敏的患者。
2.服用阿司匹林或其他非甾体类抗炎药后诱发哮喘、荨麻疹或过敏反应的患者。
3.禁用于冠状动脉搭桥手术(CABG)围手术期疼痛的治疗。
4.有应用非甾体抗炎药后发生胃肠道出血或穿孔病史的患者。
5.有活动性消化道溃疡/出血,或者既往曾复发溃疡/出血的患者。
6.重度心力衰竭患者、高血压患者。
7.严重的肝、肾及血液系统功能障碍患者。
8.正在使用依诺沙星、洛美沙星、诺氟沙星的患者。
警告:以下患者禁用:1.已知对本品过敏的患者。
2.服用阿司匹林或其他非甾体类抗炎药后诱发哮喘、荨麻疹或过敏反应的患者。
3.禁用于冠状动脉搭桥手术(CABG)围手术期疼痛的治疗。
4.有应用非甾体抗炎药后发生胃肠道出血或穿孔病史的患者。
5.有活动性消化道溃疡/出血,或者既往曾复发溃疡/出血的患者。
苯胺洛芬成分

苯胺洛芬成分一、引言苯胺洛芬是一种常用的非处方药,常用于缓解头痛、发热、肌肉疼痛等症状。
本文将详细介绍苯胺洛芬的成分、作用机制以及使用注意事项。
二、成分苯胺洛芬的化学名称为2-(2-氨基乙基)苯甲酸。
它属于非甾体抗炎药物(Non-Steroidal Anti-Inflammatory Drugs,简称NSAIDs)的一种。
三、作用机制苯胺洛芬通过抑制环氧化酶(Cyclooxygenase,简称COX)的活性,从而抑制前列腺素的合成。
前列腺素是一种在炎症反应中起重要作用的物质,它能引起疼痛、发热和炎症等症状。
苯胺洛芬的抗炎、镇痛和退热作用主要是通过抑制前列腺素的合成来实现的。
苯胺洛芬主要抑制COX-1和COX-2两种同工酶的活性。
COX-1主要参与维持胃肠道黏膜的完整性和血小板聚集,而COX-2则主要参与炎症反应的产生。
苯胺洛芬的选择性抑制作用主要针对COX-2,因此具有较好的抗炎作用,同时对胃肠道和血小板的影响较小。
四、使用注意事项1.用量:根据医生或药师的建议使用,不得超过推荐剂量。
2.适应症:适用于缓解轻至中度疼痛和发热,如头痛、牙痛、关节痛、肌肉痛、感冒等。
3.禁忌症:对苯胺洛芬过敏者禁用,孕妇和哺乳期妇女慎用。
4.不良反应:可能引起胃肠道不适,如恶心、呕吐、腹痛、消化不良等。
少数人可能出现过敏反应,如皮疹、荨麻疹、呼吸困难等。
长期大剂量使用还可能导致肝肾功能损害。
5.注意事项:–不得与其他含有苯胺洛芬的药物同时使用,以免超过推荐剂量。
–长期或大剂量使用时需监测肝肾功能。
–长期使用可能导致胃肠道溃疡和出血,需注意饮食和生活习惯。
–孕妇、哺乳期妇女和儿童使用前应咨询医生。
五、结论苯胺洛芬是一种常用的非处方药,通过抑制前列腺素的合成来实现其抗炎、镇痛和退热作用。
在使用苯胺洛芬时,需要注意用量、适应症、禁忌症以及可能的不良反应和注意事项。
如果遇到不适或有疑问,应及时咨询医生或药师的建议。
(凯纷) 氟比洛芬酯注射液说明书

氟比洛芬酯注射液药品名称:通用名称:氟比洛芬酯注射液英文名称:Flurbiprofen Axetil Injection商品名称:凯纷成份:氟比洛芬酯适应症:术后及癌症的镇痛。
规格:5ml:50mg用法用量:通常成人每次静脉给予氟比洛芬酯50mg,尽可能缓慢给药(1分钟以上) ,根据需要使用镇痛泵,必要时可重复应用。
并根据年龄、症状适当增减用量。
一般情况下,本品应在不能口服药物或口服药物效果不理想时应用。
不良反应:1.严重不良反应:罕见休克、急性肾衰、肾病综合征、胃肠道出血、伴意识障碍的抽搐。
2.在氟比洛芬的其他制剂的研究中还观察到以下严重不良反应:罕见再生障碍性贫血、中毒性表皮坏死症(Lyell综合症) 、剥脱性皮炎。
3.一般的不良反应:1.注射部位:偶见注射部位疼痛及皮下出血;2.消化系统:有时出现恶心、呕吐,转氨酶升高,偶见腹泻,罕见胃肠出血;3.精神和神经系统:有时出现发热,偶见头痛、倦怠、嗜睡、畏寒;4.循环系统:偶见血压上升、心悸;5.皮肤:偶见瘙痒、皮疹等过敏反应;6.血液系统:罕见血小板减少,血小板功能低下。
禁忌:1.已知对本品过敏的患者。
2.服用阿司匹林或其他非甾体类抗炎药后诱发哮喘、荨麻疹或过敏反应的患者。
3.禁用于冠状动脉搭桥手术(CABG)围手术期疼痛的治疗。
4.有应用非甾体抗炎药后发生胃肠道出血或穿孔病史的患者。
5.有活动性消化道溃疡/出血,或者既往曾复发溃疡/出血的患者。
6.重度心力衰竭患者、高血压患者。
7.严重的肝、肾及血液系统功能障碍患者。
8.正在使用依诺沙星、洛美沙星、诺氟沙星的患者。
警告:以下患者禁用:1.已知对本品过敏的患者。
2.服用阿司匹林或其他非甾体类抗炎药后诱发哮喘、荨麻疹或过敏反应的患者。
3.禁用于冠状动脉搭桥手术(CABG)围手术期疼痛的治疗。
4.有应用非甾体抗炎药后发生胃肠道出血或穿孔病史的患者。
5.有活动性消化道溃疡/出血,或者既往曾复发溃疡/出血的患者。
罗氏芬说明书

少有一例死亡的报道;对这名新生儿进行尸检未发现晶体状物质。除了新生儿,在其他病人 中未见类似报道(见【注意事项】)。 伪膜性肠炎及凝血障碍是极其罕见的副作用。 极为罕见的肾脏沉积病例,多见于 3 岁以上儿童,他们曾接受每日大剂量(如每天≥80mg/kg) 治疗,或总剂量超过 10g,并有其他威胁因素(如限制液体、卧床等)。这一事件可以是有 症状的或无症状的,会导致肾功能不全,但停药后可以逆转。
2007 年 11 月 09 日 2009 年 11 月 16 日 2011 年 09 月 01 日 2013 年 01 月 22 日
注射用头孢曲松钠说明书
请仔细阅读说明书并在医师指导下使用
警示:本品不能加入哈特曼氏以及林格氏等含有钙的溶液中使用。 本品与含钙剂或含钙产品合并用药有可能导致致死性结局的不良事件。
局部副作用 在极少的情况下,静脉用药后发生静脉炎,可通过减慢静脉注射速度(2-4 分钟)以减少此 现象的发生。肌肉注射时,如不加用利多卡因会导致疼痛。
【禁忌】 对头孢菌素类抗生素过敏者禁用。对青霉素过敏者也可能对罗氏芬®过敏。 头孢曲松不得用于高胆红素血的新生儿和早产儿的治疗。体外研究表明头孢曲松能取代胆红 素与血清白蛋白结合,导致这些病人有可能发生胆红素脑病的风险。 如果新生儿(≤28 天)需要(或预期需要)使用含钙的静脉输液包括静脉输注营养液治疗, 则禁止使用罗氏芬®,因为有产生头孢曲松-钙沉淀物的风险。
其他罕见副作用 头痛或头晕(0.27%),静脉炎(1.86%),症状性头孢曲松钙盐之胆囊沉积,肝脏转氨酶增 高,少尿,血肌酐增加,生殖道霉菌病,发热,寒战以及过敏性或过敏样反应(支气管痉挛 和血清病等过敏反应)(2.77%)。 与钙的相互作用 两项体外研究对头孢曲松与钙的相互作用进行了评价,其中一项研究使用成年人血浆,另一 项研究使用新生儿脐带血浆。头孢曲松的浓度最高为 1 mM(超过头孢曲松 2g 体内输注 30 分钟以上得到的血药浓度),钙浓度最高为 12 mM(48 mg/dL)。成人血浆中钙浓度为 6 mM (24 mg/dL)或更高时头孢曲松的回收率降低,新生儿血浆中钙浓度为 4 mM(16 mg/dL) 或更高时头孢曲松的回收率降低。这表明可能有头孢曲松-钙沉淀物产生。 有报道在对少数死亡病例进行尸检时,在使用罗氏芬®和含钙输液的新生儿的肺和肾脏中观 察到一种晶体状物质。其中有些病例使用同一根输液管输注罗氏芬®和含钙输液,在一些病 例的输液管中看到了沉淀物。在不同时间经不同输液管输注罗氏芬®和含钙输液的新生儿至
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Caution: Not fully tested. For research purposes only Medchemexpress LLC
m o c . s s e r p x e m e h c d e m . w w w : b e AW Sm U o ,c 0 . 4s 5s 8e 0r p Jx Ne ,m n e oh t c e cd ne i m r P @ o ,f y n a i Wl : ni a om s E n i k l i W 8 1
Mechanisms: Pathways:Others; Target:Others Biological Activity: Fenoprofen Calcium is a nonsteroidal nonsteroidal, anti-inflammatory agent. anti inflammatory antiarthritic agent Target: Prostaglandin G/H synthase 1 Fenoprofen is a non-steroidal anti-inflammatory, antipyretic, analgesic agent advocated for use in rheumatoid arthritis, degenerative joint disease, ankylosing spondylitis and gout. Fenoprofen has a serum half-life of about 150 to 180 minutes and is at least 99% bound to plasma proteins. It is extensively metabolised after oral administration, the main metabolites being fenoprofen glucuronide and 4-hydroxy-fenoprofen glucuronide [1]. Fenoprofen calcium is revealed for relief of mild to moderate pain in adults and for relief of the signs and symptoms of rheumatoid arthritis and osteoarthritis. In p patients with osteoarthritis, , the anti-inflammatory y and analgesic g effects of fenoprofen calcium have been demonstrated by decrease in tenderness as a response to p...
References: [1]. Brogden, R., et al., Fenoprofen: A review of its pharmacological properties and therapeutic efficacy in rheumatic diseases. Drugs, 1977. 13(4): p. 241-265. [2]. /pro/fenoprofen.html
Product Data Sheet
Product Name: CAS No.: Cat. No.: MWt: Formula: Purity :
Fenoprofen Calcium HY-B0288A 522.60 C30H26CaO6 >98%
y Solubility:
DMSO 105 mg/mL; g ; Water <1 mg/mL
