2020春人教版初中化学复习九年级下册必刷题第10单元 课题1 第2课时 酸的化学性质
(含答案)九年级化学人教版下册课时练《第十单元课题1 常见的酸和碱》(2)

答卷时应注意事项1、拿到试卷,要认真仔细的先填好自己的考生信息。
2、拿到试卷不要提笔就写,先大致的浏览一遍,有多少大题,每个大题里有几个小题,有什么题型,哪些容易,哪些难,做到心里有底;3、审题,每个题目都要多读几遍,不仅要读大题,还要读小题,不放过每一个字,遇到暂时弄不懂题意的题目,手指点读,多读几遍题目,就能理解题意了;容易混乱的地方也应该多读几遍,比如从小到大,从左到右这样的题;4、每个题目做完了以后,把自己的手从试卷上完全移开,好好的看看有没有被自己的手臂挡住而遗漏的题;试卷第1页和第2页上下衔接的地方一定要注意,仔细看看有没有遗漏的小题;5、中途遇到真的解决不了的难题,注意安排好时间,先把后面会做的做完,再来重新读题,结合平时课堂上所学的知识,解答难题;一定要镇定,不能因此慌了手脚,影响下面的答题;6、卷面要清洁,字迹要清工整,非常重要;7、做完的试卷要检查,这样可以发现刚才可能留下的错误或是可以检查是否有漏题,检查的时候,用手指点读题目,不要管自己的答案,重新分析题意,所有计算题重新计算,判断题重新判断,填空题重新填空,之后把检查的结果与先前做的结果进行对比分析。
亲爱的小朋友,你们好!经过两个月的学习,你们一定有不小的收获吧,用你的自信和智慧,认真答题,相信你一定会闯关成功。
相信你是最棒的!人教版九年级化学下册《第十单元课题1常见的酸和碱》课堂练习第1课时什么是酸和碱酸碱指示剂1.实验室常用的紫色石蕊溶液是由以下哪位科学家发现的()A.拉瓦锡B.阿伏加德罗C.波义耳D.道尔顿2.实验室有一瓶保管不当使标签残缺的试剂(如图),其溶质可能是()A.单质B.氧化物C.碱D.酸3.下列试剂能使紫色石蕊溶液和无色酚酞溶液都变色的是()A.石灰水B.氯化钠溶液C.盐酸D.乙醇溶液4.下列说法正确的是()A.能使石蕊变蓝的溶液一定是碱溶液B.显酸性的溶液不一定是酸溶液C.不能使酚酞变红的溶液一定显酸性D.酸和碱中一定都含有氢、氧元素5.分类是化学学习和研究常用的方法之一。
初中化学人教版九年级下第十单元课题1-4常见的酸和碱(4)习题

第十单元酸和碱课题1常见的酸和碱(4)习题1.下列变化属于物理变化的是()A.工业上常用稀硫酸来除铁锈B.活性炭使红墨水褪色C.盐酸能使紫色的石蕊试液变红D.浓硫酸使纸变黑2.下列化学反应发生后,将使用过的仪器浸泡于稀盐酸中,然后用水冲洗,不能将仪器处理干净的是()A.久置石灰水的瓶上的白膜 B.用一氧化碳还原氧化铜后的硬质玻璃管C.热水瓶内胆的水垢D.盛放过生锈铁钉后留下红棕色固体的烧杯3.酸雨对下列设施的腐蚀作用较强的是()A.铝制窗框B.铜像C.柏油马路D.木制围栏4.某同学怀疑实验室中纯净水被某种酸严重污染,他设计了几种方法进行检验,其中不可能达到目的是()A.取样品,向其中滴加紫色石蕊试液 B.取样品,向其中加入锌粒C.取样品,向其中滴加无色酚酞试液D.取样品,向其中放入生锈的铁钉5.下列物质可以直接用金属和酸反应制得的是()A.FeCl3B.CuCl2C.AgClD.MgCl26.向盛有氧化铜的试管中加入稀硫酸,微热,观察到的实验现象是,,发生反应的方程式为。
7. 氢氧化钠俗称,在表面皿上放一些固体氢氧化钠,露置在空气中,可以吸收空气中的使其表面,过一段时间,表面又出现白色粉末这是因为吸收了空气中的而变质,反应的化学方程式为。
8.写出用锌、稀硫酸、氧化铜、为原料,用两种方法制取铜的化学方程式:方法一:,;方法二:,。
9.实验室有三瓶失去标签的溶液,分别是稀盐酸、氢氧化钠溶液和澄清的石灰水。
请你选择适当的试剂把这三种溶液鉴别出来,写出实验步骤、现象和结论。
第十单元酸和碱课题1常见的酸和碱(4)习题答案1.B2.B3.A4.C5.D6.黑色粉末消失溶液变为蓝色 CuO+H2SO4==CuSO4+H2O7.火碱(或者烧碱、苛性钠)水蒸气潮解二氧化碳而变质 2NaOH+CO2==Na2CO3+H2O8.(1)Zn+H2SO4==ZnSO4+H2↑ CuO+ H加热Cu+H2O(2)CuO+H2SO4==CuSO4+H2O Zn+CuSO4==Cu+ZnSO49.分别取样于三支试管中,各滴加少量无色酚酞试液,不变色,原溶液为稀盐酸;变红为氢氧化钠溶液和澄清石灰水,再向变红的溶液中通入二氧化碳,溶液变浑浊,原溶液是澄清石灰水;不变浑浊的,原溶液是氢氧化钠溶液。
2020春人教版九年级化学下册 第10单元 10.1.2 第2课时 酸的化学性质(教学设计)

课题1《常见的酸和碱》教学设计(第2课时)
一、教学目标
(一)知识与技能
1.知道浓硫酸和浓盐酸的物理性质;
2.知道浓硫酸的特性。
3.初步学会稀释浓硫酸。
(二)过程与方法
通过浓硫酸的强腐蚀性和稀释实验,学会浓硫酸稀释的方法,强化实验及生活中的安全意识。
(三)情感态度与价值观
通过观察浓硫酸和浓盐酸的物理性质及稀释浓硫酸实验,培养善于观察、总结、勤于思考的科学精神,逐步树立认识来源于实践的观点。
二、教学重点
浓硫酸的强腐蚀性。
三、教学难点
运用实验的方法获取信息,运用比较概括等方法对获取的信息进行加工
四、教学准备
教学设备(投影仪,计算机)、纸小、木棍、布、玻璃棒、导管、双孔橡皮塞、锥形瓶、试管、浓硫酸、浓盐酸。
五、教学过程。
2020春人教版初中化学复习九年级下册必刷题第10单元 课题1 第1课时 酸碱指示剂和几种常见的酸

-11-
浓硫酸稀释的过程中易发生错误操作 10.某实验小组同学准备制取氢气,实验室只有 98%的浓硫酸,小强 用 100mL 的量筒量取了 5mL 浓硫酸,就准备在量筒里加水稀释,小刚见 了马上制止了小强的实验。指出上述已完成的和未完成的实验操作中:
(1)存在的错误有_用__1_0_0_m__L_量__筒___量__取__5_m_L__液__体__;__在__量__筒__内__稀__释___浓__硫__酸_ ; _往__浓__硫__酸___里__加__水_________。
-15-
14.已知 98%浓 H2SO4 密度为 1.84g/cm3,62%浓 HNO3 密度为
1.14g/cm3;若要配制浓 H2SO4 与浓 HNO3 的混合溶液,则应将___H_2_S_O__4 __(填 化学式)沿玻璃棒缓慢倒入盛有___H_N__O_3__(填化学式)的烧杯中,边加边搅拌, 冷却后装瓶。过程中玻璃棒的作用是_引___流__、__搅__拌__。
①硫酸 ②盐酸 ③碳酸 ④醋酸 ⑤柠檬酸
(1)可用于制造药物、金属表面除锈的是__②__。 (2)柠檬、柑橘中含有的酸是__⑤__。 (3)食醋中含有的酸是_④___。
-10-
(4)用于精炼石油、还可用作干燥剂的是__①__。 (5)汽水中大量含有的一种酸是__③__。 (6)存在于人体胃液中,可帮助消化的酸是__②__。 (7)汽车上铅蓄电池中含有的酸是_①___。
该溶液是( C )
A.酸性溶液
B.酸的水溶液
C.碱性溶液
D.碱的水溶液
-2-
2.紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素。花青素遇酸性溶液
变红色,遇碱性溶液变蓝色。在凉拌紫甘蓝丝时,观察到菜丝变成红色,
2020春单元达标必刷常考题100道:初中化学人教版九年级(下)《第十单元 酸和碱》

2020春单元达标必刷常考题100道:初中化学人教版九年级(下)《第十单元酸和碱》一、选择题(共40小题)1.(2017•上海)氢氧化钙俗称()A.烧碱B.纯碱C.熟石灰D.石灰石2.(2011•娄底)家庭生活中一些常见物质的pH如下:物质食醋牛奶食盐水牙膏肥皂水pH2~36~778~99~10当我们被蚊虫叮咬后,蚊虫能在人的皮肤内分泌蚁酸(具有酸的性质),从而使皮肤肿痛。
要减轻痛痒,应在叮咬处涂抹下列物质中的()A.食醋B.牛奶C.食盐水D.牙膏或肥皂水3.(2017•庆阳二模)如图是生活中一些物质的pH,下列说法中不正确的是()A.酱油呈酸性B.肥皂水能使无色酚酞试液变红C.胃酸过多的人适宜多喝玉米粥D.西瓜汁的酸性比苹果汁的酸性强4.(2019•西湖区校级模拟)将浓盐酸、浓硫酸敞口放置一段时间,它们共同的变化是()A.颜色发生改变B.发生化学变化C.质量变大D.溶质的质量分数变小5.(2015春•博山区校级月考)下列物质中,不能够直接证明稀硫酸是酸性溶液的是()A.pH试纸B.无色酚酞试液C.紫色石蕊试液D.蓝色的石蕊试纸6.(2016•邵阳二模)根据下列实验现象,可以判断其溶液一定呈酸性的是()A.滴加酚酞试液显无色的溶液B.滴加石蕊试液显蓝色的溶液C.能够与碱发生反应的溶液D.常温下,pH<7的溶液7.(2013•江都市模拟)下列物质中,能与稀盐酸发生中和反应的是()A.Mg B.MgO C.Mg(OH)2D.MgCO38.向盛有10mL的稀盐酸烧杯中,加入20mL水,则溶液的酸性强弱变化是()A.增强B.减弱C.不变D.无法判定9.(2015•永州)下表是健康人体内一些液体近似pH,其中呈酸性的是()胃液胆汁血浆胰液0.9~1.57.1~7.37.35~7.457.5~8.0A.胃液B.胆汁C.血浆D.胰液10.(2005•桂林)下列物质敞口久置于空气中,质量会变轻的是()A.生石灰B.浓硫酸C.浓盐酸D.石灰水11.(2008•南通)在生活、生产和科学研究中,常用pH试纸测定溶液的pH.以下测定操作正确是()A.将被测液滴到放在玻璃片上的pH试纸上,显色后,与标准比色卡比较B.将pH试纸直接投入被测液中,显色后,取出与标准比色卡比较C.先用少量水湿润试纸,后滴上被测液,显色后,与标准比色卡比较D.先用蒸馏水清洗滴管,随后吸取被测液滴到试纸上,显色后,与标准比色卡比较12.(2004•福州)鱼胆弄破后会使鱼肉粘上难溶于水的胆汁酸(一种酸)而变苦,要减少这种苦味。
人教版化学九年级下册知识点及课时测 第十单元1.2 酸的化学性质

人教版化学九年级下册第十单元课题1常见的酸和碱课时2酸的化学性质1.与指示剂作用酸溶液能使紫色石蕊溶液__变红色__,使无色酚酞溶液__不变色__。
2.与金属反应稀盐酸、稀硫酸能跟活泼金属发生__置换__反应,通常生成金属化合物(盐)和氢气。
Fe+2HCl===FeCl2+H2↑现象:有__气泡__产生,溶液由无色变成__浅绿__色。
Zn+H2SO4===ZnSO4+H2↑现象:有__气泡__产生。
3.与金属氧化物反应稀盐酸、稀硫酸能跟某些金属氧化物(如铁锈)反应,生成金属化合物(盐)和水。
Fe2O3+6HCl===2FeCl3+3H2OFe2O3+3H2SO4===Fe2(SO4)3+3H2O现象:铁锈__溶解__,溶液由无色变为__黄__色。
1.白蚁会蛀蚀木头,它分泌的蚁酸是一种酸,还能腐蚀很多建筑材料。
下列建筑材料最不容易被白蚁腐蚀的是( A )A.铜制品B.钢筋C.大理石D.铝合金2.(2019·重庆中考B卷)假设与排除是探索未知物的一种方法。
《本草纲目拾遗》中记载:“强水性最烈,能蚀五金(金、银、铜、铅、铁)。
”下列物质最可能是“强水”的是( C ) A.硫酸亚铁溶液B.稀盐酸C.浓硝酸和浓盐酸的混合物D.稀硫酸3.盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观的角度分析,该变化过程中改变的是__分子间间隔__。
(2)在盐酸中加入过量的铁粉充分反应。
①下图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号)::__H+__,:__Cl-__,:__Fe2+__;②下列金属中能与盐酸发生类似反应的是__BC__(填字母)。
A.Cu B.MgC.Al D.Ag4.小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适的物质对铁锈进行处理,这种物质是( C )A.汽油B.食盐水C.白醋(主要成分是醋酸) D.米酒5.用稀盐酸除去铁锈主要成分的原理是( D )A.FeO+2HCl===FeCl2+H2OB.FeO+2HCl===FeCl3+H2OC.Fe2O3+6HCl===2FeCl2+3H2OD.Fe2O3+6HCl===2FeCl3+3H2O6.硫酸、盐酸是重要的化工原料。
2020春人教版初中化学复习九年级下册必刷题第10单元 本章热点专练

-17-
①实验结论__N_a_O__H_溶__液__与__稀__盐__酸__恰__好__完__全__反__应_____。 ②从微观的角度分析,该反应的实质是_H__+_和__O__H_-__反__应__生__成__H_2_O_分__子___。 ③在滴入稀盐酸的过程中,若观察到有少量气泡出现,请分析产生气 泡的可能原因_2_N_a_O__H_+__C__O_2_=_=_=_N__a_2C__O_3_+__H__2O__、__N_a_2_C_O__3_+__2_H_C__l=_=_=_2_N__a_C_l_ _+__C__O_2_↑__+__H_2_O_______________________________ (用化学方程式表示)。
-12-
中和反应的应用 8.酸与碱作用生成盐和水的反应叫做中和反应。中和反应在工农生产 和日常生活中有着广泛的应用。下列应用一定与中和反应原理无关的是 (D) A.施用熟石灰改良酸性土壤 B.用肥皂水来消除蚊虫的叮咬 C.用 NaOH 溶液洗涤石油产品中的残余硫酸 D.用熟石灰和硫酸铜配制波尔多液
-18-
(2)方案Ⅱ:
实验步骤
实验现象
结论
取 2mL NaOH 溶液于试管中, 若__有__气__泡__产__生__
稀盐酸过量
滴入一定量的稀盐酸,振荡后加
NaOH 溶液与稀盐酸
若没有明显现象
入镁条
恰好完全反应
-19-
【实验反思】
(3)另有同学提出方案Ⅱ不能证明 NaOH 溶液与稀盐酸恰好完全反应, 其原因是_稀__盐__酸__量__不__足__的__情__况__下__,__也__无__明__显__现__象___。
D.无法确定
-9-
6.如图是 X、Y、Z 三种液体的对应近似 pH,下列判断不正确的是( B )
必考点解析人教版九年级化学下册第十单元酸和碱必考点解析试题(含答案解析)

人教版九年级化学下册第十单元酸和碱必考点解析考试时间:90分钟;命题人:化学教研组考生注意:1、本卷分第I 卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I 卷(选择题 30分)一、单选题(10小题,每小题3分,共计30分)1、一定条件下,溶液中反应物的质量分数越大,化学反应速率就越快,现用 50g30%的硫酸溶液与过量的镁粉反应,为了减慢反应速率而又不影响生成氢气的总质量,可向硫酸中加入适量的 ① 10%的硫酸 ②水 ③碳酸钾固体 ④氯化钠固体A .②④B .①②C .②D .③④2、在实验室里用铁屑、氧化铜、稀硫酸为原料制备铜,有下列两种途径:若用这两种方法制得的铜质量相等,则下列有关说法符合实际情况的是(1)242H SO CuO Fe H Cu(2)244H SO Fe CuO CuSO CuA .消耗氧化铜的质量不同B .消耗铁的质量相同C .消耗硫酸的质量相同D .生成硫酸亚铁的质量不同3、如图是稀盐酸和氢氧化钠溶液反应的PH 变化曲线图,据图分析能得出的结论正确的是A.该反应是将氢氧化钠溶液滴入稀盐酸B.a克是指加入稀盐酸的质量C.A点时,溶液的溶质为HCl、NaClD.B点表示稀盐酸和加入的氢氧化钠溶液质量正好相同4、下列图象与所属实验现象相符的是A.稀释NaOH溶液B.镁在空气中燃烧C.铁加入稀盐酸中D.氧气的溶解度Δ5、纳米Fe粉可治疗惊痫、癫狂、脚气冲心、贫血等。
某兴趣小组探究用氢气和碳酸亚铁(H2+FeCO3Fe+H2O+CO2)制取纳米铁粉并检验该反应的气体产物,实验装置如图(加热及部分夹持装置省略),下列说法正确的是A.①中、②中依次盛装盐酸、浓H2SO4B.反应开始时,点燃Y处的酒精灯后再打开分液漏斗的活塞C.装置③的作用是检验H2O,装置⑤是尾气处理装置D.装置②和装置④可以互换位置6、下列示意图能表示加水稀释pH=0的溶液的是A.B.C.D.7、推理是学习化学的重要思维方法,下列推理中合理的是A.氧气、氢气只含一种元素均属于单质,所以含一种元素的物质一定是单质B.燃烧都伴随有发光、放热现象,则有发光、放热现象的一定是燃烧C.在空气中铁制品比铝制品更易腐蚀,则铁比铝的金属活动性强D.酸溶液能使紫色石蕊溶液变红色,则稀盐酸能使紫色石蕊溶液变成红色8、下列物质中,属于纯净物的是A.食醋B.稀盐酸C.液氧D.加热高锰酸钾完全反应后的剩余物9、下列常见现象中,发生化学变化的是A.潮解B.乳化C.溶解D.指示剂变色10、人被蚊虫叮咬之后,皮肤红肿疼痛,这是因为被注入了一种叫做蚁酸的物质。
人教版九年级化学下册届全册中考总复习资料:第十单元酸和碱

课题1 常见的酸和碱一、酸、碱、盐的定义↓酸的定义 电离时生成的阳离子全部都是H +的化合物,叫做酸。
如HCl 、H 2SO 4、HNO 3等。
酸的水溶液呈酸性。
酸由H +和酸根离子构成。
↓碱的定义电离时生成的阴离子全部都是OH -的化合物,叫做碱。
如NaOH 、Ca(OH)2、NH 3·H 2O 等。
碱的水溶液呈碱性。
碱由OH -和金属离子构成。
↓盐的定义电离时生成金属离子和酸根离子的化合物,叫做盐。
如NaCl 、CuSO 4、FeCl 3等。
盐的水溶液呈中性。
盐由金属离子和酸根离子构成。
二、酸碱指示剂跟酸或碱的溶液起作用时,本身可显示不同颜色的物质,叫做酸碱指示剂,简称指示剂。
石蕊和酚酞是两种常见的酸碱指示剂。
石蕊试液遇酸溶液变成红色,遇碱溶液变成蓝色。
酚酞试液遇酸溶液不变色,遇碱溶液变成红色。
提 示:⒈酸碱指示剂是从植物的花瓣或果实中提取的浸出液,只要在不同酸碱性溶液中可能显示不同的颜色,都可以做酸碱指示剂使用。
⒉酸碱指示剂与酸或碱的溶液反应时,变色的是酸碱指示剂而不是酸或碱。
三、常见的酸↓盐酸(氯化氢的水溶液)物理性质纯净的浓盐酸是无色、透明的液体,有挥发性,有刺激性气味。
浓盐酸挥发出的氯化氢气体遇空气中的水蒸气形成白雾,即盐酸液滴。
化学性质1.与指示剂作用:使紫色石蕊试液变红,使无色酚酞试液不变色。
2.与活泼金属反应:Zn+2HCl=ZnCl 2+H 2↑ Fe+2HCl=FeCl 2+H 2↑3.与金属氧化物反应:⑴与氧化铁反应:Fe 2O 3+6HCl=2FeCl 3+3H 2O现象:红色逐渐溶解,溶液由无色变为黄色。
此反应可用于出铁锈。
第十单元 酸和碱腐蚀品标志⑵与氧化铜反应:CuO+2HCl=CuCl 2+H 2O现象:黑色粉末逐渐溶解,溶液由无色变为蓝色。
4.与碱的反应:⑴与氢氧化铜反应:Cu(OH)2+2HCl=CuCl 2+H 2O现象:蓝色沉淀逐渐溶解,溶液由无色变为蓝色。
2020春人教版初中化学复习九年级下册必刷题第10单元 课题2 第1课时 中和反应及应用

A.b 点时所加试剂一定是稀盐酸 B.加入试剂总体积为 V1 时,溶液中不存在 NaOH C.c 点时溶液中的溶质都是盐 Dຫໍສະໝຸດ a 点时溶液中一定不存在 Cu2+
-7-
7.芋艿(俗称毛芋)是一种常见的食品,新鲜芋艿在去皮时会出现一种
白色的汁液,汁液内含有一种碱性物质——皂角甙,沾上它会奇痒难忍。
60
40
x
5.5g
4600=5.x5g 解得 x=8.25g
所以,食醋中醋酸的质量分数为82.0205gg×100%≈4.1%。
答:食醋中醋酸的质量分数为 4.1%。
-15-
12.小华同学设计中和反应实验操作:向氢氧化钠溶液中直接滴加稀 盐酸。为确定氢氧化钠是否和盐酸恰好完全反应,他取出少量反应后的溶 液倒入一支试管中,向其中滴加酚酞试液,振荡,观察到酚酞试液不变色, 于是得出:“两种物质恰好完全反应”。
D.实验前向氢氧化钠溶液中滴加 2 滴酚酞试液
-2-
2.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观
示意图如下。由此分析下列说法正确的是( C )
A.反应前后阴、阳离子的总数目不变 B.反应前后溶剂质量不变 C.反应后溶液呈中性 D.反应前后元素种类发生了变化
-3-
3.下列反应属于中和反应的是( D )
(2)此过程中发生反应的化学方程式可能是__N_a_O__H_+__H__C_l_=_=_=_N__a_C_l_+___ _H__2_O_______。
(3)最终溶液为无色,能否说明该溶液一定呈中性?_不__能___(填“能”或 “不能”),理由是_酚__酞__溶__液__在___中__性__和__酸__性__溶__液__中__均__呈__现__无___色_。
2020春单元达标必刷常考题100道:初中化学人教版九年级(下)《第十单元 酸和碱》

2020春单元达标必刷常考题100道:初中化学人教版九年级(下)《第十单元酸和碱》一、选择题(共40小题)1.(2017•上海)氢氧化钙俗称()A.烧碱B.纯碱C.熟石灰D.石灰石2.(2011•娄底)家庭生活中一些常见物质的pH如下:物质食醋牛奶食盐水牙膏肥皂水pH2~36~778~99~10当我们被蚊虫叮咬后,蚊虫能在人的皮肤内分泌蚁酸(具有酸的性质),从而使皮肤肿痛。
要减轻痛痒,应在叮咬处涂抹下列物质中的()A.食醋B.牛奶C.食盐水D.牙膏或肥皂水3.(2017•庆阳二模)如图是生活中一些物质的pH,下列说法中不正确的是()A.酱油呈酸性B.肥皂水能使无色酚酞试液变红C.胃酸过多的人适宜多喝玉米粥D.西瓜汁的酸性比苹果汁的酸性强4.(2019•西湖区校级模拟)将浓盐酸、浓硫酸敞口放置一段时间,它们共同的变化是()A.颜色发生改变B.发生化学变化C.质量变大D.溶质的质量分数变小5.(2015春•博山区校级月考)下列物质中,不能够直接证明稀硫酸是酸性溶液的是()A.pH试纸B.无色酚酞试液C.紫色石蕊试液D.蓝色的石蕊试纸6.(2016•邵阳二模)根据下列实验现象,可以判断其溶液一定呈酸性的是()A.滴加酚酞试液显无色的溶液B.滴加石蕊试液显蓝色的溶液C.能够与碱发生反应的溶液D.常温下,pH<7的溶液7.(2013•江都市模拟)下列物质中,能与稀盐酸发生中和反应的是()A.Mg B.MgO C.Mg(OH)2D.MgCO38.向盛有10mL的稀盐酸烧杯中,加入20mL水,则溶液的酸性强弱变化是()A.增强B.减弱C.不变D.无法判定9.(2015•永州)下表是健康人体内一些液体近似pH,其中呈酸性的是()胃液胆汁血浆胰液0.9~1.57.1~7.37.35~7.457.5~8.0A.胃液B.胆汁C.血浆D.胰液10.(2005•桂林)下列物质敞口久置于空气中,质量会变轻的是()A.生石灰B.浓硫酸C.浓盐酸D.石灰水11.(2008•南通)在生活、生产和科学研究中,常用pH试纸测定溶液的pH.以下测定操作正确是()A.将被测液滴到放在玻璃片上的pH试纸上,显色后,与标准比色卡比较B.将pH试纸直接投入被测液中,显色后,取出与标准比色卡比较C.先用少量水湿润试纸,后滴上被测液,显色后,与标准比色卡比较D.先用蒸馏水清洗滴管,随后吸取被测液滴到试纸上,显色后,与标准比色卡比较12.(2004•福州)鱼胆弄破后会使鱼肉粘上难溶于水的胆汁酸(一种酸)而变苦,要减少这种苦味。
部编人教版初中化学九年级下册《第十单元 酸和碱 全单元复习同步测试题及答案》最新精品优秀完美完整实用
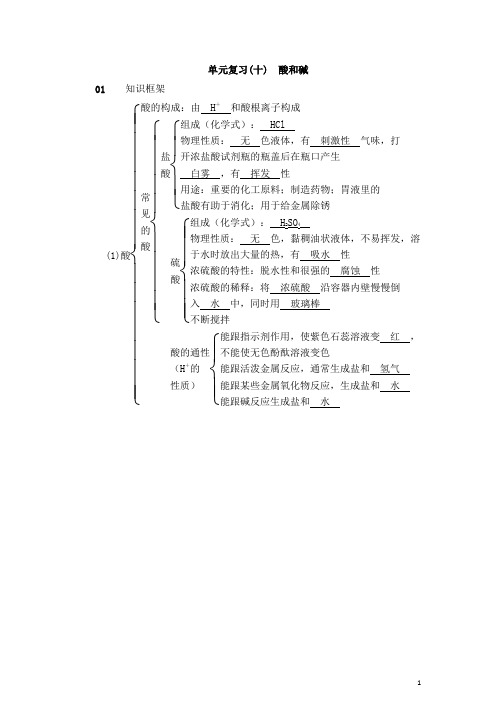
单元复习(十) 酸和碱01 知识框架(1)酸⎩⎪⎪⎪⎪⎪⎪⎪⎨⎪⎪⎪⎪⎪⎪⎪⎧酸的构成:由 H + 和酸根离子构成常见的酸⎩⎪⎪⎪⎪⎨⎪⎪⎪⎪⎧盐酸⎩⎪⎨⎪⎧组成(化学式): HCl物理性质: 无 色液体,有 刺激性 气味,打开浓盐酸试剂瓶的瓶盖后在瓶口产生 白雾 ,有 挥发 性用途:重要的化工原料;制造药物;胃液里的盐酸有助于消化;用于给金属除锈硫酸⎩⎪⎪⎨⎪⎪⎧组成(化学式): H 2SO 4物理性质: 无 色,黏稠油状液体,不易挥发,溶于水时放出大量的热,有 吸水 性浓硫酸的特性:脱水性和很强的 腐蚀 性浓硫酸的稀释:将 浓硫酸 沿容器内壁慢慢倒入 水 中,同时用 玻璃棒 不断搅拌酸的通性(H +的性质)⎩⎪⎨⎪⎧能跟指示剂作用,使紫色石蕊溶液变 红 ,不能使无色酚酞溶液变色能跟活泼金属反应,通常生成盐和 氢气能跟某些金属氧化物反应,生成盐和 水 能跟碱反应生成盐和 水(2)碱⎩⎪⎪⎪⎪⎪⎪⎨⎪⎪⎪⎪⎪⎪⎧碱的构成:由金属离子(或铵根离子)和 OH -构成常见的碱⎩⎪⎪⎪⎨⎪⎪⎪⎧氢氧化钠(NaOH )⎩⎪⎨⎪⎧俗名:火碱、烧碱、苛性钠物理性质: 白 色固体;易吸水潮解; 易溶于水并放出大量的热特性:很强的腐蚀性用途:重要的化工原料氢氧化钙[Ca (OH )2]⎩⎪⎨⎪⎧俗名:熟石灰、消石灰物理性质: 白 色粉末状固体;微溶于水制取:以氧化钙、水为原料用途:建筑业;石灰水用于检测CO 2的存在碱的通性(OH -的性质)⎩⎪⎨⎪⎧能跟指示剂作用,使紫色石蕊溶液变 蓝 色,使无色酚酞溶液变 红 色能跟某些非金属氧化物反应,生成盐和水 能跟酸反应生成盐和 水 (3)中和 反应⎩⎨⎧定义:酸和碱之间发生的反应,生成盐和水应用:日常生活、工业、农业和医药等(4)溶液的酸碱度错误!02 单元精练1.下列物质属于碱类的是(A)A .苛性钠B .食醋C .生石灰D .纯碱2.(2018·广州)下列清洁用品中碱性最强的是(D)A .厕所清洁剂pH =1B .牙膏pH =8C .肥皂pH =10D .炉具清洁剂pH =133.有关实验操作正确的是(B)。
2020春人教版九年级化学下册 第10单元 全单元典中习题(付,240)

14.小林在凉拌紫卷心菜时,加入一些食醋,发现紫卷心菜 变红了,激发了他的探究欲望,特邀你协助完成下列活 动与探究。
【提出问题】紫卷心菜等植物的汁液能做酸碱指示剂吗? 【实验探究】取紫卷心菜、牵牛花的花瓣、胡萝卜,分别在
研钵中捣烂,加入酒精溶液(乙醇与水的体积比为1∶1)浸 泡,用纱布将浸泡出的汁液挤出,分别加入到蒸馏水、 稀酸溶液和稀碱溶液中,有关颜色变化情况如下:
(2)她向画中的灯笼上喷了另一种无色溶液,灯笼由白色变成 红色,则该无色溶液及灯笼上预先涂过的试剂分别是 __氢__氧__化__钠__溶__液__、__无__色__酚__酞__溶__液__(_合__理__即__可__) ___。
12.【2018·郴州】分别将一小烧杯浓盐酸、浓硫酸露置 在空气中一段时间后,发生的共同变化是( ) A.溶液的质量减小 B.溶液的浓度减小 C.溶质的质量减小 D.溶剂的质量增大
汁液
在不同液体中的颜色变化 蒸馏水 稀酸溶液 稀碱溶液
( C)
A.NaCl溶液
B.澄清石灰水
C.稀盐酸
D.KNO3溶液
2.【2018·江西】下列“水”能使无色酚酞试液变红的是 ( A) A.氨水 B.汽水 C.冰水 D.糖水
3.【中考·枣庄】紫甘蓝是大众爱吃的蔬菜,含有丰富的 花青素,花青素遇酸性溶液变红色,遇碱性溶液变蓝 色。在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能 是加入了下列调味品中的( C ) A.食盐 B.味精 C.食醋 D.香油
4.【中考·北京】如图所示,在白色点滴板1~6的孔穴中, 分别滴加2滴紫色石蕊溶液。
(1)孔穴6中溶液变为蓝色,说明碳酸钾溶液显________(填 “酸碱性性”或“碱性”)。
(2)溶液变为红色的孔穴有___2_、__5__(填孔穴序号,下同)。 (3)作为空白对照实验的孔穴是____3____。 (4)孔穴4中溶液变为__蓝____色,若向孔穴4中滴加稀硫酸,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
B.铝
C.铜
D.表面镀锌的金属
-3-
3.将等质量的镁、铝、锌、铁分别与足量且浓度相同的稀盐酸反应,
反应速率最快的是_镁___,最慢的是_铁___;最终生成氢气最多的是__铝__,最 少的是_锌___。
-4-
酸与金属氧化物反应
4.除铁锈的试剂是( B )
A.氯化钠溶液 C.氢氧化钠溶液
B.稀盐酸 D.水
_F_e_2O__3+__6_H__C_l_=_=_=_2_F__eC__l3_+__3_H__2O_______。 (2)白醋、柠檬酸溶液也能与三氧化二铁发生类似反应,说明白醋、柠
檬酸溶液和盐酸中都含有的离子是__H_+___。 (3)理论上溶解 3.2g 三氧化二铁,需要 36.5%的盐酸_1_2__g。
-9-
9.化学变化多姿多彩,美丽如花。图中甲、乙、丙、X 分别是我们已 经学过的一种物质,甲、乙、丙均能与 X 发生反应,若 X 是稀盐酸,则甲、
乙、丙不可能是下列物质中的( A )
A.C B.Fe2O3 C.Al D.CaCO3
-10-
10.硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有_脱__水__作___用__。
第十单元 酸和碱 课题1 常见的酸和碱 第2课时 酸的化学性质
-1-
酸与金属反应
同步考点手册 P22
1.下列物质不能由金属和酸反应直接制得的是( A )
A.AgCl
B.FeCl2
C.MgCl2
D.AlCl3
-2-
2.大理石雕像很容易被酸雨腐蚀,下列材料代替大理石做雕像比较耐
腐蚀的是( C )
A.铁
(3)写出固体 B 所含的物质:__F_e_、__C_u_____。 (4)洗涤固体 B 应使用的试剂是_稀__硫__酸___。
-13-
12.某学习小组在探究酸的化学性质时,做了如图所示的两个实验:
-14-
(1)分别向两支装有碳酸钠和碳酸钙粉末的试管中注入一定量的稀盐
酸,两支试管内均观察到的现象是_有__气__泡___产__生__,固体粉末逐渐消失,最
6.实验时,李华把一枚生锈的铁钉放入足量的稀盐酸中,过一会儿,
他看到的现象是_铁__锈__逐___渐__消__失__,__溶__液__变__成__黄__色__;发生反应的化学方程式为
_F_e_2O__3+__6_H__C_l_=_=_=_2_F__eC__l3_+__3_H__2O_______;过一段时间,他又看到铁钉表面有 气泡产生,该反应的化学方程式为_F__e+__2__H_C_l_=_=_=_F__eC__l2_+__H__2↑___________。
-19-
【实验探究二】探究蚁酸分解的两种产物。
(1)小芳同学根据蚁酸中含有__氢__、__氧__(_或__H__、__O_)__元素,推测出生成物
中含有水。 (2)另一种生成物是气体,小敏提出两种猜想: 猜想①:该气体是 CO2
猜想②:该气体是__C_O___
-20-
他们将蚁酸分解产生的气体通过如下装置(铁架台已略去),观察现象。
【提出问题】蚁酸的成分是什么?它有什么性质? 【查阅资料】蚁酸是一种有机酸,化学名称叫做甲酸,化学式为 HCOOH;蚁酸在一定条件下会分解生成两种氧化物。
-18-
【实验探究一】探究蚁酸的酸性。 (1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成
__红__色,说明蚁酸溶液显酸性。 (2)将锌粒放入盛有蚁酸溶液的试管中,有气泡产生,该气体是_氢__气___。
终形成无色溶液。写出 B 试管中发生反应的化学方程式:_C_a_C__O_3_+__2_H_C__l=_=_=__ _C_a_C_l_2_+__H_2_O_+__C__O_2_↑_____________。
(2)实验结束后,同学们将 A、B 两支试管中的废液倒入同一只洁净的 烧杯中,发现烧杯中的废液变浑浊。写出产生浑浊现象的化学方程式: _C_a_C_l_2_+__N_a_2_C_O__3=_=_=__C_a_C__O_3_↓__+__2_N_a_C__l _______。
酸的通性
7.酸具有相似的化学性质的原因是( B )
A.都有酸根离子 B.都有氢离子 C.都有氢元素 D.都使紫色石蕊变红
-7-
同步考点手册 P22
-8-
8.实验室有盐酸、白醋、柠檬酸三种溶液,回答下列问题: (1)向三氧化二铁中加入足量盐酸 ,充分反应后,观察到的现象是
_红__色__固__体___溶__解__,__溶__液__由__无__色__变__为__黄__色__ , 反 应 的 化 学 方 程 式 是
-15-
小组同学将烧杯中的物质进行了过滤,对滤液中的溶质成分展开了探 究,请你一起参与。
【提出猜想】猜想 1:滤液中的溶质是氯化钠; 猜想 2:滤液中的溶质是氯化钠和碳酸钠;
猜想 3:滤液中的溶质是__氯__化__钠__和__氯__化__钙__(_或__N_a_C__l、___C_a_C__l2_)________。
上述反应中,属于酸的共同性质的是__①__②__(填编号)。 (3)盐酸的下列用途中,不能用硫酸代替盐酸的是__②__③__(填编号)。
①金属表面除锈 ②制造药物氯化锌 ③除去 NaCl 中的少量 NaOH
-11-
11.高纯度的氧化铜可用作颜料、有机合成催化剂等,如图是用粗铜粉 氧化法获得高纯度氧化铜的流程图。
-21-
Ⅰ.实验时装置 A 中无明显变化,则猜想①__不__成__立__(填“成立”或“不
成立”);
Ⅱ.装置 B 中的现象是_黑__色___粉__末__变__红__色__,装置 C 中发生反应的化学方
程式为_C__a_(O__H_)_2_+__C_O__2=_=__=_C_a_C__O_3_↓__+__H_2_O___。
-12-
回答下列问题: (1)1:1 的硫酸溶液是用 1 体积 98%的浓硫酸与 1 体积水混合而成,配
制该硫酸溶液时,一定要把_浓__硫___酸__慢慢注入_水___中,并不断搅拌。
(2)写出硫酸与氧化铜反应的化学方程式: _H__2S_O__4_+__C_u_O__=_=_=_C__u_S_O_4_+__H__2O_______。
【讨论交流】从环保角度看,该装置的缺陷是_缺__少__尾__气___处__理__装__置__。Βιβλιοθήκη 同步考点手册 P22-5-
5.用稀硫酸除铁锈的原理是( D )
A.FeO+H2SO4===FeSO4+H2O B.Fe2O3+3H2SO4===Fe2(SO4)3+3H2↑ C.Fe2O3+2H2SO4===2FeSO4+2H2O D.Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
-6-
(2)写出稀硫酸与下列物质反应的化学方程式: ①与铁粉反应:_F_e_+__H_2_S_O__4=_=__=_F_e_S_O_4_+__H__2↑___________________; ②与碳酸钠溶液反应:_N_a_2_C_O__3+__H__2S__O_4_=_=_=_N__a_2S_O__4+__H__2_O_+__C__O_2_↑____; ③与氯化钡溶液反应:_H_2_S_O__4+__B__a_C_l_2=_=__=_B_a_S_O__4↓__+__2_H__C_l_____;
-16-
【设计实验】请你选择一种猜想进行验证。
实验步骤
预计实验现象 预计结论
取少量滤液于试管中,
_加__入__适___量__稀__盐__酸__(_或__稀__硫__酸__等__)_
_产__生___气__泡__ 猜想__2_正确
(其他合理答案均可)
-17-
13.不少同学都被蚊虫叮咬过,感觉又痛又痒。同学们从化学课上知 道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤。化学兴趣小组同学 决定对蚁酸进行探究。
他又将铝片放入足量的稀盐酸中,奇怪的是开始无明显现象,过一段 时间后才看到有气泡冒出,试用学过的知识解释原因:A__l2_O__3+__6_H__C_l_=_=_=____ _2_A__lC__l3_+__3_H__2O___、_2_A__l+__6_H__C_l_=_=_=_2_A__lC__l3_+__3_H_2_↑________(用化学方程式表 示)。
