相平衡与相图
材料科学基础第四张相平衡与相图(1)

化学位: 当温度、压力不变因组元增加一个摩尔, 引起吉布斯自由能的变化,就是组元的化 学位或偏摩尔自由能。它代表了系统内物 质传递的驱动力。
组元2在β相 中化学位等于其 在α相中的化学位 推演如下:
多元系统的吉布斯自由能是温度、压力及各组元摩尔 数n1、n2…….函数,即可写成 G=f(T、P、n1、n2……….)
二元系中,三相平衡的热力学条件是每个组元在各相中的化学位相等,即 μα1=μβ1=μγ1 μα2=μβ2=μγ2 多元复相平衡的普遍条件是每个组元在各相中的化学势都必须彼此相等,即 μαi=μβi=μγ i =…=μPi
其中,α、β、γ…P表示合金中存在的相,i代表合金中的第i个组元 。 μPi则表示P相中i组元的化学位,即上标表示平衡相,下标表示组元。
温度与压力都能变动的情况
二、 SiO2系统相图 •也有晶型变化:
(<573℃)低温型α-SiO2 (α-石英) (573℃-870℃) 高温型β-SiO2 (β-石英) (870℃-1470℃) 磷石英β2-SiO2 (β2-磷石英) (1470℃-1713℃) 方石英β-方SiO2 这四种不同晶体结构的SiO2存在 的温度、压力范围不同
•确定两平衡相的相对量: •将成分坐标当作杠杆,以合金的成分点为 •支点,Wα和WL看成作用于a、b两点的力, •则与力学上的杠杆定律一样,即 • WL/Wα=0b/a0 •上式表明合金在两相区内,两平衡相的相 •对量之比与合金成分点两边的线段长度呈 •反比关系。
•合金中两平衡相的含量也可用下式表达: Wα%=(C-CL)/(Cα-CL) =a0 /abχ100% WL%=(Cα-C)/(Cα-CL) = 0b /ab χ100% 在两相区内,温度一定时,两相的质量比 是一定的。
第五章 相平衡和相图-Fe-FeC3相图131104

• 铁素体从727℃冷却时也会析出极少量的渗碳体,以三次渗碳体 Fe3CIII称之,以区别上述两种情况产生的渗碳体。
材料科学基础 第四节 Fe-C相图
4. 铁碳合金的分类
第五章 相平衡与相图
铁碳合金通常可按含碳量及其室温平衡组织分为三大类:
(1)工业纯铁,C<0.0218% (2)碳钢,0.0218%<C<2.11%
材料科学基础 第四节 Fe-C相图
三、 Fe- 石墨相图
1. 相图中的线和区 CD——从液相结晶出一次石墨GI; ES ——从奥氏体中析出二次石墨GII; PQ ——从铁素体中析出三次石墨GIII; ECF——共晶反应线,LC E + G PSK ——共析反应线, S P + G 2. Fe- 石墨结晶平衡组织
第五章 相平衡与相图
• 完全按Fe- 石墨相图结晶的的所有铸铁的平衡组织都是由铁素体和 片状石墨组成。
• 随含碳量增加,石墨数量增加,铁素体数量减少。
材料科学基础 第四节 Fe-C相图
2. 铁碳合金的石墨化
第五章 相平衡与相图
铁碳合金中形成石墨的过程称为石墨化,分为两个阶段: (1) 液态石墨化:
• 从液体中直接形成一次石墨和共晶石墨;
• 一次渗碳体和共晶渗碳体的高温分解。 (2)固态石墨化:
• 从奥氏体中形成的二次石墨和共析石墨;
• 二次渗碳体和共析渗碳体的分解。
材料科学基础 第四节 Fe-C相图
3. 铸铁的类型和组织
第五章 相平衡与相图
根据石墨化程度,铸铁可分为
(1)白口铸铁 • 完全按Fe- Fe3C相图结晶的铸铁的平衡组织由铁素体和渗碳体组成。其 断口呈现白色,故称为白口铸铁。 (2)灰口铸铁 • 第一阶段的石墨化可以充分进行,第二阶段的石墨化充分或部分,铸铁 组织由基体组织和石墨组成。其断口呈现深灰色,故称为灰口铸铁。
材料物理化学-第六章 相平衡与相图

湖南工学院
料。⑤碳纤维、石墨、金刚石与C6 。⑥计算机模拟与材料设计。⑦用新材料科 学技术武装改造传统材料产业。 GRM—巨磁电阻(Giant Magnetoresistance),通常作传感器使用,主要应 用于探测磁场、电流、位移、角速度等领域。探测微弱磁场的GM R 传感器最早 被商业化应用在磁记录领域, 作为硬盘的读出磁头。 薄膜集成的GMR磁头体积变 小, 磁记录介质的存储单元也随之变小, 这样存储密度就大大提高了。 至2000年, 存储密度为56. 3Gb/in2 的GMR 的磁头已经在日本的富士通制作所研制出来。 在21世纪初,我国的水泥产量就已跃居世界第一,但是,水泥工业的结构优 化和产品升级是当前要务。大量利用废弃的粉煤灰、矿渣、钢渣、硫酸铁渣、废 石膏、污泥等作为水泥的原料和掺合料是我国的特色,几乎占水泥产量的1/3, 这是“资源循环利用”的重大举措。研制的抗氯盐腐蚀、水化热低、抗微收缩和 后期强度高的水泥,已成功应用于我国几个超大型的海工工程中。在混凝土中, 除水泥、黄沙、石子、水和添加剂(如减水剂)的5组分外,为获得更为优异的 性能,第六组分的研究也是一个研究热点。 黄伯云:粉末冶金专家,中南大学校长,中国工程院院士。1945年11月生于 湖南益阳南县, 1969年毕业于中南矿冶学院特种冶金系,1980年至1986年在美国 依阿华州立大学获硕士、 博士学位,随后进入美国田纳西大学和橡树岭国家实验 室从事博士后研究工作。1988年回国,1997年任中南工业大学校长,2001年任中 南大学校长, 1999年当选为中国工程院院士。黄伯云是我国材料科学领域的战略 科学家,他率领团队历时20年研制出的“高性能碳/碳航空制动材料的制备技 术”,打破了国外的技术垄断,使我国成为世界上有能力生产碳/碳复合材料飞 机刹车片的四个国家之一。也正是这项技术,在2005年荣获了已连续空缺6年的 国家技术发明一等奖。 C/C复合材料的密度仅为钢的1/4在波音747——400飞机上使用了C/C复合材 料刹车盘后, 使飞机机身大约减重816.5Kg。
相平衡与相图

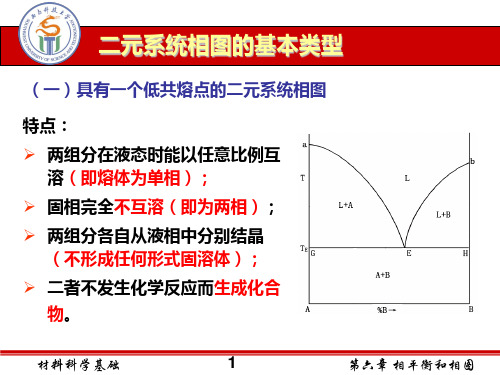
A的熔点
A和B的二元低共熔点
4个相区: 固相线 L、L+A、 L+B、A+B
特点: 两个组分在液态时能以任何比例互溶,形成单相溶液;但在 固态时则完全不互溶,二个组分各自从液相中分别结晶。 组分间无化学作用,不生成新的化合物
杠杆规则
如果一个相分解为2个相,则生成的2个相的数量与原始
65
35
35
1450
725
铁碳平衡图
铁碳平衡图 (iron-carbon equilibrium diagram ), 又称铁碳相图或铁碳状态图。它以温度为纵坐标,碳含量 为横坐标,表示在接近平衡条件(铁-石墨)和亚稳条件
(铁-碳化铁)下(或极缓慢的冷却条件下)以铁、碳为
组元的二元合金在不同温度下所呈现的相和这些相之间的 平衡关系。
4
二元系统
C=2,一般情况下,凝聚系统中的相律:
一、二元相图表示方法
F=C+P+1=3-P
当P=1时,F=2
当P=2时,F=1
当γ =3时,F=0 相数最大为3,自由度最大为2,对于浓度:A+B=A'%+B'%=100% 任意确定一个,则另一个确定相图为T组成图
二 具有一个低共熔点的简单二元相图
相平衡与相图
主要内容
发展历史 相图基础知识 单元系相图 二元系相图 三元系相图
1 相图发展历史
一 理论基础
平衡图的理论基础是吉布斯(J W Gibbs)的相律 ,他于1876年创建相律。
二 发展历程 1990年:罗泽朋(Bakhuis Roozeboom)发表了《用相律的观点来
看复相平衡》巨著的第一部分。
第二章相平衡及相图

pA p x
* A
* A A
* A
p pA pA p (1 xB ) xB * pA 适用条件:理想稀溶液中溶剂或理想液态混合物。
如果溶液中只有A,B两个组分,则
2-4-2 享利定律
在一定温度下,稀溶液中挥发性溶质在气相中 的平衡分压与在溶液中的摩尔分数(或质量摩尔浓 度、物质的量浓度)成正比。
def
S - R - R′
§2-1
R’包括:
相律
1)当规定系统中部分物种只通过化学反应由
另外物种生成时,由此可能带来的同一相的 组成关系。 2)由电中性条件带来的同一相的组成关系。
例1 (1) 仅由 NH4Cl(s) 部分分解,建立如下反应
平衡:
NH4Cl (s) =NH3(g)+HCl(g)
(2) 仅由CaCO3(s)部分分解,建立如下反应平衡: CaCO3 (s) = CaO(s)+CO2(g)
pB kx,B xB
pB kb,BbB
pB kc,BcB
式中比例系数称为亨利系数。 适用条件:稀溶液中挥发性溶质,且溶质在 气相和在溶液中的分子状态必须相同。
2-4-3 拉乌尔定律和亨利定律对比
1 共同点 (1)适用于稀溶液; (2)表达形式相似。 2区别
(1)比例常数不同;
(2)针对的具体对象不同。
和1molB(l)形成理想混合物,则
ΔmixS= J/K,
ΔmixH=
ΔmixG=
kJ,
kJ。
答案: ΔmixS = 11.53 J/K, ΔmixH = 0 kJ, ΔmixG = -3.44 kJ。
§2-6
理想稀溶液
2-6-1 理想稀溶液的定义 一定温度下,溶剂和溶质分别服 从拉乌尔定律和亨利定律的无限稀薄溶 液。
第六章相平衡与相图

上式表明:如果一个相分解为两个相,则生 成相的数量与原始相的组成点到两个新生相的组 成点之间的线段成反比。此关系式与力学上的杠 杆很相似。M点相当于杠杆的支点,M1和M2则 相当于两个力点,因此称为杠杆规则。
2.杠杆规则的含义
可以看出:
系统中平衡共存的两相的含量与两相状态点到系统 总状态点的距离成反比。
M2 B G•b%= G1•b1%+ G2•b2%(2)
将(1)式代入,得
(G1+G2)b%= G1•b1%+ G2•b2% G1(b-b1)=G2(b2-b)(3)
所以 G1(M1-M)=G2(M-M2)两个新相M1和M2在系统中的含量则为:
G1=(M-M2/M1+M2)%
G2=(M1-M/M1+M2)%
b2
b
b1
A
M1
M
若组成为M的原始混合物含B为 b%,总质量为G;新相M1含B为 b1%,质量为G1;新相M2含B 为b2%,质量为G2。因变化前、 后的总量不变,所以
G = G1+G2 (1) 原始混合物中B的质量为G•b%, 新相M1中B的质量为G1•b1%。 新相M2中B的质量为G2•b2%。 所以:
(2)熔体的冷却析晶过程
所谓熔体的冷却析晶过程是指将一定组成的 二元混合物加热熔化后再将其平衡冷却而析晶的 过程。
通过对平衡冷却析晶过程的分析律。
TA
M
TB
TC
C
L
A+L TD
TE
ME
D B+L
E
A+B
A
M′
B%
B
M(熔体) L p=1 f=2
L A
TAE线、TBE线都称之为液相线, 通过E点的水平线GH称为固相线。
第六章相平衡和相图

(4)自由度(F) 在一定范围内可以任意改变而不会引起旧相消失或新相产
生(chǎnshēng)的最大变量数,又称独立变量数
变量:浓度、温 度(wēndù)、压力 等。
F=2
双变量 系统
对于给定的相平衡系统
F = 1,在保持系统中相的数 单变量目和相的状态不发生变
系统化的条件下,并不是所
第十九页,共154页。
一、具有多晶转变的单元系统(xìtǒng)相图
关键:明确(míngquè)各分相区、各线(实线和虚线)、 多晶转变曲线 各点意义
熔融曲线
p1
F=1
F=2
F=0
F=2 蒸发曲线
升华(shēnghuá)曲线
t1
第二十页,共154页。
过热(ɡuò rè)β-晶型的介稳相区
过冷液体(yètǐ)的介稳状态区
多晶转变(zhuǎnbiàn)温度低 于两种晶型熔点
晶 型 I 晶 型 I I 熔 体
低于T3温度(wēndù),晶型I稳定, 而晶型II介稳
而高于T3温度(wēndù),晶型I介稳 ,晶型II稳定
第二十五页,共154页。
多晶转变温度(wēndù)高于两 种晶型熔点
晶型I
熔体
晶型II 晶型II的蒸气压不论在高温还是低 温(dīwēn)阶段都比晶型I的蒸气压 高,因此晶型II始终处于介稳状态
F=2
过冷液体的蒸化曲线
F=1
过热β-晶型的熔融曲线
过热β-晶型的升华曲线 过冷α-晶型的介稳相区
过冷α-晶型的升华
(shēnghuá)曲线
过热β-晶型的熔点
第二十一页,共154页。
二、单元系统(xìtǒng)相图的特点:
相平衡与相图

5.5 -6 80 327 271 451 657 1412
-26 -71 60 246 144 306 578 1090
50 24 64 88 55 69 89 32
合金体系"热分析"原理
热分析法研究固液平衡体系相图主要是依据体系发生相变时伴随着相变潜热的吸 收或放出,导致体系冷却速度的变化,来研究相变过程的规律。由实验数据所绘 制的温度(T)与时间(t)的曲线,称为“步冷曲线”,由步冷曲线斜率的变化可提 供相的产生、消失、和达成相平衡的信息。
4
610.62
273.16
水的相图
2.2 单组分体系的两相平衡- 克拉贝龙(Clapeyron)方程式
可适用于任何纯物质体系的各类两相平衡,如气~液、气~固、液~固或固~固 晶型转变等。
如气~液、气~固、液~固或固~固晶型转变等。如果 α、β 两相中有一相是气相(设 β 为气相),则因气体体积远大于液体和固体的体积,即 Vm(g)》Vm(l) 或 Vm(s) 。对比之 下可略去液相或固相的体积,而
可得 Φ = 1 ,f = 3 Φ = 2 ,f = 2 Φ = 3 ,f = 1 Φ = 4 ,f = 0
即"三变量体系" 即"二变量体系" 即"单变量体系" 即"无变量体系"
通常情况下,描述体系状态时以温度(T)、压力(p)和组成 (浓度 x1 或 x2 )三个变量为坐标构成的立体模型图。
固定 T 就得 p~x 图,固定 p 就得 T~x 图对工业上的提纯、分离、精馏、分馏 分面很有实用价值
6
三、二级相变
一类相变称之为一级相变(first order phase transition),特点是,如果改变体系的独 立强度变量(例如 pVT 系统的 t,p,x1,x2,……,xr ),一旦这些变量或其中之一 达到相变能发生的值时,从宏观上看相变将突然发生。它是一种不连续的突变现象,表 现出在确定的强度变量值时发生,同时体积、熵、焓等热力学量发生不连续的但有限的 突变。我们通常所见的气、液、固态的相变都属于这类相变。
相平衡和相图-Fe-FeC3相图

• 室温平衡组织: Fe3CII + P(+Fe3C)
.
材料科学基础
第四节 Fe-C相图
第五章 相平衡与相图
(a)
(b)
图7.21 含碳1.2%的过共析钢缓冷后的组织 500×
硝酸酒精浸蚀,白色网状相为. 二次渗碳体,暗黑色为珠光体
+Fe3C (共析转变)
• 室温平衡组织: P(+Fe3C),100%珠光体,层片状混合物。
.
材料科学基础
第四节 Fe-C相图
第五章 相平衡与相图
(3)亚共析钢(0.0218%<C<0.77%) • 0.09% > C :L • 0.09% <C < 0.17 % : L L+ • C = 0.17 %:L L+ • 0.17 % < C < 0.53 % :L L+ L • C > 0.53 %: L • (固溶体同素异晶转变) 脱溶分解( +Fe3CIII)
共析转变( +Fe3C) • 室温平衡组织: +Fe3CIII + P(+Fe3C)
.
材料科学基础
第四节 Fe-C相图
第五章 相平衡与相图
图7.20亚共析钢的室温组织 .200×
材料科学基础
第四节 Fe-C相图
第五章 相平衡与相图
(4)过共析钢,0.77%<C<2.11%; • L (匀晶转变)
• 在727 ℃时,碳在铁素体中的最大含碳量达到0.0218% C 。
• 铁素体从727℃冷却时也会析出极少量的渗碳体,以三次渗碳体 Fe3CIII称之,以区别上述两种情况相平衡与相图
相图与相平衡基础知识

推导过程
假设一个平衡系统中有C个组分,P个相, 如果C个组分在每个相中都存在,那么对每 一个相来讲,只要任意指定(C-1)个组分 的浓度就可以表示出该相中所有组分的浓度, 因为余下的一个组分的浓度可以从100中减去 (C-1)个组分的浓度之和求得。由于系统 有P个相,所以需要指定的浓度数总共有P (C-1)个,只要才能确定体系中各相浓度。
相律 吉布斯根据前人的实验素材,用严谨的热力学作 为工具,于1876年导出了多相平衡系统中,系统的 自由度数(F),独立组元数(C),相数(P)和 对系统的平衡状态能够发生影响的外界影响因素 (n)之间的关系,相律的数学表达式为: F=C-P+n 一般情况下,只考虑温度和压力对系统的平衡状态的 影响,即n=2,则相律表达式为 F=C-P+2
总之,气相只能一个相,无论多少种气体混在一起 都一样,形成一个气相,液体可以是一个相,也可 以是两个相(互溶程度有限时)。固体如果是连续 固溶体为一相;其他情况下,一种固体物质是一个 相。
一个系统中所含有相的数目,叫做相数,以符号P 表示,按照相数的不同,系统可分为单相系统 (P=1),二相系统(P=2),三相系统(P=3)等。 含有两个相以上的系统,统称为多相系统。
第六章 相平衡和相图
什么是相图
相图的研究方法有哪些 相图的应用
相图的定义
在一个多相体系中,随温度、压力和浓度的
变化,相的种类、数量及含量都要相应地发 生变化,对于变化情况可用几何图形来描绘, 这个图形就可以反映出该系统在一定组成、 温度和压力下,达到平衡时所处的状态,这 个几何图形就是相图,也叫相平衡图、状态 图。
相平衡研究方法
动态法 热分析法 差热分析法(DTA) 溶解度法 静态法(淬冷法)
相平衡和相图
30
第六章 相平衡和相图
C 例:根据下列相图 (1) 用连线规则划分副三角形。 (2) 用箭头标出界线上温度变化方向及界线性质。 C (3) 判断S、S1、S2化合物的性质。 (4) 写出各无变量点的性质及反应式。 (5)在相图下侧画出A-B二元系统相图。 u v (6) 分析熔体M1、M2的析晶路程。 S (M1在SO连线上)
第六章 相平衡和相图
13
3、背向线规则
在浓度三角形中,一个三元系统的组成点愈靠近某个顶点,
该顶点所代表的组分的含量就愈高;反之,愈少。
C 若熔体在冷却时析出某一
顶点所代表的组元,则液
相中组成点必定沿着该顶 点与熔体组成点的连线向 背离该顶点的方向 A
材料科学基础
D
B
第六章 相平衡和相图
14
4、杠杆规则
C C
b L .2 N
a
e2
K
1
.
B
x B
z y
熔体1
L LB 1[B,(B)] a[B,B+(A)] f=3 f=2
L B+N f=1
L B+A K[x,B+A+(N)] f=1
e1
L+AB+N f=0
K[y(A消失),N+B]
LN+B+C L[z,N+B+(C)] f=0
L(液相消失)[1,N+B+C]
所谓一致熔融化合物是一种稳定 的化合物。它与正常的纯物质一 样具有固定的熔点,融化时,所
产生的液相与固相的化合物组成 相同,故称一致熔融
材料科学基础
2
第六章 相平衡和相图
2、不一致熔融化合物: 一种不稳定的化合物,加热这种 化合物到某一温度便发生分解, 分解产物是一种液相和一种晶相, 二者组成与原来化合物组成完全 不同。 点:纯物质熔点;低共熔点; 转熔点等 线:液相线(3条)固相线等;
1流体包裹体一相平衡与相图

笼合物中似乎从未有气体分子完全占据,
这取决于压力和温度。这意味着这种矿物
是非化学计量的,它们的化学成分一般估
计为CO2· 7.5H2O或CO2· 7.4H2O。笼合物的
几个构造类型有:CH4、CO2、H2S、C2H6
稳定化称体中心立方体构造I,而O2、N2、
C3H8、Ar形成金刚石立方构造II,H2太小 而不能稳定形成上述构造。
在一个封闭的多相体系中,相与相之间可 以有热的交换、功的传递和物质的交流。 对具有F个相体系的热力学平衡,实际上包 含了如下四个平衡条件: (1)热平衡 (2)压力平衡
(3)相平衡: 任一物质在各相中的化学势 相等,相变达到平衡 (4)化学平衡:化学变化达到平衡
独立组分数(number of independent component)的概念:在平衡体系所处的条 件下,能够确保各相组成所需的最少独立 物种数称为独立组分数C。它的数值等于体 系中所有物种数 S 减去体系中独立的化学 平衡数R,再减去各物种间的浓度限制条件 R'。 C=S-R-R’
相律(phase rule) f+=C+2 相律是相平衡体系中揭示相数 ,独立组 分数C和自由度 f 之间关系的规律,可用上 式表示。式中2通常指T,p两个变量。相律 最早由Gibbs提出,所以又称为Gibbs相律。 如果除T,p外,还受其它力场影响,则2改 用n表示,即:
纯水的相图
三相点与冰点的区别
2017/6/5
在热动力学术语中,流体包裹体可以看作 是透热、等容、等化学系统。即包裹体可 以吸热放热,但体积和成份不变。 按照单相流体包裹体按照理想气体定律: PV = nRT , V 不变, P/T 减少一个自由度。
相平衡和相图(共294张PPT)

〔2〕如果系统中存在化学反响并建立了平衡,
那么: 独立组元数=物种数一独立化学反响数
〔指独立化学平衡关系式数〕
例如,由CaCO3、CaO、CO2组成 的系统,在高温下存在下述反响:
〔1〕稳定相平衡局部〔即实线局部〕 相区: FCD是液相区; ABE是β-晶型的相区; EBCF是α-晶型的相区, 在ABCD以下是气相区。
相界线:
CD线:是液相和气相两相平衡共存线,即液相
的蒸发曲线; BC线:是α-晶型和气相两相平衡共存线,即α-
晶型的升华曲线;
AB线:是β-晶型和气相两相平衡共存线,即β晶型的升华曲线;
〔或延长线〕的交点是该晶体的熔点。
②两种晶型的升华曲线的交点是两种晶型的多晶转 变点。
③在同一温度下,蒸气压低的相更加稳定。所以, 介稳平衡的虚线,总是在稳定平衡的实线上方 。
④交汇于三相点的三条平衡曲线互相之间 的位置遵循下面两条准那么:
a、每条曲线越过三相点的延长线必定在另 外两条曲线之间。
b、同一温度时,在三相点附近比容差最大 的两相之间的单变量曲线或其介稳延长 线居中间位置。
假设该反响能够到达平衡,那么有 一个独立的化学反响平衡常数。
此时,虽然组元数=3,但独立组元 数C=3-1=2。
4、自由度 在一定范围内,可以任意改变而不
引起旧相消失或新相产生的独立变量称 为自由度,平衡系统的自由度数用F表示。
这些变量主要指组成〔即组分的浓 度〕、温度和压力等。
5、外界影响因素 影响系统平衡状态的外界因素包括:温度、压力、电
主要区别在于固-液平衡的熔融曲线OC线倾斜
热力学中的相图和平衡状态

热力学中的相图和平衡状态热力学是关于热能的科学,它是物理、化学、生物学等科学中应用广泛的一门学科。
热力学中的相图和平衡状态是热力学的基本概念和方法。
在热力学中,物质的状态一般用三个基本量来描述:温度、压力和物质的组成。
相图则是给定组成下,不同条件下物质的各个相态出现的图解。
而平衡状态则是指系统所达到的最稳定状态,它可能是热力学极小值的位置,也可能是平衡态分界面。
相图是描绘物质的不同相态之间转换及稳定区域的图示。
它是通过测定物质在一定温度和压力下所出现的物态变化来绘制的。
在相图中,一条曲线代表两个相相平衡的条件,也就是共存条件。
这些条件通常称为共存曲线。
这些曲线分割相图中的不同相区域。
在相图中,曲线以上的区域为单相区域,也就是只包含一种相的区域;而曲线以下的区域为多相区域,也就是有两种或以上的相存在的区域。
对于多相混合系统,相图是非常重要的。
它可以帮助我们理解诸如溶解度限度等问题。
当两种物质混合时,我们希望知道当其中一种物质加入到另一种物质中时,两者之间会发生什么。
在一些情况下,混合是产生单一均相溶液的,但在其他情况下,混合后的物质会分成两个或更多的相。
这些分开的相在相图中显示为多相区域。
通过查找相图,我们可以了解物质混合会产生多少个相,该相的化学组成和比例,以及相是如何相互作用的。
相图是实验观察和理论计算相结构的研究工具。
除了相图,平衡状态也是热力学的基本概念之一。
平衡态是指系统所达到的最稳定状态。
在热力学中,存在多种平衡态,如热力学平衡态、力学平衡态、化学平衡态等。
这些平衡态是物态转化和反应的关键。
在平衡态下,一般没有净变化,因为系统已经达到最小自由能或最大熵的状态。
在这个状态下,任何额外的能量或物质的注入或移除都会导致系统远离平衡态,直到它再次达到平衡态。
平衡态存在的根本原因是系统的自由能达到了最小值,它是热力学的基本原理之一。
在热力学中,相图和平衡态是不可分割的。
相图展示了平衡态下物质的相变和稳定区域。
相平衡和相图

单元系相图
Hale Waihona Puke 相图的建立相图的建立方法:实验法和计算法。 建立过程:配制-测冷却曲线-确定转变温度 -填入坐标-绘出曲线。
杠杆定律
低共熔体系相图
形成部分互溶固溶体相图
课上作业:写出合金Ⅳ由0经12-3的变化过程
相平衡和相图
一 几个基本概念 相:体系内部物理性质和化学性质完全均匀的部 分称为“相” 相图:对于多相体系,各相间的相互转化,新相 的形成,旧相的消失与温度,压力,组成有关。 根据实验数据给出的表示相变规律的各种几何 图形称为相图。从这种几何图形上,可以直观 看出多相体系中各种聚集状态和它们所处的条 件(温度,压力,组成)。
• 相平衡:在一个热力学体系内,当不同相之间相互接 触时,若发生物质从一相迁至另一相的过程,则此过 程称为相变过程。在相变过程中,当宏观物质的迁移 停止时,称为相平衡。 • 相律:描述平衡体系中独立组元数,相数和自由度数之 间的关系 自由度是指平衡系统中保持平衡相数不变的条件下独立 可变的因素(如温度、压力、浓度等)的数目 F=C-P+2 (1) 凝聚系统,相律可写成 F=C-P+1 (2) 式中: F是自由度数; C是组成材料系统的独立组元 数; P是平衡相的数目。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
若,F=0,则P=3,即最多有三相平衡。
8
例 水的相图
状态点
9
相图分析 3条线:C=1,P=2,F=1 OA是水与冰两相平衡线 OB是冰与蒸汽两相平衡线 OC是水与蒸汽两相平衡线 3个单相区: C=1,P=1,F=2 固相区、液相区和气相区 O点是气、液、固三相的平衡共存点 F=0
10
如果外界保持一个大气压, 根据相律,C=1,P=1则F=1。 系统中只有一个独立可变的 变数。因此单元系相图可以 只用一个温度轴来表示。
wL w 1 wL CL w C 1 C o
由以上两式可以得出
wL w ob ao C Co Co C L
17
杠杆规则示意图
18
11
压力 α-Fe γ-Fe
δ-Fe
纯铁的相图
温统有两个组元,根据相律:F=C-P+1,二元系统 最大的自由度数目F=2,这两个自由度就是温度和成分。 故二元凝聚系统的相图,仍然可以采用二维的平面图形 来描述。即以温度和任一组元浓度为坐标轴的温度-成 分图表示。
第8章 相平衡与相图
重点内容: 1) 相与相平衡的基本概念,杠杆规则; 2) 单元和二元系统各种类型相图的阅读分析; 3) 三元相图的基本概念,三元匀晶相图,简单三元 共晶相图。
1
材料的性能 组织结构 相
种类
数量 尺寸 形状 分布
2
相图
表示物质的状态与温度、压力、组成之间的关系的 简明图解。
表示物质在热力学平衡条件下的情况,又称为 平衡相图。
只考虑温度和压力对系统平衡状态的影响: F=C-P+2
凝聚系统:
F=C-P+1 式中:F是自由度数;C是组成材料系统的独立组元数; P是平衡相的数目。
7
8.2 单元系相图 组元数 C=1 根据相律: F=1-P+2=3-P ∵F≥0, ∴P≤3 若,P=1,则F=2
∴可以用温度和压力作坐标的平面图 (p-T图) 来表示 系统的相图。
13
状态点
温 度 轴
成分轴
14
成分的表示方法
材料的成分是指材料各组元在材料中所占的数量。 质量分数 摩尔分数
wB xB
15
8.3.1 二元系相图的建立 热分析法 金相组织法 X射线分析法 硬度法 电阻法 热膨胀法 磁性法
物理方法
计算法
相图热力学计算
16
证明 成分为C0的材料在t1温度时处于液、固两相平衡状态
3
8.1 相与相平衡
1. 相 (Phase) 在一个系统中,成分、结构相同,性能一致的均匀 的组成部分叫做相,不同相之间有明显的界面分开,该界 面称为相界面。 注意: 相在物理性能和化学性能上是均匀的。 相界面和晶界的区别。
4
2. 组元 (Component) 组元通常是指系统中每一个可以单独分离出来, 并能独立存在的化学纯物质,在一个给定的系统中, 组元就是构成系统的各种化学元素或化合物。 化学元素:Cu, Ni, Fe等 化合物:Al2O3, MgO, Na2O, SiO2等 按组元数目,将系统分为: 一元系 二元系
三元系 ……
5
3. 相平衡 在某一温度下,系统中各个相经过很长时间也不互 相转变,处于平衡状态,这种平衡称为相平衡。 各组元在各相中的化学势相同。
A
B
热力学动态平衡
6
4.吉布斯相律(Gibbs Phase Rule) 处于热力学平衡状态的系统中自由度与组元数和 相数之间的关系定律,通常简称为相律。
