136号元素电子排布图.doc
1~36号元素电子排布图(精排版)

.1~36号元素电子排布式依次如下:1、氢H 1s12、氦He 1s23、锂Li 1s2 2s14、铍Be 1s22s25、硼 B 1s2 2s2 2p16、碳 C 1s22s22p27、氮N 1s22s22p38、氧O 1s22s22p49、氟 F 1s22s22p510、氖Ne 1s22s22p611、钠Na 1s22s22p63s112、镁Mg 1s22s22p63s213、铝Al 1s22s22p63s23p114、硅Si 1s22s22p63s23p215、磷P 1s22s22p63s23p316、硫S 1s22s22p63s23p417、氯Cl 1s22s22p63s23p518、氩Ar 1s22s22p63s23p619 钾K 1s22s22p63s23p64s120、钙Ca 1s22s22p63s23p64s221、钪Sc 1s22s22p63s23p63d14s222、钛Ti 1s22s22p63s23p63d24s223、钒V 1s22s22p63s23p63d34s224、铬Cr 1s22s22p63s23p63d54s125、锰Mn 1s22s22p63s23p63d54s226、铁Fe 1s22s22p63s23p63d64s227、钴Co 1s22s22p63s23p63d74s228、镍Ni 1s22s22p63s23p63d84s229、铜Cu 1s22s22p63s23p63d104s130、锌Zn 1s22s22p63s23p63d104s231、镓Ga 1s22s22p63s23p63d104s24p132、锗Ge 1s22s22p63s23p63d104s24p233、砷As 1s22s22p63s23p63d104s24p334、硒Se 1s22s22p63s23p63d104s24p435、溴Br 1s22s22p63s23p63d104s24p536、氪Kr 1s22s22p63s23p63d104s24p6小结:相关规律1、基态原子最外层为1个电子的是第ⅠA族、Cu、Cr2、基态原子最外层为2个电子的是第ⅡA族、He、21号至30号(Cu和Cr除外)3、基态原子只有1个未成对电子的是第ⅠA族、第ⅢA族、第ⅦA族、Cr、Cu4、基态原子只有2个未成对电子的是第ⅣA族、第ⅥA族5、基态原子只有3个未成对电子的是第ⅤA族6、基态原子没有未成对电子的是第ⅡA族、0族7、基态原子未成对电子最多的是Cr(有6个未成对电子)如有侵权请联系告知删除,感谢你们的配合!如有侵权请联系告知删除,感谢你们的配合!。
1-36号元素轨道图
dz2
价键法(VB法)价键理论一: 1、要点: ⑴、共价键的形成条件:①、先决条件: 原子具有未成对电子;②、配对电子参与 成键的原子轨道要满足对称匹配、能量相 近以及最大重叠的原则;③、两原子具有 成单的自旋相反的电子配对,服从保里不 相容原理。 ⑵、共价键的本质:是由于原子相互接近 时轨道重叠,原子间通过共用自旋相反的 电子使能量降低而成键。 ⑶、共价键的特征:①、饱和性,一个原 子有几个未成对电子(包括激发后形成的 未成对电子),便和几个自旋相反的电子 配对成键;而未成对电子数是有限的,故 形成化学键的数目是有限的。②、根据原 子轨道最大重叠原理,原子轨道沿其角度 分布最大值方向重叠,即共价键具有一定 的方向性。 ⑷、共价键的类型:单键、双键和叁键。
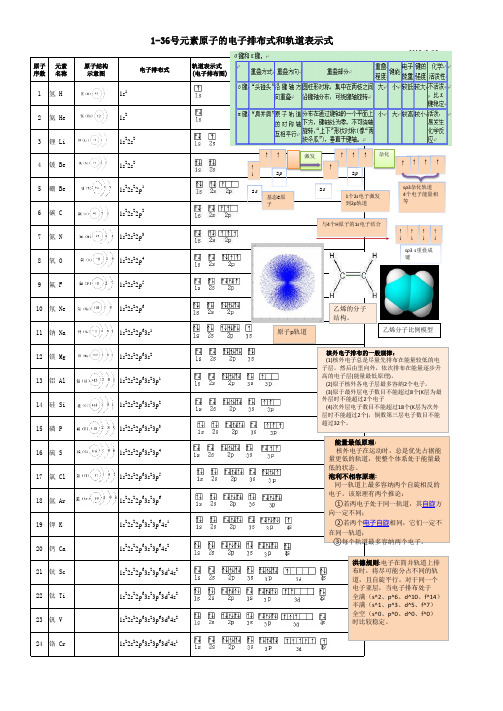
1-36号元素原子的电子排布式和轨道表示式
原子 元素 序数 名称
1 氢H
原子结构 示意图
电子排布式
1s1
轨道表示式 (电子排布图)
2013/9/12
2 氦 He
1s2
3 锂 Li 4 铍 Be 5 硼 Be 6 碳C 7 氮N 8 氧O
1s22s2 1s22s2 1s22s22p1 1s22s22p2 1s22s22p3 1s22s22p4
电离能:气态电中性基态原子失 去一个电子,转化为气态基态正离
子所需要的最低能量叫第一电离能。 符号:“I1”,单位:Kj/mol^-1。 “气态”、“电中性”、“基态” 是保证最低能量的条件。
[规律] 1.总体上金属元素第一电离能较 小非金属元素第一电离能较大. 2.同周期元素第一电离能从左到 右有增大的趋势 3.同主族元素第一电离能从上到 下逐渐减小
35 溴 Br
1s22s22p63s23p63d104s24p5
1-36号元素轨道图

电子亚层,当电子排布处于
全满(s^2、p^6、d^10、f^14) 半满(s^1、p^3、d^5、f^7) 全空(s^0、p^0、d^0、f^0) 时比较稳定。
25 锰 Mn 26 铁 Fe 27 钴 Co 28 镍 Ni 29 铜 Cu 30 锌 Zn
1s22s22p63s23p63d54s2 1s22s22p63s23p63d64s2 1s22s22p63s23p63d74s2 1s22s22p63s23p63d84s2 1s22s22p63s23p63d104s1 1s22s22p63s23p63d104s2
小。电负性的大小可以作为
判断元素金属性和非金属性
强弱的尺度。金属的电负性
一般小于1.8,非金属的电负
性一般大于1.8,而位于非金
属三角区边界的“类金属”
Px S
Py
Pz
的电负性则在1.8左右,他们 既有金属性又有非金属性。
dxy
dxz
dyz
sp 杂化轨道
sp2 杂化轨道
sp3 杂化轨道
sp3d2 杂化轨道
。
。 ,
; ,
能量最低原理: 核外电子在运动时,总是优先占据能 量更低的轨道,使整个体系处于能量最 低的状态。 泡利不相容原理: 同一轨道上最多容纳两个自旋相反的 电子。该原理有两个推论:
①若两电子处于同一轨道,其自旋方 向一定不同;
②若两个电子自旋相同,它们一定不 在同一轨道;
③每个轨道最多容纳两个电子。
洪德规则:电子在简并轨道上排 布时,将尽可能分占不同的轨
⑶ 形成的杂化轨道之间应尽可能地满足最 小排斥原理(化学键间排斥力越小,体系越稳 定),为满足最小排斥原理, 杂化轨道之间的夹 角应达到最大。
元素电子排布图

镓:1s22s22p63s23p63d104s24p1
锗:1s22s22p63s23p63d104s24p2
砷:1s22s22p63s23p63d104s24p3
硒:1s22s22p63s23p63d104s24p4
溴:1s22s22p63s23p63d104s24p5
硅:1s22s22p63s23p2
磷:1s22s22p63s23p3
硫:1s22s22p63s23p4
氯:1s22s22p63s23p5
氩:1s22s22p63s23p6
钾:1s22s22p63s23p64s1
钙:1s22s22p63s23p64s2
钪:1s22s22p63s23p63d14s2
钛:1s22s22p63s23p63d24s2
矾:1s22s22p63s23p63d34s2
铬:1s22s22p63s23p63d54s1
锰:1s22s22p63s23p63d54s2
铁:1s22s22p63s23p63d64s2
钴:1s22s22p63s23p63d74s2
镍:1s22s22p63s23p63d84s2
铜:1s22s22p63s23p63d104s1
氪:1s22s22p63s23p63d104s24p6
1s ,2s ,2p ,3s , 3p , 4s ,3d ,4p ,5s ,4d ,5p ,6s ,4f ,5d ,6p ,7s ,5f ,6d
1--36号元素轨道排布式
氢:
氦:
锂:
铍:
硼:
碳:
氮:
氧:
氟:
氖:
钠:
镁:
铝:
硅:
