大学物理热力学第一定律
大学物理化学 热力学第一定律

2.焓(H)
H≡U+PV dH=dU+PdV+VdP 推论: 恒压: dH=dU+PdV 恒压仅作体积功:
δQ=dH=dU+PdV Qp=ΔH
说明:焓的引入用了恒压过程,但并不意味只有 恒压过程才有体系的焓变; Qp是热量,非状态函数。
Cp与Cv的关系
Cp-Cv= H
T
其数值与体系中物质的量无关,不具有 加合性,整体的强度性质的数值与体系 中各部分的强度性质的数值相同。
如:
温度、压力、浓度、密度等。
容量性质:
其数值与体系中物质的量成正比,具有 加合性,整体容量性质的数值等于体系 中各部分该性质数值的总和。
如:
体积、质量、能量等。
二、状态、状态函数
1.状态 体系一系列宏观性质的综合,包括如质 量、温度、压力、体积和组成等。
推论: 1.对于理C想P=气体HT 发P 生的过程而言,当温
度不变时,则焓变为零,即ΔH=0;2.如果温 度发生改变,其焓变量为
ΔH= TT12 nCP,mdT
CP与CCPV-的CV关=系 p:
U V
T
dV
有C -C =
p
V
p
U V
T
V T
p
1.3热力学第一定律的应用
一、热力学第一定律对理想气体的应用 1. 低压气体的自由膨胀实验(焦耳)
结果:温度恒定,气体的内能不变, 内能与压力和体积无关……焦耳定律
2.理想气体的内能
热力学体系:无宏观动能(体系静止),宏观 势能对体系影响小,可不予考虑。
ΔU= Q+W
仅作体积功恒压: ΔU=QP+p ΔV
大学物理第二十四讲 热力学第一定律、摩尔热容PPT课件

U
CV ,mT
i 2
RT
3104 J
2. Qp Cp,mT Cp,m (T2 T1) Cp,m (t2 t1)
t2
t1
Qp
Cp,m
t1
2Qp
(i 2)R
36C
t1 0C
19
例:热力学系统经历如图所示过程后回到初态a。设过 程 abc 中吸热600 J;过程 cda 向外放热450J,对外做 功-150J,求系统在 abc 过程中内能的增量及对外做功。
Please Criticize And Guide The Shortcomings
讲师:XXXXXX XX年XX月XX日
R(T2
T1)
o
VV
●等容过程中系统从外界吸收的热量全部转化为
系统的内能。
10
三、等压过程
dp 0
pV RT U i RT
2 Q U A
U
i 2
R(T2T1)ppA V2 V1
pdV
p(V2
V1 )
A
R(T2 T1)
o
V1
V2 V
Qp
U
A
i 2
R(T2
T1)
R(T2
T1)
Tb 2Ta Tc , Td Ta , Vc V3 4V1
所以
U
i 2
R(Td
Ta )
0
p
p2 a
Aab p2 (V2 V1) 2 p1V1 2 RTa
Abc
RTb
ln
Vc Vb
2 RTa
ln 2
p1
o V1
Acd p1(V2 V3 ) 2 p1V1 2 RTa
b 等温线
大学物理第10章 热力学第一定律08-2

O V1
V2
R( T2 T1 )
V
i (5)内能增量: E R( T2 T1 ) CV ( T2 T1 ) 2
(6)吸热: Qp E A ( CV R )(T2 T1 ) C P (T2 T1 ) 等压膨胀过程中,A>0,△E>0,气体吸热QP>0 等压压缩过程中,A<0,△E<0,气体放热QP<0
i 1. 25 5 E RT 8. 31 1 927 ( J ). 2 0.028 2
Q E A 927 371 1298 ( J ).
二、 热 容
系统和外界之间的热传递通常 会引起系统本身温度的 变化 。这一温度的变化和热传递的关系用热容表示 。 1、摩尔热容 •定义: 一摩尔物质温度升高1K所吸收的热量,称为 该物质的摩尔热容。符号:Cm (可简记为C)
无论过程是准静态 的还是非静态的
绝热膨胀,气体对外做功, 其内能减少;温度降低
dQ 0, dA dE
绝热压缩,外界对气体做功, 其内能增加;温度升高。
(2).绝热准静态过程的过程方程(推导) 理想气体状态方程: PV RT VdP PdV RdT dA PdV dE CVVdP CV PdV RPdV PdV C dT
dQ C dT
•特性: ① 物质固有属性;
单位: J / mol K
② 因热量是过程量,所以C与过程有关: 系统压强保持不变的过程中的热容叫定压热容CP。
系统体积保持不变的过程中的热容叫定体热容CV。
2、定体摩尔热容 一摩尔理想气体在等体积过程中温度升高1K所吸 收的热量称为理想气体的定体摩尔热容
(A)T
V2 V2 V1
大学物理第4章-热力学第一定律

mol 理想气体的内能:
i E νRT 2
理想气体的内能是温度 T 的单值函数
i ΔE νR ΔT 2
QUIZ Jack’s death due to the loss of a) love b) temperature c) heat d) internal energy
热量是过程量,内能是状态量。
二、热 量
dQ 0 表示系统从外界吸热; dQ 0 表示系统向外界放热。
在SI制中:焦耳(J)
准静态过程中传递的热量是过程量。
三、热量的单位
结 论:
热量和功是系统状态变化中伴随发生的两种 不同的能量传递形式。它们的物理本质不同 宏观运动 分子热运动 功 热量 分子热运动 分子热运动
作功和传热的大小不但与系统的初、末态有关, 而且与过程有关,它们都是过程量,不是状态量, 因而微量功和微量传热分别写成 dA和dQ,它们不是全 微分。
dQ Cp ( )p dT
摩尔定压热容 Cp,m
i i Q E A RT RT 1 RT 2 2
Cp,m 1 dQ i 1 R dT p 2
:摩尔数
i:自由度数
三、迈耶公式及比热容比 摩尔定体热容 CV,m 摩尔定压热容 Cp,m 迈耶公式 比热容比
CV,m 3 R 2
5 R 2
Cp,m 5 R 2 7 R 2
1.67 1.40
刚性多原子分子
3R
4R
1.33
思考:为什么理想气体任意两状态间内能的变 化可表示成摩尔定体热容 CV,m 与温度变化乘积 的关系,而不是摩尔定压热容 Cp,m 与温度变化 乘积的关系?
大学热学物理知识点总结

大学热学物理知识点总结1.热力学基本定律热力学基本定律是热学物理的基础,它包括三个基本定律,分别是热力学第一定律、热力学第二定律和热力学第三定律。
(1)热力学第一定律热力学第一定律是能量守恒定律的热学表述,它规定了热力学系统能量的守恒性质。
简单地说,热力学第一定律表明了热力学系统能量的增减只与系统对外界做功和与外界热交换有关。
热力学第一定律的数学表达式为ΔU=Q-W,其中ΔU表示系统内能的增量,Q表示系统吸热的大小,W表示系统对外界所作的功。
由此可以看出,系统的内能变化量等于吸收热量减去做的功。
(2)热力学第二定律热力学第二定律是热力学系统不可逆性的表述,它规定了热力学系统内部的熵增原理,即系统的熵不会减小,而只会增加或保持不变。
简单地说,热力学第二定律表明了热力学系统内部的任何一种热力学过程都是不可逆的。
这意味着热力学系统永远无法使热量全部转化为功,总会有一部分热量被转化为无效热。
热力学第二定律还表明了热力学过程的方向性,即热量只能从高温物体传递到低温物体,而不能反向传递。
(3)热力学第三定律热力学第三定律规定了当温度趋于绝对零度时,任何物质的熵都将趋于一个有限值,这个有限值通常被定义为零。
简单地说,热力学第三定律表明了在绝对零度时,任何系统的熵都将趋于零。
热力学第三定律的提出对于热学物理的研究具有非常重要的意义,它为我们理解热学系统的性质提供了重要的基础。
2.热力学过程热力学过程是指热力学系统内部发生的一系列变化,包括各种状态参数的变化和热力学系统对外界的能量交换。
常见的热力学过程有等温过程、绝热过程、等容过程和等压过程等。
这些过程在日常生活以及工业生产中都有着广泛的应用。
(1)等温过程等温过程是指在恒定温度下进行的热力学过程。
在等温过程中,系统对外界做的功和吸收的热量之比是一个常数。
这意味着等温过程的压强和体积成反比,在P-V图上表现为一条双曲线。
常见的等温过程有等温膨胀和等温压缩等。
(2)绝热过程绝热过程是指在无热交换的情况下进行的热力学过程。
大学物理第三章热力学第一定律第四章热力学第二定律

B C AD
氮气 氦气
35
B C AD
氮气 氦气
解: 取(A+B)两部分的气体为研究系统, 在外界压缩A部分气体、作功为A的过程 中,系统与外界交换的热量 Q 0
Q E ( A) 0
36
B
氮气
C
AD
氦气
系统内能的变化为
E E A E B
5 E B RTB 2
内能:态函数,系统每个状态都对应着一定内能的数值。 功、热量:只有在状态变化过程中才有意义,状态不 变,无功、热可言。
9
五、热力学第一定律
1. 数学表式 ★ 积分形式 ★ 微分形式
Q E A
dQ dE dA
10
2. 热力学第一定律的物理意义 (1)外界对系统所传递的热量 Q , 一部分用于 系统对外作功,一部分使系统内能增加。 (2)热一律是包括热现象在内的能量转换和守恒 定律。
m i E RT M2
m i i m E RT R T末 T初) ( M2 2M
i dE RdT 2
8
注意 :
10 作功和传热对改变系统的内能效果是一样的。 (要提高一杯水的温度,可加热,也可搅拌)
20 国际单位制中,功、热、内能单位都是焦耳(J)。 (1卡 = 4.18 焦耳) 30 功和热量都是系统内能变化的量度,但功和热本身不 是内能。
绝热线
斜 率
PV C1
dP K 绝热 dV
P V
26
K 绝热 同一点 P0,V0,T0 斜率之比 ( ) K 等温
P0 K绝热 V0 P0 K等温 V0
P
a
等温
结论:绝热线比等温线陡峭
大学物理 第21章 热力学第一定律
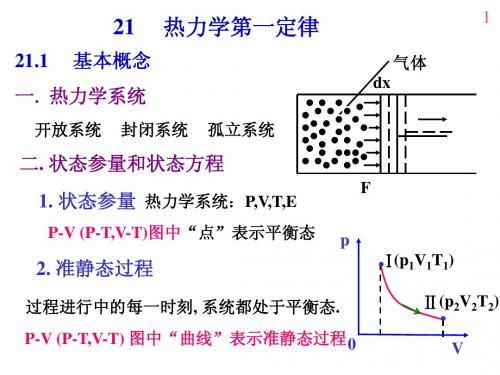
.Ⅰ(p V T )
1 1 1
Ⅱ(p2V2T2)
.
V
21.3 热力学第一定律
一. 功
系统对外做功(体积功) dx 气体 F
2
A Fdx PSdx PdV
A dA PdV
V1 V2
讨论:
1)A > 0 系统对外界做正功; A < 0 系统对外界做负功。 2)P-V 图上曲线下面积表示体积功大小。 3) 功是过程量。
CV (
定体摩尔热容量 CV , m
1 Q 摩尔热容量 C m dT
Q>0 Q<0
从外界吸收热量 系统向外界放热
dT dT 1 Q 1 dE ( )V ( ) dT dT
)V (
)V
三、内能
系统内所有粒子各种能量的总和。 热力学领域:系统内所有分子热运动动能和分子间 相互作用势能之和。 通常
绝热线比等温线陡
p1 p2 p2
0
等温线
( 1)
V
p nkT
{
等温: T不变,n
绝热: T ,n
p p
V1
V2
9
11
用比较曲线斜率的方法证明在p---V图上相交于任一点的理想 气体的绝热线比等温线陡。
证明:过p---V图上任一点(p,V)点,等温线的斜率为:
dp d C C pV p ( )T [ ( )]T 2 2 dV dV V V V V
4
E E (T ,V )
——内能是状态量。
理想气体内能:仅为分子热运动的各种动能之和。
——理想气体的内能是温度的单值函数。
M i E RT M mol 2
【大学物理】第15章热力学第一定律

例补:20mol氧气由状态1变化到状态2所经历的过程
如图,(1)沿1-m-2路径;(2)沿1-2直线。试分
别求出这两过程中的A与Q及氧气内能的变化 氧气分子当成刚性分子理想气体看待。
E2
E1
p(1.03105 pa)
20 2
m
5 0 10
1
50 V (L)
解(1)1-m-2过程:
对于1-m过程,由于体积不变(等容过程),所以
I绝热膨胀:V2 V1 T2 T1
II绝热压缩:V2 V1 T2 T1
四、绝热过程的P-V图
1、P-V图: 将绝热方程代入
A V2 PdV 可得: V1
A P1V1 P2V2
1
A
p1V1
1
1
V1 V2
1
dQ dE dA dE PdV
dE 0
PV M RT
( dQ)T dA PdV
QT
A
V2 PdV
V1
代入上式
QT
M
RT
V2 dV V V1
M
RT ln V2 V1
P1V1 P2V2
QT
M
RT
ln
P1 P2
3、理想气体等温过程作功图示:
对于AB过程,因为热力学第一定律得气体吸收的热量应等于气体对外做的功, 功可以通过过程曲线下的面积求得
QAB
WAB
1 2 (pA
pB )(VB
VA )
大学物理第二十四讲 热力学第一定律、摩尔热容

B
A
C
t T 273.15C
说明:零定律的 条件:物体A、B 和C与外界没有热 与能的交换。
2
§12-2 准静态过程、功、热量
一、准静态过程 热力学过程—热力学系统的状态随时间的变化。 ★在状态变化的过程中系统处于非平衡态。
准静态过程—变化无限缓慢的过程。 ◎准静态过程中,任意时刻系统所处状态—准平衡态 (准静态)。 如活塞运动:快—非平衡过 程,慢—准平衡。 ◎许多实际过程都可看作 准静态过程。
Q Cm dT
● Q与过程有关,故Cm和c都是过程量,其值与过程 有关。
12
一、理想气体的定容摩尔热容CV,m
★在等容过程中,一摩尔气体温度升高1K时所吸收的 热量:
CV ,m
( Q )V dT
i ( Q )V dU RdT 2 CV ,m ( Q )V i R dT 2
p1
c
V3 V
24
V2
全过程做功
A Aab Abc Acd Abc 2RTa ln2
◎上式是计算理想气体内能的普遍公式,不论何种 过程(U 是状态量,与具体过程无关)。
14
二、理想气体的定压摩尔热容 CP,m
◎在等压过程中,一摩尔气体温度升高1K时所吸收 的热量。
( Q ) p dU pdV
dU CV ,m dT
pdV RdT
pV RT dp 0
Tb 2Ta Tc , Td Ta , Vc V3 4V1
i p 所以 U R(Td Ta ) 0 2 p2 Aab p2 (V2 V1 ) 2 p1V1 2 RTa
a
b
d
大学物理第二章 热力学第一定律要点

2) 恒压过程:变化过程中p(系) = p(环) = 常数,(dp=0)
(p(始) = p(终) = 常数,为等压过程, p = 0 )
3) 恒容过程:过程中系统的体积始终保持不变 4) 绝热过程:系统与环境间无热交换的过程
5) 循环过程:经历一系列变化后又回到始态的过程。 循 环过程前后状态函数变化量均为零 。 6) 可逆过程:系统经历某过程后,能够通过原过程的反 向变化而使系统和环境都回到原来的状态
U=f (T ,V ) U U dU dV dT V T T V
又 dT = 0, dU = 0, dV 0
U 0 V T
即: 恒温时,U不随V变化
U=f (T) 理想气体单纯 pVT 变化时,U 只是 T 的函数
(液体、固体近似成立)
§2.3 恒容热、恒压热与焓的导出 1. 恒容热(QV):
对于封闭系统,W =0 时的恒容过程: ∵ dV=0 ,∴W = 0,有:
QV ΔU U2 U1
及 δQV dU
2. 恒压热(Qp):
对于封闭系统,W = 0 时的恒压过程: W= – pambV= – p(V2 – V1) = – (p2V2 – p1V1)
(H的定义虽然由恒压过程导出,但可用于任何过程的计算)
H: 状态函数, 广度量, 单位 J 理想气体,单纯 pVT 变化,恒温时: ∵ U = 0 ∴ H = U + (pV) = 0 + (pV) = (nRT) = nRT = 0 H = f ( T ) 理想气体单纯 pVT 变化时,H 只是 T 的函数
摩尔热容
相变焓
大学物理课件热学-热力学第一定律

PF S
如果活塞没有加速度(或可忽略), 由力学的动量守恒,有外压力与气 体压力相等。这时:
A PdV
3.热量:物体间通过热接触传递的能量。热量的测量方法:量热技术。
Q=?
实验时,如果电阻的欧姆热全部流入系统,有
一
Q / t RI 2
般
是
电阻
电流
间
接 地
如果一定量的机械能通过摩擦产生的热都流入了系统,有
B
如果从B到A,放热.
注意:一个过程不一定从头到尾都吸收或放热.
V
它可能有时吸收热, 有时放热.
因此分析整个过程吸收或放热是, 应一小段,一小段地考虑
6.理想气体平衡过程分析: 等温过程、绝热过程、等容过程、循环过程,……
等容过程 dV=0 : (1) A 不变化: A=0!
P
A
(2) 热:
B
Q U dU T
p1
ab
试求: ( 1)状态d的体积Vd;
d
(2)整个过程对外所作的功; o
V
(3)整个过程吸收的热量。
V1 2V1
解:(1)根据题意 Ta Td
又根据物态方程 pV RT
Td
Ta
p1V1 R
p
Tc
pcVc R
4 p1V1 R
4Ta
2p1
c
再根据绝热方程TcVc 1 TdVd 1 p1 a b
3 热力学第一定律
(能量守恒: 能量与能流)
1.物体的能量: 内能或热力学能量。有时可分为:1机械能 + 2热能。
能量概念来自对力学运动规律的研究。 从质点动力学人们认识到,比如:
弹簧质点组成的“孤立”系统:
m1
大学物理热力学第一定律

[例题25.2]以理想气体为工质的卡诺 例题 ]以理想气体为工质的卡诺 循环由两个等温过程和两个绝热过程 循环由两个等温过程和两个绝热过程 组成。试求该循环效率。 组成。试求该循环效率。
ch25
• 循环 • 卡诺循环 • 效率 温度恒定的高温热源T 温度恒定的高温热源 1 Q1 Q2 A
温度恒定的低温热源T 温度恒定的低温热源 2
ch25
=Q
外界对系统所作的功: 外界对系统所作的功:A
=0
V
Q 系统从外界吸收的热量: 系统从外界吸收的热量: = C v (T2 − T1 )
(3) 等压过程 特征: 特征: 系统压强不变 p = 常数 内能的增量: 内能的增量: ∆U
= A + Q = C v (T2 − T1 )
A 外界对系统所作的功: 外界对系统所作的功: = − p(V2 − V1 )
温度
处在同一平衡态的所有热力学系统都有一个共同 的宏观性质, 的宏观性质,这个决定系统热平衡的宏观量定义 为温度。 为温度。
ch25
温标
热力学温标
t / C = T / K − 273
理想气体的物态方程
pV = ν R T
热力学第一定律
热力学系统终态2和初态1的内能之差U 热力学系统终态2和初态1的内能之差U2-U1,等于 在过程中外界对系统所作的功A 在过程中外界对系统所作的功A与系统从外界吸收 的热量Q 的热量Q之和
系统从外界吸收的热量: = 系统从外界吸收的热量:Q= 0
p V γ = 常数 T V γ − 1 = 常数
绝热方程- 绝热方程-泊松方程
pγ − 1 T − γ = 常数
(5) 多方过程 p V m = 常量 m = 1 m = 0 —— 等温过程 —— 等压过程
大学物理第三章 热力学第一定律

§ 2.1 准静态过程 § 2.2 功、热、内能 § 2.3 热力学第一定律 § 2.4 热容量 § 2.5 理想气体的绝热过程 § 2.6 循环过程 § 2.7 卡诺循环 § 2.8 致冷循环
本章讨论热力学系统的状态发生 变化时在能量上所遵循的规律- ---热力学第一定律
§2.1 准静态过程
i i 解: E1 RT1 P 1V1 2 2
i i E2 RT2 P2V2 2 2
V1 1 V2 2
1
E1 P 1 V1 E2 P2 V2
2 7
P 1 2 P2
对双原子分子 7/5
E1 2 1.22 E2
例 2: 温度为 25C、压强为 1 atm 的
m QV E CV ,m (T2 T1 ) M
等容过程:
二、 定压摩尔热容
C p ,m dQ dT p
理想气体等压过程:
dQ dE PdV
i dV dE pdV dE dQ RR p 2 dT dT dT dT P
功、热 都能改变 系统状态
dQ<0表示系统向外界放热
总热量:
Q 1 dQ
2
积分与过程有关 。
三、系统的内能E
对理想气体、处于温度为T的平衡态:
i E RT 2
i i E RT pV 2 2
系统的内能是状态量,如同
P、V、T等量
小结
1)改变系统状态的方式有两种
作功 传热
2)作功、传热是相同性质的物理量均是 过程量 系统的内能是状态量
C p ,m Cv,m
Cv,m R Cv,m
i2 R 2
大学物理第15章-热力学第一定律

所吸收的热量为 E4 E1 A 1869 747.6 26166 J Q .
一、摩尔热容 C
系统在一个过程中从外 界吸热(放热) ,温度上升(降低) ,定义: dQ dT
热容量
dQ C dT
摩尔热容C: 物质温度升高 K所吸收的热量,即 1mol 1
C C
dQ C dT
式中m, M分别为气体的总质量和 摩尔质量。
例:如图,系统沿过程 曲线abc态变化到c态共吸收热量 J,沿 500 过程曲线cda回到a态,向外放热 J,外界对系统作功 J, 300 200 求系统在abc过程中系统内能增加及 对外作功。 P
解:在cda过程中Q 300J,A 200J, 根据热力学第一定律, 有
p
III( p3 ,V3 , T3 )
T1 300K
p1 p2 p4 1.013 105 P a m RT1 2.8 103 8.31 300 V1 M p1 28 103 1.013 105 2.46 10 ( m )
3 3
2
IV( p4 ,V4 , T4 ) I ( p1 ,V1 , T1 ) II( p2 ,V2 , T2 )
单原子分子气体( 3): i
CV
3 R 2
CP
5 R 2
5 3
刚性双原子分子理想气 体(i 5),有
CV
5 R 2
CP
7 R 2
先求出每个分过程的 E, A, Q, 然后将其相加。
i) I II等压(P 0)
A1 pdV p1 (V2 V1 ) 1.013105 2.46103 249( J )
v1 v2
《大学物理》第19章 热力学第一定律

O
V
dV 0 dW 0
dT 0 dEint 0 dQ 0
O
V
dV 0 dW 0
dT 0 dEint 0 dQ 0
上页 下页 返回 退出
热力学第一定律
dEint dQ dW
dQp
dE
dW
m M mol
(CV
R)dT
在等压过程中,理想气体吸热的一部分用于 增加内能,另一部分用于对外作功。
上页 下页 返回 退出
此外, 由于
可知
也与实验结果相符.
对于分子结构更复杂的气体,分子热容变大。 这是因为存在其他形式的内能(转动,振动等)
上页 下页 返回 退出
自由度
每一个转动或振动模式对应一个自由度。
能够描述整个运动过程的维度
上页 下页 返回 退出
z
z
C(x, y, z)
y x
单原子分子
C(x, y, z)
气体向外界释放的净热 量为多少?
上页 下页 返回 退出
系统
1
P
b
s2
膨胀过程
a
2
s1
压缩过程
外界
W1a2 s1 0 W2b1 (s1 s2) 0
O V1
V2 V
W1a2b1 W1a2 W2b1 s2 0
DEint Q W
0
S2 S2
上页 下页 返回 退出
理想气体
Q0
上页 下页 返回 退出
§19-8 气体分子热容与能量均分定理 气体的摩尔热容
气体的比热与热力学过程有关
对于气体而言,等体过程和等压过程的比热是不同的
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
绝热线的斜率大于 等温线的斜率
pdV Vdp 0
dp dV
T
pA VA
24
Note:
其他过程方程:
e.g. 等体过程: p C
T 等压过程: V C
T
等温过程: pV C
25
2. 绝热过程中,理想气体对外做功:
V2
A pdV
V1
p1V1
V2 V1
dV V
p2V2
V2 V1
dV V
p
1
2
p=const.
O 因 dQ
V 摩尔定压热容
M
Mmol C pdT
又 dE
M Mmol CV dT
且 dA M RdT
M mol
17
注:pV M RT p=const .
M mol pdV M RdT
M mol
由 dQ=dE+dA 代入、、
得 C p = CV + R ——迈耶(Mayer)公式
V1
V
RT ln V2 2.72103 J
V1
(2) 根据绝热过程方程,有
OV
T2 T1(V1 V2 ) 1 192 K
pV C2
pV C1
3V V
31
将热力学第一定律应用于绝热过程方程中,有
A E E CV (T2 T1) 2.2 103 J
所以 A 2.2 103 J
32
重力型
蓄水槽
发电机
电池
泵
蓄水槽
浮力型 毛细型 子母型 ……
即:E 0, Q 0, A 0
违反热力学第一定律,所以不可能成功。
14
§2.2 等体过程 isochoric process
p
2
V=const.
dA= 0
1
O
V
dQ=dE
摩尔定体热容
因
dQ
M M mol
CV dT
dE M i RdT
30
例 温度为 25 ℃,压强为1 atm 的1 mol 刚性双原子分子理想气 体经等温过程体积膨胀至原来的 3 倍。
求 (1) 该过程中气体对外所做的功; (2) 若气体经绝热过程体积膨胀至原来的 3 倍,气体对外所 做的功。
解 (1) 由等温过程可得
p
A V2 pdV V2RT dV
V1
若 dV > 0, 则 dA> 0,即系统体积膨胀,对 外界作正功
若 dV < 0, 则 dA< 0,即系统体积收缩,对 外界作负功
8
对于任一有限准静态过程, V1V2 :
A V2 pdV 积分的意义? V1
Note: 功是过程量, 其值依赖于过程
p
p1
1 ( p1,V1,T1)
p2
2 ( p2,V2,T2 )
理想化实验
p
p1 1 ( p1,V1,T1)
p2
o V1
2( p2 ,V2 ,T2 )
V2 V 3
准静态过程
过程进行时要破坏平衡 系统处于非平衡态。 但如果过程进行得足够缓慢,系统通过分子 的频繁碰撞来得及不断建立一系列平衡态,就 可以把这一过程看成准静态过程。
准静态过程例1:气体无穷小压缩或膨胀。
n = 0 p= C2 等压过程
n 1 pV C 等温过程
n pV C1 绝热过程
n = V= C3 等体过程
V
28
•功
A
V2 pdV
V1
V2 V1
p1V1n
dV Vn
1( n 1
p1V1
p2V2 )
R
n 1 (T2 T1) • 内能增量
E CV (T2 T1)
• 热量
pγ -1T -γ = C3 ⑥ (C1 , C2 , C3 是常量)
④⑤⑥——绝热过程方程
23
2. 绝热线和等温线
p
等温线
绝热线
pA papT A C
B
绝热 pV γ const.
γpV γ-1dV V γdp 0
dp dV
a
γ
pA VA
o VA V VB V 等温 pV const.
热力学系统随时间的变化叫做热力学过程, 简称过程。
热力学理论具有高度的可靠性和普适性,它 不仅适用于气体,也适用于液体、固体等其他 热力学系统。
热力学理论主要包括三个定律: 第一定律:系统在过程中能量的变化关系。 第二定律:自然过程进行的方向。
第三定律:通过有限过程不可能把物体冷却 到绝对零度。
第二章 热力学第一定律
§2.4 等温过程 isothermal process
p1 O
2 V
恒
温 热 源
T p
T
Δl
T=const. dE = 0 dQ = dA
于是 Q A V2 pdV V2 M RT dV
V1
M V1
mol
V
M RT ln V2
M mol
V1
20
§2.5 绝热过程 adiabatic process
热力学第一定律适用于任何过程,并不要求 过程必须经历平衡态。但为了简单,下面介绍 理想气体在准静态过程中的内能、功和热量。
1. 内能
温度 T1 T2, (mol)理想气体内能增量:
E
i
2
R(T2
T1)
i
2
RT
2. 功和热量
p
⑴系统对外做的功
S
dl
准静态过程中, 气体作功: dA = pSdl = pdV
o V1
V2 V
9
⑵系统吸收的热量
准静态过程中, TT+dT: dQ M C dT M mol 该过程中的摩尔热容
dQ >0: 系统吸热;dQ <0: 系统放热
Notes: ① C也是过程量.
e.g. 绝热压缩过程:dQ=0, dT>0 C=0
等温膨胀过程:dQ>0,
dT=0
C 10
②若有限过程中C=const.,则有
各步间压强差无穷 p+dp 小,过程足够缓慢,中
间态趋于平衡态。
准静态过程例2:无穷小温差热传导。
系统 T1
热源
有限温差传热
T2
非准静态过程
系统 T1
T1+dT T1+2dT T1+3dT
无穷小温差传热
各步间温差无 穷小,过程足够缓 T2 慢,中间态趋于平 衡态。
无穷小温差热传导——也称为等温热传导。
1
A
( 1
p1V1
p2V2 )
2. 绝热过程中,理想气体对外做功:
A
(E2
i 2
(
P1V1
E1 ) ν P2V2 )
i 2
R(T2
T1
)
γ CP i 2 CV i
i 1 2 γ 1
γ
1 1
( P1V1
P2V2
)
27
补充:多方过程**
•方程
p
O
pV n C ( n 多方指数,1 < n < )
求 压缩后的压强和温度。 解 氮气是双原子分子
C p (7 2) 7
CV (5 2) 5
根据绝热过程方程 p1V1 p2V2 C
7
p2 p1(V1 V2 ) 155 9.52 atm
根据绝热过程方程 TV 1 C2 ,有
T2
T1(V1
V2 ) 1
7 1
30055
571 K
The First Law of Thermodynamics
主要内容
功 热量 热力学第一定律 等值过程 绝热过程 循环过程
重要概念 准静态过程、热量(Q)、
功(A)、内能(E)
2
准静态过程(理想化的过程)
从一个平衡态到另一平衡态所经过的每一 中间状态均可近似当作平衡态的过程
砂子 活塞 气体
Qn
E
A
(CV
1
R n
)(T2
T1)
• 摩尔热容
说明
Cn
Qn
(T2 T1)
R n
CV
1 n
n 1 CV
若 1 < n < ,则 Cn < 0,表示系统吸热,温度反而下降。 29
例 一定量氮气,其初始温度为 300 K,压强为 1 atm。将其绝热 压缩,使其体积变为初始体积的 1/5。
对无穷小绝热过程:pdV dE , pdV CV ,mdT
dT pdV ( CV ,m ) , pdV Vdp (R CV ,m ) pdV
(CV ,m R) pdV CV ,mVdp 0, CV ,m R Cp,m , dV dp 0, lnV ln p 常量
§2.6 绝热自由膨胀 free expansion
p1、V1 T1
p2、V2、T2
不是准静态过程,但仍服从热力学第一定律
绝 热 → Q=0
绝热自由膨胀的始末态 是等温线上的二点
自由膨胀 于是
→ A=0 p
E2E1 = 0 不是绝热自由膨胀的中间态
T2=T1
O
isotherm 1 初态 2 末态 V
or
i+2 Cp = 2 R
——常量
18
于是对有限等压过程有:
Q
M M mol
C p (T2
T1 )
此外 E2 E1
M M mol
CV
(T2
T1 )
A p(V2 V1 )
M M mol
R
(T2
T1 )
