仪器分析-武大
武大仪器分析教学大纲——材料科学与技术专业本科生)

反相液相色谱法分离芳香烃
4.5
毛细管区带电泳(CZE)分离硝析
4.5
热重-差热分析法研究高分子材料的脱水过程
4.5
纳米材料的X-射线粉末衍射分析
4.5
四、教材与参考书
教材:《仪器分析实验》,武汉大学出版社,武汉大学化学实验教学中心,2004
参考书:
《材料结构分析实验》课程教学大纲(材料科学与技术专业本科生)
课程代码:1300531
课程负责人:赵发琼
课程中文名称:材料结构分析实验
课程英文名称:Experiments of Structure Analysis of Advanced Materials
课程类别:必修
课程学分数:2
课程学时数:72
三、课程内容与学时分配
光谱分析(包括吸收光谱、发射光谱、荧光光谱、X-射线粉末衍射等)、电化学分析(电位分析法、电解和库仑分析法、伏安分析法)、分离分析(气相色谱、液相色谱、毛细管电泳,新型位萃取材料及相关联用技术)以及核磁、质谱等。
课程内容与学时分配表
内容
学时
火焰原子吸收光谱法测定水中的镉
4.5
ICP-AES测定水中的微量Cu,Fe和Zn
[1]《仪器分析实验》,科学出版社,张剑荣、万惠群、戚苓,1999;
[2]《仪器分析》,科学出版社,万惠群、于俊生、史坚,2002;
[3]《基础分析化学实验》,北京大学出版社,北京大学化学系仪器分析教学组编,1993;
[4]《化学基础实验》,南京大学出版社,孙尔康,吴琴缓等,南京,1991;
[5]《现代仪器分析实验与技术》(第2版),清华大学出版社,陈培榕,李景虹,邓勃,2006。
五、考核方式
平时成绩(操作:报告=6:4)70% +期末考试30%
武汉大学第五版仪器分析仪器分析讲义

仪器分析讲义绪论(Introduction)仪器分析是化学类专业必修的基础课程之一。
通过本课程的学习,要求学生把握经常使用仪器分析方式的原理和仪器的简单结构;要求学生初步具有依照分析的目的,结合学到的各类仪器分析方式的特点、应用范围,选择适宜的分析方式的能力。
分析化学是研究物质的组成、状态和结构的科学。
它包括化学分析和仪器分析两大部份。
化学分析是指利用化学反映和它的计量关系来确信被测物质的组成和含量的一类分析方式。
测按时需利用化学试剂、天平和一些玻璃器皿。
它是分析化学的基础。
仪器分析是以物质的物理和物理化学性质为基础成立起来的一种分析方式,测按时,常常需要利用比较复杂的仪器。
它是分析化学的进展方向。
仪器分析与化学分析不同,具有如下特点:(1)灵敏度高,检出限量可降低。
如样品用量由化学分析的ml、mg级降低到仪器分析的µL、µg级,乃至更低。
它比较适用于微量、痕量和超痕量成份的测定。
(2)选择性好。
很多仪器分析方式能够通过选择或调整测定的条件,使共存的组分测按时,彼其间不产生干扰。
(3)操作简便、分析速度决,易于实现自动化。
(4)相对误差较大。
化学分析一样可用于常量和高含量成份的分析,准确度较高,误差小于千分之儿。
多数仪器分析相对误差较大,一样为5%,不适于常量和高含量成份的测定。
(5)需要价钱比较昂贵的专用仪器。
§1-1.仪器分析方式的内容和分类(Classification of Instrumental Analysis)分类:1.光学分析法以物质的光学性质为基础的分析方式(1) 分子光谱: 红外吸收可见和紫外分子荧光拉曼光谱(2) 原子光谱: 原子发射AES 原子吸收AAS 原子荧光AFS(3) X射线荧光: 发射吸收衍射荧光电子探针(4) 核磁共振顺磁共振2.电化学分析法溶液的电化学性质用于确信物质化学成份的方式(1)电导法:电导分析法电导确信物质的含量电导滴定法溶液的电导转变确信容量分析的滴定终点。
(完整版)武汉大学版仪器分析知识点总结(适用考中科院的同学)
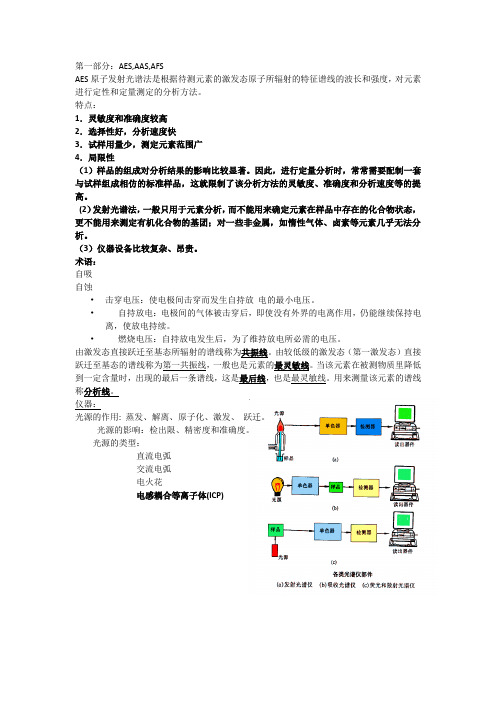
①. 自然宽度ΔυN 它与原子发生能级间路迂时激发态原子的有限寿命有关。 一般情况下约相当于 10-4 Å
②. 多普勤(Doppler)宽度ΔυD 这是由原子在空间作无规热运动所引致的。故又称热变宽。
碰撞变宽:原子核蒸气压力愈大,谱线愈宽。 同种粒子碰撞——赫尔兹马克(Holtzmank)变宽, 异种粒子碰撞——称罗论兹(Lorentz)变宽。 场致变宽:在外界电场或磁场的作用下,引起原子核外层电子能级分裂而使谱线变宽现象称 为场致变宽。由于磁场作用引起谱线变宽,称为 Zeeman (塞曼)变宽。
例如砷、锑、铋、锗、锡、铅、硒和碲等元素。 固体试样
(1). 试样直接插入进样 (2). 电弧和火花熔融法 (3). 电热蒸发进样 (4). 激光熔融法 分光仪棱镜和光栅 检测器:目视法,摄谱法,光电法 干扰:
光谱干扰: 在发射光谱中最重要的光谱干扰是背景干扰。带状光谱、连续光谱以及光学系统的
杂散光等,都会造成光谱的背景。 非光谱干扰:
与试样组成相仿的标准样品,这就限制了该分析方法的灵敏度、准确度和分析速度等的提
高。
(2)发射光谱法,一般只用于元素分析,而不能用来确定元素在样品中存在的化合物状态,
更不能用来测定有机化合物的基团;对一些非金属,如惰性气体、卤素等元素几乎无法分
析。
(3)仪器设备比较复杂、昂贵。
术语:
自吸Biblioteka 自蚀• 击穿电压:使电极间击穿而发生自持放 电的最小电压。
交流电弧 中
火花
低
4000~7000 较差 4000~7000 较好 瞬间 10000 好
定性分析,矿物、纯物质、 难挥发元素的定量分析
试样中低含量组分的定量分 析
武大仪器分析知识点总结考研,期末复习

第一部分:AES,AAS,AFSAES原子发射光谱法是根据待测元素的激发态原子所辐射的特征谱线的波长和强度,对元素进行定性和定量测定的分析方法。
特点:1.灵敏度和准确度较高2.选择性好,分析速度快3.试样用量少,测定元素范围广4.局限性(1)样品的组成对分析结果的影响比较显著。
因此,进行定量分析时,常常需要配制一套与试样组成相仿的标准样品,这就限制了该分析方法的灵敏度、准确度和分析速度等的提高。
(2)发射光谱法,一般只用于元素分析,而不能用来确定元素在样品中存在的化合物状态,更不能用来测定有机化合物的基团;对一些非金属,如惰性气体、卤素等元素几乎无法分析。
(3)仪器设备比较复杂、昂贵。
术语:自吸自蚀•击穿电压:使电极间击穿而发生自持放电的最小电压。
•自持放电:电极间的气体被击穿后,即使没有外界的电离作用,仍能继续保持电离,使放电持续。
•燃烧电压:自持放电发生后,为了维持放电所必需的电压.由激发态直接跃迁至基态所辐射的谱线称为共振线。
由较低级的激发态(第一激发态)直接跃迁至基态的谱线称为第一共振线,一般也是元素的最灵敏线。
当该元素在被测物质里降低到一定含量时,出现的最后一条谱线,这是最后线,也是最灵敏线。
用来测量该元素的谱线称分析线。
仪器:光源的作用: 蒸发、解离、原子化、激发、跃迁。
光源的影响:检出限、精密度和准确度。
光源的类型:直流电弧交流电弧电火花电感耦合等离子体(ICP)光源蒸发温度激发温度/K 放电稳定性应用范围直流电弧高4000~7000 较差定性分析,矿物、纯物质、难挥发元素的定量分析交流电弧中4000~7000 较好试样中低含量组分的定量分析火花低瞬间10000 好金属与合金、难激发元素的定量分析ICP 很高6000~8000 最好溶液的定量分析ICP原理当高频发生器接通电源后,高频电流I通过感应线圈产生交变磁场(绿色)。
开始时,管内为Ar气,不导电,需要用高压电火花触发,使气体电离后,在高频交流电场的作用下,带电粒子高速运动,碰撞,形成“雪崩"式放电,产生等离子体气流。
仪器分析答案武汉大学

仪器分析答案武汉大学【篇一:分析化学》下册武汉大学等编(第五版)作业参考答案】t>第2章光谱分析法导论2-1 光谱仪一般由几部分组成?它们的作用分别是什么?参考答案:(1)稳定的光源系统—提供足够的能量使试样蒸发、原子化、激发,产生光谱;(2)试样引入系统(3)波长选择系统(单色器、滤光片)—将复合光分解成单色光或有一定宽度的谱带;(4)检测系统—是将光辐射信号转换为可量化输出的信号;(5)信号处理或读出系统—在显示器上显示转化信号。
2-2 单色器由几部分组成,它们的作用分别是什么?参考答案:(1)入射狭缝—限制杂散光进入;(2)准直装置—使光束成平行光线传播,常采用透镜或反射镜;(3)色散装置—将复合光分解为单色光;(4)聚焦透镜或凹面反射镜—使单色光在单色器的出口曲面上成像;(5)出射狭缝—将额定波长范围的光射出单色器。
2-5 对下列单位进行换算:-(1)150pm z射线的波数(cm1)(2)li的670.7nm谱线的频率(hz)-(3)3300 cm1波数对应的波长(nm)(4)na的588.995nm谱线相应的能量(ev)参考答案:(1)??1?c?1?17?1cm?6.67?10cm ?10150?103.0?101014(hz)?4.47?10(hz) (2)????7?670.7?10(3)??1??1(cm)?3.03?10?4(cm)?3030(nm) 33006.625?10?34?3.0?108(ev)?2.1(ev) (4)e?h??9?19?588.995?10?1.602?10c2-6 下列种类型跃迁所涉及的能量(ev)范围各是多少?(1)原子内层电子跃迁;(4)分子振动能级跃迁;(2)原子外层电子跃迁;(5)分子转动能级跃迁;(3)分子的电子跃迁参考答案跃迁类型原子内层电子跃迁原子外层电子跃迁分子的电子跃迁分子振动能级跃迁分子转动能级跃迁-6~1.7 6~1.7 1.7~0.02 --第10章吸光光度法(上册)2、某试液用2cm吸收池测量时,t=60%。
《仪器分析》-武汉大学版 课后习题发答案
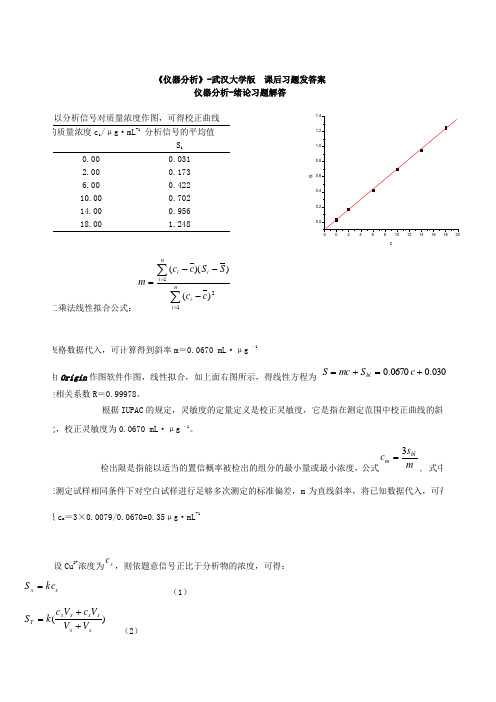
X ) ) x S =T S == =3 4 6 89.8[(M += 得.0=s /02.0光谱分析导论习题解答1、解:(1)72101067.6101050.111⨯=⨯⨯==-λσ(2)14981047.4107.670/100.3/⨯=⨯⨯==-λνc(3)303010103300/1192=⨯⨯==-σλ(4)80.1)10602.1(1095.6889100.310626.6/1910834=⨯÷⨯⨯⨯⨯===---λνhc h E2、解:由计算公式λν/hc h E ==以及各能级跃迁所处的波长范围可得能量范围分别如下:跃迁类型 波长范围 能量范围/eV 原子内层电子跃迁 10-3nm 10nm 1.261061.2102原子外层电子跃迁 200nm 750nm 6 1.7 分子的电子跃迁 200nm 750nm 6 1.7 分子振动能级的跃迁 2.5m 50m 0.50.02分子转动能级的跃迁50m100cm 210-2410-7由上表可以看出分子电子能级跃迁120eV 分子振动能级跃迁0.051eV 分子转动能级跃迁0.05eV ,其电子光谱,振动光谱以及转动光谱所对应的波长范围分别在紫外-可见区,红外区和远红外微波区。
3、解:棱镜的分光原理是光折射。
由于不同波长的光有其不同的折射率,据此能把不同波长的光分开。
光栅的分光原理是光的衍射与干涉的总效果。
不同波长的光通过光栅作用各有相应的衍射角,据此把不同波长的光分开。
光栅光谱棱镜光谱与波长成正比,所以光栅光谱是一个均匀排列的光谱 色散率与波长有关,为非均匀排列的光谱的波长越短则衍射角越小,因此其谱线从紫到红排列 长越短,其偏向角越大,因此其谱线从红到紫排列 合光通过光栅后,中央条纹(或零级条纹)为白色条纹,在中央条纹两边,对称排列着一级、二级等光谱,由于谱线间距离随光谱级数的增加而增加,出现谱级重叠现象没有谱级重叠现象光栅适用的波长范围比棱镜宽4、解:vcn r i ==θθsin sin ,式中n 为折射率,i θ为入射角,r θ为折射角,c 为光速,v 为玻璃介质中的传播速度。
仪器分析课后习题答案解析(武大版)

仪器分析课后习题(参考)(部分)第一章绪论1.仪器分析有哪些分析方法请加以简述。
答:a.光学分析法 b.电化学分析法 c.分离分析法 d.其它分析方法。
光学分析法:分为非光谱法和光谱法。
非光谱法是不涉及物质内部能级跃迁,通过测量光与物质相互作用时其散射、折射等性质变化,从而建立起分析方法的一类光学测定法。
光谱法是物质与光相互作用时,物质内部发生的量子化的能级间的跃迁,从而测定光谱的波长和强度而进行的分析方法。
电化学分析方法:利用待测组分的电化学性质进行测定的一类分析方法。
分离分析方法:利用样品中共存组分间溶解能力、亲和能力、吸附和解析能力、迁移速率等方面的差异,先分离,后按顺序进行测定的一类分析方法。
其它仪器分析方法和技术:利用生物学、动力学、热学、声学、力学等性质测定的一类分析方法。
3.仪器分析的联用技术有何显着优点答:多种现代分析技术的联用,优化组合,使各自的优点得到发挥,缺点得到克服,尤其是仪器与现代计算机技术智能融合,实现人机对话,不断开拓了一个又一个的研究领域。
第二章分子分析方法2.为什么分子光谱总是带状光谱答:因为当分子发生电子能级跃迁时,必须伴随着振动能级和转动能级的跃迁,而这些振动的能级和转动的能级跃迁时叠加在电子跃迁之上的,所以是带状光谱。
4.有机化合物分子电子跃迁有哪几种类型那些类型的跃迁可以在紫外可见光区吸收光谱中反映出来答:б→б*、П→б*、n→б*、n→б*、n→П*、П→П*。
其中n→б*、n→П*、П→П*类型的跃迁可以在紫外可见光区吸收光谱中反映出。
5.何谓生色团、助色团、长移、短移、峰、吸收曲线、浓色效应,淡色效应、向红基团、向蓝基团答:深色团:分子中能吸收特定波长的光的原子团或化学键。
助色团:与生色团和饱和烃相连且使吸收峰向长波方向移动,并使吸收强度增强的原子或原子团,如:-OH、-NH2。
长移:某些有机物因反应引入含有未珙县电子对的基团,使吸收峰向长波长的移动的现象。
武汉大学仪器分析实验总结

仪器分析实验总结一、离子选择性电极测定天然水中的F-1、实验原理:氟离子选择电极是以氟化镧单晶片为敏感膜的电位法指示电极。
氟电极和饱和甘汞电极组成的电池:Ag,AgCl|[10-3mol/L NaF,10-1mol/L NaCl]|LaF3|F-(试液)||Kcl(饱和),Hg2Cl2|HgΦISE=E内参-E M=k±0.059/n lg a外,E M=±0.059/n lg a外,E(电池)=ΦSCE-ΦISE=K-+0.059/n lg a外离子选择性电极测定的是离子的活度,故需控制离子强度(加电解质)。
实验条件控制:(1)PH5.5~6.5,用PH缓冲溶液。
(2)控制溶液离子强度,用电解质。
(3)消除Al3+,Fe3+干扰,用掩蔽剂。
常用PH=6的柠檬酸钠还溶液控制溶液PH 和作掩蔽剂。
PH过低F-易变成HF or HF2-,过高La3+会水解为La(OH)3.所用的单晶为:LaF3·EuF2,单晶中含有F-的空位,膜具有选择性和强制性。
2、关键操作:实验操作:(1)连接氟电极、甘汞电极、mV计并预热。
(2)蒸馏水浸泡氟电极和饱和甘汞电极至读数<-300mV.(3)用逐级稀释法配制浓度为10-2、10-3、10-4、10-5、10-6mol/L的F-标准溶液,测电位(要求每相邻两组电位差小于70mV),无需清洗电极,擦干即可,读数稳定5s即可记数,绘制标准曲线。
(3)一次标准溶液加入法测定水样中F-含量。
3、结果分析:计算水样中F-含量公式:cx=(c s V s/(V x+V s))(10ΔE/S-1)-14、思考题:(1)F-选择电极在使用时应注意哪些问题:一般在低浓度F-溶液中浸泡一定时间进行活化,使用时先放入蒸馏水中至电位小于-300mV方可使用测量,且保证测量溶液的PH在5.5~6.5之间,且擦干时用滤纸吸干几个,不能摩擦膜表面。
(2)为什么要清洗F-电极,使其电极响应值负于-370mV?因为电极由记忆效应,将F-电极清洗至其相应值负于-370mV可排除其离子选择性膜上其他离子的干扰,并平衡F-电极电位。
仪器分析答案武汉大学

仪器分析答案武汉大学【篇一:分析化学》下册武汉大学等编(第五版)作业参考答案】t>第2章光谱分析法导论2-1 光谱仪一般由几部分组成?它们的作用分别是什么?参考答案:(1)稳定的光源系统—提供足够的能量使试样蒸发、原子化、激发,产生光谱;(2)试样引入系统(3)波长选择系统(单色器、滤光片)—将复合光分解成单色光或有一定宽度的谱带;(4)检测系统—是将光辐射信号转换为可量化输出的信号;(5)信号处理或读出系统—在显示器上显示转化信号。
2-2 单色器由几部分组成,它们的作用分别是什么?参考答案:(1)入射狭缝—限制杂散光进入;(2)准直装置—使光束成平行光线传播,常采用透镜或反射镜;(3)色散装置—将复合光分解为单色光;(4)聚焦透镜或凹面反射镜—使单色光在单色器的出口曲面上成像;(5)出射狭缝—将额定波长范围的光射出单色器。
2-5 对下列单位进行换算:-(1)150pm z射线的波数(cm1)(2)li的670.7nm谱线的频率(hz)-(3)3300 cm1波数对应的波长(nm)(4)na的588.995nm谱线相应的能量(ev)参考答案:(1)??1?c?1?17?1cm?6.67?10cm ?10150?103.0?101014(hz)?4.47?10(hz) (2)????7?670.7?10(3)??1??1(cm)?3.03?10?4(cm)?3030(nm) 33006.625?10?34?3.0?108(ev)?2.1(ev) (4)e?h??9?19?588.995?10?1.602?10c2-6 下列种类型跃迁所涉及的能量(ev)范围各是多少?(1)原子内层电子跃迁;(4)分子振动能级跃迁;(2)原子外层电子跃迁;(5)分子转动能级跃迁;(3)分子的电子跃迁参考答案跃迁类型原子内层电子跃迁原子外层电子跃迁分子的电子跃迁分子振动能级跃迁分子转动能级跃迁-6~1.7 6~1.7 1.7~0.02 --第10章吸光光度法(上册)2、某试液用2cm吸收池测量时,t=60%。
武汉大学第五版仪器分析.光谱法仪器与光学仪器课件

一定波段的光进入检测系统进行检测
狭缝的选择:
一般来说,狭缝越小,光谱的分辨率越高,越接近真 实光谱.但狭缝太小光信号太弱,检测器难以有效测到光信 号.
所以,如果需要得到高分辨率光谱,可以采用较小宽度 的狭缝.
如果进行定量测定,则适当采用较大宽度的狭缝.
优秀课件,精彩
现代分析仪器多配有计算机完成数据采集、信号处理、 数据分析、结果打印,工作站软件系统;
优秀课件,精彩
15:16:31
无限!
36
2
棱镜的顶角α 越大或折射率n越大,角色散率越大,分开
两条相邻谱线的能力越强,但顶角越大,反射损失也增大,
通常为60度角;
优秀课件,精彩
15:16:31
无限!
19
(2)分辨率
相邻两条靠得很近的谱线分开的能力:
R b dn d
;两条相邻谱线的平均波长;△λ:两条谱线的波长差;
特点:带宽较宽,透射效率低。用于较简单的定量测定, 便宜,较好的热稳定性。
2、干涉滤光片---由两层半透明银膜和银膜间的介电薄膜 (氟化钙或氟化镁)组成。 可获得较窄的辐射宽带。 波长选择性比吸收滤光片好。
优秀课件,精彩
15:16:31
无限!
17
(三)棱镜—根据光的折射现象进行分光
棱镜对不同波长的光具有不同的折射率,波长长的光, 折射率小;波长短的光,折射率大。
15:16:31
无限!
30
(4)光栅与棱镜的比较
作为色散元件,光栅比棱镜要好: 光栅的色散几乎与波长无关 在相同色散率时,光栅的尺寸要小 光栅对棱镜不适用的远紫外远红外区可以用 光栅的杂散辐射,高级光谱干扰等问题已经可以解决 比较高的光栅价格已经降下来
仪器分析武汉大学绪论

2020/6/16
生物芯片
化学计量学
微型化 新技术 自动化 新原理 新仪器
生物分析 环境分析
在线分析
过程分析
原位分析 实时分析
分析化学 主要发展趋向
表面分析 大分子表征
活体分析
化学图象
2020/6/16
高聚焦短弧氙灯
库仑阵列电极(CoulArray)
它是穿透式多孔石 墨碳电极有多个串联在 一起,作液相色谱电化 学检测器的工作电极使 用,定量基础是库仑定 律。
2020/6/16
多毛细管电泳装置示意图
2020/6/16
仪器分析的分类
电化学分析法
质谱分析法
仪器分析
色谱分析法 分析仪器联用技术
2020/6/16
2020/6/16
2020/6/16
仪器分析
-多媒体课件
王 长 发 编 写、制 作
2020/6/16
第一章 绪 论
Introduction
• 分析化学的发展和仪器分析的产生 • 仪器分析的历史发展概况 • 近期重大突破与发明 • 仪器分析的分类 • 仪器分析的应用领域 • 发展趋势展望 • 学习方法给语
2020/6/16
Analytical chemistry is a scientific
接口 分离技术 仪器和计算机
教育
传感器
定性
固定化
无损分析 单细胞分析
联用技术 其它科技领域
单分子单聚集体分析
我们要努力啊!
我国分析仪器经过半个世纪的努力,取得了 不少成绩,两弹一星的成功,就是我国科学家在 仪器研制方面具有很高水平的最好说明。中国科 学家聪明、勤奋、爱祖国、爱科学,数十年如一 日默默奉献者大有人在。但是,另一方面我们又 不能不遗憾地看到,直到最近,国产仪器所占市 场的份额仍只有1/5左右,出口创汇甚微,具有 完全自主知识产权的分析仪器很少。高档仪器则 几乎完全被外国垄断。迄今我国分析仪器与国外 的差距还很大,而且还有扩大的趋势,一是领导 者(特别是高级领导者)的观念要转变,一定要 树立科学仪器(包括分析仪器)的创新是知识创 新的前提和基础的牢固思想,把发展国产仪器作 为国家战略。
武汉大学仪器分析实验讲义

仪器分析实验讲义武汉大学药学院目录仪器分析实验注意事项 (1)实验一色氨酸紫外吸收光谱定性扫描及定量分析 (2)实验二不同物态样品红外透射光谱的测定 (3)实验三二氯荧光素量子产率的测定 (5)实验四核磁共振波谱法测定乙基苯的结构 (7)实验五循环伏安法测定铁氰化钾的电极反应过程 (9)实验六气相色谱定量分析 (12)实验七高效液相色谱法分离巴比妥与苯巴比妥 (15)实验八毛细管区带电泳(CZE)分离硝基苯酚异构体 (165)实验九液相色谱-质谱联用技术测定饮用水中一氯酚异构体 (19)实验十饮料中咖啡因含量的测定(设计实验) (20)仪器分析实验注意事项1.实验前必须详细预习实验讲义,明了实验目的、原理方法及操作步骤。
2.要听从老师的指导,严格按照实验步骤进行,切勿随意乱动。
3.实验中所遇难题,应先独立思考,再与指导老师共同讨论研究。
4.必须如实记录观察到的现象和实验数据。
5.保持实验环境和仪器的清洁整齐。
6.必须遵守实验室的规则:(1)确保人身安全,使用强酸、强碱、有毒试剂时尤其要细心。
(2)室内不得高声谈笑,必须保持安静的实验环境。
(3)按时到实验室,不迟到,不早退。
(4)爱护仪器,不浪费药品,节约水电,遵守实验室的安全措施。
(5)滤纸、火柴棒、碎玻璃等应投入废物缸,切勿丢入水池内。
(6)各组及同学之间应相互协作,合理安排实验时间及实验内容。
(7)每次实验后由班长安排同学轮流值日,值日要负责当天实验室的卫生,安全和一些服务性工作。
最后离开实验室时,应检查水、电、门窗等是否关闭。
(8)对实验的内容和安排不合理的地方可提出改进意见。
对实验中出现的一切反常现象应进行讨论,并大胆提出自己的看法,做到生动活泼,主动地学习。
(9)实验室禁止吸烟。
实验一色氨酸紫外吸收光谱定性扫描及定量分析一、实验目的1.了解紫外-可见光谱定性分析原理。
2.掌握紫外-可见光谱定性图谱数据的处理方法。
3.熟悉紫外-可见光谱分析仪的定性、定量扫描实验操作方法。
武汉大学仪器分析讲义教案01

仪器信号放大倍数有关;而检出限与空白信号 波动或仪器噪声有关,具有明确统计含义。
1.3.3.4 动态范围(dynamic range)
定量测定最低浓度(LOQ)扩展到校准曲线偏离
线性响应(LOL)的浓度范围。 定量测定下限一般取等于10倍空白重复测定标 淮差,或10sbl。这点相对标淮差约30%,随浓 度增加而迅速降低。检测上限,相对标准差是 100%。
1.3.2.2 能源
功能:提供与被分析物或系统发生作用的探
测能源。 类型包括:电磁辐射、场、电能、机械能、 核能等。
例:光分析仪器的光源,X射线衍射仪的X光
管等。
1.3.2.3 信息发生器
检测器 转换器
信息发生器
传感器
1.3.2.3 信息发生器
检测器:通常是一个机械、电或化学装置,
分析仪器是人们感觉器官的延伸
它所测量或所获取的主要是物质的质和 量的信息。以一切可能的(化学的、物理的、 生物医学的、数学的等等)方法和技术,利 用一切可以利用的物质属性,对一切需要加 以表征、鉴别或测定的物质组分(包括无机 和有机组分)及其形态、状态(以及能态)、 结构、分布(时、空)等进行表征、鉴别和 测定,以求对样品所代表的问题有一个基本 的了解。这是当今分析科学也是分析仪器发 展所面临的任务。
仪器分析的发展趋势
科学仪器的创新是知识创新和技术创新的 重要内容。发展科学仪器应当视为国家战略。分 析仪器是科学仪器的重要组成部分。分析仪器工 业是高技术信息产业。分析仪器的发展是现代科 学、经济和社会发展的重要基础和推动力之一。 分析仪器的主要应用领域正向生物医学领域转 移.分析仪器本身将不断微型化、智能化.但人 类向时间和空间的两个极限挑战所需的高级精密 仪器也不容忽视.生命过程、生产、科研和社会 活动大量需要的将是在线、非侵入、非损坏、原 位、实时、多维分析仪器。
武汉大学仪器分析讲义教案07省名师优质课赛课获奖课件市赛课一等奖课件

可进行多元素同步分析、定性分析、定量分析、化 学状态分析、构造鉴定、无损深度剖析、微区别析等;
可进行不同形状(如平面、粉末、纤维及纳米构造) 材料,涉及有机材料旳分析(对X射线敏感材料除外), 辨别率为0.2eV。
7.2.6.2. X射线光电子能谱法旳应用
7.6. 激光共焦扫描显微镜
双光子激发是指一种分子或原子能够在同一种量 子过程中同步吸收两个光子而形成激发态,这种情况 就是双光子激发过程。
双光子共焦显微镜具有许多突出旳优点:
第一,能够采用波长比较长旳、在生物组织中穿 透能力比较强旳红外激光作为激发光源;
第二,因为双光子荧光波长远离激发光波长,所 以双光子共焦显微镜能够实现暗场成像;
4. 试样室系统和真空系统
试样预处理(如氢离子清洗等),进样系统和试样室 三部分构成了试样室系统;真空系统提供高真空环境。
7.2.6.电子能谱法旳应用
7.2.6.1.电子能谱法旳特点
1.可分析除H和He之外旳全部元素;能够直接测定来 自试样单个能级光电发射电子旳能量分布,且直接得 到电子能级构造旳信息。
1.元素定性分析
元素周期表中每一种元 素旳原子构造互不相同, 原 子内层能级上旳电子结合能 是元素特征旳反应,据此能 够进行定性分析。
2.元素定量分析
根据是光电子谱线旳强
度(光电子峰旳面积或峰高)
与元素含量有关。
(C3H7)4N+S2PF2-旳X射线光电子能谱图
7.2.6.2. X射线光电子能谱法旳应用
二次离子质谱有“静态”和“动态”两种。
7.3.2. 二次离子质谱仪
7.4. 扫描隧道显微镜和原子力显微镜
7.4.1.扫描隧道显微镜旳基本原理 基于量子力学旳隧道效应。
武汉大学(第五版)仪器分析13导论1幻灯片PPT

〔2〕 第二类电极
金属-金属难溶盐电极:
例:Ag︱AgCl︱Cl- (a)
AgCl + e Ag + Cl-
电极电位为: EE A OgC l0 /.A 0g5 lg a9 C- l 应用:测定阴离子、常用作参比电极
〔3〕 第三类电极 金属与两种具有共同阴离子的难溶盐(或
难离解的络离子)组成 例:Ag︱AgC2O4,CaC2O4 Ca2+ 应用:测Ca2+ 例:Hg︱Hg-EDTA电极
13.9.3电分析化学方法的特点
1.快速 极谱法— 一次同时测定几种元素
2.准确度高 精细的库仑滴定分析法—— 理论相对误差仅为0.0001%
3.灵敏度高 脉冲伏安法——测水中痕量砷,最低含 量达10-9 %
极谱催化波——检测矿石、金属中的 稀有元素10-9~10-11,最低10-12mol/L
极谱催化波、脉冲极谱、溶出伏安 法——微量、超微量组分的测定
6.易于自动控制,仪器简单 7.用于化学平衡常数的测定,化学反
应机理和历程的研究。
13.9.4 应用(补充) 有机化学、药物化学、生物化学、
临床化学
本章小节 1.原电池、电解池〔正负极、阴阳极〕
2.电极类型〔按用途分〕 3.液相传质过程
充电时,随着NiOOH浓度的增大,Ni(OH)2浓度的减小, 正极的电势逐渐上升;而随着Cd的增多,Cd(OH)2的减 小,负极的电势逐渐降低;当电池充满电时,正极、负 极电位均到达一个平衡值,二者电势之差即为电池之充 电电压。
放电时,反响逆向进展
NiOOH + H2O + e→ Ni(OH)2 + OHCd + 2OH- - 2e→ Cd(OH)2
武汉大学第五版仪器分析-----红外

差频峰:当吸收峰与发射峰相重叠时产生的峰 1-2。 泛频峰可以观察到,但很弱,可提供分子的“指纹”。
3. 谱带强度
分子对称度高,振动偶极矩小,产生的谱带就弱;反之则强。
如C=C, C-C因对称度高,其振动峰强度小;而C=X, C-X,因对 称性低,其振动峰强度就大。峰强度可用很强(vs)、强(s)、
C CH3
C CH 3 CH 3
O
C=O=1663cm-1
C=O=1686cm-1
空间效应的另一种情况是张力效应:四元环>五元环>六元 环。随环张力增加,红外峰向高波数移动。
6)物质状态及制样方法 通常,物质由固态向气态变化,其波数将增加。如丙酮在液 态时, C=O=1718cm-1; 气态时 C=O=1742cm-1 ,因此在查阅标准 红外图谱时,应注意试样状态和制样方法。
制作材料
工作温度
2. 吸收池 红外吸收池使用可透过红外的材料制成窗片;不同的样品状 态(固、液、气态)使用不同的样品池,固态样品可与晶体混 合压片制成。
材 料 NaCl KBr CaF2 CsBr TlBr + TlI
透光范围/m 0.2-25 0.25-40 0.13-12 0.2-55 0.55-40
光谱仪)(Fourier Transfer, FT)
一、色散型与双光束UV-Vis仪器类似,但部件材料和顺序不同。
红外光谱仪的测量光路
1. 光源 常用的红外光源有Nernst灯和硅碳棒。
类型 Nernst 灯
硅碳棒
特 点 高波数区(> 1000cm-1)有 Zr, Th, Y 1700oC 更强的发射;稳定性好; 氧化物 机械强度差; 但价格较高。 低波数区光强较大;波数 o 1200-1500 C 范围更广; SiC 坚固、发光面积大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
用不同浓度的Cd标准溶液测定9次后,算出每个浓度的RSD,记录结果。
检出限
检出限常常用能够区分背景的RSD的最小浓度来表示。IUPAC对检出限的一个定义是3×sb,sb为背景信号的标准偏差:D.L = 3×sb / SS为标准曲线的斜率.
检出限之所以成为评价仪器性能的因素,是因为它取决于灵敏度与背景信号的比值。在本实验中,用9次测量标准空白溶液计算sb,而用标准曲线的斜率计算检出限。
2.赵文宽,张悟铭,王长发,周性尧,仪器分析实验,高等教育出版社,1997.
3. /electrochem/lab5.htm
实验2石墨炉原子吸收光谱法直接测定试样中的痕量铅
一、实验目的
1.加深理解石墨炉原子吸收光谱法的原理
2.了解石墨炉原子吸收光谱法的操作技术
(3)吸入空白溶液,来冲洗进样系统。
(4)吸入样品溶液,分别得到Cu(Ⅱ)、Zn(Ⅱ)、Fe(Ⅱ)的发射信号强度。
(5)吸入自来水样品溶液,分别得到Cu(Ⅱ)、Zn(Ⅱ)、Fe(Ⅱ)的发射信号强度。
(6)吸入空白溶液,来冲洗进样系统后,结束实验。
如果标准溶液和样品溶液分析间隔较长时间,测定一中间的标准溶液,以检查仪器信号漂移。
(4)干燥温度和时间80℃(或120℃),30 s
(5)灰化温度和时间200℃,30 s
(6)原子化温度和时间1800℃,5s
(7)清洗温度和时间2100%℃,5 s
(8)氮气或氩气流量100 mL/min
2.分别取铅标准溶液B,用二次蒸馏水稀释至刻度,摇匀,配制1.00 , 10.00, 25.00,和50.00 ng/mL铅标准溶液,备用。
三、仪器和试剂
1.仪器
2.标准溶液
使用已有的10.0ppm的Cd2+溶液来配制浓度分别为2.00,1.00,0.500,0.250和0.100ppm的Cd2+标准溶液。标准溶液配制应该使用蒸馏水小心的稀释已有溶液。取一定量储备液到100mL容量瓶,稀释至100mL,充分混合均匀。
3.试样
四、实验步骤
空白溶液配制1%(v/v)硝酸溶液
3.试样制备自来水,东湖水经过滤处理后即可。
4. ICP-AES仪器操作
a.开机程序
(1)检查外电源及氩气供应;
(2)检查排废,排气是否畅通,室温控制在15-30度之间;
(3)装好进样管,废液管;
(4)打开供气开关;
(5)开启空压机,冷却器和主机电源;
(6)打开计算机后,点燃等离子体;
(3)扣除Fe, Zn和Cu的空白值,计算原试样中Fe, Zn和Cu的含量
(4)估计最终结果的不确定度
2.线性
确定工作曲线的线性范围
(1)浓度的标准溶液制作工作曲线,并进行线性拟合
(2)号较线性拟合曲线计算值下降10%的浓度为线性范围上限,线性范围下限可以视为相当于5倍检出限的浓度
3.精密度
重复10次测定一低浓度Fe, Zn和Cu标液,计算RSD
三、仪器与试剂
偏振塞曼石墨炉原子吸收分光光读计、石墨管、25mL容量瓶
铅标准溶液A(1.00mg/mL,以逐步稀释法取A液配制100mL备用)、铅标准溶液B(0.25μg/mL)、水样
四、实验步骤
1.按下列参数,设置测量条件
(1)分析线波长283.3 nm
(2)灯电流5 mA
(3)狭缝宽度0.7 nm
2.赵文宽,张悟铭,王长发,周性尧,仪器分析实验,高等教育出版社,1997。
实验3 ICP-AES测定水样中的微量Cu,Fe和Zn
一、实验目的
1.掌握ICP-AES的测定方法原理和操作技术
2.评价ICP-AES测定水样中Cu, Fe和Zn的分析性能
二、方法原理
ICP光源具有环形通道、高温、惰性气氛等特点。因此,ICP-AES具有检出限低、精密度高、线性范围宽、基体效应小等优点,可用于高、中、低含量的70个元素的同时测定。
其分析信号源于原子/离子发射谱线,液体试样由雾化器引入Ar等离子体(100%0 K高温),经干燥、电离、激发产生具有特定波长的发射谱线,波长范围在120 nm~900 nm之间,即位于近紫外、紫外、可见光区域。
发射光信号经过单色器分光、光电倍增管或其它固体检测器将信号转变为电流进行测定。此电流与分析物的浓度之间具有一定的线性关系,使用标准溶液制作工作曲线可以对某未知试样进行定量分析。
(7)检出限
重复10次测定空白溶液,计算相对于Cu, Fe和Zn的检出限
(8)精密度
选择较低浓度的Cu, Fe和Zn溶液,重复测定10次,计算ICP-AES方法测定Cu, Fe和Zn的精密度。
c.关机程序
(1)吸入蒸馏水清洗雾化器10min;
(2)关闭等离子体;
(3)退出方法编辑页面;
(4)关主机电源,冷却器,空压机,排除空压机中的凝结水;
3.熟悉石墨炉原子吸收光谱法的应用
二、方法原理
石墨炉原子吸收光谱法,采用石墨炉使石墨管升至2000℃以上的高温,让管内试样中的待测元素分解形成气态基态原子,由于气态基态原子吸收其共振线,且吸收强度与含量成正比,故可进行定量分析。它是一种非火焰原子吸收光谱法。
石墨炉原子吸收法具有试样用量小的特点,方法的绝对灵敏度较火焰法高几个数量级,可达10-14g,并可直接测定固体试样。但仪器较复杂、背景吸收干扰较大。在石墨炉中的工作步骤可分为干燥、灰化、原子化和除残渣4个阶段。
(5)按要求关闭计算机;
(6)松开进样管,废液管。
五、结果与讨论
1.工作曲线和样品分析
应用ICP软件,制作Fe, Zn和Cu工作曲线。在ICP-AES分析中,常存在与基体相关的背景信号,这可用空白溶液校正并将其设为零点。
(1)打印出软件制作的工作曲线
(2)评价工作曲线的线性
应用软件计算试样溶液和空白中Fe, Zn和Cu的浓度
待测试样溶解后以气溶胶的形式引入火焰中。产生的基态原子吸收适当光源发出的辐射后被测定。原子吸收光谱中一般采用的空心阴极灯这种锐线光源。这种方法快速、选择性好、灵敏度高且有着较好的精密度。
然而,在原子光谱中,不同类型的干扰将严重影响方法的准确性。干扰一般分为三种:物理干扰、化学干扰和光谱干扰。物理和化学干扰改变火焰中原子的数量,而光谱干扰则影响原子吸收信号的准确测定。干扰可以通过选择适当的实验条件和对试样的预处理来减少或消除。所以,应从火焰温度和组成两方面作慎重选择。
在波长228.8nm处测定标准溶液的吸收。狭缝宽度和空心阴极灯的位置预先调整好。当吸入0.500ppm标准溶液时,调整波长为228.8nm,调整到最大吸收。
1.火焰的选择:
火焰组成对Cd的测定灵敏度影响:通过溶液雾化方式引入0.500μg/ml的Cd标准溶液到空气-乙炔火焰中,小幅调节乙炔的流速,每次读数前用二次蒸馏水重新调零,以吸光度对流速作图。
l标准曲线系列:标准空白和标准溶液
l样品空白和样品溶液
l重复样品空白和样品溶液
精密度
用低浓度和高浓度的溶液来测定方法的精密度。每次读数3次。
检出限
为了得到仪器检测Cd的检出限,需对标准空白溶液读数3次。把不用的镉盐及其溶液放置到标有废弃瓶的瓶中。
五、结果和讨论
标准曲线
打印出本实验所做的标准曲线,注意任何弯曲并决定是否需要采用非线性曲线拟合。用这些曲线来测定试样空白和试样中Cd的含量,用扣除空白的方法得到试样中Cd的真实含量。计算原始试样含量中Cd的含量并估算最终结果中的不确定度。
实验1火焰原子吸收光谱法测定水中的镉
一、实验目的
1.掌握火焰原子吸收光谱仪的操作技术;
2. 2.优化火焰原子吸收光谱法测定水中镉的分析火焰条件;
熟3.熟悉原子吸收光谱法的应用。
二、方法原理
原子吸收光谱法是一种广泛应用的测定元素的方法。它是一种基于待测元素基态原子在蒸气状态对其原子共振辐射吸收进行定量分析的方法。为了能够测定吸收值,试样需要转变成一种在适合的介质中存在的自由原子。化学火焰是产生基态气态原子的方便方法。
六、问题
1.当使用雾化器时,经常使用稀释硝酸作为溶剂。为什么硝酸是个较好的选择?(提示:-硝酸盐的性质是什么?)
2.火焰原子吸收光谱法具有哪些特点?
3.狭缝的自然宽度是多大?
七、参考文献
1. Skoog, Holler and Nieman, Principles of Instrumental analysis
通常使用偏振塞曼石墨炉原子吸收分光光度计,它具有利用塞曼效应扣除背景的功能。采用的吸收线调制法是将磁场加在原子化器两侧,使吸收线分裂成л和σ+、σ-线,其中л线的方向与磁场平行,其波长与光源发出的分析线波长一致;而测定时,首先旋转检偏器,使光源发射的谱线中与磁场平行的光通过原子化器,测得原子吸收和背景吸收的总吸光度A。再将检偏器置于使光源发射的分析线中与磁场垂直的部分光通过原子化器时,测得的吸收值为背景吸收值,即A(背景),即可将背景扣除。此类仪器可扣除吸光度<1.5背景值。使测定灵敏度大大提高。
(7)进入到方法编辑页面;
(8)在方法编辑页面里,分别输入被测元素的各种参数。
(9)按下述操作进行分析测试。
b.工作曲线和试样分析
(1)吸入空白溶液,得到空白溶液中Cu(Ⅱ)、Zn(Ⅱ)、Fe(Ⅱ)的发射信号。
(2)由低浓度至高浓度分别吸入混合标准溶液,得到不同浓度所对应的Cu(Ⅱ)、Zn(Ⅱ)、Fe(Ⅱ)的发射信号强度。
4.检出限
检出限通常与可区别背景信号(噪声)的最小信号相关,IUPAC的一种定义为对应于3×Sb的浓度,Sb为背景信号的标准偏差。
2.观察高度的影响:
在选定的合适的流速下,雾化的0.500μg/ml的Cd标准溶液中,小幅调节火焰高度,每次读数前用二次蒸馏水重新调零,以燃烧器上方观察高度对流速作图。
换到标准曲线窗口,在开始一系列测定之前,用二次蒸馏水调零,同时如果再测量过程中有延误,再重新调零。在连续的一系列的测定中,记录每个溶液的吸收值,每次每个样品重复三次后转入下一个测定:
