第3讲 物质的量和气体摩尔体积
高考化学大一轮复习第一章认识化学科学第3讲物质的量气体摩尔体积教案鲁科版必修1

第3讲 物质的量 气体摩尔体积考点一 物质的量[学在课内]1.物质的量定义:表示含有一定数目粒子的集合体的物理量。
单位mol(符号) 规范表示方法:[名师点拨]由于阿伏加德罗常数太大,后面只能跟微观粒子,如跟宏观物质如1 mol 大米、1 mol 氢元素则错误。
2.三个基准量[名师点拨] 三个等量关系1.N A 与6.02×1023的关系,N A ≈6.02×1023mol -1M 与相对分子(原子)质量的关系在数值上M =相对分子(原子)质量(M 以g·mol -1为单位) V m 与22.4 L·mol -1的关系V m =22.4 L·mol -1(标准状况下)2.下列物理量的单位物质的量mol 阿伏加德罗常数mol-1质量g 摩尔质量g·mol-1体积L 气体摩尔体积L·mol-1[考在课外]教材延伸判断正误(1)1 mol OH-的质量为17 g·mol-1(×)(2)标准状况下,22.4 L H2O2中所含原子总数为4N A(×)(3)2 mol H2O的摩尔质量是1 mol H2O的摩尔质量的2倍(×)(4)常温常压下,气体摩尔体积大于22.4 L·mol-1(√)(5)20 g CD4与20 g D2O中所含电子数相等(√)(6)相同质量的甲醛与乙酸中所含碳原子数相同(√)(7)标准状况下,等物质的量的NO2与N2O4体积相同(×)(8)等质量的Na2S、Na2O2中所含阴离子数相等(√)拓展应用标准状况下,11.2 L下列物质HF、H2O、H2O2、SO3、乙醇、苯、己烷、CCl4、CO2。
物质的量为0.5 mol的有CO2。
思维探究对N A、M、V m三个基准量的认识N A、M、V m的值不随(填“随”、“不随”)物质的量多少而变化。
[基础点巩固]1.(1)2 mol CO(NH2)2中含________ mol C,________ mol N,________ mol H,所含氧原子与________ mol H2O所含氧原子个数相等。
人教版高一化学必修一《物质的量、气体摩尔体积、浓度》讲义(含答案)

物质的量(气体摩尔体积、浓度)一 气体摩尔体积1.定义: ,叫做气体摩尔体积。
2.表示符号:3.单位:4.标准状况下,气体摩尔体积约为5.数学表达式:气体的摩尔体积=, 即 【例】判断下列说法是否正确?并说明理由1.常温常压下,11.2L 氧气所含的原子数为N A2.在25℃,压强为1.01×105 Pa 时,11.2L 氮气所含的原子数目为N A3.标准状况下的22.4L 辛烷完全燃烧,生成CO 2分子数为8N A4.标准状况下,11.2L 四氯化碳所含分子数为0.5N A5.标准状况下,1L 水所含分子数为(1/22.4)N A6.标准状况下,11.2L SO 3中含1.5N A 个氧原子二 阿伏加德罗定律及其推论1.阿伏加德罗定律:在同温同压下,同体积的气体含有相同的分子数。
即:T 1=T 2;P 1=P 2 ;V 1=V 2 n 1 = n 22.阿伏加德罗定律的推论:(1)三正比:同温同压下,气体的体积比等于它们的物质的量之比.V 1/V 2=n 1/n 2同温同体积下,气体的压强比等于它们的物质的量之比.p 1/p 2=n 1/n 2同温同压下,气体的密度比等于它们的相对分子质量之比.M 1/M 2=ρ1/ρ2(2)二反比:同温同压下,相同质量的任何气体的体积与它们的相对分子质量成反比.V 1/V 2=M 2/M 1同温同体积时,相同质量的任何气体的压强与它们的摩尔质量的反比.p 1/p 2=M 2/M 1。
(3)一连比:同温同压下,同体积的任何气体的质量比等于它们的相对分子质量之比,也等于它们的密度之比。
m 1/m 2=M 1/M 2=ρ1/ρ2(注:以上用到的符号:ρ为密度,p 为压强,n 为物质的量,M 为摩尔质量,m 为质量,V 为体积,T 为温度;上述定律及其推论仅适用于气体,不适用于固体或液体。
)【例1】(2010上海卷,7)N A 表示阿伏加德罗常数,下列叙述正确的是A .等物质的量的N 2和CO 所含分子数均为N AB .1.7g H 2O 2中含有的电子数为0.9 N AC .1mol Na 2O 2 固体中含离子总数为4 N AD .标准状况下,2.24L 戊烷所含分子数为0.1 N A易错警示:进行阿伏伽德罗常数的正误判断的主要考查点有:①判断一定量的物质所含的某种粒子数目的多少;②物质的组成;③通过阿伏加德罗常数进行一些量之间的换算等,在解题时要抓住其中的易错点,准确解答。
第3讲 物质的量 气体摩尔体积-2024年高考化学一轮复习课件

非标准状况下,1 mol气体的体积则一定不是22.4 L( × ) (6)标准状况下,22.4 L己烷中含有的共价键数目为19NA(× )
关键能力 讲练提升
1.(新教材RJ必修第一册P59T4)下列说法中,正确的是( ) A.22.4 L N2中一定含有2 mol N B.80 g NaOH溶解在1 L水中,所得溶液中溶质的物质的量浓度为2 mol/L C.在标准状况下,20 mL NH3和60 mL O2所含分子个数比为1∶3 D.18 g H2O在标准状况下的体积约为22.4 L
2.12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为_6_2_g_·_m_o_l_-_1_,R的 相对原子质量为__1_6_。含R的质量为1.6 g 的Na2R,含Na+的个数为_0._2_N_A。
3.(多选)某氯原子的质量为a g,12C的质量为b g,用NA表示
阿伏加德罗常数,下列说法中正确的是( )
①同温、同压下,相同物质的量的气体,气体体积相同。
②同温、同体积下,相同物质的量的气体,气体的压强相同。
(3)应用阿伏加德罗定律及推论时不宜死记硬背,要熟记相关化学计量
的定义式,可结合
pV=nRT=
m
M
RT
进行推导。
5.计算气体摩尔质量的常用方法
(1)公式法:M
=
m
n
。
(2)根据标准状况下气体的密度ρ计算:M =ρ×22.4 (g·mol-1)。
3.阿伏加德罗定律(“三同”定“一同”)
相同温度 相同压强 相同体积
任何气体 所含___分__子_数____ 相同
pV=nRT=
第一章 第三讲 物质的量 气体摩尔体积

mol H+.
二、摩尔质量
1.概念:单位物质的量的物质所具有的 质量 .
mol-1或 kg· mol-1 . 2.单位: g· 3.数值:当摩尔质量单位是g· mol-1时,数值上等于该 物质的 相对分(原)子质量 . 4.物质的量(n)、物质的质量(m)和物质的摩尔质量(M)之
m . 间的关系式: n= M
2.阿伏加德罗定律
在相同的温度和压强下,相同体积的任何气体都含
有 相同数目的分子 .
2.标准状况下,1 mol气体的体积是22.4 L,如果当1 mol 气体的体积是22.4 L时,一定是标准状况吗? 提示:不一定,因为影响气体体积的因素是温度、 压强两个条件,非标准状况下1 mol气体的体积也可 能是22.4 L.
尔质量的单位是g· mol-1,C项错误;水的摩尔质量为18
g· mol-1,与取用水的量无关,D项错误. 答案:A
2.下列数量的各物质所含原子个数按由大到小顺序排列
的是
①0.5 mol 氨气 ④0.2 mol磷酸钠 A.①④③② C.②③④① B.④③②① D.①④②③ ②4 g氦气 ③4℃时9 mL水
解析:标准状况下,二氯甲烷为液体,A错;1个SO2分子 中含有的氧原子数为2个,故氧原子的物质的量为1 mol时, SO2的物质的量为0.5 mol,B正确;17.6 g丙烷的物质的量
为0.4 mol,而一个丙烷分子中含有8个C—H极性共价键,
故17.6 g丙烷中含有的极性共价键为3.2 mol,C错;电解精 炼铜时,阳极粗铜中往往含有铁、锌等杂质,D错. 答案:B
解析:本题考查阿伏加德罗常数,意在考查考生对有关物 质的量的计算能力.1 个 CH4 中含有 4 个 C—H 键, 则 16 g 16 g CH4 中的 C—H 键数为: ×4×nA=4nA,A 项 16 g· mol-1 正确;由于没有提供 1 mol· L-1 NaCl 溶液的体积,则溶液 所含 Na+数目无法确定,B 项错误;根据 Cu 与稀硝酸的 反应:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O, 2 2 则反应生成的 n(NO)= n(Cu),其分子数目为 nA,C 项 3 3 错误;常温常压下气体的摩尔体积不为 22.4 L· mol 1,因
第3讲 物质的量

考纲导向 1.了解物质的量的单位——摩尔(mol)、 摩尔质 量、气体摩尔体积、物质的量浓度、阿伏加德 罗常数的含义。 2.能根据物质的量与微粒(原子、 分子、 离子等) 数目、气体体积(标准状况下) 之间的相互关系 进行有关计算。 3.了解配制一定溶质质量分数、物质的量浓度 溶液的方法。 热点导学 1.有关 NA 的计算与正 误判断。 2.气体摩尔体积和阿 伏加德罗定律的应 用。 3.一定物质的量浓度 溶液的配制方法及误 差分析。 4.以物质的量为中心 的计算。
Байду номын сангаас
V cM cM w= = = 。 m 溶液 V 1000 1000
m 溶质
4.溶液稀释和同种溶质的溶液混合的计算 在稀释或混合前后,溶液中溶质的物质的量总量不 变,即有:c1·V1=c2·V2、c1·V1+c2·V2 =c 混·V 混,可以计算有关的量。 特别提示 溶液稀释或混合时,溶液的体积一般不 可直接相加,而应根据溶液质量和密度求算,求算 过程中注意密度单位一般为 g· mL ,计算体积后切
3.溶液中溶质的质量分数与物质的量浓度间的换算
1000 c= (c 为溶液的物质的量浓度,单位 mol·L-1, M
ρ 为溶液密度,单位 g·cm-3,w 为溶质的质量分数,M 为溶 质的摩尔质量,单位 g·mol-1),此公式可按溶液体积为 V L 进行推导:
n 1000 V 1000 c= = = V M V M
基础梳理
巩固演练
要点突破 点滴积累
基础梳理
知识导图
抓主干、固双基
交流展示
知识梳理
一、物质的量
1.基本概念
2.物质的量(n)与粒子数(N)、阿伏加德罗常数(NA)之 间的关系
第3讲物质的量气体摩尔体积

第3讲 物质的量 气体摩尔体积【考纲解读】1.了解物质的量及其单位、阿伏加德罗常数、摩尔质量、气体摩尔体积的含义。
2.能根据物质的量与质量、摩尔质量、气体体积(标准状况)、物质的量浓度、物质质量分数、阿伏加德罗常数、微粒数之间的相互关系进行有关计算。
3.能正确解答阿伏加德罗常数及阿伏加德罗定律与物质的组成、结构及重要反应综合应用题。
【考点解析】考点一 物质的量 摩尔质量 1. 物质的量(1)物质的量(n )物质的量是表示含有一定数目粒子的集合体的物理量,单位符号为__________。
(2)物质的量的规范表示方法:(3)阿伏加德罗常数(N A )0.012 kg 12C 所含的碳原子数为阿伏加德罗常数,其数值约为6.02×1023,单位为__________。
公式:N A =Nn2. 摩尔质量(1)摩尔质量是单位物质的量的物质所具有的质量。
单位是__________。
公式:M =mn 。
(2)数值:以__________为单位时,任何粒子的摩尔质量在_________都等于该粒子的__________。
易错警示摩尔质量与相对原子(分子)质量的易混点(1)相对原子(分子)质量与摩尔质量不是同一个物理量,单位不同,只是在数值上相等。
(2)摩尔质量的单位为g·mol -1,相对原子(分子)质量的单位为1。
【随堂练习1】1. 标准状况下有①0.112 L 水 ②0.5N A 个HCl 分子③25.6 g SO 2气体 ④0.2 mol 氨气 ⑤2 mol 氦气 ⑥6.02×1023个白磷分子,所含原子个数从大到小的顺序为______________________。
2.计算或判断下列电解质溶液中的粒子数目(1)含0.4 mol Al2(SO4)3的溶液中,含________mol SO2-4,Al3+的物质的量________0.8mol(填“>”、“<”或“=”)。
高考化学一轮复习第一章从实验学化学第3讲物质的量气体摩尔体积课件

⑥6.02×1023个白磷分子, 。
提示:(1)6.6 (2)2NA (3)(b-a)NA (4)①>⑥>⑤>③>②>④
2021/4/17
高考化学一轮复习第一章从实验学化学
10
第3讲物质的量气体摩尔体积课件
考点演练
考向一 基本概念的理解与应用 1.下列说法正确的是( D ) A.常温常压下,氯气的摩尔质量等于71 g B.1 mol H2SO4中含有2 mol氢元素 C.某物质的摩尔质量就是该物质的相对分子质量或相对原子质量 D.2 g氦气所含的原子数目约为0.5×6.02×1023
C.一个“CH3COOK”微粒的质量约为
98 6.02 10 23
g
D.含有6.02×1023个碳原子的CH3COOK的物质的量为1 mol
解析:1 mol CH3COOK 的质量为 98 g,A 错误;摩尔质量的单位是 g·mol-1,相对分子质量的单位是
“1”,B
错误;一个“CH3COOK”微粒的质量约为
9
第3讲物质的量气体摩尔体积课件
2.(1)0.1NA个臭氧分子中的氧原子数与
g CO2分子中的氧原子数相等。
(2)8 g甲烷分子中的氢原子数是
。
(3)1个NO分子的质量是a g,1个NO2分子的质量是 b g,则氧原子的摩尔质量是 g·mol-1。
(4)标准状况下有①0.112 L水 ②0.5NA个HCl分子 ③25.6 g SO2气体 ④0.2 mol氨气 ⑤2 mol氦气 所含原子个数从大到小的顺序为
2021/4/17
高考化学一轮复习第一章从实验学化学
3
第3讲物质的量气体摩尔体积课件
考点突破 真题体验
高考化学一轮 第一章 第3讲 物质的量 气体摩尔体积

冠夺市安全阳光实验学校第1章第3讲物质的量气体摩尔体积一、选择题(本题包括12小题,每小题4分,共48分)1.(2009·泰安质检)下列叙述中,错误的是( )①1 mol任何物质都含有6.02×1023个分子②0.012 kg 12C约含有6.02×1023个碳原子③1 mol水中含有2 mol氢和1 mol氧④1 mol Ne中含有6.02×1024个电子A.①② B.②③ C.①③ D.②④解析:有的物质是由分子构成的,有的物质是由离子或原子构成的,故①项说法错误;使用“mol”这一单位时,必须注明微粒名称,③项中“2 mol 氢”、“1 mol氧”表达方式均是错误的,应为“2 mol H、1 mol O”.答案:C2.阿伏加德罗常数约为6.02×1023 mol-1,下列说法正确的是( )A.1.0 L 1 mol·L-1氨水中,NH3·H2O的分子数为6.02×1023B.当有7.1 g Cl2和水完全反应时转移的电子数为0.1×6.02×1023C.白磷分子(P4)呈正四面体结构,31 g白磷中含有P-P键个数为6×6.02×1023D.20 g重水(2162H O)中含有的中子数为8×6.02×1023解析:A中在氨水溶液中,一部分的氨以NH3的形式存在,且NH3·H2O会发生电离,因此,NH3·H2O分子数小于6.02×1023;B由Cl2+H2O===HCl+HClO知,1 mol Cl2参加反应,转移1 mol电子,7.1 g Cl2为0.1 mol,与水完全反应转移0.1 mol电子;C中1 mol白磷中含6 mol P-P键,31 g白磷中含P-P键的数目为314×31×6×6.02×1023=1.5×6.02×1023;D中,20 g重水为1 mol,其中含有的中子数为1×10×6.02×1023=10×6.02×1023.答案:B3.(2009·广东高考)设n A代表阿伏加德罗常数(N A)的数值,下列说法正确的是( )A.1 mol硫酸钾中阴离子所带电荷数为n AB.乙烯和环丙烷(C3H6)组成的28 g混合气体中含有3n A个氢原子C.状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为n AD.将0.1 mol氯化铁溶于1 L水中,所得溶液含有0.1n A个Fe3+解析:A项,1 mol硫酸钾中阴离子所带电荷数为2n A.B项,应含有4n A个氢原子.D 项,由于Fe 3+水解,所得溶液含有的Fe 3+个数小于0.1n A . 答案:C4.状况下有①0.112 L 水;②3.01×1023个氯化氢分子;③13.6 g H 2S 气体;④0.2 mol 氨气,下列对这四种物质的关系由小到大排列正确的是 ( )A .体积:①③②④B .密度:④①③②C .质量:①④③②D .氢原子数:②④③①解析:A 项中n (HCl)=0.5 mol ,n (H 2S)=0.4 mol ,故体积关系V (H 2O)<V (NH 3)<V (H 2S)<V (HCl);B 项中液态水密度最大,而不是HCl ;C项中m (H 2O)=112 g ,m (HCl)=18.25 g ,m (H 2S)=13.6 g ,m (NH 3)=3.4 g ,故由小到大顺序为:m (NH 3)<m (H 2S)<m (HCl)<m (H 2O);D 项H 原子最多的是0.112 L H 2O ,n (H)=112 g 18 g·mol -1×2=12.4 mol,0.5 mol HCl 、0.4 molH 2S 、0.2 mol NH 3中H 原子的物质的量分别为0.5 mol 、0.8 mol 、0.6 mol ,故由小到大顺序为②④③①. 答案:D5.在一定的条件下,完全分解下列某化合物2 g ,产生氧气1.6 g ,此化合物是 ( )A .1162H OB .2162H O C .1182H O D .解析:选项A 中m (16O 2)= 2 g 18 g·mol-1×16 g·mol-1=1.78 g ;选项B 中m (16O 2)= 2 g 20 g·mol -1×16 g·mol -1=1.6 g ;选项C 中m (18O 2)= 2 g 20 g·mol -1×18 g·mol -1=1.8 g ;选项D 中m (18O 2)= 2 g 22 g·mol-1×18g·mol -1=1.64 g. 答案:B6.(2009·临沂质检)设阿伏加德罗常数的值为N A ,状况下某种O 2和N 2的混合气体m g 含有b 个分子,则n g 该混合气体在相同状况下所占的体积(V )应是 ( )A .22.4nb /mN A LB .22.4mb /nN A LC .22.4nN A /mb LD .nbN A /22.4m L解析:在状况下,m g 气体所占体积为:bN A ×22.4 L,则n g 气体的体积为n g m g ×b N A ×22.4 L=22.4 nb mN AL. 答案:A7.某物质A 在一定条件下加热分解,产物都是气体:2A ――→△B↑+2C↑+2D↑.测得生成的混合气体对氢气的相对密度为d ,则A 的相对分子质量为 ( )2182H OA.7d B.5d C.2.5d D.2d解析:求A的相对分子质量肯定要与生成的混合气体进行联系.由同一状况下,气体的相对分子质量之比等于其密度之比,得混合气体的相对分子质量M(混合气体)=M(H2)×d=2d.混合气体是由B、C、D三种气体按物质的量之比为1∶2∶2组成的,则混合气体的相对分子质量M(混合气体)=M (B)+2M(C)+2M(D)5=2M(A)5=2d,M(A)=5d.答案:B8.在三个密闭容器中分别充入Ne、H2、O2三种气体,当他们的温度和密度都相同时,这三种气体的压强(p)由大到小的顺序是( )A.p(Ne)>p(H2)>p(O2)B.p(O2)>p(Ne)>p(H2)C.p(H2)>p(O2)>p(Ne)D.p(H2)>p(Ne)>p(O2)解析:温度和密度分别相同时,气体的压强与摩尔质量成反比.由于M(H2)<M(Ne)<M(O2),所以p(H2)>p(Ne)>p(O2).答案:D9.(2009·上海高考)N A代表阿伏加德罗常数.下列有关叙述正确的是( )A.状况下,2.24 L H2O含有的分子数等于0.1N AB.常温下,100 mL 1 mol·L-1 Na2CO3溶液中阴离子总数大于0.1N AC.分子数为N A的CO、C2H4混合气体体积约为22.4 L,质量为28 gD.3.4 g NH3中含N—H键数目为0.2N A解析:A项,状况下水呈液态或固态.B项,Na2CO3溶液中存在水解反应:CO2-3+H2O HCO-3+OH-,故100 mL 1 mol·-1 Na2CO3溶液中阴离子总数大于0.1N A.C项,没有注明是状况下,体积不一定是22.4 L.D项,一个NH3分子中含3个N—H键,则3.4 g即0.2 mol NH3中含N—H键数目为0.6N A.答案:B10.在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是( )A.两种气体的压强相等B.O2比O3的质量小C.两种气体的分子数目相等D.两种气体的氧原子数目相等解析:根据题意,因等温度、等体积、等密度,则两者等质量,B项错;等质量的O2和O3物质的量不相等,则压强和分子数不相等,则A、C两项错,O2和O3都是由氧原子构成的,所以等质量的O2和O3原子数相等.答案:D11.在状况下,m g气体A与n g气体B的分子数相同,下列说法中不.正确的是( )A.气体A与气体B的相对分子质量比为m∶nB.同质量气体A与B的分子个数比为n∶mC.同温同压下,A气体与B气体的密度比为n∶mD.同温同压下,同体积A气体与B气体的质量比为m∶n解析:A与B物质的量相同,相对分子质量之比为m∶n,分子个数之比等于n∶m;同温同压下,二者密度之比等于摩尔质量之比,应为m∶n;同温同压下,同体积的A、B气体,其物质的量相同,质量比等于摩尔质量之比,即m∶n.答案:C12.对相同状况下的12C18O和14N2两种气体,下列说法正确的是( )A.若质量相等,则质子数相等B .若原子数相等,则中子数相等C.若分子数相等,则体积相等D.若体积相等,则密度相等解析:题给两种气体的相对分子质量分别为30、28,中子数分别为16、14,质子数都为14.因为相对分子质量不等,气体质量相等时,其物质的量不等,质子数不等,A项错误;它们都是双原子分子,原子数相等,其分子数相等,因为每个分子的中子数不等,所以中子总数不等,B项错误;相同状态,分子数相等,物质的量相等,则气体体积相等,C项正确;同状态气体体积相等,其物质的量相等,因为它们的摩尔质量不等,其质量不等,故气体的密度不等,D项错误.答案:C二、非选择题(本题包括4小题,共52分)13.(14分)(2009·枣庄质检)化合物A是一种不稳定的物质,它的分子组成可用O x F y表示.10 mL A气体分解生成15 mL O2和10 mL F2(同温、同压).(1)A的化学式是________,推断理由是_________________________________________________________________________________________________ ____________.(2)已知A分子中x个氧原子呈…O-O-O…链状排列,则A分子的电子式是__________,A 分子的结构式是__________.解析:阿伏加德罗定律及质量守恒定律.依据阿伏加德罗定律,可知反应方程式:2O x F y ===3O 2+2F 2,再由质量守恒定律知x =3,y =2.故A 的化学式为O 3F 2.答案:(1)O 3F 2 阿伏加德罗定律,质量守恒定律 (2)××F ××××·× ·×F ×××××× F -O -O -O -F14.(12分)在25℃、101 kPa 条件下,将15 L O 2通入10 L CO 和H 2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强.(1)若剩余气体的体积是15 L ,则原CO 和H 2的混合气中V (CO)=________ L ,V (H 2)=________ L.(2)若剩余气体的体积为a L ,则原CO 和H 2的混合气中V (CO)∶V (H 2)=________.解析:(1)2CO +O 2=====点燃2CO 2,2H 2+O 2=====点燃2H 2O(液态),分析这两个反应式可以发现:完全燃烧时,消耗O 2的体积是CO 和H 2体积的一半,所以O 2是过量的,燃烧掉的O 2是5 L ,剩余O 2的体积为10 L ,另外5 L 的剩余气体肯定是CO 2,CO 2的体积与CO 的体积相等,所以CO 和H 2的体积都是5 L.(2)从上面的分析中可以看出:剩余气体中O 2总是10 L ,若剩余气体总共是a L 时,则CO 2的体积为(a -10)L ,即V (CO)=(a -10)L ,V (H 2)=10 L -(a -10)L =(20-a )L.所以,V (CO)∶V (H 2)=a -1020-a .答案:(1)5 5 (2)a -1020-a15.(14分)一定量的液态化合物XY 2,在一定量的O 2中恰好能完全燃烧,反应方程式为:XY 2(l)+3O 2(g)===XO 2(g)+2YO 2(g).冷却后在状况下测得生成物的体积为672 mL ,其密度为2.56 g·L -1.则: (1)反应前O 2的体积V (O 2)=________; (2)XY 2的摩尔质量是________;(3)若XY 2分子中X 、Y 两元素的质量比是3∶16,则X 、Y 两元素分别是______和________(写元素符号).解析:由方程式知反应前后气体体积不变, 故V (O 2)=672 mL =0.672 L , n (O 2)=0.672 L22.4 L·mol-1=0.03 mol ,m (O 2)=0.03 mol×32 g·mol -1=0.96 g ,根据质量守恒m (XO 2)+m (YO 2)=m (XY 2)+m (O 2),m (XY 2)=2.56 g·L -1×0.672 L -0.96 g =0.76 g ,M (XY 2)=0.76 g 0.01 mol=76 g·mol -1.由X 、Y 两元素的质量比为3∶16,且XY 2的式量为76,得X 、Y 的相对原子质量分别为12、32,故X 、Y 分别为C 、S.答案:(1)672 mL (2)76 g·mol -1(3)C S16.(12分)生态农业涉及农家肥料的综合利用,某种肥料经发酵得到一种含甲烷、二氧化碳、氮气的混合气体.2.016 L(状况)该气体通过盛有红热CuO 粉末的硬质玻璃管,发生的反应为:CH 4+4CuO ――→△CO 2+2H 2O +4Cu.当甲烷完全反应后,硬质玻璃管的质量减轻4.8 g .将反应后产生的气体通过过量的澄清石灰水中,充分吸收,生成沉淀8.5 g. (1)原混合气体中甲烷的物质的量是__________.(2)原混合气体中氮气的体积分数为多少?(写出计算过程) 解析:设CH 4为x mol ,原混合气体中CO 2为y mol ,则有 CH 4+4CuO ――→△CO 2+2H 2O +4Cu Δm 1 mol 1 4×16 g x x 4.8 gx =0.075 mol又因为n 总= 2.016 L22.4 L·mol-1=0.09 mol ,n (CO 2)=8.5 g100 g·mol-1=0.085 mol ,所以y =0.085 mol -0.075 mol =0.01 moln (N 2)=0.09 mol -0.01 mol -0.075 mol =0.005 mol所以N 2的体积分数为0.005 mol0.09 mol ×100%=5.56%.答案:(1)0.075 mol (2)5.56%。
高三一轮复习第3讲物质的量
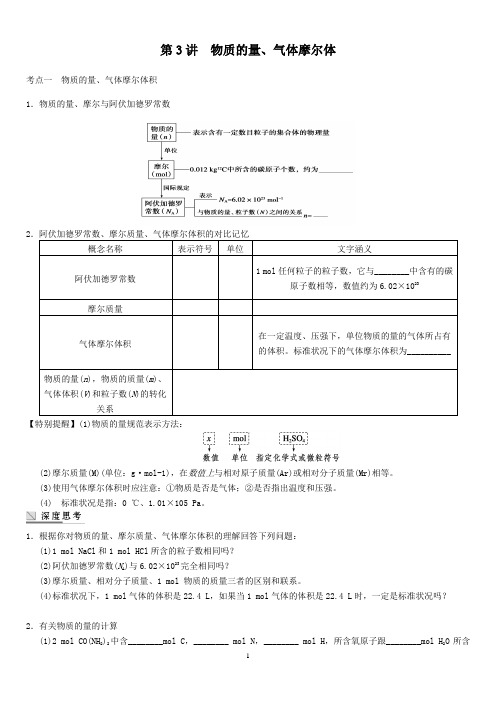
第3讲 物质的量、气体摩尔体考点一 物质的量、气体摩尔体积 1.物质的量、摩尔与阿伏加德罗常数2.阿伏加德罗常数、摩尔质量、气体摩尔体积的对比记忆概念名称 表示符号单位 文字涵义阿伏加德罗常数 1 mol 任何粒子的粒子数,它与________中含有的碳原子数相等,数值约为6.02×1023摩尔质量气体摩尔体积在一定温度、压强下,单位物质的量的气体所占有的体积。
标准状况下的气体摩尔体积为__________物质的量(n ),物质的质量(m )、气体体积(V )和粒子数(N )的转化关系【特别提醒】(1)物质的量规范表示方法:(2)摩尔质量(M)(单位:g ·mol-1),在数值上与相对原子质量(Ar)或相对分子质量(Mr)相等。
(3)使用气体摩尔体积时应注意:①物质是否是气体;②是否指出温度和压强。
(4) 标准状况是指:0 ℃、1.01×105 Pa 。
1.根据你对物质的量、摩尔质量、气体摩尔体积的理解回答下列问题: (1)1 mol NaCl 和1 mol HCl 所含的粒子数相同吗? (2)阿伏加德罗常数(N A )与6.02×1023完全相同吗?(3)摩尔质量、相对分子质量、1 mol 物质的质量三者的区别和联系。
(4)标准状况下,1 mol 气体的体积是22.4 L ,如果当1 mol 气体的体积是22.4 L 时,一定是标准状况吗?2.有关物质的量的计算(1)2 mol CO(NH 2)2中含________mol C ,________ mol N ,________ mol H ,所含氧原子跟________mol H 2O 所含氧原子个数相等。
(2)①标准状况下,22.4 L CH 4;②1.5 mol NH 3;③1.806×1024个H 2O ;④标准状况下,73 g HCl 所含H 原子个数由多到少的顺序是______________________。
06第1章 第3讲 物质的量 气体摩尔体积

思维建模
以物质的量(n)为核心的思维模板
N
÷NA NA×
n
×M M÷
m
V(g) 注 Vm与温度、压强有关,标准状况下Vm=22.4 L·mol-1。
题组二 阿伏加德罗定律及应用 5.一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,这些分子 由1.204×1024个原子组成,下列有关说法中不正确的是
√A.该温度和压强可能是标准状况
B.标准状况下该纯净物若为气态,其体积约是22.4 L C.每个该气体分子含有2个原子 D.若O2在该条件下为气态,则1 mol O2在该条件下的体积也为30 L
6.(2018·哈尔滨模拟)在甲、乙两个体积不同的密闭容器中,分别充入质量相等 的CO、CO2气体时,两容器的温度和压强均相同,则下列说法正确的是 A.充入的CO分子数比CO2分子数少 B.甲容器的体积比乙容器的体积小 C.CO的摩尔体积比CO2的摩尔体积小
0
考点二
2 识破阿伏加德罗常数判断的“6个”陷阱
陷阱1 常在气体摩尔体积的适用“对象及条件”设陷 [应对策略]
抓“两看”,突破气体与状况陷阱 一看“气体”是否处在“标准状况”。 二看“标准状况”下,物质是否为“气体”[如CCl4、CHCl3、CH2Cl2(注: CH3Cl为气体)、H2O、溴、SO3、己烷、苯、HF、NO2等在标准状况下均不为 气体]。
解题探究 JIETITANJIU
题组一 突破宏观量(质量、体积)与粒子数的换算 1.已知:①6.72 L NH3(标准状况下) ②1.204×1023个H2S分子 ③5.6 g CH4 ④0.5 mol HCl,下列关系正确的是 A.体积大小:④>③>②>①
√B.原子数目:③>①>④>②
高中化学第三节物质的量第2课时气体摩尔体积学生用书新人教版必修第一册

第2课时气体摩尔体积核心微网络素养新要求1.了解影响气体、液体、固体体积的因素。
2.了解气体摩尔体积的含义。
3.学会有关气体摩尔体积的简单计算。
4.理解阿伏加德罗定律及相关推论。
学业基础——自学·思记·尝试一、影响物质体积大小的因素特别提醒相同物质的量的同种物质在不同状态下所占的体积一般是固体<液体<气体。
二、气体摩尔体积状元随笔利用气体摩尔体积进行化学计算时的注意事项(1)22 .4 L是1 mol任何气体在标准状况下的体积,因此在非标准状况时不能随意使用22 .4 L·mol-1。
但在非标准状况下(比如温度高于0 ℃,压强大于101 kPa)的V m也可能是22 .4 L·mol-1。
(2)只适用于气态物质,对于固态物质和液态物质是不适用的。
(3)此处所指的“气体”可以是纯净物,也可以是混合物。
三、阿伏加德罗定律及其推论1.阿伏加德罗定律(1)定律:同温同压下,________的任何气体都含有________的分子(即“四同”)。
(2)解释:同温同压下的气体,体积相同时,分子数必相同;反之,分子数相同时,体积也必相同。
特别提醒(1)阿伏加德罗定律仅适用于气体,可以是单一气体,也可以是混合气体。
(2)定律中的同温、同压不一定指标准状况。
2.阿伏加德罗定律的推论[即学即练]1.判断正误,正确的打“√”,错误的打“×”(1)一定温度、压强下,气体体积由其分子的大小和数目决定。
( )(2)固态物质和液态物质的体积决定于粒子大小和粒子数目。
( )(3)同温同压下,若两种气体所占体积不同,其主要原因是气体分子间平均距离不同。
( )(4)1mol一氧化碳和1mol氧气所含的分子数相同,体积也相同。
( )(5)同温同压下,相同体积的任何气体都含有相同数目的原子。
( )(6)同温同压下,1mol气体的体积均为22.4L。
( )(7)标准状况下,1mol任何物质的体积都约为22.4L。
第一章第三讲 物质的量气体摩尔体积

×
√
(5)6.02×1023个Na+的质量等于23 g。(
)
考点突破 实验探究 高考演练 课时训练
考点一 物质的量
摩尔质量
解析:
题组一 有关概念的理解
2.下列说法中正确的是( ) A.摩尔既是物质的数量单位又是物质的质量单位 B.阿伏加德罗常数是12 kg12C中含有的碳原子数 C.1 mol水分子中含有2 mol氢原子和1 mol氧原子 D.一个NO分子的质量是a g,一个NO2分子的质量 是b g,则氧原子的摩尔质量是(b-a)g·mol-1
牙齿表面生成一层质地坚硬、溶解度小的氟磷
酸钙。其化学式为Ca5(PO4)3F。则1 mol Ca5(PO4)3F中含氧原子的物质的量为( ) A.1 mol B.4 mol C.5 mol D.12 mol
D
考点突破 实验探究 高考演练 课时训练
考点一 物质的量
摩尔质量
解析: 题组二 有关分子(或特定组合)中的微粒数计算 摩尔质量的单位是
4.下列说法正确的是( ) A.H2的摩尔质量是2 g B.1 mol H2O的质量是18 g/mol C.氧气的摩尔质量是32 g/mol D.2 g H2含 1 mol H
“g/mol”,A项不 正确,C项正确
考点突破 实验探究 高考演练 课时训练
考点一 物质的量
摩尔质量
解析: 题组二 有关分子(或特定组合)中的微粒数计算 H2O的摩尔质量是18
摩尔是物质的量的单 位,每摩尔粒子含有 阿伏加德罗常数个粒
(2)摩尔是物质的量的单位,每摩尔粒子含有阿伏加德罗常数
×
子,(1)错误
个粒子。
(
)
考点突破 实验探究 高考演练 课时训练
2022版步步高《大一轮复习讲义》人教版第1章 第3讲 物质的量及相关概念

第3讲 物质的量及相关概念复习目标 1.了解物质的量、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数的含义。
2.能准确使用“N N A =n =m M =VV m=c (B)·V (aq)”进行一定量某物质与所含指定微粒的数目换算。
3.正确使用阿伏加德罗定律及推论解答气体的体积、压强与物质的量、微粒数目相关问题。
4.掌握气体(平均)摩尔质量的计算方法。
考点一 物质的量 摩尔质量1.物质的量(1)概念:物质的量是国际单位制中的七个基本物理量之一,用来表示一定数目微粒的集合体。
符号为n ,单位是摩尔(mol)。
(2)物质的量的规范表示方法(3)使用范围:适用于微观粒子或微观粒子的特定组合。
2.阿伏加德罗常数(1)国际上规定,1 mol 粒子集合体所含的粒子数约为6.02×1023,1 mol 任何物质所含的粒子数叫做阿伏加德罗常数,符号为N A ,N A ≈6.02×1023 mol -1。
(2)物质的量、阿伏加德罗常数与微粒数目的关系 (背会公式和字母含义)n =N N A ⇒变式⎩⎪⎨⎪⎧N =n ·N A N A =N n3.摩尔质量(1)概念:单位物质的量的物质所具有的质量称为该物质的摩尔质量。
符号为M 。
(2)常用单位:g·mol -1。
(3)数值:当粒子的摩尔质量以g·mol -1为单位时,在数值上等于该粒子的相对分子(或原子)质量。
(4)公式(背会):n =m M ⇒变式⎩⎪⎨⎪⎧m =n ·M M =m n(1)物质的量是表示微粒数目多少的物理量(×)错因:物质的量是表示含有一定数目粒子的集合体的物理量。
(2)1 mol任何物质都含有6.02×1023个分子(×)错因:离子化合物不存在分子。
(3)硫酸的摩尔质量为98 g(×)错因:摩尔质量的单位是g·mol-1。
2022化学第一单元认识化学科学第3节物质的量气体摩尔体积学案

第3节物质的量气体摩尔体积备考要点素养要求1。
了解物质的量(n)及其单位摩尔(mol)、摩尔质量(M)、气体摩尔体积(V m)、物质的量浓度(c)、阿伏加德罗常数(N A)的含义。
2。
能根据微粒(原子、分子、离子等)的物质的量、数目、气体体积(标准状况下)之间的相互关系进行有关计算。
1。
宏观辨识与微观探析:认识物质的量是联系宏观物质和微观粒子的重要工具,能从宏观和微观相结合的视角分析与解决实际问题。
2。
证据推理与模型认知:在有关物质的量的计算过程中,通过分析、推理等方法认识计算的方法,建立阿伏加德罗常数、气体摩尔体积等题目解答的模型.考点一物质的量及阿伏加德罗常数必备知识自主预诊知识梳理1.物质的量、阿伏加德罗常数(1)基本概念间的关系。
(2)物质的量的规范表示方法。
(3)物质的量(n)与微粒数(N)、阿伏加德罗常数(N A)之间的关系为。
微点拨概念辨析及注意事项2。
摩尔质量—微点拨对同一物质,其摩尔质量以g·mol-1为单位、相对原子(分子)质量、1mol物质的质量在数值上是相同的,但三者的含义不同,单位不同。
摩尔质量的单位是g·mol—1,相对原子(分子)质量的单位是1,1mol物质的质量单位是g。
3。
求解气体摩尔质量的五种方法(1)根据物质的质量(m)和物质的量(n):M=。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N A):M=。
(3)根据标准状况下气体的密度(ρ g·L-1):M=g·mol-1。
(4)根据同温同压下气体的相对密度(D=ρ1/ρ2):M1/M2=。
(5)对于混合气体,求其平均摩尔质量时,上述计算式仍然成立,还可以用下式计算:M=[用M1、M2、M3、……表示各成分的摩尔质量,用a%、b%、c%……表示相应各成分的物质的量分数(或体积分数)].自我诊断1.判断正误,正确的打“√",错误的打“×”。
学案8:物质的量 气体摩尔体积

第3讲物质的量气体摩尔体积【考纲定位】1.了解物质的量(n)及其单位摩尔(mol)、摩尔质量(M)、气体摩尔体积(V m)、阿伏加德罗常数(N A)的含义。
2.能根据微粒(原子、分子、离子等)物质的量、数目、气体体积(标准状况下)之间的相互关系进行有关计算。
3.了解相对原子质量、相对分子质量的含义,并能进行有关计算。
时,通过分析、推理、数据处理等角度领悟计算的方法。
3.模型认知——建立阿伏加德罗常数、气体摩尔体积的模型认知。
考点一物质的量摩尔质量【基础梳理】1.物质的量、阿伏加德罗常数注意:(1)使用摩尔作单位时,必须指定化学式或指明微粒的种类,如1 mol H 不能描述为1 mol 氢等。
(2)阿伏加德罗常数有单位,单位为mol-1,不能仅写数值6.02×1023。
2.摩尔质量(1)概念:单位物质的量的物质所具有的质量,符号为,单位为。
(2)数值:当微粒的摩尔质量以为单位时,在数值上等于该微粒的相对分子(原子)质量。
(3)关系:物质的量、物质的质量与摩尔质量关系为或或。
注意:(1)摩尔质量、相对分子质量、质量是三个不同的物理量,具有不同的单位。
如H2O 的摩尔质量为18 g·mol-1,H2O的相对分子质量为18,1 mol H2O的质量为18 g。
(2)摩尔质量与温度、压强、物质的量多少无关。
[应用体验]1.正误判断(正确的打“√”,错误的打“×”)(1)1 mol OH-的质量是17 g·mol-1。
()(2)N A代表阿伏加德罗常数,22 g CO2中含有的氧原子数为N A。
()(3)n mol O 2中分子数为N ,则阿伏加德罗常数为N n 。
( )2.(1)硫酸钠(Na 2SO 4)的摩尔质量为________;71 g Na 2SO 4中含钠离子的物质的量为________,氧原子的物质的量为________。
(2)49 g H 3PO 4的物质的量为________,用N A 表示阿伏加德罗常数的值,其中含有________个H ,含________个O 。
高中化学---物质的量气体摩尔体积---例题解答

第三章物质的量课时作业6物质的量气体摩尔体积傑时作业・堂童時时间:45分钟满分:100分一、选择题(15 X 4分=60分)1. 常温下,向密闭容器里分别放入两种气体各0.1 mol,在一定条件下充分反应后恢复到原温度时,压强降为开始时的1/4。
原混合气体可能是( ) A .H2和02 B. HCI 和NH3C. H2 和CI2D. CO 和02占燃【解析】由2H2+。
2=占===2出0,反应剩余0.05 mol 02,容器内反应后与反应前的压强之比为0.05 : 0.2= 1 : 4, HCI和NH3在常温下恰好完全反应生成NH4CI固体,反应后容占燃器内的压强为零;H2和CI2反应:H2+ Cl2=====2HCI,反应前后气体分子数保持不变,则反占燃应前后容器内的压强也保持不变;2C0 + 02=占燃=2。
02,反应后生成0.1 moI CO 2,剩余0.05 moI O2,容器内反应后与反应前的压强之比为0.15 : 0.2= 3 :4。
【答案】A2. 在相同的温度和压强下,4个容器中分别装有4种气体,已知各容器中的气体和容器的容积分别是a.C02,100 mL ; b.02,200 mL ; c.N2,400 mL ; d.CH4,600 mL。
则4 个容器中气体的质量由大到小的顺序是( )A. a>b>c>dB. b>a>d>cC. c>d>b>aD. d>c>a>b【解析】同温同压下,气体的物质的量比即为体积比,设C02为100 mol,则:m(C02)= 100X 44 g, m(02)= 200 X 32 gm(N2)= 400X 28 g, m(CH4)= 600X 16 g比较其质量的大小即可。
【答案】C3•只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是C.③④D.③【解析】根据n=严=m=产可知①、②、⑤是正确的。
物质的量和气体摩尔体积之间的关系

物质的量和气体摩尔体积之间的关系1. 引言物质的量和气体摩尔体积是化学中非常重要的概念。
物质的量是衡量物质数量的基本单位,而气体摩尔体积则是气体在一定条件下占据的空间大小。
物质的量和气体摩尔体积之间存在着紧密的关系,本文将探讨这种关系的性质和影响因素。
2. 物质的量和摩尔2.1 物质的量的定义物质的量是描述物质中包含的基本单位数量的物理量。
其国际单位为摩尔(mol)。
摩尔的定义为:摩尔是包含有6.02214 × 10^23个粒子(通常是原子、分子或离子)的物质的量。
这个常数被称为阿伏伽德罗常数(Avogadro’s constant),记作N_A。
2.2 摩尔的概念摩尔是一个用来表示物质的量的单位,类似于计算中使用的“一打”、“一打”等。
摩尔的概念是由意大利化学家阿伏伽德罗在19世纪提出的。
通过摩尔的概念,我们可以更方便地计算和比较物质的数量。
3. 气体摩尔体积3.1 摩尔体积的定义气体摩尔体积是指气体在一定条件下所占据的空间大小。
在标准状态下,即0摄氏度和1大气压下,1摩尔气体的体积约为22.4升。
这个数值被称为摩尔体积的标准值。
3.2 摩尔体积的计算摩尔体积可以通过摩尔气体的质量和密度之间的关系来计算。
根据理想气体状态方程PV=nRT(P为气体的压强,V为气体的体积,n为气体的物质的量,R为气体常数,T为气体的温度),我们可以得到摩尔体积的计算公式为V=nRT/P。
4. 物质的量和摩尔体积的关系4.1 摩尔体积与物质的量的直接关系根据摩尔体积的定义,摩尔体积与物质的量是直接相关的。
当物质的量增加时,摩尔体积也会增加;当物质的量减少时,摩尔体积也会减少。
这是因为在相同的条件下,更多的物质会占据更大的空间。
4.2 摩尔体积与物质的量的反比关系根据摩尔体积的计算公式V=nRT/P,我们可以看出摩尔体积与物质的量之间存在着反比关系。
当物质的量增加时,摩尔体积会减小;当物质的量减少时,摩尔体积会增大。
高一化学 第三章 物质的量 第三节 气体摩尔体积培优教案

第三章 芯衣州星海市涌泉学校物质的量第三节气体摩尔体积〔一〕网上课堂1.本讲主要内容①理解气体摩尔体积的概念。
②掌握有关气体摩尔体积的计算。
③通过气体摩尔体积的有关计算,培养分析、推理、归纳、总结的才能。
2.学习指导〔1〕1mol 任何物质的体积为:ρMV =〔V :1mol 物质的体积,M :物质的摩尔质量,ρ:物质的密度〕物质体积大小取决于构成这种物质的粒子数目,粒子的大小,粒子间的间隔。
当粒子数目一定时,固态和液态物质的体积决定于构造粒子的大小,而气体物质体积大小主要决定于气体分子之间的间隔。
而气态物质分子之间的间隔,受外界温度、压强的影响。
〔2〕气体的摩尔体积:单位物质的量气体所占的体积叫作气体摩尔体积。
符号为m V ,n V V m=〔V 气体体积,n :气体的物质的量〕。
常用的单位有:L/mol ,m3/mol 。
如上所述,气体的体积受温度和压强的影响,不谈温度和压强,就不能谈气体的体积。
经实验证明,在0℃,101Kpa 下〔称为标准状况〕,1mol 任何气体的体积约为2L 。
即在标准状况下,气体的摩尔体积约为2L/mol 。
〔3〕气体的体积〔V 〕跟气体的物质的量〔n 〕,气体的质量〔m 〕和气体中的微粒数目〔N 〕之间的关系: mnVN ×V m ÷V m÷M ×M×N÷N标准状况下气体的密度:〔4〕阿伏加德律:在标准状况下,气体的摩尔体积约为2L/mol,因此我们可以认为2L/mol是在特定条件下的气体摩尔体积。
那么在非标准状况下,如何来认识气体的体积、压强、密度、质量与物质的量之间的关系呢?一样温度、一样压强下,一样体积的气体中含有一样的分子数,叫阿伏加德律。
阿伏加德罗是意大利物理学家。
我们学习的1mol气体中约含有6.02×1023个分子,称其为阿伏加德罗常数,符号用NA表示,由阿伏加德律导出如下推论:①同温同压下:气体体积之比=物质的量之比②同温同体积下:气体压强之比=物质的量之比③同温同压下:气体密度之比=摩尔质量之比为理解题的需要,有时也求混合气体的平均摩尔质量,其计算方法是:m混:混合气体总质量,n混:混合气体总物质的量,M1M2...Mi混合气体各成分的摩尔质量,x1x2 (xi)混合气体各成分的物质的量分数。
高考化学一轮复习第3讲物质的量气体摩尔体积提升练习(含解析)

第3讲物质的量气体摩尔体积1.双酚基丙烷(BPA,分子式为C15H16O2)可能会降低男性及女性的生育能力。
下列有关判断不正确的是( )A.BPA的摩尔质量是228 g·mol-1B.1 mol BPA中含有6.02×1023个分子C.BPA属于有机化合物D.1 mol BPA在标准状况下的体积约为22.4 L【答案】D【解析】BPA在标准状况下肯定不是气体。
2.下列叙述中错误的是( )A.阿伏加德罗常数的符号为N A,其近似值为6.02×1023 mol-1B.等物质的量的O2和O3,所含氧原子数相同C.在0.5 mol Na2SO4中,含有的Na+数约是6.02×1023D.摩尔是物质的量的单位【答案】B【解析】等物质的量的O2和O3,所含氧原子数不同。
3.清末成书的《化学鉴原》中有一段描述:“各原质(元素)化合所用之数名曰‘分剂数’。
养气(氧气)以八分为一分剂(即分剂数为八),……一分剂轻气(氢气)为一,……并之即水,一分剂为九”。
其中与“分剂数”一词最接近的现代化学概念是()A.摩尔质量 B.物质的量 C.化合价 D.质量分数【答案】A【解析】根据“各原质(元素)化合所用之数名曰‘分剂数’”。
氧气八分为一分剂,氢气一分为一分剂,水九分为一分剂,则氧气的分剂数为八,氢气的分剂数为一,水的分剂数为九,即8份氧气与一份氢气化合生成九份水,满足O2+2H2=2H2O中的质量守恒,因此与“分剂数”一词最接近的现代化学概念为摩尔质量,故选A。
4.下列说法正确的是()A.1 mol氢约含有6.02×1023个粒子 B.H2的摩尔质量是2 gC.1mol O2的质量是32 g,含有的氧原子数为2N A D.铁的摩尔质量等于铁原子的相对原子质量【答案】C【解析】1 mol 氢,指向不明确,没有明确微粒是氢分子还是氢原子,A 错误;摩尔质量的单位是g/mol , H 2的摩尔质量是2 g/mol ,B 错误;1mol O 2的质量是32 g ,含有2mol 氧原子,含有的氧原子数为2N A ,C 正确;摩尔质量的单位是g/mol ,相对原子质量的单位为“1”,铁的摩尔质量在数值上等于铁原子的相对原子质量,D 错误。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三讲物质的量和气体摩尔体积(1课时)
[考试目标]
(1)了解定量研究的方法是化学发展为一门科学的重要标志。
(2)了解物质的量的单位——摩尔(mol)、摩尔质量、气体摩尔体积、阿伏加德罗常数的含义。
(3)根据物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系进行有关计算。
[要点精析]
一、物质的量、摩尔、摩尔质量、气体摩尔体积
1、物质的量、摩尔:物质的量是国际单位制的七种基本量之一,摩尔是物质的量的单位。
每摩尔物质含有阿佛加德罗常数个微粒,阿伏加德罗常数:其数值为0.012 kg 12C 所含的碳原子数,大约为6.02×1023,单位:mol-1
其中微粒指微观粒子如:分子、原子、离子、质子、电子或其它粒子或它们的特定组合。
例1:下列关于物质的量的说法中不正确的是
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.是表示物质数量的单位
解析:不正确的说法是D。
2、摩尔质量:人们将单位物质的量的物质所具有的质量叫做摩尔质量,它的常用单位为
g/mol。
物质的量(n)、物质的质量(m)和物质的摩尔质量(M)之间存在着以下关系:n=m/M
3、气体摩尔体积:在相同的温度和压强下,1摩尔任何气体所占有的体积在数值上近似相
等。
人们将一定的温度和强下,单位物质的量的气体所占的体积叫做气体摩尔体积,它的常用单位是:L/mol。
1摩尔任何气体在标准状况下(00C,1.01×105Pa)所占的体积约是22.4L,这个体积叫做标准状况下气体的摩尔体积。
记作Vm,其数值为22.4mol/L。
这个概念要同时具备3个要点:①在标准状况下,②1摩尔任何气体,③体积约是22.4L。
例2:下列说法正确的是(N A表示阿伏加德罗常数的值)()
A.在常温常压下,11.2LN2含有的分子数为0.5N A
B.在常温常压下,1molNe含有的原子数为N A
C.71gCl2所含原子数为2N A
D.在同温同压下,相同体积的任何气体单质所含的原子数相同
答案:B、C
例3:同温同压下,某容器真空时的质量为201克,当它盛满甲烷时的质量为203·4克,而盛满气体Y时质量为205·5克,则Y气体的式量为多少?
解析:本题是考查的内容是气体的特征:即同温同压下,同体积的气体有相同的分子数(203·4-201)/16=(203·4-201)/M
M=32
知识延伸:混合气体平均分子量:
M=M1×n1%+M2×n2%+M3×n3%
M1、M2、M3、是每一种气体的相对分子质量;n1% 、n2% 、n3%是混合气体中每一种气体的物质的量分数。
例4:某固体A在一定的温度下分解生成气体B、C、D:2A=B+2C+3D,若测得生成气体的质量是相同体积的H2质量的15倍,则:
(1)生成的混合气体的摩尔质量为多少?
(2)固体A的摩尔质量是多少?
解析:混合气体的平均分子量:M=2×15=30
根据质量守恒定律:2M A=M B+2M C+3M D
而混合气体的平均分子量:M=(M B+2M C+3M D)×1/6=2M A×1/6=30
所以:M A=90
各物理量的相互关系
二、化学基本定律
(1)质量守恒定律
参加反应的各种物质的质量总和等于反应后生成的各物质的质量总和。
这一定律是书写化学方程式和化学计算的依据。
例5:m molC2H2跟n molH2在密闭容器中反应,当其达到平衡时,生成p mol C2H4。
将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质量是
A、3m+n
B、5/2m+n/2-p/3
C、3m+n+2p
D、5m/2+n/2
解析:本题如果按传统的方法也能得出正确结果,但费时多,而利用质量守恒定律解题快而简洁。
C~CO2~O2,4H~2H2O~O2
因此,m molC2~2m molO2(2m+2n)molH ~(2m+2n)/4 mol O2
总氧气量:2m+(2m+2n)/4=5m/2+n/2 答案为D。
(2)阿佛加德罗定律
在相同温度和压强下,同体积的任何气体都含有相同数目的分子。
阿佛加德罗定律的应用:
①标准状况下气体的体积(L)=22.4mol/L×物质的量(mol)
气体摩尔质量(g/mol)=22.4mol/L×标准状况下气体的密度(g/L)
②同温同压下任何气体的体积比等于其分子个数之比,也等于其物质的量之比
③同温同压下任何气体的密度比等于其相对分子质量之比,也等于同体积的质量之比。
④在温度和体积一定时,气体的压强与物质的量成正比;若温度和压强一定时,气体的
体积与物质的量成正比。
⑤在温度与气体的物质的量一定时,其气体的压强与体积成反比。
例6:A容器中盛有体积百分比为80%的H2和20%的O2,试求:
(1)混合气体中H2和O2的分子数之比、质量之比各为多少?
(2)混合气体的平均分子量是多少?它在标准状况下的密度是多少?
(3)在1500C时,引燃混合气体,反应结束后恢复到1500C,则反应后混合气体的平均分子量是多少?引燃前后,,A容器内的压强有什么变化?密度是否变化?
解析:(1)分子数之比等于体积比等于物质的量比,所以
H2和O2的分子数之比为:80%:20%=4:1
质量之比为:4×2:1×32=1:4
(2)混合气体的平均分子量M=2×80%+32×20%=8
在标准状态下 =8/22.4=0.357(g/L)(3) 2H2 + O2= 2 H2O
2mol 1mol 2mol
可见,4molH2和1molO2反应后,得到了2mol H2O和2molH2的混合气体,所以
反应后的平均分子量为:18×2/4+2×2/4=10;
在保持温度和体积不变的条件下,气体的压强之比等于物质的量之比
所以P前:P后=(4+1):(2+2)=5:4。
反应后压强变小,根据质量守恒定律,反应前后的质量不变。
A容器的体积不变,所以混合气体的密度不变。
(深圳大学附中陆秀臣)。
