饱和烃的结构和性质
大学有机化学第二章饱和烃

绿色化学与可持 续发展
随着环保意识的提高,绿色 化学和可持续发展已成为有 机化学的重要发展方向。研 究和发展环境友好、资源节 约的合成方法与技术,对于 实现可持续发展具有重要意 义。
计算机辅助ห้องสมุดไป่ตู้机 合成设计
随着计算机科学的发展,利 用计算机辅助设计工具进行 有机合成已成为可能。这种 方法有助于提高合成效率和 降低成本,为有机化学的发 展开辟了新的途径。
环烷烃的化学性质
01
02
03
加成反应
环烷烃中的碳碳单键可以 被氢气、卤素等试剂加成, 生成相应的烷基卤化物或 醇类。
开环反应
在酸或碱催化下,环烷烃 可以发生开环反应,生成 链状烷烃。
氧化反应
环烷烃在常温下容易被氧 化剂氧化,生成酮、醛等 化合物。
05 不饱和烃
烯烃和炔烃的结构
烯烃结构
烯烃是含有碳碳双键的烃类,双 键连接的两个碳原子为sp2杂化, 双键中的一根键为π键,另一根
命名法
系统命名法
根据国际纯粹与应用化学联合会 (IUPAC)的规定,采用系统命名法 对饱和烃进行命名。主要依据碳链的 长度和取代基的种类、位置来确定烃 的名称。
习惯命名法
对于一些简单的饱和烃,可以采用习 惯命名法,如甲烷、乙烷、丙烷等。
03 烷烃
烷烃的结构
烷烃由碳原子和氢原子组成, 碳原子之间通过单键连接,形 成链状或环状结构。
重要性及应用
01
基础理论
烷烃是学习有机化学的基础,对 于理解其他烃类和有机化合物的 性质至关重要。
工业应用
02
03
科学研究
烷烃是石油工业的主要组成部分, 用于生产燃料、润滑油、溶剂等。
烷烃是合成其他有机化合物的重 要原料,在药物合成、材料科学 等领域有广泛应用。
饱和烃烷烃和环烷烃课件

目前对烷烃和环烷烃的结构与性质关系仍有许多未知领域,深入研究这些关系有助于发现新的应用领 域和性能优化的可能性。
对未来发展的建议
加强基础研究与应用研究的结合
为了推动烷烃和环烷烃领域的发展,需要加强基础研究与应用研究的结合,促进科技成 果的转化和应用。
培养高素质人才
高素质人才是推动学科发展的关键,应重视人才培养,加强学术交流与合作,提高研究 水平和创新能力。
烃化反应和裂化反应是烷烃合成的常用方法,其中烃化反应可以生成高纯度的烷烃,但需要 使用大量的卤代烃或醇类物质,成本较高;裂化反应虽然可以大量生产烷烃,但副产物较多 ,产率较低。
环化反应和烷基化反应是环烷烃合成的常用方法,其中环化反应可以生成多种类型的环烷烃 ,但需要使用大量的烯烃或炔烃物质;烷基化反应虽然可以大量生产环烷烃,但需要使用卤 代烃或醇类物质,成本较高。
03
烷烃和环烷烃的性质比 较
物理性质比较
沸点
随着分子量的增加,烷烃和环烷 烃的沸点都逐渐升高。但在相同 分子量下,由于环烷烃的分子结 构更加紧凑,其沸点往往高于相
应的直链烷烃。
熔点
环烷烃的熔点通常比直链烷烃高 ,因为环烷烃的分子间作用力更
强。
密度
在常温常压下,烷烃和环烷烃的 密度都随着分子量的增加而增大
饱和烃烷烃和环烷烃课 件
目录 CONTENT
• 饱和烃烷烃概述 • 环烷烃概述 • 烷烃和环烷烃的性质比较 • 烷烃和环烷烃的合成方法 • 烷烃和环烷烃的工业生产 • 烷烃和环烷烃的前沿研究与展望
01
饱和烃烷烃概述
定义与分类
定义
饱和烃烷烃是只含有碳、氢两种 元素的化合物,且碳原子之间只 通过单键相互连接。
有机化学饱和烃

形排列。
,
四、烷烃的物理性质 (阅读)
五、烷烃的化学性质
(一)烷烃的卤代反应
CH4 +Cl Cl 250~400 OC CH 3 Cl + CH 2 Cl 2 + CH Cl3 +C Cl4 ,
说明:1、光照或高温作用下,发生共价键均裂的自
由基取代反应。 2、反应范围是SP3杂化的碳原子上氢的反应。 3、反应活性顺序为:F2 > C12 > Br2 > I2 4、 Br2具有高选择性。
(二)甲烷卤代反应的反应热 (了解) 根据单键均键的解离能数据计算
(三)甲烷卤代反应的机理 机理;反应物转变成产物所经历的具体途径。
(1)链引发 C1-C1键发生均裂(产生氯自由基C1·)
Cl Cl Cl + Cl
(2)键增长(链传递)
CH3 H +Cl CH3 +Cl 2
CH3 +HCl CH3Cl + Cl
说明: 1、氢的反应的相对活性顺序
叔氢 > 仲氢 > 伯氢原子 2、主要产物有相对活性和反应几率决定。 3、溴代具有高选择性,主要产物只由相对活性
决定。
3.机体内的有机自由基与活性氧 (了解)
活性氧:
超氧负离自由基 单线态氧 过氧化氢 羟基自由基
O
-
2
,
|O2
H2O2
·OH
它们的衍生物含氧有机自由基 RO·
CH3
CH3 C CH2CH3, CH3
新戊烷 2,2 - 二甲基丙烷
新己烷 2,2 - 二甲基丁烷
三、乙烷和丁烷的构象(conformation)
有机化学-第五章

5.1 饱和烃的结构和分类 5.2 链烷烃的物理性质 5.3 烷烃的化学性质
卤代反应的机理 烷烃的其他取代反应 烷烃的氧化反应 裂解及异构反应
5.4 环烷烃的化学性质
烃:分子中只含碳、氢两种元素的化合物 统称为碳氢化合物,简称为烃。烃是有机化合 物最基本的化合物,也是有机化学工业的基础 原料。
硝化反应产物复杂,除取代反应外,还有烃分子断链的 反应。 硝化反应属自由基型反应机理:
开始的· NO2来自硝酸中,· NO2是个含奇数电子的中性物种, 是一个自由基。 硝化产物作为工业溶剂,如用硝基戊烷作为纤维素酯和 合成树脂的溶剂;硝基甲烷是有机合反应的重要原料。
二. 氯磺酰化反应
烃分子中的氢被氯磺酰基(-SO2Cl)取代的反应称为 氯磺酰化反应。 常用的氯磺酰化试剂有:硫酰氯(SO2Cl2)或氯和二 氧化硫。
5469.2
2,2-二甲基己 烷
5462.1
2,2,3,3-四 甲基丁烷
5455.4
烃氧化反应的产物都是 CO2 和 H2O ,燃烧焓 -Δ Hθ 值反映了反应物的焓 Hθ反应物,即反映了异构体的 稳定性: 正构CnH2n+2 比 异构CnH2n+2 能量高,不稳定 在CnH2n+2中:支键数增多,HØ值小,稳定 每一摩尔 -CH2- 的 -ΔHθ ≈ 660 kJ· mol-1 烷烃的最大用途就是作为燃料,是目前人类的主要能 源。 合理利用现有能源,开发新的能量是人类生存面临的 主要问题之一。
可用反应--能量图表示这一反应过程:
在这一反应过程中,C 原子的杂化状态是由 Csp3 向 Csp2 的转变过程,中间体· CH3的 C 的构型是 sp2 杂化, 即平面构型。 生成的· CH3中间体的能量很高,极活泼, 很快与Cl2反应:
烃的结构式-概述说明以及解释

烃的结构式-概述说明以及解释1.引言1.1 概述烃是有机化合物中最简单的一类,由碳和氢原子组成。
烃是地球上最丰富的化合物之一,广泛存在于石油、天然气等化石燃料中。
烃分子的结构式描述了烃分子中碳原子的连接方式,它反映了烃分子中的化学键和它们之间的空间排列。
烃的结构式可以用来表示烷烃、烯烃和炔烃等不同类型的烃化合物。
烷烃是由碳-碳单键连接的碳氢化合物,烯烃是由碳-碳双键连接的碳氢化合物,而炔烃则是由碳-碳三键连接的碳氢化合物。
烃化合物的结构式告诉我们有关分子的重要信息,如分子的分子量、化学键的种类和数量以及各原子之间的空间排列。
通过对烃化合物的结构式的研究,我们可以了解到它们的物理性质和化学性质,进而推导出它们的应用领域。
烃分子的结构有助于我们理解和预测烃分子的性质和行为。
例如,通过观察一个烃化合物的结构式,我们可以判断该分子是否具有立体异构体。
立体异构体是指具有相同分子式但空间结构不同的分子。
这种异构体的存在会对烃的性质和反应产生重要影响,因此研究烃分子的结构是我们理解烃化合物的基础。
总之,烃的结构式是研究和理解烃化合物的重要工具。
通过了解烃分子的结构,我们可以深入了解烃的性质和行为,并为研究和应用烃化合物提供有力支持。
1.2 文章结构文章结构部分的内容可以包括以下内容:文章结构部分旨在介绍整篇文章的组织结构,让读者能够清晰地了解文章的分章节和主题内容。
本文主要分为引言、正文和结论三个部分。
引言部分包括概述、文章结构和目的三个部分。
概述部分将简要介绍烃的结构式及其重要性,引起读者的兴趣和阅读欲望。
文章结构部分即本部分,将详细说明文章的目录结构和各个章节的内容概要。
目的部分将说明本文的写作意图和目标,即通过对烃的结构式的介绍和分析,使读者更全面地了解烃的概念、分类和重要性。
正文部分将分为烃的概念和烃的分类两个章节进行详细阐述。
烃的概念章节将介绍烃的基本概念、定义和特点,包括碳氢化合物的基本组成和化学性质等内容。
烃基饱和和不饱和

烃基饱和和不饱和
烃基饱和和不饱和是有机化学中的两个常见概念。
烃是指仅由碳氢元素构成的化合物,其中碳氢键是主要的键类型。
烃可以分为两类:饱和烃和不饱和烃。
饱和烃,也称为脂肪烃,是指分子中所有碳原子都与最大数量的氢原子相连。
这意味着它们没有任何双键或环状结构。
最常见的饱和烃是烷烃,其中所有碳原子都是以单键链接的。
例如,甲烷(CH4)、乙烷(C2H6)和丙烷(C3H8)都是饱和烃。
饱和烃通常是液体或固体,在常温下很少存在气态。
不饱和烃是指分子中存在一个或多个碳-碳双键或环状结构。
不饱和烃分为两类:烯烃和炔烃。
烯烃是指分子中至少有一个碳-碳双键,而炔烃则是指分子中至少有一个碳-碳三键。
例如,乙烯(C2H4)和丙烯(C3H6)是烯烃,而乙炔(C2H2)是炔烃。
不饱和烃通常是气态,在常温下很少存在液态或固态。
在化学反应中,烃基的饱和或不饱和性质会对反应的类型和速率产生影响。
例如,饱和烃更难被氧化,因此烷烃的燃烧反应需要更高的温度和氧气浓度。
另一方面,不饱和烃的双键或三键更容易参与化学反应,如加成反应和聚合反应。
总之,烃基的饱和和不饱和性质对于有机化学的研究和实际应用都具有重要意义。
了解这些概念可以帮助我们更好地理解烃化合物的性质和反应行为。
- 1 -。
第2章饱和烃:烷烃和环烷烃
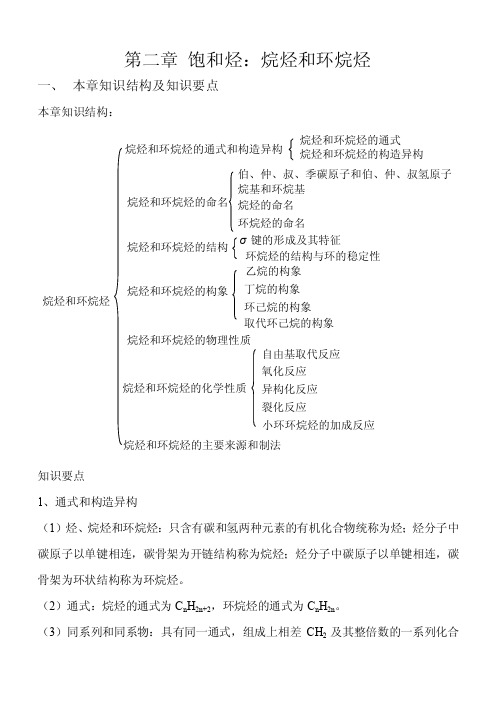
第二章 饱和烃:烷烃和环烷烃一、 本章知识结构及知识要点本章知识结构:知识要点1、通式和构造异构(1)烃、烷烃和环烷烃:只含有碳和氢两种元素的有机化合物统称为烃;烃分子中碳原子以单键相连,碳骨架为开链结构称为烷烃;烃分子中碳原子以单键相连,碳骨架为环状结构称为环烷烃。
(2)通式:烷烃的通式为C n H 2n+2,环烷烃的通式为C n H 2n 。
(3)同系列和同系物:具有同一通式,组成上相差CH 2及其整倍数的一系列化合烷烃和环烷烃烷烃和环烷烃的通式和构造异构烷烃和环烷烃的构造异构烷烃和环烷烃的命名 烷基和环烷基烷烃和环烷烃的结构σ键的形成及其特征环烷烃的结构与环的稳定性 乙烷的构象烷烃和环烷烃的主要来源和制法自由基取代反应氧化反应丁烷的构象烷烃和环烷烃的物理性质烷烃和环烷烃的化学性质 烷烃的命名环烷烃的命名烷烃和环烷烃的构象 环己烷的构象取代环己烷的构象 异构化反应裂化反应小环环烷烃的加成反应烷烃和环烷烃的通式伯、仲、叔、季碳原子和伯、仲、叔氢原子物称为同系列。
同系列中的各化合物互为同系物。
(3)构造异构:分子中原子的连接顺序不同形成的异构体叫构造异构。
2、命名(1)烷烃的命名普通命名法:用甲、乙、丙、丁、戊、己、庚、辛、壬、癸十个字分别表示十个以下碳原子的数目,十个以上的碳原子用汉字数字(十一、十二、十三……)表示,用正、异、等前缀区别同分异构体。
系统命名法:(a)选主链:在分子中选择一条最长的碳链作主链,根据主链的碳原子数叫某烷,将主链以外的其他烷基看作是主链上的取代基。
烷基是由烷烃分子除去一个或几个氢原子剩下的部分,通常用R-表示。
(b)编号:从靠近取代基的一端开始编号,使取代基编号位次最小。
(c)取代基的排列次序:用阿拉伯数字表示取代基位置,用汉字(一、二、三……)表示相同取代基个数,写在取代基名称前面,若含有不同的取代基,则优先级别低的写在前面,优先级别高的写在后面。
(2)环烷烃的命名(a)单环环烷烃:在相应的烷烃名称之前加“环”字,称为“环某烷”。
饱和烃的定义

饱和烃的定义
饱和烃是一类化合物,它们由氢和碳组成,其化学式为CnH2n+2。
这类化合物又被称为烷烃,是一种非常广泛存在于自然界和工业中的物质。
饱和烃的最显著特征是它们的化学键全部为单键,因此它们的分子结构比较简单。
由于这种单键的存在,饱和烃分子中的碳原子与周围的氢原子之间存在着最大可能的化学键,因此它们的分子结构是最稳定的。
饱和烃是一类非常常见的化合物,它们存在于许多自然界中,如石油、天然气、煤等。
在工业上,饱和烃也是一种非常重要的化学物质,广泛应用于石油加工、化工、制药等领域。
饱和烃的化学性质比较稳定,它们不容易发生化学反应。
这是由于饱和烃的分子结构比较简单,它们的化学键比较强,因此不容易被其他化学物质攻击。
但是,饱和烃也不是完全不发生反应,它们可以在高温高压下发生裂解反应,从而产生更小的碳氢化合物。
饱和烃的物理性质也比较稳定。
它们的熔点和沸点比较高,且随着碳原子数的增加而增加。
这是由于饱和烃分子中的化学键比较强,需要消耗较多的能量才能使它们分离。
因此,饱和烃在常温下一般是液体或固体状态,而不是气体状态。
在实际应用中,饱和烃有许多用途。
例如,石油中的饱和烃可以用于制备汽油、柴油、煤油等燃料,还可以用于制备塑料、橡胶、合成纤维等化学品。
此外,饱和烃还被广泛用于烹饪、加热和照明等方
面。
总之,饱和烃是一类非常重要的化合物,它们广泛存在于自然界和工业中,具有稳定的化学和物理性质,被广泛应用于石油加工、化工、制药等领域。
饱和烃的定义

饱和烃的定义饱和烃是一类由碳和氢组成的有机化合物,其分子中的碳原子数量和氢原子数量的比值为2:2n+2。
它们通常具有直链、分支链或环状结构,因此也被称为烷烃、烷基化合物或脂肪烃。
饱和烃的主要特点是与空气中的氧气不发生化学反应,不易燃烧,且在常温下呈气态、液态或固态。
这些特性使得饱和烃广泛应用于石油工业、化工工业、医药工业等领域。
饱和烃可以根据其碳链的长度、结构和性质分为以下几种:1. 甲烷(CH4):由单个碳原子和四个氢原子组成的最简单的饱和烃,常见于天然气和沼气中。
2. 乙烷(C2H6):由两个碳原子和六个氢原子组成,具有较低的沸点和比重,通常用于同类化合物的制备。
3. 丙烷(C3H8):由三个碳原子和八个氢原子组成,是石油和天然气中较常见的饱和烷烃之一,也被用作热源和燃料。
4. 正丁烷(C4H10):由四个碳原子和十个氢原子组成,因其分子结构简单而广泛应用于合成其他有机化合物的原料。
5. 异戊烷(C5H12):是一种有机溶剂和石油清洁剂,由五个碳原子和十二个氢原子组成,含有一根分支链。
6. 六碳烷:指由六个碳原子和2n+2个氢原子组成的烷基化合物,如正己烷、异己烷、环己烷等。
它们具有较高的沸点和比重,广泛用于燃料、润滑油和有机合成。
7. 高级饱和烃:指由七个或更多碳原子组成的烷基化合物,如正庚烷、正十二烷等,这些化合物具有更高的沸点和密度,通常用于合成润滑油、燃料和引发剂。
总之,饱和烃在现代工农业生产中发挥着重要的作用,同时也对环境和人类健康造成着一定的影响和挑战。
因此,需要加强饱和烃的研究和管理,从而更好地利用其优点,减少其不利影响,为人类创造更美好的生活。
烷烃性质(第三课时)
二、烷烃的化学性质
通常情况下比较稳定,与强酸,强碱不发生反应
1.氧化反应:
点燃
燃烧: CH4 +2O2
CO2+2H2O
甲烷是一种清洁高效的燃料
请用烷烃的分子式通式写出烷烃燃烧的 化学方程式:
3n+1
点燃
CnCnHO22n++2(+n+12)H2O O2
烷烃的性质(第三课时)
学习目标:
1.通过对甲烷性质的学习,依据结构决定性质, 能够推到出烷烃的性质及有机物的一些通性。
2.通过甲烷与氯气的反应学习,认识取代反应 的特点,从而学会辨识取代反应。
复习提问:
1. 烷烃(饱和烃)的结构特点?分子式通式?
碳原子间以单键结合,其余价键均与氢原子结合
CnH2n+2 n≥1
1. 反应条件为光照(室温或阴暗处不反应)
2. 烷烃和卤素的气态单质反应,溶液不行 (甲烷和溴水,溴的CCl4溶液不反应)
3. 反应一旦发生,不会停留在某一步,即使氯 气不足量产物依然是五种物质的混合物
4. 有机物参加的反应往往比较复杂,有副产物 生成,因此有机方程式中用箭头而不用等号
练习: 1.下列反应属于取代反应的是( D )
最简单的烷烃 CH4
CH4 烷烃
天然气,沼气林”,蜡烛,蜡笔中的石蜡
一、物理性质
1. CH4的物理性质: 难溶于水,无色气体
2. 烷烃的物理性质: 1)烷烃都不溶于水,可溶于有机溶剂(汽油,苯等)
读下表总结烷烃物理性质的变化规律?
名称
熔点(℃)
一氯乙烷
3.分解反应:
饱和烃

裂化反应是大分子烃在高温、高压或有催化剂的条件下,分裂成小分子烃的过程。裂化反应属于消除反应,因此烷烃的裂化总是生成烯烃。如十六烷(C16H34)经裂化可得到辛烷(C8H18)和辛烯(C8H16)。
由于每个键的环境不同,断裂的机率也就不同,下面以丁烷的裂化为例讨论这一点:
CH3-CH2-CH2-CH3 → CH4 + CH2=CH-CH3
4.烷烃都不溶于水,易溶于有机溶剂。
CH3
|
注意:新戊烷(C(CH3)4)(也称2,2-二甲基丙烷)由于支链较多,常温常压下也是气体。
新戊烷结构式|
CH3
[编辑本段]化学性质
烷烃性质很稳定,在烷烃的分子里,碳原子之间都以碳碳单键相结合成链关,同甲烷一样,碳原子剩余的价键全部跟氢原子相结合.因为C-H键和C-C单键相对稳定,难以断裂。除了下面三种反应,烷烃几乎不能进行其他反应。(在通常情况下,与强酸.强碱.强氧化剂都不反应)
理论上说,由于烷烃的稳定结构,所有的烷烃都能稳定存在。但自然界中存在的烷烃最多不超过50个碳,最丰富的烷烃还是甲烷。
由于烷烃中的碳原子可以按规律随意排列,所以烷烃的结构可以写出无数种。直链烷烃是最基本的结构,理论上这个链可以无限延长。在直链上有可能生出支链,这无疑增加了烷烃的种类。所以,从4个碳的烷烃开始,同一种烷烃的分子式能代表多种结构,这种现象叫同分异构现象。随着碳数的增多,异构体的数目会迅速增长,烷烃的熔沸点增加,但相同数目的碳原子,支链越多,熔沸点越低。
烷烃的作用主要是做燃料。天然气和沼气(主要成分为甲烷)是近来广泛使用的清洁能源。石油分馏得到的各种馏分适用于各种发动机:
C1~C4(40℃以下时的馏分)是石油气,可作为燃料;
饱和度化学有机

饱和度化学是有机化学的一个重要分支,其主要研究饱和烃(saturated hydrocarbons)的结构、性质和反应。
饱和烃是指分子中所有碳原子都共价键连接,且没有双键或三键。
这类化合物通常是稳定的,不易与其他物质反应。
饱和烃中最简单的是由一个碳原子和四个氢原子组成的甲烷(methane)。
随着碳原子数量的增加,饱和烃的分子结构可以变得更加复杂。
举例来说,两个碳原子和八个氢原子组成的乙烷(ethane),三个碳原子和十二个氢原子组成的丙烷(propane)等。
饱和烃可以进行各种化学反应,如燃烧、氧化、加氢等。
但是,由于它们没有双键或三键,所以反应通常比不饱和烃(unsaturated hydrocarbons)复杂。
饱和烃在工业上有广泛的应用,如石油和天然气中的大部分成分都是饱和烃,并且它们是燃料、化工原料和合成材料的重要来源。
饱和烃的公式通常由碳原子和氢原子组成,通常表示为CnH2n+2。
例如:甲烷(methane):CH4乙烷(ethane):C2H6丙烷(propane):C3H8丁烷(butane):C4H10戊烷(pentane):C5H12这些是饱和烃的简单例子,饱和烃可以有更多碳原子,因此公式也会变得更加复杂。
饱和度指的是一种物质中存在的饱和分子数量与总分子数量之比。
在有机化学中,饱和度指的是饱和烃分子数量与总烃分子数量之比。
饱和度公式通常表示为:S = (n_s / n_t) x 100%其中,S表示饱和度,n_s 表示饱和分子数量,n_t 表示总分子数量。
饱和度公式通常用于测量液体或气体中饱和分子的含量。
例如,在石油工业中,饱和度公式用于测量石油中饱和烃的含量。
饱和度的值通常介于0到100%之间,0%表示完全不饱和,100%表示完全饱和。
有机化合物的组成与结构

有机化合物的组成与结构1 有机化合物的概念有机化合物是指碳元素与氢、氧、氮、硫、磷、卤素等元素发生共价键构成的化合物。
它是一个广泛的化学类别,包括蛋白质、糖类、脂肪、烃类等,广泛存在于天然界和人工合成中。
2 有机化合物的分类有机化合物的分类很多,可以按照它们的来源、结构、反应性质等进行分类。
其中按照结构特征进行分类是一种较为常见的分类方法,主要分为以下几类。
2.1 饱和烃饱和烃又称为烷烃,是最简单的有机化合物,只有碳-碳键和碳-氢键。
例如甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)等。
它们的反应性很低,很难被其他物质与氧气等氧化剂反应。
饱和烃在石油和天然气中丰富,也可以通过碳氢化合物的加氢反应制备。
2.2 不饱和烃不饱和烃分为烯烃和炔烃两类,它们拥有碳-碳双键或者碳-碳三键,因此比饱和烃具有更高的反应性。
例如乙烯(C2H4)、丙烯(C3H6)、乙炔(C2H2)、丙炔(C3H4)等。
它们可以通过烷基卤化物和碱金属等反应制备。
2.3 链烃链烃是由单一的烷基连成的直链分子,例如正丁烷(CH3-CH2-CH2-CH3)、正戊烷(CH3-CH2-CH2-CH2-CH3)等。
链烃可以通过碳氢化合物的裂解反应得到。
2.4 支链烃支链烃是由链烃中部分烷基被其他烷基所替代而形成的结构,例如异丙烷(CH3-CH(CH3)-CH3)、2,2-二甲基丁烷(CH3-CH2-CH(CH3)-CH3)等。
在石油和天然气中,支链烃占有很大比例。
2.5 有机环化合物有机环化合物是由碳与其他元素构成的环状分子,如苯、萘、烷基环、芳香族有机化合物等。
它们反应性很高,具有很多特殊的物理和化学性质。
2.6 酰基化合物酰基化合物是由酰基和碳-碳键含量不同而形成的化合物,如酰氯(COCl2)、羧酸(R-COOH)、酯(R-COO-R')等。
酰基化合物很常见,也具有多种重要的化学反应。
3 有机化合物的结构有机化合物的结构可以通过分子式、结构式、键能模型等形式进行描述。
第五章饱和烃总结

第五章饱和烃总结第五章主要介绍了饱和烃的相关知识,包括饱和烃的性质、分类、制备方法以及应用领域等方面内容。
本文将对饱和烃进行总结,主要内容如下:饱和烃是由碳和氢原子组成的化合物,具有饱和的碳-碳键和碳-氢键。
由于饱和烃的碳原子上没有其他原子团,所以它们分子间的作用力较弱,导致饱和烃的熔点和沸点较低。
同时,饱和烃也是一类非极性化合物,难以溶于极性溶剂。
根据碳原子数的不同,饱和烃可以分为脂肪烃和环烷烃两类。
脂肪烃包括直链烷烃、支链烷烃和环氧烷烃,它们在化学性质上存在一定差异。
而环烷烃是由环状碳骨架组成,具有特殊的性质和结构。
在饱和烃的制备方法中,主要包括天然脂肪和石油的热解、裂解及重整等方法。
这些方法可通过控制反应条件和催化剂的选择来实现对饱和烃的制备。
饱和烃在生活和工业中有广泛的应用。
其中,甲烷是天然气中的主要成分,被广泛用于能源的生产和供应。
乙烷是一种重要的石化原料,用于合成乙烯、醇类等化学品。
丙烷和丁烷主要用于供暖和燃料燃烧。
此外,饱和烃还可以用于制备高级燃料和合成润滑油。
饱和烃还具有一定的环境效应。
由于饱和烃的非极性和低溶解度,它们在环境中的分布和迁移能力较强。
饱和烃还可能对环境产生一定的毒性和污染效应。
总的来说,饱和烃是一类由碳和氢原子组成的化合物,具有饱和的碳-碳键和碳-氢键。
它们具有低熔点和沸点、非极性、难溶于极性溶剂等特点。
饱和烃的制备方法主要有热解、裂解及重整等。
饱和烃在能源、化工等领域有广泛的应用,并对环境产生一定的影响。
对于更深入地了解饱和烃的性质和应用,还需要进一步研究和探索。
饱和烃

§4.1 烷烃的物理性质
饱和烃
分子中碳原子间均以单键相连,而其余价键被氢原子所饱和的烃, 分子中碳原子间均以单键相连,而其余价键被氢原子所饱和的烃, 称为饱和烃(又称为石蜡烃)。分为烷烃和环烷烃。 )。分为烷烃和环烷烃 称为饱和烃(又称为石蜡烃)。分为烷烃和环烷烃。 在常温常压下C 的直链烷烃是气体; 一、状态 在常温常压下 1~C4的直链烷烃是气体;C5~C17的直链 烷烃是液体;十八碳原子以上的直链烷烃是固体。 烷烃是液体;十八碳原子以上的直链烷烃是固体。 二、沸点 b.p.(boiling point) 烷烃的沸点随分子量的增加而增大, 烷烃的沸点随分子量的增加而增大,对于同碳数的烷烃来说分子 中的支链越多,则沸点越低。 中的支链越多,则沸点越低。 原因: 1)烷烃分子是靠范德华力连在一起的且烷烃分子为非极 原因: ) 性或极性较弱的分子,所以烷烃分子间力主要是色散力。 性或极性较弱的分子,所以烷烃分子间力主要是色散力。 2)分子中支链越多,分子越趋于球形,分子间的接近程度 )分子中支链越多,分子越趋于球形, 降低,分子间的作用力减弱,则沸点降低。 降低,分子间的作用力减弱,则沸点降低。
CH4 + Cl2
漫 漫光 或或或或
CH3Cl + HCl
反应难以停留在一取代阶段,生成的一取代物可继续被ห้องสมุดไป่ตู้代, 反应难以停留在一取代阶段,生成的一取代物可继续被卤代,即: CH2Cl2 + HCl 氯仿 CH3Cl + Cl2
CH2Cl2
+ Cl2
CHCl3 + HCl
CHCl3 + Cl2
CCl4
痕痕
99%
4)烷烃氯代反应机理(反应历程) 烷烃氯代反应机理(反应历程) 以甲烷的氯代反应为例: 以甲烷的氯代反应为例: 甲烷的氯代反应一般包括以下几个步骤: 甲烷的氯代反应一般包括以下几个步骤: (1)氯分子在光照或高温条件下,吸收能量发生均裂生成氯自由基, )氯分子在光照或高温条件下,吸收能量发生均裂生成氯自由基, Cl:Cl
乙烷乙烯与乙炔结构的对比

乙烷乙烯与乙炔结构的对比乙烷、乙烯和乙炔是三种简单的碳氢化合物,它们之间的结构差异导致了它们在物理性质和化学性质方面的不同。
下面将对乙烷、乙烯和乙炔的结构进行对比。
乙烷(C2H6)是一种无色、无味的气体,分子式为CH3CH3、乙烷分子由两个碳原子和六个氢原子组成,碳原子之间通过单键相连,每个碳原子上都有三个氢原子。
由于乙烷分子结构的简单性,它的空间构型是平面的。
乙烷的内部键角为109.5°,两个碳原子之间的键长为154 pm。
乙烯(C2H4)是一种无色气体,分子式为CH2CH2、乙烯分子由两个碳原子和四个氢原子组成。
乙烯的结构中有一个双键连接两个碳原子,其他两个碳上分别连接一个氢原子。
与乙烷相比,乙烯的分子结构呈现出平面的构型,碳碳双键成为平面共面的一对。
双键的存在导致乙烯的键角为120°,双键的长度约为133 pm,而单键的长度约为147 pm。
乙炔(C2H2)是一种无色的气体,在常温下具有不稳定性。
乙炔分子由两个碳原子和两个氢原子组成。
乙炔的结构是由一个三键和两个单键连接两个碳原子。
这三个键的存在导致了乙炔分子呈线性结构,其键角为180°。
乙炔分子的键长最短,碳碳三键约为120 pm,而碳碳单键约为154 pm。
从分子结构的对比中可以看出,乙烷、乙烯和乙炔在结构上的主要差异是碳原子间的键的数量和类型。
乙烷的碳原子之间通过单键相连,乙烯则包含一个碳碳双键,乙炔则包含一个碳碳三键。
这些不同的结构导致了不同的物理和化学性质。
首先是物理性质方面的对比。
乙烷是一种饱和烃,分子结构中没有双键或三键,因此其分子间相互作用力较小。
由于乙烷分子结构的简单性,它的沸点较低,约为-88.6℃,熔点也较低,约为-183.3℃。
与乙烷相比,乙烯和乙炔中包含双键和三键,这些键的存在导致分子间相互作用力增强。
乙烯的沸点为-103.7℃,熔点为-169℃,而乙炔的沸点为-84℃,熔点为-80℃。
饱和烃的定义

饱和烃的定义饱和烃是一类化合物,其分子中只含有碳和氢原子,并且所有碳-碳键都是单键。
这意味着饱和烃分子中的所有碳原子都已经与最大数量的氢原子结合,并且没有空余的键位。
饱和烃也被称为烷烃,它们是碳氢化合物的一种。
本文将介绍饱和烃的定义、结构、性质和应用。
一、饱和烃的结构饱和烃分子的结构非常简单,由一系列碳原子和氢原子组成,它们之间只有单键。
饱和烃的分子式为CnH2n+2,其中n表示碳原子数。
例如,乙烷的分子式为C2H6,丙烷的分子式为C3H8,正戊烷的分子式为C5H12,依此类推。
饱和烃分子的结构可以用结构式或简化式表示。
例如,乙烷的结构式为CH3-CH3,其简化式为CH3CH3。
丙烷的结构式为CH3-CH2-CH3,其简化式为CH3CH2CH3。
二、饱和烃的性质1. 物理性质饱和烃是无色、无味、无毒的液体或气体,具有较低的密度和比重。
它们在常温下为气体或液体,但在高压下可以变为固体。
饱和烃的沸点和熔点随着碳原子数的增加而增加。
2. 化学性质饱和烃的化学稳定性很高,与大多数化学物质不发生反应。
它们不易燃烧,但在高温下可以与氧气反应,产生二氧化碳和水。
饱和烃可以通过加氢反应转化为不饱和烃,例如,丙烷可以转化为丙烯。
三、饱和烃的应用饱和烃在工业和日常生活中有广泛的应用。
以下是一些主要的应用:1. 燃料饱和烃是石油和天然气中的主要成分,它们是燃料的主要来源。
燃料可以用于发电、加热和运输等方面。
2. 化工原料饱和烃可以用作化工原料,例如,乙烷可以用于生产聚乙烯和乙醇,正丁烷可以用于生产丁二酸和丁醇。
3. 医药饱和烃可以用作药物的成分,例如,某些饱和烃可以用于制造皮肤软化剂和药膏基质。
4. 润滑油饱和烃可以用作润滑油的成分,例如,矿物油就是一种饱和烃。
四、结论饱和烃是一类简单的化合物,其分子中只含有碳和氢原子,并且所有碳-碳键都是单键。
它们具有较高的化学稳定性和低的反应性,广泛应用于燃料、化工原料、医药和润滑油等领域。
《饱和烃》 学历案

《饱和烃》学历案一、学习目标1、了解饱和烃的定义和分类。
2、掌握饱和烃的结构特点和通式。
3、理解饱和烃的物理性质及其变化规律。
4、学会饱和烃的化学性质,包括取代反应等。
5、能够运用所学知识,解决与饱和烃相关的实际问题。
二、学习重难点1、重点(1)饱和烃的结构特点和通式。
(2)饱和烃的化学性质,特别是取代反应的原理和应用。
2、难点(1)理解饱和烃的结构与性质之间的关系。
(2)取代反应的机理和反应条件的控制。
三、知识回顾在学习饱和烃之前,我们先来回顾一下一些相关的基础知识。
1、什么是有机物?有机物通常是指含碳元素的化合物,但一些简单的含碳化合物,如一氧化碳、二氧化碳、碳酸盐等除外。
2、烃的概念烃是仅由碳和氢两种元素组成的有机化合物。
四、知识讲解1、饱和烃的定义饱和烃是指分子中的碳原子之间都以单键结合,碳原子的剩余价键都与氢原子结合,使每个碳原子的化合价都达到“饱和”的烃。
2、饱和烃的分类(1)烷烃烷烃是饱和烃的一种,其通式为CnH2n+2(n 为碳原子数,n≥1)。
例如,甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)等都是烷烃。
(2)环烷烃环烷烃是指分子中含有环状结构的饱和烃。
例如,环己烷(C6H12)。
3、饱和烃的结构特点(1)碳原子之间以单键相连,形成链状或环状结构。
(2)每个碳原子都与四个原子相连(对于链状烷烃,通常是三个氢原子和一个碳原子;对于环烷烃,与两个碳原子和两个氢原子相连)。
4、饱和烃的通式(1)链状烷烃的通式为 CnH2n+2。
(2)环烷烃的通式为 CnH2n。
5、饱和烃的物理性质(1)状态在常温常压下,C1-C4 的烷烃为气态,C5-C16 的烷烃为液态,C17 及以上的烷烃为固态。
(2)溶解性饱和烃一般难溶于水,易溶于有机溶剂。
(3)密度随着碳原子数的增加,饱和烃的密度逐渐增大,但都小于水的密度。
(4)沸点和熔点饱和烃的沸点和熔点随着碳原子数的增加而升高。
6、饱和烃的化学性质(1)稳定性饱和烃通常比较稳定,不易与强酸、强碱、强氧化剂等发生反应。
烷 烃

1.了解烷烃(饱和烃)及其结构特点。
2.了解烷烃的物理性质及其规律。
3.了解烷烃的化学性质。 4.了解烷烃的通式和名称。
5.理解同系物及同分异构体。
从石油炼制的产品中可以获得一系列和 甲烷结构相似的化合物,如
乙 烷 丙 烷
丁 烷
部分烃的结构式
思考交流以上烃的结构式,试归纳以上烃的结构特点。
省略C—C键
观察烷烃的物理性质,并归纳其规律?
常温 时的 状态 气 气 气 气 液 熔点 /℃ -182.5 -182.8 -188.0 -138.4 -129.7 沸点/ ℃ -161.5 -88.6 -42.1 -0.5 36.0 0.5005 0.5788 0.5572 相对 密度 水溶 性 不溶 不溶 不溶 不溶 不溶
它们在组成上的规 律及其区别
结论
烷烃在分子组成上都符合通式CnH2n+2 ; 分子上相差了一个或若干个CH2原子团。
像这种结构相似,在分子组成上相差一
个或若干个CH2原子团的物质互称为同
系物。
观察下列三种烷烃,试推测是根据什么来命名烷烃的?
C2H6
C3H8
C4H10
结论
根据碳原子的个数来命名:(习惯命名法)
总结
以上烃的结构特点:
1.碳原子间都以C—C键相连、其余都是C—H键; 2.碳原子都形成4个共价键,形成四面体结构; 3.碳链可以转动。
像这种碳原子之间都以碳碳单键结合成链状,剩余价键均与 氢原子结合,使每个碳原子的化合价都达到“饱和”状态。 这样的烃叫做饱和烃,又叫烷烃。
通过我们刚才认识的有机物可以发现有
C
H
C
H
H
H
C
H C H
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
饱和烃的结构和性质
饱和烃是指分子中只含有碳和氢,碳原子之间的化学键都是单
键的化合物。
饱和烃可分为烷烃和环烷烃两大类,其中烷烃分子
中只包含直链或支链的碳链,而环烷烃则包含了一个或多个碳环。
这些化合物在自然界中普遍存在,如石油和天然气中含有大量的
饱和烃,其化学性质主要是烷烃和环烷烃之间的分子量差异,长
链的分子量会比短链的分子量更大,同时在同一种分子量下,支
链烷烃的沸点也比直链烷烃的沸点低。
烷烃的结构和性质
烷烃的分子结构是由碳原子链构成的,每个碳原子上都与四个
其它原子(其中一个是氢原子)连接。
这种化学键称为单键,通
过这种单键链可以形成不同长度的直链链烷烃。
此外,由于碳原
子能够在空间上自由旋转,这种链烷烃的分子也可以通过碳原子
之间的旋转来改变的,产生的结构就是所谓的支链烷烃。
烷烃分子中每个碳原子上都有2个可能的氢原子位,因此线性
烷烃分子的数目很大。
其中,最简单的是甲烷(CH4)和乙烷(C2H6),它们的分子式分别为CH4和C2H6。
甲烷是一种无色、无味的气体,燃烧时能够发生强烈的火焰,而乙烷则具有明显的气味。
此
外,随着碳原子数量的增加,烷烃分子的物理和化学性质也在逐
渐发生着变化。
长链烷烃分子的熔点和沸点一般比较高,这是因为长链烷烃分
子之间的范德华力较强,分子之间吸引力度随分子量的增加而增强,因此大分子量的烷烃会出现固态、液态、气态三态平衡,其
沸点逐渐升高。
此外,直链烷烃分子之间的相互作用力会比支链
烷烃大,因此支链烷烃往往比直链支链烷烃的沸点低。
环烷烃的结构和性质
环烷烃是包含一个或多个碳环的烷烃,是一类由相邻的碳原子
单键组成的环状分子。
环烷烃中的环越大,则其相对稳定性越高。
六元环状的烷环烃最为稳定,如正己烷(C6H14)就是一种典型
的烷环烃。
同时,环烷烃有一个特点,它们分子内的碳——碳键、碳——氢键倾向于来回转动,从而使环内碳原子的键价能量特别
稳定。
环烷烃由于分子内强烈的形成屏障而难于引发反应,因此环烷
烃的反应活性比同分子量的非环烷烃要低。
此外,环烷烃由于分
子内部的周转结构,也比同分子量的非环烷烃要难挥发,如正环
己烷的沸点是光穴己烷的一倍以上。
总结
饱和烃的结构和性质是比较简单的,但是其却是有很大的应用
前景,在润滑油,燃料方面的应用十分广泛。
油试验学、燃料方
面的应用,饱和烃的应用前景令人期待。
由于一些技术原因,我
们的石油90%以上是由饱和烃构成的,可以说,在我们的生活中,饱和烃是无处不在的。
这使得对饱和烃的了解显得越来越重要。
