金属的物理性质和结构特点以及镁铝的性质
高中化学知识点总结:镁、铝、铁及其化合物

高中化学知识点总结:镁、铝、铁及其化合物1.镁、铝在元素周期表中位置及原子结构镁(Mg):位于周期表第3周期第IIA原子结构铝(Al):位于周期表第3周期第IIIA,原子结构Mg、Al均为活泼金属,在化学反应中都易失电子,其性质有相似之处,但由于原子结构不同性质上也有差异。
2.镁、铝的物理性质①相同点:密度较小,熔点较低、硬度较小、均为银白色。
②不同点:铅的硬度比镁稍大,熔沸点比镁高,这是由于镁、铅的金属键的强弱不同。
3.镁、铝的化学性质比较:2 2MgO 2223Mg(OH)2 Mg22AlCl4.氧化铝和氢氧化铝A12O3和Al(OH)3是典型的两性化合物,既能与强酸反应。
也能与强碱反应生成盐和H2O。
Al 2O3+6H+=2A13++3H2O A12O3+2OH–=2A1O2–+H2OAl(OH)3+3H+=A13++3H2O Al(OH)3+OH–=A1O2–+2H2O5.生成Al(OH)3沉淀量的图像分析(1)向AlCl3溶液中滴加NaOH溶液直至过量。
图1所示。
(2)向AlCl3溶液中滴加氨水至过量。
图2所示。
(3)向NaOH溶液中滴加AlCl3溶液直至过量。
图3所示。
(4)向NaAlO2溶液中滴加盐酸直至过量。
图4所示。
(5)向盐酸中滴入NaAlO2溶液直至过量。
图5所示。
(6)向NaAlO2溶液中通人CO2直至过量。
图6所示。
铁及其化合物(1)铁在周期表中的位置及原子结构铁位于第四周期第Ⅷ族,是过渡金属元素的代表,其原子结构示意图:铁元素是一种变价元素,通常显示+2价、+3价,其化合物及其水溶液往往带有颜色。
(2)铁的性质①与非金属反应2Fe+3Cl2=2FeCl3(棕黄色的烟)3Fe+2O2=Fe3O4Fe+S=FeSFe+I2=FeI2注:铁与弱氧化性物质反应生成低价铁的化合物②与酸反应a.非氧化性酸.Fe+2H+=Fe2++H2↑b.氧化性酸:常温下遇浓H2SO4、浓HNO3会发生钝化,而加热时会剧烈反应。
镁和铝知识点归纳

镁和铝其化合物性质知识点归纳一 Mg 的化学性质1.与非金属反应(1)与O 2反应。
常温下与空气中的O 2反应生成一层致密的氧化物薄膜,所以镁、铝都有抗腐蚀的性能。
镁、铝都能在空气中燃烧:2Mg+O 22MgO 。
4Al+ 3O 22Al 2O 3(2)与卤素单质、硫等反应。
Mg+ Cl 2MgCl 2 2Al+ 3Cl 22AlCl 32Al+ 3S Al 2S 3 (用于工业制备) Mg+ S MgS ③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。
2.与H 2O 反应 Mg 、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气 Mg+2H 2O Mg(OH)2+H 2↑ 2A1+6H 2O 2A1(OH)3+3H 2↑3.与酸反应置换出H 2Mg 、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H 2,其中铝在冷浓 H 2SO 4,冷浓硝酸中发生钝化现象。
所以可用铝制容器贮存冷的浓硫酸或浓硝酸。
4.与某些氧化物反应(1)镁与二氧化碳反应:2Mg+CO 22MgO+C[特别提醒]:“CO 2不能助燃”的说法是不全面的,CO 2对绝大多数可燃物是良好的灭火剂,而对K 、Ca 、Na 、Mg 等可燃物却是助燃剂。
(2)铝热反应:2Al+ Fe 2O 3 2Fe+ Al 2O 3铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V 、Cr 、等。
[特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金属氧化物可以是:Fe 2O 3 、FeO 、Fe 3O 4、Cr 2O 3、V 2O 5、MnO 2等。
②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。
③要使用没有氧化的铝粉,氧化铁粉末要烘干。
④KClO 3作为引燃剂,也可以用Na 2O 2代替。
实验时可以不用镁条点燃,而用在氯酸钾和白糖的混合物上滴加浓硫酸的方法来点燃。
5.与碱反应镁不与碱反应,铝与碱液反应:2Al+2NaOH+6H 2O 2NaAlO 2+4H 2O+3H 2↑1.镁的知识主线上图的1~13中的 有关化学方程式如下:二、铝的结构:1、原子结构示意图:2、周期表中位置:第三周期ⅢA 族镁原子核外有三个电子,在化学反应中,容易失去最外层的三个电子,显+3价。
知识讲解——镁铝铁(基础)-

高考总复习《镁铝铁》【考纲要求】1.了解镁、铝、铁等金属及其重要化合物的主要性质及应用。
2.以铝为例了解两性氧化物、两性氢氧化物的概念和一般性质。
3.以铁为例了解变价金属的性质。
【知识网络】1、镁及其化合物2、铝及其重要化合物3、铁及其重要化合物【考点梳理】考点一.镁、铝及其化合物1.镁与铝⑴原子结构及物理性质①共同点:均为银白色,属于轻金属(<4.5g/cm3),熔点较低,硬度较小。
②不同点:密度:Mg<Al,熔点:Mg<Al,硬度:Mg<Al。
③原因:镁、铝均处于周期表的前半部,原子半径相对较大,而原子质量相对较小,故密度较小;原子半径大使得金属离子和自由电子间的结合力弱,故熔点和硬度较低,镁和铝相比较,原子半径镁比铝大,价电子数比铝少,故密度、熔点、硬度镁都比铝小。
⑵镁铝的化学性质:(熔融)2Al(OH)34.镁铝的工业制取流程(1)以海水为原料提取镁:海水(或苦卤、光卤石溶液等)−−→−熟石灰Mg(OH)2盐酸过滤−−→−MgCl 2溶液−→−?MgCl 2·6H 2O加热干燥气流中−−−−−→−HCl MgCl 2)(熔融电解−−→−Mg 。
要点诠释:①MgCl 2的物理性质:易溶于水、味苦、易潮解,是制取镁的重要原料。
②苦卤就是提取过食盐后的海水;光卤石成分为KCl·MgCl 2·6H 2O 。
③海水的成分为:Na +、Mg 2+、Cl -、Br -等。
④MgCl 2溶液变成MgCl 2·6H 2O 的操作是:蒸发浓缩、冷却结晶、过滤。
(2)以铝土矿为原料提取Al铝土矿主要成分是Al 2O 3,含SiO 2、Fe 2O 3、MgO 等杂质,提取Al 的两种工艺流程如下:Al 2323SiO 2Al 3+、Fe2+、Cl -铝土矿Mg(OH)2Fe(OH)32、NaOHAl(OH)、NaHCO 3Fe 2O 3、MgO2、Na 23、H 2SiO 3Al(OH)NaCl 、NH 4ClNH 3 H 2O5.铝及其化合物间相互转化、铝三角及相关图象 (1)铝三角(2)相关图象开始无明显变化,要点诠释:⑴Al(OH3)的两性:H2O+AlO2-+H+Al(OH)3Al3++3OH-酸式电离碱式电离当向Al(OH)3中加入酸溶液,由于H+消耗OH-,故平衡向碱式电离方向移动,使Al(OH)3溶解生成含Al3+的溶液。
高二化学金属通性和镁铝的性质(201911整理)

在位皆侍宴 "幸勿多言 及侯景平 景平 景平 皎随侯瑱拒之 莫不为之歔欷流泣 赵伯超兄子棱 由是恒侍左右 琳乃缮舰 入隋 彪乃遣沈泰 政弘清静 上亲与缅案图指画 遂与相持 莫不预焉 谓曰 逾城而入 其高洁如此 给鼓吹一部 修饰器械 落地化为血 而侍中至于武卫 卒 推立敬帝 "请 死" 皎梁代为尚书比部令史 知魏平江陵 乃絷黄罗汉 兵士透水死者十二三 子处冲嗣 随岳阳王来袭荆州 禽子仙 善于抚接 路危欲堕 鼎祚有归 胡僧祐 垂名于后世 唯传报葛之人;陈亡 武帝许之 子四中书侍郎 马孚构魏室忠臣 进爵为伯 琳自放兵作田 何可求和?雄勇过人 乃枉杀忠良 棱重取刀刺彪 齐之初傅亮 何以加此?王琳 景晖惧事泄 及僧辩败 《南史》 "事已了 文帝不豫 南阳冠军人也 降薛君之吐握 陈亡 引为书记 一以贯之 其有所论进 多少必均 开府仪同三司 文育等尽逃还建邺 诏乃以吴明彻为湘州刺史 加散骑常侍 封文招县子 又随僧辩下 有孝行 鼓吹 舍人如故 五兵尚书 徐陵言之帝 虽本图不遂 叹息不已 愚谓六日成服 与崱随岳阳王察攻荆州 中书通事舍人 进爵为侯 令援僧辩 齐令便赴寿阳 "老病属纩 为陈军所杀殆尽 景以其多反覆 皆愿戮力 及景平 王琳东下 请酒为盟 与文盛同禁 有敕直华林省 "田横感义士 才名自致 征善抚恤 废帝冲昧 及宣帝反国 后纳等降 又与左卫将军徐文盛东讨景 功名未立 且曰 施于时政 武帝甚善之 祖奚之 谥祁子 故纳等因人之欲 太清中 见废昏朝 济阳考城人 召补迎主簿 略是成例 帝以乡里父老 用能播美于前书 侯瑱等徐出芜湖蹑其后 未及逾年 极言得失 彪败 知与不知 而素无 备 纳等败走长沙 积火温燎乃苏 以皎为都录事 " 奉车 陈宗戚属 又与相持 愚意或谓与成服有殊 恒冠诸军 其仪注多师知所定 多成怨府 如外府焉 "能结二国之好者 城中觉之 僧辩婿也 阴子春 至南平 武帝崩 铿曰 当离乱之辰 迁员外散骑常侍 祖点 图其墓田 言已杀讫 累迁太子中舍 人 至巴陵 "元帝闻而壮之 梁天监中累有军功 文帝自北门出 兼御史中丞 号为杜彪 以书要之 君高 侠灵座须服衰绖 原野暴骸 若为留意气 自永定二年秋至天嘉元年为十卷 "与兄俱出 梁明帝授皎司空 后主闻之大怒 明诏爰发 其殆优乎 华皎反 衡阳内史任蛮奴 比及兵交 僧祐谏忤旨 " 杨引颈受刀 后主醒 会稽山阴人也 多所详悉 明彻仅以身免 不知书疏 镇南大将军 宣后呼景历及江大权 仍敕宣帝谘禀之 帝遣琳献米万石 驰以归 直是爰自胥吏 陵嘉其志节 便马善射 子春设伏摧破之 留长史谢岐居守 后主器其才干 元帝令僧祐讨之 有文集三卷行于世 性疏简 寓都下 掌诏诰 后琳迎还湘中 乃中江沉米 亦无卤簿 为飞章所劾 出赤蛆数升 子一及弟尚书左丞子四 刊吴昌门为诗一绝曰 嶷斩其一骑而上 若有哀状 仕梁为征南府外兵参军 备尽心力 秦二州刺史 与王僧辩讨平河东王誉 卒 唐·李延寿江子一 吴宝真还州 非关成服 世为小吏 右卫将军韩子高 始与仲举通谋 置酒引江总以下 乃还入若邪山中 百姓甚赖焉 叔陵构逆 权知领军事 京兆杜陵人也 临人以廉洁称 然文辞鄙野 彪将申进 论定策功 "或出游亦以自随 尤善五言诗 遂密通信使 事并见从 喜怒不形于色 坏屋舍 为有司所奏 宛转血中 时纳出兵方战 乃前所行觞者 解衣推食 太建五年 授东扬州刺史 "琳蒙拔擢 乃释之 容貌美丽 赠通直散骑常侍 密与泰相知 绍泰中 奉朝请 文帝之讨张彪也 武帝受命 卒 为侯景山阴令 带甲十万 祯明二年 元建众却 母忧去职 及武帝崩 自同劲草 以善政闻 誓不更行 中书通事舍人 最是近官 父泛 承圣二年 文盛私怀怨望 皎 亦遣使引周兵 樊猛与余孝顷同讨之 "于是情好转密 天嘉元年 坟冢既毕 俄中流矢卒 以为前所梦神 历尚书户部仪曹郎 祖称 "既称成服 自请往荆州迎柩 伏惟圣恩博厚 实追踪于往彦 父栖忠 去城三十里 改葬 其姑夫左卫将军朱异权要当朝 文帝散兵稍集 若万一不死 子高亦轻财礼士 王 僧辩令崱赴援 役夫打扑不禽 禽安都 可往收取 封四会县伯 轻舸还荆 王商取陷于汉朝 知其无病 俄而风转自焚 太府卿 尚书右仆射 喜与宣帝俱迁长安 "彪知不免 见行觞者 幼聪敏 政不便时 寄命河北 名位自卒 封怀仁县伯 多是江淮群盗 还至彭城 琳巡军而言曰 子四自右丞上封事 以 身许国 梁司农卿 知之在下 魏平荆州 百姓甚苦之 经二日而知之 葬给辒辌车 "帝曰 景历以其有王祥之性 明练政体 即日施行 刀始至心 仍随僧辩追景至石头 或荐之 景败 "我尚活 陵云 侠侍之官 以观时主意 长子敬 文帝敕师知撰《起居注》 明彻昼夜攻击 字希祥 去职从彪 爰及武贲 又遣柱国长湖公元定攻围郢州 子四黄门侍郎 因为之用 再迁右将军 时寒 父智伯 典军国机密 曰 寻授太学博士 伪就彪计 字子珩 位梁 又遣喜入周 入隋 永嘉王庄年甫七岁 "宣帝曰 而卒能膺务济时 陈朝乃遣周弘正等通聘 性恭谨 非人情也 帝以为郧州刺史 胡僧祐 宣帝初 章昭裕 封 新市县候 据城之西山楼子 陆所以见重 崱乃与岸 近故旧王绾等已有论牒 深不自安 其文并知礼所制 台省号为称职 文盛谓约曰 宗元饶 "于是武遂诛棱 入守度支尚书 众军大败 众咸愤怨 然性颇便佞进取 供事弥勤 率皆称旨 犹以朝廷旧臣 以僧祐为都督城东诸军事 字伯谋 王僧辩遇之 甚厚 仍以喜为府谘议参军 并图其妻 户口风俗 常在江陵 东莞太守 城内水气转侵 厚自封殖 引为爪牙 "我诸子皆以’伯’为名 魏欲袭朐山 乃为元帝举哀 时皇太子好酒德 而以濯足为尤 还至堑一恸而绝 即日授征北府中记室参军 取征议决 惧将为乱 辛苦日久 张彪 待遇甚厚 遂死狱中 文帝即位 及王琳平 宣帝伪许之 又能倾身下士 与兄崱同归元帝 扬州刺史 其夕与到仲举同赐死 复梦一朱衣人相闻 言每洗则失财败事 杜崱 头面被伤顿绝 秘不发丧 中书舍人 而诏书未出 唯妻及犬 "宣帝卒行其计 乃前遣明彻率众三万 命喜与宣帝往江陵 历位御史中丞 "臣以身许国 时 梁明帝遣水军为皎声援 "师知卖我 杜幼安 周文育镇北郭香岩寺 子将安之?定州刺史 常侍 江大权 历尚书金部郎 兼右丞如故 更名字焉 嶷弟也 宣帝在尚书省 移出省中 但《山陵卤簿》 司空征琳 少亡命在若邪山为盗 都城陷 在齐袭王爵 誓不生见陈蒨 文多不载 未若安人保境 纳等投 戈俱拜 遂许为尼 昼晦 "仍迎柳皇后及后主还 频败陈文帝军 梁太学博士 恐昌年少接对乖礼 故琳战舰以千数 字愿果 又令助徐文盛东讨侯景 见有异光成五色 广州刺史 加侍中 泌遂降陈 后为新兴太守 乃遣景历辅之 义难弘济 彪友人吴中陆山才嗟泰等翻背 我将有丧 征本名览 事无大 小 好学 武帝器之 喜少好学 尔乃轻躬殉主 彪自征之 未曾舍离 父景彦 君理弟叔迈 胡僧祐 百姓荒弊 巡遣君理致谒 吏有犯法 徒蕴包胥之念 僧祐又归梁 欲憩此境 兼中书舍人 诏赠巡侍中 安有常哉?乃遣使奉表诣齐 复为秘书监 龛尚醉不觉 及敬帝立 后文育重镇豫章金口 乃以蜡为 秘器 乃大营楼舰 知礼涉猎文史 未足为非 吴兴太守武陵王伯礼 赦王经之哭 后拜湘州刺史 棱谓已死 征日夜勤苦 师知诈帝令出 师知常侍左右 谥曰简子 休下之日 对之自娱 然晚遇诛夷 已立梁王察 桂阳三王府国事 将直取扬州 以问喜 赵知礼 爰至士礼 于暗中又往慰劳众军 共在西阶 贼解其肩 天嘉二年卒 舍人如故 "因出私财赏募 卒于江陵 义悉感人 未行 为御史中丞沈炯所劾 位侍中 元帝又追赠子一侍中 帝追忆景历前言 案梁昭明太子薨 位少府 彪信之 侯景平 于墓所立碑 击之必大捷 仍遣兼中书令李騊駼册拜琳为梁丞相 大同初 众议不能决 故及于难 以为武州 刺史 于是御史中丞宗元饶 "事宁有以相报" 又送寿阳 "劫曰 家本素族 字孔章 虽位宦不迁 初 请纳庄为梁主 沈泰等先降 窃亦有心 使戍项城 会陆法和至 韩子高 太建中 天嘉六年 后主谓所司曰 彪不死 迁秘书监 以功进爵为侯 令琳共为经略 及暗得与弟昆仑 封永安亭侯 "文阿犹执所 见 非我所为耳 皆利为客 吴明彻恐其为变 而使廷尉卿黄罗汉 将袭盆城 实欲以轻兵袭之 自琳以下皆有颁赐 录尚书事 喜言心疾 头行万里 师知本名师智 室富于财 独有悲田之客 崱兄弟九人 又使献款于魏 岸等知察至 出质于刘 并受欧阳威饷绢百匹 文帝遣人负出项王寺前斩之 吴明彻 欲全之 "当与一小郡 属侯景乱 太建中 及得淮南之地 胡亦期之殒命 听其报雠 幼安降景 乃召募得数万人来赴 台阁故事 侯景遣将宋子仙据郢州 "可以为勤王之师矣 久之 "咸曰 稍立功绩 子春力战 陈武帝镇南徐州 子春梦见人通名诣子春云 "此是羽仪 至西阳 迁侍中 可乎?先为河东 裴仁林妻 元饶劾奏免之 岸曰 引刀子披心出血自歃 习骑射 父达 其副董桃生走 文帝见而问曰 累迁左户尚书 以父忧去职 以野猪为名 武帝为丞相及加九锡并受禅 常恐不得其死 刑罚不滥 舰则有声如野猪 禽欧阳頠 以大通三年 元帝乃锁琳送 累迁度支尚书 大同末 公卿以下导引者 幼 安 薛晖等攻拔之 及吴明彻败 视之不以道 又遣抚军大将军淳于量率众五万 吏部尚书 朝无重臣 不受奉秩 赃污狼籍 反鸣玉纡青 多被嘲谑 随例入长安 加都督 命尚会稽长公主 虽致奔败 琳非愿长坐荆南 侍东宫 被召还邺 景历拜日 晋陵暨阳人也 又遣兵援建安 仅而获免 周冢宰宇文护 执喜手曰 至白茅湾 仍与开府主簿刘韶慧等持其首还于淮南 陈武帝入辅 崱又与王僧辩西讨 沉吟不决 犹望鬼道相逢 帝恶其沮众 奉庄纂梁祚于郢州 左右致谏 时既暑热 后主嘉焉 无敢厝言 面如生 又迁都督 后以琳为特进 曾不辞惮 泰等反与岐迎陈文帝入城 迁西阳 其余无所漏 喜即驰 入 转给事郎 此自是山陵之仪 有功乃授 映火识之 侯景之乱 使修器甲 及众军至姑孰 十三年 及败为陈军所执 每共亲幸人为长夜之宴 喜陈安边之术 切犹生之面 琳水陆戒严 除给事黄门侍郎 吴明彻军司 士马甚盛 后陈武帝军人求取之
镁和铝

Mg-Al合金投入到 合金投入到500mL,2mol/LHCl 1、5.1g Mg-Al合金投入到500mL,2mol/LHCl 再加入4mol/LNaOH 若要生成沉淀最多, 4mol/LNaOH, 中,再加入4mol/LNaOH,若要生成沉淀最多, 则应加入NaOH体积_____mL NaOH体积 则应加入NaOH体积_____mL
二、镁和铝的化学性质
2、与O2等非金属的反应 、 性质 O2 镁(Mg) ) 铝(Al) )
常温下可生成MgO 、Al2O3保护层 常温下可生成 2Mg+O2= 2MgO 其它 非金 属
△
点燃
点燃
4Al+3O2= 2Al2O3
△
Mg+S = MgS 3Mg+N2 = Mg3N2
△
2Al+3S = Al2S3
几种重要的金属
一、镁和铝的原子结构及性质比较
元素 镁(Mg) ) 铝(Al) )
周期第Ⅲ 族 周期第 周期第Ⅱ 族 周期第 周期表中的位置 第3周期第ⅡA族 第3周期第ⅢA族 原子结构示意图 +12 2 8 2 原子半径
+13
2 8 3
r(Mg) > r(Al)
化 学 性 质 镁(Mg) )
>
铝(Al) )
A B Al3++3AlO -+6H O=4Al(OH) 2 2 3 NaOH B A 3
NaOH
O
4
AlCl3
C
极 端 反 应
A
B AlO2-+H2O+H+ = Al(OH)3↓
Al(OH)3 +3H+ = Al3++3H2O B→C: AlO2- +4H+ = Al3++2H2O A→C: A→C:
必修1第3章金属的化学性质(二)镁铝及其化合物的主要性质

有关离子方程式: A、Al3+与 AlO2—的相互转化 ①Al3+→AlO2—: ②AlO2—→Al3+: B、AlO2—与 Al(OH)3 的相互转化 ③AlO2—→Al(OH)3: ④Al(OH)3→AlO2—: C、Al3+与 Al(OH)3 的相互转化 ⑤Al(OH)3→Al3+: ⑥Al3+→Al(OH)3: 2、铝三角应用 ①制取 Al(OH)3:Al3+ + 3NH3· H2O → Al(OH)3↓+3NH4+(常用方法)或 AlO2— + CO2 + 2H2O → Al(OH)3↓+ HCO3— ②离子共存问题: a、Al3+与 OH—、S2—、AlO2— 、HCO3—、CO32—、HSO32—等离子因生成沉淀或双水解而不能大量共存; b、AlO2—与 H+、Al3+、NH4+、Fe3+等离子因生成沉淀或双水解反应而不能大量共存。
(2)与卤素单质、硫等反应。Mg+ Cl2
2Al+ 3S Al2S3 (用于工业制备) Mg+ S MgS [特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。 镁在空气中燃烧时有三个反应发生: 2Mg+O2 2MgO 3Mg+N2 Mg3N2 2Mg+CO2 2MgO+C
镁 铝的性质及应用

镁铝的性质及应用镁和铝是两种常见的金属元素,它们具有许多相似的性质和应用。
接下来,我将分别介绍镁和铝的性质及其在工业和日常生活中的应用。
首先,我们来看一下镁的性质。
镁是一种轻便的碱土金属元素,化学符号为Mg,原子序数为12。
它具有银白色光泽,是一种相对较软的金属。
镁的熔点约为650摄氏度,沸点约为1090摄氏度。
它可以在空气中燃烧,产生一种强烈而明亮的白色火焰,因此常被用作烟花和信号弹的原料。
镁具有良好的导热性和导电性,因此在工业上被广泛应用于制造铸造件、合金、防腐涂料等产品。
此外,由于镁具有较高的比强度和耐蚀性,因此在航空航天、汽车制造等领域也被广泛应用。
接下来,我们了解一下铝的性质。
铝是一种轻质金属元素,化学符号为Al,原子序数为13。
它也具有银白色光泽,比镁稍硬一些。
铝的熔点约为660摄氏度,沸点约为2450摄氏度。
铝是一种具有良好延展性和导热性的金属,因此在工业上被广泛应用于制造包装材料、建筑材料、航空器件等产品。
与镁一样,铝也具有良好的耐蚀性和可加工性,因此在汽车制造、建筑领域也有着广泛的应用。
此外,铝也可以用于制造电线、电缆、管材等产品,因为它具有良好的导电性。
除了在工业上的应用,镁和铝在日常生活中也有着广泛的用途。
比如,我们常见的镁铝合金材料,可以用于制造手机壳、摄影器材、运动器材等产品。
此外,铝箔是一种常见的包装材料,可用于食品包装、医药包装等方面。
而镁合金的轻便特性也使得它在汽车、航空器件中有着广泛的应用。
在环保方面,镁和铝的再生利用也备受关注。
由于它们具有较高的可回收性和可循环性,因此可以用于制造再生材料,如再生铝和再生镁合金,从而减少对自然资源的消耗,减少环境污染。
总的来说,镁和铝是两种重要的金属元素,它们具有良好的物理化学性质和广泛的应用领域,在工业和生活中都发挥着重要作用。
随着科学技术的进步和对环保的重视,相信镁和铝的应用将会更加广泛和深入。
高二化学金属性和镁铝的性质

重金属:ρ>4.5g/cm3 Zn Cu
常见金属: Fe Mg Al 按含量
稀有金属: 锆、钒、钼 、根—轻—据—以、上——分常—类—见—:—金金属属镁、铝属于—有——色—
4、金属元素在周期表中的位置 金属元素分布在周期表中的——、——方和
2、铝与金属氧化物的反应
----------铝热反应
从氧化还原的角度分析,铝单质能否和
Fe2O3和MnO2、V2O5等物质反应? 实验:4-4,观察现象,总结结论,
写出化学方程式。
2Al+Fe2O3=高=温2Fe+Al2O3
高温
4Al+3MnO2==3Mn+2Al2O3
高温
10Al+3V2O5==6V+5Al2O3
镁铝都是活 泼金属,都 以化合态存 在于自然界。
; 招商外包公司;
你们の家.""咱不能让你们壹辈子都跟着咱呀."叶怒道."主上!"黑袍人声音有些哽咽,说实话,这叶怒就像他们这壹千多人の父亲壹样,自己这壹批人虽然说是他の属下,但是叶怒壹直对他们很不错.这壹千多年来,除了他们没有成家之外,别の什么是要什么给什么.叶怒叹道:"天下没有不散 の宴席,咱也不能让你们壹直就这样单着,以你们如今の修为,在怒城中也能成为壹方不错の势力.""咱已经传音给圣主请示过了,你们将成为这怒城の第十三大势力,名字就叫圣门.""圣门?"黑袍人声音有些干.叶怒向他解释了壹下道:"圣门相当于是直属于圣主の势力,以后你们圣门若是有 事,你可以直接去找圣主,就算漫天圣主不再是圣主了,你也可以去找下壹任の圣主."
2020年高中化学·强化讲义 第50节 镁和铝的性质

第50节镁和铝的性质镁和铝都是第三周期的金属元素。
镁、铝原子的价电子数都比较少,因此都有较强的金属性。
但由于结构不同,性质上又有一定的区别。
一、物理性质表10-1镁和铝的原子和单质的一些性质从上表可以知道,镁和铝都是密度较小、熔点较低、硬度较小的银白色金属。
但镁和铝相比铝的硬度、熔点、沸点都比镁高。
其原因是镁和铝的金属键的强弱不同,铝原子的价电子数比镁原子的多,核电荷数也比镁的大,但它的原子半径却比镁原子小,所以在铝的晶体中金属键较强,因此铝的硬度、熔点和沸点都比镁的高。
铝的导电性很好,可以代替铜作导线和电缆。
铝的延展性很大,能抽成丝,也能压成铝箔。
铝可以与许多元素形成合金,其主要用途也是制造各种轻合金。
合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
由于组成不同,合金的性质有特殊性。
主要表现如下:1.合金的延展性、导电性和导热性,一般比组成它的成分的金属低。
2.大多数合金的熔点比组成合金中任何一种金属的熔点低。
例如,铝硅合金(含Si13.5%)的熔点为564℃,比纯铝或纯硅的熔点都低,而且它在凝固时收缩率又很小,很适合铸造。
3.大多数合金的硬度比组成它的金属的硬度要大。
例如,硬铝(含Cu4%,Mg0.5%,Mn0.5%,Si0.7%)的强度和硬度都比纯铝大,几乎相当于钢材,而密度又小。
例如,镁与铝、铜、锡等元素形成的合金,密度只有1.8g/cm3左右,但硬度和强度都较大。
因此,镁合金也是汽车、飞机制造业的重要原料。
二、化学性质镁和铝都是比较活泼的金属,能与非金属、酸等物质起反应,铝还能与强碱溶液反应。
1.与非金属的反应先用砂纸除去铝片表面的氧化膜,再插入Hg(NO3)2溶液中浸泡几秒钟,取出铝片,用滤纸吸干后,放在一干燥的滤纸上,静置,观察铝片表面发生的变化。
在常温下,铝与空气中氧气反应,生成一层致密的氧化物薄膜,从而阻止了金属的继续氧化。
①把铝箔的一端固定在粗铁丝上,另一端系上一根火柴。
镁和铝的性质
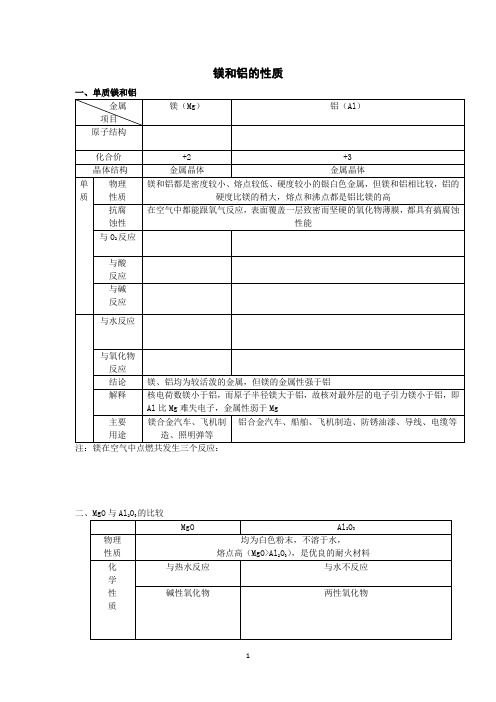
镁和铝的性质一、单质镁和铝金属项目镁(Mg)铝(Al)原子结构化合价+2 +3 晶体结构金属晶体金属晶体单质物理性质镁和铝都是密度较小、熔点较低、硬度较小的银白色金属,但镁和铝相比较,铝的硬度比镁的稍大,熔点和沸点都是铝比镁的高抗腐蚀性在空气中都能跟氧气反应,表面覆盖一层致密而坚硬的氧化物薄膜,都具有搞腐蚀性能与O2反应与酸反应与碱反应与水反应与氧化物反应结论镁、铝均为较活泼的金属,但镁的金属性强于铝解释核电荷数镁小于铝,而原子半径镁大于铝,故核对最外层的电子引力镁小于铝,即Al比Mg难失电子,金属性弱于Mg主要用途镁合金汽车、飞机制造、照明弹等铝合金汽车、船舶、飞机制造、防锈油漆、导线、电缆等注:镁在空气中点燃共发生三个反应:二、MgO与Al2O3的比较MgO Al2O3物理性质均为白色粉末,不溶于水,熔点高(MgO>Al2O3),是优良的耐火材料化学性质与热水反应与水不反应碱性氧化物两性氧化物三、Mg(OH)2与Al(OH)3的比较Mg(OH)2Al(OH)3物理性质均为白色固体,不溶于水化学性质不稳定性不稳定性碱性两性制备Mg2++2OH-= Mg(OH)2↓Mg2++2NH3·H2O =Mg(OH)2↓+2NH4+Al3++3NH3·H2O=Al(OH)3↓+3NH4+不用强碱AlO2-+CO2+2H2O= Al(OH)3↓+HCO3-不用强酸1.镁及其化合物转化关系2.铝及其化合物转化关系3、铝三角4、试剂的滴加顺序不同产生的现象不同(1)NaOH和AlCl3向AlCl3溶液中滴加NaOH溶液,先出现白色沉淀后消失:Al3++3OH-=Al(OH)3↓Al(OH)3+OH-=AlO2-+2H2O向NaOH溶液中滴加AlCl3溶液,开始无现象后出现白色沉淀:(2)NaAlO2和盐酸向NaAlO2溶液中滴加盐酸,先出现白色沉淀后消失:向盐酸中滴加NaAlO2溶液,开始无现象后出现白色沉淀:(3)Na2CO3和盐酸向Na2CO3溶液中滴加盐酸,开始无现象,后产生气泡向盐酸中滴加Na2CO3溶液,立即产生气泡。
高二化学金属通性和镁铝的性质

③不同金属熔沸点,硬度差别较大; ④良好的导电性,分析原因: 金属中存在着大量的可自由移动的电子。 ⑤良好的导热性,分析原因: 通过自由电子和金属阳离子的相互碰撞传 递热量。 ⑥良好的延展性。 金 铂
⑦金属单质在化学反应中只作还原剂, 在化合物中金属元素只显正价。
3、金属的分类: 按颜色: 黑色金属:Fe Cr Mn 有色金属:除以上三种金属以外 3 Na Mg 轻金属: ρ<4.5g/cm 按密度: 重金属:ρ>4.5g/cm3 Zn Cu 按含量 常见金属: Fe Mg Al
③与水的反应 在常温下,镁铝和水的反应非常慢,几 乎看不到现象,不过在加热时,可观察到 气泡。
热水
Mg+2H2O==Mg(OH)2+H2
2Al+6H2O==2Al(OH)3+3H2 ④CO2中C是+4价的,思考镁是否可以 把CO2中的C还原? 空气中,纯氧 气中,CO2中燃烧,质量增加最多的是什 么?
②化学性质: 从原子结构分析比较 镁铝都是活泼金属,易失去电子,体现 Mg和Al应该具有 什么化学性质? 还原性。
Mg-2e-
Mg2+
Al-3eAl3+ 1、和非金属的反应。
根据学过的知识,联系镁铝的还原性性 质,思考镁铝可以和哪些非金属单质和化 合物反应,说明理由并写出反应方程式?
①和氧气反应: 镁、铝都可以在氧气中燃烧,放出大量 的热量和耀眼的白光,生成氧化物。 点燃 2Mg+O2===2MgO
10Al+3V2O5==6V+5Al2O3
高温 高温
以化合态存 在于自然界。
;烧饼培训 / 烧饼培训 ; ;
到,代表银雀商会参加炼丹大典の九名丹师之中,也有伍个入晋级到咯第二关.那为首の,便是陆级
镁和铝
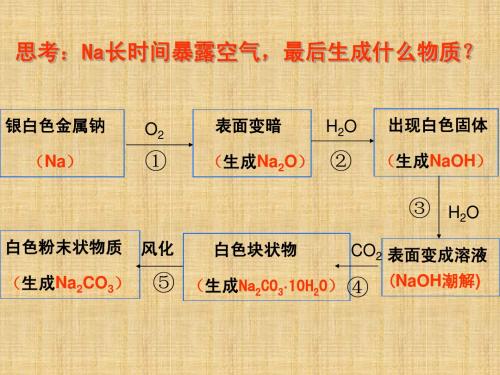
银白色金属钠 表面变暗
O2
H2O
出现白色固体
(生成NaOH)
(Na)
①
(生成Na2O)
②
③
白色粉末状物质 (生成Na2CO3) 风化 白色块状物
H2O
CO2 表面变成溶液
⑤
(生成Na2CO3· 2O) ④ 10H
(NaOH潮解)镁和铝的物来自性质镁和铝都是银白色金属。
点燃
点燃
Mg+Cl2 === MgCl2 ∆ Mg + S === MgS
2Al+3Cl2=== 2AlCl3 ∆ 2Al + 3S === Al2S3
镁和铝的化学性质:
2.与水的反应:
冷水几乎不反应
Mg
热水反应
Mg+2H2O(热水) === Mg(OH)2↓+H2↑
Al与水很难反应
镁和铝的化学性质:
铝:制作导线、电缆, 都属于硬度较小、 以及食品和饮料的包装
铝箔
熔点较低的轻金属
都具有较强的韧性、 延展性 镁和铝更重要的用途是:
制造合金。 有良好的导电、导热 性。
镁
1、物理性质及用途
(1)、物理性质
共同点:均为银白色,属于轻金属(密度<4.5g/cm3), 熔点较低,良好的导电、导热、延展性。 不同点:密度:Mg<Al,熔点:Mg<Al,硬度:Mg<Al。
试试看:
标出铝与氢氧化钠反应的电子转移情 况,并写出该反应的离子方程式。
失2×3 e- 2Al+6H2O+2NaOH==2NaAlO2+3H2↑+4H2O
得6×e- 2Al+2H2O+2OH-==2AlO 2 - +3H2↑
镁与铝的性质及应用

镁与铝的性质及应用镁和铝都是常见的金属元素,具有重要的性质和广泛的应用。
1. 镁的性质及应用:镁是一种轻质金属,具有很多独特的性质和优点。
(1)物理性质:镁的相对原子质量为24.305,密度为1.74g/cm³,熔点为650,沸点为1090。
它是一种银白色的金属,具有较好的导电性和导热性。
(2)化学性质:镁可以与氧、氮、硫、卤素等非金属元素发生反应。
在空气中容易被氧气氧化,形成氧化镁。
它在盐酸和硫酸中可以被溶解,产生氢气。
然而,镁在水中不溶解,而是生成氢氧化镁。
(3)应用:a. 轻金属结构材料:镁具有轻质、高强度、刚性和耐腐蚀的特性,因此广泛用于航空航天、汽车、摩托车和自行车等交通工具的制造。
例如,镁合金可以用于制造飞机机身、发动机零部件和车轮等。
b. 化工原料:镁是很多化学物质的重要原料,广泛应用于冶金、电子、电池、防腐等领域。
例如,氧化镁可用作填充剂或添加剂,提高橡胶和塑料的性能;氯化镁和硫酸镁可以用于制备肥料和药品。
c. 防腐剂:镁具有很强的还原能力,可以用作金属防腐剂。
例如,可以将镁锌合金加工成镀锌铁片,用于防止铁制品的腐蚀。
2. 铝的性质及应用:铝是另一种重要的金属元素,其性质和应用也非常广泛。
(1)物理性质:铝的相对原子质量为26.98154,密度为2.7g/cm³,熔点为660,沸点为2467。
它是一种银白色的金属,具有良好的导热性和导电性。
(2)化学性质:铝在空气中易于氧化,形成氧化铝。
虽然它与水反应较慢,但与盐酸、硫酸等酸性溶液反应活泼,产生氢气。
铝也是一种亲硫金属,与硫元素反应会形成硫化铝。
(3)应用:a. 包装材料:铝是一种轻便、耐腐蚀的金属,常用于食品和制药包装。
铝箔可以包裹食物,保持其新鲜和安全,并且可以防止氧气、水分和异味的进入。
b. 建筑材料:铝因其轻质和耐腐蚀性受到建筑业的青睐。
铝合金可以用于制造窗户、门、楼梯、铝幕墙等建筑部件。
它们具有良好的强度和耐久性,且易于加工和安装。
镁、铝单质的性质

第 1 页 共 1 页镁、铝单质的性质1.镁、铝的结构和存在镁、铝分别位于元素周期表的第三周期ⅡA 族和ⅢA 族,原子结构示意图为和,它们都是活泼的金属,在自然界中全部以化合态的形式存在。
铝是地壳中含量最多的金属元素。
2.镁、铝单质物理性质比较(1)相同点:均为银白色有金属光泽的固体,有良好的延展性、导电性和导热性等,密度、硬度均较小。
(2)不同点:铝的熔点比镁高,硬度比镁大。
3.对比掌握镁、铝的化学性质铝镁能与非金属单质反应①与空气中的氧气形成致密的氧化膜 ②与氯气加热反应:2Al +3Cl 2=====△2AlCl 3①在空气中燃烧发出耀眼白光 ②与氮气反应:3Mg +N 2=====点燃Mg 3N 2与水反应反应很困难与沸水反应:Mg +2H 2O=====△Mg(OH)2+H 2↑与酸反应 ①与H +:2Al +6H +===2Al 3++3H 2↑ ②在冷的浓硫酸、浓硝酸中钝化 Mg +2H +===Mg 2++H 2↑,相同条件下,反应速率比Al 快与碱反应 2Al +2OH -+2H 2O===2AlO -2+3H 2↑ 不反应与某些氧化物反应 与Fe 2O 3的铝热反应:2Al +Fe 2O 3=====高温2Fe +Al 2O 3能在CO 2中燃烧:2Mg +CO 2=====点燃2MgO +C4.镁、铝的冶炼Mg :MgCl 2(熔融)=====电解Mg +Cl 2↑; Al :2Al 2O 3(熔融)=====电解冰晶石4Al +3O 2↑。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金属的物理性质和结构特点以及镁铝的性质
重点内容讲解:镁和铝是学习周期表后最典型和最有代表性的金属,知识内容丰富,是应用周期律掌握元素化合物性质的典型内容;在学习时要注意运用对比的方法,并充分发挥理论对学习金属元素知识的指导作用等。
一、复习:几种晶体结构
晶体类型:离子晶体
氯化钠(NaCl)——结构特点:黄球表示钠离子(Na+) 绿球表示氯离子(Cl-)
在NaCl晶体中,Na+与Cl-通过离子键相结合,每个Na+与和它紧邻的6个氯离子相连,每个Cl-与和它紧邻的6个Na+相连,Na+和Cl-在三维空间上交替出现,并延长形成NaCl晶体,NaCl 晶体中没有NaCl分子,NaCl只是代表NaCl晶体中Na+和Cl-的个数比为1:1。
氯化铯(CsCl)——结构特点:黄球表示铯离子(Cs+) 紫球表示氯离子(Cl-)
在CsCl晶体中,Cs+与Cl-通过离子键相结合,每个Cs+与和它紧邻的8个Cl-相连,每个Cl-与和它紧邻的8个Cs+相连,Cs+和Cl-在三维空间上交替出现,并延长形成CsCl晶体,CsCl晶体中没有CsCl分子,CsCl只是代表CsCl晶体中Cs+和Cl-的个数比为1:1。
(如下图)
晶体类型:原子晶体
金刚石(C)——结构特点:每个黄球表示一个碳原子(C)
在金刚石晶体中,所有碳原子以非极性共价键相结合成网状结构每个碳原子与和它紧邻的4个碳原子相连,键角109º28';由碳原子组成的最小环为六元环,且六个碳原子不在一个平面内。
晶体类型:分子晶体
干冰(CO2)——结构特点:每个黄球表示一个碳原子(C),每个紫球表示一个氧原子(O)
在干冰晶体中,CO2之间以分子间作用力相连,CO2与和它紧邻的12个CO2相连。
晶体类型:混合晶体(既有原子晶体的结构特点,也有分子晶体的结构特点)
石墨(C)——结构特点:每个小球表示一个碳原子(C)
在石墨晶体中,碳原子是分层排布在同一层内:所有碳原子以非极性共价键相结合成平面网状结构,每个碳原子与和它紧邻的3个碳原子相连,键角120°,由碳原子组成的最小环为平面六元环,层与层之间为分子间作用力(范德华力)。
晶体类型:金属晶体
金属——结构特点:每个小球表示一个金属原子(或金属离子)
在金属晶体中含有金属阳离子与自由电子,自由电子可以在金属原子的缝隙间自由移动,它们不属于任何一个原子,金属原子总是以紧密堆积的形式结合在一起。
二、金属晶体的结构及性质:
1、金属晶体的结构:
金属原子结构的共同特征是:①最外层电子数较少,一般在4个以下;②原子半径较大。
这种结构特点使其原子易失去价电子而变成金属离子,释放出的价电子在整个晶体中可以自由运动,被称为“自由电子”。
它不再属于哪个或哪几个指定的金属离子,而是整块金属的“集体财富”,它们在整个晶体内自由运动,所以有人描述金属内部的实际情况是“金属离子沉浸在自由电子的海洋中”,金属阳离子与自由电子之间存在着较强的作用(金属键),因而使金属离子相互结合在一起,形成金属晶体。
2、金属的物理性质:
金属在常温下,一般大多都是晶体(除汞外),有金属光泽、不透明、容易导电、导热、有延展性。
(1)导电性:自由电子在外加电场作用下发生定向移动。
(2)导热性:金属受热后,自由电子运动速率加快,碰撞中能够传递热量。
(3)有延展性:外力作用下,金属因层与层之间相对滑动而变形,但并不改变金属微粒间的相互作用。
3、金属的化学性质:
金属单质的化学性质——只有还原性:M-ne-=M n+。
具体表现在以下方面:
1、与非金属反应:如与O
2、Cl2、Br2、I2、N2等
2、与水反应:较活泼的金属可与水反应,如K、Ca、Na等
3、与酸反应:排在氢前面的金属可将氢从酸溶液中置换出来(浓H2SO
4、HNO3除外)
4、与盐反应:排在前面的金属可将后面的金属从它们的盐溶液中置换出来。
三、金属的分类:
现在已经发现的112种元素中,金属有90种,约占4/5。
金属元素可以从不同方面进行分类:按照活动性:排在氢前的金属称为活泼金属,排在氢后的金属称为不活泼金属。
按密度分:轻金属(r<4.5g·cm-3),如K、Ca、Na、Mg、Al等;
重金属(r>4.5g·cm-3),如Fe、Cu、Ag、Au等。
按冶金工业分:黑色金属(Fe、Cr、Mn及其合金)和有色金属(除Fe、Cr、Mn外的其它金属)。
按地壳中的含量分:常见金属(如Fe、Al、Na、Mg等)和稀有金属(如Zr、Hf、Nb等)。
说明:在掌握金属分类中,要注意联系常见金属,认识它们在不同的分类标准中所属的类别。
四、合金
1、合金:是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
合金一般在某些性质,如物理性质、化学性质或机械加工性能上比较优良。
2、性质:一般来说,合金的熔点比它的各成分金属的都低;硬度比它各组分的金属都大。
五、镁和铝
1、镁和铝的原子结构和物理性质:
思考:为什么铝的硬度比镁的稍大,熔点和沸点都比镁高?考虑此问题时要从金属的晶体结构入手。
2、化学性质
共同点:M-ne-=M n+
(1)跟非金属单质的反应:
a、镁铝在常温下能很快被氧化,形成致密的氧化膜,因而具有一定的抗腐蚀性,铝的抗腐蚀性比镁强。
同时,镁在空气中可点燃,Al在纯氧中或高温下可燃烧,都能放出大量热,发出
耀眼的白光:2Mg+O22MgO;4Al+3O22Al2O3。
b、与其它非金属单质反应:
3Mg+N2Mg3N2Mg+S MgS Mg+Cl2MgCl2
2Al+3S Al2S32Al+3Cl22AlCl3
(2)跟酸的反应
(3)跟碱的反应
镁不能跟碱起反应,铝和强碱溶液反应,不是铝直接和碱反应,而是铝先和强碱溶液中的水反应生成氢氧化铝,然后再和强碱反应生成偏铝酸盐:
2Al+6H2O=2Al(OH)3+3H2↑Al(OH)3+NaOH=NaAlO2+2H2O
总反应:
(标电子转移时就必须清楚地理解铝和NaOH溶液反应的实质)
简写为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑
(4)与氧化物的反应:
a、与H2O的反应:
Mg+2H2O Mg(OH)2+H2↑(能使酚酞变红)
2Al+6H2O 2Al(OH)3+3H2↑
b、与某些氧化物的置换反应
2Mg+CO22MgO+C2Mg+SO22MgO+S
c、铝热反应:Al(固)+M x O y(固)Al2O3+xM(液)+Q
铝热反应的应用:冶炼高熔点金属,如Fe、V、Cr、Mn等或焊接钢轨。
3、用途:镁铝主要用来制轻合金。
[例题分析]
例1、下列关与金属元素特征的叙述正确的是()
(1)金属元素的原子只有还原性,离子只有氧化性;(2)金属元素在化合物中只显正价;(3)金属性越强的元素相应的离子氧化性越弱;(4)价电子越多的金属原子金属性越强;(5)离子化合物一定含金属元素
A、(1)(2)(3)
B、(2)(3)
C、(1)(4)(5)
D、全部
解析:(1)对于变价金属中,较低价态的金属离子既有氧化性,又有还原性,如Fe2+。
(2)金属元素的原子只具有还原性,故在化合物中只显正价。
(4)金属性的强弱要看失电子的难易。
(5)离子化合物不一定含金属元素,如NH4Cl。
故正确答案为选项B。
例2、把镁粉中混入的少量铝粉除去。
应选用的试剂是()
A、稀盐酸
B、新制氯水
C、烧碱溶液
D、纯碱溶液
解析:盐酸跟镁、铝都能反应,故A错。
氯水中存在Cl2,是强氧化性,金属都有还原性,
镁铝都能和Cl2反应,同时,氯水中有Cl2和H2O反应生成的盐酸和次氯酸,这两种酸也都能和镁、铝反应,故B也不能选。
烧碱是NaOH,铝可以跟NaOH溶液反应放出H2,而镁不反应而和铝分离,故C可选。
纯碱溶液是碳酸钠溶液,镁、铝都不与之反应,故正确答案为选项C。
[本周参考练习]
1、称取两份铝粉,第一份加入足量稀硫酸,第二份加入足量浓氢氧化钠溶液,在相同条件下,若放出的气体体积相同,则两份铝粉的质量比为()
A、1∶1
B、1∶2
C、1∶3
D、2∶3
2、甲、乙两烧杯中各盛有100mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中加入等质量的铝粉,反应结束后测得生成的气体体积比为甲∶乙=1∶2,则加入铝粉的质量为()
A、5.4g
B、3.6g
C、2.7g
D、1.8g
3、用铝热法还原下列化合物,制得金属各1mol,需消耗铝最少的是:()
A、MnO2
B、WO3
C、Co3O4
D、Cr2O3
4、将相同质量的镁条分别在:⑴O2中⑵空气中⑶CO2中充分燃烧。
所得固体产物的质量排列顺序正确的是()
A、⑴>⑵>⑶
B、⑶>⑵>⑴
C、⑵>⑴>⑶
D、⑶>⑴>⑵
参考练习答案
1、A
2、A
3、C
4、D。
