九年级化学(沪教版)化学方程式整理小结
沪教版九年级化学方程式总结

沪教版九年级化学方程式总结1.加热高锰酸钾制取氧气,化学方程式为2KMnO4 →K2MnO4 + MnO2 + O2↑。
这个方程式体现了氧气的氧化性和助燃性。
2.双氧水在二氧化锰作用下制取氧气,化学方程式为2H2O2 → 2H2O + O2↑。
3.加热二氧化锰和氯酸钾的固体混合物可以制取氧气,化学方程式为2KClO3 → 2KCl + 3O2↑。
4.木炭的燃烧可以在空气中燃烧红热,在氧气中发出白光,放出热量,并生成气体,能使澄清石灰水变浑浊,化学方程式为C + O2 → CO2.5.碳不完全燃烧的化学方程式为2C + O2 → 2CO。
6.一氧化碳燃烧可以放出热量、产生淡蓝色火焰,并生成气体,能使澄清石灰水变浑浊,化学方程式为2CO + O2 →2CO2.7.镁带在空气中燃烧时会剧烈燃烧,发出耀眼的白光,放出热量,并生成白色粉末状固体,化学方程式为2Mg + O2 →2MgO。
8.铁丝在氧气中燃烧时会剧烈燃烧,火星四射,放出热量,并生成黑色固体。
在空气中不能燃烧,需要预先在集气瓶底部铺少量沙子或加少量水,以防止生成的高温熔化物溅落炸裂集气瓶底,化学方程式为3Fe + 2O2 → Fe3O4.9.铜在空气中加热时会变成黑色固体,化学方程式为2Cu + O2 → 2CuO。
10.铝在空气中受热时会变成白色固体,化学方程式为4Al + 3O2 → 2Al2O3.11.红磷或白磷在空气中燃烧时会放出热量,产生大量白烟,化学方程式为4P + 5O2 → 2P2O5.12.硫粉在空气中燃烧时会产生淡蓝色火焰,在氧气中产生蓝紫色火焰,并生成有刺激性气味的气体。
需要预先在集气瓶底加少量水,以吸收有毒气体二氧化硫,化学方程式为S +O2 → SO2.13.氢气在空气中燃烧时会产生淡蓝色火焰,放出大量热,烧杯内壁凝结有水雾,化学方程式为2H2 + O2 → 2H2O,这说明水由H、O元素组成。
14.甲烷在空气中燃烧时会生成CO2和H2O,化学方程式为CH4 + 2O2 → CO2 + 2H2O。
九年级化学上册沪教版化学方程式小结

九年级化学上册沪教版化学方程式小结Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-NUT108】九年级化学上册(沪教版)化学方程式整理小结1、碳酸氢铵受热分解:NH4HCO3△NH3↑+ CO2↑+ H2O2、碱式碳酸铜(铜绿受热分解):Cu2(OH)2CO3△2CuO+ CO2↑+ H2O3、镁带在空气中燃烧:2Mg + O2点燃 2MgO4、铁丝在氧气中燃烧:3Fe + 2O2点燃 Fe3O45、磷在空气中燃烧: 4P + 5O2点燃 2P2O56、加热高锰酸钾制取氧气:2KMnO4△K2MnO4+ MnO2+ O2↑7、二氧化锰催化双氧水制氧气:2H2O2MnO2 2H2O+ O2↑8、加热氯酸钾制取氧气:2KClO3MnO2 2KCl + 3O2↑9、二氧化碳溶于水CO2 + H2O === H2CO310、碳酸不稳定易分解H2CO3△CO2↑+H2O11、实验室制取二氧化碳:CaCO3+2HCl==CaCl2+H2O+CO2↑12、二氧化碳通入澄清石灰水:CO2 +C a(O H)2==CaCO3↓+ H2O13、电解水:2H2O 通电 2H2↑+ O2↑14、氢气燃烧或爆炸: 2H2 + O2点燃2H2O15、碳的不完全燃烧: 2C + O2点燃2CO16、碳的完全燃烧:C + O2点燃 CO217、一氧化碳在空气中燃烧 2CO + O2点燃 2CO218、氢氧化钠与硫酸铜反应 Ca(OH)2+ CuSO4==CaSO4+ Cu(OH)2↓19.、铜丝在空气中加热: 2Cu + O2△ 2CuO20.、铝丝在常温时形成氧化膜:4Al+ 3O2 ==2Al2O321、镁与硫酸反应:Mg+H2SO4==MgSO4+H2↑22.、镁与盐酸反应: Mg+2HCl==MgCl2+H2↑23.、铝与盐酸反应:2Al+6HCl==2AlCl3+3H2↑?24.、铝与硫酸反应:2Al+3H2SO4==Al2(SO4)3+3H2↑25、铁与盐酸反应制氢气: Fe + 2HCl==FeCl2 + H2↑26、铁与硫酸反应制氢气: Fe+H2SO4==FeSO4+H2↑27.、锌与盐酸反应制氢气(实验室制取氢气): Zn + H2SO4==ZnSO4+ H2↑28.、湿法炼铜法:Fe+CuSO4==Cu+FeSO429、工业炼铁的原理(以赤铁矿为例):3CO+ Fe2O3高温2Fe + 3CO2。
九年级化学(沪教版)化学方程式整理小结[1]
![九年级化学(沪教版)化学方程式整理小结[1]](https://img.taocdn.com/s3/m/4f3f3738aeaad1f347933fc7.png)
九年级化学(沪教版)化学方程式整理小结一.化合反应1.镁带燃烧: 2Mg + O 2 ==== 2Mg O2.铁丝燃烧及生锈:3Fe + 2O 2 ==== Fe 3O 4 ;4Fe + 3O 2 ===== 2Fe 2O3(缓慢氧化)3.铜丝加热及生锈: 2Cu + O 2 === 2CuO ; 2Cu + O2 + H 2O + CO 2 == C u2(OH)2CO 3 4.铝丝加热或形成氧化膜:4A l + 3O 2 === 2A l2O 35.氢气燃烧或爆炸: 2H2 + O 2 === 2H 2O6.碳的燃烧:2C + O2 ==== 2C O(不完全燃烧);C + O 2 === CO 2(完全燃烧)7.硫的燃烧:S + O2 === SO 28.磷的燃烧:4P + 5O 2 === 2P 2O 59.二氧化碳被碳还原:C + C O2 === 2CO10.人工固氮(合成氨):N 2 + 3H 2 ======= 2NH 311.生石灰溶于水:CaO + H 2O == Ca (OH)212.二氧化碳溶于水:CO2 + H 2O == H2CO313.二氧化硫溶于水:SO 2 + H 2O == H2SO 314.二氧化硫在空气中转化为三氧化硫:2SO 2 + O2 ==== 2SO315.三氧化硫溶于水:SO 3 + H 2O == H 2SO 416.工业上制盐酸(氢气在氯气中燃烧):H 2 + Cl 2 === 2H Cl17.金属钠在氯气中燃烧:2N a + Cl 2 2HCl18.浓盐酸与浓氨水相靠近:NH 3 + HC l == N H4Cl二.分解反应1.碳酸氢铵(碳铵)受热分解:NH 4HCO 3 NH 3↑+ CO 2↑+ H 2O2.碱式碳酸铜(铜绿受热分解):C u2(OH)2CO 3 2C uO + H 2O + C O2↑3.加热高锰酸钾制氧气:2K MnO 4 K 2MnO 4 + MnO 2 + O 2↑4.二氧化锰催化双氧水制氧气:2H 2O2 2H2O + O 2↑5.电解水:2H 2O 2H2↑+ O 2↑6.碳酸分解:H 2CO 3 == CO 2↑+ H 2O7.碳酸钙高温煅烧分解:CaCO 3 CaO + CO 2↑8.电解熔融状态的氧化铝制取金属铝:2Al 2O3 4Al + 3O2↑三.置换反应1 氢气还原金属氧化物:Fe 2O 3 + 3H2 2Fe + 3H 2O;Fe 3O 4 + 4H23Fe 潮湿空气 △ 点燃点燃 △点燃点燃 点燃点燃 点燃高温 高温、高压催化剂 粉尘等点燃点燃 === △=== △=== △=== MnO 2 === 通电 === 高温 === 通电 === 高温 === 高温 ===+ 4H 2O;C uO + H 2 Cu + H 2O 2.碳粉还原金属氧化物:2Fe 2O 3 + 3C 4Fe + 3CO 2↑; F e3O 4 + 2C 3Fe + 2CO 2↑ 2CuO + C 2Cu + CO 2↑3.制取水煤气:C + H 2O CO + H 24.铝与盐酸、硫酸反应制氢气:2Al + 6HCl == 2AlCl 3 + 3H 2↑;2Al + 3H 2SO 4 == A l2(SO 4)3 + 3H 2↑5.镁与盐酸、硫酸反应制氢气:Mg + 2HC l == MgCl 2 + H 2↑;Mg + H 2S O4 == MgS O4 + H 2↑6.铁与盐酸、硫酸反应制氢气:Fe + 2HCl == Fe Cl 2 + H 2↑;Fe + H 2SO 4 == FeSO 4 + H2↑7.锌与盐酸、硫酸反应制氢气:Zn + 2HCl == Z nC l2 + H2↑;Zn + H 2SO 4 == ZnSO 4 + H 2↑8.湿法炼铜法,铁与硫酸铜溶液反应:Fe + CuS O4 == FeSO 4 + Cu9.铜与硝酸银溶液反应:Cu + 2Ag NO 3 == Cu (NO 3)2 + 2Ag10.铝热剂反应:2Al + Fe 2O 3 Al 2O3 + 2Fe;8Al + 3Fe 3O 4 4A l2O 3 + 9F e 11.金属镁与二氧化碳反应:2M g + CO 2 2M gO + C 四.复分解反应:1.酸碱中和反应:HCl + NaOH == NaCl + H 2O;C u(OH )2 + H 2SO 4 == CuSO 4 + 2H2OH 2S O4 + B a(OH )2 == B aSO4↓+ 2H 2O ;C a(OH)2 + 2H Cl == CaCl 2 +2H 2O2.金属氧化物与酸溶液反应:Fe 2O 3 + 6HCl == 2FeCl 3 + 3H 2O ;Cu O + H2SO 4 == CuSO 4 + H 2OMgO + 2HC l == MgCl 2 + H2O;A l2O 3 + 3H 2SO 4 == Al2(S O4)3 + 3H2O3.碳酸盐与酸溶液反应: CaCO 3 + 2HC l == CaC l2 + CO 2↑+ H 2O;Na 2CO 3 + 2H Cl == 2NaCl+ CO 2↑+ H 2OK 2CO 3 + H2SO 4 == K 2SO 4 + CO 2↑+ H 2O4.盐溶液与碱溶液反应: Na 2CO3 + Ca (OH )2 == CaCO 3↓+ 2Na OH;CuS O4 + 2NaOH== Cu (OH )2↓+N a2SO 4C uSO 4 + Ba (OH)2 == BaS O4↓+ C u(OH)2↓5.Ag +与Cl—反应:HCl + AgNO 3 == AgCl ↓+ H NO3;NaC l + AgNO 3 == A gC 高温 ===高温 ===高温 ===高温 === 高温 === 高温 ===高温=== 高温 ===l↓+ N aNO 36.B a2+与SO 42—反应:BaCl 2 + CuSO 4 == BaS O4↓+ C uCl 2;H 2S O4 + BaCl 2 == Ba SO 4↓+ 2HCl 7.纯碱与氯化钙溶液反应:Na 2CO 3 + CaCl 2 == CaC O3↓+ 2Na Cl8.铵盐与碱反应产生氨气:NH 4NO 3 + N aOH == NaNO 3 + NH 3↑+ H 2O(NH 4)2S O4 + Ca(OH )2 == Ca SO 4 + 2NH 3↑+ 2H 2O五.其他反应类型:1.一氧化碳还原金属氧化物:Fe 2O3 + 3C O 2F e + 3CO 2;Fe3O 4 + 4CO 3Fe + 4CO 2;C uO + CO Cu + CO 2 2.非金属氧化物与碱溶液反应: CO 2 + C a(O H)2 == CaCO 3↓+ H 2O;CO 2 +2Na OH == Na 2CO 3 + H 2OSO 2 +2Na OH == Na 2S O3 + H2O3.有机物燃烧:C H4 + 2O2 CO 2 + 2H 2O ; C 2H 6O + 3O 2 2CO2 + 3H 2O C 6H 12O6 + 6O 2 6CO 2 + 6H2OC x H y Oz + (424z y x -+)O 2 xCO 2 + 2y H 2O 4.绿色植物光合作用:6CO 2 + 6H 2O C 6H 12O6 + 6O 2二:其它1、构成物质的三种微粒是 分子、原子、离子。
沪教版初中化学中考常考知识点整理

沪教版初中化学中考常考知识点整理学校姓名班级一、化学实验及操作1. 称量器——托盘天平(用于粗略的称量,一般能精确到0.1克。
)(1)先调平调零。
(2)称量物和砝码的位置为“左物右码”。
(3)称量物不能直接放在托盘上。
一般药品称量时,在两边托盘中各放一张大小、质量相同的纸,在纸上称量。
潮湿的或具有腐蚀性的药品(如氢氧化钠),放在玻璃器皿(如小烧杯、表面皿)中称量。
(4)砝码用镊子夹取。
添加砝码时,先大后小。
2.测容器——量筒(1)量取液体体积时,量筒必须放平稳。
视线与量筒内液体凹液面的最低点保持水平。
(2)量筒不能用来加热,不能用作反应容器。
3.加热器皿——酒精灯(1)注意事项:①绝对禁止向燃着的酒精灯内添加酒精;②用火柴从侧面点燃酒精灯,绝对禁止用燃着的酒精灯去点燃另一盏酒精灯;③熄灭酒精灯应用灯帽盖灭,不可吹熄。
(2)酒精灯内的酒精量不可超过酒精灯容积的2/3。
(3)酒精灯的火焰分为外焰、内焰、焰心。
外焰的温度最高,用酒精灯的外焰加热。
(4)如果酒精灯在燃烧时不慎翻倒,酒精在实验台上燃烧时,应及时用沙子盖灭或用湿抹布扑灭火焰,不能用水冲。
(5)加热固体时,试管口应略下倾斜,试管受热时先预热,再集中加热。
(6)加热液体时,液体体积不超过试管容积的1/3。
4.倾倒液体:取下瓶盖,倒放在桌上,(以免药品被污染)。
标签应向着手心,(以免残留液流下而腐蚀标签)。
拿起试剂瓶,将瓶口紧挨着试管口边缘,缓缓地倒入,倾注完毕,盖上瓶盖,标签向外,放回原处。
5. 检查装置气密性:先将导管的一端浸入水中,再用手紧贴容器外壁,若导管口有气泡冒出,就说明装置不漏气。
6.过滤:操作注意事项:“一贴二低三靠”“一贴”:滤纸紧贴漏斗的内壁“二低”:(1)滤纸的边缘低于漏斗口(2)漏斗内的液面低于滤纸的边缘“三靠”:(1)漏斗下端的管口紧靠烧杯内壁(2)玻璃棒下端轻靠在三层滤纸的一边(3)用玻璃棒引流时,烧杯尖嘴靠在玻璃棒上过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损7.蒸发:(1)在加热过程中,用玻璃棒不断搅拌,防止由于局部温度过高,造成液滴飞溅。
(完整)九年级化学上册(沪教版)化学方程式整理小结

沪教版九年级化学上册化学方程式(烟雨朦胧整理)九年级化学上册(沪教版)化学方程式整理小结1、碳酸氢铵受热分解:NH4HCO3△NH3↑+ CO2↑+ H2O2、碱式碳酸铜(铜绿受热分解):Cu2(OH)2CO3△2CuO+ CO2↑+ H2O3、镁带在空气中燃烧:2Mg + O2点燃2MgO4、铁丝在氧气中燃烧:3Fe + 2O2点燃Fe3O45、磷在空气中燃烧:4P + 5O2点燃2P2O56、加热高锰酸钾制取氧气:2KMnO4△K2MnO4 + MnO2 + O2↑7、二氧化锰催化双氧水制氧气:2H2O2MnO2 2H2O+ O2↑8、加热氯酸钾制取氧气:2KClO3MnO2 2KCl + 3O2↑9、二氧化碳溶于水CO2 + H2O === H2CO310、碳酸不稳定易分解H2CO3 △CO2↑+H2O11、实验室制取二氧化碳:CaCO3+2HCl==CaCl2+H2O+CO2↑12、二氧化碳通入澄清石灰水:CO2 +C a(O H)2 ==CaCO3↓+ H2O13、电解水:2H2O 通电2H2↑+ O2 ↑14、氢气燃烧或爆炸:2H2 + O2点燃2H2O15、碳的不完全燃烧:2C + O2点燃2CO16、碳的完全燃烧:C + O2点燃CO217、一氧化碳在空气中燃烧2CO + O2点燃2CO218、氢氧化钠与硫酸铜反应Ca(OH)2+ CuSO4 ==CaSO4+ Cu(OH)2↓19.、铜丝在空气中加热:2Cu + O2△2CuO20.、铝丝在常温时形成氧化膜:4Al+ 3O2==2Al2O321、镁与硫酸反应:Mg+H2SO4==MgSO4+H2↑22.、镁与盐酸反应:Mg+2HCl==MgCl2+H2↑23.、铝与盐酸反应:2Al+6HCl==2AlCl3+3H2↑24.、铝与硫酸反应:2Al+3H2SO4==Al2(SO4)3+3H2↑25、铁与盐酸反应制氢气:Fe + 2HCl==FeCl2 + H2↑26、铁与硫酸反应制氢气:Fe+H2SO4==FeSO4+H2↑27.、锌与盐酸反应制氢气(实验室制取氢气):Zn + H2SO4 ==ZnSO4 + H2↑28.、湿法炼铜法:Fe+CuSO4==Cu+FeSO429、工业炼铁的原理(以赤铁矿为例):3CO+ Fe2O3高温2Fe + 3CO2。
沪教版九年级化学知识点总结

化学是一门研究物质组成、结构、性质以及物质之间的变化规律的科学。
以下是沪教版九年级化学的主要知识点总结。
1.原子结构-原子模型的发展-原子的构成:质子、中子和电子-原子核的结构和性质-原子的量子化学-电子排布及元素周期表2.离子和化学键-离子的定义和特性-离子化合物的性质和命名方法-配位化合物的结构和性质-各种化学键的分类和特点3.化学方程式和化学计算-化学方程式的基本要素-平衡方程式和化学平衡-摩尔质量和摩尔计算-溶液浓度的计算4.酸、碱和盐-酸碱理论和酸碱指示剂-酸和碱的性质及化学式-酸碱滴定和中和反应-盐的命名和产生方式5.氧化与还原-氧化与还原的概念-氧化还原反应的特点和类型-氧化还原反应的应用实例-金属的活动性和反应活性顺序6.有机化学基础-有机化合物的结构和命名方法-烷烃、烯烃和炔烃的命名和性质-醇、醛、酮和羧酸的基本结构和性质-重要有机化合物的应用7.化学反应的速率-化学反应速率的定义和表示方法-影响化学反应速率的因素-反应速率和反应机理的关系-表观活化能和催化剂的作用8.化学能与能量变化-化学能和化学能的转化-化学反应中的能量变化-燃烧反应的热效应-化学反应的焓变计算以上是沪教版九年级化学的主要知识点总结。
通过对这些知识点的学习,学生将能够理解物质的基本组成和结构,掌握化学方程式的书写和化学计算的方法,认识酸碱和氧化还原反应的基本原理,了解有机化学的基础知识,以及掌握化学反应速率和能量变化等方面的知识。
这些知识将为学生进一步学习高中化学打下坚实的基础。
(完整版)九年级化学上册(沪教版)化学方程式整理小结.doc

沪教版九年级化学上册化学方程式(烟雨朦胧整理)九年级化学上册(沪教版)化学方程式整理小结1、碳酸氢铵受热分解:NH 4 HCO 3△NH 3 ↑+ CO 2 ↑ + H 2O2、碱式碳酸铜(铜绿受热分解): Cu 2(OH) 2 3 △2CuO+ CO 2↑+ H 2CO O 3、镁带在空气中燃烧: 2Mg + O 2 点燃 2MgO4、铁丝在氧气中燃烧: 3Fe + 2O 2 点燃 Fe 3 O 45、磷在空气中燃烧: 4P + 5O 2点燃 2P 2 O 5 6、加热高锰酸钾制取氧气: 2KMnO 4 △K 2 MnO 4 + MnO 2 + O 2 ↑7、二氧化锰催化双氧水制氧气:2H 2O 2 MnO2 2H 2O+ O 2 ↑ 8、加热氯酸钾制取氧气: 2KClO 3 MnO2 2KCl + 3O 2↑9、二氧化碳溶于水 CO 2 + H 2O === H 2CO 310、碳酸不稳定易分解 H 2CO 3 △ CO 2↑ +H 2O11、实验室制取二氧化碳: CaCO 3+2HCl==CaCl 2+H 2O+CO 2↑12、二氧化碳通入澄清石灰水: CO +C a( O H ) 2 ==CaCO ↓ + H O2 3 2 13、电解水: 2H 2 O 通 电 ↑+ O 2 ↑2H 214、氢气燃烧或爆炸: 2H 2 + O 2 点燃 2H 2 O15、碳的不完全燃烧: 点燃 2CO2C + O 216、 碳的完全燃烧: C + O 2 点燃 CO 217、一氧化碳在空气中燃烧 2CO + O 2 点燃 2CO 218、氢氧化钠与硫酸铜反应Ca(OH) 2+ CuSO 4 ==CaSO 4+ Cu(OH) 2↓ 19.、铜丝在空气中加热:2Cu + O 2 △ 2CuO20.、铝丝在常温时形成氧化膜: 4Al + 3O 2 == 2Al 2O 321、镁与硫酸反应: Mg+H 2SO 4==MgSO 4+H 2↑22.、镁与盐酸反应: Mg+2HCl==MgCl 2+H 2↑23.、铝与盐酸反应: 2Al+6HCl==2AlCl 3+3H 2↑24.、铝与硫酸反应: 2Al+3H 2SO 4==Al 2(SO 4)3+3H 2 ↑25、铁与盐酸反应制氢气: Fe + 2HCl ==FeCl 2 + H 2 ↑26、铁与硫酸反应制氢气:Fe+H 2SO 4==FeSO 4+H 2↑ 27.、锌与盐酸反应制氢气(实验室制取氢气): Zn + H 2 SO 4 ==ZnSO 4 + H 2↑28.、湿法炼铜法: Fe+CuSO 4==Cu+FeSO 4 高温29、工业炼铁的原理(以赤铁矿为例): 3CO+ Fe 2O 3 2Fe + 3CO 2。
九年级上册化学方程式整理小结

九年级上册化学方程式整理小结一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁燃烧:2Mg + O2点燃2MgO 现象:剧烈燃烧、发出耀眼的白光、放出大量的热、生成白烟和白色固体2. 铁在氧气中燃烧:3Fe + 2O2点燃Fe3O4 现象:剧烈燃烧、火星四射、放出大量热、生成黑色的固体(瓶底要铺一层沙子或装少量水防止高温熔融物溅落而炸裂瓶底)△====2CuO现象:红色金属变为黑色固体5. 氢气燃烧:2H2 + O2点燃2H2O 现象:淡蓝色的火焰、放热6. 红磷燃烧:4P + 5O2点燃2P2O5 现象::剧烈燃烧、生成大量白烟7. 硫粉燃烧:S + O2点燃SO2现象:空气中是淡蓝色的火焰;纯氧中是蓝紫色的火焰;同时生成有刺激性气味的气体。
(瓶底装少量水吸收SO2)8. 碳在氧气中充分燃烧:C + O2点燃CO2 现象:生成能够让澄清石灰水浑浊的气体9. 碳在氧气中不充分燃烧:2C + O2点燃2CO煤炉中常见反应、空气污染物之一、煤气中毒原因(2)化合物与氧气的反应:10. 一氧化碳燃烧:2CO + O2点燃2CO2现象:蓝色火焰、放热、生成使澄清石灰水变浑浊气体11. 甲烷燃烧:CH4 + 2O2点燃CO2 + 2H2O 现象:蓝色火焰、放热、生成使澄清石灰水变浑浊气体、在烧杯内壁有水雾生成12. 酒精燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O现象:蓝色火焰、产生使澄清石灰水变浑浊的气体、放热二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑负极是氢气(可燃性),正极是氧气(助燃性),氢气和氧气体积比为:2 : 1,质量比:1 : 814. 2H2O2MnO2====2H2O+ O2↑现象:有大量气泡生成,生成的气体使带火星的木条复燃(实验室制备氧气)15. 加热氯酸钾(有少量的二氧化锰):2KClO3MnO2====2KCl + 3O2 ↑现象:生成使带火星的木条复燃的气体(实验室制备氧气)16. 加热高锰酸钾:2KMnO4△====K2MnO4 + MnO2 + O2↑现象:紫色变为黑色、生成使带火星的木条复燃的气体(实验室制备氧气)17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑紫色石蕊试液通入CO2变成红色,加热后又恢复为紫色18. 高温煅烧石灰石:CaCO3高温CaO + CO2↑工业制备二氧化碳和生石灰三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO△====Cu + H2O 现象:黑色粉末逐渐变成红色,同时有水珠生成(冶炼金属原理)20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成(冶炼金属原理)21. 焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑冶炼金属原理22. 焦炭还原四氧化三铁:2C+ Fe3O4高温3Fe + 2CO2↑冶炼金属原理23. 一氧化碳还原氧化铜:CO+ CuO△====Cu + CO2 现象:固体由黑色变成红色,同时有能使澄清石灰水变浑浊的气体生成(冶炼金属原理)24. 一氧化碳还原氧化铁:3CO+ Fe2O3高温2Fe + 3CO2 冶炼金属原理25. 一氧化碳还原四氧化三铁:4CO+ Fe3O4高温3Fe + 4CO2 冶炼金属原理五.其它反应:26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑现象:有大量气泡产生、锌粒逐渐溶解(实验室制备氢气)27. 锌和稀盐酸Zn + 2HCl=== ZnCl2 + H2↑现象:有大量气泡产生、锌粒逐渐溶解28. 镁和稀盐酸Mg+ 2HCl=== MgCl2 + H2↑现象:有大量气泡产生、镁条逐渐溶解29 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu现象:银白色金属表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色30.检验二氧化碳:Ca(OH)2 + CO2==== CaCO3↓+ H2O现象:澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁31.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑现象:白色固体逐渐溶解,有使澄清石灰水变浑浊的气体生成(实验室制备二氧化碳、除水垢)32.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑现象:固体逐渐溶解、有使澄清石灰水变浑浊的气体生成(泡沫灭火器原理)33.氢氧化钠溶液与硫酸铜溶液:2NaOH + CuSO4 ==== Cu(OH)2↓+ Na2SO4 现象:有蓝色沉淀生成34.二氧化碳溶解于水:CO2 + H2O === H2CO3 碳酸使石蕊变红(证明碳酸的酸性)。
沪教版九年级化学方程式汇总

1.碳在氧气中燃烧2.镁条燃烧碳+氧气点燃二氧化碳镁+氧气点燃氧化镁C+O2点燃CO2 2Mg+O2点燃2MgO3.红磷燃烧4.铁丝在氧气中燃烧磷+氧气点燃五氧化二磷铁+氧气点燃四氧化三铁4P+5O2点燃2P2O5 3Fe+2O2点燃Fe3O45.蜡烛燃烧6.高锰酸钾加热制氧气石蜡+氧气点燃二氧化碳+水高锰酸钾加热锰酸钾+二氧化锰+氧气2KMnO4▲ K2MnO4 + MnO2 + O2↑7.过氧化氢在二氧化锰的催化下制氧气8.加热氯酸钾和二氧化锰制氧气过氧化氢二氧化锰水+氧气氯酸钾二氧化锰氯化钾+氧气2H2O2 MnO 2H2O + O2↑2KClO3 MnO2KCl+3O2↑9.二氧化碳与水反应生成碳酸10.碳酸分解二氧化碳+水→碳酸碳酸→二氧化碳+水CO2 + H2O H2CO3 H2CO3 CO2↑ + H2O11.实验室大理石和稀盐酸反应制二氧化碳 12.二氧化碳使澄清的石灰水变浑浊碳酸钙+盐酸→氯化钙+水+二氧化碳氢氧化钙+二氧化碳→碳酸钙+水CaCO3+2HCl CaCl2+H2O+CO2↑ Ca(OH)2+ CO2 CaCO3↓+H2O13.电解水 14.氢气燃烧水通电氢气+氧气氢气+氧气点燃水2H2O 通电 2H2↑+O2↑ 2H2 +O2点燃2H2O15.碳在空气中不完全燃烧 16.一氧化碳的燃烧碳+氧气点燃一氧化碳一氧化碳+氧气点燃二氧化碳2C+O2 点燃2CO 2CO+O2点燃2CO217.铜丝在空气中加热生成氧化.... 18.铝与氧气反应生成氧化铝铜+氧气加热氧化铜铝+氧气→氧化铝2Cu+O2▲2CuO 4Al+ 3O2 2Al2O319.实验室用锌与稀硫酸反应制氢气 20、锌与盐酸反应制氢气锌+硫酸→硫酸锌+氢气锌+盐酸→氯化锌+氢气Zn +H2SO4 =ZnSO4+H2↑Zn+ 2HCl =ZnCl2+H2↑21.铁与稀硫酸反应 22.铁与盐酸反应铁+硫酸→硫酸亚铁+氢气铁+盐酸→氯化亚铁+氢气Fe +H2SO4 =FeSO4+H2↑Fe+ 2HCl =FeCl2+H2↑23.炼铁的原理一氧化碳+氧化铁高温铁+二氧化碳 3CO+ Fe2O3高温2Fe+3CO224.铁与硫酸铜溶液的反应(我国古代湿法冶金术的原理)25.甲烷燃烧生成二氧化碳和水铁+硫酸铜→铜+硫酸亚铁甲烷+氧气点燃二氧化碳+水Fe+Cu SO4Cu+ FeSO4 CH4+2O2点燃CO2+2H2O26.高温下煅烧石灰石27.氧化钙与水反应高温氧化钙+二氧化碳氧化钙+水→氢氧化钙CaCO3高温CaO+ CO2↑ CaO+ H2O Ca(OH)228.盐酸除铁锈 29.硫酸除铁锈盐酸+氧化铁→氯化铁+水硫酸+氧化铁→硫酸铁+水6HCl+ Fe2O32FeCl3+3H2O 3H2SO4+ Fe2O3 Fe2 (SO4) 3+ 3H2O 30.氢氧化钠+二氧化碳→碳酸钠+水 31.氢氧化钠+硫酸铜→氢氧化铜+硫酸钠2NaOH+ CO2Na2CO3+ H2O 2NaOH+ CuSO4 Cu(OH)2↓+ Na2SO432.碳酸钠+盐酸→氯化钠+水+二氧化. 33.碳酸氢钠+盐酸→氯化钠+水+二氧化碳Na2CO3+2HCl2NaCl+ H2O+ CO2↑NaHCO3+HCl NaCl+ H2O+ CO2↑34.碳酸钠+氢氧化钙→碳酸钙+氢氧化钠35.锌+硫酸铜→铜+硫酸锌Na2 CO3+Ca(OH) 2= CaCO3↓+2NaOH Zn+CuSO4Cu+ZnSO436.铜+硝酸银→银+硝酸....... 37.盐酸与氢氧化钠反应Cu+2AgNO32Ag+Cu(NO3)2HCl+ NaOH NaCl+ H2O。
沪教版初三化学化学方程式

化学方程式一.物质与氧气的反应:(1)单质与氧气的反应:1.镁在空气中燃烧: 2Mg + O2点燃 2MgO2.铁在氧气中燃烧: 3Fe + 2O2点燃 Fe3O43.铝在空气中燃烧: 4Al + 3O2点燃 2Al2O34.铜在空气中受热: 2Cu + O2△ 2CuO5.氢气中空气中燃烧: 2H2+ O2点燃 2H2O6.红磷在空气中燃烧: 4P + 5O2点燃 2P2O57.硫粉在空气中燃烧: S + O2点燃 SO28.碳在氧气中充分燃烧: C + O2点燃 CO29.碳在氧气中不充分燃烧: 2C + O2点燃 2CO(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧2CO + O2点燃 2CO2 11.甲烷在空气中燃烧:CH4+ 2O2点燃 CO2+ 2H2O 12.二氧化硫与氧气反应: 2SO2 + O2 尘埃2SO3二.几个分解反应:13.水在直流电的作用下分解: 2H2O 通电 2H2↑+ O2 ↑14.加热碳酸氢铵: NH4HCO3△ NH3↑ + H2O + CO2 ↑15.加热高锰酸钾: 2KMnO4△K2MnO4 + MnO2 + O2↑16.双氧水和二氧化锰制氧气: 2H2O2MnO2 2H2O + O2↑17.碳酸不稳定而分解: H2CO3 === H2O + CO2↑18.高温煅烧石灰石: CaCO3高温CaO + CO2↑“铜绿”受热的变化Cu2(OH)2CO3△2CuO + CO2↑+ H2O加热氯酸钾2KClO3 = 2KCl +3O2↑三.呼吸、光合作用:19.呼吸作用: C6H12O6 + 6O2 === 6CO2 + 6H2O20.光合作用: 6CO2 + 6H2O 光照叶绿素 C6H12O6 + 6O2四.氧化还原反应21.一氧化碳还原氧化铁: 3CO+ Fe2O3△ 2Fe + 3CO2五.单质、氧化物、酸、碱、盐的相互关系(1)金属单质 + 酸(不包括浓、稀硝酸和浓硫酸) --盐 + 氢气(置换反应)(注意:产生一克氢气所需要金属的质量等于 )22.锌和稀硫酸反应: Zn + H2SO4 === ZnSO4 + H2↑23.铁和稀硫酸反应: Fe + H2SO4 === FeSO4 + H2↑24.镁和稀硫酸反应: Mg + H2SO4 === MgSO4 + H2↑25.铝和稀硫酸反应: 2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑26.锌和稀盐酸反应: Zn + 2HCl=== ZnCl2 + H2↑27.铁和稀盐酸反应: Fe + 2HCl=== FeCl2 + H2↑28.镁和稀盐酸反应: Mg+ 2HCl=== MgCl2 + H2↑29.铝和稀盐酸反应: 2Al + 6HCl === 2AlCl3 + 3H2↑(及此类的具有相同规律的、常见物质参加的反应。
九年级化学沪教版知识点总结

九年级化学沪教版知识点总结Chemistry in the ninth grade involves a wide range of topics that are crucial for understanding the world around us. 九年级的化学涉及了许多重要的主题,这些主题对我们理解周围世界的重要性至关重要。
From the structure of atoms to chemical reactions and the properties of different elements, students will explore the building blocks of matter and how they interact. 从原子结构到化学反应以及不同元素的性质,学生将探索物质的基本构成以及它们之间的相互作用。
Understanding these concepts is not only essential for academic success but also for everyday life. 理解这些概念不仅对于学业成功至关重要,也对日常生活有重要意义。
One of the key topics in ninth-grade chemistry is the periodic table, which organizes all known elements based on their atomic structure and properties. 九年级化学中的一个关键主题是周期表,它根据元素的原子结构和性质对所有已知元素进行了组织。
Students will learn how to read the periodic table and understand the trends in properties as one moves across a period or down a group. 学生将学习如何阅读周期表,并理解在一个周期内或者一个族群中移动时性质的变化趋势。
沪教版九年级化学方程式总结

沪教版九年级上册常见化学反应现象、化学方程式式一、氧气制取,体现氧气氧化性和助燃性化学方程式总结: 1、加热高锰酸钾制取氧气 化学方程式:2KMnO 4K 2MnO 4 + MnO 2 + O 2↑2 化学方程式:2H 2O 22O + O 2↑3、加热二氧化锰和氯酸钾的固体混合物制取氧气化学方程式:2KClO 3 ====2KCl + 3O 2 ↑4、木炭(黑色固体)燃烧:在空气中燃烧红热,在氧气中发出白光,放出热量,生成气体能使澄清石灰水变浑浊。
化学方程式:C + O 2 CO 25、碳不完全燃烧。
化学方程式:2C + O 2 2CO6、一氧化碳燃烧:放出热量、产生淡蓝色火焰,生成气体能使澄清石灰水变浑浊。
化学方程式:2CO + O 2 2CO 27、镁带(银白色固体)在空气中燃烧:剧烈燃烧,发出耀眼的白光,放出热量,生成白色粉末状固体。
化学方程式:2Mg + O 2 2MgO8、铁丝(银白色固体)在氧气中燃烧现象:剧烈燃烧,火星四射,放出热量,生成。
黑色固体。
在空气中不能燃烧。
要预先在集气瓶底部铺少量沙子或加少量水,目的:防止生成的高温熔化物溅落炸裂集气瓶底。
化学方程式:3Fe + 2O 2 Fe 3O 4 9、铜在空气中加热:红色金属变为黑色固体化学方程式:2Cu + O 2 2CuO 10、铝在空气中受热:银白金属变为白色固体化学方程式:4Al + 3O 2 2Al 2O 311、红磷(暗红色固体)或白磷在空气中的燃烧:实验现象:放出热量,产生大量白烟化学方程式: 4P + 5O 2 2P 2O 5 12、硫粉(淡黄色粉末)燃烧现象:在空气中燃烧产生淡蓝色火焰,在氧气中产生蓝紫色火焰,生成有刺激性气味的气体。
要预先在集气瓶底加少量水,目的:吸收有毒气体二氧化硫。
化学方程式:S + O 2SO 213、氢气在空气中燃烧,现象:产生淡蓝色火焰,放出大量的热,烧杯内壁凝结有水雾 化学方程式:2H 2 + O 2 2H 2O 能说明水由H 、O 元素组成 14、甲烷在空气中燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△点燃点燃点燃点燃点燃△点燃点燃点燃点燃点燃Δ MnO 215、酒精在空气中燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O二、CO2制取,体现CO2化学性质方程式总结:1、实验室里常用稀盐酸与大理石或石灰石反应来制取少量二氧化碳气体。
沪教版九年级化学知识点归纳总结

九年级化学主要学习了如下内容:一、物质的性质与结构1.粉末状的二氧化硅对声音具有吸收能力,因而可以用于制作音响材料。
2.铁和铝都属于金属,但铁比铝更容易被磁化。
3.水对金属的腐蚀作用较弱,但可以与金属发生电化学反应。
4.分子运动使物质呈现三态:固态、液态和气态。
分子间作用力决定物质不同态的存在。
5.气体的压强和温度成正比,压强和体积成反比。
6.分子和离子的化学键决定了物质的性质。
二、最简单的物质,金属1.金属的物理性质:延展性、导电性、热导性。
2.金属的化学性质:金属与非金属发生化学反应时,金属通常失去电子形成阳离子。
3.金属在空气中可以与氧气反应生成金属氧化物。
4.金属可以和酸反应生成盐和氢气。
5.金属的碱性越强,与酸反应生成氢气的速度越快。
三、非金属元素和化合物1.非金属元素的特点:不良导电性、不良热导性、易聚集静电电荷。
2.卤素是一种常见的非金属元素,常见气态。
3.硫、氮、碳和氧是生物体中的重要元素。
4.氧和氮都是气体,但氧为带状结构,氮为双键结构。
5.碳可以形成多种结构,如钻石、石墨和纳米管。
四、物质的化学变化与化学方程式1.化学方程式描述了化学反应中物质的消失和生成关系。
2.反应物通过吸收或释放能量产生新的物质。
3.反应速率受温度、浓度和催化剂等因素的影响。
五、酸、碱和盐1.酸具有酸性气味,能与碎纸反应。
2.酸可以与金属生成盐和释放氢气。
3.氧化酸可以与碱反应生成盐和水。
4.碱有苦碱性气味,能与红茶叶反应。
5.碱可以与非金属氧化物反应生成酸性盐和水。
6.盐是酸和碱中的一种化合物,由正离子和负离子组成。
六、化学反应速率与化学平衡1.化学反应速率可以通过观察反应物浓度变化或生成物生成速率来确定。
2.反应速率与反应温度和催化剂等因素有关。
3.平衡状态指的是正向反应和逆向反应的速率相等。
4.平衡常数描述了平衡状态下反应物和生成物浓度的关系。
七、酸碱溶液的电离和中和反应1.弱酸和弱碱在水中不完全电离,生成的氢离子和氢氧根离子的浓度较低。
九年级初三化学方程式汇总沪教版
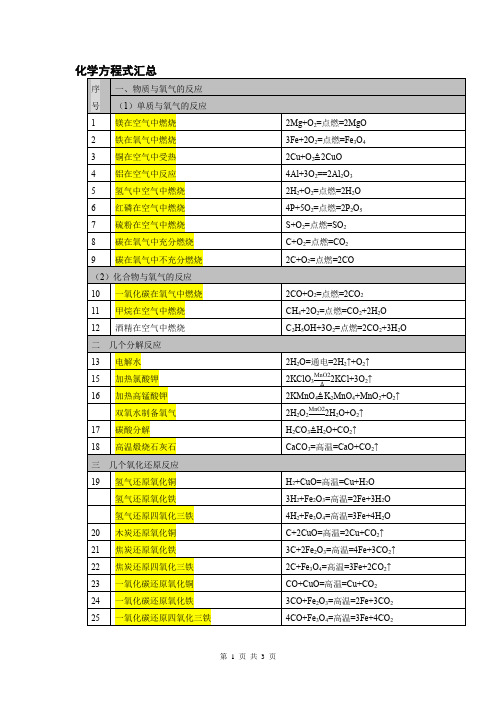
序号
一、物质与氧气的反应
(1)单质与氧气的反应
1
镁在空气中燃烧
2Mg+O2=点燃=2MgO
2
铁在氧气中燃烧
3Fe+2O2=点燃=Fe3O4
3
铜在空气中受热
2Cu+O2 2CuO
4
铝在空气中反应
4Al+3O2==2Al2O3
5
氢气中空气中燃烧
2H2+O2=点燃=2H2O
6
红磷在空气中燃烧
58
硝酸和烧碱反应
HNO3+NaOH====NaNO3+H2O
(6)酸/碱/盐+盐----另一种酸/碱/盐+另一种盐
59
大理石与稀盐酸反应
CaCO3+2HCl====CaCl2+H2O+CO2↑
60
碳酸钠与稀盐酸反应
Na2CO3+2HCl====2NaCl+H2O+CO2↑
61
碳酸镁与稀盐酸反应
MgCO3+2HCl====MgCl2+H2O+CO2↑
66
氢氧化钠与氯化铁
3NaOH+FeCl3====Fe(OH)3↓+3NaCl
67
氢氧化钠与氯化镁
2NaOH+MgCl2====Mg(OH)2↓+2NaCl
68
氢氧化钾与氯化铜
2KOH+CuCl2====Cu(OH)2↓+2KCl
69
氢氧化钙与碳酸钠
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
CaCO3=高温=CaO+CO2↑
沪教版九年级化学方程式汇总

化学方程式是一个很重要的概念,在化学学习的过程中扮演着非常重要的角色。
下面是沪教版九年级化学方程式的汇总内容,共计1200字以上,希望对你的学习有所帮助。
第一节:化学方程式的概念和基本写法(150字)化学方程式是用化学符号和化学式来表示化学反应过程的表达方式。
通常包括反应物、生成物和反应条件三个要素。
一般情况下,方程式的左边表示反应物,右边表示生成物,箭头表示反应的方向。
例如:H2+O2->H2O,表示氢气和氧气生成水。
第二节:化学方程式的平衡(200字)化学方程式的平衡是指在化学反应中反应物和生成物的物质的种类和数量都保持不变的情况下,反应物和生成物的物质量之间的关系。
在化学方程式中,反应物和生成物之间的物质量不一定是相等的,而是通过系数来表示。
例如:2H2+O2->2H2O,表示2个氢气和1个氧气可以生成2个水分子。
第三节:化学方程式的配平(250字)化学方程式的配平是调整反应物和生成物的系数,使得化学方程式中反应物和生成物的物质量之间的关系成为平衡状态。
首先,找出化学方程式中不平衡的原子的种类和数量;然后,通过添加系数来平衡化学方程式。
配平化学方程式需要满足的原则是质量守恒定律和能量守恒定律。
第四节:化学方程式的应用(300字)化学方程式在化学学习中具有广泛的应用。
首先,通过化学方程式可以计算反应物和生成物之间的摩尔比例,从而进行化学计量分析。
其次,通过化学方程式可以预测化学反应的发生和反应的产物。
例如,通过N2+3H2->2NH3的方程式可以预测氮气和氢气可以反应生成氨气。
此外,化学方程式还可以帮助我们理解化学反应的细节和原理,为我们解释化学现象和化学实验提供依据。
第五节:化学反应的类型(300字)化学反应可以分为合成反应、分解反应、置换反应和复分解反应四种类型。
合成反应是指两种或两种以上的物质反应生成一种物质。
例如,2H2+O2->2H2O表示了水的合成反应。
分解反应是指一种物质分解生成两种或两种以上的物质。
沪教版化学易错知识点总结

沪教版化学易错知识点总结化学作为一门实验性较强的科学学科,常常会遇到一些易错的知识点。
掌握这些易错的知识点,对于提高化学学科的学习成绩是非常重要的。
接下来,我们将从易错知识点的角度来总结沪教版化学的一些重点内容。
1.化学方程式的平衡化学方程式的平衡是化学学习中的重点,也是易错知识点。
在平衡化学方程式时,需要注意反应物和生成物的摩尔比例关系,以及原子的个数是否相等。
平衡化学方程式的关键在于通过添加系数来平衡反应物与生成物之间的摩尔比例关系。
2.化学键的性质化学键是分子中原子相互结合的力量。
常见的化学键包括离子键、共价键和金属键等。
其中,离子键是正离子和负离子之间的相互作用力;共价键是非金属原子之间共用电子对的相互作用力;金属键是金属原子之间的电子云共享相互作用力。
对于不同类型的化学键,需要理解其性质和特点,以便正确判断和解答相关的题目。
3.化学反应的速率化学反应的速率是指单位时间内反应物消失或生成物增加的数量。
影响化学反应速率的因素包括温度、浓度、催化剂和表面积等。
在解答与化学反应速率相关的问题时,需要根据题目给出的条件,结合反应速率与温度、浓度、催化剂等因素之间的关系,进行分析和推理。
4.酸碱中和反应酸碱中和反应是酸和碱反应生成盐和水的过程。
在解答酸碱中和反应的问题时,需要了解酸碱的性质和反应规律,以及酸碱滴定中的计算方法。
另外,还需掌握一些常见的酸碱指示剂的颜色变化规律,以便判断酸碱中和反应的终点。
5.锂、钠、钾等金属的性质锂、钠、钾等金属都属于第一族元素,具有相似的化学性质。
这些金属都具有较低的电离能,易失去一个电子形成正离子。
在解答与锂、钠、钾等金属的性质相关的问题时,需要了解它们与水的反应、与酸的反应等特点,以及它们在自然界中的存在形式和用途。
6.氧化还原反应氧化还原反应是一类常见的化学反应,也是容易出错的知识点之一。
在氧化还原反应中,氧化剂得到电子,还原剂失去电子。
根据氧化还原反应的特点,可以通过电子的转移来判断氧化还原反应的类型,如单质氧化还原反应、非金属氧化物与金属反应等。
沪教版九年级化学第一、二章现象

初中化学方程式知识点总结1、澄清石灰水中通入二氧化碳气体 Ca(OH)2 + CO2= CaCO3↓ + H2O(复分解)现象:石灰水由澄清变浑浊。
相关知识点:这个反应可用来检验二氧化碳气体的存在。
2、镁带在空气中燃烧 2Mg + O2= MgO (条件:点燃)现象:发出耀眼的白光,生成白色粉末。
相关知识点:(1)这个反应中,镁元素从游离态转变成化合态;(2)物质的颜色由银白色转变成白色。
3、水的电解 2H2O=2H2↑ + O2↑(分解)(条件:通电)现象:阴极、阳极有大量的气泡产生相关知识点:(1)阳极产生氧气,阴极产生氢气;(2)氢气和氧气的体积比为2:1,质量比为1:8。
4、生石灰和水反应 CaO + H2O = Ca(OH)2(化合)现象:白色粉末溶解。
相关知识点:(1)最终所获得的溶液名称为氢氧化钙溶液,俗称澄清石灰水;(2)在其中滴入无色酚酞,酚酞会变成红色;(3)生石灰是氧化钙,熟石灰是氢氧化钙。
5、铜粉在空气中受热 2Cu + O2=2CuO(化合)(条件:加热)现象:红色物质逐渐变成黑色粉末相关知识点:这是用来粗略测定空气中氧气体积百分含量的实验。
6、实验室制取氧气(加热氯酸钾和二氧化锰的混合物)2KClO3 = 2KCl + 3O2↑(分解)(条件:加热,MnO2,)相关知识点:(1)二氧化锰在其中作为催化剂,加快氯酸钾的分解速度或氧气的生成速度;(2)二氧化锰的质量和化学性质在化学反应前后没有改变;(3)反应完全后,试管中的残余固体是氯化钾和二氧化锰的混合物,进行分离的方法是:溶解、过滤、蒸发。
PS: 2 KMnO4 = K2MnO4+ MnO2+ O2↑(条件:加热)2 H2O2= 2H2O + O2↑(条件: MnO2,)7、木炭在空气(或氧气)中燃烧 C + O2= CO2(化合)(条件:点燃)现象:在空气中是发出红光,在氧气中是发出白光;相关知识点:反应后的产物可用澄清的石灰水来进行检验。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
四川省遂宁中学 2012-5-10
九年级化学(沪教版)化学方程式整理小结
一.化合反应
1.镁带燃烧: 2Mg + O 2 ==== 2MgO
2.铁丝燃烧:3Fe + 2O 2 ==== Fe 3O 4
3.铜丝加热: 2Cu + O 2 === 2CuO
4.铝丝加热或形成氧化膜:4Al + 3O 2 === 2Al 2O 3
5.氢气燃烧或爆炸: 2H 2 + O 2 === 2H 2O
6.碳的燃烧:2C + O 2 ==== 2CO (不完全燃烧);C + O 2 === CO 2(完全燃烧) 7.硫的燃烧:S + O 2 === SO 2
8.磷的燃烧:4P + 5O 2 === 2P 2O 5
9.二氧化碳被碳还原:C + CO 2 === 2CO
10.生石灰溶于水:CaO + H 2O == Ca(OH)2
11.二氧化碳溶于水:CO 2 + H 2O == H 2CO 3
12.二氧化硫溶于水:SO 2 + H 2O == H 2SO 3
13.二氧化硫在空气中转化为三氧化硫:2SO 2 + O 2 ==== 2SO 3
14.三氧化硫溶于水:SO 3 + H 2O == H 2SO 4
15.工业上制盐酸(氢气在氯气中燃烧):H 2 + Cl 2 === 2HCl
16.金属钠在氯气中燃烧:2Na + Cl 2 2HCl
17.浓盐酸与浓氨水相靠近:NH 3 + HCl == NH 4Cl
二.分解反应
1.碳酸氢铵(碳铵)受热分解:NH 4HCO 3 NH 3↑+ CO 2↑+ H 2O
2.碱式碳酸铜(铜绿受热分解):Cu 2(OH)2CO 3 2CuO + H 2O + CO 2↑
3.加热高锰酸钾制氧气:2KMnO 4 K 2MnO 4 + MnO 2 + O 2↑
4.二氧化锰催化双氧水制氧气:2H 2O 2 2H 2O + O 2↑
5.电解水:2H 2O 2H 2↑+ O 2↑
6.碳酸分解:H 2CO 3 == CO 2↑+ H 2O
7.碳酸钙高温煅烧分解:CaCO 3 CaO + CO 2↑
8.电解熔融状态的氧化铝制取金属铝:2Al 2O 3 4Al + 3O 2↑
三.置换反应
1. 氢气还原金属氧化物:Fe 2O 3 + 3H 2 2Fe + 3H 2O ;Fe 3O 4 + 4H 2 3Fe + 4H 2O ; CuO + H 2 Cu + H 2O
2.碳粉还原金属氧化物:2Fe 2O 3 + 3C 4Fe + 3CO 2↑;Fe 3O 4 + 2C 3Fe + 2CO 2↑; 2CuO + C 2Cu + CO 2↑
3.铝与盐酸、硫酸反应制氢气:
2Al + 6HCl == 2AlCl 3 + 3H 2↑;2Al + 3H 2SO 4 == Al 2(SO 4)3 +3H 2↑
4.镁与盐酸、硫酸反应制氢气:Mg + 2HCl == MgCl 2 + H 2↑;Mg + H 2SO 4 == MgSO 4 + H 2↑
5.铁与盐酸、硫酸反应制氢气:Fe + 2HCl == FeCl 2 + H 2↑;Fe + H 2SO 4 == FeSO 4 + H 2↑
6.锌与盐酸、硫酸反应制氢气:Zn + 2HCl == ZnCl 2 + H 2↑;Zn + H 2SO 4 == ZnSO 4 + H 2↑
7.湿法炼铜法,铁与硫酸铜溶液反应:Fe + CuSO 4 == FeSO 4 + Cu
△ 点燃 点燃 △ 点燃 点燃 点燃
点燃
点燃 高温 粉尘等 点燃 点燃 === △ === △ === △ === MnO 2 === 通电 === 高温 === 通电 === 高温 === 高温 === 高温 === 高温 === 高温 === 高温 ===
四川省遂宁中学 2012-5-10
8.铜与硝酸银溶液反应:Cu + 2AgNO 3 == Cu(NO 3)2 + 2Ag
四.复分解反应: 1.酸碱中和反应:HCl + NaOH == NaCl + H 2O ;Cu(OH)2 + H 2SO 4 == CuSO 4 + 2H 2O
H 2SO 4 + Ba(OH)2 == BaSO 4↓+ 2H 2O ;Ca(OH)2 + 2HCl == CaCl 2 +2H 2O
2.金属氧化物与酸溶液反应:Fe 2O 3 + 6HCl == 2FeCl 3 + 3H 2O ;CuO + H 2SO 4 == CuSO 4 + H 2O MgO + 2HCl == MgCl 2 + H 2O ;Al 2O 3 + 3H 2SO 4 == Al 2(SO 4)3 + 3H 2O
3.碳酸盐与酸溶液反应:CaCO 3 + 2HCl == CaCl 2 + CO 2↑+ H 2O ;
Na 2CO 3 + 2HCl == 2NaCl+ CO 2↑+ H 2O
K 2CO 3 + H 2SO 4 == K 2SO 4 + CO 2↑+ H 2O
4.盐溶液与碱溶液反应:Na 2CO 3 + Ca(OH)2 == CaCO 3↓+ 2NaOH ;
CuSO 4 + 2NaOH== Cu(OH)2↓+Na 2SO 4
CuSO 4 + Ba(OH)2 == BaSO 4↓+ Cu(OH)2↓
5.Ag +与Cl -反应:HCl + AgNO 3 == AgCl ↓+ HNO 3;NaCl + AgNO 3 == AgCl ↓+ NaNO 3
6.Ba 2+与SO 42-反应:BaCl 2 + CuSO 4 == BaSO 4↓+ CuCl 2;H 2SO 4 + BaCl 2 == BaSO 4↓+ 2HCl
7.纯碱与氯化钙溶液反应:Na 2CO 3 + CaCl 2 == CaCO 3↓+ 2NaCl
8.铵盐与碱反应产生氨气:NH 4NO 3 + NaOH == NaNO 3 + NH 3↑+ H 2O
(NH 4)2SO 4 + Ca(OH)2 == CaSO 4 + 2NH 3↑+ 2H 2O
五.其他反应类型:
1.一氧化碳还原金属氧化物:Fe 2O 3 + 3CO 2Fe + 3CO 2;Fe 3O 4 + 4CO 3Fe + 4CO 2;
CuO + CO Cu + CO 2
2.非金属氧化物与碱溶液反应:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O ;
CO 2 +2NaOH == Na 2CO 3 + H 2O
SO 2 +2NaOH == Na 2SO 3 + H 2O
SiO 2+Na 2CO 3高温Na 2SiO 3 + CO 2↑
3.有机物燃烧:CH 4 + 2O 2 CO 2 + 2H 2O ; C 2H 6O + 3O 2 2CO 2 + 3H 2O
C 6H 12O 6 + 6O 2 6CO 2 + 6H 2O
C x H y O z + (
424z y x -+)O 2 xCO 2 + 2
y H 2O 4.绿色植物光合作用:6CO 2 + 6H 2O C 6H 12O 6 + 6O 2 高温 === 高温 === 高温 === 点燃 === 点燃 === 点燃 === 点燃 === 光照 === 叶绿素。
