无机及分析化学第七章答案
无机及分析化学第七章 定量分析方法概述课后练习与答案

第七章分析化学概论一、选择题1.消除测量过程中的偶然误差的方法是( )A.空白实验 B.对照实验 C.增加平行测定次数 D.校正仪器2. 下列物质可采用直接法配制标准溶液的是 ( )A.NaOH B.HCl C.无水Na2CO3 D.KMnO43.下列说法错误的是 ( )A.系统误差又称为可测误差 B.系统误差具有单向性C.方法误差属于系统误差 D.偶然误差可完全消除4.下列属于偶然误差的是 ( )A.使用生锈的砝码称量B.标定HCl时所用Na2CO3不纯C.所用试剂含待测组分D.滴定管读数时最后一位估计不准5.05.2010 .01250.0的有效数字位数为( )A.4 B.2C.3 D.16.pH=10.02的有效数字位数为 ( )A.4 B.2C.3 D.无法确定7.用失去结晶水的Na2B4O7.10H2O标定HCl溶液,则测得的浓度会 ( ) A.偏高B.偏低C.与实际浓度一致D.无法确定8.滴定分析中,指示剂颜色发生突变的这一点称为 ( )A.化学计量点B.滴定终点C.既是化学计量点,也是滴定终点D.以上都不对9.测定CaCO3含量时,先加入一定量并且过量的HCl溶液,然后用NaOH标准溶液滴定剩余的HCl溶液,此滴定方式属于( )A.直接滴定B.返滴定C.置换滴定D.简接滴定10.常量分析的试样用量为 ( )A .大于1.0gB .1.0~10gC .大于0.1gD .小于0.1g11.滴定分析中,滴定管的读数误差为±0.01mL ,滴定管的一次滴定需读初、终两次读数,可能引起的最大误差为±0.02mL ,为使滴定的相对误差小于0.1%,终点时消耗的滴定剂的体积至少为 ( )A .10mLB .15mLC .20mLD .无法确定12.用25mL 常量酸碱滴定管进行滴定,结果记录正确的是( )A .18.2B .18.20C .18D .18.00013.已知T HCI/NaON =0.004000 g/ml 、则C HCI 为( )A .0.1000mol/LB .0.004000g/mlC .0.003600g/mlD .0.1097mol/L14.滴定管的读数误差为±0.02ml,若滴定时用去滴定液20.00ml ,则相对误差是( )A .±0.1%B .±0.01%C .±1.0%D .±0.001%15.在标定NaOH 溶液浓度时,某同学的四次测定结果分别为0.1023 mol ·L -1、0.1024 mol ·L -1、0.1022 mol ·L -1、0.1023 mol ·L -1,而实际结果应为0.1088 mol ·L -1,该学生的测定结果 ( )A .准确度较好,但精密度较差B .准确度较差,但精密度较好C .准确度较差,精密度也较差D .系统误差小,偶然误差大16.在定量分析结果的一般表示方法中,通常要求( )A .d R ≤2%B .d R ≤0.02%C .d R ≥0.2% D.d R ≤0.2% 17.T A/B 表示的意义是 ( )A .100ml 标准溶液A 中所含溶质的质量B .1ml 标准溶液A 中所含溶质的质量C .1L 标准溶液A 相当于被测物质B 的质量D .1ml 标准溶液A 相当于被测物质的质量18.T HCl/NaOH =0.003000g/ml ,终点时HCl 消耗40.00 ml ,试样中NaOH 的质量为( )A .0.1200gB .0.01200gC .0.001200gD .0.1200mg19.欲配制1000ml 0.1mol/L HCl 溶液,应取浓盐酸(12mol/L HCl)( )ml 。
无机及分析化学知到章节答案智慧树2023年齐鲁工业大学

无机及分析化学知到章节测试答案智慧树2023年最新齐鲁工业大学第一章测试1.无机及分析化学就是将无机化学和分析化学有机整合,集二者的基础性和实用性于一身的一门化学专业基础课程,是大学化学的基石和化学研究的起点。
参考答案:对2.测定常量组分的某样品中硫酸根的含量,可采用硫酸钡重量分析法。
参考答案:对3.从历史上看,无机化学是发展最早的一门化学分支学科,是化学研究的先驱。
参考答案:对4.以化学反应为基础的分析方法,称为:参考答案:化学分析法5.通常所说的四大化学是指?参考答案:物理化学;有机化学;无机化学;分析化学6.本课程包含化学的哪两个二级学科?参考答案:分析化学;无机化学7.下列哪些内容属于无机化学的研究对象?参考答案:电化学;配位化学;化学热力学;结构化学;化学动力学;元素化学第二章测试1.已知置信度为90%,n = 6 时,t =2.015,在一组平行测定中, 所得测定结果如下: 8.44, 8.32, 8.45, 8.52, 8.69, 8.38,下列内容正确的是参考答案:置信度为90%时平均值的置信区间8.47±0.11;标准偏差为0.132.已知n = 6 时,Q0.90 = 0. 56。
在一组平行测定中,所得测定结果如下:10.56,10.44,10.57,10.64,10.81,10.50,则参考答案:所有数据都是可靠值3.系统误差具有重现性,是可测误差参考答案:对4.带有偶然误差的测量数据,不能参加平均值的计算参考答案:错5.滴定分析中,指示剂确定的滴定终点与化学计量点不一致,由此产生的误差属于试剂误差。
参考答案:错6.系统误差主要影响分析测定中的准确度参考答案:对7.pM=-lg[Mn+]=3.00,金属离子浓度[Mn+]有效数字位数为3位参考答案:错8.对于同一组测定数据,置信度越小,置信区间越小。
参考答案:对9.用分析天平采用减量法称量试样,要使称量误差不大于0.1%,至少要称取试样参考答案:0.2g10.已知 pH=5.25,则[ H+ ]=5.62×10-6mol•L-1 。
无机及分析化学第七章选择题及答案

20. 重量分析中的沉淀形式应当符合(D)A. 溶解度小B. 沉淀纯净含杂质少C. 相对分子量尽量大D. A、B和C17. Ca3(PO4)2的溶解度为a/2 mol·L-1,其Ksp为 ( D)(A). 36a5 (B) 4 a5/ 9 (C) 9a5 /4 (D) 27a5 /87.已知在一定的温度下,CdCO3的Ksp=×10-12,Cd(OH)2的Ksp=×10-14,那么它们在水中的溶解度:( B )>Cd(OH)2 <Cd(OH)2= Cd(OH)2D.不能确定13. AgNO3处理[Fe(H2O)5Cl]Br溶液,产生沉淀主要是 ( A )A. AgBrB. AgClC. AgBr和AgClD. Fe(OH)3存在下,AgCl的溶解度比纯水中大,原因是(C)(A)同离子效应(B)酸效应(C)盐效应(D)配位效应9. 在沉淀反应中,加入易溶电解质会使沉淀的溶解度增加,该现象是( B)A. 同离子效应B. 盐效应C. 酸效应D. 配位效应5. 某物质的化学式是AB3,其溶解度S和容度积常数KspΘ的关系式是(C)A. Ksp Θ=2S2 B. KspΘ=2S3 C. KspΘ=27S4 D. KspΘ=4S29、已知在一定的温度下,CdCO3的Ksp=×10-12,Cd(OH)2的Ksp=×10-14,那么它们在水中的溶解度:B(1)CdCO3>Cd(OH)2(2)CdCO3<Cd(OH)2(3)CdCO3= Cd(OH)2(4)不能确定16、Ag2S的溶度积Ksp的表示式为:D(1)Ksp =c(Ag+)c(s2-) (2)Ksp= c(Ag+)c(s2-) 2(3)Ksp = 2c(Ag+)c(s2-) (4)Ksp= c(Ag+) 2c(s2-)11. 过量AgCl溶解在下列各物质中,问哪种溶液中Ag+浓度最小(D)A. 100 cm3水B. 1000 cm3水C. 1000 cm3 mol·dm-3KNO3溶液 D. 100 cm3 mol·dm-3KCl溶液20.关于晶型沉沉淀的条件,下列说法错误的是: ( D)(A)沉淀反应应当在适当稀的溶液中进行;(B)沉淀作用应当在热溶液中进行;(C)沉淀完毕后进行陈化使沉淀晶体完整、纯净;(D)当沉淀剂是挥发性物质时,沉淀剂用量应为其理论用量的200%为宜。
兰叶青无机及分析化学课后习题答案(所有章节)

第二章 习题解答2-10解:(1)×;(2)×;(3)√;(4)×;(5)×;(6)×;(7)×;(8)×;(9);(10)×;(11)×2-11解:(1)敞开体系;(2)孤立体系;(3)敞开体系;2-12解:(1) Q =100kJ W=-500 kJ △U = Q + W=-400 kJ(2)Q =-100kJ W=500 kJ △U = Q + W=400 k2-13解:因为此过程为可逆相变过程,所以Q p =△H= ·mol -1W=-p 外△V ≈-n R T =-×=- kJ ·mol -1 △U = Q + W= +(-)= kJ ·mol -12-14解:(1)r m B f m Bf m 2f m f m f m 231B)3CO g Fe,s 3CO,g Fe O ,s 3393.51203(110.52)(822.2)26.77kJ mol H H H H H H -∆=ν∆=∆∆-∆+∆=⨯-⨯-⨯---=-⋅∑((,)+2()()()()+ΘΘΘΘΘΘ(2)r m B f m Bf m 2f m 2f m f m 21B)CO g H ,g CO,g H O,g 393.510(110.52)(241.82)41.17kJ mol H H H H H H -∆=ν∆=∆∆-∆+∆=-----=-⋅∑((,)+()()()()+ΘΘΘΘΘΘ(3)r m B f m Bf m 2f m f m 2f m 31B)6H O l NO,g 5O ,g 4NH ,g 6285.834(90.25)504(46.11)1169.54kJ mol H H H H H H -∆=ν∆=∆∆-∆+∆=⨯-⨯-⨯-⨯-=-⋅∑((,)+4()()()()+ΘΘΘΘΘΘ2-15解:乙醇的Θm f H ∆反应r m H ∆Θ为:(4) 2C (s ,石墨)+3H 2(g )+1/2O 2(g )= C 2H 5OH (l ),所以:反应(4)=反应(2)×2+反应(3)×3-反应(1)r m r m r m r m -1(4)2(2)3(3)(1)2(393.5)3(571.6)(1366.7)1135.1kJ mol H H H H ∆=∆+∆-∆=⨯-+⨯---=-⋅ΘΘΘΘ对反应2C (s ,石墨)+ 2H 2(g )+ H 2O (l )= C 2H 5OH (l )r m f m f m 2f m 2f m 1()(H O,l)2(H ,g)2(C,s)1135.1(285.83)2020849.27kJ mol H H H H H -∆=∆-∆-∆-∆=----⨯-⨯=-⋅乙醇ΘΘΘΘΘ虽然,该反应的r m H ∆Θ<0(能量下降有利),但不能由r m H ∆Θ单一确定反应的方向,实际反应中还须考虑其他因素,如:混乱度、反应速率等。
分析化学第7章课后习题答案

分析化学第7章课后习题答案第七章氧化还原滴定1.条件电位和标准电位有什么不同影响电位的外界因素有哪些答:标准电极电位E′是指在⼀定温度条件下(通常为25℃)半反应中各物质都处于标准状态,即离⼦、分⼦的浓度(严格讲应该是活度)都是1mol/l(或其⽐值为1)(如反应中有⽓体物质,则其分压等于×105Pa,固体物质的活度为1)时相对于标准氢电极的电极电位。
电对的条件电极电位(E0f)是当半反应中氧化型和还原型的浓度都为1或浓度⽐为,并且溶液中其它组分的浓度都已确知时,该电对相对于标准氢电极电位(且校正了各种外界因素影响后的实际电极电位,它在条件不变时为⼀常数)。
由上可知,显然条件电位是考虑了外界的各种影响,进⾏了校正。
⽽标准电极电位则没有校正外界的各种外界的各种因素。
影响条件电位的外界因素有以下3个⽅⾯;(1)配位效应;(2)沉淀效应;(3)酸浓度。
2.是否平衡常数⼤的氧化还原反应就能应⽤于氧化还原中为什么答:⼀般讲,两电对的标准电位⼤于(K>106),这样的氧化还原反应,可以⽤于滴定分析。
实际上,当外界条件(例如介质浓度变化、酸度等)改变时,电对的标准电位是要改变的,因此,只要能创造⼀个适当的外界条件,使两电对的电极电位超过,那么这样的氧化还原反应也能应⽤于滴定分析。
但是并不是平衡常数⼤的氧化还原反应都能应⽤于氧化还原滴定中。
因为有的反应K虽然很⼤,但反应速度太慢,亦不符合滴定分析的要求。
3.影响氧化还原反应速率的主要因素有哪些答:影响氧化还原反应速度的主要因素有以下⼏个⽅⾯:1)反应物的浓度;2)温度;3)催化反应和诱导反应。
4.常⽤氧化还原滴定法有哪⼏类这些⽅法的基本反应是什么答:1)⾼锰酸钾法.2MnO4+5H2O2+6H+==2Mn2++5O2↑+8H2O.MnO2+H2C2O4+2H+==Mn2++2CO2+2H2O2) 重铬酸甲法. Cr2O72-+14H++Fe2+===2Cr3++Fe3++7H2OCH3OH+Cr2O72-+8H+===CO2↑+2Cr3++6H2O3)碘量法 3I2+6HO-===IO3-+3H2O,2S2O32-+I2===2I-+2H2OCr2O72-+6I-+14H+===3I2+3Cr3++7H2O5.应⽤于氧化还原滴定法的反应具备什么条件答:应⽤于氧化还原滴定法的反应,必须具备以下⼏个主要条件:(1)反应平衡常数必须⼤于106,即△E>。
第七章习题答案

第七章1.计算氢原子核外电子从第三能级跃迁到第二能级时产生的谱线H α的波长与频率。
解: ν = R H ⎪⎭⎫ ⎝⎛-222111n n= 3.289 ⨯ 1015⎪⎪⎭⎫⎝⎛-223121s -1= 4.57⨯1014s -1νλc= =11418s 1057.4s m 10998.2--⨯⋅⨯= 656⨯10-9m= 656nm2.计算基态氢原子的电离能为多少? 解: I = ∆E = h ν= 6.626⨯10-34 J ⋅s ⨯3.289⨯1015s -1(1/12 -1/∞)=2.179⨯10-18J3.下列各组量子数哪些是不合理的?为什么?n l m(1) 2 1 0(2) 2 2 -1(3) 2 3 +2解:(1)合理;(2) l 取值不合理,应小于n ;(3) l 、m 取值不合理,l 应小于n ,m 取值为0, ±1, ±2,⋯ ± l ;4.用合理的量子数表示:(1)3d 能级; (2)4s 1电子解:(1)3d 能级: n =3,l =2;(2)4s 1电子:n =4,l =0,m = 0;5.分别写出下列元素基态原子的电子分布式,并分别指出各元素在周期表中的位置。
9F 10Ne 25Mn 29Cu 24Cr 55Cs 71Lu解:9F 1s 22s 22p 5 第二周期VIIA 族 10Ne [He]2s 22p 6 第二周期VIIIA 族25Mn [Ar]3d 54s 2 第四周期VIIB 族 29Cu [Ar]3d 104s 1 第四周期I B 族24Cr [Ar]3d 54s 1 第四周期VI B 族 55Cs [Xe]6s 1 第六周期I A 族71Lu [Xe]4f 145d 16s 2 第六周期IIIB 族6.以(1)为例,完成下列(2)~(4)题。
(1)Na (Z = 11) [Ne]3s 1 ; (3 ) (Z =24) [ ? ] 3d 54s 1;(2) 1s 22s 22p 63s 23p 3 ; (4 ) Kr (Z = ) [ ? ] 3d 104s 24p 6;解:(1) Na (Z = 11) [Ne]3s 1 ; (3 ) Cr (Z =24) [Ar ] 3d 54s 1;(2) P(Z=15) 1s 22s 22p 63s 23p 3 ; (4 ) Kr (Z = 36 ) [Ar] 3d 104s 24p 6;7.写出下列离子的最外层电子分布式:S 2-K + Pb 2+ Ag + Mn 2+ Co 2+ 解:8.试完成下表。
无机化学第七章 练习答案

第七章 练习一、填空题1. 在H 2SO 4、Na 2S 2O 3、Na 2S 4O 6中S 的氧化值分别为_____、_____、_____。
+6;+2;+2.52. 在原电池中,流出电子的电极为_____,接受电子的电极为_____,在正极发生的是_____,负极发生的是_____。
原电池可将_____能转化为_____能。
负极;正极;还原反应;氧化反应;化学;电3. 在原电池中,θE 值大的电对为_____极,θE 值小的电对为______极;电对的θE 值越大,其氧化型______越强;电对的θE 值越小,其还原型______越强。
正;负;得电子能力;失电子能力4. 反应2Fe 3+(aq )+ Cu (s )→ 2Fe 2+(aq )+ Cu 2+(aq )与Fe (s )+ Cu 2+(aq )→ Fe 2+(aq )+Cu (s )均正向进行,其中最强的氧化剂为_____,最强的还原剂为______。
+3Fe Fe5. 电对Ag +/Ag ,I 2/I -,-3BrO /-Br ,O 2/H 2O ,Fe(OH)3/Fe(OH)2的E 值随溶液pH 变化的是________。
-3BrO /-Br ,O 2/H 2O ,Fe(OH)3/Fe(OH)26. 已知θsp K (Fe(OH)2)>>θsp K (Fe(OH)3,θf K (+363)(NH Co )>>θfK (+263)(NH Co ) 比较下列标准电极电势的大小。
θE (Fe(OH)3/Fe(OH)2)_____θE (Fe 3+/Fe 2+)θE (+363)(NH Co /+263)(NH Co )_____θE (Co 3+/Co 2+)θE (Cu 2+/-2CuI )______θE (Cu 2+/Cu +)θE (-24HgI /Hg )______θE (Hg 2+/Hg ) <;<;>;<7.已知反应(1)Cl 2(g )+2-Br (aq )→Br 2(l )+2Cl -(aq )(2)21Cl 2(g )+-Br (aq )→21Br 2(l )+Cl -(aq )则z 1/z 2=_____;θ1MF E /θ2MF E =______;θ1m r G ∆/θ2m r G ∆=______; θ1lg K /θ2lg K =______。
无机及分析化学智慧树知到课后章节答案2023年下长江师范学院

无机及分析化学智慧树知到课后章节答案2023年下长江师范学院长江师范学院第一章测试1.化学主要是在分子、原子或离子等层次上研究物质的组成,结构,性能,相互变化以及变化过程中能量关系的科学。
()A:错 B:对答案:对2.卢瑟福提出了量子化原子模型,揭示了原子内部的构造奥秘,认识了物质的无限可分性。
()A:对 B:错答案:错3.化学变化的特点是()A:反应前后质量守恒,且有新物质生成B:电荷守恒C:质量守恒D:能量守恒答案:反应前后质量守恒,且有新物质生成4.把分子中的原子重新组合,但原子不变的运动称为()A:物理运动B:核反应运动C:化学运动D:微观运动答案:化学运动5.被恩格斯称为化学之父的科学家是:()A:盖斯B:拉瓦锡C:道尔顿D:门捷列夫答案:道尔顿6.发现氧元素的科学家是()。
A:波义尔B:道尔顿C:拉瓦锡D:门捷列夫答案:拉瓦锡第二章测试1.稀溶液的依数性中起决定性的性质是溶液的蒸气压下降。
()A:对 B:错答案:对2.质量相同的N2和O2,在同温同压下,它们的体积比为7:8。
()A:错 B:对答案:错3.理想气体状态方程用于真实气体的条件是()A:高温、高压B:低温、低压C:高温、低压D:低温、高压答案:高温、低压4.由过量KBr溶液与AgNO3溶液混合得到的溶胶,其()A:溶胶是负溶胶B:反离子是NO3-C:电位离子是Ag+D:扩散层带负电答案:溶胶是负溶胶5.比较① 0.1 mol·L-1 Na2SO4溶液;② 0.1 mol·L-1 CH3COOH溶液;③ 0.1mol·L-1 C6H12O6溶液④ 0.1 mo l·L-1 NaCl溶液。
各水溶液的渗透压从大到小的顺序为:()A:①﹥③﹥④﹥②B:④﹥③﹥①﹥②C:①﹥④﹥②﹥③D:①﹥②﹥③﹥④答案:①﹥④﹥②﹥③6.68%HNO3(相对分子质量为63,密度ρ为1.40g.ml-1)水溶液,质量摩尔浓度为()。
无机及分析化学第7章 习题解答

第七章 水溶液中的解离平衡 习题解答1.写出下列物质的共轭酸。
S 2-、SO 42-、H 2PO 4-、HSO 4-、NH 3、NH 2OH 、55C H N 。
1.依次为:HS -、HSO 4-、H 3PO 4、H 2SO 4、NH 4+、NH 2OH ⋅H +、55C H N ⋅H +。
2.写出下列物质的共轭碱。
H 2S 、HSO 4-、H 2PO 4-、H 2SO 4、NH 3、NH 2OH 、3+26[Al(H O)]。
2.依次为:HS -、SO 42-、HPO 42-、HSO 4-、NH 2-、NH 2O -、2+25[Al(OH)(H O)]。
3.根据酸碱质子理论,按由强到弱的顺序排列下列各碱。
NO 2-、SO 42-、HCOO -、HSO 4-、Ac -、CO 32-、S 2-、ClO 4-。
3.下列碱由强到弱的顺序:S 2-> CO 32-> Ac-> HCOO-> NO 2-> SO 42-> HSO 4-> ClO 4-1414.151010-- 1410.251010-- 144.741010-- 143.741010-- 143.371010-- 141.991010--4.pH =7.00的水溶液一定是中性水溶液吗?请说明原因。
4.不一定。
K w 随温度的改变而改变,在常温下它的值为10-14,此时的中性溶液pH 为7.005.常温下水的离子积w K θ=1.0×10-14,是否意味着水的解离平衡常数K θ=1.0×10-14?5.不。
w K θ=[H +][OH -],而K θ=[H +][OH -]/c (H 2O);c (H 2O)=11000/18.0255.5mol L 1-=⋅ 6.判断下列过程溶液pH 的变化(假设溶液体积不变),说明原因。
(1)将NaNO 2加入到HNO 2溶液中; (2)将NaNO 3加入到HNO 3溶液中; (3)将NH 4Cl 加入到氨水中; (4)将NaCl 加入到HAc 溶液中;6. (1)pH 变大。
国开作业无机及分析化学(本)-第7章单元测验46参考(含答案)

题目:在组成原电池时,盐桥的主要作用是提供电解质保持两个半电池中的电荷平衡,维持电池反应的进行。
选项A:对
选项B:错
答案:对
题目:将氢电极 (p(H2)=100kPa) 插入纯水中与标准氢电极组成原电池,则EMF为
选项A:0.828 V。
选项B:—0.414 V;
选项C:0.414 V;
选项D:0 V;
答案:0.414 V;
题目:下列反应均能正向进行:
FeCl3 + Cu → FeCl2 + CuCl2
KMnO4 + FeSO4 + H2SO4 → MnSO4 + Fe2(SO4)3 + K2SO4 + H2O
由此可以判断,其中电极电势最大的电对是
选项A:Cu2+ / Cu ;
选项B:Fe3+ / Fe2+ ;
选项C:H+ / H2 ;
选项D:MnO4- / Mn2+ 。
答案:MnO4- / Mn2+ 。
题目:在实际应用中,经常采用饱和甘汞电极作为参比电极,其电极电势是0.2415V,电极中的离子浓度为1.0 mol·L-1 。
选项A:对
选项B:错
答案:错
题目:p ( H2 ) = 100kPa 时,在下列各溶液中, E ( H+ / H2 )最小的是选项A:1.0 mol·L-1 H2SO4 ;
选项B:1.0 mol·L-1 NaOH。
选项C:0.50 mol·L-1 NaOH ;
选项D:1.0 mol·L-1 HCl ;
答案:1.0 mol·L-1 NaOH。
无机及分析化学第7章 习题解答

第七章 水溶液中的解离平衡 习题解答1.写出下列物质的共轭酸。
S 2-、SO 42-、H 2PO 4-、HSO 4-、NH 3、NH 2OH 、55C H N 。
1.依次为:HS -、HSO 4-、H 3PO 4、H 2SO 4、NH 4+、NH 2OH ⋅H +、55C H N ⋅H +。
2.写出下列物质的共轭碱。
H 2S 、HSO 4-、H 2PO 4-、H 2SO 4、NH 3、NH 2OH 、3+26[Al(H O)]。
2.依次为:HS -、SO 42-、HPO 42-、HSO 4-、NH 2-、NH 2O -、2+25[Al(OH)(H O)]。
3.根据酸碱质子理论,按由强到弱的顺序排列下列各碱。
NO 2-、SO 42-、HCOO -、HSO 4-、Ac -、CO 32-、S 2-、ClO 4-。
3.下列碱由强到弱的顺序:S 2-> CO 32-> Ac-> HCOO-> NO 2-> SO 42-> HSO 4-> ClO 4-1414.151010-- 1410.251010-- 144.741010-- 143.741010-- 143.371010-- 141.991010--4.pH =7.00的水溶液一定是中性水溶液吗?请说明原因。
4.不一定。
K w 随温度的改变而改变,在常温下它的值为10-14,此时的中性溶液pH 为7.005.常温下水的离子积w K θ=1.0×10-14,是否意味着水的解离平衡常数K θ=1.0×10-14?5.不。
w K θ=[H +][OH -],而K θ=[H +][OH -]/c (H 2O);c (H 2O)=11000/18.0255.5mol L 1-=⋅ 6.判断下列过程溶液pH 的变化(假设溶液体积不变),说明原因。
(1)将NaNO 2加入到HNO 2溶液中; (2)将NaNO 3加入到HNO 3溶液中; (3)将NH 4Cl 加入到氨水中; (4)将NaCl 加入到HAc 溶液中;6. (1)pH 变大。
无机及分析化学第七章定量分析方法概述课后练习与答案

无机及分析化学第七章定量分析方法概述课后练习与答案第七章分析化学概论一、选择题1.消除测量过程中的偶然误差的方法是( )A.空白实验 B.对照实验 C.增加平行测定次数 D.校正仪器2. 下列物质可采用直接法配制标准溶液的是 ( )A.NaOH B.HCl C.无水Na2CO3 D.KMnO43.下列说法错误的是 ( )A.系统误差又称为可测误差 B.系统误差具有单向性C.方法误差属于系统误差 D.偶然误差可完全消除4.下列属于偶然误差的是 ( )A.使用生锈的砝码称量B.标定HCl时所用Na2CO3不纯C.所用试剂含待测组分D.滴定管读数时最后一位估计不准5.05.2010 .01250.0的有效数字位数为( )A.4 B.2C.3 D.16.pH=10.02的有效数字位数为 ( )A.4 B.2C.3 D.无法确定7.用失去结晶水的Na2B4O7.10H2O标定HCl溶液,则测得的浓度会 ( ) A.偏高B.偏低C.与实际浓度一致D.无法确定8.滴定分析中,指示剂颜色发生突变的这一点称为 ( )A.化学计量点B.滴定终点C.既是化学计量点,也是滴定终点D.以上都不对9.测定CaCO3含量时,先加入一定量并且过量的HCl溶液,然后用NaOH标准溶液滴定剩余的HCl溶液,此滴定方式属于( ) A.直接滴定B.返滴定C.置换滴定D.简接滴定10.常量分析的试样用量为 ( )A .大于1.0gB .1.0~10gC .大于0.1gD .小于0.1g11.滴定分析中,滴定管的读数误差为±0.01mL ,滴定管的一次滴定需读初、终两次读数,可能引起的最大误差为±0.02mL ,为使滴定的相对误差小于0.1%,终点时消耗的滴定剂的体积至少为 ( )A .10mLB .15mLC .20mLD .无法确定12.用25mL 常量酸碱滴定管进行滴定,结果记录正确的是( )A .18.2B .18.20C .18D .18.00013.已知T HCI/NaON =0.004000 g/ml 、则C HCI 为( )A .0.1000mol/LB .0.004000g/mlC .0.003600g/mlD .0.1097mol/L14.滴定管的读数误差为±0.02ml,若滴定时用去滴定液20.00ml ,则相对误差是( )A .±0.1%B .±0.01%C .±1.0%D .±0.001%15.在标定NaOH 溶液浓度时,某同学的四次测定结果分别为0.1023 mol ·L -1、0.1024 mol ·L -1、0.1022 mol ·L -1、0.1023 mol ·L -1,而实际结果应为0.1088 mol ·L -1,该学生的测定结果 ( )A .准确度较好,但精密度较差B .准确度较差,但精密度较好C .准确度较差,精密度也较差D .系统误差小,偶然误差大16.在定量分析结果的一般表示方法中,通常要求( )A .d R ≤2%B .d R ≤0.02%C .d R ≥0.2% D.d R ≤0.2% 17.T A/B 表示的意义是 ( )A .100ml 标准溶液A 中所含溶质的质量B .1ml 标准溶液A 中所含溶质的质量C .1L 标准溶液A 相当于被测物质B 的质量D .1ml 标准溶液A 相当于被测物质的质量18.T HCl/NaOH =0.003000g/ml ,终点时HCl 消耗40.00 ml ,试样中NaOH 的质量为( )A .0.1200gB .0.01200gC .0.001200gD .0.1200mg。
兰叶青 无机及分析化学课后答案 第七章

第 习题答案7—1解:设BaSO 4在水中的溶解度为S 1(mol ·L -1);在0.10mol•L -1Na 2SO 4溶液中的溶解度为S 2(mol ·L -1).由 )()()(aq S O aq Ba s BaSO 2424-++= 222222sp 441010BaSO Ba SO c S .S K c /c c /c S /c ΘΘΘΘΘ+-⋅+⎡⎤⎡⎤===⎣⎦⎣⎦()()()()()(纯水中) (Na 2SO 4中)已知 10sp 4BaSO 10710K .Θ-=⨯()解得 S 1=1.03×10-5mol•L -1由同离子效应知,S 2<S 1=1.03×10-5mol•L -1 所以 0.10+ S 2≈0.10 解得S 2=1.1×10-9mol•L -1 7—2解:(1)7213sp AgBr 88107710K ..Θ--=⨯=⨯()()(2)5313sp 44Mg NH PO 63102510K ..Θ--=⨯=⨯(())()(3)55213sp 32Pb IO 3110101210K ..Θ---=⨯⨯⨯⨯=⨯(())(2 3.1)7—3 解:两液混合后,13132L m o l 1001L mol 1001001001002Pb ----+⋅⨯=⋅+⨯⨯=.....c)()( 11L mol 0200L mol 1001001000400I ---⋅=⋅+⨯=.....c )()(22PbI s Pb aq 2I aq +-+ƒ()()() 根据溶度积规则,计算离子积Q :22327Q P b I 101000204010c /c c /c ...ΘΘ+---⎡⎤⎡⎤==⨯⨯=⨯⎣⎦⎣⎦()() 查表得 9sp 2PbI 84910K .Θ-=⨯() 即 )(2sp PbI Q ΘK 〉应有PbI 2沉淀产生. 7—4解:查表39sp 3Fe OH 26410K .Θ-=⨯(()) 17sp 2Fe OH 48710K .Θ-=⨯(())Fe (OH )3沉淀完全时, c (Fe 3+)≤1.0×10-5mol·L -1,此时OH c /c Θ-==()解得 c (OH -)=6.4×10-12 mol·L -1pH=14-pOH=2.81,即pH 至少为2.81。
无机及分析化学第七章答案 (2)

第七章 要求作业答案7-1 判断题 解:(1)不正确。
有些化合物不存在外界,如[PtCl 2(NH 3)2]、[CoCl 3(NH 3)3]等。
(2)不正确。
少数高氧化数的非金属元素离子也可作为形成体,如[BF 4]-、[SiF 6]2-中的B 3+、Si 4+等;另外,有些中性原子也可作形成体,如[Ni(CO)4]中的Ni 原子。
(3)不正确。
在多齿配体的螯合物中,配位体数目就不等于配位数,如[Cu(en)2]2+中。
(4)不正确。
配离子电荷应是形成体和配位体电荷的代数和。
如[Fe(CN)6]3-。
(5)正确。
7-2 填空题 解:(1)五氟·一水合铁(Ⅲ)酸铵;Fe 3+; F -,H 2O ; F ,O ; 6; sp 3d 2; 外轨(2)Co 3+;Cl -,NH 3; Cl ,N ; 6;1s 22s 22p 63s 23p 63d 6 or [Ar]3d 6;四;Ⅷ;d ;d 2sp 3;八面体;内轨型;氯化一氯·五氨合钴(III)(3)乙二胺四乙酸;1:1 (4)pH <12.47-3 选择题解 (1)D (2)B (3)A (4)B7-4 计算题1.解:(1)())L (mol 0.041000.1040Ag 1•=×=+c , ()()13L mol 1.21006.020NH -⋅=⨯=c 设平衡时[Ag(NH 3)2]+ 解离产生的Ag +的浓度为x mol·L -1。
Ag + + 2 NH 3 = [Ag(NH 3)2]+c 0/ mol·L -1 0.04 1.2 0c / mol·L -1 x 1.2-2×0.04+2x ≈ 1.12 0.04-x ≈0.04()722323107.10.1/12.1)0.1/(0.1/04.0]/)([/)(/])([⨯=•=•=++x c NH c c Ag c c NH Ag c K f θθθθ解得 c (Ag +) = x = 1.88 ×10-9 (mol·L -1)c (NH 3) ≈ 1.12 (mol·L -1)c [Ag(NH 3)2+] ≈ 0.04 (mol·L -1)(2) 在混合稀释后的溶液中加入0.010mol KCl 固体,即c (Cl -) = 0.01010000.100100⨯= (mol·L -1) ∵Q = c (Ag +)/1.0×c (Cl -)/1.0 = (1.88×10-9/1.0)×(0.10/1.0 )= 1.88×10-10 ∴Q >[]AgCl θsp K = 1.77×10-10,所以能产生AgCl 沉淀。
(完整版)无机及分析化学课后习题第七章答案

一、选择题在给出的4个选项中,请选出1个正确答案。
1. 下列物质中,酸的强度最大的是( D )A. HAc 4.75HAc)p θa=(K B. HCN 219HCN)p θa .(K = C. NH 4+4.75O)H NH p 23θb =⋅(K D. HCOOH 25.10HCOONa)(p θb =K 2. 某混合碱用盐酸滴定至酚酞变色,消耗V 1ml ,继续以甲基橙为指示剂消耗V 2ml ,已知V 1>V 2 ,其组成是( C )A. Na 2CO 3B. Na 2CO 3与NaHCO 3C. NaOH 与Na 2CO 3D. NaOH3. 用Na 2CO 3 为基准物质标定HCl 溶液时,下列情况对HCl 溶液的浓度不产生影响的是( A )A. 用去离子水溶解锥形瓶中的Na 2CO 3时,多加了5.0mL 去离子水B. 烘干Na 2CO 3时,温度控制300℃以上C. 滴定管未用HCl 溶液润洗D. 滴定速度太快,附着在滴定管壁上的HCl 溶液来不及流下来就读取滴定体积4. 蒸馏法测定铵盐中N 含量时,能用作吸收液的是( B )A. 硼砂B. HClC. HAcD. NH 4Cl5. 下列溶液能用HCl 或NaOH 标准溶液直接滴定的是(浓度均为0.1mol·L -1) ( D )A. NaAcB. NH 4ClC. HCND. HCOOH(K θa (HAc) = 1.79×10-5 ;K θb (NH 3) = 1.8×10-5 ;K θa (HCN) = 4.99×10-10 ; K θa (HCOOH) =1.7×10-4)6. 用返滴定法测定氨水含量,应选用的指示剂是( D )A. 酚酞B. 甲基橙C. 钙红D. 甲基红7. 用c (NaOH)=0.1000 mol·L -1的NaOH 溶液滴定相同浓度的弱酸(K a1 =8.6 ×10-2K a2 =6.3×10-7 K a3 =4.0×10-13)( B )A.有两个滴定终点,第一终点用酚酞、第二终点用甲基红指示B.有两个滴定终点,第一终点用甲基红、第二终点用酚酞指示C.只有一个终点,用酚酞指示D.只有一个终点,用甲基红指示8. 酸碱滴定中,选择酸碱指示剂可以不考虑的因素是( C )A. pH 突跃范围B. 指示剂的变色范围C. 指示剂的摩尔质量D. 要求的误差范围9. H3PO4的pKθa1, pKθa2 pKθa3分别为2.12、7.20、12.36,当pH=8.0时,H3PO4溶液体系中浓度最大的组分是( A )A. HPO42-B. H2PO4- C . H3PO4 D. PO43-二、填空题1. 下列离子HCO3―,H2O,S2-,NH4+只能作碱的是S2-,只能作酸的是NH4+,即可作酸又能作碱的是HCO3―,H2O 。
无机及分析化学 第七章氧化还原反应课后习题答案
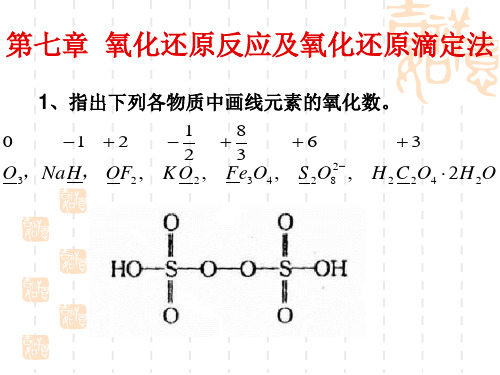
7、求下列情况下在298.15K时有关电对的电极电势。 (忽略加入固体对溶液体积变化)
nCu 2 cNa S O VNa S O 0.1000 25.13 10 3 2.513 10 3 mol
2 7 2 7
1.967 10 4 mol
解:2Cr2 O72 28H 12e 3O2 12 H 12e nO2 nCr O2
2 7
4Cr 3 14 H 2O
6 H 2O nCr O2 1.967 104
2 7
3 2
1
COD(O2, mg L )
2
0.0592 E H / H lg(1.34 103 ) 2 2 2 0.17V
9、计算在H2SO4介质中,H+浓度分别为1mol.L-1和 0.1mol.L-1的溶液中,VO2+/VO2+电对的条件电极电势 (忽略离子强度的影响)。
解:查表得VO2 2 H e VO 2 H 2 O 2 E A (VO2 / VO 2 ) E ( VO / VO ) 0.0592 lg A 2 2 E ( VO / VO ) 1.000V A 2
2
0.0592 36 0.34 lg 6.3 10 2 0.70V
(3)100kPa氢气通入0.10 mol.L-1 HCI溶液中, E H / H2 ?
0.0592 (cH / c ) E H / H2 E H / H lg 2 n (p H2 /p )
无机及分析化学第七章

分子内直接相邻的原子之间强烈的相互作用,称为化学键。化学键一般可分为离子键、共 价键和金属键。
7-1 离子键(ionic bond)
7-1-1 离子键理论的基本要点 1、离子键的形成 (1)活泼金属原子与活泼非金属原子在一定反应条件下互相接近时,都有达到稳定结构的倾向,通
过得失电子形成对应的正、负离子(△χ>2.0) (2)正、负离子相互接近,吸引力和排斥力相平衡时,体系能量最低,形成稳定结合体。
④18+2电子构型:Sn2+,Pb2+等
ns2np6nd10(n+1)s2
⑤9~17电子构型:Fe2+,Mn2+等 ns2np6nd1~9
对于不同的离子化合物,必须同时考虑其中所含离子的以上几个特征,才能对这些离子化合 物的性质及差异作出准确的解释
7-1-3 晶格能(Lattic energy) U
使体系能量降低,成键
(2)自旋相同的两H原子相互靠近时,体系能量随 R的减小而增大,即波函数异号叠加,两核之间 的电子概率密度 ׀Ψ ׀2减小,几乎为0,体系能量 升高,不能成键
2、价键理论(valence bond theory,又称电子配对法或VB法)基本要点 (1)具有自旋相反的单电子的原子相互接近时,单电子可以配对构成共价键 (2)成键的原子轨道重叠越多,形成共价键越稳定—原子轨道最大重叠原理
满足最小排斥 sp 180°, sp2 120°, sp3
109间构型
1、sp杂化 如BeCl2 由1个ns和1个np轨道杂化组合成两个等同的sp杂化轨道,每个轨道各含1/2s和1/2p, 轨道数
目=2, 轨道夹角=180°, 呈直线形
以BeCl2为例: 2p
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章 要求作业答案
7-1 判断题 解:
(1)不正确。
有些化合物不存在外界,如[PtCl 2(NH 3)2]、[CoCl 3(NH 3)3]等。
(2)不正确。
少数高氧化数的非金属元素离子也可作为形成体,如[BF 4]-、[SiF 6]2-中的B 3+、Si 4+等;另外,有些中性原子也可作形成体,如[Ni(CO)4]中的Ni 原子。
(3)不正确。
在多齿配体的螯合物中,配位体数目就不等于配位数,如[Cu(en)2]2+中。
(4)不正确。
配离子电荷应是形成体和配位体电荷的代数和。
如[Fe(CN)6]3-。
(5)正确。
7-2 填空题 解:
(1)五氟·一水合铁(Ⅲ)酸铵;Fe 3+; F -,H 2O ; F ,O ; 6; sp 3d 2; 外轨
(2)Co 3+;Cl -,NH 3; Cl ,N ; 6;1s 22s 22p 63s 23p 63d 6 or [Ar]3d 6;四;Ⅷ;d ;d 2sp 3;八面体;内轨型;氯化一氯·五氨合钴(III)
(3)乙二胺四乙酸;1:1 (4)pH <12.4
7-3 选择题
解 (1)D (2)B (3)A (4)B
7-4 计算题
1.解(1)())L (mol 0.041000.1040Ag 1•=×=+c , ()()13L mol 1.2100
6.020NH -⋅=⨯=c 设平衡时[Ag(NH 3)2]+ 解离产生的Ag +的浓度为x mol·L -1。
Ag + + 2 NH 3 = [Ag(NH 3)2]+
c 0/ mol·L -1 0.04 1.2 0
c / mol·L -1 x 1.2-2×0.04+2x ≈ 1.12 0.04-x ≈0.04
()722323107.10.1/12.1)0.1/(0.1/04.0]/)([/)(/])([×=•=•=++x c NH c c Ag c c NH Ag c K f θθθθ
解得 c (Ag +) = x = 1.88 ×10-9 (mol·L -1)
c (NH 3) ≈ 1.12 (mol·L -1)
c [Ag(NH 3)2+] ≈ 0.04 (mol·L -1)
(2) 在混合稀释后的溶液中加入0.010mol KCl 固体,即c (Cl -) = 0.01010000.100100
⨯= (mol·L -1) ∵Q = c (Ag +)/1.0×c (Cl -)/1.0 = (1.88×10-9/1.0)×(0.10/1.0 )= 1.88×10-10 ∴Q >[]AgCl θsp K = 1.77×10-10,所以能产生AgCl 沉淀。
(3)若不产生AgCl 沉淀,则须Q <[]AgCl θsp K , 即c (Ag +) < 1.77×10-9 (mol·
L -1) 则平衡时c (NH 3)≥15.110
7.11077.10.1/04.0/)(/])([7923=×××=•++θθθf K c Ag c c NH Ag c (mol·L -1) 则需()()13L mol 1.230.0421.15NH =×+=c
设应加入12.0 mol·L -1氨水V mL 则12.0 V =1.23100×即 V = 10.25 (mL)
所以若要阻止AgCl 沉淀生成,则应该取12.0 mol·L -1氨水10.25 mL 。
2、计算pH=5.0时,Mg 2+与 EDTA 形成的配合物的条件稳定常数是多少?此时Mg 2+
能否用EDTA 准确滴定?当pH=10.0时,情况如何?
解:查表得 lgK )(MgY f =8.70, 当pH=5.0时,lg )(H Y α=6.61
lg K )('MgY f =lg K )(MgY f - lg )(H Y α= 8.70-6.61=2.09<8.0,不能用EDTA 准确滴定。
当pH=10.0时,lg )(H Y α=0.50
lg K )('MgY f =lg K )(MgY f - lg )(H Y α=8.70-0.50=8.20>8.0,能用EDTA 准确滴定。
3、称取0.1005g 纯CaCO 3,溶解后,用容量瓶配成100ml 溶液。
吸取25.00ml ,在pH >12时,用钙指示剂指示终点,用EDTA 标准溶液滴定,用去24.90ml ,试计算EDTA 溶液的浓度(mol/L)。
解:Ca + Y = CaY
CaCO 3~Ca ~EDTA Δn(EDTA)=Δn(CaCO 3) c(EDTA )=V
M m /= 31090.244/1.100/1005.0×=0.01008 mol/L 4、求0.02000mol·L -1EDTA 溶液滴定同浓度的Fe 3+的适宜酸度范围。
解:
(1) 最高允许酸度 (最低pH)
lgαY(H) ≤lgK f (FeY) – 8.0=25.1-8.0=17.1 查表得 pH ≥1.4
(2) 最低酸度(pH 高限)
根据溶度积原理,为防止滴定开始时生成Fe (OH)3沉淀,应使溶液的pH 值满足:
即pH ≤1.7
滴定Fe 3+的适宜酸度范围为 pH =1.4~1.7
6、称取葡萄糖酸钙试样0.5500g ,溶解后,在pH=10的氨性缓冲液中用EDTA 滴定(EBT 为指示剂),滴定消耗浓度为0.04985mol/L 的 EDTA 标准溶液24.50ml ,试计算葡萄糖酸钙的含量。
(分子式C 12H 22O 14Ca ·H 2O) (99.57%)
解:Ca + Y = CaY
C 12H 22O 14Ca ·H 2O ~Ca ~EDTA Δn(C 12H 22O 14Ca ·H 2O )=Δn(EDTA)
w ( C 12H 22O 14Ca ·H 2O ) =s
m O H Ca O H C M EDTA V EDTA c )()()(2142212• =5500
.04.44802450.004985.0×× =99.57%
-13
{()/} 5.1910c OH c θ-===⨯。
