基础化学标准答案第
基础化学第四章习题答案

1.能够抵抗少量酸、碱或加水稀释,而本身pH 值基本保持不变的溶液,称为缓冲溶液。
2.缓冲容量是衡量缓冲能力大小的尺度。
通常用使单位体积缓冲溶液的pH 改变1个单位时,所需加入一元强酸或一元强碱的物质的量表示缓冲容量。
影响缓冲容量的主要因素是缓冲系的总浓度和缓冲比;缓冲比一定时,总浓度越大,缓冲容量越大;总浓度一定时,缓冲比越接近于1,缓冲容量越大。
缓冲容量与缓冲系中共轭酸的p K a 无关。
所以总浓度相同的HAc-NaAc 和H 2CO 3-HCO 3-缓冲系的缓冲容量相同。
3.(1)(2)(4)(5).4. 配制pH = 3的缓冲溶液,选HCOOH —HCOO -最合适,因为HCOOH 的pK a = 3.75,与所需的pH 值最接近。
5. 此混合溶液为HCO 3- -CO 32-组成的缓冲溶液。
查表4-1,H 2CO 3的p K a2=10.25。
m o l m o l g g H C O n 119.00.840.10)(13=⋅=--mol094.0molg 106g0.10)CO(123=⋅=--n代入式(4.4)得15.10mol119.0mol 094.0lg2510)HCO)CO lgp pH 323a =+⋅=+=--((n n K6. H 2C 2O 4:pKa 1 = 1.23 pKa 2 = 4.19∴应选择---242242O C O HC 缓冲体系 1]O[C ]O [HC ]O[C ]O [HC lgpKa pH 2424224242=⇒-=----则:3:2V :V NaOH O C H422=7. HAc + NaOH = NaAc + H 2O初(mol ):100×0.10 50×0.10平 (mol): 50×0.10 50×0.10c a =301501005=+(mol·L -1) c b =301501005=+(mol·L -1)pH=pKa-lg754301301754.lg.c c ba =-= 8.设需加入0.10 mol·L -1HCl 溶液x 毫升,NH 3·H 2O + HCl = NH 4Cl + H 2O生成NH 4Cl 的浓度 = 0.10x /(500+x) (mol·L -1) 剩余NH 3·H 2O 的浓度 = (0.10×500 – 0.10x )/ (500+x) (mol·L -1)pOH = 14-10 = 4 x1.0x 1.050lg75.4)x 500/(x 10.0)x 500/()x 500(10.0lg75.44--=++--=625101050.x.x .=- x = 75.5(mL) 设需加入NH 4Cl 的浓度为y mol·L -1,y1.0lg75.44-= 62.5y1.0= y = 0.018(mol/L)需加入固体NH 4Cl = 0.018×0.5×53.5 = 0.48(g)1]O[C ]O [HC ]O[C ]O [HC lgpKa pH 2424224242=⇒-=----则:3:2V :V NaOH O C H422=9.加入的NaOH 为0.20g÷40g·mol -1=0.005mol 、c (OH -)=0.005mol ÷0.100L=0.05mol ·L -1设原溶液中共轭碱 [B -]原=xmol·L -1,则加入NaOH 后,[HB]=0.25mol·L -1-0.05mol·L -1=0.20mol·L -1, [B -]=0.05mol·L -1+xmol·L -1 ,代入式(4.2)]HB []B [lga p pH -+=K11Lmol 20.0L mol )x 05.0(lg30.560.5--⋅⋅++=[B -]原=xmol·L -1=0.35mol·L -1原溶液45.5Lmol 25.0Lmol 35.0lg30.5pH 11=⋅⋅+=--10. 阿司匹林以HAsp 表示,解离后以Asp -表示。
基础化学第三版习题标准答案-章

基础化学第三版习题答案-章————————————————————————————————作者:————————————————————————————————日期:习 题 答 案第一章 绪论1、求0.010kgNaOH 、0.100kg (21Ca 2+)、0.10kg (21Na 2CO 3)的物质的量。
解:(1)m (NaOH) = 0.010kg M (NaOH) = 40g ·mol -1n (NaOH) =4010= 0.25 (mol) (2)m (21Ca 2+) = 0.100kg M (21Ca 2+) = 40g ·mol -1 n (21Ca 2+) =20100= 5.0(mol) (3)m (21Na 2CO 3) = 0.10kg M (21Na 2CO 3) = 53g ·mol -1 n (Na 2CO 3) =53100= 1.89 (mol) 2、下列数值各有几位有效数字?(1)1.026 4位 (2)0.0208 3位 (3)0.003 1位(4)23.40 4位 (5)3000 无数位 (6)1.0×10-3 2位 3、应用有效数字计算规则,计算下列各式:(1)21.10 - 0.263 + 2.3 = 23.1 (2)3.20×23.45×8.912 = 667(3)31026.117.2322.3⨯⨯= 5.93×10-3(4)=⨯⨯⨯-15.2325.21032.44.52 4.6×10-2 4、(1) 以H 2SO 4为基本单元,M(H 2SO 4)=98g/mol ; (2) 以HSO 4-为基本单元,M(HSO 4-)=97g/mol ; (3) 以3H 2SO 4为基本单元,M(3H 2SO 4)=294g/mol 。
5、答:甲的报告更为合理,百分比小数点后保留两位有效数字。
《基础化学》课后习题参考答案(有机部分)
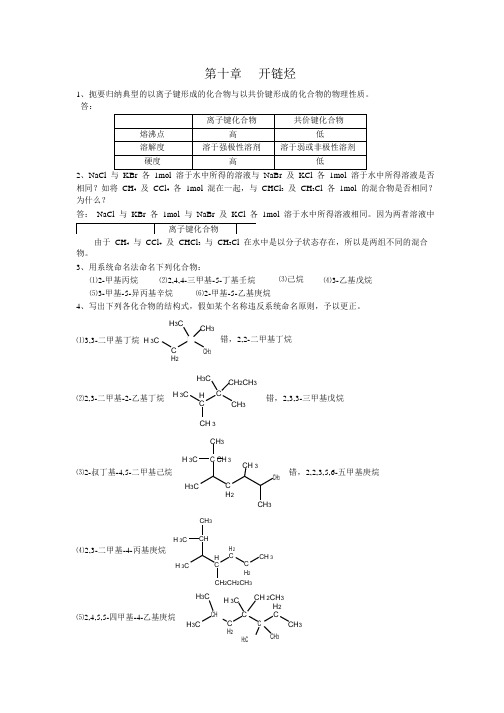
均为 Na + , K + , Br , Cl 离子各 1mol 。
第十章开链烃1、扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答:2、NaCl 相同?如将 CH 4 及 CCl 4 各 1mol 混在一起,与 CHCl 3 及 CH 3Cl 各 1mol 的混合物是否相同? 为什么?答: NaCl 与 KBr 各 1mol 与 NaBr 及 KCl 各 1mol 溶于水中所得溶液相同。
因为两者溶液中 - -由于 CH 4 与 CCl 4 及 CHCl 3 与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合 物。
3、用系统命名法命名下列化合物:⑴2-甲基丙烷⑵2,4,4-三甲基-5-丁基壬烷⑶己烷⑷3-乙基戊烷⑸3-甲基-5-异丙基辛烷⑹2-甲基-5-乙基庚烷4、写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
H 3CCH 3 ⑴3,3-二甲基丁烷 H 3CH 2CH 3H 3C错,2,2-二甲基丁烷CH 2CH 3 ⑵2,3-二甲基-2-乙基丁烷 H 3C HC C3错,2,3,3-三甲基戊烷CH 3CH 3⑶2-叔丁基-4,5-二甲基己烷H 3CC CH 3CH 33错,2,2,3,5,6-五甲基庚烷H 3CC H 2CH 3CH 3H 3CCH⑷2,3-二甲基-4-丙基庚烷H 3H CH 2 CC H 2CH 3CH 2CH 2CH 3H 3CH 3CCH 2CH 3H 2⑸2,4,5,5-四甲基-4-乙基庚烷H 3CHC H 2 CH 3CC C 3 32 CH32CH2 3CH 2 3CH 3 3CH 3 2CH 3⑹2,2,3-三甲基戊烷H3CH3CCCH3CH2CH35、写出分子式为C6H14的烷烃的各种异构体,用系统命名法命名,丙标出伯、仲、叔、季碳原子。
1oCH 32oCH 2 2 o22 oCH2 oCH 21 o己烷1oCH 3oCH 21 o CH32 o CHo1 oCH32-甲基戊烷1 o CH31oCH 32ooCH2 oCH2 1 oCH3 3-甲基戊烷1oCHo3 oCH1 o3 2,3-二甲基丁烷1 o CH31 o1 o CH31oCH2o4 oCCH32,2-二甲基丁烷H3C 1 o 1 o CH36、⑶>⑵>⑸>⑴>⑷7、写出2,2,4-三甲基戊烷进行氯代反应可能得到的一氯代产物的结构式。
基础化学习题解答(第六章)

第六章沉淀溶解平衡与沉淀滴定思考题与习题一、填空题1.同离子效应使难溶电解质的溶解度降低。
2.根据待测组分与其他组分分离方法的不同,称量分析法一般分为沉淀法、气化法和电解法。
3. 称量分析法的主要操作过程包括溶解、沉淀、过滤和洗涤、烘干和灼烧、称量4. 根据滴定方式、滴定条件和选用指示剂的不同,银量法划分为莫尔法、佛尔哈德法、法杨司法。
5.莫尔法是在中性或弱碱性介质中,K2CrO4_作指示剂的一种银量AgNO3作指示剂的一种银量法。
二、选择题1.AgCl和Ag2CrO4的溶度积分别为1.8×10-10和2.0×10-12,则下面叙述中正确的是( C )A. AgCl与Ag2CrO4的溶解度相等;B. AgCl的溶解度大于Ag2CrO4;C.二者类型不同,不能由K大小直接判断溶解度大小;spD.都是难溶盐,溶解度无意义。
2.下面的叙述中,正确的是( B )A.溶度积大的化合物溶解度肯定大;B.向含AgCl固体的溶液中加适量的水使AgCl溶解又达平衡时,AgCl溶度积不变,其溶解度也不变;C.将难溶电解质放入纯水中,溶解达平衡时,电解质离子浓度的乘积就是该物质的溶度积;D. AgCl水溶液的导电性很弱,所以AgCl为弱电解质。
3.CaF2沉淀在pH=3的溶液中的溶解度较pH=5溶液中的溶解度( B )A.小;B.大;C.相等;D.可能大可能小。
4.已知Mg(OH)2的K=1.8×10-11,则Mg(OH)2饱和溶液中的pH是( A )spA. 3.59;B. 10.43;C. 4.5;D. 9.41。
5.指出下列条件适于佛尔哈德法的是( C )A. pH6.5~10;B.以K2CrO4为指示剂;C.滴定酸度为0.1~1mol/L;D.以荧光黄为指示剂。
三、是非题(下列叙述中对的打“√”,错的打“×”)K越小,则其溶解度也越小。
( ×)1. 难溶电解质的溶度积φspK的大小有2. 加入沉淀剂于溶液中,离子的沉淀反应发生的先后顺序不仅与溶度积φsp关,而且也与溶液中离子的起始浓度有关。
基础化学习题及详细答案

基础化学习题及详细答案第三章电解质溶液首页难题解析学生自测题学生自测答案章后习题解答难题解析[TOP]例3-1 (1) NaOH和H3PO4溶液等体积混合,测得溶液pH值为4.66,溶液的渗透浓度为200 mmol·L-1,求混合前NaOH和H3PO4溶液的浓度各为多少?(2)若此NaOH和H3PO4溶液以2:1的体积混合,溶液pH和渗透浓度各为多少?(已知H3PO4:p K a1=2.16;p K a2=7.21;p K a3=12.32) 分析(1) NaOH和H3PO4溶液等体积混合,由pH=4.66知混合后只有NaH2PO4,那么NaOH和H3PO4浓度相等,再由混合溶液渗透浓度求得NaOH和H3PO4溶液的浓度。
(2)NaOH和H3PO4以2:1体积混合,可计算出溶液pH和渗透浓度。
解(1)因NaOH和H3PO4溶液等体积混合后pH=4.66=(p K a1+p K a2)/2,可判断混合溶液只含有NaH2PO4,因此混合前NaOH和H3PO4浓度相等,又混合溶液的渗透浓度为200 mmol·L-1,即2×c(NaH2PO4)= 200 mmol·L-1c(NaH2PO4)= 0.10 mol·L-1根据c(NaH2PO4)推出混合前c(NaOH)= 0.20 mol·L-1,c(H3PO4)= 0.20 mol·L-1(2) NaOH和H3PO4溶液以2:1的体积混合发生的反应为:2NaOH(aq) + H3PO4(aq)Na2HPO4(aq) + 2H2O(aq)由于混合前c(NaOH)= 0.20 mol·L-1,c(H3PO4)=0.20 mol·L-1,混合后溶液只含有Na2HPO4,浓度为c(Na2HPO4)= (2/3)×0.20 mol·L-1因此溶液的渗透浓度为3×(2/3)×0.20×1000 mmol·L-1=400 mmol·L-1由于混合溶液只含有Na2HPO4两性物质,pH=(p K a2 + p K a3)/2=(7.21+12.32)/2=9.76例3-2在0.100 mol·L-1HA溶液的解离度α为1.32%,(1)计算HA的解离常数。
《基础化学》课后习题参考答案(无机部分)
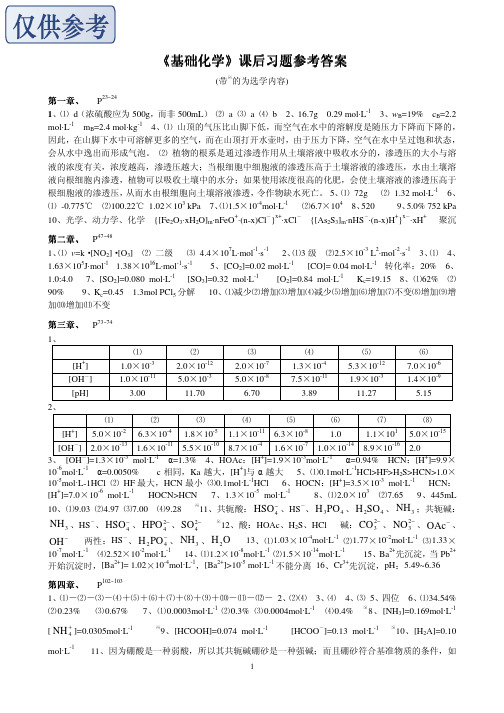
⑵
-2
⑶
-4
⑺ 1.1×10
1
⑻ 5.0×10-15
+
5.0×10
6.3×10
1.8×10
-5
1.1×10
-11
6.3×10
-8
1.0
[OH ] 2.0×10-13 1.6×10-11 5.5×10-10 8.7×10-4 1.6×10-7 1.0×10-14 8.9×10-16 2.0 3、 [OH-]=1.3×10-3 mol·L-1 α=1.3% 4、HOAc:[H+]=1.9×10-3mol·L-1 α=0.94% HCN:[H+]=9.9× -6 -1 + 10 mol·L α=0.0050% c 相同,Ka 越大,[H ]与 α 越大 5、⑴0.1mol·L-1HCl>HF>H2S>HCN>1.0× 10-5mol·L-1HCl ⑵ HF 最大,HCN 最小 ⑶0.1mol·L-1HCl 6、HOCN:[H+]=3.5×10-3 mol·L-1 HCN: + -6 -1 -5 -1 3 [H ]=7.0×10 mol·L HOCN>HCN 7、1.3×10 mol·L 8、⑴2.0×10 ⑵7.65 9、445mL 10、⑴9.03 ⑵4.97 ⑶7.00 ⑷9.28
2
1 ⑷m = 0 2
5、 n ≥ 3 、 l = 0,1 、 l = 0 、 m = 0 、 m s = ±
2
1 2
2s
n 2 2
m 0 0
ms +1/2 -1/2
2p3
※
2 2 2
1 1 1
0 +1 -1
+1/2 +1/2 +1/2
基础化学第二版课后习题答案

基础化学第二版课后习题答案【篇一:基础化学第二版习题答案chap5】1.何谓沉淀溶解平衡?同物质的量的bacl2和h2so4混合溶液中,含有哪些离子?这些离子浓度之间存在着哪些关系?答:难溶电解质溶解和沉淀速度相等,固体的量和溶液中分子或离子的量不再改变的状态,称为沉淀溶解平衡。
ba2+、cl-、so4、h+、oh-2?2.活度积、溶度积、离子积之间有何区别与联系?答:活度积、溶度积指平衡状态下的活度积或浓度积,对给定的难溶电解质其活度积只与温度有关,溶度积不但与温度有关,还和溶液离子强度有关,对于ma型难溶电解质:?ksp(ma)。
离子积指任意状态下的浓度积,其值是任意的。
?(m?)??(a?)3.无副反应时,沉淀的溶度积与溶解度有何关系?溶度积小的物质,它的溶解度是否一定小?举例说明。
答:s?mmnn不同类型难溶电解质的溶解度不能根据溶度积数值大小直接判断。
溶度积小的物质,它的溶解度是不一定小,如ag2cro4与agcl。
4.除了沉淀物质本性以外,影响沉淀溶解度的主要因素有哪些?答:除了沉淀物质本性以外,影响沉淀溶解度的主要因素还有:同离子效应、盐效应、酸碱效应、配位效应等。
5.判断下列操作中可能发生的反应和现象并予以解释。
(1)将少量caco3固体放入稀hcl中。
(2)将少量mg(oh)2放入nh4cl溶液中。
答:(1)caco3固体溶解,有无色无味气体产生。
caco3(s)ca2+ + co32-+2h+h 2co 3→co2 +h 2o(2)mg(oh)2固体溶解,有无色刺激性气体产生。
的氨水,有肉色沉淀生成。
原因是饱和h2s水溶液提供的s2-很少,此时mg(oh)2(s)mg2+ + 2oh-+2nh4+(4)黑色固体变成白色固体。
so42- +h2o(5)白色沉淀变成黄色沉淀。
agcl(白)+ i-(6)浅兰色沉淀消失,生成深兰色溶液。
cu(oh)2 + 4nh3pb2++so42-→pbso4↓(白)agi(黄)+cl-[cu(nh3)4](oh)2答:(1)(2)减小(同离子效应);(3)增大(盐效应);(4)增大(配位效应)。
基础化学题库(题库+标准答案)

第二章稀溶液依数性练习题一、就是非题(共10题)1、溶液得沸点就是指溶液沸腾温度不变时得温度。
( )2、溶液与纯溶剂相比沸点升高、凝固点降低就是由于溶剂摩尔分数减小引起得。
( )3、等物质得量硝酸钾与碳酸钾分别加入等量得水中,该两溶液得蒸气压下降值相等。
( )4、凡就是浓度相等得溶液都就是等渗溶液。
( )5、溶液得蒸气压下降与沸点升高仅适用于难挥发得非电解质溶质,而凝固点降低及渗透压则不受此限制。
( )6、电解质浓溶液也有依数性变化规律,但不符合拉乌尔定律得定量关系。
( )7、一定量得电解质加入纯水中,此溶液得沸点一定高于100℃,但无法定律计算。
( )8、任何两种溶液用半透膜隔开,都有渗透现象发生。
( )9、分散质粒子大小在合适得范围内,高度分散在液体介质中就能形成稳定得溶胶。
( )10、 AlCl3、MgCl2、KCl三种电解质对负溶胶得聚沉值依次减小。
( )二、选择题 ( 共11题 )1、以下论述正确得就是(A)饱与溶液一定就是浓溶液(B)甲醇就是易挥发性液体,溶于水后水溶液凝固点不能降低(C)强电解质溶液得活度系数皆小于1(D)质量摩尔浓度数值不受温度变化2、已知乙醇与苯得密度分别为0、800 g·cm3与0、900 g·cm3,若将86、3cm3乙醇与 901 cm3苯互溶, 则此溶液中乙醇得质量摩尔浓度为( )(A) 1、52 mol·dm3 (B) 1、67 mol·dm3(C) 1、71 mol·kg1 (D) 1、85 mol·kg13、 2、5 g 某聚合物溶于 100 cm3水中, 20℃时得渗透压为 100 Pa, 则该聚合物得相对分子质量就是( )(A) 6、1×102 (B) 4、1×104 (C) 6、1×105 (D) 2、2×1064、 1、0 mol·dm3蔗糖得水溶液、1、0mol·dm3乙醇得水溶液与1、0 mol·dm3乙醇得苯溶液, 这三种溶液具有相同得性质就是 ( )(A) 渗透压 (B) 凝固点(C) 沸点 (D) 以上三种性质都不相同5、 1、17 % 得 NaCl 溶液产生得渗透压接近于( )(相对原子质量: Na 23, Cl 35、5) (A) 1、17 % 葡萄糖溶液 (B) 1、17 % 蔗糖溶液(C) 0、20 mol·dm3葡萄糖溶液 (D) 0、40 mol·dm3蔗糖溶液6、同温同浓度得下列水溶液中, 使溶液沸点升高最多得溶质就是( )(A) CuSO4 (B) K2SO4(C) Al2(SO4)3(D) KAl(SO4)27、要使溶液得凝固点降低 1、00℃ , 必须向 200 g 水中加入 CaCl2得物质得量就是(水得K f=1、86 K·kg·mol1)( )(A) 1、08 mol (B) 0、108 mol (C) 0、0540 mol (D) 0、0358 mol8、某难挥发非电解质稀溶液得沸点为 100、400℃ , 则其凝固点为 ( ) (水得K b= 0、512 K·kg·mol1, K f= 1、86 K·kg·mol1)(A) 0、110℃ (B) 0、400℃ (C) 0、746℃ (D) 1、45℃9、与纯溶剂相比,溶液得蒸气压( )(A) 一定降低(B) 一定升高(C) 不变(D) 需根据实际情况做出判断,若溶质就是挥发性很大得化合物就不一定降低10、 60℃时, 180 g水中溶有 180 g葡萄糖, 已知60℃时水得蒸气压为19、9kPa, C6H12O6得相对分子质量为 180, 则此水溶液得蒸气压应为( )(A) 1、81 kPa (B) 9、95 kPa (C) 15、9 kPa (D) 18、1 kPa11、若氨水得质量摩尔浓度为 mmol·kg1,则其中NH3得摩尔分数为( ) mm(A) ───── (B) ──────────1000/18 [(100017m)/18]+mm(C) ─────── (D) 不确定(1000/18) + m三、填空题 ( 共 8题 )1、 (2 分)体温为 37℃时, 血液得渗透压为 775 kPa, 此时与血液具有相同渗透压得葡萄糖(相对分子质量为 180)静脉注射液得浓度应为 __________________ g·dm3。
基础化学第二章 溶液习题答案

基础化学第二章习题答案1. 将10g NaOH 、CaCl 2、Na 2CO 3分别溶于水中, 然后均配制成500mL 溶液,求溶液的浓度c (NaOH)、c (21CaCl 2)、c (21Na 2CO 3)。
解:NaOH 的摩尔质量M (NaOH)=40.021CaCl 2的摩尔质量M (21CaCl 2)=55.45 21Na 2CO 3的摩尔质量M (21Na 2CO 3)=53.0 则:c (NaOH)=5.010005004010=mol •L -1 c (21CaCl 2)=36.0100050055.4510=mol •L -1 c (21Na 2CO 3)=38.010*********=mol •L -12.正常人血浆中,每100mL 含164.7mg HCO 3-,计算正常人血浆中HCO 3-的浓度。
解:HCO 3-的摩尔质量是61.0g·mol -1,则:L mol 0.0270100164.7/61.0)HCO ()HCO (133---⋅===V n c3.某患者需补0.05mol Na +,求所需NaCl 的质量。
若用质量浓度为9.0g·L -1的生理盐水补Na +,求所需生理盐水的体积。
解:所需NaCl 的质量为0.05×58.5=2.925 g所需生理盐水的体积为2.925/9.0=0.325 L=325 mL4.20℃时,将350 g ZnCl 2溶于650 g 水中,溶液的体积为739.5 mL ,求溶液的浓度、质量浓度和质量分数。
解:c (ZnCl 2)= 47.310005.7393.136350= mol •L -1ρ(ZnCl 2)=47.05.739350= g•mL -1 ω(ZnCl 2)=35.0650350350=+ 5. 现有四种处于相同温度和压力下的理想稀溶液。
(1) 0.1 mol 蔗糖溶于80 mol 水中,水蒸气压为p 1(2) 0.1 mol 萘溶于80 mol 苯中,苯蒸气压为p 2(3) 0.1 mol 葡萄糖溶于40 mol 水中,水蒸气压为p 3(4) 0.1 mol 尿素溶于80 mol 水中,水蒸气压为p 4这四个蒸气压之间的关系为: ( )(A) p 1≠p 2≠p 3≠p 4 (B) p 2≠p 1=p 4>p 3(C) p 1=p 2=p 4=(1/2)p 3 (D) p 1=p 4<2p 3≠p 2答案:B6. 从植物中分离出一种未知结构的有抗白细胞增多症的生物碱,为了测定其相对分子质量,将19.0g 该物质溶入100g 水中,测得溶液沸点升高为0.060K 、凝固点下降为0.220K 。
《基础化学》教材习题答案(第3版)

第一章 习题答案1.答:能量单位J 、质量单位μg 、长度单位nm 、温度单位℃、属于SI 单位;其他不是。
2.答:SI 基本单位:m 、kg 、s 、A 、K 、mol 、cd 。
3.答:一切属于国际单位制的单位都是我国的法定计量单位。
根据我国的实际情况,在法定计量单位中还明确规定采用了若干可与国际单位制并用的非国际单位制单位。
第二章习题答案1. 解: 根据)()O H ()O H ()O H (222蔗糖n n n x +=0292m o l .0m o l 342g g0.10)( mol 56.5mol 18.0g g 100)O H (1-1-2=⋅==⋅=蔗糖n n 995.00.0292m o lm o l 56.5mol56.5)O H (2=+=xkPa 33.20.995kPa 34.2)O H ()O H (2*2=⨯==x p p2.解:)B ()O H ()()O H (999.00.1molmol 08mol08)O H ()O H ()O H ()O H (899.00.1molmol 04mol 04)O H ()O H ()O H ()(999.00.1molmol 80mol80)()()()O H (999.00.1mol mol 80mol80)O H ()O H ()O H (*2**2*22*22*2*22*23***2*2*22*21答案为苯苯苯苯苯∴>=+⋅===+⋅===+⋅===+⋅==p p p p x p p p p x p p p p x p p p p x p p 3.解:与人体血浆等渗。
11os f 11os f B f B f f 11-1-1-os L mmol 310L mol 31.0C58.0K58.0L mol 31.0mol kg K 86.1L mol 31.0L00.1mol 147g g33.03mol 74.6g g 30.02mol 58.5g g 50.82-----⋅=⋅=︒-==⋅⨯⋅⋅=≈≈=∆⋅=⋅⨯+⋅⨯+⋅⨯=c T c K c iK b iK T c4.解:K 85.1mol kg K 512.00.510Kmol kg K 86.1mol g 1.28mol kg 0281.00.510K 250g g 00.7mol kg K 512.011b b f B f f 111b A B b B =⋅⋅⋅⋅⋅=∆⋅=⋅=∆⋅=⋅=⨯⨯⋅⋅=∆⋅⋅=-----K T K b K T T m m K MT f = -1.85℃ 5. 解:压略高于人体眼液的渗透kPa 869K 310K mol L kPa 314.8L mol 337.0L mmol 337L mol 337.0mL10001.000LmL 1000mol 61.8g g 00.17mol 161.5g g 00.52111-os 1-1-1-1-os =⨯⋅⋅⋅⨯⋅==⋅=⋅=⨯⋅+⋅⨯=--RT c Πc6. 解:11A fB f B 11A b B b B mol kg 61.1100g0.220K g0.19mol kg K 86.1mol kg 62.1100g 0.0600K g 0.19mol kg .512K 0----⋅=⨯⨯⋅⋅=∆=⋅=⨯⨯⋅⋅=∆=m T m K M m T m K M用两种方法计算该物质的相对分子质量基本相同。
基础化学第二版课后习题答案

基础化学第二版课后习题答案【篇一:基础化学第二版习题答案chap5】1.何谓沉淀溶解平衡?同物质的量的bacl2和h2so4混合溶液中,含有哪些离子?这些离子浓度之间存在着哪些关系?答:难溶电解质溶解和沉淀速度相等,固体的量和溶液中分子或离子的量不再改变的状态,称为沉淀溶解平衡。
ba2+、cl-、so4、h+、oh-2?2.活度积、溶度积、离子积之间有何区别与联系?答:活度积、溶度积指平衡状态下的活度积或浓度积,对给定的难溶电解质其活度积只与温度有关,溶度积不但与温度有关,还和溶液离子强度有关,对于ma型难溶电解质:?ksp(ma)。
离子积指任意状态下的浓度积,其值是任意的。
?(m?)??(a?)3.无副反应时,沉淀的溶度积与溶解度有何关系?溶度积小的物质,它的溶解度是否一定小?举例说明。
答:s?mmnn不同类型难溶电解质的溶解度不能根据溶度积数值大小直接判断。
溶度积小的物质,它的溶解度是不一定小,如ag2cro4与agcl。
4.除了沉淀物质本性以外,影响沉淀溶解度的主要因素有哪些?答:除了沉淀物质本性以外,影响沉淀溶解度的主要因素还有:同离子效应、盐效应、酸碱效应、配位效应等。
5.判断下列操作中可能发生的反应和现象并予以解释。
(1)将少量caco3固体放入稀hcl中。
(2)将少量mg(oh)2放入nh4cl溶液中。
答:(1)caco3固体溶解,有无色无味气体产生。
caco3(s)ca2+ + co32-+2h+h 2co 3→co2 +h 2o(2)mg(oh)2固体溶解,有无色刺激性气体产生。
的氨水,有肉色沉淀生成。
原因是饱和h2s水溶液提供的s2-很少,此时mg(oh)2(s)mg2+ + 2oh-+2nh4+(4)黑色固体变成白色固体。
so42- +h2o(5)白色沉淀变成黄色沉淀。
agcl(白)+ i-(6)浅兰色沉淀消失,生成深兰色溶液。
cu(oh)2 + 4nh3pb2++so42-→pbso4↓(白)agi(黄)+cl-[cu(nh3)4](oh)2答:(1)(2)减小(同离子效应);(3)增大(盐效应);(4)增大(配位效应)。
基础化学第二版习题答案

基础化学第二版习题答案第一章:原子结构与元素周期表1. 根据质子数确定元素:- 质子数为1的元素是氢(H)。
- 质子数为6的元素是碳(C)。
2. 元素周期表中元素的排列规律:- 元素按照原子序数递增排列。
- 元素周期表分为s区、p区、d区和f区。
3. 元素周期表中的族和周期:- 每个周期代表一个电子壳层。
- 每个族代表一个价电子层。
第二章:化学键与分子结构1. 离子键与共价键的区别:- 离子键是由正负离子之间的静电吸引力形成的。
- 共价键是由两个原子共享电子对形成的。
2. 极性分子与非极性分子:- 极性分子具有不对称的电荷分布。
- 非极性分子的电荷分布是对称的。
3. 分子间作用力:- 包括氢键、范德华力等。
第三章:化学计量学1. 摩尔的概念:- 摩尔是化学中用于表示物质量的单位。
2. 摩尔质量的计算:- 摩尔质量是元素的相对原子质量,以克/摩尔为单位。
3. 化学方程式的平衡:- 确保方程式两边的原子数相等。
第四章:溶液与溶解度1. 溶液的类型:- 包括水溶液、有机溶液等。
2. 溶解度的定义:- 溶解度是在特定条件下,物质在溶剂中的最大溶解量。
3. 溶液的浓度表示方法:- 包括摩尔浓度、质量浓度等。
第五章:化学反应速率与化学平衡1. 反应速率的影响因素:- 包括温度、浓度、催化剂等。
2. 化学平衡的定义:- 反应物和生成物的浓度不再随时间变化的状态。
3. 勒夏特列原理:- 描述了化学平衡对系统条件变化的响应。
第六章:氧化还原反应1. 氧化与还原的定义:- 氧化是电子的损失,还原是电子的获得。
2. 氧化还原反应的平衡:- 涉及电子的转移,需要考虑电子的平衡。
3. 氧化还原电位:- 描述了氧化还原反应的倾向性。
第七章:酸碱平衡1. 酸与碱的定义:- 酸是能够释放氢离子的物质,碱是能够释放氢氧根离子的物质。
2. pH的定义:- pH是溶液酸度的度量,表示为氢离子浓度的负对数。
3. 缓冲溶液:- 能够抵抗小量酸或碱添加引起的pH变化。
现代基础化学第三版答案

现代基础化学第三版答案【篇一:基础化学答案第13】t>习题1. 与化学分析法相比,分光光度法的主要特点是什么?答与化学分析法相比,分光光度法的主要特点有灵敏度高,被测物质的最低可测浓度可达10-5mol?l-1~10-6 mol?l-1,准确度较好,测量的相对误差一般为2%-5%,仪器设备要求简单,操作简便,测定速度快等特点,特别适用于微量及痕量组分的测定。
2. 什么是质量吸光系数?什么是摩尔吸光系数?两者关系如何?为什么要选用波长为?max的单色光进行分光光度法测定?3. 什么是吸收光谱?什么是标准曲线?各有什么实际应用?在一定条件和浓度范围内,测定不同浓度的吸光度a,以溶液的浓度c为横坐标,吸光度a为纵坐标作图,可得到一条通过坐标原点的直线,此直线称为标准曲线。
标准曲线的实际应用,是在相同条件下测定被测溶液的吸光度a,根据吸光度数值,从标准曲线上查到吸光物质的对应的浓度。
4. 分光光度计主要由哪些部件组成?各部件的功能如何?答分光光度计主要由光源、单色器、吸收池、检测器、指示器等部分组成。
光源的功能是发出一定波长范围的连续光谱;单色器可从连续波长的光谱中分离出所需波长的单色光;吸收池用来盛装参比溶液和被测溶液;检测器是将光信号转变为电信号;指示器是将信号放大处理后,通过显示器获得测定的吸光度。
5. 某遵守lambert—beer定律的溶液,当浓度为c1时,透光率为t1,当浓度为0.5c1、2c1时,在液层不变的情况下,相应的透光率分别为多少?何者最大?解根据beer定律a=-lgt=kc当浓度为c1时-lgt1=kc1t2=t11/2t3=t12∵ 0t1∴ t2为最大6. 用邻二氮菲测定铁时,已知每毫升试液中含fe2+0.500 ?g,用2.00 cm吸收池于508 nm波长处测得吸光度为0.198,计算三(邻二氮菲)合铁(ii)配合物的? (508 nm)。
解三(邻二氮菲)合铁(ii)配离子的浓度为:0.500?10?6g/55.8g?mol?1c??8.96?10?6mol?l?1 ?31.00?10l三(邻二氮菲)合铁(ii)配离子的摩尔吸光系数为:??a0.198??1.10?104l?mol?1?cm?1 ?6?1b?c2.00cm?8.96?10m ol?lc2c12.0?10?4mol?l?1???1.0?10?4mol?l?122a20.200?1?1 ??400l?mol?cmb2?c25cm?1.0?10?4mol?l?1假设条件不成立,即此时不符合lambert—beer定律8. 强心药托巴丁胺(m =270)在260 nm波长处有最大吸收,摩尔吸光系数? (260nm) ═703 l?mol-1?cm-1,取该片剂1片,溶于水稀释成2.00l,静置后取上清液用1.00 cm吸收池于260 nm波长处测得吸光度为0.687,计算这药片中含托巴丁胺多少克?解溶液的浓度为:c?a0.687?4?1??9.77?10mol?l ?1?b703l?mol?1.00cm该药片中所含托巴丁胺的质量为:m?cvm?9.77?10?4mol?l?1?2.00l?270g?mol?1?0.528g化合物溶液1l,使其在稀释200倍后,于1.00 cm吸收池中测得的吸光度a=0.600,问应称取该化合物多少克?x/125g?mol?1?1.00cm ∴0.600?2.50?10l?mol?cm?1l?2005?1?1x?0.0600g10. 若将某波长的单色光通过液层厚度为1.0 cm的某溶液,则透射光的强度仅为入射光强度的1/2。
基础化学第二版习题答案

基础化学第二版习题答案基础化学是一门让人们对物质世界有更深入了解的学科。
无论是学生还是教师,习题是学习和教授化学知识的重要工具。
本文将回答《基础化学第二版》中的一些习题,帮助读者更好地理解化学知识。
1. 习题一:如何计算化学反应的摩尔比例?在化学反应中,摩尔比例是指反应物之间的化学计量比。
计算摩尔比例的方法是通过化学方程式中的系数来确定。
例如,对于反应式2H2 + O2 → 2H2O,我们可以看到氢气和氧气的系数分别为2和1,因此它们的摩尔比例为2:1。
2. 习题二:如何计算化学反应的理论产量?理论产量是指在理想条件下,根据化学计量关系计算出的产物的最大可能量。
计算理论产量的方法是根据化学方程式中的系数以及反应物的摩尔量来确定。
例如,对于反应式2H2 + O2 → 2H2O,如果我们有4摩尔的氢气和2摩尔的氧气,根据摩尔比例,氢气的限制摩尔量为2摩尔,因此理论产量为2摩尔的水。
3. 习题三:如何计算化学反应的实际产量?实际产量是指在实验条件下,通过实验测量得到的产物的量。
计算实际产量的方法是根据实验数据计算出来。
例如,如果在上述反应中,实验中得到了1.8摩尔的水,则实际产量为1.8摩尔。
4. 习题四:如何计算化学反应的反应过程中的物质的摩尔量?在化学反应中,可以通过摩尔比例和已知物质的摩尔量来计算其他物质的摩尔量。
例如,对于反应式2H2 + O2 → 2H2O,如果已知氢气的摩尔量为4摩尔,根据摩尔比例可以计算出氧气的摩尔量为2摩尔。
5. 习题五:如何计算化学反应的能量变化?化学反应的能量变化可以通过反应热进行计算。
反应热是指在化学反应中释放或吸收的能量。
计算能量变化的方法是根据反应热的数值以及反应物和产物的摩尔量来计算。
例如,如果反应热为-200 kJ/mol,反应物的摩尔量为2摩尔,产物的摩尔量为2摩尔,则能量变化为-400 kJ。
通过回答以上习题,我们可以更好地理解基础化学中的一些重要概念和计算方法。
基础化学习题解答(第四章)

思考与习题一、填空题:1.可逆反应 2A(g) + B(g)2C(g) ;Δr H m θ< 0 。
反应达到平衡时,容器体积不变,增加B 的分压,则C 的分压 ___增大_______,A 的分压 ___减小________ ;减小容器的体积,B 的分压 _____减小______, K θ___不变________。
2.由N 2和H 2合成NH 3的反应中,Δr H m θ < 0,当达到平衡后,再适当降低温度则正反应速率将________减小 _____,逆反应速率将___减小__________,平衡将向___右 _____方向移动。
3.一定温度下,反应 PCl 5(g)PCl 3(g) + Cl 2 (g) 达到平衡后,维持温度和体积不变,向容器中加入一定量的惰性气体,反应将____不 _______ 移动。
4. 基元反应 2NO + Cl 2 → 2NOCl 是_3 _分子反应,是 3_级反应,其速率方程为__)Cl (·)NO ( 2c c k ⋅=υ____。
5.在密闭容器中进行N 2(g)+3H 2(g)→2NH 3(g)的反应,若压力增大到原来的2倍,反应速率增大 __16___ 倍。
6.可逆反应: I 2+H 22HI 在713K 时K θ=51,若将上式改写为 :21I 2 +21H 2HI 则其K θ为 __51 ____ 。
7.已知下列反应的平衡常数: H 2(g) + S(s) H 2S(g) K θ1S(s) + O 2(g)SO 2(g) K θ2则反应 H 2(g) + SO 2(g)O 2(g) + H 2S(g)的K θ为( θ1K /θ2K )。
8.反应:2Cl 2 (g) + 2H 2O (g) 4HCl (g) + O 2 (g) Δr H m θ>0 ,达到平衡后进行下述变化,对指明的项目有何影响?① 加入一定量的O 2,会使n (H 2O ,g) 增大 ,n (HCl) 减小 ; ② 增大反应器体积,n (H 2O ,g) 减小 ; ③ 减小反应器体积,n (Cl 2) 增大 ;④ 升高温度,K θ 增大 ,n (HCl) 增大 ;⑤ 加入催化剂,n (HCl) 减小 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
基础化学答案第————————————————————————————————作者:————————————————————————————————日期:学生自测答案 [TOP]一、判断题1.√2.√3.×4.×5.√ 二、选择题1.B2.B3.D4.A5.C 三、填空题1. (1) 难挥发性 (2)非电解质 (3) 稀溶液2.(4)溶液的蒸气压下降 (5)沸点升高 (6)凝固点降低 (7)溶液的渗透压力。
3.(8)存在半透膜 (9)膜两侧单位体积中溶剂分子数不等 (10)从纯溶剂向溶液 (11)从稀溶液向浓溶液四、问答题1.Raoult F M 探索溶液蒸气压下降的规律。
对于难挥发性的非电解质稀溶液,他得出了如下经验公式:p = p o x A 又可表示为Δp = p o - p = K b BΔp 是溶液蒸气压的下降,比例常数K 取决于p o 和溶剂的摩尔质量M A 。
这就是Raoult 定律。
温度一定时,难挥发性非电解质稀溶液的蒸气压下降与溶质的质量摩尔浓度b B 成正比,而与溶质的本性无关。
在水中加入葡萄糖后,凝固点将比纯水低。
因为葡萄糖溶液的蒸气压比水的蒸气压低,在水的凝固点时葡萄糖溶液的蒸气压小于冰的蒸气压,两者不平衡,只有降低温度,才能使溶液和冰平衡共存。
2. 这里一个重要问题就是使补液与病人血浆渗透压力相等,才能使体内水分调节正常并维持细胞的正常形态和功能。
否则会造成严重后果。
五、计算题 1.11-4L mol 6149.0mol g 48.53L 0020.0g160.0Cl)(NH -⋅=⋅⨯=c-1-1-14os L mmol 2.299mol mmol 00012L mol 6149.0Cl)(NH ⋅=⋅⨯⨯⋅=c红细胞行为正常。
2. AB B f B f f 1000m M m K b K T ⋅⋅⋅==∆1-1-1f A B f B mol g 5.123g04.19K 245.0kg g 0001g 0113.0mol kg K 10.5Δ0001-⋅=⨯⋅⨯⨯⋅⋅=⋅⋅⋅=T m m K M磷分子的相对分子质量为123.5所以,磷分子中含磷原子数为:499.397.305.123≈= 章后习题答案 [TOP]习题1.水在20℃时的饱和蒸气压为2.34 kPa 。
若于100g 水中溶有10.0 g 蔗糖(M r = 342),求此溶液的蒸气压。
解 根据 BA AA n n n x +=,mol 56.5mol 18.0g 100g O)(H 1-2=⋅=n mol 0292.0molg 342g0.10)(1=⋅=-蔗糖n 995.0mol0292.0mol 56.5mol56.5)(O)(H O)(H O)(H 222=+=+=蔗糖n n n xkPa 33.2995.0kPa 34.2O)(H 20=⨯==x p p2. 甲溶液由1.68 g 蔗糖(M r =342)和20.00 g 水组成,乙溶液由2.45 g (M r = 690)的某非电解质和20.00 g 水组成。
⑴ 在相同温度下,哪份溶液的蒸气压高?⑵ 将两份溶液放入同一个恒温密闭的钟罩里,时间足够长,两份溶液浓度会不会发生变化,为什么?⑶ 当达到系统蒸气压平衡时,转移的水的质量是多少?解 (1) mol 004912.0molg 342g68.1)(1=⋅=-甲n mol 003551.0mol g 690g45.2)(1=⋅=-乙n1kg mol 2456.0kg0200.0mol004912.0-⋅==(甲)b1kg mol 1775.0kg0200.0mol003551.0-⋅==(乙)b溶液乙的蒸气压下降小,故蒸气压高。
(2)乙溶液浓度变浓, 甲溶液浓度变稀。
因为浓度不同的溶液置于同一密闭容器中,由于B b 不同,P 不同, 蒸发与凝聚速度不同。
乙溶液蒸气压高,溶剂蒸发速度大于甲溶液蒸发速度,所以溶液乙中溶剂可以转移到甲溶液。
(3)设由乙溶液转移到甲溶液的水为x(g ), 当两者蒸气压相等时,则(乙)甲b b =)( g)00.20(mol003551.0g )00.20(mol 004912.0x x -=+x = 3.22g3. 将2.80 g 难挥发性物质溶于100 g 水中,该溶液在101.3 kPa 下,沸点为100.51℃ 。
求该溶质的相对分子质量及此溶液的凝固点。
(K b = 0.512 K ·kg ·mol -1,K f = 1.86K ·kg ·mol -1)解 K 51.0K )15.27300.100(K )15.27351.100(0b b b =+-+=-=∆T T T11b b B kg mol 996.0molkg K 512.0K 51.0Δ--⋅=⋅⋅==K T b 11B r mol g 1.28kg100.0kg mol 996.0g80.2--⋅=⨯⋅==V b m M K 85.1kg m ol 996.0m ol kg K 86.111B f f =⋅⨯⋅⋅==∆--b K T该溶液的凝固点f T 为-1.85℃4. 烟草有害成分尼古丁的实验式是C 5H 7N ,今将538 mg 尼古丁溶于10.0 g 水,所得溶液在101.3 kPa 下的沸点是100.17 ℃。
求尼古丁的分子式。
解 K 17.00b b b =-=∆T T T11b b B kg mol 332.0molkg K 512.0K 17.0Δ--⋅=⋅⋅==K T b 11B r m ol g 162kgm ol 332.0kg 0100.0g538.0--⋅=⋅⨯==b m M 尼古丁的分子式为: 21410N H C5. 溶解3.24 g 硫于40.0 g 苯中,苯的凝固点降低1.62℃。
求此溶液中硫分子是由几个硫原子组成的?(K f = 5.10 K ·kg ·mol -1 )解 11f f B kg0.318mol mol kg 5.10K 1.62K Δ--⋅=⋅⋅==K T b 11B r mol 255g kg0.318mol 0.0400kg 3.24g --⋅=⋅⨯==b m M 此溶液中硫原子是由8个硫原子组成。
6. 试比较下列溶液的凝固点的高低:(苯的凝固点为5.5 ℃,K f = 5.12 K ·kg ·mol -1,水的K f = 1.86 K ·kg ·mol -1)⑴ 0.1 mol ·L -1蔗糖的水溶液; ⑵ 0.1 mol ·L -1乙二醇的水溶液; ⑶ 0.1 mol ·L -1乙二醇的苯溶液; ⑷ 0.1 mol ·L -1氯化钠水溶液。
解 对于非电解质溶液B f f b K T =∆,电解质溶液B f f Δb iK T =,故相同浓度溶液的凝固点的大小顺序是: ⑶>⑴=⑵>⑷7. 试排出在相同温度下,下列溶液渗透压由大到小的顺序: ⑴ c (C 6H 12O 6)= 0.2 mol ·L -1; ⑵ 132L mol 2.0)CO Na 21(-⋅=c ;⑶ 143L mol 2.0)PO Na 31(-⋅=c ; ⑷ c (NaCl)= 0.2 mol ·L -1。
解 根据非电解质溶液cRT =∏, 电解质溶液icRT =∏,渗透压大小顺序是:⑷ > ⑵ > ⑶ > ⑴8. 今有一氯化钠溶液,测得凝固点为 -0.26 ℃,下列说法哪个正确,为什么? ⑴ 此溶液的渗透浓度为140 mmol ·L -1; ⑵ 此溶液的渗透浓度为280 mmol ·L -1; ⑶ 此溶液的渗透浓度为70 mmol ·L -1; ⑷ 此溶液的渗透浓度为7 153 mmol ·L -1 。
解 由于 NaCl 在水溶液中可以电离出2倍质点数目,该溶液的渗透浓度可认为11-k g mol B L mol 0s }2{}{-⋅⋅≈b c :kg mol 140.0molkg 86.126.0211--⋅=⋅⋅=K K b B 所以(1)正确,氯化钠溶液的渗透浓度应为140 mmol ·L -19. 100 mL 水溶液中含有2.00 g 白蛋白,25 ℃ 时此溶液的渗透压力为0.717 kPa 求白蛋白的相对分子质量。
解 141-1L mol 1089.2K)25273(K mol L kPa 314.80.717kPa )(---⋅⨯=+⨯⋅⋅⋅==RT Πc 白蛋白141-4mol g 1092.6L100.0L mol 1089.2g00.2--⋅⨯=⨯⋅⨯=(白蛋白)M 10. 测得泪水的凝固点为 -0.52 ℃,求泪水的渗透浓度及 37 ℃时的渗透压力。
解 11B kg mol 280.0molkg K 86.1K52.0--⋅=⋅⋅=b 泪水的渗透浓度为1L mmol 280-⋅。
722kPa37)K (273K m ol L 8.314kPa L m ol 28.0-111=+⨯⋅⋅⋅⨯⋅=--Π 11.今有两种溶液,一为1.50 g 尿素(M r = 60.05)溶于200 g 水中,另一为42.8 g 某非电解质溶于1000 g 水中,这两种溶液在同一温度下结冰,试求该非电解质的相对分子质量。
解 若两溶液在同一温度下结冰,则 (某非电解质)尿素b b =)(,VM m K b K T B rff f /==∆ 有 g1000/8.42g 200mol g 05.60/g 50.1r 1M g =⋅-1r m ol g 343-⋅=M12. 在0.100kg 的水中溶有0.020 mol NaCl, 0.010 mol Na 2SO 4和0.040 mol MgCl 2。
假如它们在溶液中完全电离,计算该溶液的沸点升高值。
解 1kg m ol 20.0kg100.0m ol020.0(NaCl)-⋅==b142kg mol 10.0kg 100.0mol010.0)SO (Na -⋅==b12kg mol 40.0kg100.0mol040.0)(MgCl -⋅==b他们在溶液中完全电离,溶液中总质点数目为:1111242kg mol 9.1 kg mol 40.03kg mol 10.03kg mol 20.02 )MgCl (3)SO Na (3)NaCl (2)(----⋅=⋅⨯+⋅⨯+⋅⨯=⨯+⨯+⨯=b b b b 总 K 97.0kg mol 9.1mol kg K 512.011b =⋅⨯⋅⋅=∆--TExercises1. What are the normal freezing points and boiling points of the following solution?(a)21.0g NaCl in 135mLof water.(b) 15.4g of urea in 66.7 mL of water.Solution: (a )11L m ol 659.20.135Lm ol g 21.0g/58.5NaCl)(--⋅=⋅=cK 89.9L m ol 659.2m ol kg K 86.1211f =⋅⨯⋅⋅⨯=∆--TC 89.9o f -=TK 72.2L mol 659.2mol kg K 512.0211b =⋅⨯⋅⋅⨯=∆--TC 72.102ob =T(b) 1142L m ol 848.30.0667Lm ol g 15.4g/60.0)H CON (--⋅=⋅=cK 16.7L m ol 848.3m ol kg K 86.111f =⋅⨯⋅⋅=∆--TC 16.7o f -=TK 97.1L mol 848.3mol kg K 512.011b =⋅⨯⋅⋅=∆--T C 97.101o b =T2. If 4.00g of a certain nonelectrolyte is dissolved in 55.0g of benzene, the resulting solution freezes at 2.36℃. Calculate the molecular weight of the nonelectrolyte.Solution: C 14.3C 36.2C 5.5o o o f o f f =-=-=∆T T T11B kgmol 616.0mol kg K 10.5K 14.3--⋅=⋅⋅=b 11-mol g 118kg.616mol 0g/0.0550kg00.4-⋅=⋅=r M 3. The average osmotic pressure of seawater is about 30.0 atm at 25℃. Calculate the concentration (molarity) of an aqueous solution of urea (NH 2CONH 2)that is isotonic with seawater.Solution: kPa 3039atm1kPa3.101atm 0.30=⨯11122L mol 23.1 K 298mol K L kPa 314.8kPa 3039)NCONH H (---⋅=⨯⋅⋅=∏=RT c4. A quantity of 7.85g of a compound having the empirical formula C 5H 4 is dissolved 301g of benzene. The freezing point of the solution is 1.05℃ below that of pure benzene. What are the molar mass and molecular formula of this compound?Solution: 11B kg mol 206.0molkg K 10.5K05.1--⋅=⋅⋅=b 11-mol g 127kg.206mol 0301.0.85g7-⋅=⋅⨯=kg M r Since the formula mass of 45H C is 1mol g 64-⋅and the molar mass is found to be 1molg 127-⋅ ,the molecular formula of the compound is 810H C .5. Ethylene glycol (EG) CH 2(OH)CH 2(OH), is a common automobile antifreeze. it is cheap, water-soluble, and fairly nonvolatile (b.p.197℃).Calculate the freezing point of a solution containing 651g of thissubstance in 2505g of water. Would you keep this substance in your car radiator during the summer? The molar mass of ethylene glycol is 62.01g.Solution:M (EG)=62.01g·mol -11-1kg mol 19.4kg505.2mol g 651g/62.01)(-⋅=⋅=EG bK 79.7kg m ol 19.4m ol kg K 86.111f =⋅⨯⋅⋅=∆--T C 79.7o f -=TK 15.2kg mol 19.4mol kg K 512.011b =⋅⨯⋅⋅=∆--T C 15.102o b =TBecause the solution will boil at 102.15℃,it would be preferable to leave the antifreeze in your car radiator in summer to prevent the solution from boiling.6. A solution is prepared by dissolving 35.0g of hemoglobin (Hb) in enough water to make up one liter in volume.If the osmotic pressure of the solution is found to be 10.0mmHg at 25℃,calculate the molar mass of hemoglobin.Solution: the concentration of the solution:141-1L mol 1038.5K)25273(K mol L kPa 314.8760mmHg101.3kPa10.mmHg Π)Hb (---⋅⨯=+⨯⋅⋅⋅⨯==RT c141-4-mol g 1051.6L1L mol 10.385 5.0g3)Hb (-⋅⨯=⨯⋅⨯=M 7. A 0.86 percent by mass solution of NaCl is called “physiological saline” because its osmotic pressure is equal to that of the solution in blood cell. Calculate the osmotic pressure of this solution at normal body temperature (37℃). Note that the density of the saline solution is 1.005g /mL.Solution: 111L mol 148.01L 1000mL mol58.5g mL 1.005g 100g 0.86g)NaCl (---⋅=⨯⋅⋅⨯=c 763kPa37)K (273K mol L 8.314kPa L mol 148.02 1-11=+⨯⋅⋅⋅⨯⋅⨯==--RTic ΠB。
