第四章二烯烃和炔烃(6学时)
二烃和炔烃(6学时)

C120°C0.148nm223 22 43C第四章二烯烃和炔烃〔6 学时〕§4.1二烯烃的分类和命名分子中含有两个或两个以上碳碳双键的不饱和烃称为多烯烃。
二烯烃的通式为C n H 一、二烯烃的分类和命名依据二烯烃中两个双键的相对位置的不同,可将二烯烃分为三类:。
2n-21、累积二烯烃 两个双键与同一个碳原子相连接,即分子中含有C C C构造。
例如:丙二烯 CH 2=C=CH 2 。
2 、 隔 离 二 烯 烃两 个 双 键 被 两 个 或 两 个 以 上 的 单 键 隔 开 , 即 分 子 骨 架为C C (CH 2)nC C。
例如,1、4-戊二烯 CH 2=CH-CH 2-CH=CH 。
3、共轭二烯烃 两个双键被一个单键隔开,即分子骨架为CC C C。
例如,1,3-丁二烯 CH 2=CH-CH=CH 。
二烯烃的命名与烯烃相像,选择含有两个双键的最长的碳链为主链,从距离双键最近的一端经 主链上的碳原子编号,词尾为“某二烯”,两个双键的位置用阿拉伯数字标明在前,中间用短线隔开。
假设有取代基时,则将取代基的位次和名称加在前面。
例如:CH 2=C 〔CH 〕CH=CH 2-甲基-1,3-丁二烯CH 3CH 2CH=CHCH 2CH 〔CH 〕 CH 33,6-十二碳二烯假设有顺反异构请标明,例如:↑HH ↑↑H CH 3 ↑H C C↑CH C C↑CH↑3C CCH 2Z,4Z-2,4-已二烯↑3C C2Z,4E-2,4-已二烯H H HH§4.2 共轭二烯烃的构造 –共轭效应1、共轭二烯烃的构造HH HCHHCC CHHH能量2p20.134nmCH H 2Ψ4 Ψ 3 Ψ 2 Ψ 1C C C CC C C CΨ43个结点Ψ 21个结点Ψ 32个结点Ψ 1 没有结点2.共轭效应[共轭体系]: π电子不是固定在一个双键C 原子之间,而是集中到几个双键C 原子之间,形成一个整体。
炔烃和二烯烃

第四章炔烃和二烯烃(I )炔烃一、定义、通式和同分异构体定义:分子中含有碳碳叁键的不饱和烃。
通式:C n H 2n-2同分异构体:与烯烃相同。
二、结构在乙炔分子中,两个碳原子采用SP 杂化方式,即一个 2S 轨道与一个2P 轨道杂化, 组成两个等同的 SP 杂化轨道,SP 杂化轨道的形状与 SP 2、SP 3杂化轨道相似,两个SP 杂化 轨道的对称轴在一条直线上。
两个以SP 杂化的碳原子,各以一个杂化轨道相互结合形成碳碳6键,另一个杂化轨道各与一个氢原子结合,形成碳氢 6键,三个6键的键轴在一条直线上,即乙炔分子为直线型分子。
每个碳原子还有两个末参加杂化的P 轨道,它们的轴互相垂直。
当两个碳原子的两P轨道分别平行时,两两侧面重叠,形成两个相互垂直的 n 键。
三、命名炔烃的命名原则与烯烃相同,即选择包含叁键的最长碳链作主链,碳原子的编号从 距叁键最近的一端开始。
若分子中即含有双键又含有叁键时,则应选择含有双键和叁键的最长碳链为主链, 并将其命名为烯炔(烯在前、炔在后)。
编号时,应使烯、炔所在位次的和为最小。
例如:CfCfCHCHDHC 三 CH3-甲基-4-庚烯-1-炔CH 3但是,当双键和叁键处在相同的位次时,即烯、炔两碳原子编号之和相等时,则从 靠近双键一端开始编号。
如:Cf 二C 比三CH1-丁烯-3-炔四、 物理性质与烯烃相似,乙炔、丙炔和丁炔为气体,戊炔以上的低级炔烃为液体,高级炔烃为 固体。
简单炔烃的沸点、熔点和相对密度比相应的烯烃要高。
炔烃难溶于水而易溶于有机溶剂。
五、 化学性质 (一)加成反应1、催化加氢炔烃的催化加氢分两步进行,第一步加一个氢分子,生成烯烃;第二步再与一个氢分加成,生成烷烃。
催化剂HC 三 CH + H 2 —CH2、加卤素炔烃与卤素的加成也是分两步进行的。
先加一分子氯或溴,生成二卤代烯,在过量 的氯或溴的存在下,再进一步与一分子卤素加成,生成四卤代烷。
HC 三CH + Br2 -------- Br=CHBrCHB 广2CHB 2虽然炔烃比烯烃更不饱和,但炔烃进行亲电加成却比烯烃难。
4第四章 炔烃 二烯烃
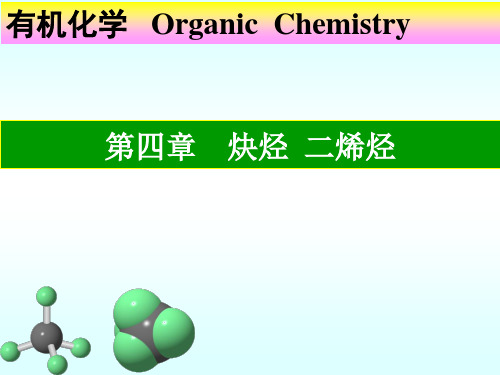
RCCR` KMnO4 RCOOH + R`COOH
H2O
(2) 缓慢氧化——二酮
OO
CH3(CH2)7CC(CH2)7COOH
KMnO4 H2O
CH3(CH2)7-C-C-(CH2)7COOH
pH=7.5
92%~96%
•利用炔烃的氧化反应,检验叁键的存在及位置
•这些反应产率较低,不宜制备羧酸或二酮.
有机化学 Organic Chemistry 第四章 炔烃 二烯烃
第四章 炔烃 二烯烃
(一) 炔烃
定义:分子中含有碳碳叁键的烃叫做炔烃,它的通式:
CnH2n-2 官能团为: -CC-
4.1 炔烃的异构和命名**
(1)异构体——从丁炔开始有异构体.
•同烯烃一样,由于碳链不同和叁键位置不同所引起的.由 于在碳链分支的地方不可能有叁键的存在,所以炔烃的 异构体比同碳原子数的烯烃要少. •由于叁键碳上只可能连有一个取代基,因此炔烃不存在 顺反异构现象.
炔烃和烯烃一样,也能和卤化氢、卤素等起亲电加成反
应,但炔的加成速度比烯慢
(A) 和卤素的加成
Br2
RC CR
Br
+
RC CR
Br-
反式加成
Br
R
CC
R
Br
卤素的活性F2>Cl2>Br2>I2
Br Br Br2 R C C R
这一反应可用于炔烃的鉴别。
Br Br
控制条件也可停止在一分子加成产物上.
❖加氯必须用FeCl3作催化剂。
•含有双键的炔烃在命名时,一般 先命名烯再命名炔 .
碳链编号以表示双键与叁键位置的两个数字之和最小
为原则。在同等的情况下,要使双键的位次最小。
第四章 炔烃和二烯烃

4.1 炔烃
二、炔烃的命名 1. 衍生物命名法
衍生物命名法只适用于简单的炔烃。以乙炔为母体,将其它的炔 烃看作乙炔的衍生物。
例如:
4.1 炔烃
2. 系统命名法
与烯烃的命名类似 ① 要选择含有 C≡C 的最长碳链为主链; ② 编号从最距离叁键最近的一端开始,并用阿位伯数字表示叁键的 位置。例:
837KJ/mol 0.120nm
611KJ/mol 0.134nm 0.108nm
( 3x347=1041)
347KJ/mol
0.154nm 0.110nm
H C C H H2C CH H
H3C C H2 H
原因: ① -C≡C-中有1个σ和2个π键; ② sp 杂化轨道中的 s 成份多。(s 电子的特点就是离核近,即 s 电子
CNa CNa + 2CH3I
CH3C CC2H5 + NaBr
CH3C CCH3 + 2NaI
炔化物作为亲核试剂,也可以与醛酮 发生亲核加成反应,得到 羟基炔化合物:
4.1 炔烃
(3) 过渡金属炔化物的生成及炔烃的鉴定
CH CH + 2Ag(NH3)2NO3 CH CH + 2Cu(NH3)2Cl
4.1 炔烃
③分子中同时含有双键和参键时,先叫烯后叫炔,编号要使双键和
参键的位次和最小。
1 2 3 45
CH C-CH=CHCH3
3-戊烯-1-炔
6 54 3 2 1
CH C-CH=C-CH=CH2
3-乙基-1,3-己二烯-5-炔
CH2CH3
④若双键、叁键处于相同的位次供选择时,优先给双键以最低编号。
4.1 炔烃
第4章 炔烃、二烯烃
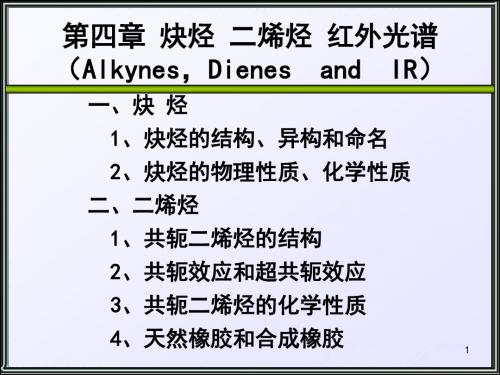
碳素酸的弱酸性
Na
+ 2 HC
+
HC
CH
CH
110℃
2 HC
CNa
+H
NH3
2
NaNH2
HC
CNa
+
13
R3C CH
Ka
R3C C
CH
+
44
H
+
物质名称
pKa
HOH
HC
H2 C
CH2
H3 C
CH3
15.7
25
50
端炔酸性的解释 端炔中的碳为sp杂化, 轨道中s成分较大, 核 对电子的束缚能力强, 电子云靠近碳原子, 使分子中的C-H键极性增加, 易断裂:
HC CH
+ 2 Ag(NH3)2NO3
+ 2 Cu(NH3)2Cl
AgC
CAg
+ 2 NH4NO3 + 2 NH3
乙炔银(白色)
HC CH
CuC
CCu
+ 2 NH4Cl + 2 NH3
乙炔亚铜(砖红色)
应用: 区别端炔与非端炔、端炔与烯烃。
RC CH
16
炔化物的生成
注意:炔化银或炔化亚铜在干燥状态下, 受热或震动容易爆炸。实验完毕后 加稀硝酸使其分解。
+
RC
CH2
> RCH
+
CH
22
炔烃的亲电加成
炔烃与烯烃反应活性比较: 炔烃的加成速度比烯烃慢。
加卤素
当化合物中同时含有双键和叁键时, 首先在双键上发生加成反应。
Br2 低温
Br Br
选择性加成
烯烃炔烃二烯烃

>
③若第一个原子以双键或三键与其它原子相连时,则把它看作与两个或 三个其它原子以单键相连.
<
<
<
<
<
<
Z/E命名实例
-1-氯-2-溴丙烯
01
-1,2-二氯-1-溴丙烯 或 反-1,2-二氯-1-溴丙烯
01
(2E,4Z)-5-甲基-2,4-庚二烯
01
命名实例
实例一
01
( 5R ,2E)-5-甲基-3-丙基-2-庚烯 (5R,2E)-5-methyl-3-propyl-2-heptene
反 应 的 立 体 化 学
(一) 催化氢化
第四节 烯烃的其它反应
稳定性增加 双键碳上连有烷基多的烯烃是内能较低的、稳定的烯烃。
二、自由基加成反应
烯烃受自由基进攻而发生的加成反应称为自由基加成反应。
CH3CH=CH2 + HBr CH3CH2CH2Br
反应机理 机理1: + X2 X+ H+
丙烯与卤素及水作用时,遵循马氏规则,卤原子主要加到丙烯末端的碳原子上。 CH3OH OCH3
反 应 条 件: 加温加压
产 率: 几乎定量
常用催化剂: Pt > Pd > Ni
1 顺式为主
2 空阻小的双键优先
3 空阻小的一侧优先
CCl4
50oC
(CH3)2CHCH=CHCH3 + Br2 (CH3)2CHCHBrCHBrCH3
CCl4
0oC
反 应 机 理
A、 反应分两步进行 B、第一步是速度控制步骤 C 、反式加成
CH3CH=CH2 + Br2 CH3CHCH2 + CH3CHCH2 Br Br Cl Br
炔烃 二烯烃

第四章炔烃二烯烃学习要点:本章学习在了解炔烃和二烯烃结构的基础上,重点掌握这两类化合物的化学性质以及由共轭二烯烃的结构特征所引起的共轭效应及其对化学性质的影响。
第一节炔烃不饱和烃除了烯烃外还有炔烃。
例如气割气焊用的乙炔(HC≡CH),就是一个炔烃,凡含有碳碳叁键的不饱和烃均称为炔烃,碳碳叁键(-C≡C-)是它的官能团,它的通式为C n H2n-2,与碳原子数相同的二烯烃,环烯烃为同分异构体。
一、炔烃的结构以炔烃中结构最简单的乙炔为例,在乙炔中两个叁键碳原子都是只和两个原子相结合,因此它只需要用两个价电子来构成两个σ键,亦即炔碳原子中的s电子轨道只要和一个p电子轨道进行sp杂化就可以了,形成了两个相等的sp杂化轨道,如图4-1所示。
图4-1 碳原子轨道的sp杂化每个sp杂化轨道包含1/2s轨道成分和1/2p轨道成分,其形状与sp3,sp2杂化轨道相似,只是更“胖”些,两个sp杂化轨道对称地分布在碳的两侧,成为一条直线,两者之间的夹角为180º。
如图4-2所示。
所以在乙炔中每一个碳都以一个sp杂化电子轨道与氢的1s电子轨道相互重迭成为一个C-H键,两个碳又各以一个sp杂化轨道相重迭,形成C-C键,这些都是σ键。
图4-2 碳原子的sp杂化电子轨道两个C原子尚各余两个p电子轨道,它们的对称轴都与sp杂化轨道的对称轴互相垂直,这两个p轨道可以在各自侧面重迭形成两个π键,所以炔键叁键中一个是σ键,两个是π键。
实际上叁键中四个π电子的电子云是混合在一起,它们围绕着连接两个碳核的直线成圆筒形分布。
如图4-3所示。
图4-3 乙炔分子的圆筒形π电子云其他炔烃的碳碳叁键与乙炔相同,也是由一个σ键和两个π键组成。
二、炔烃的同分异构和命名炔烃中除了乙炔和丙炔没有异构体外,从丁炔开始有构造异构现象,但由于叁键碳上只有一个取代基,因此炔烃的构造异构体比烯烃少,也无顺反异构体。
例如丁烯有三个构造异构体,但丁炔只有两个构造异构体,如下:CH3CH2C CH CH3C CCH31-丁炔2-丁炔简单的炔烃可采用衍生物命名法,即以乙炔作母体,将其它基团看成取代基,而复杂的炔烃必须采用系统命名法,炔烃的命名与烯烃相似,只须将“烯”改为“炔”即可。
第四章炔烃和二烯烃全解

1
2
CH2
CH CH2 C CH
1-戊烯-4-炔
3
4
5
应命名为 3-戊烯-1-炔,而不命名为 2-戊烯-4-炔。
H3C C C CH2CHCH3
H3C C C C CH H H
5-乙基-1-庚烯-6-炔
not 3-乙基-6-庚烯-1-炔
(CH3)2CH C C H
H CH2C CH
(E)-6-甲基-4-庚烯-1-炔
CH3C CNa
HBr ROOR CH3CH2CH2Br
CH3C
CH
H2
Lindlar
CH3CH=CH2
CH3C
H2 Ni
CNa CH3C lig . NH3
CCH2CH2CH3
CH3CH2CH2CH2CH2CH3
3、与重金属盐的反应
♦ 1- 炔烃与银氨溶液反应,立即生成白色的炔化银沉 淀;与氯化亚铜氨溶液反应则生成砖红色的炔化亚 铜沉淀,只有端炔有此性质,是 区别端炔与非端炔 及烯烃的方法。
[Ag(NH3)2]
+
R C CH
R C CAg
炔化银
白色沉淀
HC
CH
[Cu(NH3)2]
+
CuC
CCu
砖红色沉淀
乙炔亚铜
区别乙烷、乙烯、乙炔
CH CH CH2=CH2 CH3CH3
Ag(NH3)2+
白色 ( ( ) )
(CH CH )
Br2/CCl4
褪色(CH2=CH2) ( -)
爆炸品——炔化银
炔烃的命名
炔烃的普通命名法是将其他炔烃看成乙炔 的衍生物命名。例如: (CH3)3C–C≡C–H 叔丁基乙炔 (CH3)3C–C≡C–C(CH3)3 二叔丁基乙炔 F3C–C≡C–H 三氟甲基乙炔 系统命名法与烯烃相似,只是将“烯”字 改为“炔”字。
第四章 炔烃和二烯烃 炔烃 二烯烃 共轭效应速度控制和平衡控制

H C=C H
R C=C H
(1)乙炔生成炔化银和炔化铜的反应
乙炔通入硝酸银的氨溶液或氯化亚铜的 氨溶液中,析出白色的乙炔银沉淀 或棕 红色的乙炔亚铜沉淀 。
RC CH + NaNH2 lig.NH3 RC C-Na+ + NH3
式烯烃。
C6H5 C6H5
C6H5-C≡C-C6 H5+H2 Lindlar Pd C=C
HH
(2)化学还原
在液氨中钠或锂还原炔烃主要得到反式 烯烃.
C3H7-C≡C-C3H7 +2Na+2NH3
C3H7
H
C==C + 2Na+NH-2
H
C3H7
(E)-4-辛烯 97%
化学还原过程:Na/lig NH3
更大. 乙炔的丙酮 溶液安定,乙炔在1.2MPa下压
入盛满丙酮浸润饱和的多孔物质的钢筒 中.
(1)乙炔的聚合反应
乙炔的聚合反应在不同的催化剂作用下, 发生二聚,三聚,四聚等低聚作用。与烯烃 的聚合反应不同,它一般不聚合成高聚 物。
在氯化亚铜-氯化铵的强酸溶液中,发生 线性型偶合而生成乙烯基乙炔。
碳叁键。
碳原子以SP杂化轨道 形成C-C键和C-H键。
每个碳原子以两个互相垂直的
未杂化的P轨道,两两互相侧面 重叠形成两个互相垂直的π键。
CC
乙炔分子的键参数:C≡C键长为0.12nm, 键能为835kJ/mol.
HC
CH
乙炔的π电子云
第四章 炔烃和二烯烃
思考:炔烃是否有顺反异构? 思考:炔烃是否有顺反异构?
杂化的碳上只连接一个基团。 无!因为炔烃的sp杂化的碳上只连接一个基团。
(二) 物理性质
Physical Properties
简单炔烃的沸点、 简单炔烃的沸点、熔点以及密度比碳 原子数相同的烷烃和烯烃高一些。 原子数相同的烷烃和烯烃高一些。炔烃 分子极性比烯烃稍强。炔烃不易溶于水, 分子极性比烯烃稍强。炔烃不易溶于水, 而易溶于石油醚、乙醚、 而易溶于石油醚、乙醚、苯和四氯化碳 中。
酸 性 逐 渐 增 强
C-H键中,C使用的杂化轨道 轨道成分越多,H的酸性越强。 键中, 使用的杂化轨道 轨道成分越多, 的酸性越强 使用的杂化轨道S轨道成分越多 的酸性越强。 键中
碳氢化合物中H的酸性顺序: 的 C H> sp
HC CH Na
C H> sp
2
C H sp3
HC CNa
H2
生成的炔钠是一个亲核试剂
1. 分别用纽曼投影式和锯架式画出1-氯丙烷 分别用纽曼投影式和锯架式画出1 的优势构象。 的优势构象。
CH3CH2CH2Cl
CH3 H H Cl H H
CH3 H H Cl H H
第四章
炔烃和二烯烃
第一节
炔烃( 炔烃(alkynes) )
(一) 结构和命名
C C
H C C H 线型分子
一个σ键两个π 一个σ键两个π键
聚集二烯 二烯烃 共轭二烯 隔离二烯
CH2=C=CH2 CH2=CH-CH=CH2 CH2=CH-CH2-CH=CH2
聚集二烯: 聚集二烯
sp2
H C=C=C H
H H
CH2=C=CH2 sp
是一类少见的结构,聚集的双键使分子能量高 是一类少见的结构 聚集的双键使分子能量高。 聚集的双键使分子能量高 隔离二烯: 隔离二烯: 分子中的两个双键缺少相互影响, 分子中的两个双键缺少相互影响,其性质与 单烯烃无差别。 单烯烃无差别。 共轭二烯: 共轭二烯: 分子中两个双键存在相互影响, 分子中两个双键存在相互影响,共同组成共轭 体系,含共轭体系的多烯烃称为共轭烯烃。 体系,含共轭体系的多烯烃称为共轭烯烃。
第四章--炔烃和二烯烃

180°
1.sp杂化轨道
2p 2s
激发
2p 2s
杂化 p
sp
杂化后形成两个sp杂化轨道(含1/2 S和1/2 P成份),
剩余两个杂化P旳轨道。两个sp杂化轨道成1800分布,两个
未杂化旳P(PY、PZ)轨道相互垂直,它们与中一碳旳两个P轨 道两两相互侧面重叠形成两个相互垂直旳键。
py
②其他炔化物 乙炔或碳碳三键在链端旳炔烃与硝酸银或氯化 亚铜旳氨溶液作用,立即生成白色旳炔化银或 红色旳炔化亚, H2O
RC CAg (白)
RC CH + Cu2Cl2 NH3 , H2O
RC CCu (红)
炔化银和炔化亚铜在干燥状态下,受热或撞击易分解
6 氧化反应
•(1) 炔烃用高锰酸钾氧化,碳链在三键处断裂,生成羧酸。 反应后KMnO4旳颜色褪去,所以能够用作炔烃旳定性鉴 定(反应难于烯烃)。
(2) O3氧化,可发生叁键旳断裂,生成两个羧酸,例如:
O R C C R' O3 R C C R' H2O
OO R C C R' + H2O2 RCOOH + R'COOH
第四章
炔烃和二烯烃
1. 通式:CnH2n-2 2. 炔烃官能团:-C≡C3. 二烯烃官能团:-C=C-
【学习要求】
炔烃和二烯烃
1 掌握炔烃旳构造和命名。 2 掌握炔烃旳旳化学性质,比较烯烃和炔烃化学性 质旳异同。 3 掌握共轭二烯烃旳构造特点及其主要性质。 4 掌握共轭体系旳分类、共轭效应及其应用。
分子轨道理论解释: 1,3-丁二烯旳分子轨道
因为离域键旳存在使得丁二烯分子中旳C = C和C-C不 同于一般旳双键和单键,丁二烯分子中碳碳单键旳键长 为0.148nm,比乙烷中旳0.153nm短,这阐明丁二烯分子 中碳碳单键具有某些双键旳性质。
有机化学课件(李景宁主编)第4章_炔烃和二烯烃

CH3 C CH
Br2
CH3 C CH Br Br
Br2
CH3
Br Br C CH Br Br
现象:溴的红棕色消失,用于检验烯烃、炔烃及其他含有碳碳 重键的化合物。
C
C
CH3 + Br2
C
Br +
C
CH3
Br-
C Br
C
Br CH3
反式加成
CH2 CH CH2 C CH + Br2
-20 C CCl4
其过程为自由基加成得反马式加成产物与水的加成烯醇式不稳定酮式稳定互变异构两种构造异构体处于相互转化的平衡中在转化tomerizm
作业
P98 2(1)(2)(3); 8; 14(6); 19. 11;
第四章 炔烃和二烯烃
alkyne and diene
AgNO3
6、聚合
TiCl4 Al(C2H5)3 聚乙炔类导电聚合物由日本化学家白川英树研 n HC CH CH CH 制成功,2000年获诺贝尔化学奖。顺式和反式 n
炔烃和二烯烃

Ni(CO)2 CH3
[(C6H5)3P]2· Ni(CO)2 3 CH3 CH CH
H3C
CH3
均三甲苯
有机化学
炔烃
36
四、金属炔化物的生成
乙炔和1-炔烃(R-C≡CH)分子中,连接在叁键碳(sp杂化) 上的氢原子受叁键碳电负性的影响,其C-H σ键中共用电 子对偏向叁键碳一侧,而使得该H原子能以质子(H+)的形 式离去,则该H具有弱酸性,是活泼氢原子。
Zn(OOCCH3)2
170~230℃
此法是制备聚乙烯醇的重要方 法,因乙烯醇极不稳定,无法聚 合。此产物经聚合后水解,得聚 乙烯醇。在碘溶液中快速拉伸, 制得偏振片。
O
CH3 C O CH CH2
乙酸乙烯酯 又称“醋酸乙烯酯” 生产维尼纶的主要原料。
有机化学
炔烃
30
二、氧化反应
炔烃更易被氧化剂(如 KMnO4、臭氧化) 氧化。 乙炔通入高锰酸钾溶液中,即可被氧化成CO2和H2O,同时
42
5
3
1
3-戊烯-1-炔
4-甲基-1-庚烯-5-炔
有机化学
炔烃
6
二、炔烃的系统命名法
④. 当从两侧起,双键、叁键处于相同位置时,则应选择使 双键的位置较小的编号方式。
5
3
1
6
4
2
1-己烯-5-炔
有机化学
炔烃
7
4.2 炔烃的结构
炔烃的结构特征是分子中含有“C≡C”,它与“C=C”一 样,是由σ 键和 π 键构成。
下面以乙炔为例说明叁键的形成及结构 乙炔为一直线型分子,全部四个原子在同一直线上,
第4章-2 不饱和烃-炔烃及二烯烃

2. 还原反应
(1) 催化加氢反应
炔烃的还原反应可以还原到烯烃, 也可以还原到烷烃。
炔烃加氢反应也需要催化剂,可以加一分子氢,也可以加两分 子氢,实际应用中多数控制在加一分子氢。
如果使用钝化催化剂,可以得到顺式烯烃:
CH3CH2 CH3CH2C CCH2CH3 + H2 钝化催化剂 C C H H CH2CH3
H3 C C C CH3 HCI CI HCI H3 C C C H CH3 CI CH3 CH2C CH3 CI
乙炔与HCl加成需要有催化剂才能顺利反应,是合成氯乙烯 的工业方法: HgCI2/C + HCI HC CH H2C CHCI 溴化氢也能与炔烃加成:
CH3CH2CH2CH2C CH + HBr 无水 Fe
对称内炔烃 不对称内炔烃
例如: NaC
R1C
R C R1 C
+ R2
炔烃的重要合成方法之一
3.过渡金属炔化物的生成
乙炔、端炔烃能与硝酸银或氯化亚铜的氨溶液反应,生成白色 炔化银或砖红色炔化亚铜沉淀,可用来鉴定乙炔和端炔的存在:
白色 砖红色
乙炔 和 端炔 的特征反应
干燥的炔化银、炔化亚铜易爆炸。 20
(2)亲核加成反应的机理:
CH3OH + -OH HC CH + CH3O
以乙炔与甲醇在氢氧化钾催化下反应为例说明: CH3O + H2O
慢
快
HC C OCH3 H H2C C OCH3 + CH3O H
12
- HC C OCH + CH OH 3 3 H
4.6.2 氧化和还原反应
1. 氧化反应
炔烃经KMnO4或臭氧氧化后再水解,在叁键 处断裂,生成相应的酸:
第四章炔烃和二烯烃习题答案第五版

第四章炔烃和二烯烃习题答案第五版第四章炔烃和二烯烃(P98-101)1.写出C6H10的所有炔烃异构体的构造式,并用系统命名法命名之。
2.命名下列化合物。
(1)2,2,6,6-四甲基-3-庚炔(给官能团以最低系列)(2)4-甲基-2-庚烯-5-炔(烯炔同位,以先列的烯给小位次)(3)1-己烯-3,5-二炔(烯炔同位,以先列的烯给小位次)(4)(Z)-5-异丙基-5-壬烯-1-炔(5)(2E,4Z)-3-tert-butylhexa-2,4-diene,(2E,4Z)-3-叔丁基-2,4-己二烯(注意构型的对应)3.写出下列化合物的构造式和键线式,并用系统命名法命名。
(1)烯丙基乙炔(2)丙烯基乙炔(3)二叔丁基乙炔(4)异丙基仲丁基乙炔4.写出下列化合物的构造式,并用系统命名法命名。
(1)(3)(2)(4)5.下列化合物是否存在顺反异构体,若存在则写出其构型式。
(1)(4)分子存在两个顺反异构体。
(2)(3)分子不存在顺反异构体。
6.提示:ΔH等于断开各个键所需能量之和减去生成各个化学键所放出的能量之和。
正值为吸热反应,负值为放热反应。
(1)ΔH=835.1-610+188.3-2×284.5=-155.6kJ.mol-1(2)ΔH=835.1-610-345.6=-120.5kJ.mol-1(3)ΔH=835.1-610+368.2-415.3-284.5= -106.5kJ.mol-17.分析:1,4-戊二烯氢化热的值为:2(π键键能)+2(H-Hσ键键能)-4(C-Hσ键键能)=2*(610-345.6)+2*436-4*415.3=-260.4kJ.mol-1因此,1,3-戊二烯的离域能为:260.4-226=34.4kJ.mol-18.写出下列反应的产物。
(1)(2)(3)(4)(5)(6)(7)9.用化学方法区别下列化合物。
(2)解:10.戊烯与溴等摩尔加成,反应用去0.005摩尔溴,因此混合物中戊烯的质量为0.35克,质量分数为7:20。
炔烃和二烯烃

农业化学品
除草剂
01
炔烃和二烯烃可用于合成除草剂,如草甘膦、百草枯等,这些
除草剂在农业生产中有广泛应用。
杀虫剂
02
炔烃和二烯烃可用于合成杀虫剂,如滴滴涕、马拉硫磷等,这
些杀虫剂在防治农业害虫方面有重要作用。
植物生长调节剂
03
炔烃和二烯烃可用于合成植物生长调节剂,如赤霉素、细胞分
裂素等,这些调节剂可调节植物生长和发育。
05 炔烃和二烯烃的未来发展
新材料的开发
高性能聚合物
利用炔烃和二烯烃的特殊化学性质,开发出具有优异力学 性能、热性能和化学稳定性的新型聚合物材料,用于航空 航天、汽车、电子等领域。
功能性材料
通过炔烃和二烯烃的聚合反应,制备具有光、电、磁等功 能的材料,应用于传感器、光电转换器件、磁存储等领域。
生物医用材料
03 炔烃和二烯烃的反应
加成反应
01
碳碳双键和碳碳三键的加成反应
炔烃和二烯烃中的碳碳双键和碳碳三键容易发生加成反应,可以与氢气、
卤素、卤化氢等发生加成反应,生成相应的烷烃或卤代烃。
02
加成反应的催化剂
某些金属催化剂如铂、钯、镍等可以促进炔烃和二烯烃的加成反应。
03
加成反应的立体化学特征
加成反应可以遵循不同的立体化学规则,如顺式加成、反式加成和协同药物合成Leabharlann 1 2 3激素类药物
炔烃和二烯烃可用于合成激素类药物,如雌二醇、 睾酮等,这些药物在调节人体生理功能和治疗某 些疾病方面有重要作用。
抗生素类药物
炔烃和二烯烃可用于合成抗生素类药物,如青霉 素、头孢菌素等,这些药物在抗菌、消炎等方面 有广泛应用。
其他药物
炔烃和二烯烃还可用于合成其他药物,如抗癌药 物、镇痛药等。
有机化学第4章 炔烃和二烯烃

1、碳sp杂化轨道的电负性大于碳sp2杂化轨道的电负性,炔中 电子控制较牢。三键键长短,两个P轨道重叠程度大,稳定。
2、从反应形成的碳正离子的稳定性来看,炔加成形成的烯基
碳正离子中,C+与CSP2相连,SP2的电负性大,不利于正电荷 的分散,故稳定性不如烷基碳正离子。
R-C CH + E+ R-C CH2 + E+
98%
3-庚炔
(E)-3-庚烯
6、HCN、EtOH、CH3COOH等的亲核加成反应
定义:亲核试剂进攻炔烃的不饱和键而引起 的加成反应,称为炔烃的亲核加成。
常用的亲核试剂有: ROH(RO-)、HCN(-CN)、RCOOH(RCOO-)
碱,150-180oC
(1). CHCH + HOC2H5
聚合,催化剂
NH3(L) RC C Na
RC C Na + CH3X
RC C + CH3 X
RC CCH3
RC CCH3
(可看作是强碱与弱酸之间的盐的反应)
CH3CH2C≡CNa + CH3CH2CH2Br CH3CH2C≡CCH2CH2CH3 + NaBr ( R-X=1°RX)
乙炔基负离子、乙烯基负离子、乙基负离子的结构:
SP 乙炔基负离子
碱性: 酸性:
SP2 乙烯基负离子
SP3 乙基负离子
5、还原
1)催化加氢
R C C R' + H2
pd
R C
R' C
H2
H
H pd
RCH2CH2R'
Lindlar Cat. RC CR' + H2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四章 二烯烃和炔烃(6学时)§4.1二烯烃的分类和命名分子中含有两个或两个以上碳碳双键的不饱和烃称为多烯烃。
二烯烃的通式为C n H 2n-2。
一、二烯烃的分类和命名根据二烯烃中两个双键的相对位置的不同,可将二烯烃分为三类:1、累积二烯烃 两个双键与同一个碳原子相连接,即分子中含有 结构。
例如:丙二烯 CH 2=C=CH 2 。
2、隔离二烯烃 两个双键被两个或两个以上的单键隔开,即分子骨架为 。
例如,1、4-戊二烯CH 2=CH-CH 2-CH=CH 2。
3、共轭二烯烃两个双键被一个单键隔开,即分子骨架为 。
例如,1,3-丁二烯 CH 2=CH-CH=CH 2。
二烯烃的命名与烯烃相似,选择含有两个双键的最长的碳链为主链,从距离双键最近的一端经主链上的碳原子编号,词尾为“某二烯”,两个双键的位置用阿拉伯数字标明在前,中间用短线隔开。
若有取代基时,则将取代基的位次和名称加在前面。
例如:CH 2=C (CH 3)CH=CH 2 2-甲基-1,3-丁二烯 CH 3CH 2CH=CHCH 2CH (CH 2)4CH 3 3,6-十二碳二烯 若有顺反异构请标明,例如:C H 3CH C C HCCH 3HH↑↑↑↑2Z,4Z-2,4-已二烯C H 3CH CC HC3HH↑↑↑2Z,4E-2,4-已二烯↑§4.2 共轭二烯烃的结构 – 共轭效应1、共轭二烯烃的结构C C C C C C (CH 2)n C C C C C HHC HC HH HCH 2H CC HCH 20.134nm0.148nm31242p3ΨΨ43个结点2个结点12ΨΨ没有结点1个结点2.共轭效应[共轭体系]:π电子不是固定在一个双键C 原子之间,而是扩散到几个双键C 原子之间,形成一个整体。
这种现象叫离域。
这样的体系,叫共轭体系。
π-π共轭体系:CH 2=CH-CH=CH 2,CH=CH-, CH=O ,苯等。
p-π共轭体系:CH 2=CHCl[共轭效应]:指共轭体系中,原子间的一种相互影响。
这种影响,使得分子更稳定,内能更小,键长趋于平均化,并引起物质性质的一系列改变。
静态共轭效应和动态共轭效应 正共轭效应(+C )和负共轭效应(-C )[共轭效应特点] 1).共平面性。
2).键长趋于平均化。
3).折射率高。
4).共轭链中π电子云转移时,链上出现正负性交替现象。
5).共轭效应,使得体系内能降低。
例:1,3丁二烯,其氢化热较低。
单烯烃的氢化热为125.5KJ/mol预计: 1,3丁二烯的氢化热为 实测: 1,3丁二烯的氢化热为238KJ/mol 1,3丁二烯238KJ/mol[超共轭效应]:烷基上的C 原子与H 原子结合,对于电子云屏蔽的效力很小,所以这些电子比较容易与邻近的H 2CCH +CH 2CH -Cδ -δ+H 2CCH 2δ+δ -π电子共轭,发生电子的离域现象。
即σ键与π键之间的电子位移,使体系变得稳定,这种σ键的共轭称为超共轭效应。
超共轭效应一般是给电子的,其大小顺序如下:-CH3> -CH2R > -CHR2> -CR3H超共轭效应所起的影响比共轭效应要小得多。
例:1-丁烯和2-丁烯H2C3HC碳正离子的稳定性可由超共轭效应解释。
+CCH3H3CCH3+CCH3HCH3+CHHCH3+CH3>>>共轭效应与诱导效应是不相同的。
诱导效应是由键的极性所引起的,可沿σ键传递下去,这种作用是短程的,一般只在和作用中心直接相连的碳原子中表现得最大,相隔一个原子,所受的作用力就很小了。
而共轭效应是由于P电子在整个分子轨道中的离域作用所引起的,其作用可沿共轭体系传递。
共轭效应不仅表现在使1,3-丁二烯分子中的碳碳双键健长增加,碳碳单键健长缩短,单双键趋向于平均化。
由于电子离域的结果,使化合物的能量降低,稳定性增加,在参加化学反应时,也体现出与一般烯烃不同的性质。
§4.3二烯烃的物理性质(自学)§4.4二烯烃的反应H2氢化热:126.8 KJ/mol+H2C CH CH2CH3CH3CH2CH2CH3H2氢化热:119.6 KJ/mol+HC CH CH3CH3CH2CH2CH3H3C一、亲电加成反应( 1,2-和1,4-加成反应)与烯烃相似,1,3-丁二烯能与卤素、卤化氢和氢气发生加成反应。
但由于其结构的特殊性,加成产物通常有两种。
例如,1,3-丁二烯与溴化氢的加成反应:这说明共轭二烯烃与亲电试剂加成时,有两种不同的加成方式。
一种是发生在一个双键上的加成,称为1,2-加成另一种加成方式是试剂的两部分分别加到共轭体系的两端,即加到C1和C4两个碳原子上,分子中原来的两个双键消失,而在C2与C3之间,形成一个新的双键,称为1,4-加成。
CH2=CH-CH2CH2CH2CH2=CH-CH-CH2CH2-CH=CH-CH2Br BrBr Br3,4-二溴-1-丁烯(E)-1,4-二溴-2-丁烯1,2加成1,4加成(共轭加成) 1,4-加成的解释:1. Br+离子进攻C1位:,结合成键,生成碳正离子C+Br2CH2δδ-+δ+-1234BrH2C CH CH CH2+1234BrH2CHCHC CH2+1234------------δ+δ2. Br –负离子进攻C2位或C4,电子云发生转移,形成双键:BrH2CHCHC123-------------BrH2C CHHC CH21234BrBrH2C CHCHCH21234Br1,2加成和1,4加成的多少,取决于双烯的结构和反应条件:A 一般:较高温度和长时间反应得:1,4加成产物(热力学稳定控制);B 低温反应得1,2加成产物(动力学控制)C 共轭烯烃结构的影响:加成产物的稳定性对加成的方式有时起着重要作用。
例如2-甲基-1,3-丁二烯的加成,只得到1,4-加成产物:D 溶剂极性的影响:加成反应在极性溶剂中进行,主要按1,4-加成加成反应在非极性溶剂中进行,主要按1,2-加成二、双烯合成反应(Diels-Alder反应)(合成六元环的重要反应)共轭二烯烃与某些具有碳碳双键的不饱和化合物发生1,4-加成反应生成环状化合物的反应称为双烯合成,也叫第尔斯-阿尔德(Diels-Alder)反应。
这是共轭二烯烃特有的反应,它将链状化合物转变成环状化合物,因此又叫环合反应。
+一般把进行双烯合成的共轭二烯烃称作双烯体,另一个不饱和的化合物称为亲双烯体。
一些常见的二烯体:O一些常见的亲二烯体:R CHO CN CO2R COOCORDiels-Alder反应的特点:(1) 共轭二烯的电子密度高,亲二烯体上有吸电子基团时,反应很容易进行:如亲二烯体=R—CH=CH—,如R= -CN、-COOR、—CHO、-COR、—COOH等吸电子的基团时,对反应有利。
(2) Diels-Alder反应是顺式加成反应, 加成产物仍保持二烯和亲二烯体原来的构型.CO2CH3CO2CH3CO2CH3H3CO2C2CH32CH32CH32CH3++150-160℃150-160℃(3) 反应无需酸碱的催化,为协同反应,一步反应完成,无反应中间体产生,有一个6员环状过渡态三、聚合反应共轭二烯烃在聚合时,即可发生1,2-加成聚合,也可发生1,4-加成聚合。
C H2C H2C H2CN CN+C H2CH2C H2CN124,加成聚合物1,顺式CHCH CH 2H 2C CH 2C HH CH 2Cn 催化剂n CC CH 2HH H 2C CCCH 2HH H 2Cnn反式加成聚合物41,加成聚合物顺式CH 2HC C HH 2Cn CC CH 2HHH 2C n41,加成聚合物用Ziegler-Natta 催化剂,可定向聚合:§4.5 炔烃的结构一、定义、通式和结构炔烃:分子中含碳碳叁键的不饱和烃。
通式为C n H 2n-2在乙炔分子中,两个碳原子采用SP 杂化方式,即一个2S 轨道与一个2P 轨道杂化,组成两个等同的SP 杂化轨道,SP 杂化轨道的形状与SP 2、SP 3杂化轨道相似,两个SP 杂化轨道的对称轴在一条直线上。
两个以SP 杂化的碳原子,各以一个杂化轨道相互结合形成碳碳σ键,另一个杂化轨道各与一个氢原子结合,形成碳氢σ键,三个σ键的键轴在一条直线上,即乙炔分子为直线型分子。
每个碳原子还有两个末参加杂化的P 轨道,它们的轴互相垂直。
当两个碳原子的两P 轨道分别平行时,两两侧面重叠,形成两个相互垂直的π键。
碳原子杂化示意图碳碳键 单 键 双 键 叁 键键长(nm) 0.154 0.134 0.120 键能(KJ)345.6 6108352s 2p sp 杂化 2p22C1C2H3H4§4.6 炔烃的同分异构和命名1.异构: 碳键异构, 三键位置异构.2.命名:(1)普通命名:乙炔为母体,其他炔烃作为乙炔的衍生物:(CH3)3CC≡CH(CH3)3CC≡CC(CH3)2CF3C≡CH叔丁基乙炔三氟甲基乙炔二叔丁基乙炔(2) 系统命名A. 以含三键的最长碳链为主链, 称为某炔.B. 从靠近三键的一端开始编号.C. 以位次最小的炔碳表示三键的位置.D. 取代基的位次和书写遵守优先基团后列原则.E. 当有卤原子取代时, 卤原子作为取代基, 炔为母体.当有烯键时,以炔为母体,编号应使烯键和叁键的位次之和最小. 若两者都位于同等位次, 则应以双键位次为最小(次要基团优先)F. 复杂的化合物在命名时可把炔基作为取代基.§4.7 炔烃的物理性质1. bp: 沸点比相应的烯烃高(1) 乙炔,丙炔,1-丁炔为气体.(2) 碳架相同的炔烃, 三键在链端的较低.2. 密度比相应的烯烃高d < 13. 溶解性:弱极性,不溶于水,易溶于非极性或弱极性有机溶剂中;4. 炔烃具有偶极矩.5. 烷基支链多的炔烃较稳定.6. 易燃烧,炔氧焰温度高达:3500 0C,可用于熔融及焊接。
4.8 炔烃的反应●炔烃中的叁键中的碳为sp杂化,sp杂化轨道含较多的s成分,电子离核比较近,不易给出电子。
●杂化轨道的电负性问题:●电负性大小: sp >sp2>sp3,sp杂化轨道的原子电负性大。
虽然炔烃中有两个π键,也不易给出电子,因此炔烃的亲电加成速度比烯烃的亲电加成速度慢。
●由于sp 杂化C电负性较大,故≡C—H 上的H 有一定酸性。
(一)末端炔烃的酸性和炔化物与叁键碳原子直接相连的氢原子活泼性较大。
因SP 杂化的碳原子表现出较大的电负性,使与叁键碳原子直接相连的氢原子较之一般的碳氢键,显示出弱酸性,可与强碱、碱金属或某些重金属离子反应生成金属炔化物。
叁键碳上H 原子的活性1、乙炔与熔融的钠反应,可生成乙炔钠和乙炔二钠:CH≡CH+ Na + Na 2、丙炔或其它末端炔烃与氨基钠反应,生成炔化钠:+ NaNH 2 炔化钠与卤代烃(一般为伯卤代烷)作用,可在炔烃分子中引入烷基,制得一系列炔烃同系物。
