高中化学考点知识网络梳理(一本通)
2024年高中高三化学的必背必考知识点总结范本(二篇)

2024年高中高三化学的必背必考知识点总结范本高中化学是一门重要的学科,它是其他自然科学的基础。
高三化学是高中阶段的最后一年,是学生备战高考的关键时期。
下面是高中高三化学的必背必考知识点总结,帮助学生复习备考。
一、化学基本概念1.原子与元素:原子的结构、元素的表示方法、元素周期表。
2.离子与化合物:离子的定义、离子化合物的性质、离子式和分子式的表示方法。
3.化学方程式:化学方程式的基本形式、配平化学方程式的方法。
4.化学计量与电子结构:摩尔与质量关系、原子量与摩尔质量。
二、化学反应与化学平衡1.化学反应类型:酸碱反应、氧化还原反应、置换反应等。
2.氧化还原反应:电子的概念、氧化剂和还原剂的定义、氧化数的计算。
3.化学平衡:化学平衡的条件、反应速率与化学平衡、平衡常数与平衡常数表。
4.勃朗斯特(E)方程:电解质的溶解与电离度、电解质溶液的性质、离子反应与化学平衡。
5.平衡常数计算:物质摩尔浓度与化学平衡、化学反应的平衡常数计算、平衡常数与温度的关系。
三、化学反应动力学1.化学反应速率:化学反应速率的概念、速率与反应物浓度的关系。
2.反应速率与反应动力学:反应速率的影响因素、速率方程与速率常数。
3.反应速率与反应级数:反应级数、反应速率与反应物浓度的关系。
4.表观活化能与反应速率:表观活化能的概念、表观活化能与温度的关系。
4.平衡与反应速率:平衡体系与反应速率、平衡常数与反应速率的关系。
五、化学体系的熵1.熵的概念与变化:熵的定义、反应熵与熵变、熵变与反应性质的关系。
2.化学反应的熵变:化学反应的熵变计算、熵变与平衡常数的关系。
3.熵变与化学平衡:熵变与反应方向、熵变与平衡常数的关系。
六、化学平衡与电子转移1.电荷转移与配位反应:电子转移的概念、电子转移反应的特点。
2.电子转移反应类型:氧化还原反应、配位反应。
3.电子转移反应与化学平衡:电子转移反应的平衡常数、电子转移反应与温度的关系。
4.电解与电池:电解概念与原理、电解与化学变化、电池的基本概念。
高中化学必修一知识点归纳总结

高中化学必修一知识点归纳总结一、基本概念与原理1. 物质的组成与分类- 物质由元素组成,分为纯净物和混合物。
- 纯净物包括单质和化合物,单质是由同种元素构成,化合物由不同元素以化学键结合。
2. 原子结构- 原子由原子核和电子云组成,原子核包含质子和中子。
- 电子云由电子按能级排布,电子排布遵循保里不相容原理、洪特规则和能量最低原理。
3. 元素周期律- 元素周期表按照原子序数排列元素,显示元素的周期性和族性。
- 元素的性质(如原子半径、电负性、离子化能)随周期表位置变化呈现规律性。
4. 化学键- 化学键包括离子键、共价键和金属键。
- 离子键由电荷吸引力形成,共价键由电子对共享形成,金属键由金属原子间的电子海形成。
5. 化学反应- 化学反应是旧化学键断裂和新化学键形成的过程。
- 化学反应遵循质量守恒定律,即反应前后物质的总质量不变。
二、化学反应类型1. 合成反应- 多种反应物合成一种生成物的反应,如:A + B → AB。
2. 分解反应- 一种反应物分解成多种生成物的反应,如:AB → A + B。
3. 置换反应- 一种单质与一种化合物反应,生成另一种单质和化合物,如:A+ BC → AC + B。
4. 双置换反应- 两种化合物互相交换成分,生成两种新的化合物,如:AB + CD→ AD + CB。
三、化学计算1. 摩尔概念- 摩尔是物质的量单位,1摩尔物质含有阿伏伽德罗常数(6.022×10^23)个粒子。
2. 浓度计算- 溶液浓度用摩尔浓度(mol/L)表示,通过溶质的摩尔数除以溶液体积计算。
3. 质量守恒- 化学反应中,通过质量守恒定律计算反应物和生成物的质量关系。
4. 能量变化- 化学反应伴随能量变化,通过热化学方程式计算反应的热效应。
四、溶液与酸碱1. 溶液的分类- 根据溶质和溶剂的状态,溶液分为气态溶液、液态溶液和固态溶液。
2. 酸碱理论- 酸碱指示剂、pH值、缓冲溶液等概念,以及布朗斯特-劳里酸碱理论。
高二化学知识点归纳总结

2022高二化学知识点归纳总结高二化学知识点归纳总结1、亲电取代反应芳香烃图册主要包含五个方面:卤代:与卤素及铁粉或相应的三卤化铁存在的条件下,可以发生苯环上的H被取代的反应。
卤素的反应活性为:FClBrI不同的苯的衍生物发生的活性是:烷基苯苯苯环上有吸电子基的衍生物。
烷基苯发生卤代的时候,如果是上述催化剂,可发生苯环上H取代的反应;如在光照条件下,可发生侧链上的H被取代的反应。
应用:鉴别。
(溴水或溴的四氯化碳溶液)如:鉴别:苯、己烷、苯乙烯。
(答案:step1:溴水;step2:溴水、Fe粉)。
硝化:与浓硫酸及浓硝酸(混酸)存在的条件下,在水浴温度为55摄氏度至60摄氏度范围内,可向苯环上引入硝基,生成硝基苯。
不同化合物发生硝化的速度同上。
磺化:与浓硫酸发生的反应,可向苯环引入磺酸基。
该反应是个可逆的反应。
在酸性水溶液中,磺酸基可脱离,故可用于基团的保护。
烷基苯的磺化产物随温度变化:高温时主要得到对位的产物,低温时主要得到邻位的产物。
F-C烷基化:条件是无水AlX3等Lewis酸存在的情况下,苯及衍生物可与RX、烯烃、醇发生烷基化反应,向苯环中引入烷基。
这是个可逆反应,常生成多元取代物,并且在反应的过程中会发生C正离子的重排,常常得不到需要的产物。
该反应当苯环上连接有吸电子基团时不能进行。
如:由苯合成甲苯、乙苯、异丙苯。
F-C酰基化:条件同上。
苯及衍生物可与RCOX、酸酐等发生反应,将RCO-基团引入苯环上。
此反应不会重排,但苯环上连接有吸电子基团时也不能发生。
如:苯合成正丙苯、苯乙酮。
亲电取代反应活性小结:连接给电子基的苯取代物反应速度大于苯,且连接的给电子基越多,活性越大;相反,连接吸电子基的苯取代物反应速度小于苯,且连接的吸电子基越多,活性越小。
2、加成反应与H2:在催化剂Pt、Pd、Ni等存在条件下,可与氢气发生加成反应,最终生成环己烷。
与Cl2:在光照条件下,可发生自由基加成反应,最终生成六六六。
2023高中化学必修一必背知识点梳理

2023高中化学必修一必背知识点梳理高中化学需要大家掌握的知识点非常多,因此学会归纳总结有利于提高复习效率。
为了方便大家学习借鉴,下面小编精心准备了高中化学必修一必背知识点梳理内容,欢迎使用学习!高中化学必修一必背知识点梳理一、概念判断:1、氧化还原反应的实质:有电子的转移(得失)2、氧化还原反应的特征:有化合价的.升降(判断是否氧化还原反应)3、氧化剂具有氧化性(得电子的能力),在氧化还原反应中得电子,发生还原反应,被还原,生成还原产物。
4、还原剂具有还原性(失电子的能力),在氧化还原反应中失电子,发生氧化反应,被氧化,生成氧化产物。
5、氧化剂的氧化性强弱与得电子的难易有关,与得电子的多少无关。
6、还原剂的还原性强弱与失电子的难易有关,与失电子的多少无关。
7、元素由化合态变游离态,可能被氧化(由阳离子变单质),也可能被还原(由阴离子变单质)。
8、元素价态有氧化性,但不一定有强氧化性;元素态有还原性,但不一定有强还原性;阳离子不一定只有氧化性(不一定是价态,,如:Fe2+),阴离子不一定只有还原性(不一定是态,如:SO32-)。
9、常见的氧化剂和还原剂:10、氧化还原反应与四大反应类型的关系:【同步练习题】1.Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。
S2O32-和Cl2反应的产物之一为SO42-。
下列说法不正确的是()A.该反应中还原剂是S2O32-B.H2O参与该反应,且作氧化剂C.根据该反应可判断氧化性:Cl2 SO42-D.上述反应中,每生成lmolSO42-,可脱去2molCl2答案:B点拨:该反应方程式为:S2O32-+4Cl2+5H2O===2SO42-+8Cl-+10H+,该反应中氧化剂是Cl2,还原剂是S2O32-,H2O参与反应,但既不是氧化剂也不是还原剂,故选B。
2.(2023河南开封高三一模)分析如下残缺的反应:RO3-+________+6H+===3R2↑+3H2O。
2023化学衡水中学一本通

目录专题01物质的组成、性质和分类3专题02物质的量及其化学计算27专题03离子反应方程式和离子共存42专题04氧化还原反应及其应用57专题05化学反应中的能量变化76专题06化学能与电能的转化90专题07化学反应速率和化学平衡103专题08水溶液中的离子平衡129专题09元素周期律与元素周期表152专题10元素及其化合物167专题11工艺流程题189专题12常见有机化合物212专题13化学实验基础227专题14综合实验探究251专题15有机化学基础286专题16物质结构与性质317专题01物质的组成、性质和分类【考情探究】课标解读内容物质的组成、性质和分类分散系解读1.理解混合物和纯净物、单质、化合物概念;2.理解酸、碱、盐、氧化物的概念及其相互联系;3.理解物理变化与化学变化的区别与联系。
1.了解溶液的含义。
了解溶解度、饱和溶液的概念。
理解溶液中溶质的质量分数的概念,并能进行有关计算;2.了解胶体是一种常见的分散系。
考情分析物质的组成、性质和分类多结合生产、生活实际及传统文化内容以选择题的形式进行考查。
预计化学与STSE、中华民族传统文化依旧是命题热点。
备考策略2022年高考备考关注物质的组成、性质和分类。
熟记常见物质的性质及用途,多关注化学与环境、化学与能源、化学与生命科学、化学与材料。
【高频考点】高频考点一物质的分类1.依据标准对物质进行分类2.识记常见混合物的成分与俗名(1)水煤气:主要成分是CO、H2。
(2)天然气(沼气):主要成分是CH4。
(3)液化石油气:以C3H8、C4H10为主。
(4)裂解气:以乙烯、丙烯、甲烷为主。
(5)水玻璃:Na2SiO3的水溶液。
(6)王水:浓盐酸与浓硝酸的混合物(体积比3∶1)。
(7)波尔多液:主要成分是CuSO4和Ca(OH)2。
(8)肥皂:主要成分是高级脂肪酸钠。
(9)碱石灰:NaOH和CaO的混合物。
(10)铝热剂:铝粉和高熔点的金属氧化物的混合物。
万唯高考化学知识点

万唯高考化学知识点高考化学是中学生必须面对的一门重要科目。
无论是理科生还是文科生,都需要掌握一定的化学知识。
下面将为大家介绍一些高考化学的重点知识点,希望能够帮助同学们更好地备考。
一、化学元素与化合物在高考化学中,了解化学元素的基本性质和化合物的组成是非常重要的。
首先,我们需要熟悉周期表上常见元素的化学性质,如金属元素的导电性、非金属元素的化学活性等。
同时,要了解化合物的组成以及其在化学反应中的作用。
二、化学反应与能量变化化学反应是化学学科的核心内容之一。
在高考中,我们需要掌握化学反应的分类及其特点。
例如,酸碱中和反应、氧化还原反应等。
同时,了解反应的能量变化对于理解化学反应过程也非常重要。
反应的放热、吸热性质以及与焓变的关系都是需要掌握的知识点。
三、溶液与饱和度溶液是化学中常见的概念。
在高考中,我们需要了解溶液的组成、溶解度以及饱和度等概念。
饱和度是指在一定温度下溶液中能够溶解的溶质的最大量。
这一概念对于理解溶液的特性及其与溶剂的相互作用有着重要意义。
四、化学平衡与动力学化学平衡是高考中的重要知识点之一。
我们需要了解平衡态的特点,如溶液中的化学平衡、气体平衡等。
动力学则是研究化学反应速率的学科,我们需要掌握化学反应速率与反应条件的关系,如温度、浓度等因素对反应速率的影响。
五、无机化学与有机化学无机化学和有机化学是高考化学中的两个重要分支。
无机化学主要研究无机物质及其反应规律,如硅酸盐、金属氧化物等。
有机化学则研究有机物质的结构、性质及其合成方法。
我们需要掌握一些常见有机物的结构及其反应特点。
通过了解以上知识点,同学们可以更好地备考高考化学。
当然,注意理解与应用的结合也是非常重要的。
化学是一门实践性很强的学科,理论知识与实际应用的结合是成功备考的关键。
希望同学们能够在备考过程中注重基础知识的掌握,加强对实验操作的理解,提高解题能力。
总之,化学是一门综合性较强的学科,在高考中占有重要的分值。
通过掌握化学元素与化合物、化学反应与能量变化、溶液与饱和度、化学平衡与动力学、无机化学与有机化学等知识点,同学们可以更好地备考,取得优异的成绩。
化学步步高练透高一123~124

化学步步高练透高一123~124化学步步高练透高一123~124化学是一门研究物质性质、组成、结构、变化以及与能量之间的关系的学科,被广泛学习和应用于各个领域。
高中化学作为一门基础学科,贯穿整个高中化学课程。
在高一123~124单元,我们将学习有关离子和离子键、金属元素和金属化合物以及有机化学的基本概念和原理。
以下是对这两个单元的详细介绍。
在123单元,我们学习了离子和离子键。
离子是指带电的原子或分子,可以通过失去或获取电子而带正或负电荷。
离子键是指正负两种离子通过电荷引力互相结合形成的化学键。
本单元的学习内容包括:离子的成因、离子的命名和离子键的特点。
我们首先学习了离子的成因。
离子的生成可以通过原子的电子转移形成。
当金属元素失去外层电子时,形成带正电荷的离子,称为阳离子;而当非金属元素获取外层电子时,形成带负电荷的离子,称为阴离子。
离子的生成可以通过电离和电子亲和力的概念进行解释。
接下来,我们学习了离子的命名。
离子的命名可以根据其所含元素及其电荷情况来命名。
对于单负离子,一般以元素名字加上“化”字作为离子的名字;而对于常见的多负离子,一般采用特定命名规则进行命名。
学习离子的命名有助于我们更好地理解化学式及离子的组成。
最后,我们学习了离子键的特点。
离子键的特点主要表现在:离子键的结构稳定性较高、离子键通常在晶体中存在、离子键在物理性质上具有一定特点等。
了解离子键的特点有助于我们理解化合物结构和性质。
在124单元,我们学习了金属元素和金属化合物。
金属是指一类具有特殊性质和结构的元素,在自然界中广泛存在,并且在人类生活和工业中发挥着重要作用。
本单元的学习内容包括:金属元素的性质、金属的化合物和金属的应用。
我们首先学习了金属元素的性质。
金属元素具有一系列特殊的性质,如导电性、导热性、延展性和塑性等。
这些性质是由金属的结构和金属键的特点所决定的,有助于解释金属的各种特点和应用。
接下来,我们学习了金属的化合物。
2023高中化学必背基础知识点归纳大全

2023高中化学必背基础知识点归纳大全高中化学必背的基础知识归纳1高一化学知识重点离子反应一、电解质和非电解质电解质:在水溶液里或熔融状态下能导电的化合物。
1、化合物非电解质:在水溶液中和熔融状态下都不能导电的化合物。
(如:酒精[乙醇]、蔗糖、SO2、S03、NH3、CO2等是非电解质。
)(1)电解质和非电解质都是化合物,单质和混合物既不是电解质也不是非电解质。
(2)酸、碱、盐和水都是电解质(特殊:盐酸(混合物)电解质溶液)。
(3)能导电的物质不一定是电解质。
能导电的物质:电解质溶液、熔融的碱和盐、金属单质和石墨。
电解质需在水溶液里或熔融状态下才能导电。
固态电解质(如:NaCl晶体)不导电,液态酸(如:液态HC1)不导电。
2、溶液能够导电的原因:有能够自由移动的离子。
3、电离方程式:要注意配平,原子个数守恒,电荷数守恒。
如: A12(S04)3=2A13++3SO42-二、离子反应:1、离子反应发生的条件:生成沉淀、生成气体、水。
2、离子方程式的书写:(写、拆、删、查)①写:写出正确的化学方程式。
(要注意配平。
)②拆:把易溶的强电解质(易容的盐、强酸、强碱)写成离子形式。
常见易溶的强电解质有:三大强酸(H2S04、HC1、HN03),四大强碱[NaOH、KOH、Ba(OH)2. Ca(OH)2(澄清石灰水拆,石灰乳不拆)],可溶性盐,这些物质拆成离子形式,其他物质一律保留化学式。
③删:删除不参加反应的离子(价态不变和存在形式不变的离子)。
④查:检查书写离子方程式等式两边是否原子个数守恒、电荷数守恒。
3、离子方程式正误判断:(看几看)①看是否符合反应事实(能不能发生反应,反应物、生成物对不对)。
②看是否可拆。
③看是否配平(原子个数守恒,电荷数守恒)。
④看“/"""I”是否应用恰当。
4、离子共存问题(1)由于发生复分解反应(生成沉淀或气体或水)的离子不能大量共存。
生成沉淀:AgCl、BaS04、BaSO3、BaCO3、CaCO3、Mg(OH)2、Cu(OH)2等。
辽宁高中化学知识点总结

辽宁高中化学知识点总结一、基本概念与原理1. 物质的组成与分类- 物质由元素组成,分为纯净物和混合物。
- 纯净物包括单质和化合物,单质是由同种元素组成的纯净物,化合物是由不同种元素组成的纯净物。
2. 原子结构- 原子由原子核和核外电子组成。
- 原子核包含质子和中子,质子带正电,中子不带电。
- 电子带负电,围绕原子核运动。
3. 元素周期律- 元素的性质随着原子序数的增加而呈现周期性变化。
- 元素周期表是按照原子序数排列的元素表,分为7个周期和18个族。
4. 化学键- 化学键是原子之间的相互作用力,包括离子键、共价键和金属键。
- 离子键是由电荷相反的离子间的静电作用形成的。
- 共价键是由原子间共享电子对形成的。
- 金属键是金属原子间的电子共享形成的。
5. 化学反应- 化学反应是原子重新排列形成新物质的过程。
- 化学反应遵循质量守恒定律,即反应前后物质的总质量不变。
二、无机化学1. 氧化还原反应- 氧化还原反应是电子转移的反应,包括氧化和还原两个过程。
- 氧化是失去电子的过程,还原是获得电子的过程。
2. 酸碱反应- 酸碱反应是酸和碱反应生成盐和水的反应。
- 酸是能够提供质子的物质,碱是能够接受质子的物质。
3. 沉淀反应- 沉淀反应是两种溶液混合时形成不溶于水的固体(沉淀)的反应。
4. 配位化学- 配位化学研究的是中心离子与配体之间形成的配合物。
- 配体是能够通过孤对电子与中心离子形成配位键的分子或离子。
三、有机化学1. 有机化合物的分类- 有机化合物主要分为烃、醇、酚、醛、酮、羧酸、酯、胺等。
- 烃是只含有碳和氢的有机化合物。
2. 有机反应类型- 取代反应:一个原子或基团被另一个原子或基团取代。
- 加成反应:不饱和化合物与另一个分子结合形成新的化合物。
- 消除反应:分子中的一个或多个原子或基团脱离,形成不饱和化合物。
- 重排反应:分子内部的原子或基团重新排列。
3. 有机化学中的立体化学- 立体化学研究的是分子的空间结构和构型。
高三化学复习知识清单(通用版) 知识清单15 化学反应速率和限度
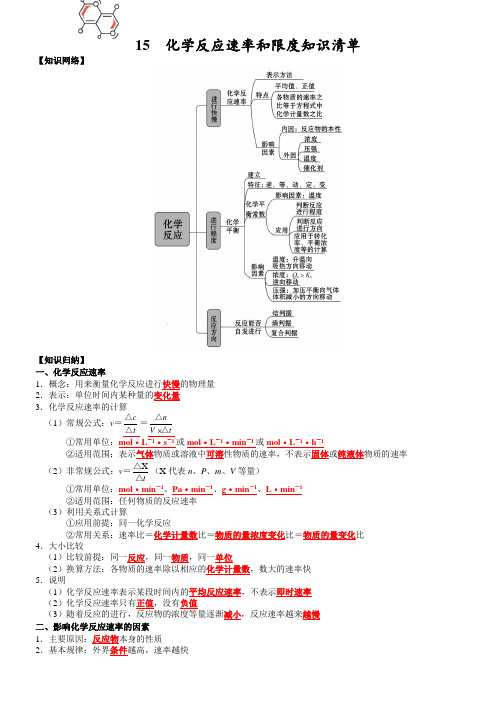
15 化学反应速率和限度知识清单【知识网络】【知识归纳】一、化学反应速率1.概念:用来衡量化学反应进行快慢的物理量 2.表示:单位时间内某种量的变化量 3.化学反应速率的计算(1)常规公式:v =t c △△=tV n△△①常用单位:mol ·L -1·s -1或mol ·L -1·min -1或mol ·L -1·h -1②适用范围:表示气体物质或溶液中可溶性物质的速率,不表示固体或纯液体物质的速率(2)非常规公式:v =t△△X(X 代表n 、P 、m 、V 等量)①常用单位:mol ·min -1、Pa ·min -1、g ·min -1、L ·min -1 ②适用范围:任何物质的反应速率 (3)利用关系式计算①应用前提:同一化学反应②常用关系:速率比=化学计量数比=物质的量浓度变化比=物质的量变化比4.大小比较(1)比较前提:同一反应,同一物质,同一单位(2)换算方法:各物质的速率除以相应的化学计量数,数大的速率快 5.说明(1)化学反应速率表示某段时间内的平均反应速率,不表示即时速率 (2)化学反应速率只有正值,没有负值(3)随着反应的进行,反应物的浓度等量逐渐减小,反应速率越来越慢 二、影响化学反应速率的因素 1.主要原因:反应物本身的性质2.基本规律:外界条件越高,速率越快(1)温度:温度越高,化学反应速率越快(2)压强:气体反应的压强越大,化学反应速率越快(3)浓度:浓度越大,化学反应速率越快(4)催化剂:显著的改变(加快或减慢)正逆反应速率,一般有催化剂,化学反应速率越快(5)接触面积:反应物的颗粒越小,接触面积越大,化学反应速率越快(6)原电池:形成原电池,可以加快氧化还原反应的速率3.特殊情况(1)温度①催化反应,升高温度,催化剂可能失活,反应速率减慢②有机反应,升高温度,有可能发生副反应,主反应速率减慢(2)压强①改变非气体反应的压强,反应速率不变②改变等体反应的压强,v正和v逆变化幅度相同(3)浓度①固体和纯液体的浓度为定值,改变固体或纯液体的用量,反应速率不变②加入固体物质,有可能改变接触面积,反应速率可能加快(4)无关气体①恒容容器通无关气体,压强增大,浓度不变,速率不变②恒压容器通无关气体,体积变大,浓度减小,速率减慢4.活化分子、有效碰撞与反应速率的关系实质5.速率-时间图像(1)温度:升高温度,瞬间v正和v逆均增大或(2)压强:增大压强,气体物质的浓度均增大,瞬间v正和v逆均增大或(3)浓度①增大反应物浓度,瞬间v正增大,v逆不变②增大生成物浓度,瞬间v正不变,v逆增大或③恒压:增大反应物浓度,瞬间v正增大,v逆减慢④恒压:增大生成物浓度,瞬间v正减慢,v逆增大(4)催化剂:能够同等程度改变正逆反应速率6.全程速率-时间图像(1)OB段反应速率变化的可能原因为:①反应放热,使温度升高,反应速率加快②反应生成催化剂,反应速率加快(2)BC段反应速率变化的可能原因为:反应物浓度降低,反应速率减慢7.探究外界条件对化学反应速率的影响(1)方法:控制变量法(2)溶液反应:加水调节溶液的总体积不变,以保证某种成分的浓度不变(3)实例:探究Y溶液浓度对反应速率的影响实验(混合溶液) 1 2 3 4 5 64mol/LX溶液/mL 60 60 60 60 60 60饱和Y溶液/mL 0 1.0 5.0 10 2040H2O/mL 4039353020 0 8.速率方程(1)意义:表示反应物浓度与反应速率的定量关系(2)举例:A2(g)+B2(g)2AB(g),v=kcα(A2)·cβ(B2)(3)测定方法:α、β必须通过实验测定,无法直接写出。
高考化学知识点归纳总结2024

高考化学知识点归纳总结2024高考化学知识点归纳总结(人教版2024)一、化学基本概念。
1. 物质的组成与分类。
- 元素:具有相同核电荷数(质子数)的一类原子的总称。
例如,碳元素包含^12C、^13C、^14C等不同的原子。
- 混合物与纯净物:混合物由多种物质组成,没有固定的组成和性质,如空气(含氮气、氧气、二氧化碳等);纯净物由一种物质组成,有固定的组成和性质,如蒸馏水。
- 单质与化合物:单质是由同种元素组成的纯净物,如氧气O_2;化合物是由不同种元素组成的纯净物,如二氧化碳CO_2。
- 酸、碱、盐、氧化物:- 酸:在水溶液中电离出的阳离子全部为H^+的化合物,如HCl、H_2SO_4。
- 碱:在水溶液中电离出的阴离子全部为OH^-的化合物,如NaOH、Ca(OH)_2。
- 盐:由金属离子(或铵根离子)和酸根离子组成的化合物,如NaCl、Na_2CO_3。
- 氧化物:由两种元素组成,其中一种元素为氧元素的化合物,如CO、MgO。
2. 化学用语。
- 元素符号:表示元素的符号,如H表示氢元素。
- 化学式:用元素符号表示物质组成的式子。
例如,H_2O表示水的组成。
- 化学方程式:用化学式表示化学反应的式子。
如2H_2 +O_2{点燃}{===}2H_2O,表示氢气和氧气反应生成水。
- 离子符号:表示离子的符号,如Na^+表示钠离子,Cl^-表示氯离子。
3. 化学中的计量关系。
- 物质的量(n):是国际单位制中七个基本物理量之一,单位为摩尔(mol)。
- 阿伏伽德罗常数(N_A):1mol任何粒子的粒子数,约为6.02×10^23mol^-1。
- 摩尔质量(M):单位物质的量的物质所具有的质量,单位为g/mol。
例如,H_2O的摩尔质量为18g/mol。
- 气体摩尔体积(V_m):在标准状况(0^∘C,101kPa)下,1mol任何气体所占的体积约为22.4L,即V_m = 22.4L/mol。
2023-2024学年高一上学期化学人教版(2019)必修第一册知识点总结

高一上学期化学必修第一册知识点总结第一章化学物质及其变化一、物质的分类(1)同素异形体;由同一种元素形成几种性质不同的单质Eg:①O2,O3;②金刚石,石墨,C60;③红磷P和白磷P4注意:由同一种元素组成的物质不一定是单质,还可能是几种同素异形体Eg:①O2和O3的混合物(2)分类方法:①树状分类法:按统一标准(采用树状形式)对同类事物进行再分类的方法。
特征:同一层次的物质类别间一般相互独立,没有交叉。
②交叉分类法:根据多种不同分类标准对同一事物进行分类的方法。
特征:物质类别间有交叉的部分。
1、分散系(1)定义:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系,叫分散系。
被分散的物质称作分散质(可以是气体、液体、固体),容纳分散质作用的物质称作分散剂(可以是气体、液体、固体)。
(2)区别***:分散质粒子的大小是胶体区别于溶液、浊液的本质特征。
(3)溶液、胶体、浊液三种分散系的比较***:分散质粒子大小/nm 外观特征能否通过滤纸能否通过半透膜有否丁达尔效应实例溶液小于1nm均匀、透明、稳定能能没有NaCl 、蔗糖溶液胶体在1—100nm之间均匀、有的透明、较稳定能不能有Fe(OH)3胶体浊液大于100nm 不均匀、不透明、不稳定不能不能没有泥水胶体的性质*****:丁达尔效应*,聚沉*,电泳*,渗析*,介稳性。
丁达尔效应**:可见光通过胶体时,可看到一条“光的通路”,是由于胶体粒子对光的散射形成的。
(鉴别胶体和溶液的物理方法)聚沉的三方法***:加热,加入电解质,加入带相反电荷胶粒的胶体。
注意*:胶体不带电,胶体微粒带电(Fe(OH)3胶体微粒带正电)胶体的分类;根据分散剂的状态胶体根据分散质的构成导师指点:1Fe(OH)3胶体粒子是由许多Fe(OH)3小分子聚集所形成的的微粒,其直径为1~100nm,故称为粒子胶体。
2淀粉属于高分子,其单个分子的直径为1~100nm,故称为分子胶体。
高一化学每一章知识点梳理框架图

高一化学每一章知识点梳理框架图化学是一门研究物质的性质、组成和变化的科学,对于高一化学来说,掌握每一章的知识点是建立后续学习基础的关键。
为了帮助同学们更好地理解每一章的内容,我将为大家梳理高一化学每一章的知识点,并提供一个框架图,帮助大家更好地掌握整个科目。
1. 第一章:化学的基本概念这一章主要介绍了化学的基本概念和化学实验的基本操作。
在这个章节中,我们需要了解化学的定义、化学反应和化学方程式的表示方法,以及一些实验室常用的瓶子、玻璃仪器等。
2. 第二章:物质的基本性质这一章重点介绍了物质的基本性质,包括物理性质和化学性质。
在这个章节中,我们需要掌握物质的颜色、硬度、密度等物理性质的定义和计量方法,以及物质的燃烧、氧化和还原等化学性质。
3. 第三章:离子反应和化合价这一章主要介绍了离子反应与离子方程式的表示方法,以及化合价的概念和计算方法。
在这个章节中,我们需要了解离子的定义和离子反应的特点,以及如何根据元素的电子数确定元素的化合价。
4. 第四章:元素的周期性这一章重点介绍了元素周期表的结构和元素周期性的规律。
在这个章节中,我们需要熟悉周期表的排列方式,了解周期表中各个元素的一些重要信息,如原子序数、相对原子质量等,并掌握元素的周期性趋势,如原子半径、电离能、电负性等。
5. 第五章:化学键和分子结构这一章主要介绍了化学键的形成和分子结构的性质。
在这个章节中,我们需要了解化学键的概念和类型,如离子键、共价键等,以及分子的空间结构和分子极性对物质性质的影响。
6. 第六章:化学反应和化学方程式这一章重点介绍了化学反应和化学方程式的表示方法,以及反应速率和平衡的概念。
在这个章节中,我们需要了解化学反应的条件和类型,如合成反应、分解反应等,以及如何平衡反应方程式和计算反应速率。
7. 第七章:常见化合物的性质和用途这一章主要介绍了常见化合物的性质和用途。
在这个章节中,我们需要了解氧化物、酸、碱和盐的性质和反应,以及它们在日常生活和工业生产中的应用。
2019年高考化学思维导图知识点

2019年高考化学思维导图知识点目录化学基本概念和基本理论元素与化合物有机化学基础化学计算化学实验化学工业知识化学基本概念和基本理论一、物质的分类二、组成原子的粒子间的关系:1、核电荷数(Z)=核内质子数=核外电子数2、质量数(A)=质子数(Z)+中子数(N)三、元素周期律与周期表四、化学键与分子结构五、晶体类型与性质晶体类型性质比较离子晶体分子晶体原子晶体金属晶体结构组成粒子阴、阳离子分子原子金属阳离子和自由电子粒子间作用离子键范德瓦耳斯力共价键金属键物理性质熔沸点较高低很高有高有低硬度硬而脆小大有大有小、有延展性溶解性易溶于极性溶剂,难溶于非极性溶剂极性分子易溶于极性溶剂不溶于任何溶剂难溶(钠等与水反应)导电性晶体不导电;能溶于水的其水溶液导电;熔化导电晶体不导电,溶于水后能电离的,其水溶液可导电;熔化不导电不良(半导体Si)良导体(导电传热)典型实例NaCl、NaOHNa2O、CaCO3干冰、白磷冰、硫磺金刚石、SiO2晶体硅、SiCNa、Mg、AlFe、Cu、Zn六、化学反应类型七、离子反应八、氧化还原反应的有关概念的相互关系九、化学反应中的能量变化十、溶液与胶体十一、化学反应速率十二、化学平衡十三、弱电解质的电离平衡十四、溶液的酸碱性十五、盐类的水解十六、酸碱中和滴定十七、电化学元素与化合物钠及其化合物碱金属氯及其化合物卤素氧族元素硫的重要化合物碳及其化合物硅及其化合物材料氮族元素氮和磷氨硝酸镁和铝铁及其化合物铜及其化合物有机化学基础烃不饱和链烃芳香烃分类通式结构特点化学性质物理性质同分异构烷烃C n H2n+2(n≥1)①C-C单键②链烃①与卤素取代反应(光照)②燃烧③裂化反应一般随分子中碳原子数的增多,沸点升高,液态时密度增大。
气态碳原子数为1~4。
不溶于水,液态烃密度比水的小碳链异构烯烃C n H2n(n≥2)①含一个C≡C键②链烃①与卤素、H:、H2O等发生加成反应②加聚反应③氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构炔烃C n H2n-2(n≥2)①含一个C≡C键②链烃①加成反应②氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构苯及其同系物C n H2n-6(n≥6)①含一个苯环②侧链为烷烃基①取代反应:卤代、硝化、磺化②加成反应③氧化反应:燃烧,苯的同系物能被KMnO4酸性溶液氧化简单的同系物常温下为液态;不溶于水,密度比水的小侧链大小及相对位置产生的异构烃的衍生物烃的衍生物结构、通式、化学性质鉴别类别官能团结构特点通式化学性质卤代烃-X(卤素原子)C-X键在一定条件下断裂C n H2n+1O2(饱和一元)(1)NaOH水溶液加热,取代反应(2)NaOH醇溶液加热,消去反应醇-OH(羟基)(1)—OH与烃基直接相连(2)—OH上氢原子活泼C n H2n+2O2(饱和一元)(1)取代:脱水成醚,醇钠,醇与羧酸成酯,卤化成卤代烃(2)氧化成醛(—CH2OH)(3)消去成烯醛(1)醛基上有碳氧双键(2)醛基只能连在烃基链端C n H2n O2(饱和一元)(1)加成:加H2成醇(2)氧化:成羧酸羧(1)—COOH可电离出H+(2)—COOH难加成C n H2n O(饱和一元)(1)酸性:具有酸的通性(2)酯化:可看作取代酯,R 必须是烃基C n H2n O2(饱和一元)水解成醇和羧酸酚(1)羟基与苯环直接相连(2)—OH上的H比醇活泼(3)苯环上的H比苯活泼(1)易取代:与溴水生成2,4,6-三溴苯酚(2)显酸性(3)显色:遇Fe3+变紫色代表物质转化关系糖类类别葡萄糖蔗糖淀粉纤维素分子式(C6H12O6)(C12H22O11)(C6H10O5)(C6H10O5)结构特点多羟基醛分子中无醛基,非还原性糖由几百到几千个葡萄糖单元构成的天然高分子化合物由几千个葡萄糖单元构成的天然高分子化合物主要性质白色晶体,溶于水有甜味。
【高中化学】2017年短平快高考考点突破一本通之16 物质结构(选修)考点二 原子结构与元素性质 Word版含解析
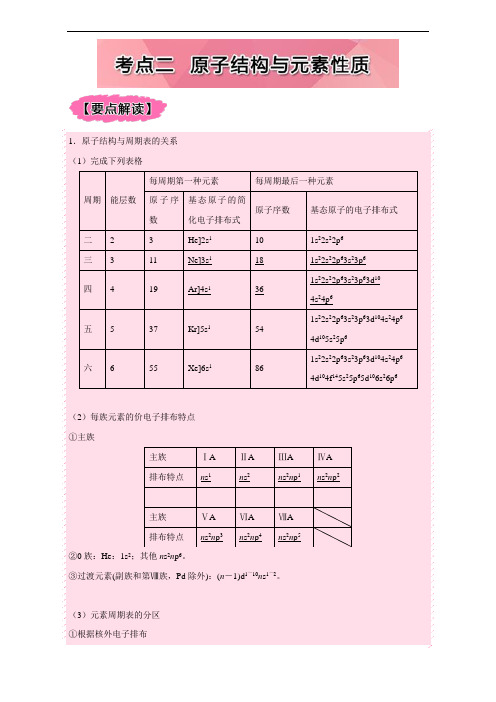
.各区元素化学性质及原子最外层电子排布特点元素分布 外围电子排布 元素性质特点A 族 n s1~2除氢外都是活泼金属元素;常是最外层电子参与反应即“价电子层”,对于主族元素,价电子层就是最外电子层,而对于过渡元素原子不仅仅是最外电子层,如Fe的价电子层排布为3d64s2。
某些主族元素与右下方的主族元素的有些。
3.元素周期律【重难点指数】★★★【重难点考向一】元素推断与元素逐级电离能【典型例题1】根据下列五种元素的第一至第四电离能数据(单位:kJ·mo1-1),回答下列各题:(1)在周期表中,最可能处于同一族的是________。
A.Q和R B.S和T C.T和U D.R和T E.R和U(2)下列离子的氧化性最弱的是________。
A.S2+B.R2+C.T3+D.U+(3)下列元素中,化学性质和物理性质最像Q元素的是________。
A.硼B.铍C.氦D.氢(4)每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明:________________________________,如果U元素是短周期元素,你估计它的第2次电离能飞跃数据将发生在失去第________个电子时。
(5)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是________________,其中________元素的第一电离能异常高的原因是________________________________________。
【答案】(1)E(2)D(3)C(4)电子分层排布,各能层能量不同10(5)R<S<T S S元素的最外层电子处于s能级全充满状态,能量较低,比较稳定,失去第一个电子吸收的能量较多【解析】(1)根据电离能的变化趋势知,Q为稀有气体元素,R为第ⅠA族元素,S为第ⅡA 族元素,T为第ⅢA族元素,U为第ⅠA族元素,所以R和U处于同一主族。
(2)由于U+为第ⅠA族元素且比R电离能小,所以U+的氧化性最弱。
高二化学选择性必修一知识点总结笔记

高二化学选择性必修一知识点总结笔记(实用版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如教案大全、书信范文、述职报告、合同范本、工作总结、演讲稿、心得体会、作文大全、工作计划、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of practical materials for everyone, such as lesson plans, letter templates, job reports, contract templates, work summaries, speeches, reflections, essay summaries, work plans, and other materials. If you want to learn about different data formats and writing methods, please stay tuned!高二化学选择性必修一知识点总结笔记本店铺整理的《高二化学选择性必修一知识点总结笔记》希望能够帮助到大家。
全国高中化学方程式一本通.DOC

高考总复习之高中化学方程式总结 化学 第一册第一章 卤素第一节 氯气1、NaCl 2Cl Na 22−−→−+点燃2、22CuCl Cl Cu −−→−+点燃3、32FeCl 2Cl 3Fe 2−−→−+点燃4、HCl 2Cl H 22−−−−→−+点燃(光照)5、32PCl 2Cl 3P 2−−→−+点燃6、523PCl Cl PCl →+7、HClO HCl O H Cl 22+→+8、O H 2CaCl ClO Ca Cl 2OH Ca 222222++→+)()(9、HClO 2CaCO O H CO ClO Ca 3222+↓→++)(10、O H NaCl NaClO Cl NaOH 222++→+11、↑++−→−+∆2222Cl O H 2MnCl MnO HCl 412、O H 8Cl 5KCl 2MnCl 2HCl 16KMnO 22224+↑++→+(浓) 13、2O HCl 2HClO 2+−−→−见光第二节 氯化氢14、↑+→+HCl NaHS O S O H NaCl 442(浓) 15、↑+−→−+∆HCl S O Na NaCl NaHS O 42416、↑+−→−+∆HCl 2S O Na S O H NaCl 24242(浓)(14、15结合) 17、33HNO AgCl AgNO HCl +↓→+18、33NaNO AgCl AgNO NaCl +↓→+19、33KNO AgCl AgNO KCl +↓→+20、↑++→+2223CO O H CaCl CaCO HCl 2第三节 氧化还原反应21、O H Cu H CuO 22+−→−+∆22、O H 2NO 4CO HNO 4C 2223+↑+↑→+23、O H 3NO NH NO Zn 4HNO 10Zn 4234233++−→−+∆)((极稀) 24、4243324S O H 15PO H 6P Cu 5O H 24CuS O 15P 11++→++ 25、O H 3KCl Cl 3HCl 6KClO 223+↑→+(浓)26、O H 3NO NH NO Mg 4HNO 10Mg 4234233++−→−+∆)((极稀) 27、O H 31S O K S O Fe 9S O Cr S O H 31O Fe 6O Cr K 2423423424243722+++→++)()( 28、↑+↑+→++2223CO 3N S K S C 3KNO 2第四节 卤族元素29、HF 2F H 22→+30、HBr 2Br H 22→+31、HI 2I H 22→+32、22Br NaCl 2Cl NaBr 2+→+33、22I KCl 2Cl KI 2+→+34、22I KBr 2Br KI 2+→+35、33NaNO AgBr AgNO NaBr +↓→+36、33KNO AgI AgNO KI +↓→+37、2Br Ag 2AgBr 2+−−→−光照 第二章 摩尔 反应热第一节 摩尔38、22CO O C →+39、↑+→+22H MgCl HCl 2Mg第二节 气体摩尔体积40、22H ZnCl HCl 2Zn +→+第三节 物质的量浓度41、O H 2SO Na SO H NaOH 224242+→+第四节 反应热42、kJ 5.393CO O C 22+−−→−+(气)(气)(固)点燃 43、kJ 6.483O H 2O H 2222+→+(气)(气)(气) 44、kJ 6.571O H 2O H 2222+→+(液)(气)(气) 45、kJ 3.131H CO O H C 22-+−→−+∆(气)(气)(气)(固) 第三章 硫 硫酸第一节 硫46、S Cu S Cu 22−→−+∆47、FeS S Fe −→−+∆48、S H H S 22−→−+∆49、2CS C S −−→−+高温50、22S O O S −−→−+点燃51、O H 3S O K S K 2KOH 6S 32422++−→−+∆第二节 硫的氢化物和氧化物52、↓+−→−∆S H S H 2253、2222S O 2O H 2(O 3S H 2+−−→−+点燃足)54、↓+−−→−+S 2O H 2(O S H 2222点燃不足)55、↓+−−→−+S 3O H 2S O S H 2222点燃56、HBr 2S Br S H 22+↓→+57、↑+→+S H FeCl HCl 2FeS 2258、4224S O H CuS S H CuS O +↓→+59、HAc 2PbS S H PbAc 22+↓→+60、O H NaHS NaOH S H 22+→+61、O H S Na NaOH NaHS 22+→+62、O H 2S Na NaOH 2S H 222+→+(60、61结合) 63、HCl 2FeCl 2S FeCl 2S H 232++↓→+64、↑+→+S H FeS O FeS S O H 2442(稀) 65、3222S O H O H S O ⇔+66、3OV 22SO 2O SO 252∆−−→←+ 67、4223S O H O H S O →+68、↑++→+22424232S O O H S O Na S O H S O Na69、O H S O Na NaOH 2S O 2322+→+70、32CaSO CaO SO →+71、O H CaSO OH Ca 2S O 2322+↓→+)( 72、23232HS O Ca O H CaS O S O )(→++73、O H 2S 3S H 2S O 222+↓→+74、42222SO H HCl 2O H 2Cl SO +→++75、42222SO H HBr 2O H 2Br SO +→++76、42424422SO H 2SO K MnSO KMnO 2O H 2SO 5++→++第三节 硫酸的工业制法77、↑+−−→−+23222S O 8O Fe 2O 11FeS 4高温78、3OV 22SO 2O SO 252∆−−→←+79、4232S O H S O O H →+第四节 硫酸 硫酸盐80、O H 2S O 2CO S O H 2C 22242+↑+↑−→−+∆(浓) 81、O H 2S O 3S O H 2S 2242+↑−→−+∆(浓) 82、O H 2S O PO H S O H P 224342+↑+−→−+∆(浓) 83、O H 2S O S S O H S H 22422++−→−+∆(浓) 84、O H 2S O CuS O S O H 2Cu 22442+↑+−→−+∆(浓) 85、HCl 2BaS O S O H BaCl 4422+↓→+86、NaCl 2BaS O S O Na BaCl 4422+↓→+87、NaCl 2BaCO CO Na BaCl 3322+↓→+88、↑++→+2223CO O H BaCl HCl 2BaCO89、↑++→+222333CO O H NO Ba HNO 2BaCO )( 90、↑++→+2223232CO O H S Na S O H CO Na91、42232S O H 2O S O H 2→+92、42232S O Na 2O S O Na 2→+93、423CaSO 2O CaSO 2→+94、O H 6SO 3S O Fe S O H 6Fe 22234242+↑+−→−+∆)((浓) 95、O H S O Na S O Br S O H 2NaBr 22422242++↑+−→−+∆(浓) 96、↑+−→−+∆HCl 2S O Na S O H NaCl 24242(浓) 97、O H 11C 12O H C 2SOH 11221142+−−−→−浓 第四章 碱金属第一节 钠98、O Na 2O Na 422→+99、222O Na O Na 2→+2101、S Na S Na 22−−→−+研磨102、↑+→+22H NaOH 2O H 2Na 2103、↑++→++242242H SO Na OH Cu CuS O O H 2Na 2)( 第二节 钠的氧化物104、NaOH 2O H O Na 22→+105、↑+→+2222O NaOH 4O H 2O Na 2106、3222CO Na CO O Na →+107、232222O CO Na 2CO 2O Na 2+→+108、O H NaCl 2HCl 2O Na 22+→+109、↑++→+2222O O H 2NaCl 4HCl 4O Na110、O H CO NaCl 2HCl 2CO Na 2232+↑+→+111、O H CO NaCl HCl NaHCO 223+↑+→+112、O H CO CO Na NaHCO 222323+↑+−→−∆113、O H CO Na NaOH NaHCO 2323+−→−+∆114、O H 2CO Na CaCO OH Ca NaHCO 2232323++↓→+(少量))( 115、O H NaOH CaCO OH Ca NaHCO 2323++↓→+(足量))( 116、NaCl 2BaCO BaCl CO Na 3232+↓→+117、NaCl 2CaCO CaCl CO Na 3232+↓→+118、O H 2CO 2CaCl HCl 2HCO Ca 22223+↑+→+)( 119、O H 2CO Na CaCO NaOH 2HCO Ca 232323++↓→+)( 120、O H S O NaCl HCl NaHS O 223+↑+→+第三节 碱金属元素22122、22KO O K −−→−+点燃123、MX 2X M 22→+(M 表示氧族元素,X 代表卤族元素) 124、MH 2H M 22→+125、↑+→+22H MOH 2O H 2M 2第五章 物质结构 元素周期律本章内容、性质特殊,所有化学反应方程式均融在其他章节中。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2010届高中化学考点知识网络梳理化学基本概念和基本理论元素与化合物有机化学基础化学计算化学实验化学工业知识化学基本概念和基本理论物质的分类组成原子的粒子间的关系核电荷数(Z)=核内质子数=核外电子数质量数(A)=质子数(Z)+中子数(N)元素周期律与周期表化学键与分子结构晶体类型与性质晶体类型性质比较离子晶体分子晶体原子晶体金属晶体结构组成粒子阴、阳离子分子原子金属阳离子和自由电子粒子间作用离子键范德瓦耳斯力共价键金属键物理性质熔沸点较高低很高有高有低硬度硬而脆小大有大有小、有延展性溶解性易溶于极性溶剂,难溶于非极性溶剂极性分子易溶于极性溶剂不溶于任何溶剂难溶(钠等与水反应)导电性晶体不导电;能溶于水的其水溶液导电;熔化导电晶体不导电,溶于水后能电离的,其水溶液可导电;熔化不导电不良(半导体Si)良导体(导电传热)典型实例NaCl、NaOHNa2O、CaCO3干冰、白磷冰、硫磺金刚石、SiO2晶体硅、SiCNa、Mg、AlFe、Cu、Zn化学反应类型离子反应氧化还原反应的有关概念的相互关系化学反应中的能量变化溶液与胶体化学反应速率化学平衡弱电解质的电离平衡溶液的酸碱性盐类的水解酸碱中和滴定电化学返回页顶元素与化合物钠及其化合物碱金属氯及其化合物卤素氧族元素硫的重要化合物碳及其化合物硅及其化合物材料氮族元素氮和磷氨硝酸镁和铝铁及其化合物铜及其化合物返回页顶有机化学基础烃不饱和链烃芳香烃分类通式结构特点化学性质物理性质同分异构烷烃C n H2n+2(n≥1)①C-C单键②链烃①与卤素取代反应(光照)②燃烧③裂化反应一般随分子中碳原子数的增多,沸点升高,液态时密度增大。
气态碳原子数为1~4。
不溶于水,液态烃密度比水的小碳链异构烯烃C n H2n(n≥2)①含一个C≡C键②链烃①与卤素、H:、H2O等发生加成反应②加聚反应③氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构炔烃C n H2n-2(n≥2)①含一个C≡C键②链烃①加成反应②氧化反应:燃烧,被KMnO4酸性溶液氧化碳链异构位置异构苯及其同系物C n H2n-6(n≥6)①含一个苯环②侧链为烷烃基①取代反应:卤代、硝化、磺化②加成反应③氧化反应:燃烧,苯的同系物能被KMnO4酸性溶液氧化简单的同系物常温下为液态;不溶于水,密度比水的小侧链大小及相对位置产生的异构烃的衍生物烃的衍生物结构、通式、化学性质鉴别类别官能团结构特点通式化学性质卤代烃-X(卤素原子)C-X键在一定条件下断裂C n H2n+1O2(饱和一元)(1)NaOH水溶液加热,取代反应(2)NaOH醇溶液加热,消去反应醇-OH(羟基)(1)—OH与烃基直接相连(2)—OH上氢原子活泼C n H2n+2O2(饱和一元)(1)取代:脱水成醚,醇钠,醇与羧酸成酯,卤化成卤代烃(2)氧化成醛(—CH2OH)(3)消去成烯醛(1)醛基上有碳氧双键(2)醛基只能连在烃基链端C n H2n O2(饱和一元)(1)加成:加H2成醇(2)氧化:成羧酸羧(1)—COOH可电离出H+(2)—COOH难加成C n H2n O(饱和一元)(1)酸性:具有酸的通性(2)酯化:可看作取代酯,R 必须是烃基C n H2n O2(饱和一元)水解成醇和羧酸酚(1)羟基与苯环直接相连(2)—OH上的H比醇活泼(3)苯环上的H比苯活泼(1)易取代:与溴水生成2,4,6-三溴苯酚(2)显酸性(3)显色:遇Fe3+变紫色代表物质转化关系糖类类别葡萄糖蔗糖淀粉纤维素分子式(C6H12O6)(C12H22O11)(C6H10O5)(C6H10O5)结构特点多羟基醛分子中无醛基,非还原性糖由几百到几千个葡萄糖单元构成的天然高分子化合物由几千个葡萄糖单元构成的天然高分子化合物主要性质白色晶体,溶于水有甜味。
既有氧化性,又有还原性,还可发生酯化反应,并能发酵生成乙无色晶体,溶于水有甜味。
无还原性,能水解生成葡萄糖和果糖白色粉末,不溶于冷水,部分溶于热水。
能水解最终生成葡萄糖;遇淀粉变蓝色;无还原性无色无味固体.不溶于水及有机溶剂。
能水解生成葡萄糖.能发生酯化反应,无还原性重要用途营养物质、制糖果、作还原剂食品食品、制葡萄糖、乙醇造纸、制炸药、人造纤维油脂通式物理性质化学性质密度比水小,不溶于水,易溶于汽油、乙醚、苯等多种有机溶剂中。
1.水解:酸性条件碱性条件——皂化反应2.氢化(硬化)蛋白质和氨基酸类别氨基酸蛋白质结构特点分子中既有酸性基(羧基)又有碱性基(氨基),是两性物质由不同的氨基酸相互结合而形成的高分子化合物。
分子中有羧基和氨基,也是两性物质主要性质①既能和酸反应,又能和碱反应②分子间能相互结合而形成高分子化合物①具有两性②在酸或碱或酶作用下水解,最终得多种。
—氨基酸③盐析④变性⑤有些蛋白质遇浓HNO3呈黄色⑥燃烧产生烧焦羽毛的气味⑦蛋白质溶液为胶体合成材料(有机高分子化合物)基本概念基本概念单体结构单元(链节)聚合度高聚物含义能合成高分子化合物的小分子,一般是不饱和的或含有两个或更多官能团的小分子高聚物分子中具有代表性的、重复出现的最小部分每个高分子里链节的重复次数由单体聚合而成的相对分子质量较大的化合物,相对分子质量高达数千至数万以上实例(以聚乙烯为例)CH2=CH2—CH2—CH2—n结构与性质线型高分子体型(网状)高分子结构分子中的原子以共价键相互联结成一条很长的卷曲状态的“链”分子链与分子链之间还有许多共价键交联起来,形成三度空间的网状结构溶解性能缓慢溶解于适当溶剂很难溶解,但往往有一定程度的胀大性能具热塑性,无固定熔点具热固性,受热不熔化特性强度大、可拉丝、吹薄膜、绝缘性好强度大、绝缘性好,有可塑性合成有机高分子化合物的常见反应类型反应类型概念示例加聚反应由相对分子质量小的化合物分子互相结合成相对分子质量大的化合物分子的反应。
均聚反应发生加聚反应的单体只有一种。
共发生加聚反应的单n CH2=CH2+n CH2=CH—CH2聚反应体有两种或多种缩聚反应有两个或两个以上官能团的单体相互结合,生成高分子化合物,同时生成小分子(如H2O、HX、NH3和醇等)。
①以某分子中碳氧双键中的氧原子与另一个基团中的活泼氢原子结合成水而进行的缩聚反应。
+n H2O②以醇羟基中的氢原子和酸分子中的羟基结合成水的方式而进行的缩聚反应。
n HOOC—COOH+n HOCH2CH2OH−−−−→−一定条件下+2n H2O③以羧基中的羟基与氨基中的氢原子结合成H2O的方式而进行的缩聚反应。
n H2O-(CH2)5-NH2+n HOOC-(CH2)6-COOH−−−−→−一定条件下+2H2O返回页顶化学计算物质的量及气体摩尔体积的计算(1)n =A N N n =M m n =mV V n =1molL 22.4-⋅V(标准状况) n =c ·V n =M ρV ω⋅⋅ (2)M =n mm =M ·nV =ρm V m =n V cB =V nB c 1V 1=c 2V 2 (浓溶液稀释)相对原子质量、相对分子质量及确定化学式的计算物质溶解度、溶液浓度的计算pH及有关氢离子浓度、氢氧根离子浓度的计算化学反应方程式的有关计算返回页顶化学实验化学实验基本操作常见气体及其他物质的实验室制备固体+固体·加热固体+液体·不加热固(或液)体+液体·加热图4-1图4-2图4-3常见气体的制备制取气体 反应原理(反应条件、化学方程式) 装置类型 收集方法 注意事项O 2 2KClO 32KCl+3O 2↑或 2KMnO 4K 2MnO 4+MnO 2+O 2↑固体 + 固体·加热 排水法①检查装置气密性。
②装固体的试管口要略向下倾斜。
③先均匀加热,后固定在放药品处加热。
④用排水法收集,停止加热前,应先把导气管撤离水面,才能熄灭酒精灯 NH 3 2NH 4Cl+Ca(OH)2CaCl 2+2NH 3↑+2H 2O 向下 排气法Cl 2 MnO 2+4HCl(浓)MnCl 2+Cl 2↑+2H 2O固 液体 体 + +液 液体 体· 加 热 向上排气法①同上①、③、④条内容。
②液体与液体加热,反应器内应添加碎瓷片以防暴沸。
③氯气有毒,尾气要用碱液吸收。
④制取乙烯温度应控制在170℃左右 NO3Cu+8HNO 3(稀)3Cu(NO 3)2+2NO ↑+4H 2O 排水法 C 2H 4 CH 3CH 2OHCH 2==CH 2↑+H 2OH 2 Zn+H 2SO 4(稀)==ZnSO 4+H 2↑固体 +液体·不加 热 ①检查装置气密性。
②使用长颈漏斗时,要把漏斗颈插入液面以下。
③使用启普发生器时,反应物固体应是块状,且不溶于水(H 2、CO 2、H 2S 可用)。
④制取乙炔要用分液漏斗,以控制反应速率。
⑤H 2S 剧毒,应在通风橱中制备,或用碱液吸收尾气。
不可用浓H 2SO 4向下排 气法或 排水法 C 2H 2 CaC 2+2H 2O →Ca(OH)2+CH ≡CH ↑CO 2 CaCO 3+2HCl==CaCl 2+CO 2↑+H 2O 向上 排气法 NO 2 Cu+4HNO 3(浓)==Cu(NO 3)2+ 2NO 2↑+2H 2O H 2S FeS+H 2SO 4(稀)==FeSO 4+H 2S ↑气体的干燥干燥是用适宜的干燥剂和装置除去气体中混有的少量水分。
常用装置有干燥管(内装固体干燥剂)、洗气瓶(内装液体干燥剂)。
所选用的干燥剂不能与所要保留的气体发生反应。
常用干燥剂及可被干燥的气体如下: (1)浓硫酸(酸性干燥剂):N 2、O 2、H 2、Cl 2、CO 、CO 2、SO 2、HCl 、NO 、NO 2、CH 4、C 2H 4、C 2H 2等(不可干燥还原性或碱性气体)。
(2)P 2O 5(酸性干燥剂):可干燥H 2S 、HBr 、HI 及浓硫酸能干燥的气体(不可干燥NH 3等)。
(3)无水CaCl 2(中性干燥剂):可干燥除NH 3以外的其他气体(NH 3能与CaCl 2反应生成络合物CaCl 2·8NH 3)。
(4)碱石灰(碱性干燥剂):可干燥NH 3及中性气体(N 2、O 2、H 2、CO 、NO 、CH 4、C 2H 4、C 2H 2等)。
不能干燥酸性气体。
(5)硅胶(酸性干燥剂):可干燥Cl2、O2、H2、CO2、CH4、C2H4、C2H2(硅胶能吸附水,也易吸附其他极性分子,只能干燥非极性分子气体)。
(6)其他:如生石灰、NaOH也可用于干燥NH3及中性气体(不可干燥有酸性或能与之作用的气体)。
物质的分离提纯化学分离提纯化学法要同时考虑到各组成成分及杂质的化学性质和特点,利用它们之间的差别加以分离提纯。
