常见实验动物的捉持和给药方法
常用动物实验操作指南

常用动物实验操作指南一、实验动物的抓取与固定。
(一)小鼠。
1. 抓取。
- 用右手拇指和食指抓住小鼠尾巴中部,将小鼠提起,放在鼠笼盖上或其他粗糙表面。
- 当小鼠试图抓住粗糙表面时,迅速用左手拇指和食指捏住小鼠双耳及颈部皮肤,无名指、小指和手掌心夹住小鼠背部皮肤及尾部,将小鼠固定成头部向上的直立位。
- 原因:抓住尾巴提起小鼠是为了能够将其从饲养环境中移出,而后续的固定方式可以限制小鼠的活动,避免被咬伤,同时方便进行各种操作,如注射等。
这种固定方式能够稳定地控制小鼠的身体,保证操作的准确性。
2. 固定。
- 如需进行尾静脉注射等操作,可将小鼠放入专门的小鼠固定器中,固定器可调节大小以适应不同体型的小鼠,固定器上有开口以便露出尾巴等部位进行操作。
- 对于一些简单操作如灌胃,也可以由一人用上述抓取方法固定小鼠,另一人进行操作。
(二)大鼠。
1. 抓取。
- 先用右手抓住大鼠尾巴中部,将大鼠提起,放在较粗糙的平面上。
- 然后用左手戴防护手套(大鼠体型较大且可能会用力挣扎和咬伤实验者),从大鼠背部抓住其肩部和颈部皮肤,将大鼠固定。
- 原因:大鼠力量较大,戴手套是为了保护实验者。
先抓尾巴提起是为了便于后续的抓取固定操作,从背部抓住肩部和颈部皮肤可以有效限制大鼠的活动,使其头部和身体得到控制,便于进行实验操作。
2. 固定。
- 对于需要长时间操作的情况,可将大鼠放入大鼠固定架中,固定架可以固定大鼠的四肢,使大鼠呈仰卧或俯卧位,根据实验需求调整。
- 在进行一些短期操作如皮下注射时,可由实验者用上述抓取方法固定大鼠,助手协助进行操作。
二、实验动物的给药操作。
(一)口服给药。
1. 小鼠灌胃。
- 准备合适的灌胃针(一般为1 - 2ml注射器连接特制的灌胃针头)。
- 将小鼠固定如前所述,使小鼠头部向上。
- 灌胃针从小鼠嘴角插入口腔,沿上腭后壁轻轻推进食管,插入深度约为3 - 4cm(根据小鼠大小调整)。
- 缓慢推动注射器活塞,将药物注入食管,然后缓慢拔出灌胃针。
药理学动物实验基本方法

右手拿注射器, 针尖的斜面朝 上,将针 头从远心端插 入血管
回抽有血即可
注射,拔针后 用棉球止血
豚鼠可用足 背静脉注射
实验动物的 给药.MPG
二、实验动物的采血
1 尾尖采血
眼眶静脉丛采血
2
断头采血 腹主动腹脉主动采脉血采血 心脏采血 静脉采血
3 4 5 6
1
尾尖采血
方法:固定动物并露出鼠尾,将尾部在45℃的温水中 浸泡数分钟(或以二甲苯棉球涂擦),使尾部血管扩 张。将鼠尾擦干,用锐器切去尾尖0.3~0.5cm,让血 液滴入盛器或直接以血红蛋白吸管吸取。 对象:大、小鼠 特点:小量采血,可以多次采血。
药理学动物实验基本方法
药学院药理学科组
Contents
1 实验动物的捉持与给药 2 实验动物的采血 3 实验动物的编号和分组 4 实验动物的麻醉
一、捉持与给 药
小鼠 大鼠 豚鼠 家兔 犬
•小鼠的捉持
1、用右手拇指 和食指捏住小鼠 尾巴中部将小鼠 提起,放在饲养 合的面罩上。
用左手拇指和 食指迅速、准 确地捏住小鼠 的两耳后及颈 背部的皮肤, 将小鼠提起。
笼或大小鼠固定 器的孔拉出鼠尾 巴
用左手捏住鼠 尾巴中下部, 用75%
酒精棉球反 复擦拭尾部
大鼠亦可用 舌下静脉注
射
注射时,以左 手拇指和中指 捏住鼠尾两侧, 用食指从下面 托起尾,
右手持4号针 头的注射器, 使针头与
静脉平行 (小于30度角)
•静脉注射给药——犬
前肢皮下头静脉 或后肢小隐静脉 注射 。
用右手食指将 针栓慢慢往下 压,将注射器 中的药液灌入 动物的胃中。
•灌胃给药——兔
将兔放进固 定架
内,灌胃者用左 手拇指和中指挤 压兔两颊,将下 颌挤开使兔被动 张口。
动物实验操作基本方法

33
LOGO
随机区组分组
实验动物的捉 拿.MPG
8
LOGO
•灌胃给药——大小鼠
剂量:小鼠约0.1-0.5ml/10g体重。最大体积为1.0ml/只 大鼠约1-2 ml/100g体重,最大体积为1.0ml/只
1、将灌胃针连 接在注射器上, 吸入一定量的 药液。
左手捉持动物, 使头部向上。
右手持针,把 灌胃针头的前 端放进动物的 口腔,顺着上 腭部插入咽部, 顺咽后壁轻轻 往下推。
29
LOGO
30
LOGO
(二)分组的方法
完全随机分组 完全随机分组时将试验对象完全按随机原则分组。它的设计、
分组、和统计处理都比较简单,但试验效率较低。 例:将30只SD 大鼠随机分配到甲、乙、丙3组。 使用excel对试验对象完全随机分组的操作步骤如下:
31
LOGO
1.在单元格A1、B1、C1中分别键入编号、随机号、分组号, 随后在A2、A3中分别键入1、2,然后拖动鼠标利用excel 的自动填充功能完成1~30的编号。
•兔的捉持
用右手抓住兔 颈部的被毛和 皮肤,轻轻把 兔提起。
用左手托住兔 的臀部
家兔的固定方 式有腹卧式和 仰卧式两种
7
LOGO
•犬的捉持
实验者先抚摩, 逐步接近,勿 使其惊恐或将 其激怒。
用粗棉绳兜住 狗的下颌,并 在上颌打结 (勿太紧)。
动物实验的基本操作

动物实验的基本操作(动物的捉拿与给药方法)小鼠捉拿法有二种:一种是用右手提起尾部,放在鼠笼盖或其他粗糙面上,向后上方轻拉,此时小鼠前肢紧紧抓住粗糙面,迅速用左手拇指和食指捏住小鼠颈背部皮肤并用小指和手掌尺侧夹持其尾根部固定手中;另一种抓法是只用左手,先用拇指和食指抓住小鼠尾部,再用手掌尺侧及小指夹住尾根,然后用拇指及食指捏住其颈部皮肤。
大鼠捉拿时,右手抓住鼠尾基部,将大鼠放在粗糙面上,左手戴上防护手套或用厚布盖住大鼠,抓住其整个身体并固定其头部以防咬伤。
捉拿时勿用力过猛,勿捏其颈部,以免引起窒息。
家兔捉拿时一手抓住其颈背部皮肤。
轻轻将兔提起,另一手托住其臀部。
猫捉拿时先轻声呼唤,再慢慢将手伸入猫笼中,轻抚猫的头、颈及背部,抓住其颈背部皮肤并以另一手抓其背部。
如遇凶暴的猫,不让接触或捉拿时,可用套网捉拿,必要时可用固定袋将猫固定。
实验动物的给药方法1.灌胃法小鼠灌胃法将小鼠放在粗糙面上,左手拇指和食指捏住小鼠颈背部皮肤,无名指或小指将尾部紧压在手掌上,使小鼠腹部朝上,注意使口腔和食管成一直线。
右手持灌胃针管从小鼠口角插入口腔内,经舌面紧贴上腭进入食管,进针2~3cm 后,如此时动物安静并无呼吸异常,即可将药注入。
如遇阻力或动物憋气时则应抽出重插,不能强插以免刺破食管或误入气管使动物死亡。
兔灌胃法用兔固定箱,可一人操作。
右手将开口器固定于兔口中,舌压在开口器下面,左手将导管经开口器中央小孔插入。
如无兔固定箱,则需两人协作进行,一人就坐,腿上垫好围裙,将兔的躯体夹于两腿间,左手紧握双耳,固定其前身,右手抓住其两前肢。
另一人将开口器横放于兔上下颌之间,固定在舌面上,将导管自开口器中央的小孔插入,慢慢沿兔口腔上腭壁插入食道约15~18cm。
插管完毕将胃管的外口端放入水杯中,切忌伸入水过深。
如有气泡从胃管逸出,说明不在食道内而是在气管内,应拔出来重插。
如无气泡逸出,则可将药推入,并以少量清水冲洗导尿管保证管内药液全部进入胃内。
实验1实验动物的捉持法和给药法

实验1 实验动物的捉持法和给药法一、常用实验动物的捉持法1.蛙和蟾蜍通常以左手握持,用食指和中指夹住左前肢,拇指压住右前肢,右手将下肢拉直,左手用无名指及小指夹住(图1)。
图1 蟾蜍捉持法2.小鼠(1)双手法:右手提鼠尾,放在鼠笼盖或其他粗糙面上,向后方轻拉鼠尾,使小鼠前肢固定在粗糙面上。
迅速用左手拇指和食指捏其双耳间颈背部皮肤,无名指、小指和掌心夹其背部皮肤和尾部,便可将小鼠牢固捉持(图2)。
图2 小鼠双手捉持法(2)单手法:小鼠置于笼盖上,先用左手食指和拇指抓住鼠尾,后手掌尺侧和小指夹住鼠尾,然后左手拇指与食指捏住颈部皮肤(图3)。
图3 小鼠单手捉持法3. 大鼠大鼠容易激怒咬人,捉持时应戴防护手套。
先用右手抓住鼠尾,再用左手拇指和食指握住头部,其余手指与掌部握住背部和腹部。
注意不要捏其颈部,以防用力过大、过久,窒息死亡。
4.家兔一只手抓住兔颈背部皮肤,将兔轻轻提起,另一只手托住臀部,使兔呈蹲坐姿势(图4)。
切不可用手握持双耳提起兔子。
图4 家兔捉持法5.豚鼠豚鼠性情温和,不咬人,用手轻轻握住身体即可抓起。
6. 猫应戴好防护手套。
轻声呼唤,慢慢将手伸入猫笼,轻抚猫头、颈和背部,一只手抓住颈背部皮肤,另一只手抓住腰背部。
性情凶暴的猫可用布袋或网套捉持,操作中应防其利爪和牙齿伤人。
7. 狗驯服的狗可戴上特制嘴套,用绳带固定于耳后颈部;凶暴的狗可用长柄捕狗夹钳住狗的颈部,然后套上嘴套。
狗嘴也可用绳带固定,操作时先将绳带绕过狗嘴的下颌打结,再绕到颈后部打结,以防绳带滑落。
狗麻醉后四肢固定于手术台上,取下嘴套或绳带,将一金属棒经两侧嘴角,穿过口腔压于舌上,再用绳带绕过金属棒绑缚狗嘴,并固定于手术台上。
应将狗舌拉出口腔,以防窒息。
二、常用实验动物给药法1. 经口给药法此法有口服与灌胃两种方法。
适用于小鼠、大鼠、豚鼠、兔、犬等动物。
口服法可将药物放入饲料或溶于饮水中令动物自由摄取。
若为保证剂量准确,可应用灌胃法。
实验动物的捉拿和给药方法

实验一实验动物的捉拿和给药方法【目的】结合实验内容逐步学会实验常用动物的捉拿和给药方法。
【内容】(一)小自鼠的捉拿和给药方法1.捉拿法用右手捉住小白鼠的尾巴将鼠提起.置于鼠笼上面或其他粗糙面上,向后拉轻鼠尾,迅速用左手拇指和示指挥住其两耳及头部皮肤,翻转鼠体,使腹部朝上,然后以无名指及小指压往鼠尾,使小鼠完全固定(实验图1).实验图1 小白鼠的捉拿法2.给药方法(1)灌胃将小白鼠固定后,使口部向上,将颈部拉直,右手持灌胃器自口角插入口腔,沿上颚轻轻进入食管,如动物安静,呼吸元异常、口唇无紫绀现象,即可注入药液(实验图2).灌胃器0.1一O.25ml/10g。
实验图2 小白鼠灌胃器(左)和灌胃法(布)(2)腹腔注射将小白鼠固定后,右手持注射器自下膜一侧向头部方向以30~45度刺入腹腔(角度太小易刺入皮下)。
针头刺入不宜太深或太近上腹部,以免刺伤内脏,注射量一般为0.1~O.2 ml/10g 。
(3)皮下注射捉鼠方法同前,右手持注射器,将计头刺人背部皮下注人药液。
注射量一般不超过0.25 ml/10g。
(4)肌内注射由两人合作,一人固定小白鼠后,另一入持注射器,将针头刺入后肢外侧肌肉内注入药液,注射量为每腿不超过0.lml。
(二)螗蜍或蛙的捉拿和给药方法1.捉拿法通常用左手握蛙,食指和中指夹住蛙的两上肢,无名指和小指夹住蛙的两下肢,将蛙固定于手中。
2.给药方法(淋巴囊注射) 蛙皮下淋巴囊分布见实验图3。
多采用腹囊给药。
由于蛙的皮肤弹性差,被针头刺破后,针眼不易闭合会便药波外溢,故注射针头必须通过一层隔膜,再进人皮下淋巴囊。
如腹囊绐药时,针头应自大腿上端刺人,经过大腿肌层入腹壁肌层.再浅出进人腹壁皮下入腹囊。
注射量每只可达0.25—1.Oml.(三)家免的捉拿和给药方法1.捉拿祛用左手抓住颈背部皮肤将兔提起,以右手托住其臀部,使兔呈坐位姿势。
2.给药方法(1)灌胃两人合作,由一人固定兔身,另一人用兔开口器(实验图4)将兔口张开,并将兔舌压在开曰器下边横放于兔口中。
实验动物的捉拿和给药方法

实验一实验动物的捉拿和给药方法【目的】结合实验内容逐步学会实验常用动物的捉拿和给药方法。
【内容】(一)小自鼠的捉拿和给药方法1.捉拿法用右手捉住小白鼠的尾巴将鼠提起.置于鼠笼上面或其他粗糙面上,向后拉轻鼠尾,迅速用左手拇指和示指挥住其两耳及头部皮肤,翻转鼠体,使腹部朝上,然后以无名指及小指压往鼠尾,使小鼠完全固定(实验图1).实验图1 小白鼠的捉拿法2.给药方法(1)灌胃将小白鼠固定后,使口部向上,将颈部拉直,右手持灌胃器自口角插入口腔,沿上颚轻轻进入食管,如动物安静,呼吸元异常、口唇无紫绀现象,即可注入药液(实验图2).灌胃器0.1一O.25ml/10g。
实验图2 小白鼠灌胃器(左)和灌胃法(布)(2)腹腔注射将小白鼠固定后,右手持注射器自下膜一侧向头部方向以30~45度刺入腹腔(角度太小易刺入皮下)。
针头刺入不宜太深或太近上腹部,以免刺伤内脏,注射量一般为0.1~O.2 ml/10g 。
(3)皮下注射捉鼠方法同前,右手持注射器,将计头刺人背部皮下注人药液。
注射量一般不超过0.25 ml/10g。
(4)肌内注射由两人合作,一人固定小白鼠后,另一入持注射器,将针头刺入后肢外侧肌肉内注入药液,注射量为每腿不超过0.lml。
(二)螗蜍或蛙的捉拿和给药方法1.捉拿法通常用左手握蛙,食指和中指夹住蛙的两上肢,无名指和小指夹住蛙的两下肢,将蛙固定于手中。
2.给药方法(淋巴囊注射) 蛙皮下淋巴囊分布见实验图3。
多采用腹囊给药。
由于蛙的皮肤弹性差,被针头刺破后,针眼不易闭合会便药波外溢,故注射针头必须通过一层隔膜,再进人皮下淋巴囊。
如腹囊绐药时,针头应自大腿上端刺人,经过大腿肌层入腹壁肌层.再浅出进人腹壁皮下入腹囊。
注射量每只可达0.25—1.Oml.(三)家免的捉拿和给药方法1.捉拿祛用左手抓住颈背部皮肤将兔提起,以右手托住其臀部,使兔呈坐位姿势。
2.给药方法(1)灌胃两人合作,由一人固定兔身,另一人用兔开口器(实验图4)将兔口张开,并将兔舌压在开曰器下边横放于兔口中。
常见实验动物的捉持和给药方法

常见实验动物的捉持和给药⽅法常见实验动物的捉持和给药⽅法⼀、⼩⽩⿏的捉持和给药⽅法1、捉持⽅法右⼿提起⿏尾,放在粗糙物(如⿏笼)上⾯,轻向后拉其尾;此时⼩⿏前肢抓住粗糙⾯不动;⽤左⼿拇指和⾷指捏住双⽿及头部⽪肤,⽆名指、⼩指和掌⼼夹其背部⽪肤及尾部,便可将⼩⿏完全固定。
腾出右⼿,可以给药。
此外,也可单⼿捉持,难度较⼤,但速度快。
先⽤拇指和⾷指抓住⼩⿏尾巴,⽤⼩指、⽆名指和⼿掌压住尾根部,再⽤腾出的拇指、⾷指及中指抓住⿏双⽿及头部⽪肤⽽固定。
2、给药⽅法a.灌胃法⼩⿏固定后,使腹部朝上,颈部拉直,右⼿⽤带灌胃针头的注射器吸取药液(或事先将药液吸好),将针头从⼝交插⼊⼝腔,再从⾆背进沿上腭进⼊⾷道。
若遇阻⼒,应退出后再插,切不可⽤⼒过猛,防⽌损伤或误⼊⽓管导致动物死亡。
灌胃量⼀般不超过0.25ml/10g。
b.腹腔注射法抓⿏⽅法同上,右⼿持注射器(5~6号针头),从耻⾻联合上⼀侧向头端以30度⾓刺⼊腹腔(应避开膀胱)。
可先刺⼊⽪下2~3mm,再刺⼊腹腔,以防药液外漏。
针头刺⼊部位不宜太⾼太深,以免刺破内脏。
注射量⼀般为0.1~0.25ml/10g。
c.⽪下注射法⼀般两⼈合作。
⼀⼈左⼿抓住⼩⿏头部⽪肤,右⼿拉住⿏尾;另⼀⼈左⼿提⾼背部⽪肤,右⼿持住注射器(针头号同上),将针头刺⼊提起的⽪下。
若⼀⼈操作,左⼿⼩指和⼿掌夹住⿏尾,拇指和⾷指提起背部⽪肤,右⼿持注射器给药。
⼀般⽤量为0.05~0.25ml/10g。
d.肌⾁注射法两⼈合作时,⼀⼈抓⿏⽅法同上,另⼀⼈左⼿拉直⼀侧后肢,右⼿持注射器,注射部位多选后腿上部外侧(针头号同上)。
如⼀⼈操作,抓⿏⽅法类似腹腔注射,只是药液注射在肌⾁内。
每腿的注射量不宜超过0.1ml。
e.尾静脉注射法将⼩⿏置于待置的固定筒内,使⿏尾外露,并⽤酒精或⼆甲苯棉球涂擦,或插⼊40℃~50℃温⽔中浸泡⽚刻,使尾部⾎管扩张。
左⼿拉尾,选择扩张最明显的⾎管;右⼿持注射器(4~5号针头),将针头刺⼊⾎管,缓慢给药。
11.常用实验动物的给药途径和方法

常用实验动物的给药途径和方法在动物实验中,为了观察药物对机体功能、代谢及形态的变化,常需将药物注入动物体内。
由于实验目的、动物种类、药物剂型不同,给药途径和方法也多种多样。
一经口给药法(一)灌胃法此法给药剂量准确,是借灌胃器将药物直接灌到动物胃内的一种常用给药方法。
1、白鼠灌胃法:抓起小鼠,以左手拇指、食指固定头部,小指、无名指和掌心夹注尾巴,使腹部朝上,颈部拉直,右手持灌胃器,将灌胃针从鼠的口角插入口腔,从舌背沿上腭插入食道。
灌胃量0.2~0.5ml/10g。
胃管可用适宜口径的硬质塑料管或磨去针头的8号注射针头弯成适当的弧度制成。
注意,操作时不要用力猛插,以免插破食道或误插入器官造成动物死亡。
2、白鼠灌胃法:左手戴上棉手套,用左手拇指和食指将大鼠头部固定,将大鼠灌胃器沿腭后壁慢慢插入食道。
灌胃针插入时应无阻力,如有阻力或动物挣扎则应退针或将针拔出,重新再插。
灌胃器由注射器和特殊的灌胃针构成。
灌胃量10~20ml/kg3 兔、犬等:灌胃一般要借助于开口器、灌胃管进行。
先将动物固定,再将开口器固定于上下门齿之间,然后将灌胃管(常用导尿管代替)从开口器的小孔插入动物口中,沿咽后壁而进入食道。
插入后应检查灌胃管是否确实插入食道。
可将灌胃管外开口放入盛水的烧杯中,若无气泡产生,表明灌胃管被正确插入胃中,未误入气管。
此时将注射器与灌胃管相连,注入药液。
4、猪的胃内灌注法:给猪下鼻饲管较困难,因猪的鼻翼与上唇联合形成吻突,鼻腔内上下鼻夹与鼻中隔通道极窄,只能通过F10-12号的导尿管,F14号以上的导尿管不能插入,故一般均给猪采用经口入胃的灌胃方法。
具体方法是,预先做好一矩形小木块,中间有一洞,让小猪咬住,将其固定,然后再由此洞下胃管。
此种操作较为简便。
5、鸟类:包括鸽、鸡等,经口灌胃给药,可由助手将其身体用毛巾裹住固定好。
实验者用左手将动物向后拉,使其颈部倾斜,用左拇指和食指将动物嘴撬开,其他三只手指固定好动物头部,右手取带有灌胃针头的注射器,将灌胃针头由动物舌后插入食管。
实验动物常用操作(抓取、麻醉、给药)

实验动物常用操作方法1.小鼠的抓取与固定抓取和固定是动物实验操作中一项最基本的技术,所有的动物实验都要涉及到。
由于动物害怕陌生人接触其身体,对于非条件性的各种剌激会进行防御性反抗。
因此,在抓取、固定前应对动物的生活习性有所了解,根据其生活习性采用相应的抓取固定方法。
一般在抓取固定动物过程中首先慢慢友好地接近动物,并注意观察其反应,让动物有一个适应过程。
抓取时的动作力求准确、迅速、熟练,争取在动物感到不安之前抓取到动物。
(1)抓取方法习惯用右手者,首先用右手从笼盒内将小鼠尾中部或基部抓住(不可抓尾尖),并提起或放在左手上或笼盖表面。
如下图。
也可用尖端带有橡皮的镊子夹住小鼠的尾巴。
抓取时需注意如果过分用力,会使动物窒息或颈椎脱臼,力过小,动物头部能反转来咬伤实验者的手。
因此实验者必须反复练习,熟练掌握。
(2)固定方法①徒手固定:右手抓取小鼠尾,将小鼠放在笼盖(或表面粗糙的物体)上,轻轻向后拉鼠尾。
然后在小鼠向前挣脱时,用左手(熟练者也可用同一只手)拇指和食指抓住两耳和颈部皮肤,无名指、小指和手掌心夹住背部皮肤和尾部,并调整好动物在手中的姿势。
习惯用左手者,操作时可调整左右手。
这类抓取方法多用于灌胃以及肌肉、腹腔和皮下注射等实验。
②固定板固定:小鼠麻醉后置小鼠固定板上,取仰卧位,用胶布缠粘四肢,再用针透过胶布扎在板上,从而将小鼠固定在小鼠固定板上。
此方法常用作心脏采血、解剖、外科手术等实验。
③固定架固定:让小鼠直接钻入固定架里,封好固定架的封口,露出尾巴。
此装置特别适用于小鼠尾静脉注射等。
④简易固定:进行尾静脉注射或抽血时,如果没有这些固定装置,也可采用一种简易的办法。
即倒放一个烧杯或其他容器,把小鼠扣在里面,只露出尾巴。
然后酒精擦拭,暴露血管,注射或采样。
这种烧杯或容器的大小和重量要适当,既能够压住尾部不让其活动,同时起到压迫血管的作用。
2.小鼠的麻醉方法实验动物的麻醉就是用物理的或化学的方法,使动物全身或局部暂时痛觉消失或痛觉迟饨,以利于进行实验。
药理实验

实验一常用动物的捉拿与给药方法【实验目的】1、了解小鼠的饲养方法2、练习并掌握小鼠的捉拿与给药方法【实验材料】1、器材:鼠笼、饮水瓶、大烧杯、托盘天平、灌胃器、注射器、棉签2、药品:生理盐水、苦味酸溶液、75%酒精3、动物:小白鼠,20~30g【实验方法】1、捉拿与固定:用右手捉住鼠尾,将其提起置于鼠笼或者粗糙平面上,向后轻拉鼠尾,用左手的拇指和食指抓住小鼠两耳及颈背部皮肤,将小鼠置于左手掌心,以小指夹住小鼠尾巴即可。
2、给药法⑴灌胃:将小鼠固定,口朝上,颈部拉直,右手持灌胃针,先从口角处插入口腔,再沿上颚轻轻插入食管。
一般给药剂量0.1-0.3ml/10g。
⑵腹腔注射:将小鼠固定,右手持注射器自下腹部一侧刺入皮下后,再刺入腹腔,缓慢注入药物。
一般给药剂量0.1-0.3ml/10g。
⑶皮下注射:两人合作,一人左手抓住小鼠头部,右手拉住小鼠尾巴固定小鼠,另外一人用左手提起皮肤,右手持注射器刺入皮下注入药物。
一般给药剂量为0.1-0.2ml/10g⑷肌肉注射:最好两人合作,一人固定小鼠,另外一人将针头迅速垂直刺入后肢外侧肌肉,回抽无回血即可注入药物,一侧给药剂量为0.02-0.05ml/10g。
⑸静脉注射:一般采用尾静脉注射。
将小鼠固定,使尾巴露出来,在50℃热水中浸泡或者用75%酒精擦拭尾巴,使血管扩张,左手拉住鼠尾,右手持注射器,从鼠尾巴末梢开始进针,注入药液。
一般给药剂量为0.1-0.2ml/10g【心得体会】实验二不同给药途径对药物作用的影响【实验目的】观察不同给药途径对药物作用的影响【实验材料】4、器材:大烧杯、托盘天平、灌胃器、注射器、棉签少许5、药品:10%硫酸镁溶液、5%氯化钙溶液、苦味酸溶液6、动物:小鼠,18~22g【实验方法】1、取小鼠3只,称重编号,分别放入大烧杯中,观察小鼠的正常活动,记录半个小时内活动、呼吸、粪便情况。
2、给药:一号小鼠灌胃10%硫酸镁溶液0.2ml/10g二号小鼠肌肉注射10%硫酸镁溶液0.2ml/10g三号小鼠静脉注射10%硫酸镁溶液0.2ml/10g3、观察小鼠的反应及活动,记录半小时内小鼠活动、呼吸及粪便变化。
11.常用实验动物的给药途径和方法

常用实验动物的给药途径和方法在动物实验中,为了观察药物对机体功能、代谢及形态的变化,常需将药物注入动物体内。
由于实验目的、动物种类、药物剂型不同,给药途径和方法也多种多样。
一经口给药法(一)灌胃法此法给药剂量准确,是借灌胃器将药物直接灌到动物胃内的一种常用给药方法。
1、白鼠灌胃法:抓起小鼠,以左手拇指、食指固定头部,小指、无名指和掌心夹注尾巴,使腹部朝上,颈部拉直,右手持灌胃器,将灌胃针从鼠的口角插入口腔,从舌背沿上腭插入食道。
灌胃量0.2~0.5ml/10g。
胃管可用适宜口径的硬质塑料管或磨去针头的8号注射针头弯成适当的弧度制成。
注意,操作时不要用力猛插,以免插破食道或误插入器官造成动物死亡。
2、白鼠灌胃法:左手戴上棉手套,用左手拇指和食指将大鼠头部固定,将大鼠灌胃器沿腭后壁慢慢插入食道。
灌胃针插入时应无阻力,如有阻力或动物挣扎则应退针或将针拔出,重新再插。
灌胃器由注射器和特殊的灌胃针构成。
灌胃量10~20ml/kg3 兔、犬等:灌胃一般要借助于开口器、灌胃管进行。
先将动物固定,再将开口器固定于上下门齿之间,然后将灌胃管(常用导尿管代替)从开口器的小孔插入动物口中,沿咽后壁而进入食道。
插入后应检查灌胃管是否确实插入食道。
可将灌胃管外开口放入盛水的烧杯中,若无气泡产生,表明灌胃管被正确插入胃中,未误入气管。
此时将注射器与灌胃管相连,注入药液。
4、猪的胃内灌注法:给猪下鼻饲管较困难,因猪的鼻翼与上唇联合形成吻突,鼻腔内上下鼻夹与鼻中隔通道极窄,只能通过F10-12号的导尿管,F14号以上的导尿管不能插入,故一般均给猪采用经口入胃的灌胃方法。
具体方法是,预先做好一矩形小木块,中间有一洞,让小猪咬住,将其固定,然后再由此洞下胃管。
此种操作较为简便。
5、鸟类:包括鸽、鸡等,经口灌胃给药,可由助手将其身体用毛巾裹住固定好。
实验者用左手将动物向后拉,使其颈部倾斜,用左拇指和食指将动物嘴撬开,其他三只手指固定好动物头部,右手取带有灌胃针头的注射器,将灌胃针头由动物舌后插入食管。
试验动物保定方法

一、实验动物的捉拿、固定及给药方法1.小白鼠:右手抓住鼠尾,放在台上或鼠笼盖铁丝网下,然后用左手拇指沿其背部向前抓住其颈部皮肤,并以左手的小指和掌部夹住其尾固定在手上。
另一抓法是只用左手,先用食指和拇指抓住小鼠尾尖,后用手掌及小指夹住其尾巴,再以拇指及食指捉住其颈部皮肤。
前一方法易学,另一方法稍难,但便于快速捉拿给药。
小鼠灌胃(PO)法:将小鼠固定后,右手持装有灌胃器的注射器,自口角外插入口腔,沿上颚插入食道。
如遇阻力,可将注射器拔出再插,以免穿破食道或误入气管,造成动物死亡。
灌胃容量一般为0.1~0.2ml/10g,不超过0.5ml/只。
小鼠皮下注射法:两人合作,一人一手抓住小白鼠头部皮肤,另一手抓住鼠尾。
另一人注射药物。
注射部位在背部皮下组织。
如一人操作时,左手抓鼠尾,让鼠爬在铁丝笼上,右手将抽好药液的注射器针头插入背部皮下组织。
如一人操作时,左手抓鼠尾,让鼠爬在铁丝笼上,右手将抽好的药液的注射器针头插入背部皮下将药注入。
注射量不超过0.5ml/只。
小鼠腹腔注射法:左手持鼠,右手持注射器从下腹左或右侧(避开膀胱)朝头部方向刺入,宜先刺入皮下,经2~3mm再刺入腹腔,此时针头与腹壁的角度约45度。
针尖插入不宜太深或太近上腹部,避免刺破内脏,注射量一般为0.1~0.25ml/只。
小鼠尾静脉注射法:将小鼠置于固定器内,使其尾巴露出,用70%酒精擦尾部,或将鼠尾浸入50℃热水中。
待尾部静脉扩张后,左手拉尾,右手进针。
注射容量不超过0.5ml/只。
2.兔:用手抓起它脊背近后颈处皮肤,抓的面积越大其持重点越分散。
如家兔肥大,应再以另一手托住它的臀部,将持重点承托于手上。
将兔作仰卧位,一手仍抓住颈部皮肤,另一手顺其腹部抚摸至膝关节,压住关节。
另一人用绳带捆绑四肢,使兔腹部向上,固定在兔手术台上。
头部则用兔头固定夹固定。
兔灌胃法:二人合作,一人固定家兔于两膝之间,一手固定兔头,使头部后仰,另一手将开口器插入兔口,并向后翻转数次,使兔舌伸直并压在开口器下面。
实验一实验动物的捉拿和给药方法

陈品 10 11
药物作用与溶解度的关系;给药途径对药物作用影响 解热镇痛药对发热家兔体温的影响
谢书宇 12
利尿药对家兔的利尿作用观察
13
盐类泻药的泻下机理分析
编辑ppt
3
兽医药理学实验规则
实验前:温故知新 实验准备:提前去兽医院领取实验动物。 实验时:科学、严谨、认真。 避免无端浪费。 注意安全操作:防火、电、中毒、感染及咬伤事故。 污物放入污物桶内集中处理;
兔子的给药方法
耳缘静脉注射 iv 腹腔注射 ip 皮下注射 ih 肌内注射 im
编辑ppt
18
➢ 兔静脉注射
部位:耳缘静脉。 方法:酒精棉球涂擦耳缘静脉部皮肤,
左手食指放在耳下将兔耳垫起, 并以拇指压耳缘部分, 右手持带有针头的注射器, 尽量从血管远端刺入血管, 注射时针头先刺入皮下, 沿皮下向前推进少许,然后刺入血管。 针头刺入血管后再少向前推进, 轻轻推动针栓,若无阻力即可注药。 注射完毕后,用棉球压住针眼,拔去针头。
编辑ppt
4
• 实验设计基本原则(3R)
• 随机原则(Random)
• 每一实验对象都有同等的机会抽到实验组或对照组中。
• 对照原则(Reference)
• 组间对照:阴性对照,阳性对照,同因素不同水平对照; • 自身前后对照
• 重复原则(Repeat)
编辑ppt
5
• 实验动物的选择
• 小白鼠、大白鼠:大量动物的实验,药理毒理学常用动物。 • 豚鼠: 对组胺敏感---抗过敏药、平喘药和抗组胺药的实验; 离体心脏、心房、肠管实验;对结核敏感---抗结核病药实验。 • 家兔: 家兔体温变化敏感---体温实验、热原检查; 脑电生理作用;药物对小肠的作用。 • 狗: 狗是记录血压、呼吸最常用的大动物;胃瘘、肠瘘;慢性毒 性实验
实验一 小白鼠和家兔的捉持与给药方法(doc)

实验一小白鼠和家兔的捉持与给药方法(doc)实验动物的捕持和给药是实验操作中非常关键的步骤。
本文主要介绍小白鼠和家兔的捉持和给药方法。
1. 捕持方法小白鼠较为敏感,需要小心捉持。
可以采用直接手抓或使用器械相结合的方法。
① 直接手抓:用左手握住小白鼠的尾巴,将其抬离地面,右手用力抓住身体。
捉持的位置应该落在肩胛骨的后面。
捉持后,将小白鼠稳定住,不要摇晃。
② 使用器械:可以使用长柄刷子、网兜、特殊夹具等工具将小白鼠从底部壁上向上推,然后在手掌捉持。
2. 给药方法对于小鼠的给药方法,有多种选择。
下面分别介绍常见的口服给药和腹腔注射。
① 口服给药:使用灌胃针或切口方法。
前者通常用于液体或悬浮物,后者通常用于固体或片剂。
灌胃针方法:将灌胃针插入小鼠口中,直到其到达胃部。
然后缓慢注入待给药物。
给药完毕后,针头要缓慢拔出。
切口方法:用手或器械拓宽小鼠口腔,将给药物放在其舌根处。
然后轻轻地按住小鼠的颈部,使其吞咽。
② 腹腔注射:使用注射器在小鼠腹部注射待给药物。
首先选择注射部位,一般建议在小鼠的下腹部。
然后用适量的酒精消毒注射部位。
将注射器插入腹部,确保局麻针穿过腹膜。
缓慢注射待给药物后,注射针要慢慢拔出。
二、家兔的捕持和给药方法① 直接手抓:用两只手同时抓住家兔颈部和臀部。
抓住后,将家兔稳定住,不要晃动。
② 使用器械:可以使用外科手套或草绳将家兔绑定在固定位置上。
需要特别注意的是,草绳不要绑定得太紧,以免影响家兔的呼吸。
总的来说,实验动物的捉持和给药方法需要谨慎操作,以保证实验的成功和动物的健康。
在进行操作前,需要进行必要的训练,熟悉其生理特征,了解其习性,确保操作更加顺利。
同时,在实验过程中,也要注意动物的福利和健康,确保其得到最好的关怀和保障。
1常用实验动物的给药途径和方法

常用实验动物的给药途径和方法在动物实验中,为了观察药物对机体功能、代及形态的变化,常需将药物注入动物体。
由于实验目的、动物种类、药物剂型不同,给药途径和方法也多种多样。
一经口给药法(一)灌胃法此法给药剂量准确,是借灌胃器将药物直接灌到动物胃的一种常用给药方法。
1、白鼠灌胃法:抓起小鼠,以左手拇指、食指固定头部,小指、无名指和掌心夹注尾巴,使腹部朝上,颈部拉直,右手持灌胃器,将灌胃针从鼠的口角插入口腔,从舌背沿上腭插入食道。
灌胃量0. 2〜0. 5mL/'10gc胃管可用适宜口径的硬质塑料管或磨去针头的8号注射针头弯成适当的弧度制成。
注意,操作时不要用力猛插,以免插破食道或误插入器官造成动物死亡。
2、白鼠灌胃法:左手戴上棉手套,用左手拇指和食指将大鼠头部固定,将大鼠灌胃器沿腭后壁慢慢插入食道。
灌胃针插入时应无阻力,如有阻力或动物挣扎则应退针或将针拔出,重新再插。
灌胃器由注射器和特殊的灌胃针构成。
灌胃量10〜20ml/kg3兔、犬等:灌胃一般要借助于开口器、灌胃管进行。
先将动物固定,再将开口器固定于上下门齿之间,然后将灌胃管(常用导尿管代替)从开口器的小孔插入动物口中,沿咽后壁而进入食道。
插入后应检查灌胃管是否确实插入食道。
可将灌胃管外开口放入盛水的烧杯中,若无气泡产生,表明灌胃管被正确插入胃中,未误入气管。
此时将注射器与灌胃管相连,注入药液。
4、猪的胃灌注法:给猪下鼻饲管较困难,因猪的鼻翼与上唇联合形成吻突,鼻腔上下鼻夹与鼻中隔通道极窄,只能通过F10-12号的导尿管,F14号以上的导尿管不能插入,故一般均给猪采用经口入胃的灌胃方法。
具体方法是,预先做好一矩形小木块,中间有一洞,让小猪咬住,将其固定,然后再由此洞下胃管。
此种操作较为简便。
5、鸟类:包括鸽、鸡等,经口灌胃给药,可由助手将其身体用毛巾裹住固定好。
实验者用左手将动物向后拉,使其颈部倾斜,用左拇指和食指将动物嘴撬开,其他三只手指固定好动物头部,右手取带有灌胃针头的注射器,将灌胃针头由动物舌后插入食管。
实验1 实验动物的捉持法和给药法
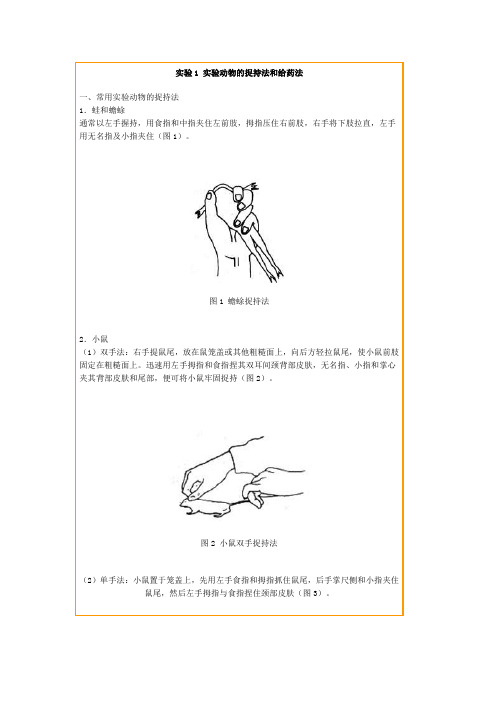
实验1 实验动物的捉持法和给药法一、常用实验动物的捉持法1.蛙和蟾蜍通常以左手握持,用食指和中指夹住左前肢,拇指压住右前肢,右手将下肢拉直,左手用无名指及小指夹住(图1)。
图1 蟾蜍捉持法2.小鼠(1)双手法:右手提鼠尾,放在鼠笼盖或其他粗糙面上,向后方轻拉鼠尾,使小鼠前肢固定在粗糙面上。
迅速用左手拇指和食指捏其双耳间颈背部皮肤,无名指、小指和掌心夹其背部皮肤和尾部,便可将小鼠牢固捉持(图2)。
图2 小鼠双手捉持法(2)单手法:小鼠置于笼盖上,先用左手食指和拇指抓住鼠尾,后手掌尺侧和小指夹住鼠尾,然后左手拇指与食指捏住颈部皮肤(图3)。
图3 小鼠单手捉持法3. 大鼠大鼠容易激怒咬人,捉持时应戴防护手套。
先用右手抓住鼠尾,再用左手拇指和食指握住头部,其余手指与掌部握住背部和腹部。
注意不要捏其颈部,以防用力过大、过久,窒息死亡。
4.家兔一只手抓住兔颈背部皮肤,将兔轻轻提起,另一只手托住臀部,使兔呈蹲坐姿势(图4)。
切不可用手握持双耳提起兔子。
图4 家兔捉持法5.豚鼠豚鼠性情温和,不咬人,用手轻轻握住身体即可抓起。
6. 猫应戴好防护手套。
轻声呼唤,慢慢将手伸入猫笼,轻抚猫头、颈和背部,一只手抓住颈背部皮肤,另一只手抓住腰背部。
性情凶暴的猫可用布袋或网套捉持,操作中应防其利爪和牙齿伤人。
7. 狗驯服的狗可戴上特制嘴套,用绳带固定于耳后颈部;凶暴的狗可用长柄捕狗夹钳住狗的颈部,然后套上嘴套。
狗嘴也可用绳带固定,操作时先将绳带绕过狗嘴的下颌打结,再绕到颈后部打结,以防绳带滑落。
狗麻醉后四肢固定于手术台上,取下嘴套或绳带,将一金属棒经两侧嘴角,穿过口腔压于舌上,再用绳带绕过金属棒绑缚狗嘴,并固定于手术台上。
应将狗舌拉出口腔,以防窒息。
二、常用实验动物给药法1. 经口给药法此法有口服与灌胃两种方法。
适用于小鼠、大鼠、豚鼠、兔、犬等动物。
口服法可将药物放入饲料或溶于饮水中令动物自由摄取。
若为保证剂量准确,可应用灌胃法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常见实验动物的捉持和给药方法
一、小白鼠的捉持和给药方法
1、捉持方法
右手提起鼠尾,放在粗糙物(如鼠笼)上面,轻向后拉其尾;此时小鼠前肢抓住粗糙面不动;用左手拇指和食指捏住双耳及头部皮肤,无名指、小指和掌心夹其背部皮肤及尾部,便可将小鼠完全固定。
腾出右手,可以给药。
此外,也可单手捉持,难度较大,但速度快。
先用拇指和食指抓住小鼠尾巴,用小指、无名指和手掌压住尾根部,再用腾出的拇指、食指及中指抓住鼠双耳及头部皮肤而固定。
2、给药方法
a.灌胃法
小鼠固定后,使腹部朝上,颈部拉直,右手用带灌胃针头的注射器吸取药液(或事先将药液吸好),将针头从口交插入口腔,再从舌背进沿上腭进入食道。
若遇阻力,应退出后再插,切不可用力过猛,防止损伤或误入气管导致动物死亡。
灌胃量一般不超过0.25ml/10g。
b.腹腔注射法
抓鼠方法同上,右手持注射器(5~6号针头),从耻骨联合上一侧向头端以30度角刺入腹腔(应避开膀胱)。
可先刺入皮下2~3mm,再刺入腹腔,以防药液外漏。
针头刺入部位不宜太高太深,以免刺破内脏。
注射量一般为0.1~0.25ml/10g。
c.皮下注射法
一般两人合作。
一人左手抓住小鼠头部皮肤,右手拉住鼠尾;另一人左手提高背部皮肤,右手持住注射器(针头号同上),将针头刺入提起的皮下。
若一人操作,左手小指和手掌夹住鼠尾,拇指和食指提起背部皮肤,右手持注射器给药。
一般用量为0.05~0.25ml/10g。
d.肌肉注射法
两人合作时,一人抓鼠方法同上,另一人左手拉直一侧后肢,右手持注射器,注射部位多选后腿上部外
侧(针头号同上)。
如一人操作,抓鼠方法类似腹腔注射,只是药液注射在肌肉内。
每腿的注射量不宜超过0.1ml。
e.尾静脉注射法
将小鼠置于待置的固定筒内,使鼠尾外露,并用酒精或二甲苯棉球涂擦,或插入40℃~50℃温水中浸泡片刻,使尾部血管扩张。
左手拉尾,选择扩张最明显的血管;右手持注射器(4~5号针头),将针头刺入血管,缓慢给药。
如推注有阻力而且局部变白,说明针头不在血管内,应重新插入。
穿刺时宜从近为尖部1/3处静脉开始,以便重复向上移位注射。
一般用药量为0.1~0.2ml/10g,不宜超过0.5ml/10g。
二、家兔的捉持和给药方法
1、捉持方法
一般左手抓住兔颈背部皮肤,将其提起,右手托住臀部称坐位姿态。
不要抓两耳,以防兔挣扎。
2、给药方法
a.耳缘静脉注射法
一人操作时,将兔放入固定箱或试验台上,选好耳缘静脉(在耳背的下缘),拔除局部的毛,用酒精棉球涂擦,并用食指轻弹耳壳,使血管扩张。
用左手的食指和中指夹住耳根部,拇指和无名指夹住耳尖部拉直;右手将抽好药液的注射器(6~7号针头)刺入血管,用拇指和食指使针头和兔耳固定,将药液推入。
如针头在血管内,推注轻松,并可见血液被药液冲走;如不在血管内,则推注有阻力,耳局部变白或肿胀,应立即拔除重新注射。
注射完毕,则用手指或棉球压在针眼上,再拔出针头,并继续按压片刻,防止出血。
如两人操作,一人夹住兔子,右手暴露血管,压住耳根部使血管充盈,另一人注射给药。
两人合作,一人坐下,两腿夹住兔身,左手固定兔耳,右手抓住前肢;另一人将开口器从嘴角插入口腔,压在舌上,并向后翻转几下,使兔舍伸直。
取8号导尿管由开口器中部的小孔插入食道约15cm。
如插入气管,兔子则剧烈挣扎、呼吸困难。
也可将导尿管外端浸入水中,不见气泡则表示插在胃中。
插好后,把注射器接在导尿管上,将药液推入。
再注入少量空气,使导尿管中所有药液进入胃内。
灌完药液后,先慢慢抽出导尿管,再取出开口器。
一般用药量为5~20ml/┧。
c.腹腔、肌肉、皮下注射法
基本同小白鼠,唯针头可稍大(6~7号),给药量可稍多,一般腹腔为1.0~5.0ml/┧,肌肉、皮下为0.5~1.0ml/┧。
d.眼结合膜内给药法
将兔固定在兔箱内或夹在腋下,左手拇指和食指拉开兔下眼睑成杯状,中指压住眼内眦,以防药液由鼻泪管流入鼻腔内而被吸收。
滴入药液1~2滴,将下眼睑向上合拢,使眼球充分接触药液。
约1min后将手放开,让药液自然流出。
e.家兔眼睑滴加药液方法。
三、大白鼠的捉持和给药方法
1、捉持方法
大白鼠比小白鼠攻击性强,不要突然袭击去抓它,以免被咬伤。
捉持前先戴上手套,右手夹住尾巴,放在粗糙面上;左手拇指和食指捏住颈及前颈部,其余三指握住整个身体。
有力适当,过松容易挣脱而被咬伤,但用力过大会使其窒息死亡。
类似于小白鼠,只是工具和用药量大点,静脉给药除尾静脉注射外还可舌下静脉给药。
四、豚鼠的捉持和给药方法
1、捉持方法
豚鼠性情温和,可直接用左手抓住身体即可,或以左手抓住其头颈部,右手抓住两后肢。
2、给药方法
皮下、肌肉及腹腔注射方法与小白鼠类似,只是用药量稍大。
灌胃方法与兔类似。
静脉注射方法与兔相似,可选后脚掌外侧静脉、外颈部静脉、或作股静脉切开注射。
作后脚掌外侧静脉注射时,有一人捉豚鼠并固定一条后腿,另一人剪去注射部位的毛,用酒精棉球涂擦后脚掌外侧的皮肤,使血管显露。
再将连在注射器上的小儿头皮静脉输液针头刺入血管。
作外颈静脉注射时需先剪去一点皮肤,使血管暴露,然后将针头刺入。
豚鼠的静脉灌壁比较脆弱,操作时需特别小心。
