分析化学作业(第十四章)参考答案
第十四章 胶体分散系统和大分子溶液.

第十四章胶体分散系统和大分子溶液一、选择题1. .以下说法中正确的是:( ) A通过超显微镜能看到胶体粒子的大小和形状;B溶胶和真溶液一样是均相系统;C溶胶能产生丁铎尔效应;D溶胶在热力学和动力学上都是稳定系统。
2.溶胶的基本特性之一是( ) A热力学上和动力学上皆属于稳定系统;B热力学上和动力学上皆属于不稳定系统;C热力学上不稳定而动力学上属于稳定系统;D热力学上稳定而动力学上属于不稳定系统。
3外加直流电场于胶体溶液,向某一电极作定向移动的是:( ) A胶粒;B胶核;C胶团;D紧密层4.区别溶胶与真溶液和悬浮液最简单灵敏的方法是:( ) A乳光计测定粒子浓度; B观察丁铎尔效应;C超显微镜测定粒子大小;D观察ζ电位。
5.工业上为了将不同蛋白质分子分离,通常采用的方法是利用溶胶性质中的: ( ) A电泳;B电渗;C沉降;D扩散。
6.当溶胶中加入大分子化合物时:( ) A一定使溶胶更稳定;B一定使溶胶更容易为电解质所聚沉;C对溶胶稳定性影响视加入量而定;D对溶胶稳定性没有影响。
7.对于Donnan平衡,下列哪种说法是正确的:( ) A膜两边同一电解质的化学位相同;B膜两边带电粒子的总数相同;C膜两边同一电解质的浓度相同;D膜两边的离子强度相同。
8.Donnan平衡产生的本质原因是:( ) A溶液浓度大,大离子迁移速度慢;B小离子浓度大,影响大离子透过半透膜;C大离子不能透过半透膜,且因静电作用使小离子在膜两边的浓度不同;D大离子浓度大,妨碍小离子通过半透膜。
9.对大分子溶液发生盐析的现象,不正确的说法是:( ) A加入大量电解质才能使大分子化合物从溶液中析出;B盐析过程与电解质用量无关;C盐析的机理包括电荷中和和去极化两个方面;D电解质离子的盐析能力与离子价态关系不大。
10.有关胶粒ζ电势的叙述中,下列说法不正确的是:( )A正比于热力学电势φ;B只有当固液相对运动时,才能被测定;C与胶粒的扩散速度无关;D不能利用能斯特公式计算。
苏州大学物理化学考研、期末考试复习-第十四章 胶体分散体系和大分子溶液练习题及答案

第十四章胶体分散体系和大分子溶液练习题一、选择题2.对于有过量KI存在的AgI溶液,电解质聚沉能力最强的是:()(A)K3[Fe(CN)6](B)MgSO4(C)FeCl3(D)NaCl3.在大分子溶液中加入大量的电解质,使其发生聚沉的现象称为盐析,产生盐析的主要原因是:()(A)电解质离子强烈的水化作用使大分子去水化(B)降低了动电电位(C)由于电解质的加入,使大分子溶液处于等电点(D)动电电位的降低和去水化作用的综合效应4.(1)在晴朗的白昼,天空呈蔚蓝色的原因是:()(2)日出和日落时,太阳呈鲜红色的原因是:()(A)蓝光波长短,透射作用显著(B)蓝光波长短,散射作用显著(C)红光波长长,透射作用显著(D)红光波长长,散射作用显著5.关于电动电位描述正确的是:()(A)电动电位是恒定不变的(B)电动电位是胶核与介质间的电位差(C)电动电位是可以粗略地看成吸附层与扩散层间的电位差(D)电动电位仅与吸附的离子浓度有关7.在分析化学上,有两种利用光学性质测定胶体溶液浓度的仪器,一是比色计,另一个是比浊计,分别观察的是胶体溶液的:()(A)透射光;折射光(B)散射光;透射光(C)透射光;反射光(D)透射光;散射光8.向FeCl3(aq)中加入少量氨水,可制备稳定的氢氧化铁溶胶,此时胶体粒子带电荷情况为:()(A)总是带正电(B)在pH较大时带正电(C)总是带负电(D)在pH较大时带负电9.对于Helmholz紧密双电层模型,下列描述中不正确的是:()(A)带电的固体表面和带相反电荷的离子构成平行的两层,称为双电层(B)此双电层距离约等于离子半径,如同一个平板电容器(C)在此双电层内,热力学电势φ0呈直线下降(D)由于模型上的缺陷,此双电层模型不能说明电泳现象10.用三氯化铝AlCl3水解制备的氢氧化铝溶胶,哪种物质聚沉能力最强?()哪种物质聚沉能力最弱?()(A)Na2SO4(B)MgCl2(C)La(NO3)3(D)K4[Fe(CN)6]二、填空题11.超离心沉降分为两种方法:(1)沉降平衡法,它是_______________平衡(2)沉降速度法,它是________________平衡12.界面吉布斯自由能和界面张力的相同点是不同点是。
华中师范大学等六校合编《分析化学》(下册)笔记和课后习题(含考研真题)详解-第十四章至第十六章【圣才

第十四章极谱法与伏安法14.1复习笔记一、极谱分析法的基本原理1.极谱法的装置图14-1极谱分析基本装置1—储汞瓶2—汞3—塑料管4—毛细管5—试液6—电解容器7—甘汞电极2.极谱波的形成(1)极谱波极谱波是指当外加电压变化,使被测溶液中某物质能在滴汞电极上发生还原或氧化时,记录下的电流-电压关系的曲线。
图14-2镉离子极谱图(2)极谱波的形成①残余电流部分(AB);②电流上升部分(BC);③极限电流部分(CD)。
(3)定量分析的基础——极限扩散电流极限扩散电流是指在排除了其他电流的影响后,极限电流减去残余电流后的值;i d与被测物的浓度成正比。
(4)定性分析的依据——半波电位半波电位是指当电流等于极限扩散电流的一半时相应的滴汞电极电位,符号为E1/2。
3.极谱过程的特殊性(1)电极的特殊性①极谱法的基础必须使滴汞电极在电解过程中完全极化,电流密度要小。
②滴汞电极的优点a.电极表面吸附杂质少,数据重现性好;b.在酸性溶液中可进行极谱分析;c.金属与汞形成汞齐使金属离子更易电解析出;d.汞易提纯。
③滴汞电极的缺点a.汞易挥发且有毒;b.不能用于比甘汞电极正的电位;c.残余电流较大,限制了其测定的灵敏度。
(2)电解条件的特殊性①溶液保持静止,对流切向运动可以忽略不计;②使用大量的支持电解质,电子迁移运动可以被消除。
二、极谱定量分析1.扩散电流方程式(1)Ilkovic方程式中,i d为平均极限扩散电流(μA),z为电子转移数,D为扩散系数(cm2·s-1),m为汞滴流量(mg·s-1),t为测量时,汞滴周期时间(s),c为待测物浓度(mmol·L-1)。
(2)极谱定量分析方法的类型①标准曲线法②标准加入法③直接比较法在相同实验条件下,分别测定已知浓度为c s的标准溶液与未知试液的扩散电流。
2.影响扩散电流的主要因素(1)溶液组分的影响组分不同,溶液黏度不同,因而扩散系数D不同。
分析化学习题十四

第十四章荧光分析法一、单项选择题(类型说明:每一道试题下面有A、B、C、D四个备选答案,请从中选择一个最佳答案。
)1、下列哪种化学反应可以产生化学发光?()A.中和反应 B.离子交换反应 C氧化反应 D置换反应2、分子荧光与化学发光均为第一激发态的最低振动能级跃迁至基态中各振动能量能级产生的光辐射,它们的主要区别在于()A.分子中的电子层不同B.跃迁至基态中的振动能级不同C.产生光辐射的能源不同D.无辐射驰豫的能源不同3、受激单线态的平均寿命应为()秒。
A.10-8 B.10-7 C.10-6 D.1受激三线态的平均寿命应为()秒。
A.10-8 B.10-7 C.10-6 D.10-55、下列那种离子不能产生荧光?()A. B.2+ C.3+ D.V()6、根据下列化合物的结构,判断那种物质的荧光效率最大?()A.苯B.联苯C.对联三苯D.蒽7、下列结构中那一种能产生荧光的强度最大? ( )A.苯酚B.苯C.硝基苯D.苯甲酸8、苯胺在下列哪个值能产生荧光(苯胺以分子形式产生荧光) ( )A.1B.2C.7D.139、下列那种说法是正确的 ( )A.荧光物质的浓度增加,荧光强度增大。
B. 荧光物质的浓度增加,荧光强度减弱。
C. 荧光物质的浓度减弱,荧光强度减弱。
D. 荧光物质的浓度减弱,荧光强度减弱。
10、下列说法那种是正确的 ( )A.溶液温度升高,荧光效率增加,荧光强度增大。
B.溶液温度降低,荧光效率增加,荧光强度增大。
C.溶液温度升高,荧光效率降低,荧光强度增大。
D.溶液温度降低,荧光效率降低,荧光强度增大。
11、下列那种基团能使单线态转让三线态 ( )A. 2NH -B. OH -C. 65C H -D. I -12、下列那种溶剂对荧光的光谱干扰最小 ( )A.水B.乙醇C.环已烷D.四氯化碳13、荧光光度计和分光光度计的主要区别是 ( )A.光源B.光路C.单色器D.检测器瑞利散射是在那种情况下产生的 ( )A.自发辐射B.受激辐射C.辐射能照射分子产生热运动D. 光子和物质分子发生弹性碰撞,只是光子运动方向发生了改变15、拉曼散射是在那种情况下产生的 ( )A.自发辐射B.受激辐射C.辐射能照射分子产生热运动D.辐射能照射分子产生非弹性碰撞,并发出光辐射。
无机及分析化学第十四章 光谱法课后练习与答案

第十四章 光谱法紫外-可见分光光度法一.选择题1.CuSO 4溶液呈蓝色,是由于CuSO 4溶液选择性地吸收了白光中的( ) 。
A .紫色光B .绿色光C .黄色光D .蓝色光2.用吸光光度法测得某溶液的透光率为T 0,若将该溶液稀释一倍,则此时溶液的透光率为( ) 。
A .20T B .0T C .02T D .20T3.分光光度法的吸光度与下列哪个因素无关( ) 。
A .溶液的浓度B .入射光的波长C .液层厚度D .液层的高度4.吸光度A 为0时,透光率T 为( ) 。
A .0B .10C .100%D .20%5.某溶液在某波长处测得A 为0.22,若浓度增加一倍,比色皿厚度减为原来的一半,则吸光度变为( )。
A .0.44B .0.22C .0.66D .0.116.现测定A 、B 两个不同浓度的某溶液,若A 比色皿的厚度为1cm,B 比色皿的厚度为2cm,测得两溶液的吸光度相同,则AB 浓度关系为( ) 。
A .B A c c = B .B A c c 2=C .B A c c =2D .B A c c 31= 7.分光光度法中,吸光系数与( )有关。
A.光的强度B.溶液的浓度C.入射光的波长D.液层的厚度 8.摩尔吸光系数很大,则说明( )。
A.该物质的浓度很大B.光通过该物质溶液的光程长C.该物质对某波长光的吸收能力强D.测定该物质的方法的灵敏度低 9.符合比耳定律的有色溶液稀释时,其最大的吸收峰的波长位置( )。
A.向长波方向移动B.向短波方向移动C.不移动,但峰高降低D.无任何变化 10.分光光度计测定中,工作曲线弯曲的原因可能是( )。
A 、溶液浓度太大 B.溶液浓度太稀C.参比溶液有问题D.仪器有故障11.在分光光度法中运用光吸收定律进行定量分析,应采用()作为入射光。
A.白光B.单色光C.可见光D.锐线光12.可见分光光度法中,使用的光源是()。
A 钨丝灯B 氢灯C氘灯D汞灯三、判断题1.溶液的浓度越大,则该溶液的吸光系数越小;比色皿厚度越小,则吸光系数越大。
无机及分析化学习题精选及答案

无机及分析化学习题及答案精选xxx科技大学第十四章分析化学基础1.对某组分的含量进行测定时,若被分析样品的质量大于100mg,则该分析方法属于( )A. 常量分析B. 半微量分析C. 微量分析D. 超微量分析2.对某溶液中的铝进行测定时,若取分析试液25ml进行分析测定,则该分析方法属于( )A. 常量分析B. 半微量分析C. 微量分析D. 超微量分析3.由精密度好就可断定分析结果可靠的前提是( )A. 偶然误差小B. 系统误差小C. 标准偏差小D. 相对偏差小4.下列各种分析纯的化学试剂,其中不能用直接配制法配制标准溶液的是A. KHCO3B. KMnO4C. K2CrO7D. KCl5.下列各种措施中,可以减小偶然误差的是( )A. 进行空白试验B. 进行对照试验C. 进行仪器校准D. 增加平行测定次数6.下述情况引起的误差中,不属于系统误差的是( )A. 移液管转移溶液之后残留时稍有不同B. 称量时使用的砝码锈蚀C. 滴定管刻度未经校正D. 天平的两臂不等长7.下列叙述中错误的是()A.系统误差呈正态分布 B. 系统误差又称可测误差C. 方法误差属于系统误差D. 系统误差具有单向性8. 分析测定中出现下列情况,何者属于系统误差( )A. 滴定时有溶液溅出B. 试样未经充分混匀C. 滴定管未经校正D. 读错法码9. 下列计算式的计算结果(X)应有几位有效数字?( )X= [0.3120⨯48.12⨯(21.65-16.10)]÷(1.2845⨯1000)A. 二位B. 三位C. 四位D. 五位第 1 页10. 欲测某组分含量,由四人分别进行测定,试样称取量皆为2.2g,问下列结果中哪一个是合理的?( )A. 2.085%B. 2.08%C. 2.09%D. 2.1%11. 称取一定质量的邻苯二甲酸氢钾基准物质以标定NaOH溶液的浓度,下列何者将引起正误差( )A. 称取基准物重量时用的一只10mg法码,事后发现其较正后的值为9 .7mgB.滴定时滴定终点在等量点后到达。
有机化学-第14章 习题解答
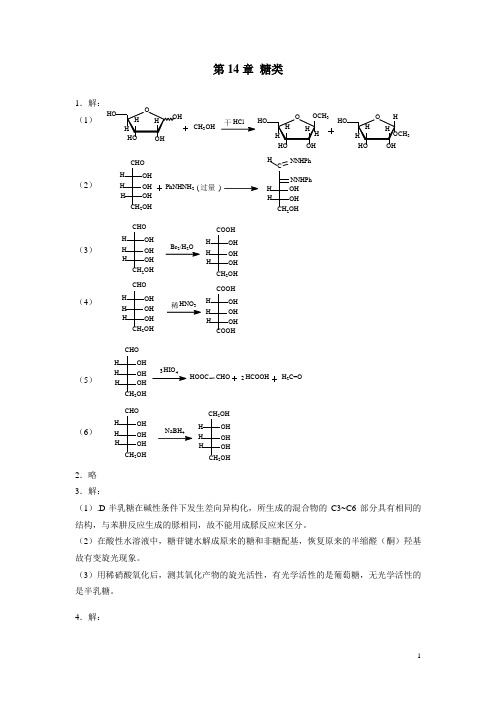
6.解:
7.解:
葡萄糖二酸(D或L构型)
8.解:
海藻糖4-O-(α-D-吡喃葡萄糖基)-α-D-吡喃葡-吡喃葡萄糖
异海藻糖4-O-(α-D-吡喃葡萄糖基)-β-D-吡喃葡萄糖
9.解:
蜜二糖蜜二糖酸
2,3,4,5-四-O-甲基-D-葡萄糖酸2,3,4,6-四- O-甲基-D-半乳糖
10.解:
11.解:
(1)A与B互为对映体;
(2)A与C、D;B与C、D互为非对映体;
(3)A与D;A与C互为差向异构体。
(3)用稀硝酸氧化后,测其氧化产物的旋光活性,有光学活性的是葡萄糖,无光学活性的是半乳糖。
4.解:
(1)
(2)
5.解:
(1)用Fehling(Benedict)或Tollens试剂,生成砖红色沉淀或银镜的是葡萄糖;
(2)用溴水,使溴水褪色的是葡萄糖;
(3)用Fehling(Benedict)或Tollens试剂,有砖红色沉淀或银镜生成的是麦芽糖。
第14章糖类
1.解:
(1)
(2)
(3)
(4)
(5)
(6)
2.略
3.解:
(1).D-半乳糖在碱性条件下发生差向异构化,所生成的混合物的C3~C6部分具有相同的结构,与苯肼反应生成的脎相同,故不能用成脎反应来区分。
(2)在酸性水溶液中,糖苷键水解成原来的糖和非糖配基,恢复原来的半缩醛(酮)羟基故有变旋光现象。
分析化学第14章核磁共振波谱法

第十四章 核磁共振波谱法
仪器分析
为了提高单位时间的信息量,可采用多道发射 机同时发射多种频率,使处于不同化学环境的核 同时共振,再采用多道接收装置同时得到所有的 共振信息。例如,在100MHz共振仪中,质子共振 信号化学位移范围为10时,相当于1000Hz;若扫 描速度为2Hz∙s1,则连续波核磁共振仪需500s才 能扫完全谱。而在具有1000个频率间隔1Hz的发射 机和接收机同时工作时,只要1s即可扫完全谱。 显然,后者可大大提高分析速度和灵敏度。
仪器分析
图14-4
原子核的进动
第十四章 核磁共振波谱法
仪器分析
)与外加磁场强度(H0)的 进动频率(
关系用Larmor方程来说明:
H0 2
—— 磁旋比
第十四章 核磁共振波谱法
仪器分析
1H 的
2.67519 10 T S
8 -1
-1
H0 = 1.4092 T (Tesla)
第十四章 核磁共振波谱法
仪器分析
脉冲傅里叶变换共振仪是用一个强的射频,以脉冲 方式(一个脉冲中同时包含了一定范围的各种频率 的电磁辐射)将样品中所有化学环境不同的同类核 同时激发,发生共振,同时接收信号。而试样中每 种核都对脉冲中单个频率产生吸收。为了恢复平衡, 各个核通过各种方式驰豫,在接受器中可以得到一 个随时间逐步衰减的信号,称自由感应衰减( FID) 信号,经过傅里叶变换转换成一般的核磁共振图谱。 脉冲傅里叶变换共振实验脉冲时间短,每次脉冲的 时间间隔一般仅为几秒。许多在连续波仪器上无法 做到的测试可以在脉冲傅里叶变换共振仪上完成。
弛豫过程所需的时间用半衰期 T1 表示,
T1 是高能态寿命和弛豫效率的量度,T1
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
14-1 填充柱气相色谱分析某试样,柱长为1 m 时,测得A 、B 两组分的保留时间分别为5.80 min 和6.60 min ,峰底宽分别为0.78 min 和0.82 min.,死时间为1.10 min ,试计算以下各项(1)载气的平均线速度;(2)组分B 的分配比;(3)组分A 的有效塔板数;(4)选择性因子;(5)分离度;(6)条件不变情况下,A 、B 完全分离时所需的柱长。
解:(1)10min m 91.010.1/1t /L u -⋅===
(2)00.510
.110
.160.6k B =-=
(3)()()()58178.010.180.516A W t A t 16A n 2
2
0r eff =⎪
⎭⎫ ⎝⎛-⨯=⎪⎭
⎫ ⎝⎛-⨯=
(4)()()17.110
.180.510
.160.6A t B t 'r 'r =--==α
(5)()
0.178
.082.080.560.62R =+-⨯=
(6)m 25.20.10.15.1L 2
5.1=⋅⎪⎭
⎫ ⎝⎛=
14-2 已知组分A 和B 的分配系数分别为7.6和9.3,当它们通过相比β=90的填充柱时,能否达到基本分离?(基本分离时R=1.0)
解:2.16.7/3.9K /K A B ===α;10.090/3.9/K k B B ==β=
6969610.010.0112.12.1116k k 11R 16n 2
22
2
B B 2
2=⎪
⎭
⎫ ⎝⎛+⨯⎪⎭⎫ ⎝⎛-⨯⨯=⎪⎭⎫ ⎝⎛+⋅⎪⎭⎫ ⎝⎛-αα⋅= 填充柱柱长最多5 m (通常为2 m ),单位长度塔板数为1500/m ,因此无法达到这样的柱效,因此在上述条件下,不能实现分离。
(计算柱效时,用A 的分配比也行,本来就是估算)
14-3 某组分在一2 m 长的色谱柱上的分配比为3.0,若载气流速为28 cm ⋅min -1,请问在理想状态下20 min 后该组分柱中的位置(即谱带中心距进样端的距离)以及该组分流出色谱柱所需时间(以色谱峰值所对应的时间表示)。
解:100r min cm 70.3128
k 1u u u L u L
u L
t t t k -⋅=+=+=⇒-
=-=载气组分载气
载气组分
20 min 时,组分移动了20⨯7=140 cm (即距进样端140 cm )
该组分流出色谱柱的时间:t=L/u 组分=200/7=28.6 min
14-4 长度相等的两根色谱柱,其Van Deemter 常数如下:
(1)若载气流速为0.50 cm ⋅s -1,则哪根柱子的理论塔板数大?(2)柱1的最佳流速为多少? 解:(1)H 1=0.18+0.40/0.50+0.24⨯0.50 =1.1cm
H 2=0.05+0.50/0.50+0.10⨯0.50=1.1 cm 相等 (2)1111opt s cm 3.124.0/40.0C /B u -⋅===
14-5 用柱长为2 m ⨯2.0 mm 的色谱柱分离乙酸甲酯、丙酸甲酯和正丁酸甲酯。
它们的峰面积分别为18.1、43.6、29.9,相对质量校正因子分别为0.60、0.78、0.88,试计算丙酸甲酯的质量分数。
解:%78.47%1009
.2988.06.4378.01.1860.06
.4378.0w =⨯⨯+⨯+⨯⨯=丙酸甲酯
14-6 用内标法测定乙醛中水分的含量,以甲醇为内标。
称取0.0213g 甲醇加到4.586g 乙醛试样中进行色谱分析,测得水和甲醇的峰面积分别为150和174(具体单位与计算无关,因此忽略)。
已知水和甲醇的相对校正因子分别为0.55和0.58,计算乙醛中水分的含量。
解:%38.0%100586
.417458.0150
55.00213.0m A f A f m m m w s
OH CH OH CH O H O H OH CH s
O H O H 3322322=⨯⨯⨯⨯
=
⨯⋅⋅⨯=
=
14-7 为了测定一混合样品中的间苯二甲酸的含量,首先应了解样品的性质。
该样品大致含有间苯二甲酸和对苯二甲酸,还有一些不明的其它杂质。
现在称取样品0.3578 g ,内标癸二酸0.1029g 。
将样品衍生化,使其中的酸转化为相应的甲酯,然后进行分析。
测得间苯二甲酸二甲酯和癸二酸二甲酯的峰面积分别为23.7单位和24.5单位,已求得这两种酯的定量校正因子为0.77和1.00。
试问:(1)间苯二甲酸的质量分数;(2)为什么要将样品预先进行衍生化?(间苯二甲酸、癸二酸、间苯二甲酸二甲酯、癸二酸二甲酯的分子量分别为166、202、194、230)(此题暂不强求,有经理同学可尝试做一下)
%9.20%1003578
.05.2400.1202230
1029.07.2377.0194
166m A f m m m A f m m m m %w s
s s X x x
=⨯⨯⨯⨯
⨯⨯⨯=⋅⋅⋅⋅⋅==
试样
癸二酸
癸二酸二甲酯间苯二甲酸二甲酯间苯二甲酸
试样
气相色谱适合测定沸点低、极性小的且热稳定性高的试样。
间苯二甲酸的极性大且挥发性差,直接进样需较高柱温且易形成拖尾峰,导致分离效果变差。
酯化后极性变小、挥发性增强,分离效果变好。
