中国抗结核病药品管理评价过程介绍
实施抗结核药品统管是加强结核病归口管理的有效途径之一

责任 书 , 实行抗 结 核 药 品 统 管一 票 否 决 制 度 。 明确 规定 各级 医疗卫 生单 位 除不 能擅 自销 售使用 抗结 核
药 品 外 , 核 病 人 或 可 疑 结 核 病 人 向 当 地 结 防 机 构 结
广泛 宣 传的基 础 上 , 得 市政 府 对 结 核 病 防治 工作 取
表现 好 的单位进 行 表彰 。该措 施 的实 施保证 了结 核
病人 归 口管理 的落 实 。 实 行 目标 管 理 是 加 强 结 核 病 归 口管 理 的 有 效 措 施 各 级 卫 生 局 每 年 与 医 疗 卫 生 单 位 签 订 目标 管 理
实 施 抗 结 核 药 品 统 管 的 关 键 我 们在通 过 电 台 、 电视 台 、 纸 等 新 闻 媒 介 进 行 报
为 充分 发挥各 级结 核 病 防治机 构 的业 务指 导作 用 , 政府 发文 授 权 各 级结 防 机 构享 有 传 染 病 管 理 市
执 法 监 督 权 。 在 此 基 础 上 , 们 充 实 建 立 并 培 训f 我 了 各 级 结 核 病 防 治 执 法 监 督 队 伍 。 市 级 结 防 机 构 设 置 了5 ~6名 执 法 监 督 员 , 级 设 置 3~ 县 4名 , ( ) 乡 镇 设 置 2 ~3名 执 法 监 督 员 , 对 结 核 病 疫 情 报 告 、 转 、 除 诊
病 药 品 。对 违 反 者 , 通 报 批 评 外 , 收 其 抗 结 核 药 除 没 品 并 处 以罚 款 要 求 各 级 各 类 医 疗 卫 生 机 构 发 现 结
步 落实 。
实 施 效 果 和 评 价
核病人或 疑似结 核病人 , 必须转 至 当地结 防机构 正规 治疗管理 , 切实落 实结核病归 口管理 工作 。 各级 结核 病 防治 机构 的检 查 督促
抗结核药品议价综合评审标准

企业生产规模(9分)
销售额(5分)
年度销售额≥10亿得5分,5亿≤年度销售额<10亿得3.5分,1亿≤年度销售额<5亿得2分,年度销售额<1亿得1分。
5
以2017年度企业增值税纳税报表中上缴增值税对应的销售金额对应相应分值。
行业排名(4分)
化学药品:1-50名(含50名)得4分,51-100名(含100名)得3分,101-200(含200名)得2分,其他得1分。
7
专家根据供应情况Байду номын сангаас定。
经营业绩(8分)
同类产品政府采购的省级合同,每份合同得1分,累计不超过8分,无合同者为0分。
8
根据申报人提供2016年以来的本公司签订的同产品政府财政预算资金采购的省级合同及验收报告为依据。合同出现字迹不清晰、缺页、无签字盖章者将按无合同处理。
合计
100
3.专家组认为申报人的报价明显偏低,可能存在质量和供应风险,不能诚信履约的,将进行综合评估,避免恶性竞争,确定其是否作为无效报价处理。
技术部分(22分)
样品测评(10分)
有效期>2年得5分,有效期=2年得4分,有效期=1.5年得3分,
有效期<1.5年不能参与本次采购。
5
根据所提供的样品说明书上的有效期评定。
生产材料、生产工艺先进性的证明材料。有得3分,无得0分。
3
药品质量抽检抽查情况(5分)
申报企业无生产环节抽检不良记录得5分,申报企业非报名品种有1次生产环节抽检不良记录得2分,申报企业非报名品种有2次以上(含2次)生产环节抽检不良记录得0分。
5
以2016年以来国家食品药品监管总局发布的国家药品质量公告和重庆市食品药品监管局监督抽验结果或记录为依据,可由企业提供并进行承诺。
肺结核患者健康管理服务项目绩效考核指标体系及评分细则

宣传教 开展宣传活动及 育情况 讲座
1.开展结核病宣传讲座或宣传活动;2.组织开展 3.24肺结核宣传活动。
1.有开展宣传讲座或者宣传活动得2分,未开展不得分,材料整理齐全得2分,缺1项扣 8 0.5分。 2.组织开展3.24宣传活动2分,未开展不得分,活动材料(包括活动通知,照
片、小结)整理齐全2分,缺1项扣0.5分。
总分
100
标、具体措施、时间安排、责任人等内容)有计划且完整得4分,无不得分,缺1项扣
0.5分;有工作总结(内容含有工作目标完成情况、采取具体措施、存在问题、下步打
算等方面进行总结)有总结且完整得4分,无不得分,缺1项扣0.5分。
2.上级通知应管理人数 ,实际管理人数 未管理人数管理人数/上级通知应管理人数×100%)肺结核患者管理率
33
本信息,既往史,生命体征,身高体重等内容)真实6分,不真实每份扣2分,扣完为止 。
3.有中断治疗追踪反馈信息登记表得3分,漏登记1例扣1分,扣完为止。
4.加强学生群体肺结核病人管理,发现在校生患有结核病的需告知其所在学校负责人,
有告知得2分,无不得分;同时做好相关记录及追踪、督导服药、随访管理工作,有记
录得2分,无不得分。
1.有病例转诊/追踪信息登记汇总表且填写完整得4分,漏登记1例扣1分,扣完为止。
2.随机抽查3份已网报的病例核实其原始诊断材料,一致 份,不一致 份,不一致原
因
,完全一致得3分,不一致每份扣1分
3.推介转诊病例有转诊单得2分,少1份扣1分,扣完为止
15 4.应转诊人数 ,已转诊人数 ,到位人数 ,本月转诊到位率 %,应追踪人数
抗结核治疗疗效评估及停药标准

抗结核治疗疗效评估及停药标准英文回答:Assessing the efficacy of anti-tuberculosis treatment and determining when to stop treatment are crucial aspectsof tuberculosis management. In order to evaluate the effectiveness of treatment, various parameters are considered, including clinical improvement, radiological findings, and bacteriological conversion.Clinical improvement is assessed by monitoring the patient's symptoms, such as cough, fever, and weight loss.If these symptoms gradually improve or completely disappear, it indicates a positive response to treatment. For example, I personally experienced persistent cough and weight loss before starting tuberculosis treatment. After a few weeksof treatment, my cough gradually diminished, and I started gaining weight, which showed that the treatment was effective.Radiological findings play a significant role in assessing treatment response. Chest X-rays or CT scans are commonly used to evaluate the extent of lung involvement and monitor any changes over time. The disappearance or reduction of lung lesions on imaging studies is an indication of treatment efficacy. For instance, my chest X-ray showed multiple nodules and infiltrates before starting treatment. After a few months of treatment, a follow-up X-ray revealed a significant reduction in the size and number of these abnormalities, confirming the effectiveness of the treatment.Bacteriological conversion is another important criterion for evaluating treatment efficacy. Sputum samples are collected and tested for the presence of acid-fast bacilli (AFB) using smear microscopy or culture methods. Negative conversion of sputum smears and cultures indicates a successful response to treatment. For example, my sputum smears initially showed numerous AFB before treatment. However, after a few weeks of treatment, the follow-up smears were negative for AFB, indicating a favorable response to the medication.In addition to assessing treatment efficacy, it is crucial to determine when to stop anti-tuberculosis treatment. The World Health Organization (WHO) provides guidelines for discontinuing treatment based on specific criteria. These criteria include completing the recommended duration of treatment, having a negative sputum culture at the end of the intensive phase, and showing clinical improvement. For example, if a patient completes the full course of treatment, has negative sputum cultures, and shows significant clinical improvement, it is usually safe to stop the medication.中文回答:抗结核治疗的疗效评估和确定停药时间是结核病管理的关键方面。
绩效考核结核病内容和方法资料讲解

(5)到2010年,项目地区发现的耐多药结核病人接受治疗 率达90%;
(6)到2010年,项目地区符合抗病毒治疗的结核/获得性 免疫缺陷病毒双重感染病人,其接受治疗率达80%以上;
(7)到2010年,项目地区流动人口肺结核病人的接受治疗 率达90%以上;
(8)到2010年,村医生结核病防治技术培训率达90%;
(9)到2010年,全民结核病防治知识的知晓率达80%。
2020/8/4
3
疾病预防控制机构绩效评估指标(县级)
指标 新涂阳病人发现率 病人系统管理率 新涂阳病人治愈率 医疗机构病人报告率 病人转诊率
指标要求 ≥70% ≥95% ≥85% ≥95% ≥95%
资料收集途径 A+D A+D A+D A+D A+D
核查规律服药,应该核查病人治疗记录卡,统计强 化期和全疗程的各自服药次数,一项达不到即为非 系统管理;根据病历记载统计督导管理服药的次数, 达不到90%者,即为非系统管理。
2020/8/4
11
四、医疗机构结核病人报告率(市县指标 95%)
定义:指一定期间内某辖区医疗机构网络报告的肺 结核病人和疑似肺结核病人数占其同期发现的肺结 核病人和疑似肺结核病人数的百分比。
结核病防治绩效考核 内容及方法
长治市疾病预防控制中心 李美蓉 2009.9.1
结核病有专门的评估体系 国际合作、中央转移支付等项目很多 国家有统一的要求 原则
– 以国家规划和技术方案为依据 – 结合项目管理的指标管理体系和结核病考核评估体系 – 可以用单项评估结果,符合绩效考核指标要求的直接
督导管理:即实际督导管理次数占应督导管理次 数的90%以上。
规则治疗:强化期和全疗程个体规则治疗率均在 90%以上,治疗转归为治愈、完成疗程、死亡、 失败、迁出的肺结核病人应视为进行了系统管理, 但不包括丢失、副反应停药等。
药品质量评估途径与流程

药品质量评估途径与流程1. 引言药品质量评估是确保药品安全和有效性的重要环节。
它旨在评估药品的制造过程和质量控制措施是否符合国家相关标准和规定。
本文将介绍药品质量评估的主要途径和流程。
2. 药品质量评估途径药品质量评估主要通过以下途径进行:2.1 药品注册申报药品注册是一种常用的药品质量评估途径。
在国家药品监管机构的指导下,药品生产企业将申报需要上市销售的药品,并提交相关的质量控制文件和检测报告。
国家药品监管机构将根据这些申报材料进行审评和审核,以确定药品是否符合质量要求。
2.2 药品抽样检验药品抽样检验是另一个重要的药品质量评估途径。
国家药品监管机构有权对市场上销售的药品进行定期抽样检验。
这些抽样检验可以包括对药品外观、含量、纯度等方面的检测,以确保药品质量符合标准要求。
2.3 药品生产企业评估对药品生产企业进行评估也是一种常用的药品质量评估途径。
国家药品监管机构可以对药品生产企业进行现场考察,评估其生产工艺、设备设施、质量管理体系等方面的情况,以确保药品生产过程中的质量控制措施符合要求。
3. 药品质量评估流程药品质量评估的流程通常包括以下步骤:3.1 提交申报材料药品生产企业需要将药品注册申报所需的材料提交给国家药品监管机构。
这些材料可以包括药品的质量控制文件、制造工艺描述、原辅材料的来源和质量要求等。
3.2 审评与审核国家药品监管机构将对药品注册申报材料进行审评与审核。
他们会评估药品的质量控制措施是否符合相关标准和规定,以及是否存在安全隐患和质量问题。
3.3 抽样检验在药品上市销售后,国家药品监管机构会对市场上的药品进行抽样检验。
他们会从市场中随机选择样品,并对样品进行检测,以确保药品质量与注册申报时一致。
3.4 生产企业评估国家药品监管机构可能会对药品生产企业进行现场考察和评估,以确保生产企业生产过程中的质量控制措施符合要求。
4. 结论药品质量评估途径包括药品注册申报、药品抽样检验和药品生产企业评估等。
中国抗结核病药品管理评价过程介绍

说明数据收集是为基线调查而不是来挑工 作中的问题。
•28
时间
每个省分为两个组,2个地市一组, 建议第一组在本次培训后的一周后开
始(6月27日),每个县约1天时间(含路 程),一个地市约1周,共2周时间。
建议第二组在本次培训后的两周后开 始(7月4日),同上安排,应该在7月15 日结束现场调查。
•3
•4
目的
提供抗结核药品管理的数据 寻找提高抗结核药品管理系统绩效的方法 寻找督导高质量的抗结核药品持续不间断
供应的方法 通过传授这种自我评估的技术,培养各级
开展抗结核病实施性研究的能力
•5
找出影响药品供应实施的需要优先解决的问题, 并指出下一步的活动。
通过横断面调查,为将来干预措施的评价收集基 线数据。
根据特定的数据收集表,标记可以采用确认标记 ,写上是或否,对回答画上圆圈、写上短语或句 子来解释一特定的结论。
这些指示很重要,因为录入数据或对结果编制表 格的人可能与最终完成表格的不是同一个人。
•41
在数据收集完成时,督导人员应对数据的完整性 和正确性进行检查。并注明已经检查的字样。
这一步骤非常有用,因为它将发现数据收集中的 任何问题并及时实施纠正措施以避免再次错误。
分发:包括办理交割手续、库存控制、库存管理 、药品运输到药品库房和结防机构。
使用:包括诊断、开具处方、分发药品和病人正 确服药。
•8
为什么要管理?
药品能挽救生命、促进健康 药品增进了人们对卫生服务的信任 药品昂贵 显著提高药品的管理通常是可行的 结核病的治疗需要几个月的时间,任何药
品供应的中断都很容易导致治疗失败和耐 药的产生
抗结核药品的需求测算与管理

抗结核药品的需求测算与管理引言结核病是一种严重威胁人民健康的传染病,也是目前全球范围内最大的传染病之一。
根据世界卫生组织的数据,每年约有1000多万人感染结核病,其中近150万人因此死亡。
抗结核药品是治疗结核病的关键工具,因此准确测算抗结核药品的需求并进行有效的管理至关重要。
本文将介绍抗结核药品需求测算的重要性,并提供一些测算和管理抗结核药品需求的方法和技巧。
1. 抗结核药品需求测算的重要性准确测算抗结核药品的需求对于保证患者的合理用药和公共卫生安全至关重要。
以下是几个重要原因:1.1 确保药物供应准确测算抗结核药品的需求可以帮助医疗机构和药品供应商根据患者的实际需求进行合理的药物采购和储备,避免供应短缺或荒废情况的发生。
1.2 控制耐药性的发展抗结核药物的滥用和不当使用是导致结核病耐药性发展的主要原因之一。
准确测算抗结核药品的需求可以帮助制定合理的用药指南和政策,降低结核病的耐药性风险。
1.3 优化资源配置准确测算抗结核药品的需求可以帮助医疗机构合理安排药品资源,提高资源利用效率,降低医疗成本。
2. 抗结核药品需求测算的方法下面介绍几种常用的抗结核药品需求测算方法:2.1 流行病学方法流行病学方法是一种基于流行病学数据分析的药品需求测算方法。
通过调查患者数量、流行病学特征、诊断和治疗方案等数据,结合数学模型和统计方法,可以较为准确地预测抗结核药品的需求量。
2.2 基于统计的方法基于统计的方法是一种基于历史用药数据分析的药品需求测算方法。
通过分析过去几年的结核病患者数量、用药情况和治疗周期等数据,结合时间序列分析和回归分析等统计方法,可以预测未来一段时间内抗结核药品的需求量。
2.3 专家咨询方法专家咨询方法是一种基于专家经验和专业知识的药品需求测算方法。
通过请教医学专家、流行病学专家和药学专家等,结合他们的经验和知识,可以获得较为准确的抗结核药品需求估计。
3. 抗结核药品需求管理的技巧以下是一些抗结核药品需求管理的技巧:3.1 建立监测系统建立一个抗结核药品需求监测系统是有效管理抗结核药品需求的第一步。
中国抗结核病药品管理评价过程介绍

2021/9/13
1
2021/9/13
DOTS STOPTB、GDF、GFATM、GLC 目标难于实现的原因:政府承诺和经费投
入、病人管理不当、抗结核药品短缺等 2000年,在美国国际发展署(USAID)
的支持下,推动药品合理化管理项目 (RPM Plus)制定了抗结核药品供应管理 系统评价手册。
2021/9/13
20
预算
食宿费 交通费 材料费 必要的补贴 参加培训费用
2021/9/13
21
抽样
1. 选择调查的省和地市 2. 选择调查的县 3. 选择调查的结, 国家结控中心决定选择选出宁夏、 河南、吉林、山东作为候选省,从中将选2个省 开展评估。
设计和计划干预措施 为经费预算和资源需求服务 改善监督系统和衡量干预措施的效果 不同的供应系统和国家之间的绩效比较
2021/9/13
10
相关机构
2021/9/13
世界卫生组织遏制结核的部门 参与结核病防治规划的国际合作伙伴和组织
(GDF、GFATM、GLC等) 卫生部决策者、国家结核病防治规划负责人 、制
王林、赖钰基、王倪和徐敏等四人承担, 王林为负责人。 必要时,另有3人:方群(办公室)、黄飞(监 测部)和刘二勇(培训部)将协助上述小组的工 作。
2021/9/13
18
2021/9/13
19
课题负责人1人(省级主管领导) 督导员2人(省级) 省和地市数据收集人员2人(省级) 县级数据收集人员4人(地市级)
40
在数据收集完成时,督导人员应对数据的完整性 和正确性进行检查。并注明已经检查的字样。
这一步骤非常有用,因为它将发现数据收集中的 任何问题并及时实施纠正措施以避免再次错误。
药物治疗效果评估及上报流程(干货)

药物治疗效果评估及上报流程(干货)药物治疗效果评估及上报流程 (干货)
目标
此文档旨在介绍药物治疗效果评估及上报流程,帮助医疗机构
和相关人员了解并正确执行该流程,以确保患者的治疗效果准确评
估和及时上报。
流程概述
1. 建立评估指标:医疗机构应根据药物治疗的特点和患者需求,制定明确的评估指标,如疗效评价标准、不良反应评估等。
2. 开展药物治疗:根据临床实际情况,医疗机构为患者开展药
物治疗,并记录相关信息,如药物种类、剂量、频次等。
3. 治疗效果评估:定期或治疗周期结束后,根据评估指标对患
者的治疗效果进行评估,包括疗效、症状改善情况等,并进行记录。
4. 不良反应评估:监测患者可能出现的药物不良反应,如过敏
反应、药物相互作用等,并及时记录和报告。
5. 效果上报:医疗机构应根据相关规定及时将患者的治疗效果
数据上报给上级医疗管理部门或相关研究机构,以便统计和研究。
注意事项
- 评估指标应尽可能客观、准确,并能反映患者的治疗效果。
- 治疗效果评估和不良反应评估应由专业医务人员进行,确保
评估结果准确可靠。
- 效果上报需遵循相关规定和流程,确保数据的可信性和保密性。
结论
药物治疗效果评估及上报流程对于医疗机构和患者的治疗管理
和研究具有重要意义。
医疗机构应根据该流程建立相应的管理机制,并加强培训与宣传,以确保流程的有效执行和数据的准确性。
以上为药物治疗效果评估及上报流程的简要介绍,希望对您有
所帮助。
药品质量评价途径与流程

药品质量评价途径与流程简介药品质量评价是确保药品安全和有效性的重要环节。
药品质量评价的目的是对药品进行全面、综合的评估,包括药品的质量、安全性和功效。
本文将介绍药品质量评价的途径和流程。
药品质量评价途径药品质量评价可以通过以下途径进行:1. 化学分析:通过对药品进行化学分析,确定药品的成分和含量是否符合标准要求。
化学分析是药品质量评价的基础,在药品研发、生产和质量控制过程中起着重要作用。
2. 生物学评价:通过对药品在生物体内的作用进行评估,确定药品的安全性和效果。
生物学评价可以包括体外实验、动物实验和临床实验等方法,以评估药品对生物体的影响和效果。
3. 传统药理学评价:对传统草药等药物进行药理学评价,通过对其化学成分和药理作用的研究,评估药物的质量和疗效。
4. 临床评价:通过对患者进行药物治疗的临床观察和评估,确定药品的疗效和安全性。
临床评价是药品质量评价的最终环节,也是药品上市前的必要步骤。
药品质量评价流程药品质量评价的流程通常包括以下步骤:1. 药品研发:药品质量评价始于药物的研发阶段,包括药物的合成、提取和制备等过程。
在这一阶段,需要对药物进行化学分析、生物学评价和传统药理学评价等。
2. 药品注册:药品的注册是药品质量评价的重要环节,需要提交药品质量评价报告和相关数据,申请药品注册。
注册机构会对药品的质量、安全性和疗效进行评估。
3. 药品生产:药品的生产需要严格按照质量管理体系执行,包括原材料的采购、生产工艺的控制、药品质量的监测和产品追溯等环节。
4. 药品监管:药品质量评价涉及药品监管部门的监督和管理,包括对药品生产企业、药品注册持有人和药品市场的监督检查。
5. 药品上市:经过质量评价和监管部门的审批,药品才能上市销售。
上市后仍需进行药品监测和不良反应监测等工作,确保药品的质量和安全性。
结论药品质量评价是保证药品安全和有效性的重要环节。
通过化学分析、生物学评价、传统药理学评价和临床评价等途径,对药品进行全面评估。
有关抗结核药物的质量
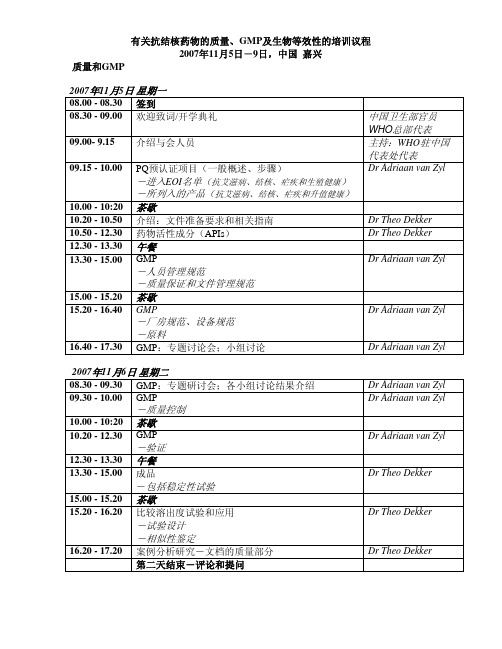
有关抗结核药物的质量、GMP及生物等效性的培训议程2007年11月5日-9日,中国嘉兴质量和GMP2007年11月5日星期一08.00 - 08.30签到08.30 - 09.00欢迎致词/开学典礼中国卫生部官员WHO总部代表09.00- 9.15介绍与会人员主持:WHO驻中国代表处代表Dr Adriaan van Zyl 09.15 - 10.00PQ预认证项目(一般概述、步骤)-进入EOI名单(抗艾滋病、结核、疟疾和生殖健康)-所列入的产品(抗艾滋病、结核、疟疾和升值健康)10.00 - 10:20茶歇10.20 - 10.50介绍:文件准备要求和相关指南Dr Theo Dekker 10.50 - 12.30 药物活性成分(APIs)Dr Theo Dekker 12.30 - 13.30 午餐Dr Adriaan van Zyl 13.30 - 15.00 GMP-人员管理规范-质量保证和文件管理规范15.00 - 15.20 茶歇Dr Adriaan van Zyl 15.20 - 16.40 GMP-厂房规范、设备规范-原料16.40 - 17.30 GMP:专题讨论会;小组讨论Dr Adriaan van Zyl2007年11月6日星期二08.30 - 09.30GMP:专题研讨会;各小组讨论结果介绍Dr Adriaan van ZylDr Adriaan van Zyl 09.30 - 10.00GMP-质量控制10.00 - 10:20茶歇Dr Adriaan van Zyl 10.20 - 12.30GMP-验证12.30 - 13.30午餐Dr Theo Dekker 13.30 - 15.00成品-包括稳定性试验15.00 - 15.20茶歇Dr Theo Dekker 15.20 - 16.20比较溶出度试验和应用-试验设计-相似性鉴定16.20 - 17.20案例分析研究-文档的质量部分Dr Theo Dekker第二天结束-评论和提问生物等效性2007年11月7日星期三08.30-0 9.30 案例分析研究-材料中的质量组成部分Dr Theo DekkerDr Jan Welink 09.30- 10.00介绍-等效性文件中的授权资质-等效性试验的不同检验方法-相对生物利用度(生物等效性)研究-药效学比较研究-比较性临床试验-体外方法10.00 - 10.20茶歇Dr Jan Welink 10.20 -11.00 生物等效性研究实验设计- 单剂量与多剂量e- 交叉和平行- 重复与不重复-禁食与饱食Dr Henrike Potthast 11.00 - 12.30BE试验的规划-试验目的-方案制定-伦理问题-临床、实验室和分析仪器-受试者的选择-受试者的特征-受试者的数量-受试者的排除12.30 - 13.30午餐Dr Henrike Potthast 13.30 - 15.00-试验设计-设计-标准化-设盲-食物和水的摄取-身体姿势及身体活动15.00 - 15.20茶歇Dr Henrike Potthast 15.20 - 16.30-给药间隔-样本收集和处理-不良事件Dr Jan Welink 16.30-17.30 BE试验的统计思考-生物利用度参数-证明生物等效的方法-非重复设计中的统计学影响-延滞效应-序列效应-叠加设计-突出值第三天结束时-评论和提问2007年11月8日星期四Dr Jan Welink 08.30 - 09.15-二阶段交叉生物等效性试验的取样分析-生物等效性试验实例中的数据和图表,包括对数据的统计分析Dr Jan Welink09.15 - 10.00 生物等效性的法规要求-概述和比较:WHO、EU、USA、其他-口服速释制剂-口服缓释制剂-其他:例如,透皮制剂、气雾剂10.00 - 10.20茶歇Dr Jan Welink10.20 - 11.40 复杂的药物动力学-非线性药代动力学-治疗范围狭窄的药物-高变异性药物对照药的选择-WHO、EU、USA、其他-生物等效性试验中拟提供的试验药物批次要求-用于生物利用度研究的批次的处方 VS.拟上市销售产品的处方Dr Henrike Potthast 11.40 - 12.30 其他的思考-生物等效性评估中代谢数据的使用-立体化学和生物等效性评估-生物等效性评估中有关小便数据的使用12.30 - 13.30午餐Dr Jan Welink13.30 - 15.00 测定方法/分析方法的验证-放射免疫法/色谱法-验证-灵敏度(定量限度;检测限度)-线性-特异性-耐用性-准确性和精确度-稳定性-临床样本的测定-标准曲线-质量控制-样本复验-记录保存/文件15.00 - 15.20茶歇15.20 - 16.30体内生物等效性试验的豁免和生物药剂学分类系统-多剂量-生物药剂学分类系统Dr Henrike Potthast16.30 - 17.30 案例分析研究-评估生物等效性试验报告Dr Jan WelinkDr Henrike Potthas 第4天结束-评论和提问2007年11月9日星期五08.30 - 10.00 案例分析研究-评估生物等效性试验报告Dr Jan WelinkDr Henrike Potthas10.00 - 10.20茶歇10.20 - 11.30 生物等效性试验的质量-质量保证-检查/审核Dr Henrike Potthast11.00 - 12.30 案例分析研究-生物药剂学分类系统Dr Henrike Potthast12.30 -13.00午餐13.30 - 14.30总结和提问,结业典礼WHO总部代表WHO驻中国代表处代表。
抗结核药品管理工作介绍

山东省结核病防治中心 耿红
2008年10月14日
1
主要内容
一、推广SOP手册的背景 二、试点工作进展 三、药品管理循环 四、药品管理人员职责
2
一、背景介绍-1 背景介绍防治策略 建立持续不间断的免费抗结核药品供应系统是 DOTS五要素之一 遏制结核病策略的要求 建立具有内在质量保证体系的高效、持续不间断 的免费抗结核药品供应系统,提高药品管理能力, 从而降低采购和实施的费用 抗结核药品管理的最终目标 使结核病人能够得到持续不间断供应的高质量的 药品,同时避免药品的浪费,使系统运行的成本 降到最低。
HRE
板
复治涂阳病人继续期
19
常见的固定剂量复合制剂
药品名 怡诺尼康片(60s) 乙胺利福异烟片 异福胶囊(60s) 异福酰胺胶囊 (90s) 异福酰胺胶囊 (60s) 剂型 片剂 片剂 胶囊 胶囊 胶囊 剂量 R150mgH75mgZ400mgE275mg R120mgH120mgE250mg R150mgH100mg R75mgH50mgZ250mg R75mgH50mgZ250mg
12
二、抗结核药品管理试点进展
效果评价: 效果评价:
统一的表、 使药品管理工作更加规范、 统一的表、卡、本,使药品管理工作更加规范、 操作性更强 库存控制卡的使用能监测药品月消耗量和最小库 存量及周转期限,掌握申请调拨额度, 存量及周转期限,掌握申请调拨额度,不至于发 生药品使用中断。 生药品使用中断。 使用带有价格的药品调拨/入库单 入库单, 使用带有价格的药品调拨 入库单,符合项目经费 财务审计工作要求, 财务审计工作要求,做到了项目管理与财务管理 的统一。 的统一。 实现动态监测,特别是对于市/区库存调整 区库存调整, 实现动态监测,特别是对于市 区库存调整,预防 药品积压或短缺起到了警示作用。
抗结核药物分级管理制度

抗结核药物分级管理制度1. 引言结核病是一种严重危害人类健康的传染病,为了加强对结核病的治疗管理,制定抗结核药物分级管理制度具有重要意义。
本制度旨在科学合理地对抗结核药物进行分类管理,确保药物的使用安全与有效性。
2. 分级管理原则抗结核药物分级管理应遵循以下原则:- 根据药物的安全性、有效性和副作用等特征,将抗结核药物分为不同级别;- 依据结核病的严重程度和患者情况,确定适用的药物级别;- 确定每一级别药物的使用原则和限制条件;- 加强药物使用监测和评价,以及不良反应和药物相互作用的应对措施。
3. 抗结核药物分类与级别3.1 一线药物一线药物是指对结核菌活性有直接抑制作用的主要药物,包括异烟肼、利福平、吡嗪酰胺、链霉素等。
这些药物具有较强的疗效,并且副作用相对较小。
一线药物是结核病治疗的基础,优先应用于结核病初治和非耐药性结核病的治疗。
3.2 二线药物二线药物是指在一线药物失效或出现耐药情况下使用的药物,包括丙胺夫咯明、卡那霉素、氟哌利多等。
这些药物具有较强的疗效,但可能引起严重的副作用,应在严密监测下使用。
3.3 特殊药物和药物联合应用特殊药物是指用于耐药性结核病治疗的特殊情况下的药物,如环酸酯、利奈唑胺等。
药物联合应用是指根据患者耐药情况,将多种药物联合使用以提高疗效。
特殊药物和药物联合应用应在专家指导下进行。
4. 药物使用原则和限制条件不同级别的抗结核药物在使用上应遵循以下原则和限制条件:- 一线药物:一般作为结核病的首选治疗药物,应严格遵循治疗方案、剂量和疗程的要求。
- 二线药物:仅在一线药物无效或耐药情况下使用,应在医生指导下合理使用,严密监测患者的药物反应和副作用。
- 特殊药物和药物联合应用:应在专家指导下应用,根据患者的特殊情况和耐药性选择合适的药物和联合方案。
5. 药物使用监测与评价抗结核药物的使用应建立完善的监测与评价机制,包括但不限于以下方面:- 监测患者的治疗效果和药物不良反应;- 监测耐药性情况,进行药物敏感性检测;- 监测抗结核药物的合理使用情况,及时发现和纠正不合理使用行为;- 评价不良反应和药物相互作用的危害程度,并及时采取措施应对。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
使用:包括诊断、开具要管理?
药品能挽救生命、促进健康 药品增进了人们对卫生服务的信任 药品昂贵 显著提高药品的管理通常是可行的 结核病的治疗需要几个月的时间,任何药
品供应的中断都很容易导致治疗失败和耐 药的产生
(衡量长期药品质量的指标,指标在中央级使用)
K-5.平均每种药品最近一次正规采购的价格占国际价格中 位数的百分比。
(一个衡量药品价格的指标,指标在中央级使用)
K-6.根据最近12个月药品使用情况计算平均每月的消耗量 并估算目前库存各种药品平均可使用的时间
(衡量长期药品供应水平的指标,通常是1年,用于省级、地 市级和县级)
药品管理常见问题
治疗指南不一致的抗结核药品选择 数量错误 价格过高 质量差 药品丢失 不正确的储存 药品过期 不合理的处方 病人用药错误
以指标为基础的评价药品管理
为结核病防治规划负责人和合作伙伴量化 药品供应系统的现状并揭示存在的优缺点
设计和计划干预措施 为经费预算和资源需求服务 改善监督系统和衡量干预措施的效果 不同的供应系统和国家之间的绩效比较
相关机构
世界卫生组织遏制结核的部门 参与结核病防治规划的国际合作伙伴和组织
(GDF、GFATM、GLC等) 卫生部决策者、国家结核病防治规划负责人 、制
定卫生计划的人员、卫生经济学家和捐赠人代表 国家级、省级、地市级和县级希望评价药品供应
和管理系统的负责人 对实施性研究和管理工具感兴趣的社会学家和卫
K-2. 目前结防机构药品库房中免费抗结核药品有库存的种 类百分比
(衡量当前药品供应水平的指标,用于省级、地市级和县级) K-3. 接受正确治疗方案的结核病人百分比 (衡量长期药品使用水平的指标,通常是1年或更长时间,用
于县级)
K-4.最近三次抗结核药品供货中有质量检验报告的药品批 次数占药品总批次数的百分比(包括所有途径最近采购的 3批药)
C-5.帐物相符率。(衡量目前药品库房管理水平的 指标,用于省级、地市级和县级)
C-6.过期或者破损药品占实际库存的百分比。(衡 量目前药品库房管理水平的指标,用于省级、地市 级和县级)
C-7. 前两个季度结防机构及时、准确、完整报告各 类药品的平均百分比。(衡量长期药品报告准确性 的指标,用于省级、地市级和县级结防机构)
中国抗结核病药品管理 评价过程介绍
中国CDC结控中心 王林
一、前 言
DOTS
STOPTB、GDF、GFATM、GLC
目标难于实现的原因:政府承诺和经费投 入、病人管理不当、抗结核药品短缺等
2000年,在美国国际发展署(USAID) 的支持下,推动药品合理化管理项目 (RPM Plus)制定了抗结核药品供应管理 系统评价手册。
然后,按照上述的方法从每个试点地市随机地选 了5个县级结防机构。
山东省17个地市中,6个以工业为主,其余11个 以农业为主。因此,随机地从6个工业地市中选1 个试点地市。需要注意的是,山东有5个地市属 于山区,12个地市属于平原。而济南市既属于工 业地区,又属于山区,因此选为调查点。
从11个农业地市中再随机选择3个地市为调查点
课题负责人1人(省级主管领导) 督导员2人(省级) 省和地市数据收集人员2人(省级) 县级数据收集人员4人(地市级)
预算
食宿费 交通费 材料费 必要的补贴 参加培训费用
抽样
1. 选择调查的省和地市 2. 选择调查的县 3. 选择调查的结核病人
2004年12月, 国家结控中心决定选择选出宁夏、 河南、吉林、山东作为候选省,从中将选2个省 开展评估。
补充指标
C-1.目前使用的抗结核药品种类中 属于国家基本 药品清单的百分比。(在中央级使用)
C-2.目前使用的抗结核药品种类中 属于世界卫生 组织基本药品清单的百分比。(在中央级使用)
C-3. 过去一年中药品质量抽检不合格率。 (在中 央级使用)
C-4.所调查的县级结防机构有最新版本国家结核病 治疗手册的百分比。(在县级使用)
生项目或机构的经理
调查指标
主要指标主要是保证与规划治疗方案一致 的抗结核药品在保证质量和成本效益的前 提下正常供应。
补充指标是用来扩展抗结核药品供应体系 的监督活动。
主要指标
K-1. 过去一年结防机构药品库房中各种免费抗结核药品缺 货时间的平均百分比
(衡量长期药品供应水平的指标,通常是1年,用于省级、地 市级和县级)
目的
提供抗结核药品管理的数据 寻找提高抗结核药品管理系统绩效的方法 寻找督导高质量的抗结核药品持续不间断
供应的方法 通过传授这种自我评估的技术,培养各级
开展抗结核病实施性研究的能力
找出影响药品供应实施的需要优先解决的问题, 并指出下一步的活动。
通过横断面调查,为将来干预措施的评价收集基 线数据。
二、准 备
选拔研究人员和分配任务
中国数据收集小组的主要成员如下: 组长:刘剑君 副组长:成诗明
负责确保评估的实施。 评价过程中的所有技术和管理工作将由
王林、赖钰基、王倪和徐敏等四人承担, 王林为负责人。 必要时,另有3人:方群(办公室)、黄飞(监 测部)和刘二勇(培训部)将协助上述小组的工 作。
不是比较各个地区的工作情况,而是通过 样本地区药品供应系统的调查来反映全国 的情况。
抗结核药品管理系统
使用
选择
管理支持:组织、 经费、信息管理和
人力资源管理
分发
政策和法律框架
采购
选择:包括挑选高质量的抗结核药品和适当的剂 量剂型。
采购:包括确定需求的抗结核药品数量、选择采 购方法、招标管理、制定合同条款、确保药品质 量、保证合同履行。
在确定2个试点省之前,收集了4省的基本信息。 最后选定山东和河南。
河南省18个地市中,7个以工业为主,11个以农 业为主。因此,随机地从7个工业地市中选1个试 点地市。
另3个农业市是从11个农业市中随机选出的,这 样一共有4个地市。
由于河南省各地市间没有特别的地理或其他差异, 所以不考虑分层统计分析。
