有机化学第四版_第二章烷烃
有机化学 第二章 烷烃

分子式相同(即分子组成相同),而结构不同的化合物 在同分异构体中如果它们的结构不同是由于分子中各原子 连结的次序和方式不同引起的,叫“构造异构”。
同分异构现象: 产生于同分异构体的现象 构造异构:
三种戊烷的同分异构体的相互比较 化学式 键线式 b.p (°) C 31.6
正戊烷 CH3CH2CH2CH2CH3
CH4
CH3CH3 CH3CH2CH3
不存在构造异构体 m.P -138.3 0C m.P -159.4 0C
从丁烷 丁烷开始,碳链出现了不同的连接方式 丁烷 CH3CH2CH2CH3 b.P 0.5 0C 正丁烷 CH3CHCH3 b.P -11.7 0C 异丁烷 CH3 ∴正丁烷和异丁烷是两种不同的化合物 同分异构体:
构象用投影式或透视式表示,Ex.乙烷的构象
重叠式构象
交叉式构象
重叠式构象
交叉式构象
重叠式构象
交叉式构象
在交叉式构象 交叉式构象中,两个C上H原子互相距离最远,相互间排斥 交叉式构象 重叠式构象中, 力最小,分子的内能最低,是最稳定的构象;在重叠式构象 重叠式构象 两个C上H原子相距最近,互相排斥力最大,内能最高,这种分子 内存在一种张力,也就是要趋于最稳定的交叉式构象而产生的键 的扭转张力,所以重叠式构象最不稳定。
五. 烷烃的性质 物理性质: 常T常P下: C1
的直链烷烃是气体 C5 C17 的直链烷烃是液体 C18 以上的直链烷烃是固体 b.p: 随着分子量增加,分子的体积增大,范德华引 力增大,b.p相应升高。分子量相同,支链越多,b.p 越低,因为支链多,分子间接近难, 引力减小。 m.p:随着分子量增加,m.p升高,含偶数碳原子比 含奇数碳原子的m.p高,因前者结构上更对称。 d:随着分子量增加,分子间作用力增大,距离减小, 比重升高。 溶解度:根据“相似相溶原理” 溶解度:根据“相似相溶原理”,烷烃一般不溶于水, 而易溶于非极性溶剂。
有机化学—烷烃

例:用衍生命名法给下列烷烃命名
CH3CHCH2CH3 CH3
戊烷
烷烃
同分异构
同分异构的分类
构造异构
碳链异构(正丁烷和异丁烷) 官能团位置异构(1-丁烯和2-丁烯) 官能团异构(乙醇和二甲醚)
互变异构(乙酰乙酸乙酯酮式和烯醇式)
立体异构
构型异构
顺反异构(烯烃) 光学异构(旋光异构)
构象异构(烷烃,环己烷,糖类)
一、烷烃的构造异构 分子构造:分子中原子间互相连接的顺序和方式。
CH4
C2H6
C3H8
C4H10
H
HH
HHH
HHHH
H C HH C C HH C C C HH C C C C H
H 甲烷
HH 乙烷
HHH 丙烷
HHHH 丁烷
第一节 烷烃的命名
一、伯、仲、叔、季碳原子和伯、仲、叔氢原子
1 H(伯氢)
2 H(仲氢)
H3C CH2 CH2 CH3
1 C(伯碳,一级碳) 2 C (仲碳,二级碳)
➢同系列 同系差 同系物 具有同一通式,结构、性质相似,组成上相差一个或若干个CH2 的一系列化合物称为同系列。CH2称为系差,同系列中各化合物 互称为同系物。如甲烷,乙烷,丙烷等都属于烷烃系列,三者彼此 之间互称烷烃同系物。
CH4 甲烷
C2H6 乙烷
C3H7 丙烷
C4H8 丁烷
有机化学 第二章 烷烃(alkane)

同系列:具有相同的结构通式,性质相近,组成上相
差CH2及其整数倍的称为同系列。 同系物:同系列中的各化合物互为同系物。 同系差:相邻同系物之间的差CH2叫同系差。
H H C H H H H C H H C H H H H C H H C H H C H H H H C H H C H H C H H C H H
2013-8-2
17
碳架异构体用正、异、新等词头区分。
正(n-):直链烃 异(iso-):从链端 起第二个碳原子 上带一个甲基 新(neo-):从链 端起第二个碳原 子上带两个甲基
CH3
CH3 CH3
CH3CH2CH2CH2CH2CH3 CH3CHCH2CH2CH3 CH3CCH2CH3
正己烷 异己烷 新己烷
I > Br > Cl > F > O > N > C > D > H
2013-8-2
27
② 如果两个多原子基团第一个原子相同,则比较与 其相连的其它原子。 比较时,按原子序数排列, 先比较最大的,若相同,再顺序比较较中的、最小 的。
CH2CH2CH3 C(C、H、H、)
CHCH3 CH3 C(C、C、H)
第二章 烷烃(alkane)
2013-8-2
1
本章重点讲解:
1. 2. 3. 4.
烷烃的命名-重点 烷烃的结构 烷烃的物理性质 烷烃的化学性质
2013-8-2
2
烃的分类及结构特征
分 类 脂 肪 烃 饱和烃 不饱 和烃 单 环 烃 烷烃 烯烃 炔烃 环烷烃 环烯烃 分子式通式 CnH2n+2 CnH2n CnH2n—2 CnH2n CnH2n—2 结构特征 含饱和C-C单键 含不饱和CC双键 含不饱和CC叁键 含饱和碳环 含带双键的碳环 CH3CH3 乙烷 CH2CH2 乙烯 CHCH 乙炔 C6H12 环己烷 C6H10 环己烯 实 例
有机化学课件-第二章-烷烃

CH3 CH CH CH CH2 CH3 CH2 CH3 CH3
CH3
主链
2,4-= 甲基-3-乙基己烷
次序规则
①将单原子取代基按原子序数大小排列,原子序 数大的顺序大,原子序数小的顺序小,有机化合 物中常见的元素其顺序由大到小排列如下:
I>Br>Cl>S>P>O>N>C>D>H
②如果多原子基团的第一个原子相同,则比较与他相连的 其它原子,比较时,按原子序数排列,先比较最大的,仍 相同,在顺序比较居中的、最小的。如果有些基团仍相同, 则沿取代链逐次比较。
烷烃分子之中碳原子为正四面体构型 。甲烷分子 之中,碳
原子位于正四面体构的中心,四个氢原子在四面体的四个顶
点上,四个C-H键长都为0.109nm,所有键角 ∠ H-C-H都是
109.5º
H
CH
H
H
109.5o H
H 0.109nm
H H
甲烷的球棒模型
甲烷的正四面体构型
sp3杂化轨道
杂化就是由若干个不同类型的原子轨道混合起来,重新组 合成数目相等的.能量相同的新轨道的过程。 C的电子构型:1S22S22P2
H-(-CH2-)n-H
或: CnH2n+2
同分异构体——由于分子式相同,但它们的构 造不同(分子中各原子相连的方式和次序不同). 又叫构造异构体。
戊烷可看成是正丁烷和异丁烷上的一个 H被甲基-CH3 取代的产物: (正戊烷,异戊烷,新戊烷)......
烷烃分子中,随着碳原子数的增加,烷烃的构造异 构体的数目也越多. 写出C7H16的同分异构体?
6C
C 2 1 编号错误
(2) 若第一个支链的位置相同,则依次比较第二 、第三个支链的位置,以取代基的系列编号最小( 最低系列原则)为原则。
有机化学第二章

KMnO4
RCOOH + R'COOH
3 异构化反应-提高汽油的质量
AlBr3/HBr 27oC
4 裂化反应
400~700oC or heat, cat.
CnH2n+2
H2 + C mH2m+2 + C n-mH2(n-m)
2.6 烷烃的天然来源
► 烷烃的天然来源
(P:38)
C5-C6 C7-C9 C11-C16 C16-C18
说明:烷烃的溴代反应常用于叔氢原子的选择性卤代。
理论解释
烷烃的结构 键能 KJ/mol
-1
不同卤原子的比较 Cl2 Br2
伯氢
仲氢 叔氢
RCH2-H
R2CH-H R3C-H
405.8
393.3 376.6 活性增大 易形成自由基
1
4 5
1
82 1600
自由基的稳定性: R3C>R2HC>RH2C>CH3
► 结构简式
CH3CH3
► 键线式
CH2 CH2
CH3CH2OH
CH3 O CH3
2.1.2
戊烷(pentane)的异构体
CH3CH2CH2CH2CH3
CH3CHCH2CH3 CH3
CH3 H3C C CH3 CH3
练习:写出分子式为C6H14的同分异构体
随碳原子数的增多,同分异构体数目剧增,这是有机 化合物分子多样性的原因之一。
溴的选择性比氯好 F2易爆炸,I2难反应
过渡态理论
► 始态(反应物) ►A
过渡态
终(产物)
+ B-C
►A
+ B-C
A-B +C (Transition state) [A B C ] A-B +C
有机化学--第二章烷烃

重叠式构象 扭转张力大
重叠式和交叉式 构象之间的能量差 约为12.6 kJ·mol-1, 此能量差称为能垒。 其它构象的能量介 于此二者之间。
有机化学--第二章烷烃
2.3.4丁烷的构象
正丁烷可以看作是乙烷分子中每个碳原子上各有一 个氢原子被甲基取代的化合物,其构象更为复杂,我们 主要讨论沿C2和C3之间的σ键键轴旋转所形成的四种典型 构象:
仲氢 伯氢
叔氢 有机化学--第二章烷烃
2. 烷基 (alkyl group)
烷烃分子从形式上去掉一个氢原子后余下的基团称为烷
基,其通式为CnH2n+l,通常用R— 表示。最常见的烷基有:
烷基名称
烷基
中文名 英文名 缩写
烷基
中文名 英文名 缩写
CH3 CH3CH2
甲基 methyl 乙基 ethyl
Me-
仲丁基 sec-butyl s-Bu-
CH3CH2CHCH3
(s-butyl)
Et-
异丁基 isobutyl i-Bu
(C H 3 )2 C H 2 C H 2
C H 3C H 2C H 2 CH3CHCH3
正丙基 Propyl
Pr-
异丙基 isopropyl i-Pr-
(CH3)3C (C H 3)3C C H 2
6-tert-butyl-5-ethyl-2-methyldecane
有机化学--第二章烷烃
(4)如果烷烃比较复杂,在支链上还连有取代基时,可用带撇 的数字标明取代基在支链中的位次或把带有取代基的支链的 全名放在括号中。例如:
12
3
有机化学--第二章烷烃
2.3 烷烃的结构
碳原子基态时的 电子层结构为:
有机化学课件-第二章烷烃

第 二 章 烷 烃
1.烷烃的概念和分类
烷烃的分类:按照碳链骨架可分为链烷烃和环烷烃; 链状烷烃的结构通式:
H H C H H H
H C H H C H H H
H C H H C H H C H
H H
H
H
C
H
甲烷 CH4
• •
乙烷 C2H5
丙烷 C3H8
n
CnH2n+2
含有n个碳原子的直链烷烃
卤代反应的机理: 链引发: 自由基锁链反应
Cl
H
Cl
Cl
hv
2Cl
CH3
CH3
H
Cl
链增长:
CH3
Cl Cl H3C Cl
Cl
Cl
CH3
H3C
Cl
链终止:
CH3 Cl
CH3 Cl
CH3CH3 Cl2
练习题 2.14(1)
第 二 章 烷 烃
6.烷烃的化学性质
反应过程中能量的变化: 反应物 过渡态
第 二 章 烷 烃
6.烷烃的化学性质
热裂解反应 烷烃在隔绝空气和高温条件下反应,分子中碳碳键断裂,生 成小分子的烷烃,也可转变为烯烃和氢气等复杂混合物。
600℃
CH4 CH3CH3 CH3CH2CH3
H2C C CH3 H H2C CH2
CH3CH2CH2CH3
丁烷加热至600℃反应,得甲烷、乙烷、乙烯、丙烯等
第 二 章 烷 烃
6.烷烃的化学性质
烷基自由基的相对稳定性:
H3C H3C CH H3C CH2 H3C CH H3C C CH3 CH3
CH3
有机化学第四版(胡宏纹)第二章烷烃

n-pentane
n-hexane n-heptane
CH3(CH2)6CH 正辛烷
CH3(CH2)7CH 正壬烷 CH3(CH2)8CH 正癸烷
n-octane
n-nonane n-decane
2 烷基的命名
烷烃分子中去掉一个氢原子剩下的原子团称为烷基。 烷基的英文名是将烷烃的词尾-ane改为-yl。
如果有几种不同的烷基连接在母体链上, 按次序规则从小到大的先后次序来命 名。 CH
2,4-二甲基-3-乙基戊烷
3 CH3CH2CHCHCH3 2 1 CH3 CH 4 CH3 5
3
1.选主链(母体)
CH 2CH3
1 2 3 4 5 6
2.编号
2
3.书写
1 5
CH 2CH3
3 4
CH3CHCH 2CHCH 2CH3
仲丁基(s-Bu) sec-butyl
CH3C CH3
叔丁基(t-Bu) tert-butyl
两价的烷基lidene
CHCH3
亚乙基 ethylidene
C(CH3)2
亚异丙基 isopropylidene
CH2CH2
1,2-亚乙基 dimethylene
CH2CH2CH2
CH3 CH3CHCHCH3 CH3CH2CHCHCH2CH2CH3 CH3
2,3,5-三甲基-4-丙基庚烷 2,3,5-trimethyl-4-propylheptane
第二步给定编号:
如果烷基在母体碳链上可因位置不同 而引起异构现象时,就必须对母体碳链进 行编号,并用数字指明烷基所连的碳原子。 编号时,以离取代基最近的一端为1。
•同分异构现象:具有分子式相同而结构
高教第四版有机化学第二章 烷烃和环烷烃

2
3
4
5
6
7
8
C
8
C
7
C
6
C C 5 C 4
C C 3 C 2 C
C
1Байду номын сангаас
编号错误 编号正确
1
2
3
4
5
6 编号正确
C
6
C C
C
C C
C
2
C
1
编号错误
2)从碳链任何一端开始,第一个支链的位置都相同时,则从较简 )从碳链任何一端开始,第一个支链的位置都相同时, 单的一端开始编号。 单的一端开始编号。 1 2 3 4 5 6 7 编号正确
CH3CH2CH(CH3)2,
C(CH3)4
2.1.2、烷烃和环烷烃的同分异构 、
例如: 例如:己烷
这种分子式相同而构造式不同的化合物称为同分异构体,这种现象称为 构造异构现象。
环戊烷: 环戊烷:
2.2 烷烃的命名
2.2.1伯、仲、叔、季碳原子和伯、仲、叔、季氢原子 伯 季碳原子和伯、 在烃分之中仅与一个碳相连的碳原子叫做伯碳原子(或一级碳原子, 在烃分之中仅与一个碳相连的碳原子叫做伯碳原子(或一级碳原子,用 1°表示)与两个碳相连的碳原子叫做仲碳原子(或二级碳原子,用2°表示) °表示)与两个碳相连的碳原子叫做仲碳原子(或二级碳原子, °表示) 与三个碳相连的碳原子叫做叔碳原子(或三级碳原子, 与三个碳相连的碳原子叫做叔碳原子(或三级碳原子,用3°表示)与四个 °表示) 碳相连的碳原子叫做季碳原子(或四级碳原子, 碳相连的碳原子叫做季碳原子(或四级碳原子,用4°表示) °表示) 例如:
2,4-= 甲基-3-乙基己烷 CH3
主链
(完整word版)有机化学(第四版)习题解答
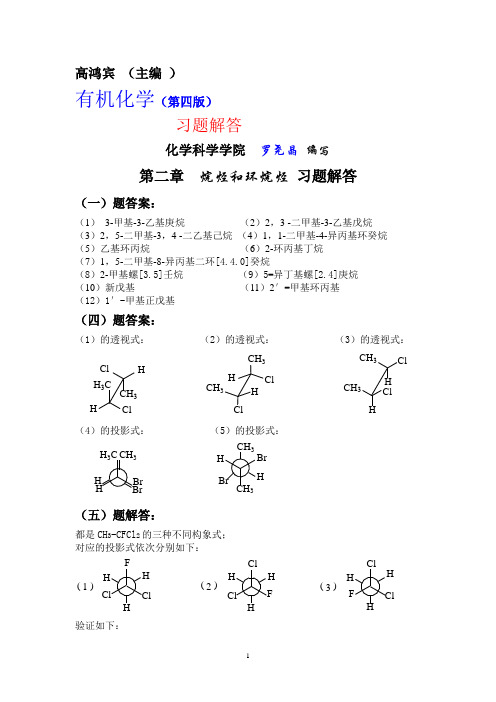
高鸿宾 (主编 )有机化学(第四版)习题解答化学科学学院 罗尧晶 编写第二章 烷烃和环烷烃 习题解答(一)题答案:(1) 3-甲基-3-乙基庚烷 (2)2,3 -二甲基-3-乙基戊烷 (3)2,5-二甲基-3,4 -二乙基己烷 (4)1,1-二甲基-4-异丙基环癸烷 (5)乙基环丙烷 (6)2-环丙基丁烷 (7)1,5-二甲基-8-异丙基二环[4.4.0]癸烷(8)2-甲基螺[3.5]壬烷 (9)5-异丁基螺[2.4]庚烷 (10)新戊基 (11)2′-甲基环丙基 (12)1′-甲基正戊基(四)题答案:(1)的透视式: (2)的透视式: (3)的透视式:Cl HCH 3H 3C ClHCH 3CH 3ClClHHCH 3ClClCH 3H H(4)的投影式: (5)的投影式:BrBr CH 3HH H 3CBrBr CH 3CH 3HH(五)题解答:都是CH 3-CFCl 2的三种不同构象式; 对应的投影式依次分别如下:ClClCl ClClCl FFF H HHH H H H H ( )( )( )123验证如下:把投影式(1)的甲基固定原有构象位置不变,将C-C 键按顺时针方向分别旋转前面第一碳0°、60°、120°、180°、240°得相应投影式如下:ClClClClClClClCl ClClFF FF F H HH H H HHH H H H H HH H ( )( )( )( )( )ab c de各投影式对应的能量曲线位置如下:由于(a )、(c )、(e )则为(1)、(2)、(3)的构象,而从能量曲线上,其对应能量位置是一样的,所以前面三个透视式只是CH 3-CFCl 2的三种不同构象式。
(六)题解答:(1)、(2)、(3)、(4)、(5)所代表的都是相同的化合物(2,3-二甲基-2-氯丁烷),只是构象表示式之不同,而(6)代表的则为2,2-二甲基-3-氯丁烷,是不同于(1)~(5)的另一个化合物。
有机化学 第二章 烷烃

C
C
C C C
C
C C C
2-甲基-4-乙基己烷
4)支链上有取代基时,取代支链的名称可放在括 号中表明。例:
CH 3 H3C CH 2 C CH 3 10 9 8 7 6 5 4 3 2 1 H3C CH 2 CH 2 CH 2 CH 2 C CH 2 CH 2 CH CH 3 H3C CH 2 C CH 3 CH 3 H3C
1.普通命名法
a. 链烃分子碳原子数目在10以内时,用天干数 表示,即甲、乙、丙、丁、、、、、、壬、癸; 在10以外,则用汉文数字表示。
例: 甲烷 乙烷 壬烷 十一烷 二十烷
b. 用正、异等来表示异构体
CH3 CH3 C CH3 CH2
CH3 CH CH3
异辛烷
异辛烷中的异不符合命名的规定,是一个特例。
偶数碳
奇数碳
二 沸点
沸点大小取决于分子间的作用力 烷烃沸点的特点 (1)沸点一般很低( 烷烃为非极性分子,不存在静电引力, 诱导力) ,只有色散力)。 (2)随相对分子质量增大而增大(运动能量增大,范德华 引力增大)。 (3)相对分子质量相同、叉链多、沸点低。(叉链多,分 子不易接近)
三 密度
小于1
A
B
C
D
E
F
(2)正丁烷的构象势能关系图
沿C2-C3键轴 旋转的转动能 垒 22.6 kJ· -1 mol
能 量
CH3 H H CH3 H H 1
H3CCH3
H3CH
H H
4
H H
H3CH
H H 2
H CH3
CH3 H 6
4 全重叠 2,6 部分重叠 3,5 邻位交叉 1=7 对位交叉
有机化学 第2章烷烃和环烷烃

CH3 H3C CH
3 H(叔氢)
CH3 H3C C CH3 CH3
CH3
3 (叔碳,三级碳)
4 (季碳,四级碳)
tertiary carbon
quaternary carbon
CH 1。 3
3。 CH CH3 1。
2。 CH2 C CH3 4。 1。 CH3 1。
1。 CH3
二、烷烃的构造异构和命名( Constitutional
碳链异构—由于碳链结构的不同而产生的异
构现象称为碳链异构现象,简称碳链异构。异构
体互称为碳链异构体。如:C4H10
H H C H H C H H C H H C H H H H C H H H C C H H C H H H
正丁烷
异丁烷
mp bp
-138℃ -0.5℃
-160℃ -12℃
随着分子中碳原子数目的增加,异构体的数
第二章 烷烃和环烷烃
(Alkanes and Cycloalkanes)
学习要求:
1.掌握烷烃和环烷烃的基础理论和基本知识。
2.掌握构象异构的基本概念。 烃的概念: 烃—指分子中只含C、H两种元素的化合物,又称碳 氢化合物。
烃 碳氢化合物 (hydrocarbons)
烃的分类:
饱和烃——烷烃 链烃 烯烃 不饱和烃 脂肪烃 炔烃 环烷烃 脂环烃 环烯烃 环炔烃 苯型芳香烃 芳香烃 非苯型芳香烃
较稳定。
C C H
(一)稳定性(Stability) 一般情况下烷烃化学 性质不活泼、耐酸碱、不与强氧化剂和还原剂作用。 (常用作低极性溶剂,如正己烷、正戊烷、石油醚 等) (二)卤代反应(Halogenation reation)
和含碳原子数较少的烷烃。
第二章 烷烃

㈠ 稳定性 • C-C键和C-H键均很牢固 键和C • C-H键的极性小,C和H都很难被极化 键的极性小, 都很难被极化 • 在常温下,与强酸、强碱、强氧化剂、强还原剂 在常温下,与强酸、强碱、强氧化剂、 都不发生反应 ㈡ 燃烧 燃烧产物为CO 并放出大量的热, 燃烧产物为CO2和H2O,并放出大量的热,因 此烷烃成为可作为重要的能源. 此烷烃成为可作为重要的能源.
CH3 H + Cl Cl CH3 Cl + H Cl
kJ/mol 435
243
351
431
∆H = (435+243) -(351+431) = -104kJ/mol 3.卤代反应机制 卤代反应机制 反应机制又称反应历程, 反应机制又称反应历程,是化学反应所经 反应历程 具体途径. 具体途径. 历的
扭转张力 非稳定构象具有恢复成稳 定构象的力量;
2、正丁烷的构象 、
正丁烷的构象比较乙烷要较为复杂一些。 正丁烷的构象比较乙烷要较为复杂一些。 正丁烷的极端典型构象有四种: 正丁烷的极端典型构象有四种:
全重叠式 邻位交叉 部分重叠式 对位交叉式
(1)正丁烷的构象势能关系图
沿C2-C3键轴旋转 的转动能垒 22.6 kJ·mol-1
CH3
CH2 CH2 CH2 CH3 正戊烷或戊烷(n (n-Pentane) 正戊烷或戊烷(n
CH3 C CH3
CH3
CH2
CH CH3
CH3
CH3
异戊烷(iso 异戊烷(iso- Pentane) (iso
CH3 新戊烷(neo (neo新戊烷(neo Pentane)
㈡系统命名法
⒈ 烷基的命名 烃分子中去掉一个氢原子, 烃分子中去掉一个氢原子,所剩下的部分叫做烃基 一价烷基的通式为C 脂肪烃基常用 R-表示 一价烷基的通式为 nH2n+1- -表示,一价烷基的通式为 常见烷基的结构和名称 CH3- 甲基 C2H5-乙基 CH3CH2CH2- (正)丙基
有机化学第二章 烷烃

二、烷烃的同分异构
烷烃同系列中,甲烷、乙烷、丙烷只有一种结合 方式,没有异构现象,从丁烷起就有同分异构现象。
CH3 CH2 CH2 CH3
正丁烷 b.p -0.5℃
CH3 CH CH3 CH3 异丁烷 b.p -10.2℃
正丁烷和异丁烷是同分异构体。这种分子式相同而 结构式不同的现象叫做同分异构现象。由于碳链的连 接方式不同而产生的异构现象属于同分异构中的碳链 异构。
二、氧化反应
在室温和常压下,烷烃与氧不发生反应,如果点 火引发,则烷烃可以燃烧生成二氧化碳和水,同时
放出大量的热。
作业 P-32 1 (1)(3)(5) 4
三、熔点(m.p.)
随分子分子量增加而升高。
四、相对密度
随分子量增加而增大。其相对密度都小1,比水轻。
五、溶解度
根据“相似相溶” 的经验规则,脂烃分子没有 极性或极性 很弱,因此难溶于水,易溶于有机溶剂。 (石油醚,石蜡油,凡士林)
第五节 烷烃的化学性质
一、卤代反应
二氯甲烷
三氯甲烷
四氯化碳
X2的反应活性: F2>Cl2>Br2>I2 其中氟代反应太剧烈,难以控制;而碘代反应太慢, 难以进行,实际上广为应用的是氯代和溴代反应。
Davissson和Germer
出) 如果我们能准确测定微 粒的位置, 那就不能准确 测定其速度, 反之亦然.具 有波粒二象性的电子,已 不再遵守经典力学规律, 它们的运动没有确定的轨 道,电子在核外空间出现 机会最多的区域就是轨道。
海森堡(Heisenberg W) 德国物理学家 重要暗示——微观世界不可能存Rutherford 和 Bohr 模型中行星绕太阳那样的电子轨道:
*价键理论的形成与发展
《有机化学》(第四版)复习提纲

有机化学复习提纲《有机化学》(第四版)第一章绪论1、有机化合物的定义。
2、碳原子的SP、SP2、SP3杂化轨道的杂化原理和共价键的构成方式。
3、诱导效应的概念。
4、酸碱的概念。
第二章饱和烃:烷烃和环烷烃1、烷烃的命名。
脂环烃、桥环烃、螺环烃的命名方法。
2、环烷烃的环结构与稳定性的关系。
3、取代环已烷的稳定构象。
4、烷烃的卤代反应历程(自由基型取代反应历程)。
5、烷烃的卤代反应取向与自由基的稳定性。
6、脂环烃的取代反应。
7、脂环烃的环的大小与开环加成活性关系。
8、取代环丙烷的开环加成规律。
9、环烯烃的π键加成与α-氢的卤代反应区别。
第三章不饱和烃:烯烃和炔烃1、碳-碳双键、碳-碳三键的组成。
2、π键的特性。
3、烯烃、炔烃的命名;烯烃的Z,E-命名法,烯炔的命名。
4、烯烃、炔烃的加氢催化原理及其烯烃、炔烃的加氢反应活性比较。
5、炔烃的部份加氢——注意区分顺位部分加氢和反位部分加氢的条件或试剂。
6、何谓亲电加成?(烯烃中被亲电试剂进攻的不饱和碳上电子密度越高,亲电加成活性越大)7、烯烃、炔烃可以与哪些试剂进行亲电加成,这些加成有哪些应用。
8、烯烃亲电加成反应机理。
9、亲电加成反应规律(MalKovniKov规律)。
10、烯烃、炔烃与HBr的过氧化物效应加成及其规律。
(惟一只有溴化氢才能与烯烃、炔烃存在过氧化物效应,其它卤化氢不存在过氧化物效应。
)11、烯烃亲电加成与炔烃亲电加成活性的比较。
12、不同结构的烯烃亲电加成活性的比较——不饱和碳上电子密度越高的烯烃或越容易生成稳定碳正离子的烯烃,亲电加成反应的活性越大。
13、碳正离子的结构和碳正离子的稳定性之间的关系——正电荷越分散,碳正离子就越稳定。
14、烯烃经硼氢化—氧化水解在合成醇上的应用;炔烃经硼氢化—氧化水解在合成醛或酮上的应用。
15、碳-碳双键的α-碳上有支链的烯烃与卤化氢加成时的重排反应。
(P88)16、烯烃与次卤酸加成及加成规律。
炔烃与水加成及重排产物。
有机化学课件-2-烷烃

二、同分异构:
定义:分子式相同而结构(或物理或化学性质)不同的现象; 分类:同分异构可分为构造异构和立体异构;
构造异构:分子式相同而构造式不同(构造是指分子中原子的连 接顺序); 如:CH3CH2OH和CH3OCH3;
构造异构又可分为:碳架异构、碳链异构、官能团异构和位置异 构。
如:环己烷和己烯 (碳架异构)
HHH HH
其立体结构为:
H
C
H
C
C
H
H
H H
C-C(σ键): 154pm,sp3-sp3; C-H(σ键): 110pm,sp3-s; 由于所有C原子都采用sp3杂化,所以所有的键角都约在109.5 0;
为了书写方便,碳链可写成折线式, 如己烷可写成:
碳原子上的氢原子可省略,但也可标出;但若标出某个碳原子 上的氢原子,则必须标齐。
如: CH3(CH2)4CH3 正己烷
3. 带有支链的烷烃;
CH3
末端具有 CH3CH 结构的,加“异”,
CH3
末端具有 CH3 C 结构的,加“新”,
CH3
CH3
如:CH3CH CH2CH3 异戊烷
CH3
CH3 C CH2CH3 新己烷
CH3
普通命名法只能命名结构简单的有机物,局限性大;但名称可 直接反映出有机物的结构。
CH3CH2CH2CH3和CH3CH(CH3)2(碳链异构) CH3CH2OH和CH3OCH3 (官能团异构)、 CH3CH2CH=CH2和CH3CH=CHCH3 (位置异构);
立体异构: 构造式相同而原子在空间的立体位置不同; 可分为: 顺反异构(见第三章“环烷烃”和第六章“烯烃”)
和对映异构(见第四章“对映异构”)。 烷烃只存在构造异构(碳链异构),没有立体异构; 如:
有机化学第2章_烷烃和环烷烃
以甲烷的氯代反应为例,有如下反应事实: (1)在室温、黑暗中不反应;加热或光照下 进行,一经开始便可自动进行; (2)产物中有少量乙烷; (3)如有氧或有一些能捕捉自由基的杂质存 在,会推迟反应的进行。
以上实验事实,说明该反应是为自由基反应! 自由基反应大多可被光照、高温、过氧化物 所催化,一般在气相或非极性溶剂中进行。
H 一氯甲烷
生成的一氯甲烷还会继续被氯代,生成二氯甲 烷、三氯甲烷和四氯化碳四种产物的混合物。
CH2Cl2
二氯甲烷
CHCl3
三氯甲烷
CCl4
四氯甲烷
(二)卤代反应 2、卤代反应的反应机制
反应机制(反应历程):化学反应所经历的途 径或过程 ,是根据实验事实,对反应做出的 详细描述和理论解释。
研究反应机理的目的是认清反应本质,掌握反 应规律,从而达到控制和利用反应的目的。
σ(s-sp3)
键角为109.5°
σ(s-sp3)
(2)乙烷(CH3CH3)分子的结构
除了H原子的s轨道电子与C原子的sp3轨道 电子以“头碰头”方式重叠形成s-sp3共价键外 ,也存在两个C原子的sp3轨道电子之间的配对
。σ(s-spσσ3) 键键可:沿旋键转轴不“影自响由轨道”重转叠动程;度重叠,程即
自由基
概念:带有孤电子的原子或原子团称为自由基
结构特点:三种可能结构(1)刚性角锥体, (2)迅速翻转的角锥体,(3)平面型。
C
C
C
自由基非常活泼,具有很强的反应活性。
CH2 > CH2 CHCH2 > (CH3)3C > (CH3)2CH
> CH3CH2 > CH3 >
《有机化学》(第四版)高鸿宾,华南理工大学课件

CH3 CH3 CH2 C CH CH3
CH3 CH3
二甲基乙基异丙基甲烷
(3) 系统命名法
International Union of Pure and Applied Chemistry,缩写作IUPAC
系统命名是由三部分构成:
取代基
的
母体
位次与名称
化合物 的
名称
碳原子的个数
直链烷烃的命名与普通命名法相同。
1
2
3
4 CH2CH2CH3
CH3 CH2 CH2 CH C5H C6H2 C7H2 C8H2 C9 H3
CH CH3
CH3
4-isopropyl-5-propylnonane
(5–丙基–4 –异丙基壬烷)
• 当两个或更多的相同取代基出现时,使用 前缀di-, tri-, tetra-等:
CH3
CH3
98
CH3CH2
CH3 CH2CH3
CH3
CH
7
C6 H2
C5 H2
CH CH
43
C2H2C1H3
(I)
1
2
CH3CH2
CH3 CH2CH3
CH3 C3 H
C4 H2
C5 H2
CH CH
67
C8 H2C9 H3
( II )
(c) 确定化合物的名称 • 将取代基的名称写在母体名称的前面,在
取代基名称的前面加上它的位次号,并用 半个汉字长的横线“–”将两者连接。 • 当含有几个不同的取代基时,按照“次序 规则”,将“优先”的基团列在后面,各取 代基 之间用半个汉字长的横线“–”连接。
上“环”字,称“环某烷”。环上有支链时,支 链作为取代基。
有机化学--烷烃

通式相同,组成上相差“ 通式相同,组成上相差“CH2”及 其整倍数的一系 及 同系列。 列化合物 - 同系列。 同系物。 同系列中的各个化合物互为同系物 - 同系物。 “CH2”称为系差 - 系差。 称为系差 系差。 同系物具有相似的化学性质, 同系物具有相似的化学性质,但反应速率往 具有相似的化学性质 往有较大的差异;其物理性质(例如沸点、熔点、 往有较大的差异;其物理性质(例如沸点、熔点、 沸点 相对密度、溶解度等 相对密度、溶解度等)一般是随着相对分子质量 的改变而呈现规律性的变化 规律性的变化。 的改变而呈现规律性的变化。
9 8 7 6 5 4
CH3 CH2 CH CH2 CH2 CH CH2 CH3 CHCH2CH3 CH3 3 2 1 CH3
3,7-二甲基 乙基壬烷 二甲基-4-乙基壬烷 二甲基
7
6
5
4
3
2
CH3
1
CH3-CH—CH-CH2-CH2-C-CH3 1 2 3 4 5 6 7 CH3 CH3 CH3 从右到左: , , , 从右到左:2,2,5,6 从左到右: , , , 从左到右:2,3,6,6
不重复的只能写出5 不重复的只能写出5个。
随着分子中碳原子数目的增加,同分异构体的数目 增加。 随着分子中碳原子数目的增加,同分异构体的数目也增加。 碳原子数目的增加 数目也 碳原 子数 异构 体数 4 2 5 3 7 9 10 75 11 159 15 4347 20 366319
3、烷烃构造式的书写方法
CH3CH2CHCHCHCH2CH2CH3
4-Ethyl-3,5-dimethyloctane
3,5-二甲基 乙基辛烷 二甲基-4-乙基辛烷 二甲基
1
2
烷烃指由碳和氢两种元素组成的饱和

碳数 31 32 33 40 50 60 70 80 90 100 132
中文名
三十一烷 三十二烷 三十三烷 四十烷 五十烷
六十烷 七十烷 八十烷 九十烷 一百烷
一百三十 二烷
英文名 hentriacontane dotriacontane tritriacontane tetracontane pentacontane hexacontane heptacontane
icosane
碳数 21 22 23 24 25 26 27 28 29 30
中文名
二十一烷 二十二烷 二十三烷 二十四烷 二十五烷 二十六烷 二十七烷 二十八烷 二十九烷 三十烷
英文名 henicosane docosane tricosane tetrcosane Penacosane Hexacosane Heptacosane Octacosane Nonacosane triacontane
2-甲基-5-(1,1-二甲基丙基)癸烷
CH3
(三)烷烃的结构
(1)碳原子轨道的sp3杂化
跃迁
sp3杂化
2p 2s
2p 2s
sp3
每个sp3杂化轨道含1/4 s 成分和 3/4 p成分
键角为 109.5°
sp3杂化轨道形状
碳原子的sp3杂化轨道
•σ键的形成及其特性
原子 轨道沿键轴相互交盖,形成对键轴呈圆柱 形对称的轨道称为σ 轨道。σ轨道构成的共价键称为 σ键。
3%
CH3 CH3 CH CH2Br
<1%
Br>Cl>F
(2)氧化反应
CH4 + 2O2 燃烧 CO2 + 2H2O + 891 kJ mol-1
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
四、烷基
烃分子中去掉一个氢原子后剩下的原子团叫做烃基。
脂肪烃基:脂肪烃去掉1个H所剩下的部分。
“R-”
芳香烃基:芳香烃去掉1个H后剩下的部分。
“Ar-”
烷基:烷烃的基。
烷烃同一碳上去掉2个H或3个H后, 分别称为亚基、次基。
如:
碳原子外层电子排布为1s22s22px12py1,有2个未成对电子,应该是二价的,但碳原子实际上是四价的.
由于2S轨道的能量与2p较接近,2S上的1个电子可以激发到2pz空轨道上.激发态的碳原子有4个单电子。
第三节烷烃的构象p23
第四节烷烃的物理性质
1.状态:
在常温常压下,1至4个碳原子的直链烷烃是气体,5至17个碳原子的是液体,18个及以上的是固体。
2.沸点:。
