高中化学:铁及其化合物
【高中化学】高中化学知识点:铁及其化合物

【高中化学】高中化学知识点:铁及其化合物高中化学知识点:铁及其化合物。
(一)铁的反应1)铁丝在纯氧中燃烧生成四氧化三铁(现象?)2)红热的铁丝在氯气中反应分解成氯化铁(三价铁)3)铁粉与硫粉混合加热时反应生成硫化亚铁4)铁与非水解性酸(盐酸、稀硫酸、醋酸等)反应分解成氢气和亚铁盐5)铁与浓硫酸或浓硝酸作用发生“钝化”现象6)铁与过量叶唇柱硝酸反应分解成一氧化氮和硝酸铁(三价),铁与严重不足量叶唇柱硝酸反应可能将分解成一氧化氮和硝酸亚铁7)红热的铁与水蒸气反应生成四氧化三铁和氢气8)铁从硫酸铜等盐溶液中转让出来金属(条件?)9)铁与三价铁离子反应(二)铁的氧化物1)种类:氧化亚铁,黑色,不稳定;氧化铁,红色(红色颜料--铁红);四氧化三铁,黑色(磁性氧化铁)(价态?)2)跟盐酸反应,分解成氯化物,铁的价态维持不变;跟硝酸反应,二价铁可以被水解。
3)跟co高温反应,铁被还原(炼铁)页面查阅:高考化学知识点汇总(三)铁的盐类1)fe2+浅绿色;fe3+棕黄色2)fe2+还原性,被氯气、硝酸等氧化成fe3+3)fe3+水解性,通常被转换成fe2+fe3+与fe反应fe3+与cu反应fe3+跟h2s溶液反应生成浑浊4)亚铁盐溶液中重新加入碱溶液分解成白色结晶,快速变为灰绿色,最后变为红褐色;三价铁盐溶液中加入碱溶液,生成红褐色沉淀5)三价铁盐溶液中滴提kscn或nh4scn,溶液变小血红色(检验fe3+)二价铁盐溶液滴加kscn溶液不变红色,如果再加氯水,变红色(检验fe2+)6)三价铁盐与酚类促进作用表明紫色7)苯与卤素(cl2,br2)反应时加铁屑催化,实质是铁盐起催化作用。
高中化学知识点:铁及其化合物

高中化学知识点:铁及其化合物高中化学知识点:铁及其化合物铁的存在和主要性质铁是一种活泼的元素,具有较强的还原性,主要化合价为+2价和+3价。
它在自然界中广泛存在,并且在生活中有着重要的应用。
铁的化学性质铁与非金属单质的反应包括与氧气、氯气和硫的反应。
在常温下,铁会被氧气腐蚀生成铁锈,其中主要成分为Fe2O3·xH2O。
当加热时,铁会与氧气反应生成Fe3O4.铁还可以与氯气和硫反应生成FeCl3和FeS。
在与水的反应中,常温下铁不会与水反应,但在高温条件下,铁会与水蒸气反应生成Fe3O4和H2.铁还可以与酸反应,包括与非氧化性酸和氧化性酸的反应。
与非氧化性酸反应时,铁会被氢离子还原成Fe2+离子,并释放出氢气。
与氧化性酸反应时,铁会被氧化成Fe3+离子,并释放出氮氧化物和水。
铁还可以与某些盐溶液反应,包括与CuSO4溶液反应生成Cu和FeSO4,以及与FeCl3溶液反应生成Fe2+和Fe3+离子。
铁的重要化合物铁的氧化物包括FeO、Fe2O3和Fe3O4.这些化合物可以与盐酸反应生成Fe2+离子和水。
FeO还可以与硝酸反应生成Fe(NO3)3、NO和H2O。
铁的氢氧化物包括Fe(OH)2和Fe(OH)3.这些化合物可以与H+反应生成Fe2+或Fe3+离子和水。
在空气中,Fe(OH)2会迅速被氧气氧化成Fe(OH)3,现象是白色固体变成红褐色固体。
此外,氧化亚铁(FeO)、氧化铁(Fe2O3)和四氧化三铁(Fe3O4)也是铁的重要氧化物,它们分别呈黑色粉末、红棕色粉末和磁性氧化铁黑色晶体。
Fe2+、Fe3+→Fe+2Fe3+→3Fe2+、Fe+2H+→Fe2++H2↑点燃Fe→Fe3O4的两个反应:3Fe+2O2→Fe3O4高温3Fe+4H2O(g)→Fe3O4+4H2铁的三种氧化物,两种氢氧化物,两种离子的颜色:FeO与Fe3O4均为黑色,Fe2O3为红棕色;Fe(OH)2为白色,Fe(OH)3为红褐色;Fe2+为浅绿色,Fe3+为棕黄色。
第三章第一节 铁及其化合物-高一化学期末复习(人教版2019必修第一册)(解析版)

第三章铁金属材料第一节铁及其化合物铁及其化合物,是高中阶段学习的非常典型的一种变价金属元素系列,这一部分内容和氧化还原理论联系密切,又和好多的实验物质制备,工业产品生产相关联,所以在实验题和化学工艺流程题中经常见到铁及其化合物的身影,为了好好掌握,还是先看看价类二维图吧!一、铁及其化合物的颜色铁粉是黑色的;铁块是银白色的Fe2+—浅绿色Fe3O4—黑色晶体Fe(OH)2—白色沉淀Fe3+—黄色Fe(OH)3—红褐色沉淀Fe(SCN)3—血红色溶液FeO—黑色粉末Fe2O3—红棕色粉末FeS—黑色固体这部分内容有时候作为基础题考察记忆颜色的准确性,更多的时候是作为一些推断题的突破口。
(2020·浙江高一月考)下列关于Na、Fe及其化合物的说法不正确的是A.Na着火时不能使用泡沫灭火器灭火B.Na2O在空气中久置变为Na2CO3C.Fe2O3常用作油漆、涂料的红色颜料D.铁粉与水蒸气反应生成黑色的氧化亚铁【答案】D【详解】A.Na着火时生成的过氧化钠可以和泡沫灭火器喷出的CO2反应生成O2,使燃烧更旺,故A 正确;B.Na2O在空气中与水反应生成NaOH,NaOH与CO2反应生成Na2CO3,所以Na2O在空气中久置变为Na2CO3,故B正确;C. Fe2O3是红棕色固体,常用作油漆、涂料的红色颜料,故C正确;D. 铁粉与水蒸气反应生成黑色的四氧化三铁,故D错误;答案选D。
二、铁与水蒸气反应的实验探究常温下,铁与水不反应,只有在高温条件下,Fe才会与水蒸气反应。
实验时只要注意以下细节,就能顺利完成。
a、棉花最好是一整块的,揉捏到合适大小后伸入试管底部。
如果只有多块小棉花,则必须沿试管的纵向,用较大的包裹较小的,然后再塞入。
不要把小块棉花简单堆积,因热水沸腾时会使外面的棉花冲出,一旦接触到高温铁粉,一方面使水突然剧烈沸腾,另一方面降低了铁粉的温度,不利于反应。
b、铁粉的用量要较多,铺满中部试管为宜,略有鼓起,最好较为集中,因火焰的加热面积有限(可观察直接加热区域与两端铁粉变化的区别)。
高中化学:第三章金属及其化合物铁的重要化合物

第3课时铁的重要化合物1.铁(1)铁的存在铁元素在地壳中的含量仅次于氧、硅和铝,主要以+2和+3价化合物的形式存在。
(2)物理性质铁是银白色金属,具有金属光泽,质软,熔沸点高,具有良好的导电、导热性,可以被磁铁吸引,也可以被磁化。
铁粉呈黑色。
2.铁的氧化物(1)物理性质。
①氧化亚铁(FeO):不溶于水的黑色粉末。
②氧化铁(Fe2O3):俗称铁红,不溶于水的红棕色粉末。
③四氧化三铁(Fe3O4):俗称磁性氧化铁,不溶于水的黑色晶体.(2)化学性质.①稳定性Fe2O3、Fe3O4较稳定;FeO不稳定,受热能氧化为Fe3O4。
②与酸反应:FeO、Fe2O3是碱性氧化物,与盐酸反应的离子方程式。
FeO:FeO+2H+===Fe2++H2O;Fe2O3:Fe2O3+6H+===2Fe3++3H2O。
(3)用途:Fe2O3常用作红色油漆和涂料,赤铁矿主要成分是Fe2O3,是炼铁原料。
3.铁的氢氧化物(1)物理性质Fe(OH)2Fe(OH)3色、白色固红褐色态体固体溶解性难溶于水(2)化学性质①稳定性:Fe(OH)2在空气中易转化为Fe(OH)3,化学方程式:4Fe(OH)2+O2+2H2O===4Fe(OH)3;反应现象:白色沉淀迅速变为灰绿色,最终变为红褐色。
Fe(OH)3受热易发生分解,化学方程式是2Fe(OH)3错误!Fe2O3+3H2O,②与盐酸反应(离子方程式)。
Fe(OH)2:Fe(OH)2+2H+===Fe2++2H2O;Fe(OH)3:Fe(OH)3+3H+===Fe3++3H2O.(3)制备(离子方程式).制备Fe(OH)2:Fe2++2OH-===Fe(OH)2↓。
制备Fe(OH)3:Fe3++3OH-===Fe(OH)3↓。
4.铁盐和亚铁盐(1)Fe2+和Fe3+的检验。
(2)Fe2+与Fe3+的转化。
①实验及现象。
―→溶液由棕黄色变为浅绿色,离子方程式:2Fe3++Fe===3Fe2+↓―→无明显现象↓―→溶液变为红色离子方程式:2Fe2++Cl2===2Fe3++2Cl-②结论.Fe3+错误!Fe2+(3)铁盐的净水作用:向混有少量泥沙的浑水中加入少量Fe2(SO4)3(或明矾),浑水会变澄清。
高中化学必修一铁及其化合物

高中化学必修一铁及其化合物要点一:单质铁的物理及化学性质1、铁单质的物理性质铁具有金属的通性,具有被吸引的特性,一般铁粉为黑色,铁块为银白色。
2、化学性质3、注意事项(1)铁与弱氧化剂(如S、I2、H+、Fe3+、Cu2+)等反应所得产物为Fe2+,铁元素的价态为+2价。
(2)铁与强氧化剂(如Cl2、Br2、浓H2SO4、硝酸等)反应所得产物为Fe3+,铁元素的价态为+3价。
①在氯气中燃烧,只生成氯化铁;与稀硝酸反应时则先产生+3价铁,若铁过量时则+3价铁再变为+2价铁;②铁在常温下遇到冷的浓硫酸、浓硝酸时发生钝化,属于化学反应。
(3)铁在纯氧中燃烧以及在高温下与H2O(g)反应得到的产物为Fe3O4,铁元素的价态为+2、+3价。
(4)铁不能与冷、热水反应,但能与水蒸气反应,与水蒸汽反应的产物也是Fe3O4。
典型例题1、某稀溶液中含有4mol KNO3和2.5mol H2SO4,向其中加入1.5mol Fe,充分反应(已知NO3﹣被还原为NO).下列说法正确的是()A.反应后生成NO的体积为28 LB.所得溶液中c(Fe2+):c(Fe3+)=1:1C.所得溶液中c(NO3﹣)=2.75 mol/LD.所得溶液中的溶质只有FeSO4解:溶液中氢离子总物质的量为:n(H+)=2.5mol×2=5mol,n(NO3﹣)=4mol,铁粉的物质的量为1.5mol,由3Fe+2NO3﹣+8H+=3Fe2++2NO↑+4H2O,3 2 81.5mol 1mol 4mol,则1.5molFe完全反应时,硝酸根离子与氢离子均过量,则发生Fe+NO3﹣+4H+=Fe3++NO↑+2H2O,若1.5molFe完全反应时,氢离子不足,则两个反应均发生,Fe+NO3﹣+4H+=Fe3++NO↑+2H2Ox 4x x x3Fe+2NO3﹣+8H+=3Fe2++2NO↑+4H2Oy y y y则:x+y=1.5、4x+y=5,解得:x=0.75mol,y=0.75mol生成NO的体积为(0.75mol+0.75mol×)×22.4L/mol=28L,A.根据分析可知,反应后生成标况下28LNO,不是标况下,NO气体不一定为28L,故A错误;B.反应后生成铁离子为0.75mol,亚铁离子为0.75mol,c(Fe2+):c(Fe3+)=n(Fe2+):n(Fe3+)=1:1,故B正确;C.反应消耗硝酸根离子等于生成NO的量=0.75mol+0.75mol×=1.25mol,缺少溶液体积,无法计算溶液中硝酸根离子浓度,故C错误;D.反应后中含有硫酸铁和硫酸亚铁,故D错误;故选B.变式训练1、向500mL 2mol/L 的CuSO4溶液中插入一块铁片,反应片刻后取出铁片,经洗涤、烘干,称其质量比原来增重2.0g.下列说法错误的是(设反应后溶液的体积不变)()A.则此过程中参加反应的铁的质量是14gB.析出铜物质的量是0.25molC.反应后溶液中溶质物质的量浓度:c(CuSO4)=1.5mol/LD.反应后溶液中溶质物质的量浓度:c(FeSO4)=1.5mol/L2、将15g两种金属的混合物投入足量的盐酸中,反应完全后得到11.2L H2(标准状况),该混合物的组成可能是()A.钠和铁B.镁和铜C.铝和镁D.锌和铁要点二:铁的氧化物要点三:铁的氢氧化物1、常见的物理及化学性质4Fe(OH)2 + O2 + 2H2O =4Fe(OH)32Fe(OH)3Fe2O3+3H2O(受热分解)(2)Fe(OH)2的制备Fe(OH)2易被空气中的氧气氧化,生成Fe(OH)3,所以在制备Fe(OH)2时:①要确保Fe2+溶液中无Fe3+,故需加Fe粉,把Fe3+转化为Fe2+。
3.1 铁及其化合物 讲义【新教材】人教版(2019)高中化学必修一(知识点+习题+作业)

第三章铁金属材料第一节铁及其化合物【必备方程式】知识点一铁的单质一、铁元素的存在1、含量铁元素在地壳中的含量仅次于氧、硅和铝。
2、存在形态(1)游离态:存在于陨铁中。
(2)化合态:主要以+2、+3价铁的化合物存在。
如黄铁矿(FeS2)、赤铁矿( Fe2O3)、磁铁矿(Fe3O4)、菱铁矿(FeCO3)等。
【习题】判断正误。
(1)铁元素在地壳中含量位于第三位。
()(2)在工业中炼制铁单质,所以自然界中无游离态铁。
()(3)工业炼铁,需加入还原剂。
()(4)钢和铁都是铁的合金,钢不易生锈,生铁易生锈,铁锈的主要成份是Fe3O4。
()二、铁的单质1、物理性质:银白色光泽、密度大,熔沸点高,延展性、导电、导热性较好、能被磁铁吸引。
2、化学性质:铁是较活泼的金属,铁原子的最外层电子数为2个,可失去2个或3个电子而显+2价或+3价,但+3价的化合物较稳定。
①与非金属反应:3Fe + 2O2Fe3O42Fe + 3C122FeCl3说明:铁丝在氯气中燃烧时,生成棕黄色的烟,加水振荡后,溶液显黄色。
△Fe + S FeS说明:铁跟氯气、硫反应时,分别生成+3价和+2价的铁,说明氧化性:氯气>硫。
①与水反应:A.在常温下,在水和空气中的O2、CO2等的共同作用下,Fe易被腐蚀(铁生锈)。
B.在高温下,铁能与水蒸气反应生成H2:3Fe + 4H2O(g)Fe3O4 + 4H2①与酸反应:A.与非氧化性酸(如稀盐酸、稀H2SO4等)的反应。
例如:Fe + 2H+Fe2++ H2↑B.铁遇到冷的浓H2SO4、浓HNO3时,产生钝化现象,因此金属铁难溶于冷的浓H2SO4或浓HNO3中。
但在加热条件也可以反应。
①与比铁的活动性弱的金属的盐溶液发生置换反应。
例如:Fe + Cu2+Fe2++ Cu【习题】1、下列物质中,不能与铁发生化学反应的是()A.盐酸B.氯化铁溶液C.氢氧化钠溶液D.氯气2、下列关于铁的叙述正确的是()。
高中化学(新人教版)必修第一册:铁及其化合物【精品课件】

+2 自然界中以
价和
+3 价化合物的形式存在。铁单质在
陨铁 的形态存在。
2.物理性质
纯净的铁是光亮的 银白 色金属,密度较大,熔点较高。具
有
导热性 、
磁体 吸引。
导电 ___ 性 、
延展 性 , 能 被
3.化学性质
(1)与非金属反应
2Fe+3Cl2=点==燃==__2_F_e_C_l_3_ 3Fe+2O2=点==燃==__F_e_3O__4 __ (_2_)_与__水3_F_反e_+_应_4_H_2_O_(_g_)=_高_=_=温_=_=_F_e_3O__4+__4_H__2 _ (3)与酸反应 ____F_e_+__2_H_C_l_=_=_=_F_e_C_l_2_+_H__2_↑________ (4)与盐溶液反应 Fe+CuSO4===_F_e_S_O_4_+__Cu 结论:铁在化学反应中做为还原剂:
_明__含__F_e_3_+_______________________________________________。 (3)保存 C 溶液时要加固体 A 的原因是__防__止__F_e_2_+_被__O__2 氧__化_______。
(4)写出下列转化的离子方程式: ①D→C:_2_F_e_3+_+__F_e_=_=_=_3_F_e_2_+__________; ②C→D:_2_F_e_2+_+__C_l_2_=_=_=_2_F_e_3+_+__2_C__l-____。
如 2Fe3++Cu===2Fe2++Cu2+ 3CO+Fe2O3==△===2Fe+3CO2
与 Fe3+、Fe2+有关的离子共存问题: ①Fe3+与 I-、S2-、HS-、SO23-、HSO- 3 等因发生氧化还原反应而 不能大量共存。
高中铁及其化合物教案化学

高中铁及其化合物教案化学教学内容:高中化学——铁及其化合物教学目标:学生能够掌握铁及其在日常生活和工业中的应用,理解铁的性质、反应特性以及相关化合物的性质和制备方法。
教学重点:铁的性质、反应特性、制备方法以及常见的铁化合物。
教学难点:理解铁在氧气和酸中的反应特性,掌握铁的制备方法及其在工业中的应用。
教学准备:教学课件、实验器材、教学资料等。
教学过程:一、铁的性质及制备方法1. 铁的性质:介绍铁的物理性质和化学性质,重点讲解铁的磁性、铁的稳定性等。
2. 铁的制备方法:简要介绍铁的提取方法,如高炉法、直接还原法等。
二、铁的化合物及其性质1. FeO(氧化铁):介绍FeO的性质、制备方法以及在工业生产和日常生活中的应用。
2. Fe2O3(三氧化二铁):讲解Fe2O3的性质、制备方法以及在颜料和磁性材料中的应用。
3. Fe3O4(亚铁氧化铁):探讨Fe3O4的性质、制备方法以及在制备磁性材料中的应用。
三、实验环节1. 实验一:观察铁与氧气的反应产物,观察其物理性质和化学性质。
2. 实验二:用盐酸溶液浸泡铁片,观察反应产生气体,验证铁的酸性反应特性。
四、课堂讨论1. 根据实验结果,讨论铁在氧气和酸中的反应特性。
2. 探讨铁在工业生产中的应用和为什么选择铁作为原料。
五、作业布置1. 完成相关的练习题和实验报告。
2. 阅读相关教材,了解更多有关铁及其化合物的知识。
教学结束后,学生应该能够全面了解铁及其化合物的性质、反应特性和制备方法,以及在日常生活和工业中的应用。
同时,能够对铁的性质和化合物有更深入的理解,为今后学习化学提供坚实的基础。
高中化学《铁及其化合物》优质课教学设计、教案

教学设计:考纲要求:1.理解Fe 的化学性质,铁的重要化合物。
2.理解以Fe2+、Fe3+的相互转化为例,理解变价金属元素的氧化性、还原性。
3.使学生掌握实验探究活动的一般步骤和方法。
(即发现问题→形成课题→建立假说→检验论证→评价发展)通过小组讨论、口语汇报的形式锻炼学生的表达能力。
4.通过探究铁及其化合物的氧化性和还原性,培养学生用发展的眼光、科学的态度、勇于探索的品质学习化学;通过创设问题情景,营造宽松和谐的学习气氛诱导学生积极思维,激发学生的学习兴趣和求知欲望。
教学环节教学活动设计意图小组合作铁处于元素周期表中什么位置?画出铁的原子结构示意图并分析铁的原子结构特点及主要化合价根据原子结构分析铁的常见价态26Fe 位于第四周期第VIII 族通过原子结构分析化合价,加深学生对元素周期表的理解铁的主要化合价为+2、+3:Fe- 2e- = Fe2+Fe-3e- =Fe3+小组合作总结铁跟哪些物质反应能生成+2 价铁的化合物?跟哪些物质反应能生成+3 价铁的化合物?从氧化还原的角度找氧化剂还原剂找到常见的氧化剂分辨它们氧化性的相对强弱小组合作铁的重要氧化物有哪些?它们各有哪些重要的性质?从铁与氧气反应条件的不同得到反应产物不同,从而复习铁的三种氧化物氧化物FeO Fe2O3 Fe3O4FeO+2H+=Fe2++H2OFe2O3+6H+=2Fe3++3H2O色态黑色粉末红棕色粉末磁性黑色Fe3O4+ 8H +=Fe2++2Fe3++4H2O 晶体,俗称 铁红 磁性氧化铁小组合作 铁的氢氧氧化物有哪些?它们各有哪些重要的性质?Fe (OH )2 Fe (OH )3特别强调氢氧化亚铁的不稳定白色不溶固体 红褐色不溶固体 性,易被氧气氧化为氢氧化铁 4Fe(OH)2+O 2+2H 2O=4Fe(OH)3白色沉淀迅速变成灰绿色,最后变成红褐色实验探究 如何制取铁的氢氧氧化物? 培养学生思维的发散性,通过实验现象得出实验结论讨论研究讨论研究方法,设计实验方案方法, 设分小组谈论,然后小组评价计实验方案小组活动 如何实现Fe 2+和Fe 3+之间的相互 探讨铁及其化合物的氧化性和转化?还原性交流探究结果,总结相互转化关系合理选用氧化剂和还原剂交流探究如何检验溶液中Fe 2+ 和Fe3+的存在小组展示对学生总结的规律进行总结性描述有利于学生形成完整准确的认识小组活动实验室中如何保存铁盐和亚铁盐?如何配制其溶液?小组展示亚铁盐:因Fe 2+易被氧化,其晶体应密封保存。
高中化学铁及其化合物教学设计

高中化学铁及其化合物教学设计一、教学任务及对象1、教学任务本节课的教学任务是针对高中化学课程中的铁及其化合物进行深入讲解,通过引导学生学习铁的化学性质、铁的常见化合物及其应用,使学生能够掌握铁元素在化学反应中的变化规律,培养他们的化学思维和实验操作能力。
此外,本节课还将结合生活实际,让学生了解铁及其化合物在现实生活中的应用,提高他们的学习兴趣和社会责任感。
2、教学对象本节课的教学对象为高中二年级的学生,他们在之前的化学学习中已经掌握了原子结构、元素周期律等基础知识,具备了一定的化学素养。
此外,学生在初中阶段已经接触过铁的化学性质,但对于铁及其化合物的深入了解和应用尚显不足。
因此,本节课将针对学生的知识水平和认知特点,采用适当的教学策略,帮助他们更好地理解和掌握铁及其化合物的相关知识。
二、教学目标1、知识与技能(1)理解铁的化学性质,掌握铁的常见化合物及其化学式,了解铁及其化合物在化学反应中的变化规律。
(2)学会运用化学知识解释铁及其化合物在生活中的应用,提高理论联系实际的能力。
(3)通过实验操作,掌握铁及其化合物的制备和检验方法,培养实验操作能力和观察能力。
(4)培养运用化学方程式进行计算的能力,提高解决实际问题的化学素养。
2、过程与方法(1)采用以退为进的教学策略,引导学生从已知的铁的性质出发,逐步深入探讨铁及其化合物的相关知识。
(2)运用以点带面的方法,通过讲解典型的铁及其化合物实例,帮助学生掌握铁元素在化学反应中的普遍规律。
(3)通过以动带静的教学方式,组织学生进行实验操作,使他们在实践中掌握铁及其化合物的制备和检验方法。
(4)利用问题驱动法,引导学生主动思考、发现问题,培养他们的探究精神和解决问题的能力。
3、情感,态度与价值观(1)激发学生对化学学科的兴趣,培养他们热爱科学、追求真理的情感。
(2)通过学习铁及其化合物在生活中的应用,使学生认识到化学知识对人类社会的贡献,增强社会责任感和使命感。
人教版高中化学必修第一册 第三章 第一节 第二课时《铁及其化合物》

酸
物质 类别
1.下列有关铁的化合物的说法不正确的是( ) A. FeO不稳定,在空气中加热生成Fe2O3 B. FeO、Fe2O3均为碱性氧化物,均可与盐酸反应 C. Fe(OH)3可通过化合反应得到,Fe(OH)2则不能 D. Fe3O4为磁性氧化铁,其中铁的化合价为+2和+3
2.有关铁的氧化物的说法中,不正确的是( ) A. 赤铁矿主要成分是Fe2O3,Fe2O3俗称铁红,常用作红
胶头滴管 伸入液面
以下
加热 煮沸
现配 现用
(3) Fe(OH)2制备实验改进
实验名称
改进实验
装置图
药品
NaOH溶液、铁屑、稀H2SO4
思考 该实验能较长时间保持白色沉淀,其理由是?
三、课堂小结
化合价
Fe
酸
Fe2O3 △Fe(OH)3 酸 Fe3+
碱
Fe3O4 氧 化 剂 FeO
氧 化 剂
Fe(OH)2 酸 Fe2+ 碱
Fe2O3+6H+ = 2Fe3++3H2O FeO+2H+= Fe2++H2O
二、铁的氢氧化物 1. Fe(OH)3 (1) Fe(OH)3制备
实验名称 制备原理
氢氧化铁制备 Fe3++3OH-=Fe(OH)3↓
实验装置图
实验现象
有红褐色沉淀
(2) Fe(OH)3性质
化学式 物理性质
化合价角度
高中化学人教版必修第一册 第三章 第一节 第二课时
《铁及其化合物》
化合价
Fe2O3 Fe(OH)3 Fe3O4 FeO Fe(OH)2
Fe
物质
类别
一、铁的氧化物 1.物理性质
化学式 俗名
颜色状态
FeO \ 黑色粉末
高中化学《铁及其化合物》教案

课题备课人:时间:课型:学情分析学生已经掌握了氧化还原反应的判断,以及物质的氧化性和还原性。
铁是生活中常见的元素,并且是具有可变价态的金属。
这一部分的学习,可以帮助学生通过实际的化学反应进一步理解氧化还原反应。
教学目标1、能列举描述以及辨识铁及其重要化合物的重要性质、化学性质及实验现象。
2、能设计氢氧化亚铁的制备方案。
3、能说出Fe2+、Fe3+的检验及其相互转化。
重难点不同价态铁的化合物间的转化规律授课流程、内容、时间双边活动设计意图一、引入:时间---1、如果人体缺铁,会出现什么症状?怎么办?2、铁元素都有那些常见化合价?不同价态能体现出什么性质?板书课题 2.3.3 铁及其化合物的性质二、出示学习目标:时间---1、能列举描述以及辨识铁及其重要化合物的重要性质、化学性质及实验现象。
2、能设计氢氧化亚铁的制备方案。
3、能说出Fe2+、Fe3+的检验及其相互转化。
三、出示自学指导:时间---阅读课本53-56页,填写学案中知识梳理部分。
四、后教:时间-----一、铁元素的存在1.铁的物理性质:地壳含量_____,纯铁为_____,熔沸点______,良好的____________。
2.存在形态:(1)_____态:0价(_______)(2)_____态:+2,+3价(矿石,如黄铁矿:_____赤铁矿:______磁铁矿:______、菱铁矿:_____)3化学性质:以及Fe + S加热条件下生成FeS,Fe +H2O (g)高温条件下生成Fe3O4和H2_________________________________________。
高中化学:铁及其化合物

高中化学:铁及其化合物高中化学:铁及其化合物在本文中,我们将了解铁的主要性质及应用,以及铁的重要化合物的主要性质及应用。
我们将以Fe2+、Fe3+的相互转化为例,理解变价金属元素的氧化还原反应。
铁的存在和主要性质铁是一种活泼的元素,具有较强的还原性,主要化合价为+2价和+3价。
铁的化学性质包括:1)与非金属单质的反应①与氧气的反应:在常温下,铁被腐蚀生成铁锈,其主要成分为Fe2O3·xH2O。
点燃铁可以生成Fe3O4.②与氯气的反应:2Fe+3Cl2→2FeCl3.③与硫的反应:Fe+S→FeS。
2)与水的反应在常温下,铁与水不反应,但在高温条件下与水蒸气反应:3Fe+4H2O(g)→Fe3O4+4H2.3)与酸的反应①与非氧化性酸反应的离子方程式:Fe+2H+→Fe2++H2↑。
②与氧化性酸反应的离子方程式:遇冷的浓硫酸或浓硝酸钝化,与稀硝酸或在加热条件下与浓硫酸、浓硝酸反应的离子方程式为Fe+4H++NO-3→Fe+NO↑+2H2O。
4)与某些盐溶液的反应①与CuSO4溶液反应的离子方程式:Fe+Cu2+→Cu+Fe2+。
②与FeCl3溶液反应的离子方程式:Fe+2Fe3+→3Fe2+。
铁的重要化合物铁的氧化物包括FeO、Fe2O3、Fe3O4,它们分别与盐酸反应的离子方程式为:XXX→Fe2++H2O、Fe2O3+6H+→2Fe3++3H2O、XXX与硝酸反应的化学方程式为:3FeO+10HNO3→3Fe(NO3)3+NO↑+5H2O。
铁的氢氧化物包括Fe(OH)2和Fe(OH)3,它们与H+反应的离子方程式为:Fe(OH)2+2H+→Fe2++2H2O、2Fe(OH)3+6H+→2Fe3++6H2O。
铁的氢氧化物有不同的色态和价态,例如氧化亚铁(FeO)、氧化铁(Fe2O3)和四氧化三铁(Fe3O4)等。
的制备方法改写为:可以将FeCl3和NaOH溶液反应得到Fe(OH)3沉淀,再将其加热分解得到Fe2O3在空气中继续加热,Fe2O3会被氧化成Fe3O44.亚铁盐和铁盐的性质改写为:1)亚铁盐含有Fe2+的溶液呈浅绿色,Fe2+既具有氧化性,也具有还原性。
高中化学-铁及其化合物

高中化学 - 铁及其化合物第3 讲铁及其化合物一、铁1、位置、结构:(1)Fe 位于第四周期第VIII 族(过渡元素);(2)原子结构示意图:(3)常见离子: Fe 3+(强氧化性)Fe2+(强还原性)。
3、物理性质:(1)纯铁抗蚀能力强(2)具有一般金属的物理通性。
(3)黑色金属(铁铬锰)4、化学性质:较活泼(1)与非金属单质:点燃3Fe + 2O 2 Fe 3O4Fe + S =△== FeS点燃2Fe + 3Cl 2 2FeCl 3 (棕黄色烟)(2)与H2O高中化学 - 铁及其化合物3Fe + 4H 2O(g)Fe 3O4 + 4H 2 (3)与酸①与非氧化性酸:如盐酸、稀硫酸Fe + 2H + = Fe 2+ + H 2↑ ②与氧化性酸:如浓硫酸、浓硝酸、稀硝酸Fe+4HNO3(稀)=Fe(NO3)3+NO↑ +2H2O 2Fe+6H2SO4(浓)=△==Fe2(SO4) 3 +3SO2↑+6H2O (常温钝化)Fe+6HNO3(浓)=△==Fe(NO3)3+3NO2↑+3H2O (常温钝化)(4)与盐:Fe + Cu 2+ = Fe 2+ + CuFe + 2Fe 3+ = 3Fe 2+二、铁的氧化物和氢氧化物1、氧化物高中化学 - 铁及其化合物2、铁的氢氧化物高中化学 - 铁及其化合物[ 注] 制取Fe(OH)2时, 为什么要用新制的FeSO4 溶液?为什么要将吸有NaOH溶液的胶头滴管插入液面以下?三、Fe 和Fe 的相互转化网络图:高中化学 - 铁及其化合物FeS FeO Fe2+Fe(OH)2(1) 判断离子共存① Fe2+、Fe3+均水解,与HCO3-、[Al(OH)4] -、CO32-等因水解相互促进在溶液中不能大量共存② Fe3+与S2-、I -、HS-、SO32-,Fe2+与NO3-(H+) 、ClO-、MnO4-(H+)在溶液中因氧化还原反应不能大量共存。
(2)盐溶液的配制与保存① Fe2+的盐溶液:加少量铁粉,防止Fe2+被氧化;加少量相应的酸,防止Fe2+水解。
高中化学知识点:铁及其化合物
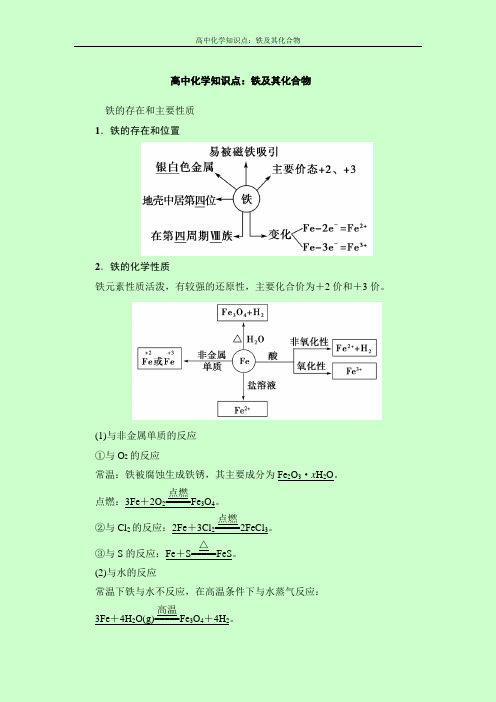
高中化学知识点:铁及其化合物铁的存在和主要性质 1.铁的存在和位置2.铁的化学性质铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
(1)与非金属单质的反应 ①与O 2的反应常温:铁被腐蚀生成铁锈,其主要成分为Fe 2O 3·x H 2O 。
点燃:3Fe +2O 2=====点燃Fe 3O 4。
②与Cl 2的反应:2Fe +3Cl 2=====点燃2FeCl 3。
③与S 的反应:Fe +S=====△FeS 。
(2)与水的反应常温下铁与水不反应,在高温条件下与水蒸气反应: 3Fe +4H 2O(g)=====高温Fe 3O 4+4H 2。
(3)与酸的反应①与非氧化性酸反应的离子方程式:Fe+2H+===Fe2++H2↑。
②与氧化性酸遇冷的浓硫酸或浓硝酸钝化,与稀硝酸或在加热条件下与浓硫酸、浓硝酸反应无H2产生。
Fe与足量稀HNO3反应的离子方程式为Fe+4H++NO-3===Fe3++NO↑+2H2O。
(4)与某些盐溶液的反应①与CuSO4溶液反应的离子方程式:Fe+Cu2+===Cu+Fe2+。
②与FeCl3溶液反应的离子方程式:Fe+2Fe3+===3Fe2+。
铁的重要化合物1.铁的氧化物氧化亚铁(FeO) 氧化铁(Fe2O3) 四氧化三铁(Fe3O4) 俗名铁红磁性氧化铁色态黑色粉末红棕色粉末黑色晶体铁元素价态+2 +3 +2、+3 说明:①FeO、Fe2O3、Fe3O4分别与盐酸反应的离子方程式:FeO+2H+===Fe2++H2O、Fe2O3+6H+===2Fe3++3H2O、Fe3O4+8H+===2Fe3++Fe2++4H2O。
②FeO与硝酸反应的化学方程式:3FeO+10HNO3===3Fe(NO3)3+NO↑+5H2O。
2.铁的氢氧化物Fe(OH)2Fe(OH)3色态白色固体红褐色固体与H+反应Fe(OH)2+2H+=== Fe2++2H2O Fe(OH)3+3H+=== Fe3++3H2O二者的关在空气中,Fe(OH)2能够非常迅速地被氧气氧化成Fe(OH)3,现象是白色絮状沉淀迅速变成灰绿色,最后变成红褐色,反应方程式为4Fe(OH)2+系O2+2H2O===4Fe(OH)3说明:Fe(OH)2、Fe(OH)3的制备可利用相应亚铁盐、铁盐与碱液反应。
高中化学知识点:铁及其化合物

高中化学知识点:铁及其化合物
铁的性质
- 铁是一种金属元素,符号为Fe,原子序数为26。
- 铁是一种有色金属,具有良好的导电性和导热性。
- 铁在常温下是固态,可以延展和变形。
铁的化合物
氧化铁
- 氧化铁是铁常见的氧化物,由铁和氧组成。
- 三种常见的氧化铁是氧化亚铁(FeO)、氧化铁(Fe2O3)和氧化铁(Fe3O4)。
- 氧化亚铁是黑色的,氧化铁是红色的,氧化铁是黑色的。
铁的酸性氧化物
- 铁还可以形成酸性氧化物,可以和酸反应生成盐和水。
- 铁的酸性氧化物有氧化铁(Fe2O3)和氧化铁(Fe3O4)。
金属铁
- 金属铁是纯铁,具有较高的熔点和延展性。
- 金属铁通常用于制造各种工具和建筑材料。
铁的应用
- 铁是常见的金属材料,在工业和日常生活中有广泛的应用。
- 铁通常用于制造建筑材料、机械、电器、车辆等。
- 铁的化合物也有一些应用,例如氧化铁可以用于制作颜料。
总结
铁是一种有色金属,具有良好的导电性和导热性。
铁的主要化合物是氧化铁。
铁及其化合物在工业和日常生活中有广泛的应用。
高中化学必修第一册铁及其化合物

Fe3++3OH-=
Fe2++2OH-=Fe(OH)2↓
Fe2++2OH-=Fe(OH)2↓
程式
Fe(OH)3↓ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
?
【思考与讨论】由实验3-1可知,白色的氢氧化亚铁会被 溶解在溶液中的氧气氧化。那么,在实验室里,
Байду номын сангаас
如何使生成白色的氢氧化亚铁保持较长时间以便于观察?
实验3-3
向FeCl3溶液 中加入少量铁
粉。充分反应
后加入几滴 KSCN溶液。
现象 不显红色
把上层清液
倒入另一只试 管中,再滴入 几滴氯水。
溶液显红色
反应的方程式 2FeCl3+Fe = 3FeCl2 2Fe3++Fe = 3Fe2+
2FeCl2+Cl2 = 2FeCl3 2Fe2++Cl2=2Fe3++2Cl-
第2课时
名称
氧化亚铁 氧化铁 四氧化三铁
温
故 而
共 与酸
知
FeO + 2H+ = Fe2+ + H2O Fe2O3 + 6H+ = 2Fe3+ + 3H2O Fe3O4 + 8H+ = 2Fe3+ + Fe2+ + 4H2O
新 :
高温
FeO + CO === 2Fe + 3CO2
性 与还原剂
高温
具有 还原性
较强的氧化剂(O2、 Cl2、Br2、H2O2、浓 H2SO4 、HNO3 等)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学:铁及其化合物
1.了解铁的主要性质及应用。
2.了解铁的重要化合物的主要性质及应用。
(中频)
3.以Fe 2+、Fe 3+的相互转化为例,理解变价金属元素的氧化还原反应。
(高频)
铁的存在和主要性质 1.铁的存在和位置
2.铁的化学性质
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
(1)与非金属单质的反应 ①与O 2的反应
常温:铁被腐蚀生成铁锈,其主要成分为Fe 2O 3·x H 2O 。
点燃:3Fe +2O 2=====点燃
Fe 3O 4。
②与Cl 2的反应:2Fe +3Cl 2=====点燃
2FeCl 3。
③与S 的反应:Fe +S=====△
FeS 。
(2)与水的反应
常温下铁与水不反应,在高温条件下与水蒸气反应: 3Fe +4H 2O(g)=====高温
Fe 3O 4+4H 2。
(3)与酸的反应
①与非氧化性酸反应的离子方程式:Fe +2H +===Fe 2++H 2↑。
②与氧化性酸
遇冷的浓硫酸或浓硝酸钝化,与稀硝酸或在加热条件下与浓硫酸、浓硝酸反
应无H 2产生。
Fe 与足量稀HNO 3反应的离子方程式为Fe +4H ++NO -3===Fe
3+
+NO ↑+2H 2O 。
(4)与某些盐溶液的反应
①与CuSO 4溶液反应的离子方程式:Fe +Cu 2+
===Cu +Fe 2+。
②与FeCl 3溶液反应的离子方程式:Fe +2Fe 3+===3Fe 2+。
铁的重要化合物 1.铁的氧化物
说明:
①FeO 、Fe 2O 3、Fe 3O 4分别与盐酸反应的离子方程式: FeO +2H +===Fe 2++H 2O 、 Fe 2O 3+6H +===2Fe 3++3H 2O 、 Fe 3O 4+8H +===2Fe 3++Fe 2++4H 2O 。
②FeO 与硝酸反应的化学方程式:
3FeO +10HNO 3===3Fe(NO 3)3+NO ↑+5H 2O 。
2.铁的氢氧化物
说明:Fe(OH)2、Fe(OH)3的制备可利用相应亚铁盐、铁盐与碱液反应。
3.亚铁盐与铁盐
(1)亚铁盐
含有Fe2+的溶液呈浅绿色,Fe2+既有氧化性,又有还原性,Fe2+与Zn、Cl2反应的离子方程式分别为:Zn+Fe2+===Zn2++Fe、2Fe2++Cl2===2Fe3++2Cl-。
(2)铁盐
①氧化性
含有Fe3+的溶液呈棕黄色,Fe3+具有氧化性,Fe3+与Fe、Cu反应的离子方程式分别为:2Fe3++Fe===3Fe2+、2Fe3++Cu===2Fe2++Cu2+。
②特性
含有Fe3+的盐溶液遇到KSCN溶液时变成红色。
1.易误诊断(正确的打“√”,错误的打“×”)。
(1)铁元素性质活泼,自然界中的铁几乎都是以化合态形式存在,只有在陨石中有游离态的铁元素()
(2)过量的铁与氯气反应,不会生成FeCl2,因为铁还原三价铁必须在水溶液中进行()
(3)铁能被磁铁吸引,则任何金属都能被磁铁吸引()
(4)过量的铁粉与稀硝酸溶液反应的离子方程式为
Fe+4H++NO-3===Fe3++NO↑+2H2O()
(5)将NaOH溶液滴入FeSO4溶液中,可以看到稳定的白色沉淀()
(6)FeCl2溶液保存时加Fe粉的目的是防止Fe2+被还原()
(7)FeCl2溶液中加入KSCN溶液不变红,加入氯水后溶液变红色()
(8)FeCl3溶液中加入KSCN溶液变红,再加入足量Fe,红色消失()
【答案】(1)√(2)√(3)×(4)×(5)×(6)×(7)√(8)√。
