体外诊断仪器标准检验-电气安全要求-1
医疗器械检验标准

医疗器械检验标准一、引言医疗器械是现代医疗中不可或缺的重要工具,它们的质量和安全性直接关系到人们的生命和健康。
为了确保医疗器械的质量和安全性,各国都制定了一系列的检验标准。
本文将介绍一些常见的医疗器械检验标准,帮助人们更好地了解和选购医疗器械。
二、体外诊断类器械检验标准体外诊断类器械通常包括试纸、血糖仪、尿常规仪等。
这些器械的准确性和可靠性对于诊断结果的准确性至关重要。
因此,制定相应的检验标准是必要的。
常用的检验项目包括:1. 准确性检验:对于不同的体外诊断类器械,需要测试其准确性和稳定性,确保诊断结果符合临床要求。
2. 可靠性检验:包括器械的重复性、重现性、检出限等指标,以评估其在实际使用中的可靠性。
3. 生物安全性检验:包括对器械使用过程中可能产生的有害物质、细菌等的检测,确保使用者和患者的安全。
三、手术器械检验标准手术器械主要包括手术刀、钳子、缝合线等。
它们的品质和功能对于手术质量有着直接的影响。
常见的手术器械检验标准包括:1. 加工工艺检验:对手术器械的加工工艺进行检验,确保其表面光滑、无裂纹、无锈蚀等。
2. 功能性检验:包括手术器械的耐用性、操作性、切削力等指标,以评估其在手术过程中的功能。
3. 生物相容性检验:手术器械与人体组织接触,因此需要进行生物相容性检验,确保手术器械对人体组织没有损害。
四、诊断治疗设备检验标准诊断治疗设备包括X光机、心电图仪、超声波仪等。
这些设备的质量和准确性直接关系到医生的诊断和治疗效果。
常见的检验标准包括:1. 准确性检验:对诊断治疗设备进行准确性检验,确保其测量结果的准确性和可靠性。
2. 安全性检验:包括电磁辐射、噪声、电气安全等指标,以评估设备在使用过程中对人员和环境的安全性。
3. 健康监测功能检验:对诊断治疗设备的健康监测功能进行检测,确保设备对患者的监测能力。
五、口腔口腔医疗器械主要包括牙刷、牙膏、洗牙器等。
这些器械直接应用于口腔环境,因此对其质量和安全性要求较高。
gb4793.1-2007

实施Gb4793.1-2007以替代GB 4793.1-1995。
GB 4793.1-2007(以下简称GB 4793.1-2007指GB 4793.1-2007)对于许多医疗器械制造商来说是相对陌生的,对标准的理解也不尽相同。
因此,笔者对许多厂商的出厂检验进行了简单分析,希望对大多数医疗器械厂商有所帮助。
同时,我们认为读者具有一定的GB9706.1知识库,因此我们将在本文中讨论GB 4793.1 GB诊断(IVD)设备。
常用的临床分析仪器,如血细胞分析仪,化学分析仪和尿液分析仪,属于GB 4793.1的适用范围。
对于医疗体外诊断设备,国家食品药品监督管理局发布了行业标准YY 0648-2008“测量,控制和实验室使用的电气设备的安全要求2-101:体外诊断(IVD)医疗设备的特殊要求””,它将在2009年在工厂进行GB4793.1的检查,并且医疗器械制造商相对熟悉GB 9706.1医用电气设备。
由于具有通用安全标准,许多企业在制定产品注册标准和进行产品生产时会不自觉地参考GB 9706.1。
交货检验。
他们认为GB 4793.1也是一种保护性接地阻抗,泄漏电流和介电强度的测试,通常称为“旧三者”,但事实并非如此:GB 4793.1 4.1测试摘要中明确规定:制造商应对制造商生产的9706.1进行简单比较,以利于理解GB 4793.1。
当然,由于作者水平的限制,一些观点是基于对标准附录的100%理解,因此不可避免地会在设计中存在一些缺陷。
我们欢迎同行专家提出批评和指正。
例行测试:F.1保护性接地,F.2电源电路,F.3其他电路。
F.1防护接地试验GB4793.1的适用范围GB 4793.1适用于医疗器械行业的医疗测量,控制和实验室电气设备,是指用于测量,指示,监测或分析物质的设备或所用设备用于准备材料,包括在体外进行的保护接地阻抗的测量与在类型试验中的测量不同。
指定的测试是在设备输入插座的接地插头或电源插头的接地插头或保护导体端子之间进行接地导通永久连接的设备和所有可触及的导电部件,用于保护性接地。
化学发光体外诊断系统产品注册技术审查指导原则

化学发光体外诊断系统产品注册技术审查指导原则本指导原则的目的是为了帮助注册申请人准备和撰写化学发光体外诊断试剂和仪器的注册申报资料,并为技术审评部门提供参考。
申请人应根据产品特性确定本指导原则是否适用,并在不适用时提供相应的科学依据。
本指导原则适用于直接/酶促/电化学发光检测的全自动或半自动化学放光免疫分析仪及配套试剂。
综述资料是申请人提交的重要资料之一,包括产品预期用途、产品描述、生物安全性说明、研究结果的总结评价以及同类产品上市情况介绍等。
同类产品上市情况介绍部分应着重比较拟申报产品与已获批准的同类产品之间的主要区别。
对于新诊断试剂产品,还需提供被测物与预期适用的临床适应症之间关系的文献资料。
二)技术资料技术资料主要包括产品的组成、制备工艺、性能指标、使用说明、质量标准、稳定性、储存条件、包装、标签等方面的资料。
其中,性能指标应包括灵敏度、特异性、准确性、重复性、检出限、线性范围等指标。
使用说明应包括试剂和仪器的使用方法、操作步骤、注意事项、常见问题解答等内容。
三)生物安全性资料生物安全性资料主要包括试剂和仪器对人体、动物、环境等的影响评估资料。
其中,人体安全性评估资料应包括对人体的毒理学、免疫学、过敏学等方面的评估结果。
动物实验安全性评估资料应包括对实验动物的毒理学、免疫学、过敏学等方面的评估结果。
环境安全性评估资料应包括试剂和仪器对环境的影响评估结果。
四)质量控制资料质量控制资料主要包括质量控制方案、质量控制结果、质量控制记录等。
其中,质量控制方案应包括质量控制的方法、频率、样品来源、目标值、允许误差等指标。
质量控制结果应包括质量控制样品的测定结果、质量控制指标的满足情况等。
质量控制记录应包括质量控制样品的标识、测定时间、测定结果、分析人员等信息。
五)临床试验资料临床试验资料主要包括临床试验方案、临床试验结果、临床试验报告等。
其中,临床试验方案应包括试验设计、入选标准、排除标准、随访时间、终点指标等内容。
3.1.1体外诊断仪器标准检验-电气安全要求 2018.6

30
重要术语和定义
v 接触电流 touch current(非本标准定义) 正常工作条件下或故障条件下,当人体接触设备的一个 或多个可触及零部件时通过人体的电流 本标准6.3条中的电流限值即为接触电流限值
31
试验导则
32
试验概述
v 本标准进行的试验为型式试验
v 在附录F中给出了对例行检验的建议 v 被试样品应是用户将要接收的设备的代表性样品, 或者应是准备向用户交货的设备 v 对满足本标准规定的相关标准要求且按这些要求 使用的设备的分组件,在整个设备的型式试验期间 不必再重复进行试验
28
重要术语和定义
v 3.6.7 电气间隙 clearance 两个导电零部件在空气中的最短距离 v 3.6.8 爬电距离 creepage distance 两个导电零部件沿绝缘材料表面的最短距离 附录C (测量方法)
29
重要术语和定义
v 相比漏电起痕指数(CTI):五个测试样品能经受50滴 的试验过程而不产生漏电起痕失效及持续火焰的最高电 压值。它还包括对材料在进行100滴测试时所显现的特 性的有关说明 v 相比漏电起痕指数主要用于表示材料的基本特性和 特性的比较
YY 0648-2008 (IEC61010-2-101:2002)
《测量、控制和试验室用电气设备的安全要求 第2-101部 分:体外诊断(IVD)医用设备的专用要求》
GB 4793.9-2013 (IEC 61010-2-081:2009)
《测量、控制和实验室用电气设备的安全要求 第9部分: 实验室用分析和其他目的自动和半自动设备的特殊要求》
体外诊断仪器标准检验 电气安全要求
中国食品药品检定研究院 光机电医疗器械检验室 李佳戈
(完整版)医疗器械研究资料模板

5.研究资料5.1 产品性能指标5.1.1功能性要求及验证方法5.1.1.1准确度按GB/T 19634-2005中5.4.1.1的规定进行,血糖仪和配套血糖试测量结果偏差的95%应符合表1的要求。
5.1.1.2XXX测量重复性按GB/T 19634-2005中5.3的规定进行,重复测试结果的精密度应符合表2的要求。
5.1.1.3 XXX的测试时间5.1.2安全性指标要求及验证指标本产品的电气安全的指标完全遵循《测量、控制和实验室用电气设备安全要求第1部分通用要求》(GB 4793.1-2007)和《测量、控制和实验室用电气设备安全要求第2-101部分:体外诊断(IVD)医用设备的专用要求》(YY 0648-2008)的要求,安全性指标的验证方法也按以上两个标准进行。
5.1.3电磁兼容性指标及验证方法本产品的电磁兼容性指标完全遵循《测量、控制和实验室用的电设备电磁兼容性要求第1部分:通用要求》(GB /T 18268.1-2010)和《测量、控制和实验室用的电设备电磁兼容性要求第26部分:特殊要求体外诊断(IVD)医疗设备》(GB /T 18268.26-2010)的要求,电磁兼容性指标的验证方法也按以上两个标准进行。
5.1.4主要性能要求确定的依据本产品的研发设计主要的性能指标依据以下标准和原则进行:①GB/T 191-2008包装储运图示标志②GB 4793.1-2007测量、控制和实验室用电气设备的安全要求第1部分通用要求③GB/T 9969-2008 工业产品使用说明书总则④GB/T 14710-2009 医用电器设备环境要求及试验方法⑤GB /T 18268.1-2010 测量、控制和实验室用的电设备电磁兼容性要求第1部分:通用要求⑥GB /T 18268.26-2010 测量、控制和实验室用的电设备电磁兼容性要求第26部分:特殊要求体外诊断(IVD)医疗设备⑦YY/T 0466.1-2009 医疗器械用于医疗器械标签、标记和提供信息的符号第1部分:通用要求⑧YY 0648-2008 测量、控制和实验室用电气设备安全要求第2-101部分:体外诊断(IVD)医用设备的专用要求5.2生物相容性评价说明生物相容性一般是指材料与宿主之间的相容性,包括组织相容性和血液相容性。
医用电气设备安全要求试验

医用电气设备安全要求试验
1.绝缘电阻试验:该试验是为了检测设备的绝缘性能,包括设备外壳和内部电路之间的绝缘性能。
通过对设备进行电气绝缘测试,以保障设备在正常使用情况下不会发生触电事故。
2.导线电阻试验:该试验是为了检测医用电气设备的导线电阻是否符合标准要求,以确保设备通电时不会因导线电阻过大而导致危险。
3.电气强度试验:该试验是为了检测医用电气设备在较大电压下的绝缘性能。
通过对设备进行高压电测试,以确保设备在正常使用情况下不会出现漏电等安全隐患。
4.电焊弧焊缺陷检测试验:该试验是为了检测设备的电焊弧焊缺陷,以防止因焊接不牢固导致的设备安全问题。
5.抗震试验:该试验是为了检测设备在地震或其他振动情况下的稳定性和可靠性。
通过模拟地震情况,以确保设备在地震情况下不会因受力过大而产生破坏或危险。
6.防火性能试验:该试验是为了检测医用电气设备的防火性能,以确保设备具有一定的耐火性能,防止发生火灾造成更大危害。
7.泄漏电流试验:该试验是为了检测医用电气设备的泄漏电流是否符合标准要求,以防止因泄漏电流过大而导致触电风险。
8.耐静电试验:该试验是为了检测医用电气设备的静电保护性能,以确保设备防止静电释放而导致的设备损坏或对患者产生影响。
9.温度上升试验:该试验是为了检测医用电气设备正常使用时的温度变化情况,以确保设备在正常工作范围内能够保持稳定的温度。
以上是医用电气设备安全要求试验的一些常见内容,通过这些试验,可以保证医用电气设备的安全性能,减少对患者和操作人员的潜在风险,提高医疗环境的安全水平。
60601-1测试标准

60601-1测试标准60601-1是一项医疗电气设备的安全性标准,它是国际电工委员会(IEC)制定的,被广泛应用于医疗设备行业。
该标准规定了医疗电气设备的设计、制造和使用过程中的安全要求,以确保设备在医疗环境中的安全性和可靠性。
60601-1标准的目的是保护患者、操作人员和环境免受电气设备可能带来的危险。
该标准涵盖了各种类型的医疗设备,包括但不限于监护设备、手术设备、诊断设备、治疗设备和实验室设备等。
在60601-1标准中,安全性要求主要包括以下几个方面:1. 电气安全,要求设备在正常使用和异常情况下的电气安全性,包括绝缘、接地、电击风险和火灾风险等方面的考虑。
2. 机械安全,要求设备在设计和制造过程中考虑到机械结构的安全性,防止可能的伤害或损坏。
3. 化学安全,要求设备在使用过程中不会产生有害化学物质或释放有害气体,以保护患者和操作人员的健康。
4. 生物安全,要求设备在设计和制造过程中考虑到生物兼容性,防止对患者产生不良影响。
5. 辐射安全,要求设备在使用过程中不会产生过高的电磁辐射或其他辐射,以保护人体健康。
6. 环境安全,要求设备在使用过程中对环境没有负面影响,符合环保要求。
此外,60601-1标准还包括了设备的标识、标志和使用说明等方面的要求,以确保用户能正确、安全地操作设备。
需要注意的是,具体的测试方法和要求可能会因不同类型的医疗设备而有所不同。
因此,在进行60601-1测试时,需要根据具体的设备类型和应用领域,参考标准的具体要求和相关的测试规范进行测试。
总之,60601-1标准是医疗电气设备安全性的国际标准,通过遵循该标准的要求,可以提高医疗设备的安全性和可靠性,保护患者和操作人员的健康和安全。
医学仪器的电气安全

输入阻抗100k
频率范围0~100MHz
漏电电流值=交流电压表的读数/1k
交流电压表
•45
从电源的初级回路通过绝缘物质流入安全地线的电流
•46
从仪器外壳的某处通过安全地线以外导体流入大地的电流
•47
从仪器的触体部分通过患者流入大地的电流
•48
绝缘电阻-仪器带电部分与人体间的阻抗,代表两者的绝缘程度
故在医院里接受诊断和治疗的病人比 一般人更容易受到电击。
测量的正确性和电击的危险性是生物 医学测量中的一对矛盾,应当加以重 视。
•35
第三节 电击的防护措施
为了最大限度地减小病人遭受电击的可能 性,使通过病人的电流减到最小,则:
将病人同所有接地物体和所有电流源绝缘 开来;
将所有病人够得着的导电表面,都保持在 同一电位上(不一定是地电位)。
各个国家均有自己的医疗设备的 电气安全标准:
美国-UL544 法国-VDE0750 国际电气标准委员会IEC-IEC医用
电气设备安全准则 中国-IEC标准
•1
医用电子仪器电气安全的概念:
工程学上的安全是指“发生危险的概 率尽可能小”。
医用电子仪器在临床上的安全,是指 应用过程中确保对患者和医护人员不 造成危害,即保证人员的安全;
电线越长,分布电容越大,产生的 泄漏电流也越大。
射频滤波器、电源变压器、电源线 以及具有杂散电容的一切部件都可 产生电容泄漏电流。
•26
电阻泄漏电流(传导漏电流)-产生 电阻漏电流的原因很多,如绝缘材料 失效、导线破损、电容短路等。
由于仪器故障造成的漏电流一般属于 电阻产生的传导漏电流。
•27
人体的体液是由含有多种离子的水 构成,是一种较复杂的电解液;
CB体系医疗器械电气设备标准

CB体系医疗器械电气设备标准医疗器械CB体系的电气安全及电磁兼容符合性测试标准如下所示:1.CB医疗电气设备安全标准CB体系中与医疗电气设备相关的安全标准如下表所示,主要由SC62A、SC62B、SC62C分技术委员会制定。
详情请访问CB Scheme-MED。
CB体系中医疗电气设备相关的安全标准序号标准编号CB检测的版本号标准范围1.IEC 60601-1 Ed.2+Am1+Am2医用电气设备安全的通用要求Ed.32.IEC 60601-1-1 Ed.1+Am1医用电气系统的安全要求Ed.23.IEC 60601-1-3 Ed.1诊断用X射线设备的辐射防护Ed.24.IEC 60601-1-4 Ed.1+Am1 可编程的医用电气设备的安全要求5.IEC 60601-1-6 Ed.1医用电气设备基本安全与性能的通用要求——使用性Ed.2Ed.36.IEC 60601-1-8 Ed.1+Am1 医用电气设备和医用电气系统中警报系统的通用要求、测试和指南Ed.27.IEC 60601-1-9 Ed.1 医疗电气设备-第1-9部分:基本安全和主要性能的通用要求-附属标准:环境意识设计用要求8.IEC 60601-1-10 Ed.1 生理性闭环控制器的开发要求9.IEC 60601-1-11 Ed.1 医疗电气设备-第1-11部分:基本安全和主要性能的通用要求-附属标准:用于家庭保健环境下的医疗电气设备和医疗电气系统要求10.IEC 60601-2-1 Ed.1+Am1+Am21~50MeV范围的电子加速器安全的特殊要求Ed.2+Am1Ed.311.IEC 60601-2-2 Ed.2高频手术设备安全的特殊要求Ed.3Ed.4Ed.512.IEC 60601-2-3 Ed.2+Am1 短波治疗设备安全的特殊要求13.IEC 60601-2-4 Ed.1心脏除颤器安全的特殊要求Ed.2Ed.3。
GB4793.1—2007《测量、控制和实验室用电气设备的安全要求 第1部分:通用要求》检测中需注意的几个常

电气设备 防触 电等级在 G 731 95的附 B49 . —19 录 H中做 了如下说明: I类 设备 是其 带 电件和 曝露零 部件 间采 用基 本 绝缘 ,且其曝露导电零部件接到保护导体连接装置 ( 651 的设备 。 见 ..) Ⅱ类 设备 是指对 间接 接触 的防护不 仅依靠 基本 绝缘 ,而且还提供避免带电件间故障的附加结构配
sL E ( E V— 接地 的隔离特低 电压)电路连接或者仅 由内部 sL E V或 S L E供电,且其内部产生的电 E V—
压 不会 高压 SL E V的设 备 。 在 G 761中有两 条定 义 可对 以 上说 明的 理 B90 . 解 提供 参 考 。G 76 1中 224I类 设 备 ,对 电 B 90 . .. 击 的防护不 仅依 靠基 本绝 缘 ,而且 还提 供 了与 固定
没有 问题 的 ,至 于一些 国外 的仪器 由于国外 报告 中
未指出设施类别 ,可 以理解为标称等级为过压类别 Ⅱ ,因为从一些 国外报告 的具体章节 ( . 67电气 间 隙和爬 电距离和 68 电强度试验程序等)分析是 .介 这样 的 。
() 电气设 备 防触 电等级 2
19 95的 37 1 ..:根 据对 地 的标 称 电压 ,用 标 准 化 了
1
式设备等的本机等级 ,其瞬态过压小于 Ⅲ类设施类
收 稿 日期 :20 08—0 5 5—0
医疗装备 20 第 8 08 期
维普资讯
置 ,或者设 备全 部是 采 用加强 绝缘 。 Ⅲ类设 备 是 指仅 与 sL ( E V 隔离 特 低 电压 )或
【 中图分类号]T 9 M3 【 文献标识码]A 【 章编号 ]1 2 27 【 0 )0 — 01 0 文 0 — 36 2 8 8 00 — 4 0 0
医用电气设备的安全检测

医用电气设备的安全检测首先,医用电气设备的安全检测需要保证设备的电气部分符合国家相关标准。
这包括对设备的接地情况、漏电保护器的可靠性、绝缘电阻的测试等检测项目。
这些检测项目的目的是确保设备在正常使用过程中不会因电气故障导致对患者造成电击伤害。
其次,医用电气设备的安全检测需要检查设备的机械部分是否完好无损。
包括检查设备的外壳是否有裂纹或磨损、设备的操作按钮是否灵活可靠、设备的移动部件是否稳固等。
这些检测项目的目的是确保设备在使用过程中不会因机械故障而对患者造成伤害。
最后,医用电气设备的安全检测还需要对设备的性能进行测试。
例如,对X射线机的辐射剂量进行测试、超声诊断设备的声强进行测试、心电图机的波形质量进行测试等。
这些检测项目的目的是确保设备在使用过程中能够提供准确的诊断和治疗信息。
总的来说,医用电气设备的安全检测是保障患者安全的重要环节。
只有通过定期的安全检测,医用电气设备才能够保持良好的工作状态,确保医疗过程中患者的安全和健康。
医用电气设备在医疗诊断和治疗中的重要性不言而喻。
然而,由于医用电气设备的复杂性和特殊使用环境,其安全性和稳定性显得尤为重要。
因此,对医用电气设备进行严格的安全检测和定期的维护至关重要。
首先,医用电气设备的安全检测需要通过合格的专业机构进行。
这些机构应当具备相关资质和经验,能够进行全面、系统地安全检测。
他们会按照国家相关标准和法规的要求,对医用电气设备的各项性能进行检测和评估,包括电气安全、机械安全、辐射安全等方面。
只有通过这些合格的机构进行检测,才能够确保检测结果的准确性和可靠性。
其次,医用电气设备的安全检测需要定期进行。
一般来说,医用电气设备的安全检测应当按照国家相关标准的要求,进行定期的年检、半年检或季度检,以确保设备的安全性和可靠性。
对于高风险设备,如手术机器人、超声刀、CT机等,其安全检测的频率更应当加强。
在进行安全检测时,需要对医用电气设备的不同部分进行全面的检测。
医疗器械的电气安全措施及其分类

医疗器械的电气安全措施及其分类医学仪器的电气安全主要是指仪器在使用时防止电击的性能.它是医学仪器安全性的重要组成部分。
诊断和治疗用的医学仪器是为了取得人体信息及给人体以某种作用。
它以患者为主要对象,而患者往往对于外来作用处于非常脆弱的状态.或者处于意识不清醒状态而对危险失去感觉.或者处于不能自由的状态。
因此.在评价医学仪器时,医学仪器的安全性与医学仪器的有效性成为同等重要.相辅相成的两个重要方面。
仪器的电气安全性.取决于仪器的合理设计和合理使用。
常见的医学仪器的安全措施有:仪器的可靠接地;减少漏电流;双重绝缘;低压供电;采用浮地措施或人体妥善接地;心脏与仪器的电气绝缘等等。
医学仪器的电气安全措施有一定的通用性,但尚需根据电气装置及患者使用部位的特殊性决定安全对策。
根据附加的安全措施不同.一般将医学仪器的级别分为I级、ll级.III级及内部电源仪器四类.如表1所示。
表1:医学仪器的级别分类在国际电工技术委员会(IEC)通则中.也可以根据设备防止电击的程度进行分类.通常分为B型、BF型和CF型(B是Body;躯体,C代表Cor;心脏,F表示floating;绝缘). B型是适用于体表、体腔的。
但触体部分不绝缘的仪器; BF型代表适用于体表、体腔的,但具有绝缘触体的仪器;显然,连接心脏的部分一定是绝缘触体部分(CF型);(不绝缘的C型的医学仪器实际上是不存在的)。
在IEC安全通则和医用电气设备暂定标准中对B型、BF型和CF型的仪器分别规定了容许漏电流值.如表2所示。
注:·接地漏电流.从电源的初级回路,通过绝缘物流八设备保护接地线的电流。
·外壳漏电流从仪器外壳的一部分.通过保护接地线以外的导体流入大地或外壳的其他部分的电流。
·患者漏电流从触体部分通过患者流入大地的电流.或者因外部电源加到患者身上的电压,从患者通过绝缘触体部分流入大地的电流。
·患者测量电流放大器的偏置电流,测量皮肤阻抗用的电流等,无意中通过触体部分和患者的电流.它对患者给以生理影响。
《分析仪器安全要求》word版

题目:IEC 61010-2-081,第一版:测量、控制和试验室用电气设备的安全要求,2-801部分:全自动和半自动分析设备的专用要求。
本文由IEC TC 66 WG 10起草,传阅并征求意见。
国家委员会被请求对7.2部分的秘书记录特别加以讨论,以确定是否同意该部分。
如不同意,则将该部分从现行的IEC 61010-1标准中删除。
- 1 -测量、控制和试验室用电气设备的安全要求2-081部分:全自动和半自动分析设备和体外诊断医疗设备的专用要求。
1.范围与目的:除下列内容外,第一部分中这一条款适用。
1.1 范围代替为:本标准适用于全自动和半自动分析设备,包括体外诊断医疗(IVD)设备和自测IVD 设备。
注1:如果设备的一部分既属于IEC 61010 另外第二部分标准的范畴,也属于本标准的范畴,则该设备须满足所有适用标准的要求。
实用文档全自动和半自动分析设备包括仪器和系统,用来测量样品的一个和多个特征或参数,其测量过程本身不需要手工干预。
完整的分析过程由下列步骤组成:- 取一定量的样品;- 使用化学药品加热或使用机械方法进行样品预备;- 测量;- 显示、发送或打印测量结果;IVD医疗设备,无论单独使用还是与其他设备联合使用,都是用来在体外对人体标本,包括血样品和组织样品进行检测的。
其唯一或主要的目的是提供下列一方面或多方面的信息:- 生理或病理状况;- 先天畸形;- 确定可能接受者的安全性和相容性;- 监控治疗措施;自测IVD医疗设备是供非专业人员在家庭环境中使用的。
- 2 -1.1.1 不包括在本标准范围内的内容补充:实用文档增加下列四个破折号部分;- 分析材料安全性方面的问题;- 在设备以外处理或操作分析材料;- 由于错误的分析结果所引起危险的发生;- 电磁兼容性(见IEC 61326);注包含此类危险的标准由起草性能标准的委员会负责编写。
1.2 目的代替为:第一句改为:本标准要求的目的是确保设备所用结构的设计和方法在发生可容许危险情况下对操作者和周围环境提供足够的保护。
医疗器械安全检验标准

医疗器械安全检验标准概述医疗器械的安全性是评估其质量和可靠性的关键指标。
安全检验标准用于确保医疗器械在设计、制造和使用过程中符合相关的安全要求。
本文档旨在介绍医疗器械安全检验标准的重要性及其应用范围。
重要性医疗器械的安全性对患者和医务人员的生命和健康至关重要。
合格的安全检验标准能够帮助减少医疗事故的发生,确保医疗器械的正常运行和有效使用。
应用范围医疗器械安全检验标准的应用范围涵盖了各种类型的医疗器械,包括但不限于医用电器设备、医用耗材、外科器械、体外诊断试剂和医疗保健产品等。
安全检验标准建立了对医疗器械的基本要求,并规定了相应的测试方法和评估流程。
常见的安全检验项目医疗器械的安全检验项目通常包括以下方面:1. 电气安全性:包括绝缘电阻、接地电阻、外壳阻燃性等测试。
2. 机械安全性:包括结构强度、机械耐久性、可靠性等测试。
3. 生物相容性:包括皮肤刺激性、细胞毒性、体内注射等测试。
4. 辐射安全性:包括电磁兼容性、辐射防护等测试。
5. 化学安全性:包括重金属、有害物质释放等测试。
安全检验标准的制定和执行安全检验标准的制定由有关的监管机构和标准化组织负责。
这些标准通常是经过广泛的研究和讨论,由行业专家参与制定的。
医疗器械生产商和运营商需要确保其产品符合相应的安全检验标准,并在生产过程中进行严格的控制和验收。
结论医疗器械安全检验标准的制定和执行对于确保患者和医务人员的安全至关重要。
通过遵循相关的标准和测试方法,可以降低医疗风险,保障医疗器械的质量和可靠性。
各个相关方应积极参与制定和执行安全检验标准,共同致力于提升医疗器械的安全性水平。
研究资料范本(有源体外诊断设备)

5.4 灭菌和消毒工艺研究
本成品为非无菌产品,使用者仅需按使用说明书的要求对仪器定期进行清洁和消毒。每周的清洁之后进行,对所有可触及的部位用 75%医用消毒酒精擦拭消毒。
5.5 有效期和包装研究
该产品采用三层包装,最里层为塑料薄膜,主要目的是为了防水、防潮,最外层为木箱结构,中间层为泡沫,起到缓冲的作用, 经环境试验和模拟运输试验验证,产品的包装符合运输和贮存的要求。通过加速老化试验,产品的正常使用有效期等效大于 5 年,考 虑一些不可预期的因素,确定有效期为 5 年,到期后经制造商维护并确认后,可按确定的期限延期使用。产品的有效期研究见《产品 有效期验证报告》 (编号: )
研究资料
5.1 产品性能研究
5.1.1 项目来源 A 法和 A 法是目前临床检验用得最多的方法,各种各样的分析领域都在利用它。A 法具有高灵敏度、特异性强等特点,B 法具有 准确性高,能提供定量结果的特点,采用 A 法的全自 A 仪和采用 B 法的全自动 B 仪已被广泛用于临床诊断、医学研究、食品安全分析 等领域,经过多年的应用,都得到了临床诊断行业的肯定。 目前临床检验机构使用的是仅能进行 A 试验的全自动 A 仪和仅能进行 B 试验的全自动 B 仪,如想开展 A 和 B 试验,则需要采购两 台仪器,采购成本高,占用空间大。 为了解决这些问题,我公司吸取了全自动 A 仪和全自动 B 仪的特点和优点,把两者的优点和特点 进行了有机的整合,研发出了全自动 XXXXX 仪。 5.1.2 研制情况 公司组织生产,质量,技术人员通过认真学习、理解相关标准,研究市场上同类产品的技术指标,临床应用情况,参考了公司已 上市的全自动酶免仪和国内外同类产品的先进技术,制定了本产品的质量标准、技术指标,工艺要求、关键技术等,研发一开始就遵 循 ISO13485:2003 中对设计和开发的要求,做好了前期的输入确定,加强了设计过程的评审,进行了系统的验证和确认,试制的样品 符合相关标准和法规要求。 5.1.3 关键技术
医学实验室与体外诊断器械和试剂标准清单
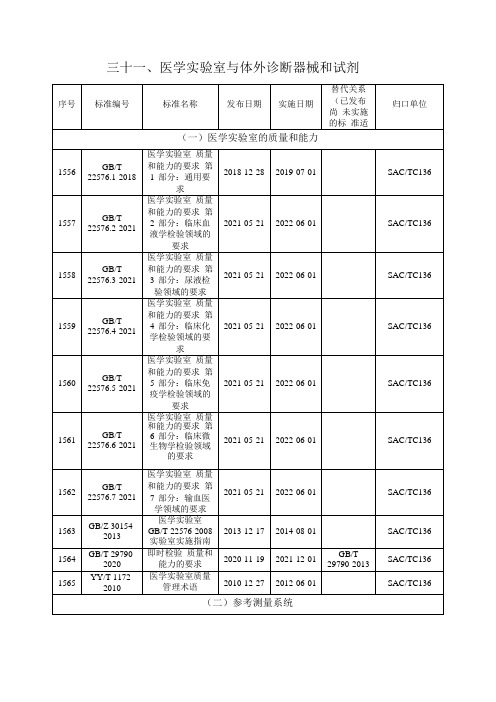
(六)临床检验用仪器设备
1603
YY/T0014-
2005
半自动生化分析
仪
2005-12-07
2006-12-01
SAC/TC136
1604
YY/T0032-
2004
血红蛋白计
2004-11-08
2005-11-01
SAC/TC136
1605
YY/T0087-
2004
电泳装置
2008
检验医学参考测
量实验室的要求
2008-05-28
2009-01-01
SAC/TC136
1569
YY/T0638-
2008
体外诊断医疗器
械 生物样品中量 的测量 校准品和 控制物质中酶催 化浓度赋值的计 量学溯源性
2008-04-25
2009-06-01
SAC/TC136
1570
YY/T1195-
2014-02-01
SAC/TC136
1581
GB/T 29791.5-2013
体外诊断医疗器
械 制造商提供的 信息(标示) 第5部分:自测用 体外诊断仪器
2013-10-10
2014-02-01
SAC/TC136
1582
YY/T0639-
2019
体外诊断医疗器
械 制造商为生物 学染色用体外诊 断试剂提供的信 息
1559
GB/T 22576.4-2021
医学实验室质量
和能力的要求 第4部分:临床化 学检验领域的要 求
2021-05-21
2022-06-01
SAC/TC136
1560
GB/T 22576.5-2021
IEC 61010-1:2010体外诊断设备电击防护要求分析

IEC 61010-1:2010体外诊断设备电击防护要求分析张文忠;刘继广;林联君;邵秀稳;邓振进;邱栋梁【期刊名称】《医疗卫生装备》【年(卷),期】2017(038)011【摘要】目的:探讨体外诊断设备的防电击要求,帮助制造商理解以便合理地设计相关产品.方法:介绍IEC 61010-1:2010标准的要求,分析各种电击防护措施,阐述保护接地阻抗防电击的原理,并引入实例分析全自动生化分析仪采样针的电击防护措施,解析其设计是否存在电击危害.结果:虽然采样针不满足保护接地和双重绝缘/加强绝缘的要求,但在基本绝缘失效时采样针不会危险带电,可判定采样针的结构设计满足标准要求.结论:只有对标准进行全面深入的了解,识别出产品内部的危险带电部件,并逐一进行防电击措施的分析,才能对防电击的要求做出正确的判断.【总页数】4页(P79-82)【作者】张文忠;刘继广;林联君;邵秀稳;邓振进;邱栋梁【作者单位】510663 广州,广东省医疗器械质量监督检验所;518057 广东深圳,国家医用诊断仪器工程技术研究中心可靠性检测实验室;310018 杭州,浙江省医疗器械检验院;510663 广州,广东省医疗器械质量监督检验所;410001 长沙,湖南省医疗器械与药用包装材料(容器)检测所;518057 广东深圳,深圳迈瑞生物医疗电子股份有限公司【正文语种】中文【中图分类】R318.6;TH776【相关文献】1.体外诊断医用设备系统电击防护要求浅析 [J], 刘继广;徐勤;刘继刚2.IEC 62368-1∶2010(音视频以及信息和通信设备)的防火要求 [J], 李长军;龙运健;李金泉3.关于IEC1010《测量,控制和试验室用电气设备的安全要求》标准中的防电击要[J], 肖向荣4.IEC 61010-2-101《测量、控制和实验室用电气设备的安全要求第2-101部分:体外诊断(IVD)医用设备的专用要求》国际标准简析 [J], 李妍达5.IEC家用断路器和类似设备分技委电击防护工作组2010年意大利会议纪要 [J],因版权原因,仅展示原文概要,查看原文内容请购买。
体外诊断医疗器械标准

体外诊断医疗器械标准体外诊断用检测仪器和设备标准仪器和器具通用标准体外诊断用检测仪器除基本性能应符合相应的标准要求外,其安全性也应满足相关安全标准要求,通用标准为GB/T 18268.26, YY 0648oGB/T 18268.26根据体外诊断设备的特性及其电磁环境,规定了其电磁兼容性的抗扰度和发射的基本要求。
同常规医用电气设备一样, 体外诊断设备也被广泛应用于各种电磁环境中,除了应在典型的医用环境(医院、诊所等)中正常工作外,也应在家庭环境中正常、安全地工作。
也就是说,体外诊断设备应有与这些环境相适应的基本抗扰度等级。
YY 0648是强制性国家标准GB 4793.1的专用标准之一,适用于预期用作体外诊断医用目的的医用实验室仪器。
基于体外诊断设备预期用途特殊性,操作人员可能接触各类具有生化危险的人体样本、化学试剂等。
为保护操作人员安全,YY 0648等同转化了IEC 61010—2—101 , 为安全性标准,提示操作人员操作设备可能产生的生化危险、电气危险等,以保护操作人员防电击、防生化危险等。
该标准的全部内容都与强制性国家标准GB 4793.1相关。
血液学和流式细胞学检测仪器标准血细胞分析是临床常规检验之一。
血细胞分析仪集成了生物、化学、光学、流体力学、电子电路、计算机软件等多学科技术,自20世纪50 年代以来,经过多年发展和技术革新,不仅能对血液中的红细胞、白细胞、血小板等有形成分进行计数和定量分析,还能对细胞群进行识别、区分和分析。
同时,利用计算机强大的信号采集、分析和运算能力,更多具有临床意义的参数也被发掘出来。
随着高性能计算机、高精密度和快速图像获取设备及大数据库的诞生,自动化细胞图像分析设备正在以准确度高、速度快、网络化和人性化走进临床实验室。
流式细胞术是利用流式细胞仪对人体样本中的有形成分,包括细胞、血小板、细胞器、精子、微生物以及人工合成微球等的多种生物和物理、生化特性进行计数和定量分析,并能对特定细颍羊体加以分选的细胞参量分析技术。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
26
附录F
F.2 电网电源电路
连接在一起的电网电源端子
27
附录F
F.2 电网电源电路
电网电源电路的加载
28
附录F
F.3 其他电路 在一端为连接在一起的在正常工作时能成为危险 带电的浮地输入电路的端子,以及另一端为连接在一 起的可触及导电零部件之间施加试验电压 还要在一端为连接在一起的在正常使用时能成为 带电的浮地输出电路的端子,以及另一端为连接在一 起的可触及导电零部件之间施加试验电压
39
5.1.101 运输和贮存 v 包装上应贴上标签用来指示任何特殊的运输或贮 存条件(与5.4.101、8.101联合)
40
5.2 警告标志 v 正常使用时能够从设备中取下的装有生物危害废 料的容器或袋子应标记表1的符号101 (废液瓶/盒/袋)
41
5.4.1 概述 v 如果需要培训或使用附加的保护措施(接地)或 个人防护设备(手套、防护镜/服)来将风险降低到 容许的风险水平,对这些内容应该做出规定
45
5.4.4 设备的操作 v e)设备上使用的符号的解释,以及在涉及危险 的地方,在每一种特殊情况下使用符号的原因 v f)如果发生故障,任何操作人员可以采取的行 动的说明(常见故障解决表格) v g)清洗和消毒的说明和建议,以及推荐的材料 v h)废弃物处理的说明 v i)如果正常使用涉及危险物质的处理,正确使 用和需要培训或个人防护措施的说明
29
附录F
F.3 其他电路 v 目的:验证设备隔离电路的绝缘,即输入/输出电 路端子与可触及金属部分的绝缘 v 试验要点: 1)不进行潮湿预处理,设备电源开关置于通位 2)试验电压值为工作电压的1.5倍/或0.9倍的箝位 电压,但不小于工作电压
30
附录F
F.3 其他电路 v 试验要点: 3)试验时,设备要与外部接地装置断开 4) 试验持续时间明确要求,可参考F.2进行(2s内升 至规定值,并至少保持2s) 5)不得出现击穿或重复的飞弧,不考虑电晕效应和 类似现象
46
5.4.4 设备的操作 v j)处理潜在的传染性物质(如人体样本或试剂) 时,如果有可能接触到皮肤,需要使用防护手套或 其他防护措施 v k)如果在正常使用中设备可能释放出危险的气 溶胶蒸气,对口、鼻或眼睛进行防护的说明
47
5.4.4 设备的操作 v l)如果潜在的危险的可见或不可见辐射可能被 释放出来,对防护装置的说明和要求,如防护眼镜 v m)在说明书中应声明,如果不按制造商规定的 方法来使用设备,则设备所提供的防护可能会被破 坏(注意加入相关内容)
6
6.10.1a)、6.10.1d) GB 5023.1或GB 5013.1
17
序号
7 8 9 10 11 12 电池
关键件
电线组件
涉及条款
6.10.1d) 5.4.5、13.2.2 11.2 4.4.2.4、14.2.1 14.3
所需认证
GB 15934-2008 EN55022、 EN55024 / GB 8898、 GB 12350 GB 9816
31
附录F
F.3 其他电路
32
附录F
例行试验 v 可作为出厂检验项目 v 不限于上述项目,还可加入性能试验
33
YY 0648-2008
34
YY 0648与GB 4793.1的关系
v YY 0648-2008《测量、控制和试验室用电气设备 的安全要求 第2-101部分:体外诊断(IVD)医用 设备的专用要求》等同采用IEC61010-2-101:2002 v YY 0648-2008是体外诊断(IVD)医用设备的专 用要求,相关要求优先于GB4793.1-2007
48
v 自测体外诊断医用设备的使用说明书应符合 规范性附录BB要求
49
8 耐机械冲击和撞击
50
51
8 耐机械冲击和撞击
8.101 运输和贮存 v 当装在制造商的包装中,在制造商规定的条件下 运输或贮存后,设备不应在正常使用中产生危险 v 均符合5.10.10、5.4.101 v ASTM D4169和国家运输安全协会给出试验指导 v 制造商提供相关运输试验报告
44
5.4.4 设备的操作 替换:如果适用,使用说明应包括: v a)在所有操作方式下操作控制件及其使用的详 细内容和操作的顺序 v b)不要将设备放在难以操作断开装置的位置的 说明 v c)与附件和其他设备互联的说明,包括合适的附 件,可拆卸的零部件和任何专用的材料的详细内容 v d)间歇工作的限值(连续工作不适用)
涉及条款
6.7、14.8 5.1.6、6.11.1、 6.11.3.1 5.1.4、5.4.5、14.4 4.4.2.6、14.7 6.10.3a)
所需认证
GB/T 11020 GB 14048.1或GB 14048.3 GB 9364系列 GB 4943、GB 19212、GB 13028 GB 2099或GB 1002、GB 17465
15
关键元器件 元器件名称 生产厂/商标 型号/编号 技术参数 认证标记
…… v 清单、器件证书及元器件标记内容应一致 v 器件使用额定值应与设备的使用额定值一致 v 器件证书执行的标准应与设备中此器件用途相符 v 器件证书执行的标准应是安全标准
16
序号
1 2 3 4 5
关键件
网电源部分的零部件 作为断开装置的电源 开关 熔断器及熔断器座 网电源变压器及开关 电源 网电源插头、连接器 和器具输入插座 电源线
43
5.4.3 设备的运输、安装和装配说明 v g)12.5.1要求的声音数据(与4793.1判断一致) v h)有关对危险物质的处理,封闭和排放,包括防 止回流的要求的说明(废液、废料等的处理) v i)流出生物的,化学的物质和热的液体可能产生 危险时,所需要的排水系统 v j)有关危险辐射保护措施的详细内容(见第12章) (与4793.1判断一致) v k)与电源的连接
24
附录F
F.2 电网电源电路 v 目的:验证设备可触及金属部分的绝缘(BI) v 试验要点: 1)正常工作条件下进行,不进行潮湿预处理 2)设备电源开关置于通位 3)连接在一起的电网电源端子 = L、N端短接
25
附录F
F.2 电网电源电路 v 试验要点: 4)试验电压(1390V)应当在2s内升至规定值,并至 少保持2s 5)试验不得出现击穿或重复飞弧,不考虑电晕效应 和类似现象
21
附录F
F.1 保护接地 v 目的:既验证了保护接地的有效可靠,又不至于频 繁大电流测试破坏保护接地连续性 v 试验要点: 1)试验电流不作规定(设备额定电流的1.5或2倍) 2)试验时间可以很短(5s~10s) 3) 试验部位:从保护接地端子到尽可能远的易触及 导电零部件之间 4)无保护接地端子设备不适用
53
通标与专标的关系: v 专标优于通标 v 专标中“替换”、“删除”条款的处理 通标不适用;专标判断 v 专标中“修改”条款的处理 通标、专标均判(具体情况具体分析) v 专标中“增加”条款的处理 以专标为准
54
7.2 运动零部件
55
56
7.2 运动零部件
7.2.101 正常使用时可触及性 v 作为一种例外,如果运动零部件在正常使用中的暴 露不可避免,应通过风险管理(见附录AA)确定运动 零部件是否会导致操作者受到伤害 注: 1.YY 0648适用设备参照本标准执行 2.其他设备,参考GB/T 0316
35
通标与专标的关系: v 专标优于通标 v 专标中“替换”、“删除”条款的处理 通标不适用;专标判断 v 专标中“修改”条款的处理 通标、专标均判(具体情况具体分析) v 专标中“增加”条款的处理 以专标为准
36
5 标志和文件
37
5.1.1 v 可使用附加符号,但不应与国际上认可符号混淆 v 符号101有颜色要求(黄底黑框) v 图形符号应在文件中给予解释
38
5.1.2 标识 下列附加的内容应标在设备上或包装上或使用说明书中: 1)序列号 2)下列内容: i)该设备为体外诊断医用设备的清晰的指示(IVD) ii)如果适用,该设备为自测体外诊断医用设备的清晰的 指示(文字) iii)如果会形成潜在的风险,通过制造商和部件标识, 以及适当时批号等,对可拆卸器件进行识别(适配器等) iv)消耗部件的有效期限,按年、月和日(如相关)顺序 表达
9பைடு நூலகம்
短路工装
10
过载: v 达热稳态(2.5h)后测量 v 取额定电压的90%~110%的最不利条件(输入功率 辅助) v 按GB 9706.1标准表20设定试验电流值(次级) v 加载30min(GB9364熔断器) v 熔断器应采用可忽略阻抗的连线代替
11
温 度 巡 测 仪
带电 绕组 温升 测试 仪
直流 低电 阻测 试仪
交直 流电 子负 载
12
14.8 印刷线路板 v 企业提供符合性认证可资料 v 按GB/T 11020要求进行50W垂直燃烧试验确定材料 可燃性等级——V1或更优
13
14
厂家应提供关键元器件清单 v 电源插头、插座、电线、组件 v 熔断器/座 v 网电源变压器/开关电源 v 电动机 v 附相关认证证书…
56
57
7.2 运动零部件
7.2.101 正常使用时可触及性 v 按照下面优先级顺序,通过保护措施的执行尽可能 使这些风险减到最小 a)保护装置(联锁系统或其他方法,使用工具移除) b)保护罩 c)机械挡板 d)安全区域和运动零部件间有足够的距离 e)警告信号(听觉或视觉) f)警告标志
42
5.4.3 设备的运输、安装和装配说明 如果适用,提供给责任者的文件应包含下面内容: v a)在交付给责任者后运输的说明 v b)地面承载要求(一般设备不适用) v c)主要重部件各自的重量 v d)定位和安放说明,包括通风以及安全和有效 的操作人员维护所要求的空间 v e)装配说明 v f)保护接地说明(注意细节)
