基础化学电子教案习题解答(第七章)
高中化学第二册第七章探究电解质溶液的性质7.1电解质的电离(第1课时)教案沪科版(2021学年)

高中化学第二册第七章探究电解质溶液的性质7.1 电解质的电离(第1课时)教案沪科版编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(高中化学第二册第七章探究电解质溶液的性质 7.1电解质的电离(第1课时)教案沪科版)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为高中化学第二册第七章探究电解质溶液的性质 7.1 电解质的电离(第1课时)教案沪科版的全部内容。
7.1电解质的电离(共3课时)第1课时电解质的电离[设计思想]通过硝酸钾、氢氧化钠、蔗糖固体,硝酸钾、氯化氢、氢氧化钠、蔗糖、酒精、甘油等水溶液,以及熔化的硝酸钾和蔗糖等导电性实验的比较、分析、归纳得出电解质和非电解质的概念,理解电解质与非电解质的区别:电解质必须满足三个条件:一是纯净物、二是化合物、三是在水溶液里或熔化状态下能电离。
如:KNO3是电解质,KNO3溶液并不是电解质,只是电解质溶液,混合物如溶液既不是电解质,也不是非电解质,而蔗糖、酒精是纯净的化合物是非电解质;理解电解质与金属导电的区别,电解质导电含化学变化,金属导电只是物理变化。
结合离子化合物、共价化合物的知识,在解释实验现象的过程中,理解电解质导电的原因是电解质在溶于水或熔融状态下,发生电离,电解质溶液中或熔融态的电解质有自由移动的离子,因而导电,即电解质因电离而导电;理解常见的酸、碱、盐是电解质。
一、教学目标1.知识与技能(1)电解质、非电解质(B)(2)电离(B)(3)电离方程式(A)2.过程与方法(1)通过硝酸钾、氢氧化钠、蔗糖固体,硝酸钾、氯化氢及其水溶液、氢氧化钠、蔗糖、酒精、甘油等水溶液,以及熔化的硝酸钾和蔗糖等导电性实验的比较,领悟比较性实验研究、分析、归纳的科学方法.(2)结合离子化合物、共价化合物的知识,尝试解释实验现象,领悟物质结构决定物质性质的学科思想。
高中化学竞赛第7章_化学动力学基础课件

0 BB B
已知 d dnB B
转化速率的定义为:
•
d
1 dnB
dt B dt
2022/4/16
反应速率(rate of reaction)
IUPAC推荐反应速率用单位体积内的转化速率表示,
反应的速率定义为:
r
1
d
V dt
( d 1 dnB ) dt B dt
1 dnB /V 1 d c B
动力学认为:
1 2
N2
3 2
H2
NH3(g)
需一定的T,p和催化剂
1 H 2 2 O 2 H 2O(l)
点火,加温或催化剂
2022/4/16
7.1 化学动力学的任务和目的
化学动力学发展简史
•1848年 van’t Hoff
dlnKc U
提出:
dT RT2
dlnkEa dT RT2
Kc
kf kb
例如:
r k 0
r k 反 应
r k [ A ] [ B ] 二 级 , 对 A 和 B 各 为 一 级
r k [ A ] 2 [ B ] 三 级 , 对 A 为 二 级 , 对 B 为 一 级
r k [ A ] [ B ] - 2
负 一 级 反 应
r k [ A ] [ B ] 1 /2
k 的单位随着反应级数的不同而不同。
2022/4/16
准级数反应(pseudo order reaction)
在速率方程中,若某一物质的浓度远远大于其 他反应物的浓度,或是出现在速率方程中的催化 剂浓度项,在反应过程中可以认为没有变化,可 并入速率系数项,这时反应总级数可相应下降, 下降后的级数称为准级数反应。例如:
《基础化学》课后习题参考答案(有机部分)
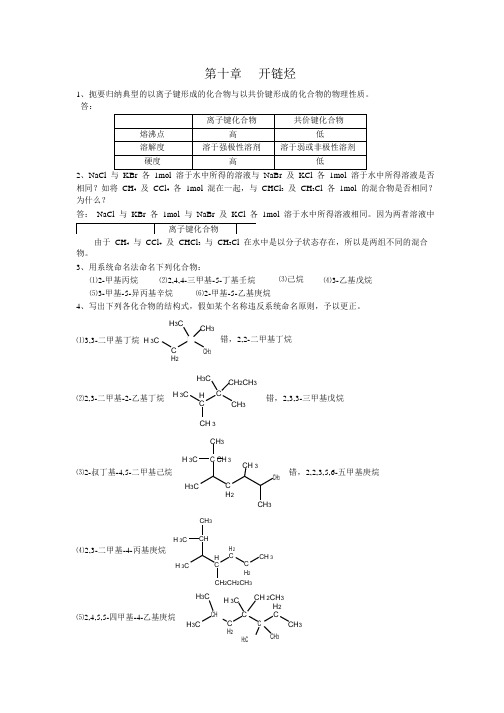
均为 Na + , K + , Br , Cl 离子各 1mol 。
第十章开链烃1、扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答:2、NaCl 相同?如将 CH 4 及 CCl 4 各 1mol 混在一起,与 CHCl 3 及 CH 3Cl 各 1mol 的混合物是否相同? 为什么?答: NaCl 与 KBr 各 1mol 与 NaBr 及 KCl 各 1mol 溶于水中所得溶液相同。
因为两者溶液中 - -由于 CH 4 与 CCl 4 及 CHCl 3 与 CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合 物。
3、用系统命名法命名下列化合物:⑴2-甲基丙烷⑵2,4,4-三甲基-5-丁基壬烷⑶己烷⑷3-乙基戊烷⑸3-甲基-5-异丙基辛烷⑹2-甲基-5-乙基庚烷4、写出下列各化合物的结构式,假如某个名称违反系统命名原则,予以更正。
H 3CCH 3 ⑴3,3-二甲基丁烷 H 3CH 2CH 3H 3C错,2,2-二甲基丁烷CH 2CH 3 ⑵2,3-二甲基-2-乙基丁烷 H 3C HC C3错,2,3,3-三甲基戊烷CH 3CH 3⑶2-叔丁基-4,5-二甲基己烷H 3CC CH 3CH 33错,2,2,3,5,6-五甲基庚烷H 3CC H 2CH 3CH 3H 3CCH⑷2,3-二甲基-4-丙基庚烷H 3H CH 2 CC H 2CH 3CH 2CH 2CH 3H 3CH 3CCH 2CH 3H 2⑸2,4,5,5-四甲基-4-乙基庚烷H 3CHC H 2 CH 3CC C 3 32 CH32CH2 3CH 2 3CH 3 3CH 3 2CH 3⑹2,2,3-三甲基戊烷H3CH3CCCH3CH2CH35、写出分子式为C6H14的烷烃的各种异构体,用系统命名法命名,丙标出伯、仲、叔、季碳原子。
1oCH 32oCH 2 2 o22 oCH2 oCH 21 o己烷1oCH 3oCH 21 o CH32 o CHo1 oCH32-甲基戊烷1 o CH31oCH 32ooCH2 oCH2 1 oCH3 3-甲基戊烷1oCHo3 oCH1 o3 2,3-二甲基丁烷1 o CH31 o1 o CH31oCH2o4 oCCH32,2-二甲基丁烷H3C 1 o 1 o CH36、⑶>⑵>⑸>⑴>⑷7、写出2,2,4-三甲基戊烷进行氯代反应可能得到的一氯代产物的结构式。
基础化学电子教案习题解答(第八章)

习题解答(第八章)一、选择题1. 下列反应中,属于氧化还原反应的是( C )A.硫酸与氢氧化钡溶液的反应B.石灰石与稀盐酸的反应C.二氧化锰与浓盐酸在加热条件下反应D.醋酸钠的水解反应2. 单质A和单质B化合成AB(其中A显正价),下列说法正确的是( C )A. B被氧化B. A是氧化剂C. A发生氧化反应D. B具有还原性3. 对于原电池的电极名称,叙述中有错误的是( B )A.电子流入的一极为正极B.发生氧化反应的一极是正极C.电子流出的一极为负极D.比较不活泼的金属构成的一极为正极4. 根据下列反应:2FeCl3+Cu→2FeCl2+CuCl22Fe3++Fe→3Fe2+2KMnO4+10FeSO4+8H2SO4→2MnSO4+5Fe2(SO4)3+K2SO4+8H2O 判断电极电势最大的电对为( C )A.Fe3+/Fe2+B.Cu2+/CuC.MnO4-/Mn2+D.Fe2+/Feϕ5. 在含有Cl-,Br-,I-离子的混合溶液中,欲使I-氧化成I2,而Br-,Cl-不被氧化,根据φ值大小,应选择下列氧化剂中的( B )A.KMnO4B.K2Cr2O7C.(NH4)2S2O8D.FeCl36. 在酸性溶液中和标准状态下,下列各组离子可以共存的是( D )A.MnO4- 和Cl-B.Fe3+ 和Sn2+C.NO3- 和Fe2+D.I- 和Sn4+7. 利用标准电极电势表判断氧化反应进行的方向,正确的说法是( B )A.氧化态物质与还原态物质起反应;ϕ较大电对的氧化态物质与φϕ较小电对的还原态物质起反应;B. φC.氧化性强的物质与氧化性弱的物质起反应;D.还原性强的物质屯还原性弱的物质起反应。
二、是非题(下列叙述中对的打“√”,错的打“×”)1. MnO4-离子中,Mn和O的化合价分别为+8和-2。
( ×)2. 根据标准电极电势判定SnCl2 + HgCl2 =SnCl4 + Hg反应能自发向右进行。
基础化学电子教案习题解答(第七章)

思考与习题一、填空题1.中心离子是配合物的形成体,它位于配离子的中心。
常见的中心离子是带正电的金属元素的离子.2.配位体中具有孤对电子、直接与中心离子(或原子)结合的原子叫配位原子。
如NH3中的N 原子是配位原子。
在配离子中与中心离子直接结合的配位原子数目叫中心离子或原子的配位数。
3.填充下表:配合物的化学式命名中心离子配离子电荷配位体配位数[Ag(NH3)2] NO3K4[Fe(CN)6 ]K3[Fe(CN)6 ]H2[PtCl6][Zn(NH3)4]( OH)2[Co(NH3)6] Cl3硝酸二氨合银(Ⅰ)六氰合铁(Ⅱ)酸钾六氰合铁(Ⅲ)酸钾六氯合铂(Ⅳ)酸氢氧化四氨合锌(Ⅱ)(三)氯化六氯合钴(Ⅱ)Ag+Fe2+Fe3+Pt4+Zn2+Co3++1-4-2-2+2+3NH3CN-CN-Cl-NH3NH32666464.配合物在水溶液中全部电离成配离子和外界离子,而配离子在水溶液中部分电离,存在着配位平衡。
在[Ag(NH3)2]+水溶液中的离解平衡式为[Ag(NH3)2]+ Ag++2NH3。
5.配位数相同的配离子,若K稳愈大或K不稳愈小,则该配离子愈稳定,若K不稳值愈大,表示该配离子离解程度愈大。
6.在AgNO3溶液中加入NaCl溶液,产生AgCl (写化学式)沉淀,反应的离子方程式为Ag++Cl-→AgCl↓。
静置片刻,弃去上面清液,在沉淀中加入过量氨水,沉淀溶解,生成了[Ag(NH3)2] Cl (写化学式),反应的离子方程式为AgCl+2NH3→[Ag(NH3)2] ++Cl- 。
7.当配离子中的配位体能与H+合成弱酸时,则溶液中酸度增大时,配离子的稳定性会减弱。
8.当一种配离子转化为另一种配离子时,反应物中配离子的K稳愈小,生成物中配离子的K稳愈大,那么这种转化愈完全。
9.络合滴定曲线滴定突跃的大小取决于 配合物条件稳定常数和被滴定金属离子浓度 。
在金属离子浓度一定的条件下, K ’MY 越大,突跃 范围越大 ;在条件常数K ’MY 一定时, 金属离子浓度 越大,突跃 越大 。
九年级化学下册第七章溶液7.4结晶现象教案新版粤教版

九年级化学下册:7.4结晶现象本节内容是初中溶液知识体系的继续和完善。
教材开始以展示漂亮的晶体图片让学生欣赏,再通过实验与溶解现象相反过程的另一种现象——结晶现象学习结晶的原理和方法,在此基础上进一步学习两种分离混合物的方法——结晶法和过滤法。
本课程利用之前学习的天然水的净化中,过滤的方法来具体操作,结合有关溶液的知识,向学生介绍分离混合物的一般方法,培养学生实验操作能力及对实验过程和实验结果的表达能力。
【教学目标】1.知识与技能(1)了解晶体和结晶现象。
(2)了解结晶方法的原理和过滤操作要点。
(3)学习使用结晶、过滤的方法分离混合物。
2.过程与方法通过观察常见晶体结晶形成等活动,提高运用观察、实验等方法获取知识的能力。
3.情感、态度与价值观通过分离混合物、制造晶体等活动和过滤操作要点等的学习,培养严谨求实和勇于实践的科学精神。
【教学重点】结晶法分离混合物的原理和操作。
【教学难点】可溶性杂质除去方案的设计;课堂时间的调控。
【教学准备】教学设备:投影仪,计算机实验用品:烧杯、玻璃棒、药匙、量筒(10mL)、胶头滴管、蒸发皿、坩埚钳、酒精灯、漏斗、铁架台(带铁圈)、托盘天平、滤纸、火柴、明矾、粗盐。
一、导入新课国庆节,我去做客,我妈妈冲了一杯很甜的糖水,开始我没喝完,等过了一段时间,发现杯底有白糖析出。
我问妈妈是否当时没搅拌?妈妈说当时糖已经全部溶解,你能帮我分析白糖析出的原因吗?这节课我们学习有关晶体和结晶的知识。
二、推进新课活动1 知道晶体可由饱和溶液形成[复习提问]1.什么叫做饱和溶液?2.温度对固体物质溶解度影响的三种情况?3.将硝酸钾的饱和溶液恒温蒸发掉部分水和将硝酸钾饱和溶液降温冷却分别会有什么现象发生?为什么?(都会有硝酸钾固体析出。
前者因为溶剂量减少,后者因为硝酸钾的溶解度随温度降低而减小。
)[过渡]蒸发溶剂和冷却饱和溶液都可以从硝酸钾饱和溶液中得到硝酸钾固体这个过程化学上称为结晶现象,得到的硝酸钾固体我们称为硝酸钾晶体。
0601高一化学(人教版)-第七章第一节认识有机化合物(1)-1教案

教学重点
碳原子之间的成键方式、碳骨架的连接方式。
教学难点
全考虑多个碳原子可能形成的结构。
教学过程(表格描述)
教学环节
主要教学活动
设置意图
引出主题
1、介绍有机物名称的由来、展示生活中常见的有机物的图片和分子组成,让学生寻找有机物的组成特点,进而给出有机物概念的界定。
总结碳骨架的多种方式:碳原子数增多时候,连接方式可以是链状或环状;而链状分为直链和支链。
在上一环节的基础上继续深化,让学生掌握碳骨架的多种构成方式,体会有机物数量繁多的原因。
习题练习和课堂小结
用教材中的思考与讨论和例题帮学生巩固夯实有机化合物的基础知识和概念界定。梳理本节课知识脉络,整理出有机化合物中碳的成键特点:碳原子成四个共价键;碳原子之间可以形成单、双、三键;碳骨架可以有链状(直链、支链)和环状。
教 案
教学基本信息
课题
认识有机化合物(1)
——有机化合物中碳原子的成键特点
学科
化学
学段:高中
年级
高一
教材
书名:普通高中教科书化学必修第二册
出版社:人民教育出版社出版日期:2019年6月
教学目标及教学重点、难点
教学目标
1.借助实物模型将微观结构呈现出来,使问题具象化,建立宏观与微观的联系,在这个过程中,提升模型认知和科学探究的素养。
2、从化学史的角度提出“用模型来研究物质结构”,为接下来的内容提供着力点。
用原子结构的知识确定碳要形成四个共价键,用简单的甲烷、一氯甲烷举例,为下一步更深一步的研究提供指导核心。
物理化学电子教案.doc

物理化学电子教案第七章统计热力学基础物理化学教研室【基本概念·基本知识】1、统计热力学系统的分类:独立/非独立粒子系统、可别/不可别粒子系统2、独立粒子系统的分布、最可几分布、平衡态分布3、系统的微观状态4、粒子的配分函数5、转动特征温度,振动特征温度6、焓函数、吉布斯自由能函数7、统计熵、量热熵【基本定律与基本理论】1、等几率假设2、玻兹曼分布定律(推导和表达式的意义)3、Maxwall 速率分布的意义及与平动有关的各种统计平均值4、粒子配分函数与热力学函数的关系5、最低能级能量数值的选取对配分函数的影响6、双原子分子转动、振动、平动的能级公式7、波兹曼公式:ln S k =Ω8、热力学定律的统计解释【基本计算与基本方法】1、独立可别与不可别粒子系统Ω的计算2、用波兹曼分布定律计算简单系统的粒子分布3、单原子分子、双原子分子各种运动形式的配分函数4、单原子及双原子分子各种运动形式对热力学性质的贡献5、分别用配分函数和自由能函数计算简单理想气体反应的平衡常数第一讲:统计热力学概论·Boltzmann 统计一、统计热力学概论(一)、统计热力学的基本任务1、统计热力学的基本任务回 顾:A 、 经典热力学的任务:a )解决某一过程的能量衡算;b )过程的方向判断据; 基础:热力学三定律;优点:着眼与系统的状态而不依赖系统的微观结构,高度可靠; 缺点:无法描述系统的微观结构和微观运动规律B 、统计热力学的任务:用统计学的原理,从系统的微观结构和运动状态出发,揭示系统宏观性质的本质。
物质的宏观性质本质上是微观粒子不停地运动的客观反映,虽然每个粒子都遵守力学定律,但是无法用力学中的微分方程去描述整个系统的运动状态,所以必须用统计学的方法。
根据对物质结构的某些基本假定,以及实验所得的光谱数据,求得物质结构的一些基本常数,如核间距、键角、振动频率等。
利用这些数据可以计算分子配分函数,再根据配分函数求出物质的热力学性质,这就是统计热力学的基本任务。
基础化学第7章知识点总结

基础化学第7章知识点总结第七章化合价与化合价化学式本章学习的主要内容有:1、化合价。
2、化合价的应用。
3、离子和离子化学式。
4、共价化学式和价键。
5、离子键。
一、化合价和化合价符号1. 化合价的含义化合价是指原子在化合物中的化合态所带的电荷数。
例如,氢气分子H2中,两个氢原子都是单价,氧气分子O2中,两个氧原子也都是双价,因此H2的量子化学式是H2,O2的量子化学式是O2。
氯气分子Cl2中,两个氯原子都是单价,在氯化钠NaCl中Cl是一价而Na是一价离子。
又如H2O的量子化学式是H2O,氧化氢的量子化学式是H2O,氧气的量子化学式是O2。
又如氢氧化钙Ca(OH)2中,氧是二价离子,高锰酸钾_KMnO4中,氧是二价离子。
2. 化合价的测定和改变化合价有原子内阴外电子数1:1或2:7跟原子化合价能力的规律。
测定它之前,要先分解化合物。
原子内阴外电子数如果满足1:1或2:7则改变不了化合价。
一般一价化合物都分子式是MX,原子间相对距离与中心原子半径之间的比值可以发现离子间离子键的关系。
二价化合物个分子的结构也可以确定化合物M的化合价。
分子间键能和结合能也与化合价有关。
3. 化合价化学式的性质化合价化学式有基本结构、原子分布、原子排列和化合价等等。
它和化合物化学式的相关性也很强。
比如α-铝石榴石结构,β-锡的晶识结构。
还有结构和性质之间的关系,化合价不同的化合物在Ι型结构等等的现象也表明了自己的性质。
4. 具有多种化合价的元素对于具有多种化合价的元素,其化合价在不同情况下可以有多种选择。
如铜,氮,碲等,都是有多种化合价的元素,主要是由于这些元素的内外电子数没满足1:2的要求所以很难只保留一个化合价。
二、化合价的应用1. 确定共价键和离子键通过化合价的计算可以确定共价键和离子键。
化合价差大于等于1.7都一般认为是离子键,小于等于1.7的一般认为是共价键。
碳的化合价结构中化合价原是共价性的。
2. 写化合价式可以根据化合价来写化合价式。
基础化学第七章课件

2011-5-25
酸和碱互为共轭,并组成共轭酸碱对,彼此之间差一 个H+,所以酸碱共轭统一在同一体系中的H+的传递。 质子理论中的酸碱不局限于分子,也可以是离子。 质子酸可以是:分子(HCl)、正离子(NH4+)、负离子 (HCO3-) 质子碱可以是:分子(NH3)、负离子(Ac-)、正离子 [Fe(H2O)5OH]2+ 有些酸碱物质在不同共轭酸碱对中既可以作酸,又可作 碱,称为两性物质。(HCO3-H2O)
电子教案
扬州工业职业技术学院应用化学系 朱权
1.掌握酸碱的定义、酸碱的强度及其影响因素、酸碱反 .掌握酸碱的定义、酸碱的强度及其影响因素、 应的实质; 应的实质; 2.掌握酸碱平衡中总浓度、平衡浓度及物料平衡的概念 .掌握酸碱平衡中总浓度、 ; 3.掌握 的含义,熟悉 与氢离子浓度的相互换算; 的含义, 与氢离子浓度的相互换算; .掌握pH的含义 熟悉pH与氢离子浓度的相互换算 4.了解溶液pH的近似测定; .了解溶液 的近似测定; 的近似测定 5.能利用化学平衡移动原理分析水、弱酸、弱碱的电离 .能利用化学平衡移动原理分析水、弱酸、 平衡; 平衡; 6.掌握多元弱酸电离的机理; .掌握多元弱酸电离的机理; 7.掌握同离子效应、盐效应等影响电离平衡移动的因素 .掌握同离子效应、 ; 8.熟练掌握有关离子浓度的计算; .熟练掌握有关离子浓度的计算; 9.说明同离子效应和缓冲溶液的特点,并掌握溶液 .说明同离子效应和缓冲溶液的特点,并掌握溶液pH 的计算了解缓冲容量和缓冲范围, 的计算了解缓冲容量和缓冲范围,会根据需要选择配制缓 上一内容 下一内容 回主目录 返回 冲溶液。 冲溶液。 2011-5-25
第三章酸碱平衡 第一节 酸碱理论基础
基础化学电子教案习题解答(第二章)

习题解答(第二章)1.选择题(1)25℃时,0.01mol/kg的糖水的渗透压为π1,而0.01 mol/kg的尿素水溶液的渗透压为π2,则____②____。
①π1<π2②π1 =π2③π1>π2④无法确定(2)应用克-克方程回答问题:当物质由固相变为气相时,平衡压力随温度降低而__③_____。
①不变②升高③降低④视不同物质升高或降低(3)通常称为表面活性剂的物质,是指当其加入少量后就能____③_____的物质。
①增加溶液的表面张力②改变溶液的导电能力③显著降低溶液的表面张力④使溶液表面发生负吸附(4)兰格缪尔(Langmuir)等温吸附理论中最重要的基本假设是_④___。
①气体为理想气体②多分子层吸附③固体表面各吸附位置上的吸附能力是不同的④单分子吸附(5)溶胶的基本特征之一是____④____。
④①热力学上和动力学上皆稳定的系统②热力学上和动力学上皆不稳定的系统③热力学上稳定而动力学上不稳定的系统④热力学上不稳定而动力学上稳定的系统(6)下列各性质中,属于溶胶的动力学性质的是___①_____。
①布朗运动②电泳③丁达尔现象④流动电势(7)引起溶胶聚沉的诸因素中,最重要的是___④______。
①温度的变化②溶胶浓度的变化③非电解质的影响④电解质的影响(8)用KBr加入浓的AgNO3溶液中,制备得AgBr溶胶,再向其中加入下列不同的电解质,能使它在一定时间内完全聚沉所需电解质最少的是__③______。
①Na2SO4②NaNO3 ③K3[Fe(CN)6] ④KCl(9)等体积0.10mol/dm3 KI和0.12mol/dm3的AgNO3溶液混合制成的AgI溶胶,下列电解质中,聚沉能力最强的是___④_______。
①Na 2SO 4 ②MgSO 4 ③K 3[Fe(CN)6] ④FeCl 32. 简答题(1) 理想气体存在吗?真实气体的pVT 行为在何种条件下可用pV=nRT 来描述?答:事实上,理想气体不存在。
基础化学第三版习题解答

基础化学(第3版)思考题和练习题解析第一章 绪 论1. 为什么说化学和医学的关系密切,医学专业学生必须学好化学?答:(略)2. “1 mol 硫酸的质量是98.0g ”,对吗?答:错误!未指明基本单元,正确说法是1 mol H 2SO 4的质量是98.0g 或1 mol[(1/2) (H 2SO 4)]的质量是49.0g 。
3. 0.4 mol H 2SO 4溶解于水,配成500 m L 溶液,其浓度表示正确的是A. c (H 2SO 4) = 0.8 mol·L -1B. c [21(H 2SO 4)] = 0.8 mol·L -1 C. c [21 (H 2SO 4) ]= 0.4 mol·L -1 D. 硫酸的浓度为0.8 mol·L -1 答;正确的是A 。
根据定义,1L 溶液中含有0.8 mol H 2SO 4,c (H 2SO 4) = 0.8 mol·L -1。
4. 下列说法正确的是A. “1 mol O ”可以说成“1 mol 原子O ”B. 1摩尔碳C 原子等于12gC. 1 L 溶液中含有H 2SO 4 98 g ,该溶液的摩尔浓度是1 mol·L -1D. 基本单元不仅可以是构成物质的任何自然存在的粒子或粒子的组合,也可以是想象的或根据需要假设的种种粒子或其分割与组合答:正确的是D 。
A 应说成“1 mol 氧原子”;B 应为“1摩尔碳C 原子的质量等于12g ”; C 不应该使用“摩尔浓度”,此术语已被废除。
5. 求0.100kg (21Ca 2+)的物质的量。
解:M (21Ca 2+) =(40.08 / 2)= 20.04 (g · mol -1), n (21Ca 2+) = [ m / M (21Ca 2+) ] = (0.100×103 )/20.04 = 4.99 (mol) 6. 每100m L 血浆含K + 为20mg ,计算K +的物质的量浓度,单位用mmol·L -1表示。
基础化学课后习题答案

基础化学课后习题答案在基础化学课后习题中,通常会涉及到化学反应原理、化学计量学、化学键、物质的分类、化学平衡、溶液的浓度计算等方面的问题。
以下是一些基础化学课后习题的典型答案示例:1. 化学反应原理- 题目:解释为什么铁在氧气中燃烧会产生火花?- 答案:铁在氧气中燃烧是一个氧化反应。
当铁与氧气接触时,铁原子失去电子形成Fe²⁺或Fe³⁺离子,而氧气获得电子形成O²⁻离子。
这个过程中释放出大量的能量,表现为火花和热量。
2. 化学计量学- 题目:计算2摩尔的氢气(H₂)与1摩尔的氧气(O₂)反应生成水的摩尔数。
- 答案:根据化学方程式 \(2H_2 + O_2 \rightarrow 2H_2O\),2摩尔的氢气与1摩尔的氧气完全反应生成2摩尔的水。
3. 化学键- 题目:描述离子键和共价键的区别。
- 答案:离子键是由正负离子之间的静电吸引力形成的,通常存在于金属和非金属之间。
共价键则是由两个原子共享电子对形成的,通常存在于非金属元素之间。
4. 物质的分类- 题目:区分纯净物和混合物。
- 答案:纯净物是由单一物质组成的,具有固定的化学组成和性质。
混合物则是由两种或两种以上的物质混合而成,没有固定的化学组成。
5. 化学平衡- 题目:解释勒夏特列原理。
- 答案:勒夏特列原理指出,如果一个处于平衡状态的化学反应系统受到外部条件的改变(如温度、压力或浓度的变化),系统会自动调整以减少这种改变的影响,从而重新达到平衡状态。
6. 溶液的浓度计算- 题目:如果将50毫升的0.1摩尔/升的盐酸溶液稀释到200毫升,计算稀释后的浓度。
- 答案:稀释前后溶质的物质的量不变。
稀释前的盐酸物质的量为\(50 \text{ mL} \times 0.1 \text{ mol/L} = 5 \text{ mmol}\)。
稀释后的浓度为 \(5 \text{ mmol} / 200 \text{ mL} = 0.025\text{ mol/L}\)。
高中化学 第七章 有机化合物 1.2 烷烃教案 新人教版必修2-新人教版高二必修2化学教案

(2)在烷烃的同系物中,随碳原子数增加,其熔、沸点依次升高(其中碳原子数满足小于或等于4条件的烷烃常温下呈气态),液态时密度依次增大。
解析:理解同系物、同分异构体的概念,会判断同系物、同分异构体。了解随碳原子数增加,烷烃熔点、沸点、密度的递变规律。
4.(双选)下列各组物质中一定互为同系物的是( BD )
题组一
1.下列有关烷烃的叙述中,正确的是( C )
①在烷烃分子中,所有的化学键都是单键
②烷烃中除甲烷外,很多都能使酸性KMnO4溶液的紫色褪去
③分子通式为CnH2n+2(n为正整数)的烃不一定是烷烃
④所有的烷烃在光照条件下都能与氯气发生取代反应
⑤光照条件下,乙烷通入溴水中,可使溴水褪色
A.①③⑤B.②③
(1)物理性质
烷烃的物理性质随C原子个数的增多呈现规律性的变化:
递变性
①烷烃的熔、沸点较低,且随碳原子数的增加烷烃的熔、沸点逐渐升高;
②碳原子数≤4的烷烃在常温常压下是气体,其他烷烃在常温常压下是液体或固体;
③烷烃的相对密度都较小,且随碳原子数的增加,烷烃的相对密度逐渐增大;
④碳原子数相同的烷烃,支链越多,熔、沸点越低。
4.习惯命名法
(1)当碳原子数(N)≤10时,用甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示;若N>10,用数字表示。
如:C8H18命名为辛烷,C11H24命名为十一烷。
[氧化还原反应教案(精选多篇)]氧化还原反应口诀
![[氧化还原反应教案(精选多篇)]氧化还原反应口诀](https://img.taocdn.com/s3/m/95f52c920b1c59eef9c7b4cf.png)
[氧化还原反应教案(精选多篇)]氧化还原反应口诀第一篇:氧化还原反应教学反思我们学生基础特别差,学生学习中存在困难有:1、不会写氧化还原反应的方程式;2、不会判断氧化剂和还原剂;3、更不会算转移的电子数;4、不会进行简单的物质的量与与转移电子数间的互算,氧化还原反应教学反思。
5、不会标“双线桥”“单线桥”。
我认为造成这些困难的原因有:1、学生基础差,许多同学初中都没认真学,现在学,很吃力,跟不上;2、不会根据化合价写化学式,就不会判断化合价的升降了;3、记不住常见元素的化合价,不会合理标出有变价元素的化合价。
4、不会进行简单的计算。
我在教学中,采用的方法是:1、先复习化合价的口诀,根据化合价书写化学式的方法,反复练习书写常见物质的化学式,并让学生标出化合价;2、再从最简单的氧化还原反应入手,从得氧失氧的角度引导学生分析氧化剂和还原剂,提出问题:有些不含氧的怎样判断呢?引导学生观察和分析反应物和生成物中的元素的化合价是不同的,并作比较,得出化合价升降与得失电子以及与氧化剂和还原剂的关系,再多举几例进行练习,归纳方法,启发学生编成顺口溜:升——失——氧化——还原剂;降——得——还原——氧化剂,教学反思《氧化还原反应教学反思》。
使学生记住,每次遇到一个新方程式,就拿出来进行判断,反复练习,慢慢的有所提高。
3、氧化还原反应中转移电子数的计算,就从最简单的算数教起,一步一步的教给学生,先找有变价元素的化合物,标出变价元素的化合价,计算出一个原子得(失)几个,该分子中有几个该原子,共几个分子,一共多少,就像教小学生一样,慢慢地许多同学赶上来了。
总之,每节课,都要复习前面的旧知识,做好铺垫,慢慢学,慢慢提高,用得时间就会很多。
第二篇:氧化还原反应学习总结氧化还原反应学习总结任丘二中刘文芳氧化还原反应属于抽象概念教学,是中学化学教学的重点和难点。
氧化还原反应在中学阶段占有非常重要的地位,贯穿于中学化学教材的始终。
基础化学第七版课后练习题含答案

基础化学第七版课后练习题含答案简介基础化学是大学生必修的专业课程之一。
此文档为基础化学第七版的课后练习题及其答案,旨在为学生提供参考和指导。
第一章:物质的基本结构选择题1.以下不属于分子性固体的是() A. CO2 B. NaCl C. SiO2 D. H2O2.具有离子特征的物质是() A. 氧气 B. 水蒸气 C. 纯净水 D. 氢气3.分子式为C6H12O6的物质是() A. 脱氧核糖 B. 核苷酸 C. 葡萄糖 D. 羟基脂4.下列哪个元素对地球物质成分占比最之() A. Na B. K C. Ca D.Fe填空题1.第一位圆周率的值为()2.化学元素周期表中排列的准则是()3.水是一种()4.茶叶发酵过程中,由于微生物作用,会产生一种重要的香气化合物,叫做()简答题1.描述原子的基本结构,明确原子核和电子的作用。
2.简要介绍离子键和共价键的区别。
3.简述一下水的性质及其在生命中的重要作用。
答案选择题: 1. A 2. B 3. C 4. C 填空题: 1. 3.1415926 2. 原子序数的递增排列规则 3. 液体 4. 芳香化合物简答题: 1. 原子是由原子核和电子组成的。
原子核由带正电荷的质子和不带电的中子组成,位于原子的中心,占据了原子的绝大部分质量。
电子带负电荷,以电子云的形式环绕在原子核周围的各层轨道上,是原子的化学性质的决定因素。
质子数等于电子数时,原子是稳定的。
2. 离子键是由带相反电荷的离子相互作用形成的。
共价键是由原子之间共用一个或多个电子对形成的。
3. 水是一种氢原子与氧原子形成的分子化合物。
具有极性分子,可以与其他极性或离子化合物发生相互作用。
水在生命中的重要作用有很多,它是生命体内的主要组成成分之一,对维持机体的正常生理状态具有重要意义。
作为溶剂,水可以溶解许多物质,为生物体内大量化学反应提供了必要的条件。
同时,水也可以调节体内的温度,起到保温作用。
_《基础化学》(第三版)电子教案[4页]
![_《基础化学》(第三版)电子教案[4页]](https://img.taocdn.com/s3/m/bb885ce1ba1aa8114531d94e.png)
基础化学(第三版)
机化合物。 电子教案内容可根据需要进行增减调整,既为使
用该教材的广大教师备课和进行多媒体教学提供了便 利,又为学生自学提供了参考。
电子教案由王宝仁组织制作。制作过程中得到大 连理工大学出版社支持与帮助,在此表示诚挚谢意。
由于制作时间和编者水平所限,教案中不妥和错 误之处在所难免,敬请读者批评指正,以便修改。
基础化学(第三版)
前言
本电子教案供王宝仁 王英健主编的“十二五” 职业教育国家规划教材修订版《基础化学》(第三 版)一书配套使用。
电子内容紧扣教材,主要包括气体、溶液及相 平衡,化学热力学基础,化学反应速率和化学平衡, 酸碱平衡与酸碱滴定法,沉淀溶解平衡与沉淀滴定 法,物质结构基础知识,氧化还原平衡与氧化还原 滴定法,配位平衡和配位滴定法,脂肪烃,环烃和 杂环化合物,卤烃和含氧有机化合物、含氮有
基础化学 (第三版)
电子教案
主编: 王宝仁
大连理工大学出版社
第1章 气体、溶液与相平衡 第2章 化学热力学基础 第3章 化学反应速率和化学平衡 第4章 酸碱平衡与酸碱滴定法 第5章 沉淀溶解平衡与沉淀滴定法 第6章 物质结构基础知识 第7章 氧化还原平衡与氧化还原滴定法 第8章 配位平衡和配位滴定法 第9章 脂肪烃 第10章 环烃和杂环化合物 第11章 卤烃和含氧有机化合物 第12章 含氮有机化合物
编者E-mail联系地址:wbr8886@ 王宝仁
2017年9月
上页 下页
化学人教版高中必修二(2019年新编)-第七章第三节乙醇与乙酸-乙醇教案

生活中常见的有机物——乙醇山西省榆次第一中学校李博融【教学目标与评价目标】1.教学目标(1)通过总结乙醇在日常生活与工业生产中的广泛应用、关注与化学有关的社会热点问题,辩证看待化学对人类的影响,形成将化学知识应用于生产与生活的意识,培养正确的科学态度与社会责任。
(2)通过对乙醇分子组成、结构和性质的探究,建立官能团等立体结构模型,能够运用结构模型解释性质,形成“结构决定性质”的基本观念。
(3)形成“(组成)结构—性质—用途”的学习有机物的认知模型,掌握有机化学的学习方法。
2.评价目标(1)通过球棍模型分析乙醇分子的断键情况,提升学生的宏观辨识与微观探析素养。
(2)通过解释乙醇性质,发展学生“结构决定性质”观念。
【教学重点】乙醇的分子结构、乙醇的化学性质【教学难点】建立乙醇的立体结构模型【教学方法】1、PBL(Problem-Based Learning,问题导向式学习):创设问题情境,激发学习兴趣,调动学生内在的学习动力。
2、生活化教学:观看资料、总结身边的事例,了解乙醇的物理、化学性质。
通过学习乙醇的应用,感受化学知识在生活、生产中的重要作用。
3、实验探究法:提出问题→作出假设→设计方案→进行实验→实验结果→分析讨论→实验结论。
培养学生的科学探究精神。
4、多媒体教学法:观看flash动画,对宏观现象进行微观解释,形成“结构决定性质”的基本观念。
【教学用具】实验试剂:钠、乙醇、铜丝实验仪器及用品:试管、试管夹、注射器针头、橡皮塞、坩埚钳、玻璃片、小刀、镊子、滤纸、酒精灯、火柴、手帕、球棍模型【教学流程】教学环节学生活动教师活动导入新课物理性质取代反应氧化反应课堂小结展示资料观看、思考点拨指导创设问题情境点拨指导分组实验探究结合生产生活小结知识分组实验探究归纳学习方法组成结构写乙醇结构式组装乙醇结构实验总结创设问题情境形成基本观念【教学过程】[趣味实验]“烧不坏的手帕”实验步骤:①手帕放在盛有无色液体的烧杯中浸泡②将手帕平铺开,点燃[S观察]观察实验现象:①手帕”剧烈燃烧②火焰熄灭,手帕完好无损[过渡]这种“神奇的无色液体”是谁呢?就是我们今天的主角——乙醇。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
思考与习题一、填空题1.中心离子是配合物的形成体,它位于配离子的中心。
常见的中心离子是带正电的金属元素的离子.2.配位体中具有孤对电子、直接与中心离子(或原子)结合的原子叫配位原子。
如NH3中的N 原子是配位原子。
在配离子中与中心离子直接结合的配位原子数目叫中心离子或原子的配位数。
3.填充下表:配合物的化学式命名中心离子配离子电荷配位体配位数[Ag(NH3)2] NO3K4[Fe(CN)6 ]K3[Fe(CN)6 ]H2[PtCl6][Zn(NH3)4]( OH)2[Co(NH3)6] Cl3硝酸二氨合银(Ⅰ)六氰合铁(Ⅱ)酸钾六氰合铁(Ⅲ)酸钾六氯合铂(Ⅳ)酸氢氧化四氨合锌(Ⅱ)(三)氯化六氯合钴(Ⅱ)Ag+Fe2+Fe3+Pt4+Zn2+Co3++1-4-2-2+2+3NH3CN-CN-Cl-NH3NH32666464.配合物在水溶液中全部电离成配离子和外界离子,而配离子在水溶液中部分电离,存在着配位平衡。
在[Ag(NH3)2]+水溶液中的离解平衡式为[Ag(NH3)2]+ Ag++2NH3。
5.配位数相同的配离子,若K稳愈大或K不稳愈小,则该配离子愈稳定,若K不稳值愈大,表示该配离子离解程度愈大。
6.在AgNO3溶液中加入NaCl溶液,产生AgCl (写化学式)沉淀,反应的离子方程式为Ag++Cl-→AgCl↓。
静置片刻,弃去上面清液,在沉淀中加入过量氨水,沉淀溶解,生成了[Ag(NH3)2] Cl (写化学式),反应的离子方程式为AgCl+2NH3→[Ag(NH3)2] ++Cl- 。
7.当配离子中的配位体能与H+合成弱酸时,则溶液中酸度增大时,配离子的稳定性会减弱。
8.当一种配离子转化为另一种配离子时,反应物中配离子的K稳愈小,生成物中配离子的K稳愈大,那么这种转化愈完全。
9.络合滴定曲线滴定突跃的大小取决于 配合物条件稳定常数和被滴定金属离子浓度 。
在金属离子浓度一定的条件下, K ’MY 越大,突跃 范围越大 ;在条件常数K ’MY 一定时, 金属离子浓度 越大,突跃 越大 。
10. K ’MY 值是判断络合滴定误差大小的重要依据。
在pM ’一定时,K ’MY 越大,络合滴定的准确度 愈高 。
影响K ’MY 的因素有 酸效应与金属离子配合物的稳定常数 ,其中酸度愈高 lg αY(H) 愈大,lgK ’MY 越小 ; 配离子 的络合作用常能增大 lg αY(H) ,减小 lgK ’MY 。
二、选择题1. AgCl 在下列哪种溶液中(浓度均为1mol/L)溶解度最大?( A ) A. NH 3水 B. Na 2S 2O 3 C. KI D. NaCN2.下列关于酸效应系数的说法正确的是( AC ) A.αY(H)值随着pH 增大而增大 B. 在pH 低时αY(H)值约等于零 C. lg αY(H)值随着pH 减小而增大 D. 在pH 高时lg αY(H)值约等于是1 E. 在pH 低时αY(H)值约等于13.一般情况下,EDTA 与金属离子形成的络合化合物的络合比是( A ) A. 1:1 B. 2:1 C. 1:3 D. 1:24. )(L M α=1表示( A )A. M 与L 没有副反应B. M 与L 的副反应相当严重C. M 的副反应较小D. [M] = [L] 5. EDTA 滴定金属离子,准确滴定的条件是( D )A. lgK MY ≥6B. ≥'lg MY K 6 C. lg(c sp K MY )≥6 D. ≥)lg('MY sp K c 66. 用EDTA 直接滴定有色金属离子M ,终点所呈现的颜色是( A ) A. 游离指示剂的颜色 B. EDTA-M 络合物的颜色 C. 指示剂-M 络合物的颜色 D. 上述A+B 的混合色 三、是非题 (下列叙述中对的打“√”,错的打“×”)1.配合物在水溶液中可以全部离解为外界离子和配离子,配离子也能全部离解为中心和配位体。
( × )2.当配离子转化为沉淀时,难溶电解质的溶解度愈小,则愈易转化。
( √)3.一种配离子在任何情况下都可以转化为另一种配离子。
( ×)4.由于配离子的生成,使金属离子的浓度发生改变,从而改变了其电极电势,所以配离子的生成对氧化还原反应有影响.( √)5.只要金属离子能与EDTA形成配合物,都能用EDTA直接滴定。
( ×)6.一般来说,EDTA与金属离子生成配合物的K(MY)越大,则滴定允许的最高酸度越大。
( ×)7.对一定的金属离子来说,溶液酸度一定,当溶液中存在的其他配位剂浓度愈高,则该金属与EDTA配合物的条件稳定常数K’MY越大。
( √)8.游离金属指示剂本身的颜色一定要和与金属离子形成的配合物颜色有差别。
( √)9.EDTA滴定中,当溶液中存在某些金属离子与指示剂生成极稳定的配合物,则产生指示剂的封闭现象。
( √)10. 用EDTA直接滴定有色金属离子M,终点所呈现的颜色是EDTA-M络合物的颜色。
( ×)四、问答题1.无水CrCl3和氨作用能形成两种配合物,组成相当于CrCl3·6NH3及CrCl3·5NH3。
加入AgNO3溶液能从第一种配合物水溶液中将几乎所有的氯沉淀为AgCl,而从第二种配合物水溶液中仅能沉淀出相当于组成中含氯量2/3的AgCl,加入NaOH并加热时两种溶液都无味。
试从配合物的形式推算出它们的内界和外界,并指出配离子的电荷数、中心离子的氧化数和配合物的名称。
答案:内界外界配离子电荷数中心离子的氧化数配合物的名称[Cr(NH3)6]Cl [Cr(NH3)6]+ Cl- 1 +1 一氯化六氨合铬[CrCl·(NH3)5]Cl2[CrCl·(NH3)5]2+ Cl22- 2 +3 二氯化一氯·五氨合铬(Ⅰ)答案关键词:[Cr(NH3)6]Cl [CrCl·(NH3)5]Cl22.写出下列配合物的化学式(1) 二硫代硫酸合银(Ⅰ)酸钠 (2) 三硝基三氨合钴(Ⅲ) (3) 氯化二氯三氨一水合钴(Ⅲ) (4) 二氯二羟基二氨合铂(Ⅳ)(5) 硫酸一氯一氨二(乙二胺)合铬(Ⅲ) (6) 二氯一草酸根一(乙二胺)合铁(Ⅲ)离子答案:(1) Na[Ag(S 2O 2)] (2)Co[(NO 3)3(NH 3)2] (3) [CoCl 3(NH 3)2(H 2O)]Cl(4) [PtCl 2(OH)2(NH 3)2] (5) [CrCl (NH 3)en]SO 4 (6) [FeCl 2en] C 2O 4答案关键词:3. EDTA 与金属离子的配合物有何特点? 答案:①EDTA 分子中具有六个可与金属离子形成配位键的原子因此EDTA 能与许多金属离子形成稳定的配合物;②EDTA 与金属离子能形成摩尔比为1:1的配合物,只有极少数金属离子例外,对多数金属离子而言,不存在逐级配位现象。
③无色金属离子与EDTA 生成的配合物仍为无色的,有色金属离子与EDTA 形成的配合物的颜色加深,因此地丁这些离子时,试液的浓度不能过大。
答案关键词:EDTA 配合物五、计算题1. 已知[AlF 6]3-的逐级稳定常数的对数值分别为6.13、5.02、3.85、2.74、1.63、0.74,试求它们的K 稳。
解:根据K 稳=K 1·K 2·K 3…K n[]=-36AlF K 稳10(6.13+5.02+3.85+2.74+1.63+0.74)=1020.112. 在含有2.5⨯10-3 mol/L AgNO 3和0.41 mol/L NaCl 溶液里,如果不使AgCl 沉淀生成,溶液中最少应加入CN - 浓度为多少? 已知)])(([2-CN Ag K 稳 = 1.26 ⨯1021 ,K sp (AgCl) =1.56 ⨯10-10解:首先根据不使AgCl 沉淀生成,求解出游离[Ag +]必须小于的浓度 AgCl (s)Ag + + Cl -x 0.41 0.41x= K sp (AgCl)=1.56⨯10-10x=3.8⨯10-10mol/L没达到平衡时[CN -]=y 则:Ag + + 2CN -[ Ag(CN - )2]-3.8⨯10-10 y 2.5⨯10-3-3.8⨯10-102121031026.1108.3105.2⨯=⋅⨯⨯--y即 y=0.72⨯10-7故 最小CN -为:2.5⨯10-3⨯2+0.72⨯10-7=5.0⨯10-3mol/L3. 0.1mol/L AgNO 3溶液50ml ,加入相对密度为0.932含氨18.24%的氨水30 ml 后,加水稀释至100 ml ,求此溶液中[Ag +]、[Ag(NH 3)2]+和[NH 3]? (已知)])(([23+NHAg K 稳=1.7×107)解:两种溶液混合后,因溶液中NH 3·H 2O 过量,Ag +能定量地转化为[Ag(NH 3)2]+,且每形成1mol[Ag(NH 3)2]+要消耗2molNH 3·H 2OAg ++ 2NH 3[Ag(NH 3)2]+初始浓度 0.05 3.0 0平衡浓度 x 3.0-0.05⨯2+2x 0.05⨯2-x [][][]72323107.1)(⨯=++NH Ag NH Ag K=稳θx=()72107.1205.00.3205.0⨯⨯⨯⨯-=6.99⨯10-10即 [Ag +]=6.99⨯10-10[NH 3]=2.9mol/L[Ag(NH 3)2]=0.1mol/L*4.计算[Ag(NH 3)2]+ +eAg + + 2NH 3体系的标准电极电势(已知)])(([23+NHAg K 稳=1.7×107,φοAg+/Ag =0.80V)解:首先计算平衡态时离解出的Ag +的浓度: [Ag(NH 3)2]+Ag ++ 2NH 3[]稳稳=K NH Ag NH Ag K /1])([][2323=⋅++θ由于反应在标准状态下进行,配离子和配体的浓度均为1mol/L ,则[Ag +]=()[]()+231NH Ag K 稳代入能斯特方程式: ()[]()[]++=++Ag Ag Ag Ag NHAg lg 059.0//23θθϕϕ=0.8955.用CaCO 3 基准物质标定EDTA 溶液的浓度,称取0.1005g CaCO 3 基准物质溶解后定容为100.0mL 。
移取25.00mL 钙溶液,在pH=12时用钙指示剂指示终点,以待标定EDTA 滴定之,用去24.90mL 。
(1)计算EDTA 的浓度;(2)计算EDTA 对ZnO 和Fe 2O 3的滴定度。
