眼刺激性体外评价方法研究进展
严重眼睛损伤 眼睛刺激性(GB20594-2006)

化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性GB20594-2006化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性Safety rules for classification,precautionary labeling and precautionary statements of chemicals-Serious eye damage/eyeirritation前言本标准第4章、第6章、第7章、第8章为强制性的,其余为推荐性的。
本标准与联合国《化学品分类及标记全球协调制度》(GHS)的一致性程度为非等效,其有关技术内容与GHS中一致,在标准文本格式上按GB/T 1.1—2000做了编辑性修改。
本标准由全国危险化学品管理标准化技术委员会(SAC/TC 251)提出并归口。
本标准负责起草单位:江苏出入境检验检疫局。
本标准参加起草单位:安徽出入境检验检疫局、中化化工标准化研究所、山东出入境检验检疫局、中国疾病预防控制中心。
本标准主要起草人:汤礼军、温劲松、吕伯钦、韩德平、张君玺、卞学东、周飞舟。
本标准自2008年1月1日起在生产领域实施;自2008年12月31日起在流通领域实施,2008年1月1日~12月31日为标准实施过渡期。
化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性1 范围本标准规定了化学品引起的严重眼睛损伤/眼睛刺激性的术语和定义、分类、判定流程、类别和警示标签、类别和标签要素的配置及警示性说明的一般规定。
本标准适用于化学品引起的严重眼睛损伤/眼睛刺激性按联合国《化学品分类及标记全球协调制度》的危险性分类、警示标签和警示性说明。
2 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
严重眼睛损伤眼睛刺激性(GB20594-2006)综述

化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性GB20594-2006化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性Safety rules for classification,precautionary labeling and precautionary statements of chemicals-Serious eye damage/eyeirritation前言本标准第4章、第6章、第7章、第8章为强制性的,其余为推荐性的。
本标准与联合国《化学品分类及标记全球协调制度》(GHS)的一致性程度为非等效,其有关技术内容与GHS中一致,在标准文本格式上按GB/T 1.1—2000做了编辑性修改。
本标准由全国危险化学品管理标准化技术委员会(SAC/TC 251)提出并归口。
本标准负责起草单位:江苏出入境检验检疫局。
本标准参加起草单位:安徽出入境检验检疫局、中化化工标准化研究所、山东出入境检验检疫局、中国疾病预防控制中心。
本标准主要起草人:汤礼军、温劲松、吕伯钦、韩德平、张君玺、卞学东、周飞舟。
本标准自2008年1月1日起在生产领域实施;自2008年12月31日起在流通领域实施,2008年1月1日~12月31日为标准实施过渡期。
化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性1 范围本标准规定了化学品引起的严重眼睛损伤/眼睛刺激性的术语和定义、分类、判定流程、类别和警示标签、类别和标签要素的配置及警示性说明的一般规定。
本标准适用于化学品引起的严重眼睛损伤/眼睛刺激性按联合国《化学品分类及标记全球协调制度》的危险性分类、警示标签和警示性说明。
2 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
刺激性、过敏性和溶血性试验的方案设计与实施

过敏性实验
实验目的:观察动物接触受试物后是否产生全身或局 部过敏反应,为临床用药提供安全性依据。
实验分类:经皮给药过敏性实验:豚鼠最大化实验 (GPMT)和Buehler实验(BT) 注射给药过敏性实验:被动皮肤过敏实验 (PCA)和全身主动过敏实验(ASA)
被动皮肤过敏实验
实验动物:常用的动物是大鼠,亦用小鼠、豚鼠。 实验分组:阴性对照组:同体积的溶媒;
它是临床前安全性评价的组成部分。
刺激性实验
实验目的:观察动物的血管、肌肉、皮肤、粘膜等 部位接触受试物后是否引起红肿、充血、渗出、变 性或坏死等局部反应,为临床用药提供安全性依据。
实验分类:皮肤刺激性实验; 注射给药部位的刺激性实验; 眼刺激性实验; 皮肤光毒性(光刺激性)实验
刺激性实验
实验设计:
阳性对照组:卵白蛋白1-5mg/只; 受试物低剂量组:临床最大剂量(/kg或m2); 受试物高剂量组:低剂量的数倍量。 每组动物数至少6只。
被动皮肤过敏实验
实验方法:
➢ 致敏:
抗体的制备 :选择容易产生抗体的给药方法,如静脉、腹腔或皮 下注射等,隔日一次,共3-5次。末次致敏后10-14天左右采血, 2000转/分离心10分钟,分离血清,-20℃保存,2周内备用。
表 2.皮肤刺激强度评价标准
注射给药部位刺激性实验
适用范围:注射剂应考虑进行注射给药部位刺激性实验。 实验动物:首选家兔,每组动物数不少于3只。 实验方法:
⑴应设生理盐水对照,采用同体左右侧自身对法; ⑵用药部位根据药物的给药途径确定,可选用耳缘静脉、 耳中心动脉、股和背部肌肉、静脉旁组织等; ⑶一般按临床给药方案给予受试物,多次给药一般不超过7 天;
➢ 结果观察: 无溶血:红细胞全部下沉,上清液体无色澄明; 溶血:溶液呈澄明红色,管底无细胞残留或有少量红细胞残留; 凝聚:溶液中有棕红色或红棕色絮状沉淀,振摇后不分散。
严重眼睛损伤 眼睛刺激性(GB20594-2006)汇编

化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性GB20594-2006化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性Safety rules for classification,precautionary labeling and precautionary statements of chemicals-Serious eye damage/eyeirritation前言本标准第4章、第6章、第7章、第8章为强制性的,其余为推荐性的。
本标准与联合国《化学品分类及标记全球协调制度》(GHS)的一致性程度为非等效,其有关技术内容与GHS中一致,在标准文本格式上按GB/T 1.1—2000做了编辑性修改。
本标准由全国危险化学品管理标准化技术委员会(SAC/TC 251)提出并归口。
本标准负责起草单位:江苏出入境检验检疫局。
本标准参加起草单位:安徽出入境检验检疫局、中化化工标准化研究所、山东出入境检验检疫局、中国疾病预防控制中心。
本标准主要起草人:汤礼军、温劲松、吕伯钦、韩德平、张君玺、卞学东、周飞舟。
本标准自2008年1月1日起在生产领域实施;自2008年12月31日起在流通领域实施,2008年1月1日~12月31日为标准实施过渡期。
化学品分类、警示标签和警示性说明安全规范严重眼睛损伤/眼睛刺激性1 范围本标准规定了化学品引起的严重眼睛损伤/眼睛刺激性的术语和定义、分类、判定流程、类别和警示标签、类别和标签要素的配置及警示性说明的一般规定。
本标准适用于化学品引起的严重眼睛损伤/眼睛刺激性按联合国《化学品分类及标记全球协调制度》的危险性分类、警示标签和警示性说明。
2 规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
不同红细胞溶血实验替代兔眼刺激性实验比较研究

不同红细胞溶血实验替代兔眼刺激性实验比较研究1. 引言1.1 背景红细胞溶血实验是一种常用的实验方法,用于评估各种物质对红细胞的溶解程度。
而兔眼刺激性实验则是一种常用的实验方法,用于评估化妆品等化学物质对眼部组织的刺激程度。
兔眼刺激性实验存在一定的局限性,包括对动物造成痛苦和不准确的实验结果等问题。
寻找一种替代方法来评估物质对眼部组织的刺激性变得十分重要。
一种可能的替代方案是利用不同的红细胞溶血实验,通过评估物质对红细胞的溶解程度来预测其对眼部组织的刺激性。
这种方法的优势包括更快速、更准确地评估物质的刺激性,同时避免对动物进行残酷实验。
在本研究中,我们将比较不同红细胞溶血实验替代兔眼刺激性实验的优势和局限性,并探讨这种替代方法的可行性。
希望通过这项研究,能为替代动物实验提供新的思路和方法,推动科学研究向更加人道化和有效的方向发展。
1.2 目的为了减少动物实验对动物的伤害,提高实验效率和准确性,本研究旨在比较不同红细胞溶血实验替代兔眼刺激性实验的优劣势,并探讨其在实验应用中的可行性。
通过对不同实验方法的原理和特点进行分析和比较,旨在为相关领域的实验设计和实践提供参考,促进替代方法的推广和应用。
本研究旨在探讨不同实验方法在红细胞溶血和刺激性评价中的准确度和可靠性,并为未来的研究和实验设计提供理论基础和实践参考。
最终目的是为了推动科学研究领域的动物实验替代方法的发展,促进动物保护和实验伦理的进步。
1.3 意义红细胞溶血实验是一种常用的生物学实验方法,用于评估各种物质对红细胞膜的破坏作用。
而兔眼刺激性实验则是一种常用的生物毒性试验方法,用于评估各种化学物质对眼部组织的刺激性和损伤程度。
传统的兔眼刺激性实验存在一定的局限性,例如操作复杂、动物使用数量大、费时费力等问题。
寻找一种更加简便、快速、可靠的替代方法具有重要的现实意义。
本研究旨在探讨不同红细胞溶血实验作为替代兔眼刺激性实验的可行性及优劣势。
通过对比两种实验方法的原理、优势、局限性以及相关研究现状,可以为寻找一种更合适的生物毒性测试方法提供参考和指导。
眼刺激试验替代方法研究进展

受精鸡卵尿囊绒膜试验 ( hen’s egg test2chorioal2 lantoic membrane , HET2CAM) 即是利用受精鸡卵尿囊 绒膜 (CAM) 与结膜结构相似的特性 ,来检测化学物 质对 CAM 的损伤 。步骤大致为 ,去除受精鸡卵气室 端卵壳 ,水封壳膜 ,然后去壳膜 ,受试物通过硅酮橡 胶环作用于 CAM ,用显微镜观察评分法 ( HET2CAM score) 5 和台盼蓝染色法 ( CAM - TB) 6 ,7 检测 CAM 的损伤 。 2. 2 检测细胞膜损伤
理化学技术 、数学计算机模型和体外模型而不使用 整体动物来进行试验研究 。
在“3R”运动的推动下 ,许多国家的毒理学安全 性评价 方 法 有 所 改 革 。欧 共 体 要 求 其 成 员 国 从 2002 年 7 月 1 日起禁止使用动物对化妆品及其原料 进行安全性检测 ,并列入 WTO 双边协议的条款 。我 国目前各类产品的安全性评价仍主要沿用传统的动 物实验 ,与有关国际条约没有接轨 。
【Abstract】 On account of the limitation of Draize eye irritation test , alternative methods in vitro for Draize test have been developed and validated recently , with the prosperity of the“three Rs”movement. Because they have different mechanisms and
药物刺激性、过敏性和溶血性研究技术指导原则 (2014-05-13)分析

附件4药物刺激性、过敏性和溶血性研究技术指导原则一、概述刺激性、过敏性、溶血性是指药物制剂经皮肤、粘膜、腔道、血管等非口服途径给药,对用药局部产生的毒性(如刺激性和局部过敏性等)和/或对全身产生的毒性(如全身过敏性和溶血性等),为临床前安全性评价的组成部分。
药物的原形及其代谢物、辅料、有关物质及理化性质(如pH值、渗透压等)均有可能引起刺激性和/或过敏性和/或溶血性的发生,因此药物在临床应用前应研究其制剂在给药部位使用后引起的局部和/或全身毒性,以提示临床应用时可能出现的毒性反应、毒性靶器官、安全范围。
本指导原则适用于中药、天然药物、化学药物。
二、基本原则(一)试验管理根据《药品注册管理办法》,药物刺激性、过敏性和溶血性研究必须执行《药物非临床研究质量管理规范》(GLP)。
(二)随机、对照、重复试验设计应遵循随机、对照、重复的原则。
(三)整体性、综合性原则应根据受试物特点,充分考虑和结合药学、药效学、其他毒理学及拟临床应用情况等综合评价,体现整体性、综合性的原则。
(四)具体问题具体分析应在遵循安全性评价普遍规律的基础上,具体问题具体分析,结合受试物的特点,在阐明其研究方法或技术科学、合理的前提下进行规范性试验,对试验结果进行全面分析评价。
三、基本内容(一)受试物和实验动物1.受试物中药、天然药物:受试物应能充分代表临床试验样品或上市药品。
应采用工艺路线及关键工艺参数确定后的工艺制备,一般应为中试或中试以上规模的样品,否则应有充分的理由。
应注明受试物的名称、来源、批号、含量(或规格)、保存条件及配制方法等,由于中药的特殊性,建议现用现配,否则应提供数据支持配制后受试物的质量稳定性及均匀性。
试验中所用溶媒和/或辅料应标明名称、标准、批号、规格及生产单位。
化学药物:受试物应采用工艺相对稳定、纯度和杂质含量能反映临床试验拟用样品和/或上市样品质量和安全性的样品。
受试物应注明名称、来源、批号、含量(或规格)、保存条件及配制方法等,并附有研制单位的自检报告。
利用离体牛角膜多次暴露方法评测化妆品套装的眼刺激性

利用离体牛角膜多次暴露方法评测化妆品套装的眼刺激性黄健聪;陈志杰;陈义珠;秦瑶【摘要】Five commercially available cosmetic kits were evaluated by using the standard and modified bovine corneal opacity and permeability (BCOP) test,and the changes of opacity and permeability were compared in different test alternatives,developed a preliminary evaluation method of in vitro bovine corneal multi-exposure.Results show that according to the standard test method,each of five kits tested is non-irritation.On the other hand,the five kits,by the modified test,may cause eye irritation resulted from the various changes of opacity and permeability of the corneas.In conclusion,the modified BCOP test is demonstrated to be an appropriate method for multi-exposure eye irritation assessment of cosmetic kits,which can provide reference for improving product safety.%采用标准和改良的牛角膜浑浊度和渗透性(BCOP)试验对市售5种化妆品洗护套装进行评测,并比较不同方案下渗透性和浑浊度2个参数的变化,初步建立多次眼暴露的离体牛角膜试验体外评价方法.结果表明,采用标准方法套装内单个产品均显示无眼刺激性,而多次暴露后,发现角膜浑浊度和渗透性均出现了不同程度的变化,可能产生眼刺激性.改良后的BCOP测试方法可用于多次暴露的眼刺激性评价,为产品安全性的提升提供了参考.【期刊名称】《日用化学工业》【年(卷),期】2018(048)002【总页数】4页(P109-112)【关键词】化妆品;眼刺激;牛角膜;多次暴露【作者】黄健聪;陈志杰;陈义珠;秦瑶【作者单位】广州市华代生物科技有限公司,广东广州 510535;广州市华代生物科技有限公司,广东广州 510535;广州市华代生物科技有限公司,广东广州 510535;广州市华代生物科技有限公司,广东广州 510535【正文语种】中文【中图分类】TQ658从20世纪90年代开始,眼刺激的动物实验替代方法陆续进入验证程序。
眼用药物临床前安全性评价的一些考虑

发布日期20040220栏目化药药物评价>>非临床安全性与有效性评价标题眼用药物(改剂型改途径)临床前安全性评价的一些考虑作者文宇部门正文内容眼用药物(改剂型改途径)临床前安全性评价的一些考虑审评三部医学组文宇部分国内申请中对改剂型眼用药存在一些较为突出的现象,就就是对临床前安全性研究缺乏较系统的认识,大多仅提供了眼部刺激性试验资料,未能结合所申报品种的具体情况进行综合分析。
针对上述问题,参考国内外有关问题提出以下改剂型眼用药物临床前安全性评价的一些考虑,愿与大家共同探讨。
一、一般考虑与一般药物的临床前评价安全性评价原则相同,改剂型眼用药物临床前评价的重点也在于安全性。
只就是这种安全性的考虑即要体现在系统性上,又要结合眼科用药的特点与化合物本身情况进行综合分析。
改剂型的眼用药物临床前安全性评价的一般考虑为:(一)全身毒性:眼部用药的给药剂量甚微,据测定人结膜囊内的最大液体容量为20-30ul,除去10ul的正常泪液,最多只能容纳20ul药液。
眼部给药后药物进入体循环的量非常少,一般不产生具有临床意义的全身药理作用。
通常下列情况下无需进行进一步的全身毒性研究:1.已证明药物眼部吸收缓慢,可明确排除该药物眼部给药的全身作用。
2.药物可被吸收,但以前已进行了充分的全身毒性研究(包括急性毒性、长期毒性、生殖毒性、致突变、致癌试验等)。
(二)眼部耐受性:1.眼部刺激性试验:眼用药物的临床前安全性首先需评价眼部刺激性,这项试验对于各种类型眼用药物的研发均必不可少。
1.1试验的意义:药物直接接触角膜后会引起刺激作用,表现为炎症反应。
短期内接触刺激性较强的药物可产生灼痛、流泪、畏光等症状以及结膜充血、水肿等体征。
长时间接触刺激性较弱的药物可引起慢性结膜炎或睑缘炎,表现为充血、分泌物增多。
兔眼与人眼结构相似,故可采用兔眼进行眼部刺激性试验以提供初步的眼部用药安全性信息,保证受试药物用于人眼时无明显的刺激性。
(推荐)戊二醇、己二醇、辛酰羟肟酸等防腐剂的眼刺激性评价
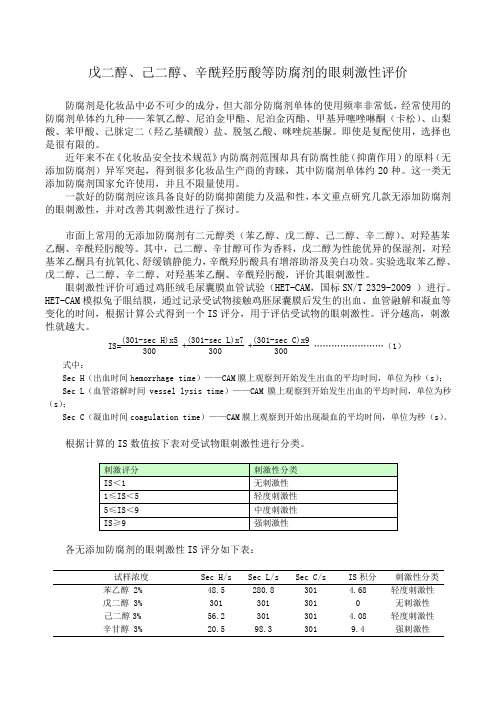
戊二醇、己二醇、辛酰羟肟酸等防腐剂的眼刺激性评价防腐剂是化妆品中必不可少的成分,但大部分防腐剂单体的使用频率非常低,经常使用的防腐剂单体约九种——苯氧乙醇、尼泊金甲酯、尼泊金丙酯、甲基异噻唑啉酮(卡松)、山梨酸、苯甲酸、己脒定二(羟乙基磺酸)盐、脱氢乙酸、咪唑烷基脲。
即使是复配使用,选择也是很有限的。
近年来不在《化妆品安全技术规范》内防腐剂范围却具有防腐性能(抑菌作用)的原料(无添加防腐剂)异军突起,得到很多化妆品生产商的青睐,其中防腐剂单体约20种。
这一类无添加防腐剂国家允许使用,并且不限量使用。
一款好的防腐剂应该具备良好的防腐抑菌能力及温和性,本文重点研究几款无添加防腐剂的眼刺激性,并对改善其刺激性进行了探讨。
市面上常用的无添加防腐剂有二元醇类(苯乙醇、戊二醇、己二醇、辛二醇)、对羟基苯乙酮、辛酰羟肟酸等。
其中,己二醇、辛甘醇可作为香料,戊二醇为性能优异的保湿剂,对羟基苯乙酮具有抗氧化、舒缓镇静能力,辛酰羟肟酸具有增溶助溶及美白功效。
实验选取苯乙醇、戊二醇、己二醇、辛二醇、对羟基苯乙酮、辛酰羟肟酸,评价其眼刺激性。
眼刺激性评价可通过鸡胚绒毛尿囊膜血管试验(HET-CAM ,国标SN/T 2329-2009 )进行。
HET-CAM 模拟兔子眼结膜,通过记录受试物接触鸡胚尿囊膜后发生的出血、血管融解和凝血等变化的时间,根据计算公式得到一个IS 评分,用于评估受试物的眼刺激性。
评分越高,刺激性就越大。
IS=(301-sec H)x5300 +(301-sec L)x7300 +(301-sec C)x9300 (1)式中:Sec H (出血时间hemorrhage time )——CAM 膜上观察到开始发生出血的平均时间,单位为秒(s ); Sec L (血管溶解时间vessel lysis time )——CAM 膜上观察到开始发生出血的平均时间,单位为秒(s );Sec C (凝血时间coagulation time )——CAM 膜上观察到开始出现凝血的平均时间,单位为秒(s )。
Draize眼刺激性试验的评价

Draize眼刺激性试验的评价
王庆利;彭健
【期刊名称】《中药新药与临床药理》
【年(卷),期】2005(16)4
【摘要】在药物安全性评价中,眼用药物及可能接触到眼的化学物质均应考虑进行眼刺激性试验,Draize试验是评价眼刺性的主要方法。
作者综述了国外有关Draize 眼刺激性试验的文献,并对其存在问题进行了讨探,提出改进的建议,希望有助于研究人员和评价人员对该试验的理解、运用和评价。
【总页数】4页(P301-304)
【关键词】眼刺激性试验;安全性评价;Draize试验
【作者】王庆利;彭健
【作者单位】国家食品药品监督管理局药品审评中心
【正文语种】中文
【中图分类】R99;R285.1
【相关文献】
1.揭秘化妆品安全性评价技术(四)——化妆品眼刺激性及试验方法 [J], 潘芳;敖华英
2.溶血试验用于评价隐形眼镜护理液眼刺激性的可行性研究 [J], 林美琼;田胜慧;杨立峰;杨文润;柯军
3.鸡胚绒毛尿囊膜试验用于化妆品的体外眼刺激性评价 [J], 陆泽安;郑赛华;吴越;
马来记;魏少敏
4.多层试验组合策略对1,2-己二醇眼刺激性/腐蚀性的评价 [J], 陈秀娟;王强;黄宇锋;刘香梅;庞增雄;江漪;李培宁;李光先;陈梓灵;孙侠
5.红细胞溶血试验用于评价淋洗类化妆品眼刺激性的初步研究 [J], 田妮娜; 刘兴国; 李岩; 王月玲
因版权原因,仅展示原文概要,查看原文内容请购买。
急性眼刺激性、腐蚀性实验

五、急性眼刺激性/腐蚀性试验Acute Eye Irritation/Corrosion Test1 范围本规范规定了动物急性眼刺激性或腐蚀性试验的基本原则、要求和方法。
本规范适用于化妆品原料及其产品安全性毒理学检测。
2 规范性引用文件OECD Guidelines for Testing of Chemicals(No 405,April 2002)USEPA OPPTS Harmonized Test Guidelines(Series 870.2400,Aug.1998)3 试验目的确定和评价化妆品原料及其产品对哺乳动物的眼睛是否有刺激作用或腐蚀作用及其程度。
4 定义4.1 眼睛刺激性(Eye irritation):眼球表面接触受试物后所产生的可逆性炎性变化。
4.2 眼睛腐蚀性(Eye corrosion):眼球表面接触受试物后引起的不可逆性组织损伤。
5 试验的基本原则受试物以一次剂量滴入每只实验动物的一侧眼睛结膜囊内,以未作处理的另一侧眼睛作为自身对照。
在规定的时间间隔内,观察对动物眼睛的刺激和腐蚀作用程度并评分,以此评价受试物对眼睛的刺激作用。
观察期限应能足以评价刺激效应的可逆性或不可逆性。
动物如果在试验的任何阶段出现严重抑郁、痛苦的表现,则应该给予人道地处死,依据试验情况对受试物进行适当评价。
动物如出现角膜穿孔、角膜溃疡、角膜4分超过48h、缺乏光反射超过72h、结膜溃疡、坏疽、腐烂等情况,通常为不可逆损伤的症状,也应该给予人道地处死。
6试验方法6.1 受试物液体受试物一般不需稀释,可直接使用原液,染毒量为0.1mL。
若受试物为固体或颗粒状,应将其研磨成细粉状,染毒量应为体积0.1mL或重量不大于100mg(染毒量应进行记录)。
受试物为强酸或强碱(pH值≤2或≥11.5),或已证实对皮肤有腐蚀性或强刺激性时,可以不再进行眼刺激性试验。
气溶胶产品需喷至容器中,收集其液体再使用。
6.2 实验动物和饲养环境首选健康成年白色家兔。
揭秘化妆品安全性评价技术(四)——化妆品眼刺激性及试验方法

方 法 已经 包括 在试 验 策 略 中, 为动 作
物 试 验 的 补 充 , 体 内 兔 眼 试 验 仅 而 需 要 在 最 后 一 步 进 行 , 就 是 说 当 也 全 部 其他 序 列 试 验 已 经 得 出 阴 性 评
价 结 果 , 要 对 轻 度 到 中度 的 刺 激 需
性 混 合 物 进 行 评 价 时 才 考 虑 性体 内
1 牛 角 膜 浑 浊 和 渗 透 性 实 验
( vn Bo i e Cor ea n lOp ci nd a t a y
P r a iy B eme bl , COP 使 用 屠 宰场 获 i t ) 得 的标 本 , 新 鲜 分离 的角膜 水平 将
固 定 于 支 持 架 , 后 放 置 于 特 殊 改 然 进 的透 光 容 器 里 。 温 条 件 下, 闭 恒 封
生细 胞 毒 性 , 表面 活化 剂 和一 些 如
有 机 溶 剂 是 这 类 物 质 的 代 表 。那 些 作 用 于 细 胞 能 量 代 谢 的物 质 也 可 快 速 产 生作 用 , 可 能 没 有 第 一 类 物 质 但 迅 速 。化 学 物 质 还 可 以 通 过 对 大 分 子 的 烷 化 或者 其 他 影 响 而产 生作 用 ,
这些年来 , 为了减 轻 动 物 遭 受 的
在 第 一 位 。 些 可 溶 解 细 胞 膜 或 者 那
是 导 致 蛋 白质 凝 集 的 物 质 可 立 即产
痛 苦 和使 受 损组 织 更快 恢 复 , 已经
提 出一些 优 化 意见 , 如低 眼容量 例 实 验 ( VE 。目前 , 少 和 优 化 的 L T) 减
试验 。
这 类 物 质 的 作 用 可 能 表 现 为 一 种 迟 发 性 的 细 胞 毒 性 ( 迟 发 性 坏 死 或 如
化妆品眼刺激试验替代方法标准化与展望

检 查可 提高 预测 能 力 。该 方 法 对 碱 性 物 质 、 阴离子 和 阳离子 表面 活性 剂 、 妆 品成 分 和化 学物 质 较 敏 化
SS熊胆眼药水刺激性研究

SS熊胆眼药水刺激性研究摘要:目的:构建滴眼液刺激性体外评价方法,筛查SS熊胆眼药水刺激性原因并采取适宜方法解决。
方法:采用兔角膜上皮细胞毒性试验(SIRC-MTT)对4种熊胆滴眼液进行评价,将结果与临床刺激性评分进行相关性分析,运用SIRC-MTT 筛查SS熊胆眼药水的刺激性原因并进行解决。
结果:相关系数为0.961,说明SIRC-MTT能较好评价熊胆滴眼液眼刺激性;造成熊胆眼药水刺激性较强的原因为羟苯乙酯与熊胆原液的共存;采用减少羟苯乙酯用量(调整至0.04%)、添加羧甲基纤维素钠(0.2%~0.25%)均能增加角膜上皮细胞存活率。
结论:SIRC-MTT是SS 有效的体外刺激性评价方法;降低羟苯乙酯用量和添加羧甲基纤维素钠均能降低熊胆眼药水的刺激性。
关键词:刺激性;熊胆眼药水;细胞毒性试验;角膜上皮细胞SS熊胆眼药水由熊胆单味中药研制而成,具有清热解毒,祛翳明目的功效,主要用于治疗急、慢性卡他性结膜炎,但大多患者在使用中发现该药具有较强刺激性,严重影响了其临床用药。
现今评价眼刺激性的方法为兔眼刺激法(draize test),该法具有主观性强,实验差异大等缺点[1],难以寻找出SS熊胆眼药水刺激性较强的内在原因。
该研究拟建立SS新的体外刺激性评价方法,用于筛查该眼药水的刺激性原因,并解决该问题。
1 材料与方法1.1 受试物、仪器与试剂SS熊胆眼药水(成都某药业公司提供),熊胆粉滴眼液(某药业公司),熊胆黄芩滴眼液(黑龙江黑宝药业),复方熊胆滴眼液(长春普华药业),熊胆、羟苯乙酯、羧甲基纤维素钠(成都某药业公司提供),氯化钠、硼酸、硼砂(科龙试剂有限公司),透明质酸钠(Solarbio);二氧化碳培养箱(Thermo),超净工作台(苏州净化),倒置显微镜(奥林巴斯),自动酶标仪(BIO-RAD),DMEM低糖(GIBCO,USA),胎牛血清(甘肃民海),MTT(SIGMA,USA),F12(GIBCO,USA),青霉素(石家庄制药有限公司),链霉素(华北制药股份有限公司),L-谷氨酰胺DMSO(SIGMA,USA)。
鸡胚尿囊膜(HET-CAM)眼刺激替代试验对产品及原料评价的比较

鸡胚尿囊膜(HET-CAM)眼刺激替代试验对产品及原料评价的比较邱璐;李小林;卞俐娜;山口能宏【摘要】目的比较鸡胚尿囊膜试验(HET-CAM)作为一种眼刺激替代方法对产品或原料的评价.方法采用HET-CAM和兔眼Draize试验方法,对19种原料和23种化妆品及家用洗涤产品眼刺激性进行检测,对体内体外试验的结果进行统计比较.结果比较体内体外试验,原料和产品的kappa系数分别为0.826,0.531;灵敏度分别为100%,81.8%;特异度分别为85.7%,77.8%.结论 HET-CAM可作为Draize试验的替代试验,HET-CAM系统更适合对单纯化学品原料进行眼刺激试验.%Objective To compare the adaptability of HET-CAM eye irritation test for products and ingredients.Methods Test 19 ingredients and 23 products by HET-CAM and Draize eye irritation protocol. Compare the data from in vitro and in vivo test. Result Compare in vitro data and in vivo data, The Kappa coefficient , sensitivity, specificity are 0. 826,100% ,85.75 for ingredient. 0. 531,81.8% ,77. 8% for cosmetics as well. Conclusion HET-CAM eye irritation test can be used to be alternative test of Draize test. HET-CAM system is more suitable for ingredients test.【期刊名称】《中国比较医学杂志》【年(卷),期】2011(021)003【总页数】6页(P27-30,35,后插3)【关键词】鸡胚尿囊膜试验;Draize眼刺激试验;替代试验【作者】邱璐;李小林;卞俐娜;山口能宏【作者单位】上海出人境检验检疫局,上海,200135;上海出人境检验检疫局,上海,200135;上海出人境检验检疫局,上海,200135;日本小林制药株式会社,大阪【正文语种】中文【中图分类】R185;R332眼刺激试验是化妆品安全性评价的重要指标,一般采用Draize[1]眼刺激试验进行评价,经济合作和发展组织(OECD)将这个方法纳入了指南[2]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
眼刺激性体外评价方法研究进展
摘要:在中药滴眼液的研发中,寻找一种简单、快速的刺激性评价方法体系非常必要。
兔眼刺激试验(TheDraize test)作为眼部安全评价标准已逾几十载,缺点较多:评分系统主观性强、动物外推至人种属差异大、实验室间变异性大等。
许多实验室在近20年间相继提出了新的体外试验方法,对体外眼刺激性试验方法进行了综述。
关键词:Draize眼刺激试验;刺激性;体外试验;综述
毒理学一直致力于保证人类免受各种物质的伤害,如药品、化工产品、化妆品及家庭用品等。
最易导致偶然接触伤害的部位一般是眼睛和皮肤。
这种由化合物刺激导致的生理反应一般称为刺激性,包括客观的生理变化(局部红肿、水肿)和主观感受(瘙痒、疼痛)。
在生产、使用这些物品时,都需要对其刺激性进行评价。
时至今日,最可靠的安全性评价方法还依赖于动物试验。
但是当今社会,动物福利日益受到重视,兔眼刺激性试验在伦理、科学上均受到质疑,因此寻找节约高效的试验方法推动了眼刺激性试验评价方法的进展。
1Draize兔眼刺激性试验简介
随着制药工业的发展,特别是一些对眼睛有副作用的药物的发现,在20世纪初形成了眼毒理学。
其主要研究目标之一是建立一种能用于评价新物质潜在刺激性的方法。
Jonas Friedenwald(1897-1955)提出了采用对眼睛各部位毒性分别进行等级评分的方法评价刺激性的方法体系。
在Friedenwald的基础上,John H.Draize(1900-1992)和他的同事在1944年提出了一种新的评价方法,该方法采用皮肤和兔眼作为试验对象,描述了如何进行剧烈的、温和的和长期刺激性的评价。
这些方法相继被其它实验室用以筛选化合物刺激性,被称为“Draize试验”。
此后,Draize的技术标准被FDA采用并用以评价某些物质的安全性,在相当长的一段时间里被FDA视为当时最有价值和最可靠的方法,有金标准(Golden standard)之称。
由于该方法每个步骤都要认真审查和观察,其重复性、关联性、经费及伦理等诸多方面均遭到了科学界的质疑与批评,20世纪60年代,这种试验方法更是遭到广泛的批评。
实验数据变化较大导致试验重复性较差,特别是轻微刺激性更为明显。
Draize test结果重复性较差主要源于两个方面。
其一,受试动物兔的种属个体差异难以控制;其二,试验员在对兔眼的观察和评分上存在的诸多差异难以控制。
虽然可以通过扩大样本容量和培训试验员来减少这些误差,但是重复性较差的缺点还是难以克服。
相同种属的动物可以以各种不同的方式对刺激性物质进行应急,不同的试验者在相同的试验中可能得到不同的数据。
加之兔眼的解剖学结构、生物化学和人眼也不尽相同,如:兔眼眼泪产量相对较少,眨眼频率与人眼不同,眼表面的敏
感性较人眼差。
Draize test只是从炎症和毒性两个方面的表现对刺激性进行评价,难以全面反映刺激性作用。
其外部的观察只能将结果限制在某几种特定的变化中,不能够探知其内在的机制。
当受试物质直接接触外眼时,不仅能造成毒性损伤与炎症反应,还能带来烦躁、迟发型变态反应、结构变化、各种分子的改变以及全身效应。
而这种眼部刺激性试验却难以全面体现这些变化。
这种人眼与兔眼的关联性遭到质疑也就在所难免。
很多科学家对Draize test主要根据两种思路进行修订,一种是用尽量少的动物挖掘尽量多的信息,同时保证其与人眼反应的较好相关性。
另外一种是避免直接将化合物作用于眼,而是先进行皮肤刺激性试验。
科学家在Draize test的基础上研究形成了一种新的可被用作替代Draize test的体内研究方法,称作低容量眼部试验法(10wvolume eyetest:LVET),该方法相比Draizetest与人眼具有更好的相关性,优于Draize试验,被证明是一种可以接受的替代方法。
但LVET与Drame test都过高估计了人眼对刺激物的反应。
2Draize eye test体外试验方法概述
为了将试验给动物带来的痛苦降到最低程度,人道主义者提出了3R(Replacement,Reduction,Refinement)的理念,提出了多种多样的体外试验方法,这些方法运用的技术越来越先进,检测的范围与部位也越来越丰富,现将这些常用的体外试验方法及其优缺点简述如下。
2.1红细胞溶血试验(Red Blood Cells Test)
用多因素分析方法发现Draize test的检测原理大部分可以用蛋白变性和细胞膜破坏来解释。
由此发展了基于测定从红细胞中漏出的血红蛋白的量来评价膜损伤的试验方法——溶血试验(Hemolysis test)。
RBCs试验用来评价某些受试物引起的细胞初始反应(例如接触化合物后的角膜浑浊度改变),这些受试物主要损伤细胞胞浆膜以及使某些蛋白质变性;而非刺激性物质则不会造成这样的反应。
该方法的假说认为这种反应与眼部组织的刺激反应所产生的初始事件具有一定的相关性。
该方法通过分光光度法测定化学物作用后的红细胞悬液吸光度,计算出溶血率和HC50值(即使50%红细胞溶血的受试物的浓度值)用作评价受试物的刺激性指标。
RBCs试验是一种作用机制明确、不需用特殊的仪器和设备、操作快速简便、不需无菌处理、费用低廉等优点。
但该法检测终端过于单一,难以替代Draize test 用于全面评价受试物的刺激性,只能用于粗筛试验。
2.2血红蛋白变性试验(Haemoglobin Denaturation Test)
血红蛋白变性试验(Haemoglobin Denaturation test,HD test)是用评价蛋白变性的指标RDC50(血红蛋白变性率为50%的受试物浓度)和1%λmax(1%受试物的最大可吸收波长变化值)来预测化学物质的眼刺激性的一种试验方法。
这种方法的理论基础是眼刺激性反应是由一系列的蛋白质变性所引起的,而血红蛋白变
性时会引起吸光度特性的改变,利用血红蛋白变性试验来检测表面活性剂对血红蛋白结构活性的量化改变作为评价刺激性的指标。
最初的方法是通过吸光度值计算血红蛋白的变性率而建立的。
后来发明者提出了新的方程式用以与Draize分值进行相关性研究,比如进行log数值代换等。
Hayashi T等发现蛋白质变性试验(HD test)与红细胞溶血试验(RBCs test)联合试验结果与Draize评分的相关性非常高。
在刺激性评价中,应适当考虑二者结合进行。
该法不需要特别设备,操作简单,试验流程短,可大大缩短粗筛的时间。
但血红蛋白变性试验不能用于在418 nm有强吸收峰的有色物质和超过磷酸盐缓冲液范围的强酸,也不能检测磷酸。
